白色念珠菌(Candida albicans)作为条件致病真菌,在生理状态下可与宿主维持共生平衡。然而,当宿主局部微生物群失衡、组织屏障功能受损或免疫防御系统失调时,白色念珠菌可通过黏附定植、菌丝分化及水解酶分泌等毒力表型转换,导致口咽念珠菌病(oropharyngeal candidiasis,OPC)等浅表感染[1-3]。流行病学研究表明,OPC的发生与宿主免疫状态存在显著关联,其高危因素主要包括人类免疫缺陷病毒感染、糖尿病、放化疗治疗,以及长期使用广谱抗生素或糖皮质激素所致的免疫抑制状态等[4-5],这提示宿主免疫状态是影响 OPC 感染发生的核心决定因素。白色念珠菌侵袭口腔黏膜的机制呈现双重特征:其一,菌丝表面侵袭蛋白Als3和Ssa1等与宿主上皮细胞E-钙黏蛋白、表皮生长因子受体等分子互作,触发宿主引导的内吞作用[6-7];另一方面通过机械穿透作用破坏上皮屏障并形成生物膜,加剧组织损伤[8]。这些致病机制均与宿主免疫监视及防御应答失衡密切相关,因此,靶向干预宿主-病原体互作中的免疫调控节点,为开发宿主导向的免疫调控策略提供理论依据。
当前临床干预策略主要集中于直接拮抗病原体,通过抗真菌药物或益生菌抑制白色念珠菌的增殖,而针对宿主内源性防御系统的微生态调控策略尚未得到充分探索,且传统抗真菌药物可能加剧菌群失衡。事实上,宿主口腔免疫防御系统具有多维调控网络:上皮屏障通过Toll样受体(Toll-like receptors, TLRs)、NOD样受体(NOD-like receptors, NLRs)、白细胞介素-17受体(interleukin-17 receptor, IL-17R)、蛋白酶激活受体等模式识别受体感知病原微生物信号[9-10],可激活NOD/NF-κB/β-defensin-2、IL-17R/IκBζ等信号通路调节β-防御素的分泌[11-13]。这些内源性防御机制为疾病防治提供了新视角,通过精准调控宿主固有免疫应答,既可避免广谱杀菌引发的微生态失衡,又能通过增强宿主防御功能预防白色念珠菌对宿主的侵袭。另外,后生元是当前益生菌研究领域的重要发展方向,其作用机制不依赖于菌株的活力和在宿主生态位的定植能力,且非活菌成分在免疫低下人群中应用的安全性更高。
基于此,本研究提出一种宿主导向的微生态-免疫协同调控策略:通过在细胞层面筛选出能够增强宿主防御物质表达的后生元,随后构建小鼠OPC模型,进一步探究该菌株对抵抗白色念珠菌侵袭的效果以及对宿主的免疫调控能力,并解析其调控机制。该策略突破传统益生菌疗法的定植竞争局限,通过靶向宿主固有免疫网络实现长效免疫防护,为开发精准化抗真菌疗法提供理论依据。
1 材料与方法
1.1 材料与试剂
15株唾液联合乳杆菌(Ligilactobacillus salivarius),江南大学食品微生物菌种保藏中心(Culture Collection of Food Microorganisms,CCFM);人口腔角质细胞HOK-16B,青旗(上海)生物技术发展有限公司;白色念珠菌SC5314,宁波明舟科技有限公司;6周龄Balb/c雌鼠,北京维通利华实验动物技术有限公司。
胎牛血清、DMEM细胞培养基、胰酶、青霉素和链霉素,美国Gibco公司;人源β-防御素-2(human β-defensin-2,HBD-2)、鼠源IL-17、鼠源β-防御素-3(murine β-defensin 3,mBD3)、多聚免疫球蛋白受体(polymeric immunoglobulin receptor,pIgR)、分泌型免疫球蛋白(secretory immunoglobulin A,SIgA)试剂盒,南京森贝伽生物科技有限公司;沙氏葡萄糖琼脂(含氯霉素)、YPD、MRS培养基,青岛海博生物技术有限公司;醋酸可的松,MCE公司;NaCl、PBS,国药集团化学试剂有限公司。
1.2 仪器与设备
SW-CJ-1FD超净工作台、BSC-1000IA2生物安全柜,苏州安泰空气技术有限公司;GPR-9160隔水式恒温培养箱,上海森信实验仪器有限公司;Multiscan Go多功能酶标仪、371二氧化碳培养箱,赛默飞世尔科技有限公司;XStream Lab Homogenizer 2000高压均质机,意大利GEA公司;SCIENTZ-48高通量组织研磨机,中国宁波新芝生物科技股份公司;PANNORAMIC MIDI Ⅱ组织切片电子扫描仪,匈牙利3DHISTECH公司。
1.3 实验方法
1.3.1 细胞实验
将唾液联合乳杆菌接种于MRS固体培养基上,37 ℃培养48 h后挑取单菌落,于对应的液体培养基中活化3代,37 ℃培养18 h制备得到种子液。取第3代菌液离心收集菌体,用无菌PBS调整混悬液至1.5×109 CFU/mL,经高压均质处理后(800~1 200 MPa,10次循环),调节pH为7.2~7.4,用0.22 μm滤膜过滤,获得对应浓度菌悬液制备的菌体裂解液。
6孔板中每孔接种2×105个细胞,培养24 h后分组干预:对照组加入含5%(体积分数)PBS的培养基,处理组加入含5%(体积分数)菌体裂解液的培养基。干预24 h后收集上清液,4 ℃、2 000 r/min离心20 min,按ELISA试剂盒说明书检测HBD-2含量。
1.3.2 动物实验
1.3.2.1 动物实验设计
本研究由江苏省血吸虫病防治研究所实验动物伦理审查委员会监督实施(IACUC-JIPD-2023145)。18只无特定病原体的6周龄Balb/c雌鼠,体质量15~18 g,饲养在温度为20~24 ℃,湿度为(50±10)%,光照和黑暗周期为12 h的动物屏障中。适应性饲养7 d后,随机分为3组(n=6):空白对照组、OPC模型组、唾液联合乳杆菌CCFM1417菌体裂解物组(CCFM1417组)。按1.2.1节的方法制备CCFM1417菌体裂解物:菌泥(5×1010 CFU/mL)经65 ℃灭活30 min、高压均质后冻干,使用前以无菌生理盐水复溶至原浓度。
如图1所示,从第0天到第17天,对照组和模型组小鼠用30 μL的生理盐水进行口腔冲刷,CCFM1417组用等体积的菌体裂解液进行冲刷,冲刷后将小鼠头朝上放置2 min,以防止样本流出。第14、16天,各组均于颈背部皮下注射醋酸可的松(225 mg/kg)诱导免疫抑制。在第15天,麻醉小鼠参照文献[14-15]的方法进行白色念珠菌感染,除对照组外,将浸有50 μL白色念珠菌(1×107 CFU/mL)的棉片至于各组小鼠舌下60 min,以构建OPC模型。在第18天处死小鼠,取舌组织检测白色念珠菌载量,并行苏木精-伊红(hematoxylin-eosin staining,H&E)染色和碘酸-希夫(periodic acid-Schiff stain,PAS)染色及免疫指标分析。

图1 动物实验设计方案流程图
Fig.1 Flow chart of animal experiment design scheme
1.3.2.2 小鼠舌头组织病理学分析
收集小鼠舌头组织,用0.04 g/mL多聚甲醛(pH 7.4)固定24 h,随后包埋在石蜡中。将石蜡块切成5 μm厚的切片,参照文献[16]的方法进行H&E染色和PAS染色。切片样本使用Case Viewer软件放大40倍进行观察。
1.3.2.3 小鼠舌头组织中白色念珠菌载量
处死后取小鼠舌组织,经组织研磨仪匀浆后无菌梯度稀释,取1 mL稀释液倾注于含氯霉素沙氏葡萄糖琼脂平板,37 ℃培养48 h统计白色念珠菌菌落数。
1.3.2.4 酶联免疫吸附测定
取小鼠舌组织按料液比1∶9(g∶mL)加入4 ℃预冷PBS,经组织研磨仪(70 Hz,60 s/次,循环6次)破碎后,2 000 r/min离心20 min收集上清液,按照试剂盒说明书测定组织中的mBD3、pIgR、IκBζ、SIgA和IL-17的浓度。
1.4 数据处理
所有实验至少重复3次,并以“平均值±标准差”的形式呈现。统计分析和图形绘制使用了GraphPad Prism 9.0软件。2组之间的方差分析采用双尾Student’s t检验。多组之间的比较采用单因素方差分析(One-way ANOVA)和Tukey’s检验。
2 结果与分析
2.1 菌株对细胞HBD-2蛋白表达的影响
HBD-2属于防御素家族的成员,是人体内首个被发现的可诱导性表达的防御素,在口腔中主要由上皮细胞分泌产生,作为抵御微生物入侵、炎症和疾病的主要屏障,同时维持生理稳态[17],在黏膜的固有免疫中具有重要作用[18]。HBD-2具有广谱的抗菌活性,能够对多种微生物产生抑制和杀灭作用,包括白色念珠菌等多种可能引发OPC的病原体[19]。
本研究基于人口腔角质细胞HOK-16B体外模型,系统评估了15株唾液联合乳杆菌对HBD-2表达的调控作用,旨在筛选具有免疫调节潜力的益生菌株。如图2所示,干预后空白组HBD-2蛋白的表达量为198.94 pg/mg,CCFM1417组的表达量为238.87 pg/mg,与空白组相比上调了20.10%,具有显著性差异(P<0.05),其余14株菌蛋白表达量与空白组相比无显著性差异(P>0.05)。综上所述,本研究通过体外细胞筛选发现,在15株唾液联合乳杆菌中CCFM1417可显著上调人口腔上皮细胞HBD-2蛋白的表达,随后构建小鼠OPC模型,以进一步探究该菌株在动物模型中对口腔疾病的预防效果。
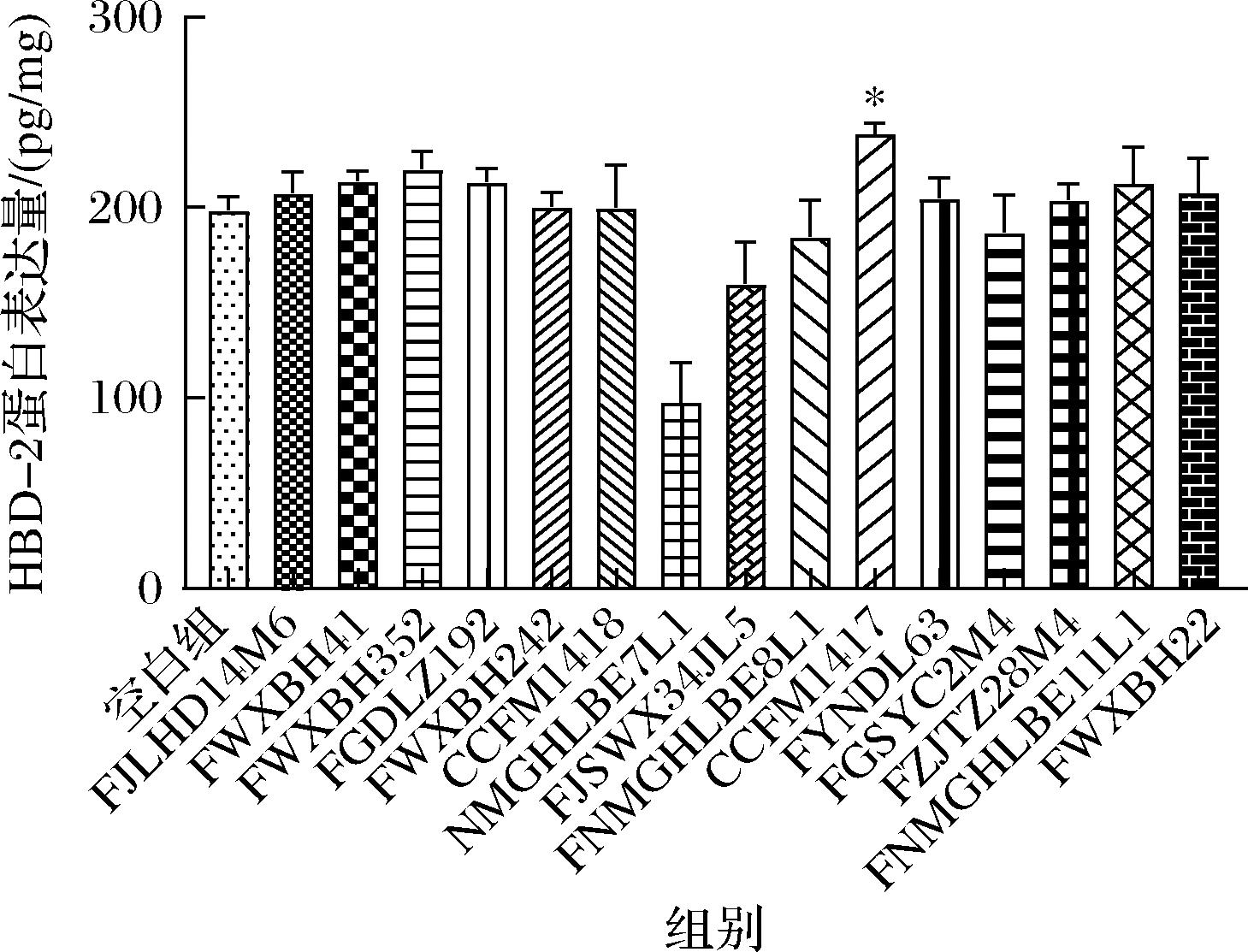
图2 不同菌株对HOK-16B细胞HBD-2蛋白表达的影响
Fig.2 Effects of different strains on HBD-2 protein expression in HOK-16B cells
注:与空白组比较,*表示P<0.05。
2.2 CCFM1417口腔冲刷对小鼠体质量和表观指标的影响
在菌株干预的整个过程中,每天对小鼠的行为状态、饮食饮水、毛发顺滑程度进行观察。白色念珠菌感染建模后,记录小鼠体质量变化并观察舌头黏膜的念珠菌定植情况。感染后第3天,模型组小鼠舌头开始出现大量的白色念珠菌菌斑附着,处死小鼠并对小鼠舌头进行拍照记录。
如图3-a~图3-c所示,空白组小鼠舌体形态完整,舌背光滑润泽,色泽淡红,用镊子容易拉出口腔外,未见舌乳头萎缩或角化异常;相比之下,模型组小鼠舌背覆盖有一层由白色念珠菌形成的伪膜,黏膜质地粗糙且色泽暗红,舌头不易拉出口腔外,同时观察到舌乳头存在萎缩现象。CCFM1417组干预后舌背上白色念珠菌的定植量明显减少,舌体光滑湿润,表明唾液联合乳杆菌CCFM1417能够较好地预防小鼠OPC的发生。如图3-d所示,在第18天,模型组的体质量显著下降至初始体质量的78.41%,由于造模期间空白组同样也注射了免疫抑制剂,体质量下降至初始体质量的93.30%;CCFM1417组体质量仅下降至初始体质量的88.58%,与模型组相比存在显著性差异(P<0.000 1),与空白组相比无显著性差异(P>0.05),表明唾液联合乳杆菌CCFM1417菌体裂解物干预能够显著缓解白色念珠菌感染造成的小鼠体质量的急剧下降。
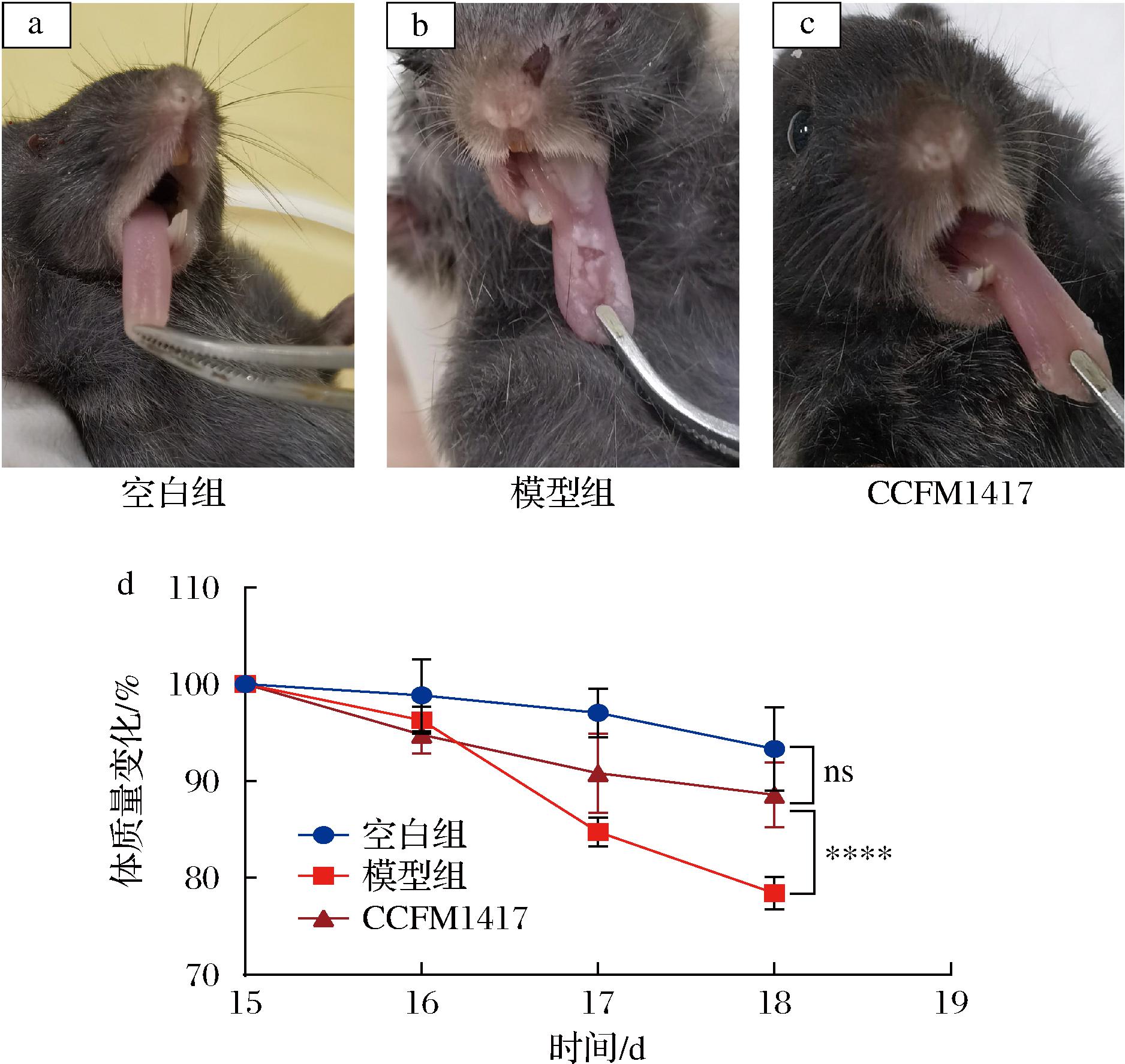
a-空白组小鼠舌体形态;b-模型组小鼠舌体形态;c-CCFM1417组小鼠舌体形态;d-感染期间小鼠体质量变化
图3 菌株口腔冲刷对小鼠舌背白色念珠菌定植和体质量变化的影响
Fig.3 Effects of oral lavage with strain on C.albicans colonization in the dorsal tongue and body weight changes in mice
注:****表示P<0.000 1,ns表示无显著性差异。
2.3 CCFM1417口腔冲刷对小鼠舌头组织病理学的影响
PAS染色可通过标记真菌细胞壁的β-葡聚糖和几丁质,将白色念珠菌的菌丝和孢子染成紫红色,与周围组织形成鲜明对比,从而判断白色念珠菌对组织的侵袭情况。如图4-b所示,模型组舌头表面有大量的白色念珠菌菌丝入侵组织,这些菌丝呈细长的杆状并以一定的角度入侵到组织内部。CCFM1417组与模型组相比,白色念珠菌对组织的侵袭程度较小,无大量的白色念珠菌菌丝或孢子聚集在舌黏膜表面(图4-c)。
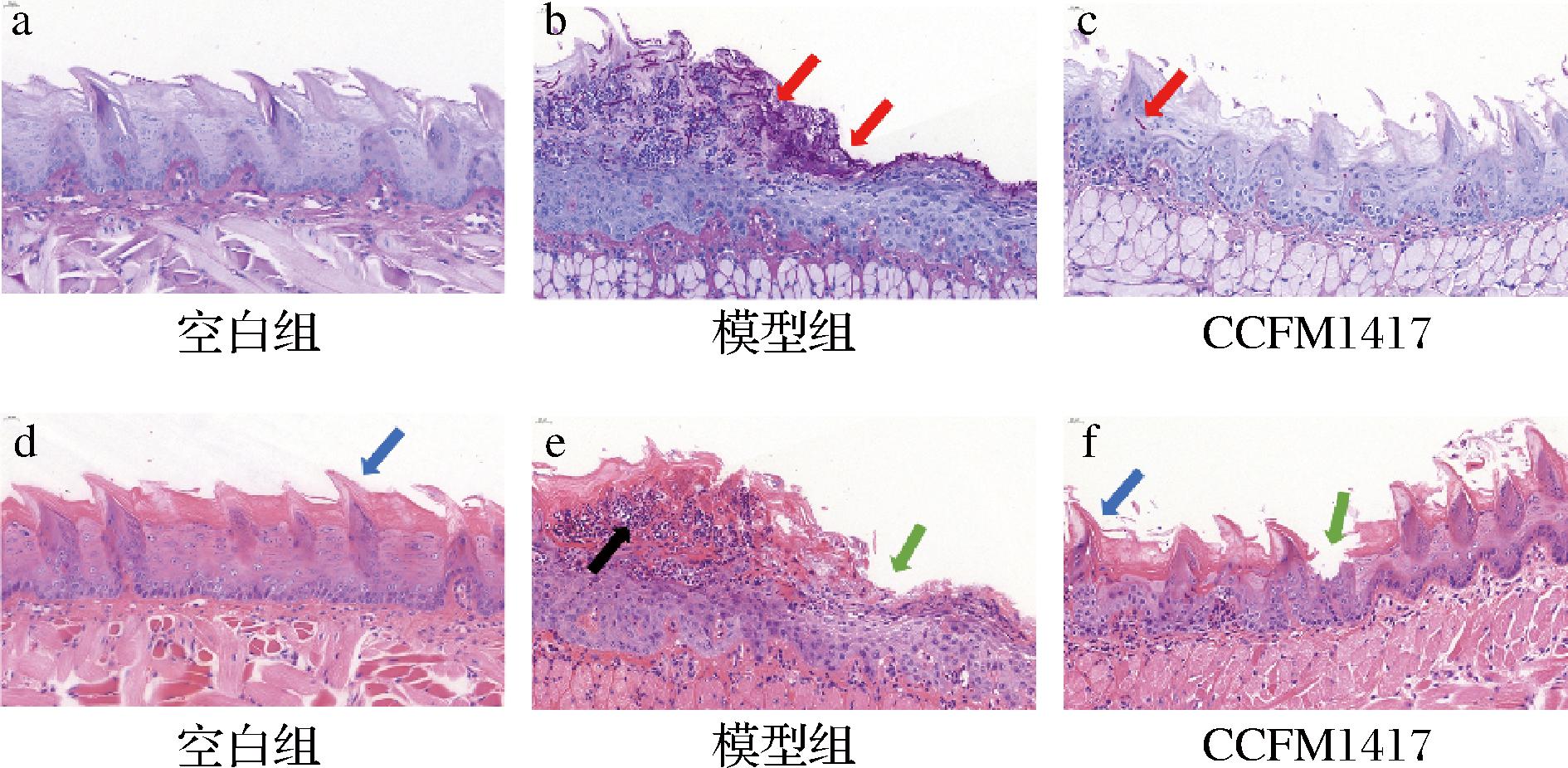
a-空白组小鼠舌头PAS染色;b-模型组小鼠舌头PAS染色;c-CCFM1417组小鼠舌头PAS染色;d-空白组小鼠舌头H&E染色;e-模型组小鼠舌头H&E染色;f-CCFM1417组小鼠舌头H&E染色
图4 菌株口腔冲刷对小鼠舌背组织病理学的影响
Fig.4 Effects of oral lavage with strain on the histopathology of the dorsal tongue in mice
注:红色箭头-白色念珠菌菌丝;蓝色箭头-舌黏膜丝状乳头;黑色箭头-组织炎症细胞募集;绿色箭头-黏膜表面糜烂和孔洞。
H&E染色观察小鼠舌头组织的损伤情况。如图4-d~图4-f所示,空白组舌背黏膜表面丝状乳头排列整齐,组织内无炎症细胞聚集;模型组舌背黏膜表面丝状乳头皱缩,舌背表面有多处糜烂和孔洞的形成,组织内有大量的炎症细胞聚集。CCFM1417组舌黏膜表面虽然存在组织破损,但丝状乳头基本完整,且组织无明显的炎症细胞浸润。综上所述,唾液联合乳杆菌CCFM1417菌体裂解物干预后,能够在一定程度上减少感染期间白色念珠菌对小鼠舌头的侵袭,呈现出优异的抗致病菌感染的作用。
2.4 CCFM1417口腔冲刷对小鼠舌头组织真菌载量的影响
对小鼠舌头组织进行匀浆计数,以评估舌头组织中白色念珠菌的定植量。如图5所示,模型组小鼠舌头组织白色念珠菌平均定植量约为7.52×105 CFU/g,CCFM1417组舌头组织中致病菌白色念珠菌的载量为8.67×104 CFU/g,显著性低于模型组舌组织中白色念珠菌的数量(P<0.05),这也与小鼠舌背组织病理学分析的结果相一致。
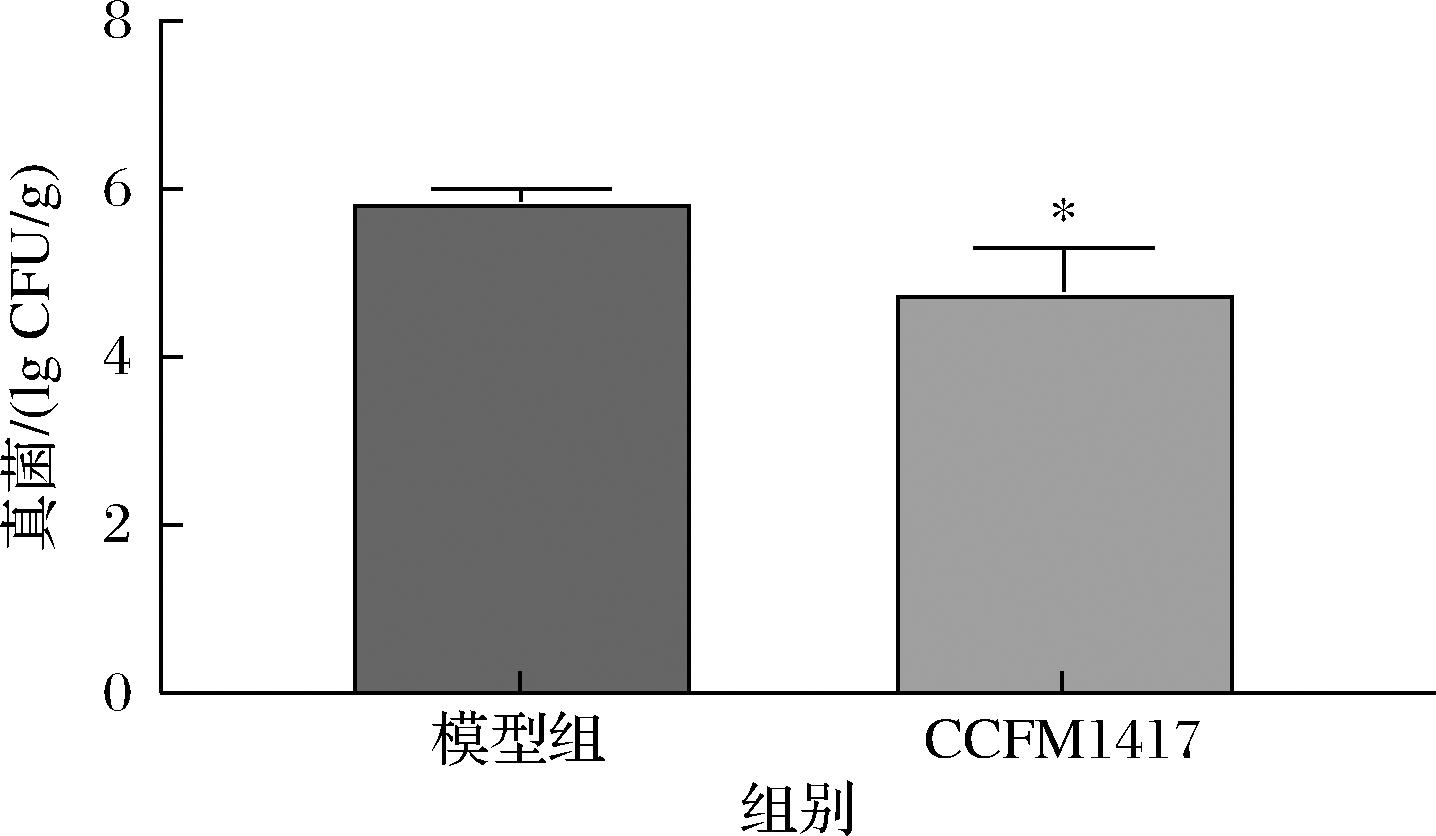
图5 菌株口腔冲刷对小鼠舌头真菌载量的影响
Fig.5 Effect of oral lavage with strain on fungal load in the mouse tongue
注:与模型组相比,*表示P<0.05(下同)。
2.5 CCFM1417口腔冲刷对小鼠口腔抗感染指标的影响
上述研究表明,唾液联合乳杆菌CCFM1417能够有效预防白色念珠菌对宿主口腔的侵袭,为了研究菌株预防白色念珠菌侵袭的机制,对各组小鼠舌头组织中抗白色念珠菌感染的相关指标mBD3、pIgR和SIgA进行检测,其中人HBD-2的鼠源同系物为mBD3[13]。
如图6-a所示,模型组防御素mBD3的表达量为13.64 pg/mg,空白组和CCFM1417组的mBD3表达量分别为20.90、30.69 pg/mg,与模型组相比均存在显著性差异。造模期间各组小鼠均接受了免疫抑制剂注射,但空白组mBD3表达量显著性高于模型组(P<0.05),表明白色念珠菌侵袭会破坏宿主机体的免疫防御机制,加剧疾病的发生。经过唾液联合乳杆菌CCFM1417菌体裂解物干预后,其mBD3表达量显著性高于模型组(P<0.01),表明唾液联合乳杆菌CCFM1417可通过增强抗菌肽介导的固有免疫应答,有效提升宿主口腔黏膜对致病菌的防御能力。
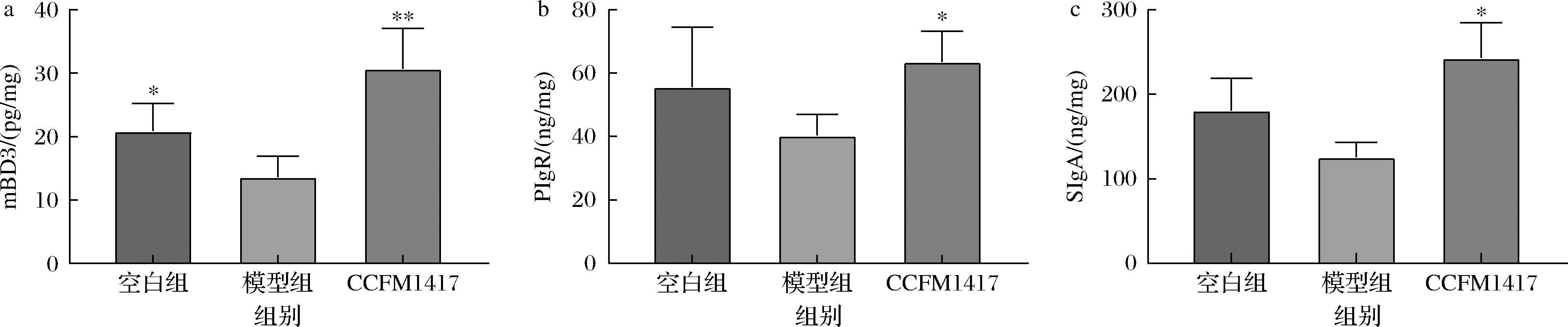
a-舌头组织mBD3含量;b-舌头组织pIgR含量;c-舌头组织SIgA含量
图6 菌株口腔冲刷对小鼠抗感染指标的影响
Fig.6 Effect of oral lavage with strain on anti-infection indicators in mice
注:与模型组相比,**表示P<0.01(下同)。
pIgR存在于上皮细胞基底,可协助转运IgA形成SIgA以增加黏膜表面分泌型免疫球蛋白的含量。SIgA在黏膜免疫中发挥着关键作用,它能够中和病原体和毒素,阻止其黏附于上皮细胞,从而限制微生物和环境抗原的入侵[20]。如图6-b所示,模型组pIgR的表达量为40.40 pg/mg;CCFM1417组的表达量为63.54 pg/mg,与模型组相比存在显著性差异(P<0.05)。进一步对各组小鼠舌头组织中的SIgA表达量进行测定,如图6-c所示,模型组SIgA的平均表达量为125.56 ng/mg;CCFM1417组的表达量为243.12 ng/mg,与模型组相比显著上调(P<0.05)。
综上所述,唾液联合乳杆菌CCFM1417菌体裂解物能够调控小鼠口腔抗感染指标mBD3、pIgR和SIgA的表达,并在一定程度上预防小鼠OPC的发生。
2.6 CCFM1417口腔冲刷对小鼠口腔抗感染信号通路的影响
研究表明,IL-17/IκBζ通路在口腔抗感染中扮演重要角色,尤其是在抵抗口咽念珠菌感染方面。在口腔黏膜中,IL-17可激活NF-κB非经典通路关键调节蛋白IκBζ的表达,从而上调下游防御素mBD3的表达[13]。另外,IL-17可以上调上皮细胞pIgR和IgA的表达[21-22],在宿主黏膜免疫和稳态方面起着不可或缺的作用。
如图7-a所示,空白组IL-17含量约为17.69 pg/mg,模型组IL-17含量约为13.69 pg/mg,由于空白组小鼠造模期间也接受了免疫抑制剂注射,因此两者之间没有显著性差异。CCFM1417组IL-17的表达量为19.67 pg/mg,与模型组相比显著上调(P<0.01)。
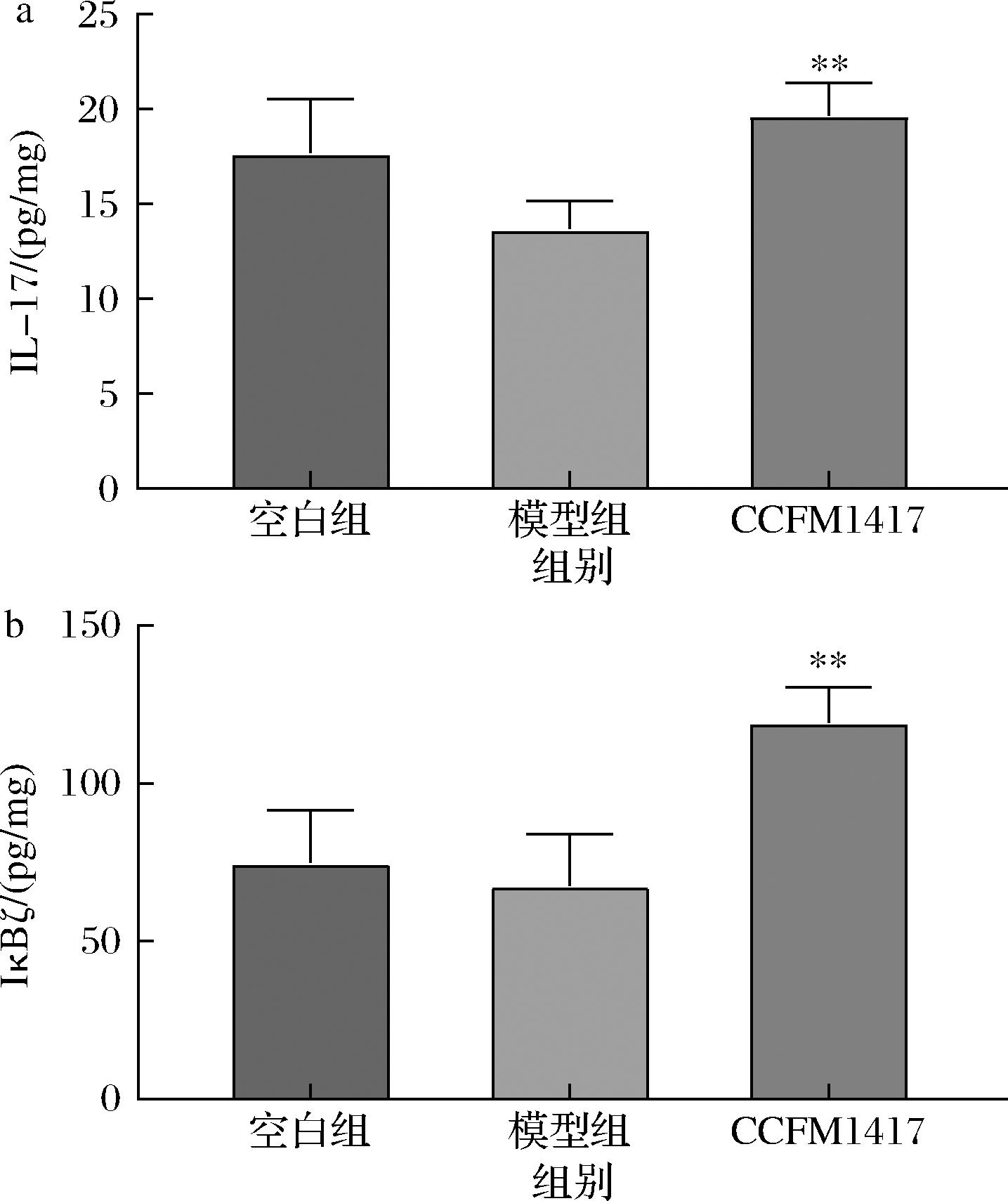
a-舌头组织IL-17含量;b-舌头组织IκBζ含量
图7 菌株口腔冲刷对小鼠抗感染信号通路的影响
Fig.7 Effect of oral lavage with strain on anti-infection signaling pathways in mice
如图7-b所示,模型组的IκBζ表达量约为67.73 pg/mg;CCFM1417组IκBζ表达量为119.35 pg/mg,与模型组相比有显著差异(P<0.01)。
前人研究表明,唾液链球菌、鼠李糖乳杆菌等可以抵抗白色念珠菌对小鼠口腔的侵袭,但其作用机制多局限于微生物间的直接竞争,尚未深入解析菌株与宿主的免疫互作机制[23-25]。本研究从菌株与宿主相互作用的层面出发,揭示了唾液联合乳杆菌CCFM1417菌体裂解物能够调控小鼠口腔抗感染指标mBD3、pIgR和SIgA的表达,进而对小鼠OPC有一定的预防作用,且其免疫调控机制与宿主的IL-17信号通路相关。
基于以上数据,唾液联合乳杆菌CCFM1417的菌体裂解物可通过激活宿主体内的IL-17/IκBζ通路,上调防御素mBD3的产生,这与TAYLOR等[13]的研究理论相吻合。另外,有研究表明IL-17细胞因子可促进黏膜表面pIgR的表达[21,26],这也更好地解释了CCFM1417组干预后pIgR和SIgA上调的原因。
3 结论
本研究基于口腔角质细胞模型,筛选得到了1株唾液联合乳杆菌CCFM1417能够较好地调控防御素HBD-2的分泌。在小鼠OPC模型中,唾液联合乳杆菌CCFM1417的菌体裂解物能够显著减少在造模期间白色念珠菌对宿主舌头的黏附与侵袭,并有效缓解造模期间小鼠体质量的急剧下降。机制解析表明,唾液联合乳杆菌CCFM1417干预激活IL-17/IκBζ信号通路上调了mBD3的表达,同时pIgR和SIgA水平的协同升高可能与IL-17的上调存在正向关联。该发现从宿主-微生物互作角度揭示了口腔共生菌调控黏膜免疫的新机制,为开发靶向先天免疫应答的精准抗感染疗法提供了重要的理论依据和实验基础。
[1] D’ENFERT C, KAUNE A K, ALABAN L R, et al.The impact of the Fungus-Host-Microbiota interplay upon Candida albicans infections:Current knowledge and new perspectives[J].FEMS Microbiology Reviews, 2021, 45(3):fuaa060.
[2] VILA T, SULTAN A S, MONTELONGO-JAUREGUI D, et al.Oral candidiasis:A disease of opportunity[J].Journal of Fungi, 2020, 6(1):15.
[3] VAZQUEZ-MUNOZ R, THOMPSON A, SOBUE T, et al.A prebiotic diet modulates the oral microbiome composition and results in the attenuation of oropharyngeal candidiasis in mice[J].Microbiology Spectrum, 2023, 11(5):e01734-23.
[4] LASS-FLÖRL C, KANJ S S, GOVENDER N P, et al.Invasive candidiasis[J].Nature Reviews Disease Primers, 2024, 10:20.DOI:10.1038/s41572-024-00503-3.
[5] PATEL M.Oral cavity and Candida albicans:Colonisation to the development of infection[J].Pathogens, 2022, 11(3):335.
[6] SWIDERGALL M, SOLIS N V, MILLET N, et al.Activation of EphA2-EGFR signaling in oral epithelial cells by Candida albicans virulence factors[J].PLoS Pathogens, 2021, 17(1):e1009221.
[7] PHAN Q T, SOLIS N V, CRAVENER M V, et al.Candida albicans stimulates formation of a multi-receptor complex that mediates epithelial cell invasion during oropharyngeal infection[J].PLoS Pathogens, 2023, 19(8):e1011579.
[8] 王娜, 韩琦, 桑建利.白色念珠菌的形态类型及致病性[J].生物学通报, 2015, 50(10):3-8.
WANG N, HAN Q, SANG J L.Morphological types and pathogenicity of Candida albicans[J].Bulletin of Biology, 2015, 50(10):3-8.
[9] KAWAI T, IKEGAWA M, ORI D, et al.Decoding Toll-like receptors:Recent insights and perspectives in innate immunity[J].Immunity, 2024, 57(4):649-673.
[10] DANIS J, MELLETT M.Nod-like receptors in host defence and disease at the epidermal barrier[J].International Journal of Molecular Sciences, 2021, 22(9):4677.
[11] SUGAWARA Y, UEHARA A, FUJIMOTO Y, et al.Toll-like receptors, NOD1, and NOD2 in oral epithelial cells[J].Journal of Dental Research, 2006, 85(6):524-529.
[12] UEHARA A, TAKADA H.Synergism between TLRs and NOD1/2 in oral epithelial cells[J].Journal of Dental Research, 2008, 87(7):682-686.
[13] TAYLOR T C, COLEMAN B M, ARUNKUMAR S P, et al.IκBζ is an essential mediator of immunity to oropharyngeal candidiasis[J].Cell Host &Microbe, 2023, 31(10):1700-1713.e4.
[14] SOLIS N V, FILLER S G.Mouse model of oropharyngeal candidiasis[J].Nature Protocols, 2012, 7(4):637-642.
[15] LAUNDER D, DILLON J T, WUESCHER L M, et al.Immunity to pathogenic mucosal C.albicans infections mediated by oral megakaryocytes activated by IL-17 and candidalysin[J].Mucosal Immunology, 2024, 17(2):182-200.
[16] 鲍孟媛. 黄连提取物通过gC1qR-EGFR/ERK/c-Fos轴诱导口腔上皮细胞内吞作用来缓解口咽念珠菌病[D].合肥:安徽中医药大学,2024.
BAO M Y.Coptidis rhizoma extract alleviates oropharyngeal candidiasis by gC1qR-EGFR/ERK/c-Fos axis-induced endocytosis of oral epithelial cells[D].Hefei:Anhui University of Chinese Medicine, 2024.
[17] CHEN M M, HU Z H, SHI J, et al.Human β-defensins and their synthetic analogs:Natural defenders and prospective new drugs of oral health[J].Life Sciences, 2024, 346:122591.
[18] 周海, 卫丽, 马萍.人β-防御素-2的研究进展[J].重庆医学, 2014, 43(11):1386-1387.
ZHOU H, ZHOU H, ZHOU H.Research progress of human β-defensin-2[J].Chongqing Medicine, 2014, 43(11):1386-1387.
[19] PEREZ-RODRIGUEZ A, ERASO E, QUIND S G, et al.Antimicrobial peptides with anti-Candida activity[J].International Journal of Molecular Sciences, 2022, 23(16):9264.
S G, et al.Antimicrobial peptides with anti-Candida activity[J].International Journal of Molecular Sciences, 2022, 23(16):9264.
[20] JOHANSEN F E, KAETZEL C S.Regulation of the polymeric immunoglobulin receptor and IgA transport:New advances in environmental factors that stimulate pIgR expression and its role in mucosal immunity[J].Mucosal Immunology, 2011, 4(6):598-602.
[21] JAFFAR Z, FERRINI M E, HERRITT L A, et al.Cutting edge:Lung mucosal Th17-mediated responses induce polymeric Ig receptor expression by the airway epithelium and elevate secretory IgA levels[J].Journal of Immunology, 2009, 182(8):4507-4511.
[22] JIE Z L, YANG J Y, GU M D, et al.NIK signaling axis regulates dendritic cell function in intestinal immunity and homeostasis[J].Nature Immunology, 2018, 19(11):1224-1235.
[23] ITO R, MINE Y, YUMISASHI Y, et al.In vivo efficacy of Lacticaseibacillus rhamnosus L8020 in a mouse model of oral candidiasis[J].Journal of Fungi, 2021, 7(5):322.
[24] ISHIJIMA S A, HAYAMA K, BURTON J P, et al.Effect of Streptococcus salivarius K12 on the in vitro growth of Candida albicans and its protective effect in an oral candidiasis model[J].Applied and Environmental Microbiology, 2012, 78(7):2190-2199.
[25] AZAD A, RANJBARAN A, ZARESHAHRABADI Z, et al.Protective effects of the probiotic bacterium Streptococcus thermophilus on Candida albicans morphogenesis and a murine model of oral candidiasis[J].Iranian Journal of Medical Sciences, 2021, 46(3):207-217.
[26] KUMAR P, MONIN L, CASTILLO P, et al.Intestinal interleukin-17 receptor signaling mediates reciprocal control of the gut microbiota and autoimmune inflammation[J].Immunity, 2016, 44(3):659-671.