肥胖症是指机体总脂肪含量过多和/或局部脂肪含量增多及分布异常[1],是我国第六大致死致残主要危险因素[2]。《中国居民营养与慢性病状况报告(2020年)》最新数据显示,我国成人中的超重或肥胖人群占比首次超过1/2[3]。肠道微生物群是胃肠道内复杂的生态系统,菌群及其代谢产物可以通过调节营养素的吸收和利用、调节食欲以及影响脂肪组织的发育和功能,对能量代谢产生实质性影响[4]。国内外研究报道证实肠道菌群与肥胖症和代谢性疾病的发生密切相关[5]。各种植物化学物质或天然产物可以通过重塑肠道菌群来缓解肥胖及其相关并发症。
花椒(Zanthoxylum bungeanum),芸香科植物,性辛、温,归脾、胃、肾经,是药食同源的代表之一,具有温中止痛、杀虫止痒的功效[6]。花椒因其产地的不同又被称为“秦椒”“蜀椒”。《神农本草经》中记载:“蜀菽味辛温……久服之,头不白,轻身增年,生川谷”。唐·孙思邈在《千金要方·食治篇》中也提到:“蜀椒,味辛,大热,主邪气,温中下气,留饮宿食”。可见花椒用于减脂历史悠久。花椒果皮中化学成分丰富,主要有挥发油、生物碱、酰胺、黄酮、木质素、香豆素、三萜类等化合物[7]。现代药理研究证明,花椒具有抗炎镇痛、抗氧化、杀虫、抗肿瘤等作用[8]。LI等[9]发现花椒提取物羟基-β-山椒素通过激活P13K/AKT通路起到抗氧化作用,魏鲟钰[10]研究证实花椒麻味物质通过抑制TNF-α/NF-κB信号通路抑制炎症反应的发生。氧化应激和炎症将脂肪积累引起的变化和多种健康问题的发展联系起来。目前,关于中药花椒能否减轻肥胖症的相关实验研究较少,且相关作用机制并不明确。本研究建立由高脂饮食(high fat diet,HFD)诱导的肥胖小鼠模型,期间给予或不给予花椒,检测小鼠血脂四项、观察肝、脂肪、结肠组织病理变化,并进行16S rDNA测序观察肠道菌群变化来探究花椒治疗肥胖的相关作用机制,为进一步临床应用提供实验依据。
1 材料与方法
1.1 材料与试剂
中药花椒,广东爱心大药房连锁有限公司(产地四川,批号23060101);高脂饲料(H10060,脂肪60%、蛋白质20%、碳水化合物20%,能量比),北京华阜康生物科技股份有限公司;基础饲料,斯贝福(北京)生物技术有限公司;甘油三酯(total triglycerides,TG)、总胆固醇(total cholesterol,TC)等测量试剂盒,深圳雷杜生命科技有限公司。
1.2 仪器与设备
AF-05S中药粉碎机,温岭市奥力中药机械有限公司;徕卡-2016转轮式切片机,德国徕卡公司;JT-12S自动脱水机,武汉俊杰电子有限公司;BMJ-A组织包埋机,常州郊区中威电子仪器厂;PHY-Ⅲ病理组织漂烘仪,常州市中威电子仪器有限公司;BA210Digital数码三目摄像显微镜,麦克奥迪实业集团有限公司。
1.3 实验方法
1.3.1 花椒水提液制备
参照文献[11-12]的方法,称取花椒中药饮片1 kg,使用中药粉碎机破碎磨粉,过60 目筛后,将花椒粉末混匀,干燥阴暗处密封保存。实验时,取一定量花椒粉末,浸泡30 min后,加入10倍质量超纯水,置于超声波清洗器中,设置参数温度60 ℃、超声波功率240 W,持续30 min。冷却后过滤浓缩,置于4 ℃冰箱贮存备用。
1.3.2 动物实验
1.3.2.1 动物模型和干预
健康C57BL/6J雄性小鼠60只,8周龄(18~25 g),陕西中医药大学实验动物中心,许可证号SYXK(陕)2022-008,饲养于陕西中医药大学实验动物中心无特定病原体级动物房,维持环境温度(22±2) ℃,湿度(50±15)%,光暗周期12 h/12 h循环,实验前,所有动物适应性饲养7 d,保证自由摄食及饮水。实验过程符合陕西中医药大学动物实验伦理委员会的相关规定(动物伦理审查备案编号:SUCMDL20231106002)。
实验将60只小鼠随机分成5组,每组12只。空白组(NC)采用普通饲料喂养,模型组(HFD)、花椒低剂量组(ZBL)、花椒中剂量组(ZBM)、花椒高剂量组(ZBH)饲喂高脂饲料。期间对照组和模型组每日灌胃等体积的生理盐水,花椒低、中、高剂量组每天灌胃等体积的0.6165、1.233、2.466 g/kg花椒溶液,其中花椒低剂量组干预给药参照成人的单日用量[6]推算小鼠等效剂量[13],每周测量2~3次小鼠体质量,灌胃处理8周。
1.3.2.2 血清学检测
第8周后,进行眼眶取血,静置50 min后,在冷冻离心机4 ℃、3 000 r/min离心15 min,取上层血清按照试剂盒说明书测量血脂水平(TG、TC)。
1.3.2.3 肝脏、脂肪和结肠组织病理学分析
将小鼠麻醉处死后,分离小鼠肝脏、附睾脂肪组织和结肠,并使用PBS清洗采集的组织,用滤纸沾干表面水分后,放置于4%(体积分数)多聚甲醛溶液中固定,经过脱水、石蜡包埋、制片、苏木精-伊红(hematoxylin-eosin,H&E)染色后,在光学显微镜200倍镜下观察各组小鼠肝脏、脂肪和结肠组织的结构变化并测量结肠组织的肌层肠壁厚度。
1.3.2.4 肠道菌群测序
在末次给药12 h后,用无菌冻存管收集小鼠粪便,置于-80 ℃冰箱保存待测。用DNA提取试剂盒提取粪便样品中的细菌基因组DNA,使用基迪奥生物科技有限公司illumina NovaSeq 6000测序系统进行肠道菌群16S rDNA(V3~V4区域)基因高通量测序,对测序结果进行α多样性分析和β菌群结构分析及功能预测分析。
1.4 数据处理
采用GraphPad Prism 8.0.2软件对实验数据进行处理,结果以“平均数±标准差”表示,采用ANOVA及Dunnett’s t检验进行组间差异性分析,P<0.05认为差异有统计学意义。
2 结果与分析
2.1 花椒对高脂饮食小鼠体质量、血脂水平的影响
如图1所示,HFD组小鼠体质量及其增长趋势均显著高于NC组,花椒补充降低了小鼠体质量与体质量增长速率。
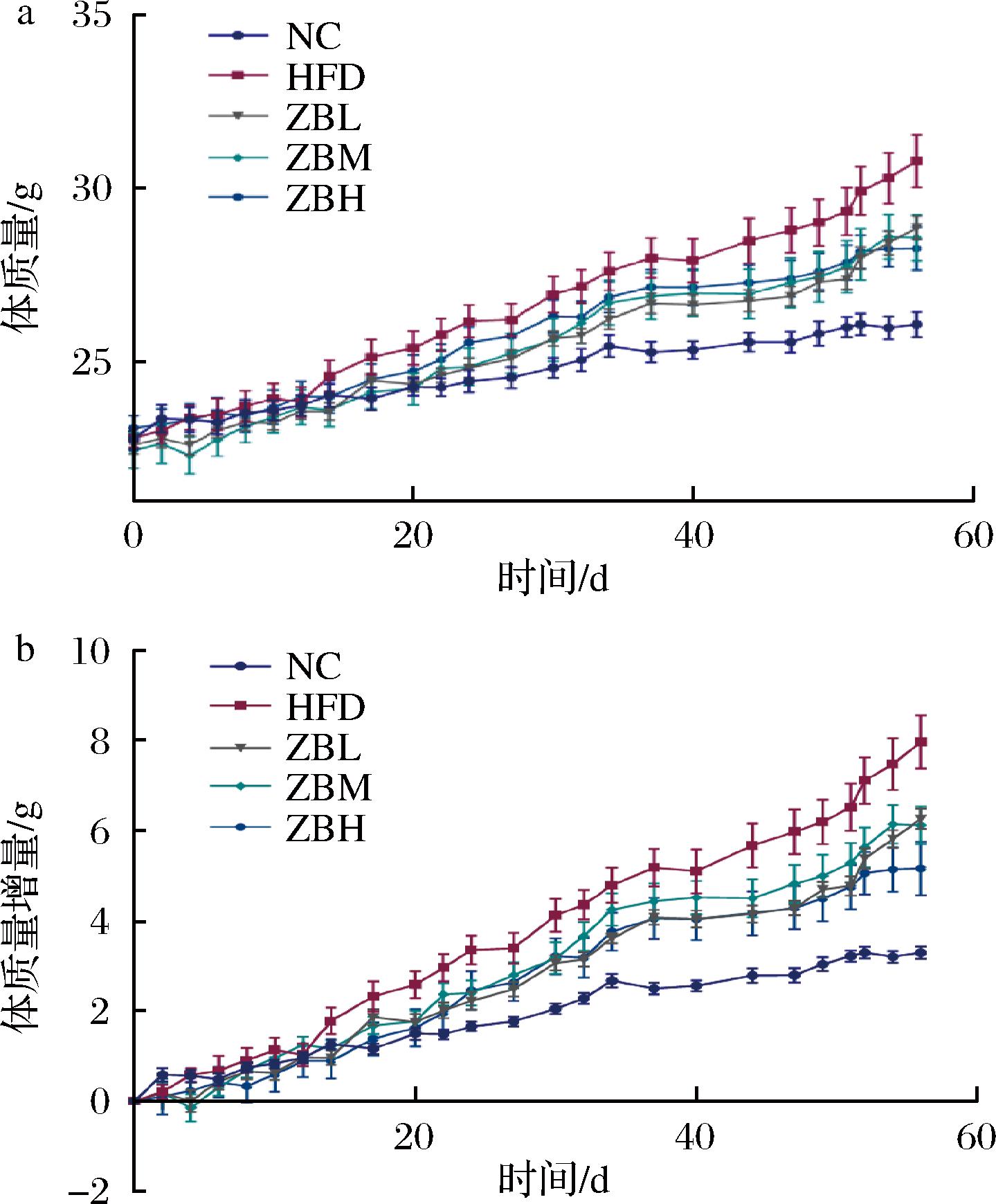
a-体质量变化;b-体质量增量
图1 小鼠体质量变化
Fig.1 Weight changes in mice
如图2所示,与NC组相比,HFD组小鼠血清TG和TC含量明显升高,花椒干预能够改善上述变化,结果呈现量效相关性。研究表明,高脂饮食能有效增加小鼠体质量,花椒补充在一定程度上能够控制小鼠由于高脂饮食造成的体质量变化,且能有效降低血清脂质水平。
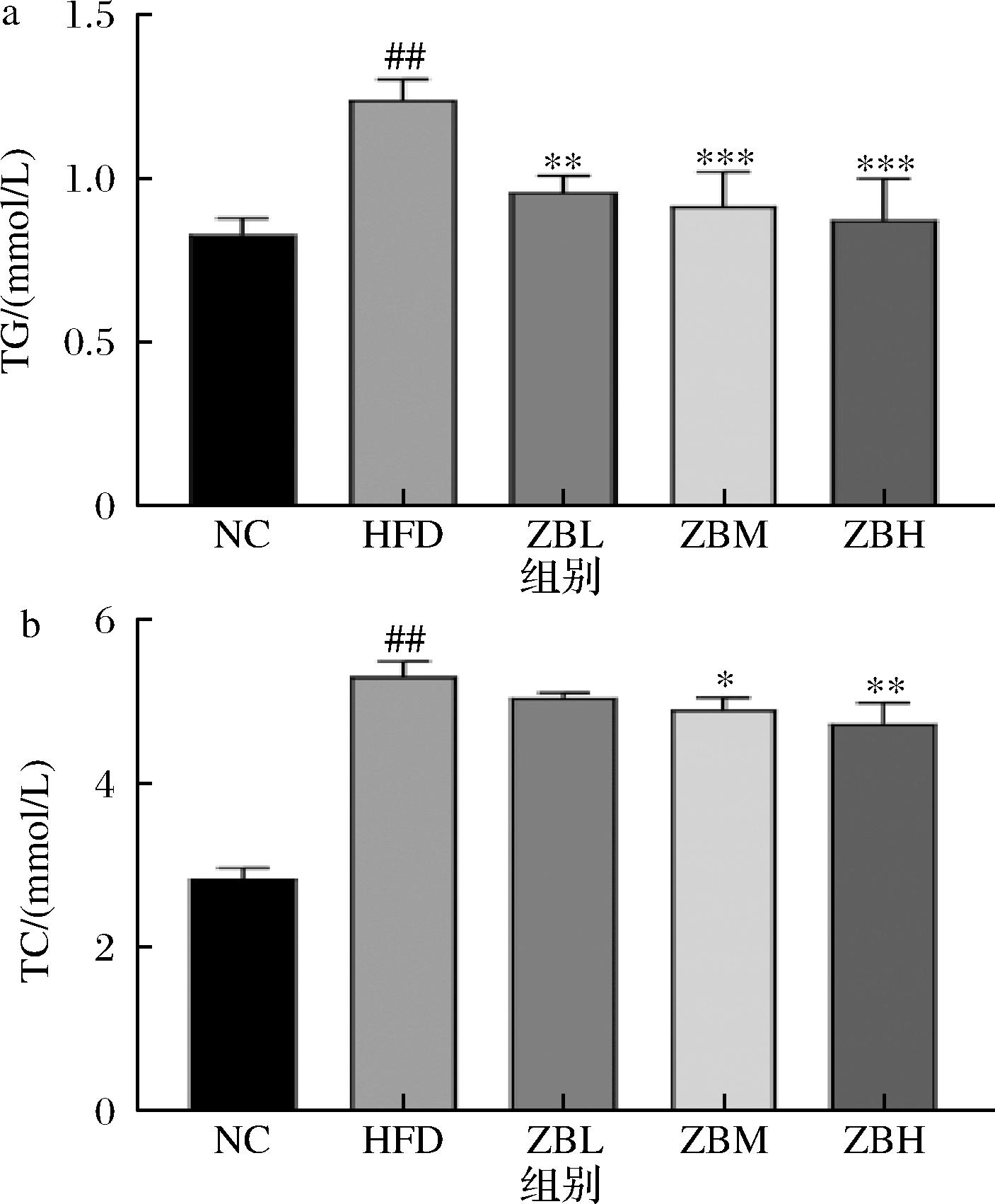
a-TG;b-TC
图2 小鼠血清水平
Fig.2 Lipid levels in mice
注:与NC组相比,##表示P<0.01;与HFD组相比,*表示P<0.05,**表示P<0.01,***表示P<0.001(下同)。
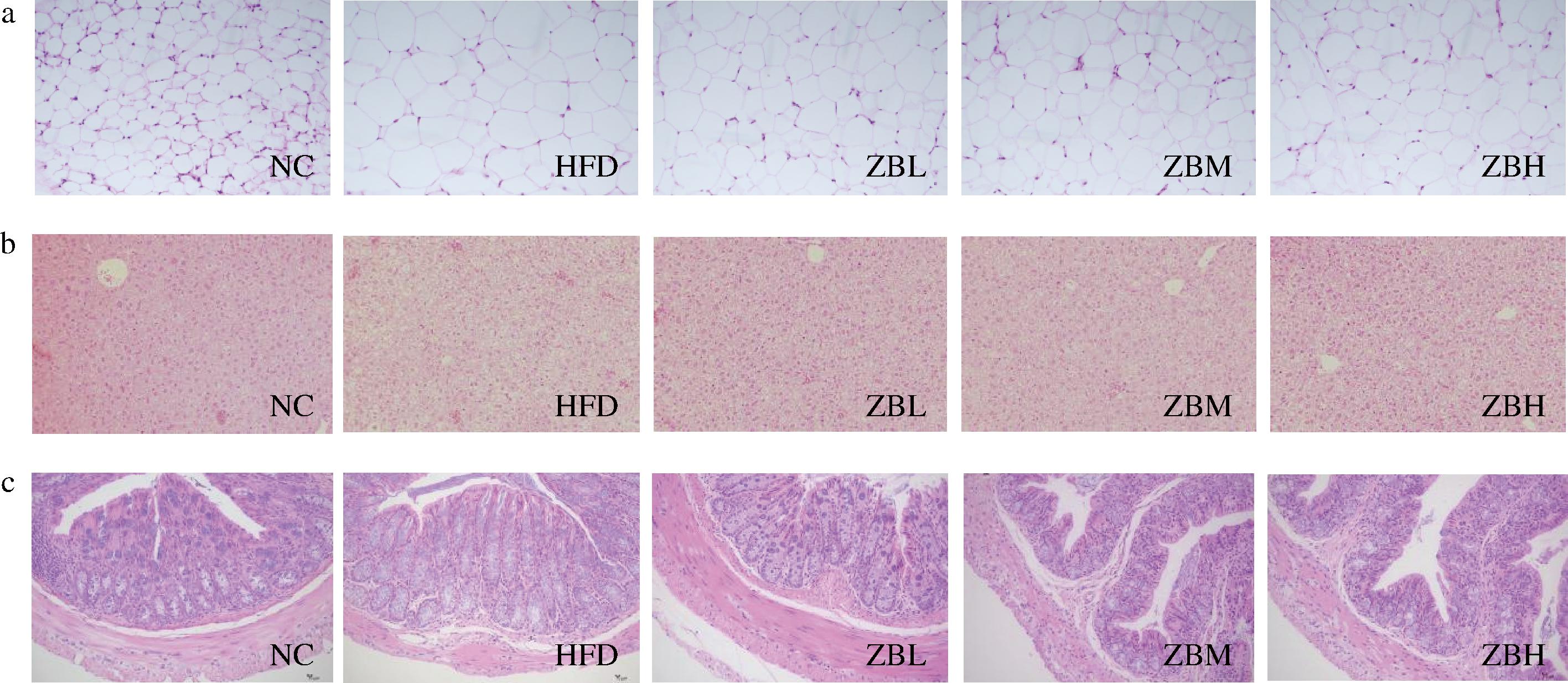
a-附睾脂肪;b-肝脏;c-结肠
图3 干预对小鼠组织形态的影响
Fig.3 Effect of the intervention on tissue morphology in mice
2.2 花椒对肥胖小鼠脂肪、肝脏和结肠组织的影响
高脂饮食引起的肥胖常伴随一定程度的脂质蓄积[14]。如图3-a所示,HFD喂养使得附睾脂肪组织中脂肪细胞肥大,花椒干预组脂肪细胞大小明显低于HFD组。肝脏中脂质蓄积与导致肝脂肪变性的脂质代谢相关[15]。如图3-b所示,相较NC组,HFD组肝内染色变浅,肝内脂滴增多,提示肝脏脂肪变性,花椒减轻了HFD诱导的脂滴在肝脏中的积聚,上述变化低中高剂量组未显示出明显差异。既往研究证实,高脂饮食可损伤肠道屏障继而诱发肠道炎症[16]。与NC组相比,HFD组小鼠结肠肌层肠壁厚度明显变薄。花椒干预后,小鼠结肠肌层厚度恢复,如图3-c、图4所示。综上,高脂喂养能引起小鼠脂肪、肝脏和结肠形态变化,花椒的使用改善了HFD诱导的脂肪组织肥大、肝脏脂肪变性及肠道屏障损伤,这种改变或许与小鼠肠道菌群重塑及炎症浸润变化有关。
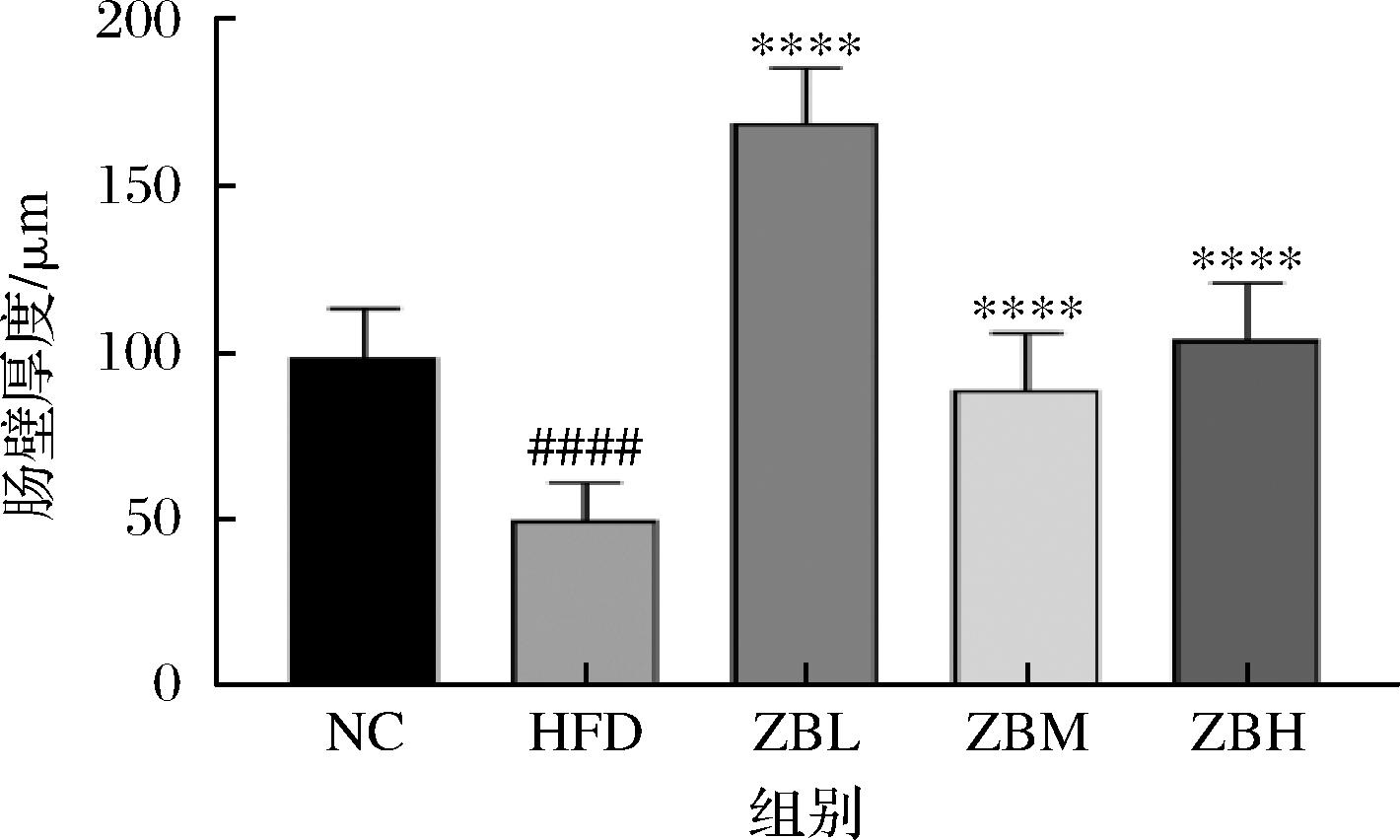
图4 小鼠结肠壁厚度
Fig.4 Thickness of the colonic wall in mice
注:与NC组相比,####表示P<0.01;与HFD组相比,****P<0.000 1。
2.3 花椒对高脂饮食小鼠肠道菌群的影响
2.3.1 肠道菌群多样性分析
参与检测的样品平均有效序列为106 061条,产生了1 856个分类操作单元(operational taxonomic unit,OTU)。如图5所示,稀释曲线均趋于平缓,表明3组小鼠粪便中的菌群数量从群落丰富度、均匀度,多样性及覆盖度方面均满足测序。Sobs、Chao1和Ace指数反映物种丰富度,Shannon、Simpson指数可用于衡量物种均匀度。如表1所示,与NC组相比,HFD组Sobs、Chao1、Ace、Shannon、Simpson指数均降低,而ZBM组指数均高于HFD组。主坐标分析(principal coordinates analysis,PCoA)可用于反映微生物群落的β多样性,距离越近越相近。如图6所示,基于Bray-Curtis距离进行PCoA可知,R2为0.974(P=0.003),PCo1贡献度为81.39%,PCo2贡献度为17.07%,NC组与HFD组间距离较大,相较而言ZBM距离较近。上述结果表明高脂饮食喂养显著降低小鼠肠道微生物群α多样性和β多样性,花椒干预能够部分恢复肥胖小鼠的肠道微生物菌群多样性。
表1 肠道菌群α多样性统计表
Table 1 Statistical of α-diversity of intestinal microbiota
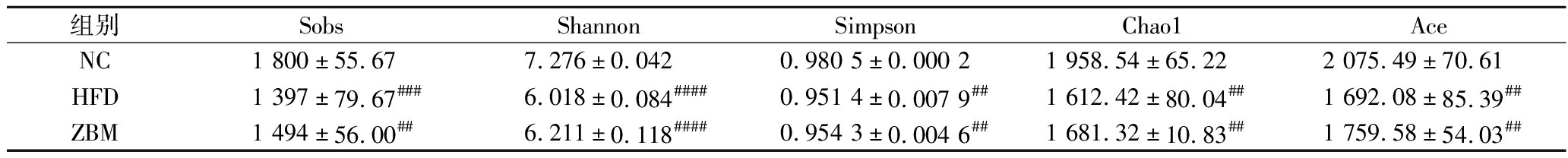
组别SobsShannonSimpsonChao1AceNC1 800±55.677.276±0.0420.980 5±0.000 21 958.54±65.222 075.49±70.61HFD1 397±79.67###6.018±0.084####0.951 4±0.007 9##1 612.42±80.04##1 692.08±85.39##ZBM1 494±56.00##6.211±0.118####0.954 3±0.004 6##1 681.32±10.83##1 759.58±54.03##
注:与NC组相比,#P<0.05,##P<0.01,###P<0.001,####P<0.000 1。
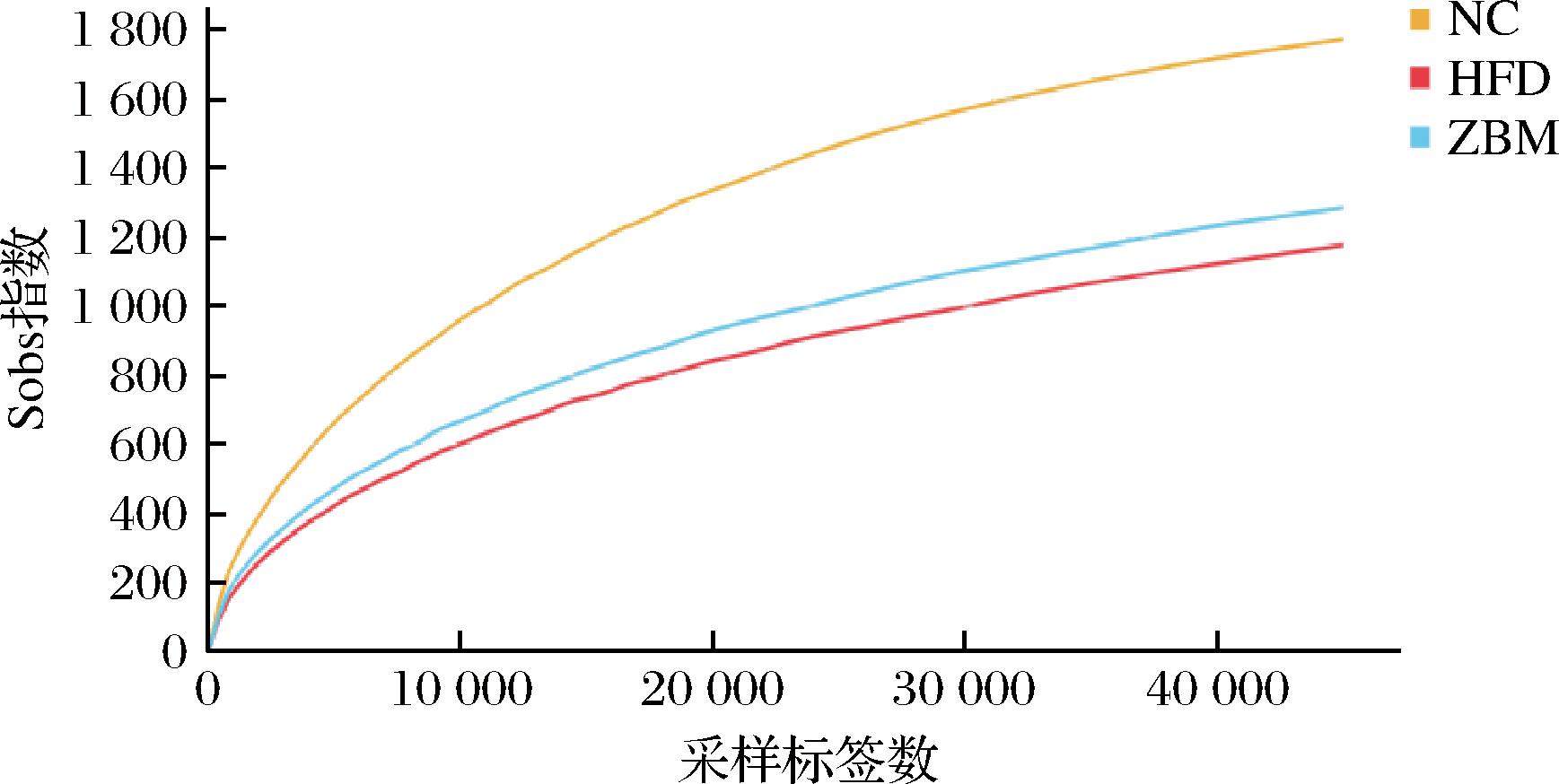
图5 稀释曲线
Fig.5 Dilution curve
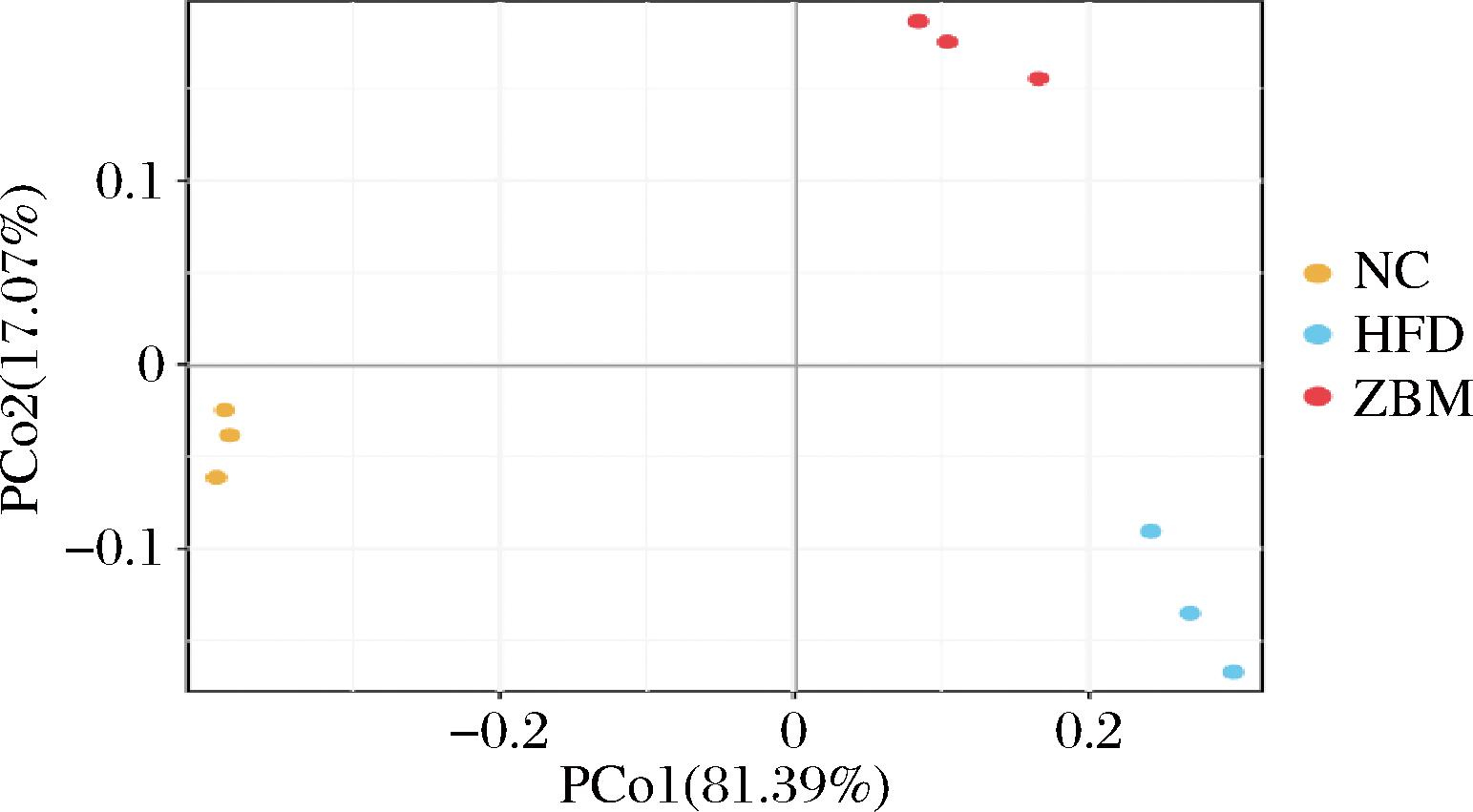
图6 PCoA散点图
Fig.6 PCoA scatter plot
2.3.2 门水平上的菌群相对丰度与显著性分析
如图7-a所示,在门水平上,厚壁菌门(Firmicutes)、拟杆菌门(Bacteroidota)、脱硫杆菌门(Desulfobacterota)等菌门为优势菌门,与NC组相比,HFD组Firmicutes、Desulfobacterota显著升高,Bacteroidota显著降低,Firmicutes/Bacteroidota(F/B)比值显著上调(图7-b)。如图7-b所示,ZBM组显著富集了Firmicutes和Bacteroidota,使F/B比值标准化,且大幅度降低了肥胖小鼠肠内有害菌Desulfobacterota相对丰度,少量提升了髌骨菌门(Patescibacterias)相对丰度(图7-c)。综上,花椒干预能有效地调控小鼠肠道微生物群落结构,改善高脂饮食引起的肠道菌群门水平紊乱。
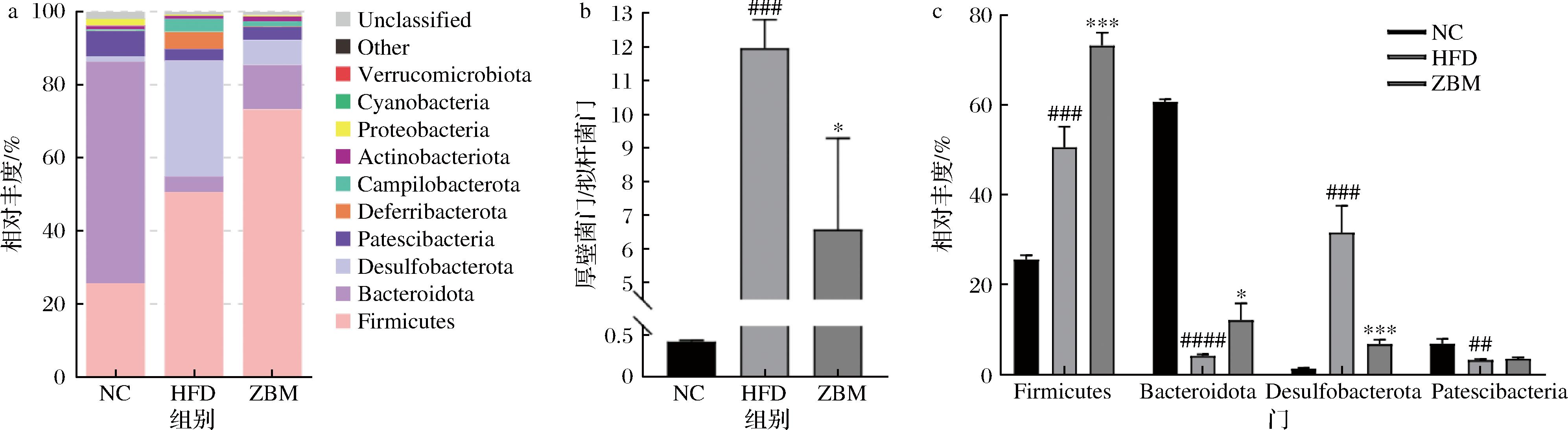
a-门水平相对丰度;b-厚壁菌门/拟杆菌门;c-部分菌群门水平相对丰度
图7 小鼠肠道菌群门水平物种相对丰度
Fig.7 Relative abundance of mice intestinal flora at phylum level
注:ns表示无统计学差异。
2.3.3 科水平和属水平上的菌群相对丰度与显著性分析
如图8-a所示,在科水平的主要菌群组成为鼠杆菌科(Muribaculaceae)、脱硫弧菌科(Desulfovibrionaceae)、乳杆菌科(Lactobacillaceae)、毛螺菌科(Lachnospiraceae)、丹毒丝菌科(Erysipelotrichaceae)、消化链球菌科(Peptostreptococcaceae)等。其中与肥胖密切相关的主要包括Muribaculaceae、Lactobacillaceae和Desulfovibrionaceae,HFD组肠内Muribaculaceae相对丰度显著低于NC组,而Desulfovibrionaceae的丰度显著高于NC组,花椒干预显著逆转了这一转变,且大幅提高了Lactobacillaceae的相对丰度(图8-b)。如图8-c所示,在属水平上的优势菌群为乳杆菌属(Lactobacillus)、罗姆布茨菌属(Romboutsia)、杜氏杆菌属(Dubosiella)、候选糖单胞菌属(Candidatus_Saccharimonas)、肠易伸菌属(Colidextribacter)、粪杆菌属(Faecalibaculum)、拟杆菌属(Bacteroides)等。其中Lactobacillus、Romboutsia、Dubosiella和Bacteroides与肥胖关联较大,如图8-d所示,与NC组相比,HFD组Lactobacillus、Romboutsia相对丰度上调,Dubosiella和Bacteroides相对丰度下调。经花椒干预后,Lactobacillus、Romboutsia、Dubosiella和Bacteroides相对丰度显著上调,调节了肠道内有益菌和有害菌占比,减轻了高脂饮食对机体的损害。
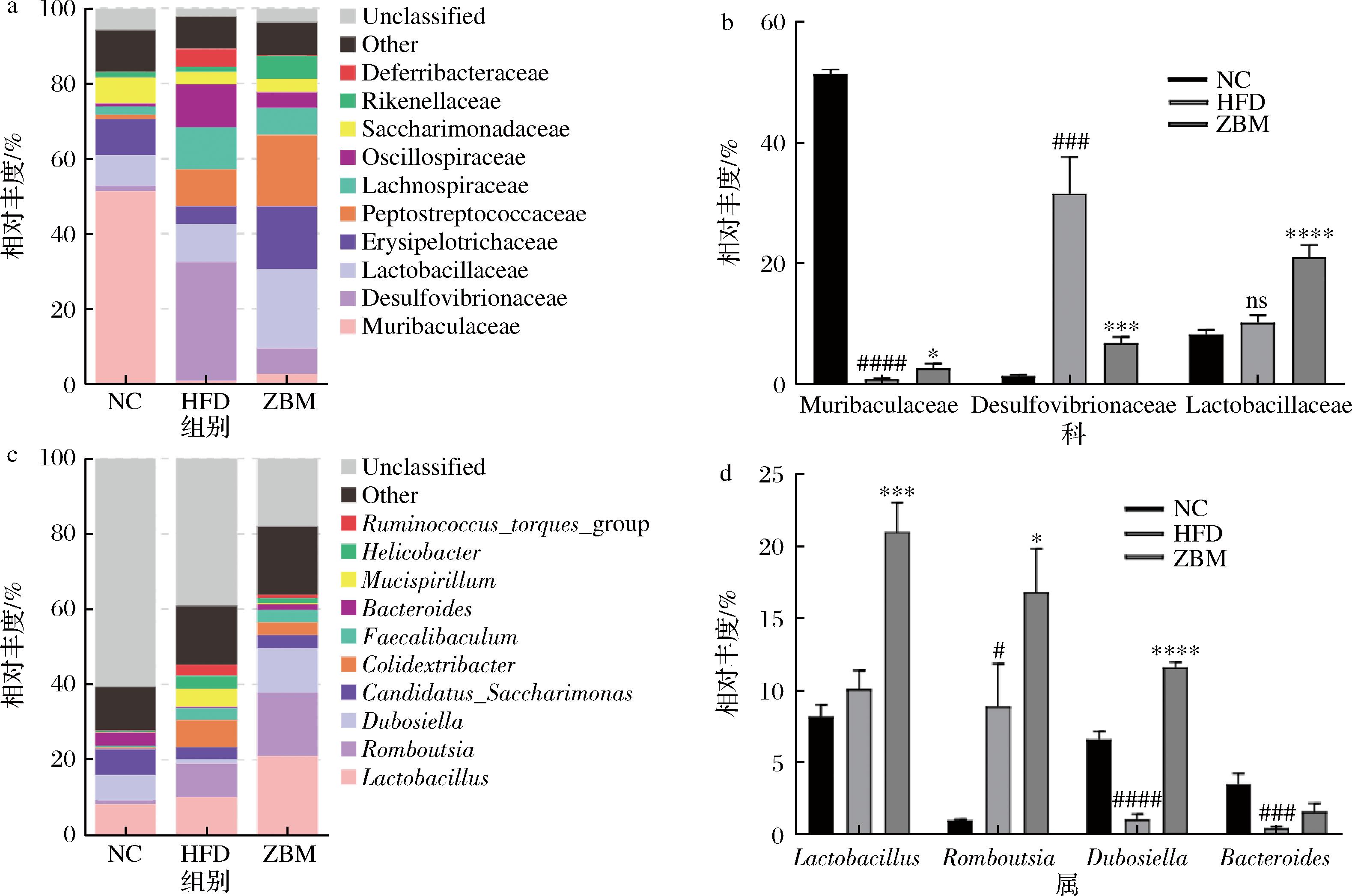
a-科水平相对丰度;b-部分菌群科水平相对丰度;c-属水平相对丰度;d-部分菌群属水平相对丰度
图8 小鼠肠道菌群科水平和属水平相对丰度
Fig.8 Relative abundance of mice intestinal flora at family level and genus level
2.3.4 肠道菌群结构差异性分析
将属水平相对丰度排名前20的菌群,根据物种丰度及注释信息进行相似性聚类,通过颜色梯度及菌属相似程度来反映各组间小鼠肠道菌群结构的相似性及多样性。如图9所示,NC组与HFD组间肠道菌群在属水平上存在显著结构差异,ZBM组与HFD组既存在结构差异也存在一定的相似性。而ZBM组与NC组菌群结构相似度更为接近,表明花椒干预对于肥胖小鼠的肠道菌群改善效果良好。
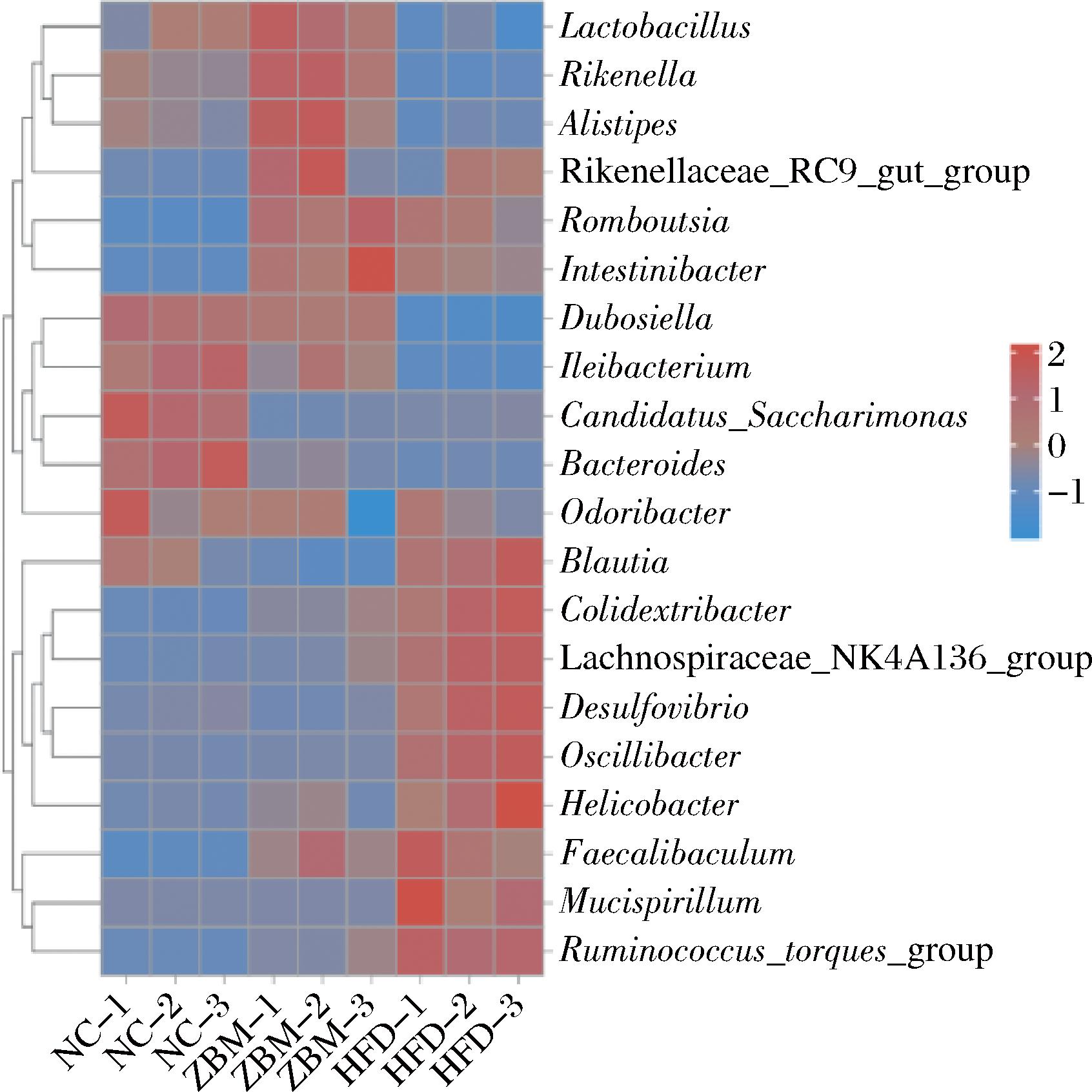
图9 小鼠肠道菌群的热图
Fig.9 Heatmap of intestinal flora in mice
2.3.5 肠道菌群功能预测分析
肠道菌群结构组成与生物学功能密切相关。PICRUSt软件可基于标记基因序列来预测功能丰度。如图10所示,与HFD组相比,ZBM组肠道菌群功能中,碳水化合物代谢(Carbohydrate metabolism)、辅因子及维生素代谢(Metabolism of cofactors and vitamins)、氨基酸代谢(Amino acid metabolism)、能量代谢(Energy metabolism)、外源物质的生物降解和代谢(Xenobiotics biodegradation and metabolism)、其他次生代谢物的生物合成(Biosynthesis of other secondary metabolites)、运输和分解代谢(Transport and catabolism)等代谢途径显著下调(P<0.05),提示花椒干预可以缓解肠道菌群代谢功能。
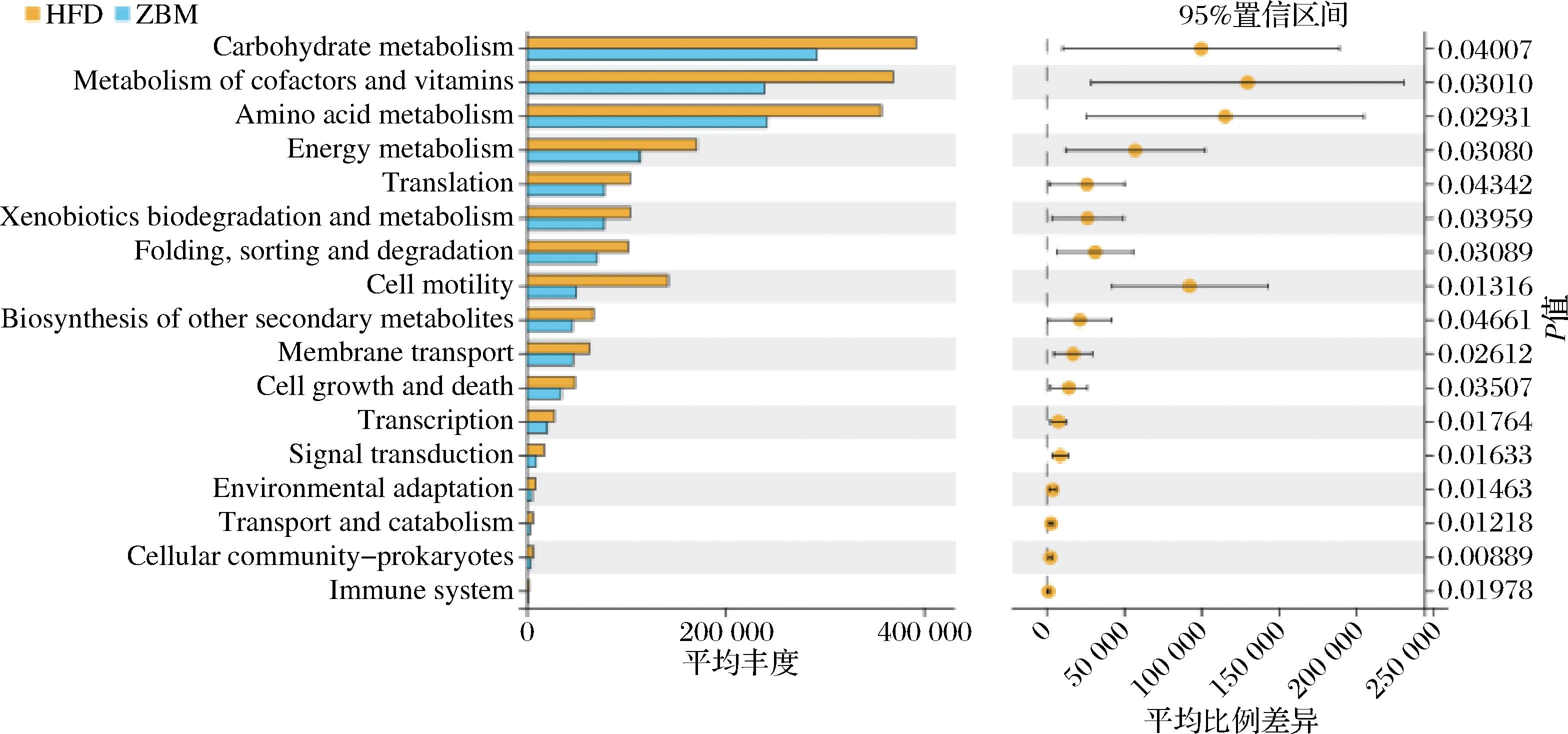
图10 小鼠肠道菌群功能预测分析
Fig.10 Functional prediction analysis of intestinal flora in mice
3 讨论
长期高脂饮食可诱发机体肥胖及其相关代谢紊乱,中药由于具有多成分、多途径、多靶点的协同调控作用而备受关注,而这种机制常常与肠道微生态的改变相关。TC是血液中所有脂蛋白所含胆固醇的总和,TG是动脉粥样硬化斑块形成和发展的重要因素[17]。本实验证明,花椒能够有效降低高脂饮食诱导的肥胖小鼠体质量及血清TC和TG水平,从而改善HFD引起的脂代谢紊乱。肝脏和脂肪是内源性脂质合成和代谢的主要部位,花椒干预降低了HFD造成的肝损伤及脂肪组织肥大。肥胖作为炎症性肠病的危险因素,通常伴随一定程度的肠道屏障损伤和炎症浸润。本研究证明,花椒干预修复了HFD引起的小鼠结肠肌层肠壁损伤,这可能与花椒改善肠道微环境相关。
既往研究显示,小鼠长期高脂喂养易刺激肝脏分泌过量胆汁酸,并诱导肠道促炎环境的形成,引发慢性低度炎症,抑制肠道内有益菌生长[18]。有害菌因其对胆汁酸的耐受性较强成为肠内优势菌群,产生内毒素等有害代谢产物,参与破坏肠道屏障,加上膳食纤维的缺乏,进一步造成肠道菌群失衡。本研究通过16S rDNA扩增测序技术分析发现,花椒干预能够部分提升肥胖小鼠的肠道菌群多样性,并显著调节肠内有益菌和有害菌占比,改善高脂饮食诱发的肠道菌群紊乱。在门水平上,花椒干预显著提升了肥胖小鼠的Bacteroidota相对丰度,降低了F/B比值及Desulfobacterota相对丰度。Firmicutes与Bacteroidota是肠道菌群的主要菌门,大多数研究显示,F/B比值升高与Bacteroidota相对丰度下降,均与肥胖程度呈正相关[19]。高脂饮食除了升高F/B比值外,还大幅度增加了肠内有害菌Desulfobacterota的相对丰度。QI等[20]的研究揭示了Desulfobacterota调控宿主代谢的一条关键途径:该菌门在代谢综合征患者体内富集,可通过产生H2S抑制肠道激素胰高血糖素样肽-1的合成,进而破坏宿主代谢稳态。花椒作为温性的中药材,其温肾助阳之功效恰好契合肥胖“脾肾阳虚”的核心病机[21],推测这一治疗作用可能与花椒有效调控Desulfobacterota的相对丰度相关,其具体分子机制仍需进一步深入探究。Muribaculaceae 属于拟杆菌目鼠杆菌科,该菌科可分解内源性与外源性多糖并产生短链脂肪酸。本研究发现,高脂饮食会显著降低其相对丰度,这与既往研究报道结果一致;而花椒干预后,该菌科的相对丰度得以明显回升。这一结果进一步印证了Muribaculaceae丰度与饮食模式密切相关的特性[22]。LIM等[23]研究表明,乳杆菌属(Lactobacillus)通过减少肠道胆固醇的吸收,抑制肠内致病菌的繁殖及减轻炎症抗肥胖。本实验中,花椒干预显著增加了Lactobacillus的相对丰度,增加了肠内有益菌占比。MA等[24]研究显示,牡蛎可通过富集Lactobacillus等有益菌改善HFD诱导的肠道菌群失调,这与本研究相似。此外,YIN等[25]研究表明,Romboutsia可改善肥胖大鼠的脂质代谢,花椒干预显著提升了这一菌种的相对丰度。Dubosiella、Bacteroides与肥胖发生发展呈负相关,高脂饮食喂养后,Dubosiella、Bacteroides丰度下降,花椒干预逆转了这一趋势。PAN等[26]研究表明,桑叶提取物可提高HFD喂养小鼠中Dubosiella等有益菌相对丰度从而抵抗肥胖,而Dubosiella与特定磷脂呈负相关,这与本研究结果一致。提示花椒防治小鼠肥胖的作用与改善肠道微生态密切相关。花椒干预不仅对于肥胖小鼠肠道菌群结构产生了影响,对代谢功能也产生了调控效应。肠道菌群在维持宿主氨基酸稳态[27]和糖脂代谢稳态[28]方面起着重要作用。氨基酸稳态紊乱与糖尿病等疾病进展和恶化密切相关,LI等[29]研究发现肠道微生物通过高效利用相对较大比例的肠道氨基酸,从而减少宿主组织和器官对氨基酸的吸收和利用。花椒干预可显著下调肥胖小鼠肠道菌群相关的碳水化合物代谢、氨基酸代谢及能量代谢等关键代谢功能,减少机体对各类营养物质的吸收效率,进而有效改善肥胖表型。
4 结论
本研究表明,花椒干预可以有效改善高脂饮食诱导的小鼠肥胖和脂质代谢紊乱,同时调节了小鼠肠道微生态紊乱,优化了肠道内有益菌占比,减轻了高脂饮食对机体造成的损害。而花椒干预能显著改善由高脂饮食引起的有害菌脱硫弧菌科丰度升高,进一步阐明花椒对于肥胖治疗的潜力,也为药食同源物质在肥胖治疗领域的开发和应用奠定理论基础。
[1] 孙铭遥, 陈伟.《中国超重/肥胖医学营养治疗指南(2021)》解读[J].协和医学杂志, 2022, 13(2):255-262.
SUN M Y, CHEN W.Interpretation of the Chinese guidelines on medical nutritional therapy for overweight/obesity(2021)[J].Medical Journal of Peking Union Medical College Hospital, 2022, 13(2):255-262.
[2] GBD 2019 R F C.Global burden of 87 risk factors in 204 countries and territories, 1990-2019:A systematic analysis for the Global Burden of Disease Study 2019[J].Lancet, 2020, 396(10258):1223-1249.
[3] 中国居民营养与慢性病状况报告(2020年)[J].营养学报,2020,42(6):521.
Nutrition and chronic diseases in China (2020)[J].Acta Nutrimenta Sinica, 2020,42(6):521.
[4] COLANGELI L, ESCOBAR MARCILLO D I, SIMONELLI V, et al.The crosstalk between gut microbiota and white adipose tissue mitochondria in obesity[J].Nutrients, 2023, 15(7):1723.
[5] CANI P D, VAN HUL M.Gut microbiota in overweight and obesity:Crosstalk with adipose tissue[J].Nature Reviews Gastroenterology &Hepatology, 2024, 21(3):164-183.
[6] 国家药典委员会. 中华人民共和国药典:一部[M].北京:中国医药科技出版社, 2020.
Chinese Pharmacopoeia Commission.Pharmacopoeia of the People’s Republic of China:the First One[M].Beijing:China Medical Science and Technology Press, 2020.
[7] 娄京荣. 花椒化学成分及药理活性研究[D].济南:济南大学, 2019.
LOU J R.The study on the pharmacological activities and chemical constituents from barks of Zanthoxylum bungeanum Maxim[D].Jinan:University of Jinan, 2019.
[8] 贺梦媛, 张兵, 徐桐, 等.花椒化学成分、药理作用研究进展及质量标志物预测分析[J].山东中医杂志, 2022, 41(12):1351-1358.
HE M Y, ZHANG B, XU T, et al.Research progress on chemical constituents and pharmacological effects of Huajiao (Zanthoxyli pericarpium) and predictive analysis of quality markers[J].Shandong Journal of Traditional Chinese Medicine, 2022, 41(12):1351-1358.
[9] LI R L, ZHANG Q, LIU J, et al.Hydroxy-α-sanshool possesses protective potentials on H2O2-stimulated PC12 cells by suppression of oxidative stress-induced apoptosis through regulation of PI3K/Akt signal pathway[J].Oxidative Medicine and Cellular Longevity, 2020, 2020:3481758.
[10] 魏鲟钰. 花椒麻味物质对2型糖尿病大鼠蛋白质代谢影响的机制研究[D].重庆:西南大学, 2021.
WEI X Y.The effects and mechanisms of Zanthoxylum alkylamides on protein metabolism in type 2 diabetes mellitus rats[D].Chongqing:Southwest University, 2021.
[11] 尹含靓, 肖何, 邓高文, 等.基于GC-IMS技术分析不同香辛料水煮液的风味物质组成差异[J].食品工业科技, 2021, 42(17):278-284.
YIN H L, XIAO H, DENG G W, et al.Based on GC-IMS technology to analyze the difference in flavor composition of different spice boiling liquids[J].Science and Technology of Food Industry, 2021, 42(17):278-284.
[12] 贺宇, 贺泽民, 薛雅荣, 等.花椒水提液的体外抗氧化活性研究[J].河南工业大学学报(自然科学版), 2016, 37(5):87-90.
HE Y, HE Z M, XUE Y R, et al.In vitro antioxidant activities of water extraction liquid from Zanthoxylum bungeanum[J].Journal of Henan University of Technology (Natural Science Edition), 2016, 37(5):87-90.
[13] 黄继汉, 黄晓晖, 陈志扬, 等.药理试验中动物间和动物与人体间的等效剂量换算[J].中国临床药理学与治疗学, 2004, 9(9):1069-1072.
HUANG J H, HUANG X H, CHEN Z Y, et al.Dose conversion among different animals and healthy volunteers in pharmacological study[J].Chinese Journal of Clinical Pharmacology and Therapeutics, 2004, 9(9):1069-1072.
[14] SAKERS A, DE SIQUEIRA M K, SEALE P, et al.Adipose-tissue plasticity in health and disease[J].Cell, 2022, 185(3):419-446.
[15] CHU Z X, HU Z M, LUO Y, et al.Targeting gut-liver axis by dietary lignans ameliorate obesity:Evidences and mechanisms[J].Critical Reviews in Food Science and Nutrition, 2025, 65(2):243-264.
[16] YANG N, PANG Y S, ZHENG Y L, et al.Nobiletin restores the intestinal barrier of HFD-induced obese mice by promoting MHC-Ⅱ expression and lipid metabolism[J].Molecular Medicine, 2025, 31(1):26.
[17] ATTANASIO A, ABOYANS V, PIEPOLI M.Editorial comments:focus issue on obesity, food consumption, blood lipids, and cardio-metabolic risk[J].European Journal of Preventive Cardiology, 2024, 31(8):917-919.
[18] LIN H, AN Y P, TANG H R, et al.Alterations of bile acids and gut microbiota in obesity induced by high fat diet in rat model[J].Journal of Agricultural and Food Chemistry, 2019, 67(13):3624-3632.
[19] LIU B N, LIU X T, LIANG Z H, et al.Gut microbiota in obesity[J].World Journal of Gastroenterology, 2021, 27(25):3837-3850.
[20] QI Q Q, ZHANG H J, JIN Z Y, et al.Hydrogen sulfide produced by the gut microbiota impairs host metabolism via reducing GLP-1 levels in male mice[J].Nature Metabolism, 2024, 6(8):1601-1615.
[21] 杲春阳, 秦海宁, 邱林杰, 等.基于“气化”理论探讨温阳药治疗肥胖的作用[J].现代中医药, 2024,44(2):37-41.
GAO C Y, QIN H N, QIU L J, et al.Exploration of warming Yang medicine effects in treating obesity based on “qi transformation” theory[J].Modern Chinese Medicine, 2024, 44(2):37-41.
[22] ZHU Y Q, CHEN B R, ZHANG X Y, et al.Exploration of the Muribaculaceae family in the gut microbiota:Diversity, metabolism, and function[J].Nutrients, 2024, 16(16):2660.
[23] LIM S Y M, CHONG E J, MAH W Y, et al.Exploring the anti-obesity effects of Lactobacillus in C57BL/6 mice:Mechanisms, interventions, and future directions[J].Letters in Applied Microbiology, 2025, 78(3):ovaf024.
[24] MA Y Y, ZHU L Q, KE H W, et al.Oyster (Crassostrea gigas) polysaccharide ameliorates obesity in association with modulation of lipid metabolism and gut microbiota in high-fat diet fed mice[J].International Journal of Biological Macromolecules, 2022, 216:916-926.
[25] YIN H G, HUANG J H, GUO X Z, et al.Romboutsia lituseburensis JCM1404 supplementation ameliorated endothelial function via gut microbiota modulation and lipid metabolisms alterations in obese rats[J].FEMS Microbiology Letters, 2023, 370:fnad016.
[26] PAN Y, SONG Y S, ZHAO M J, et al.Mulberry leaf extract ameliorates high-fat diet-induced obesity in mice by regulating the gut microbiota and metabolites[J].Food Bioscience, 2024, 62:105359.
[27] LIN R, LIU W T, PIAO M Y, et al.A review of the relationship between the gut microbiota and amino acid metabolism[J].Amino Acids, 2017, 49(12):2083-2090.
[28] FAN Y, PEDERSEN O.Gut microbiota in human metabolic health and disease[J].Nature Reviews Microbiology, 2021, 19(1):55-71.
[29] LI T T, CHEN X, HUO D, et al.Microbiota metabolism of intestinal amino acids impacts host nutrient homeostasis and physiology[J].Cell Host &Microbe, 2024, 32(5):661-675.e10.