过去几十年里,肥胖人群数量逐渐增多,而肥胖会引发高血压、高血脂,进而诱发心血管相关疾病[1]。而现代饮食结构中,高脂饮食的长期摄入是主要影响因素。相关研究表明,肠道菌群在高脂饮食诱导的代谢紊乱中扮演关键角色,而高脂饮食可破坏肠道微生物生态平衡,导致厚壁菌门(Firmicutes)/拟杆菌门(Bacteroidetes)比例升高,类杆菌属S24-7和瘤胃菌科等丁酸盐产生菌以及副杆菌属、大肠杆菌、志贺菌等革兰氏阴性条件致病菌的相对丰度升高,拟杆菌属、杆菌属、肠杆菌属等有益菌群丰度降低,短链脂肪酸含量降低[2-4]。近年来,关于膳食成分对肠道菌群影响的研究日益受到关注,诸如膳食纤维和食用菌含有的生物活性成分(如多糖),能够调节肠道菌群组成,并有助于重建健康的肠道微生物群落[5-6]。
菊粉作为一种天然的水溶性膳食纤维,凭借其持水性、凝胶性和甜度特性,被广泛应用于食品工业领域。菊粉具有调节血糖代谢、降低血清胆固醇、增强免疫调节功能,降低结肠癌风险等生理作用,并能选择性地促进肠道双歧杆菌、乳杆菌等有益菌增殖,可通过微生物发酵产生短链脂肪酸,调节肠道菌群平衡,可用于医药领域缓解便秘、肠易激综合征及炎症性肠病的辅助治疗[7-8]。冯焱等[9]通过添加质量分数10%的菊粉干预高脂饲粮喂养的小鼠,干预8周后血清低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)和总胆固醇(total cholesterol,TC)水平显著降低,高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)水平升高,超氧化物歧化酶和谷胱甘肽过氧化物酶活性升高,并可通过调节结肠菌群结构及其代谢产物短链脂肪酸的产生,调节血脂水平、血清与海马中炎症因子含量,对T2D小鼠海马神经元损伤和认知行为起到改善作用。LI等[10]研究发现,菊粉可通过提高双歧杆菌和乳酸菌的比例来降低内毒素血症的发生风险;而菌群所产短链脂肪酸的菌属比例及浓度提升,还能发挥抗炎作用,进而预防高脂饮食诱导的内毒素血症与炎症反应。
黑木耳多糖(Auricularia auricula polysaccharides,AAP)是从黑木耳中提取的一类具有生物活性的天然高分子化合物,主要由葡萄糖、甘露糖、木糖、阿拉伯糖等单糖组成。AAP具有抗氧化、免疫调节、降血脂、抗动脉粥样硬化、调节肠道菌群等生物活性。作为天然抗氧化剂和膳食补充剂应用于食品加工、功能性食品开发中。在疾病预防中,已为心血管疾病、高血脂、糖尿病等慢性病患者,设计了针对性功能性配方[11]。张廷婷等[12]使用AAP对高脂饮食大鼠进行干预6周,研究发现AAP能够显著降低高脂饮食大鼠的肝重及肝指数,血清TC和LDL-C含量,并且大鼠的肝脏脂肪堆积程度较对照组有所减轻。ZHAO等[13]使用AAP给予6周龄雄性 ICR 小鼠5周管饲喂养,高通量测序发现,AAP 喂养小鼠粪便微生物群的多样性、丰富度和组成发生改变,厚壁菌门/拟杆菌门比率显著降低(P<0.05),卟啉单胞菌科(Porphyromonadaceae)和拟杆菌科(Bacteroidaceae)相对丰度有所增加。
目前对菊粉、AAP的研究都是针对两者单独的生理活性,而忽视了两者复配的协同作用。基于团队前期的研究积累与本地资源优势,以利用菊粉优化肠道微生态作为基础,进而增强AAP在调节脂质代谢中的效能。通过探讨补充不同比例菊粉复配AAP对高脂饮食小鼠血清、肝脏脂肪堆积及肠道菌群的影响,以期为开发功能性食品、对地方特色资源高值化利用提供参考价值。
1 材料与方法
1.1 材料与试剂
菊粉(质量分数95%),陕西森弗天然制品有限公司;AAP(质量分数50%),西安瑞迪生物科技有限公司;DPPH,福州飞净生物科技有限公司;甘氨胆酸钠、牛磺胆酸钠、胰蛋白酶(猪胰脏)(1∶250)、胃蛋白酶(猪源)(1∶10 000)、脂肪酶(猪胰)(30 000 U/g),上海源叶生物科技有限公司。
KM小鼠70只,雄性,6~8周龄,体重(20±2) g,SPF级,均购于西安交通大学医学部实验动物中心(许可证号:SCXK(陕)2023-002)。普通维持饲料、H10060高脂饲料,重庆腾鑫生物技术有限公司西安分公司。本实验小鼠饲养及方案设计均符合学校实验动物伦理审查要求(伦理批准号:商研伦审函〔2025〕13号)。
1.2 仪器与设备
HC1-AS30超纯水机,重庆华创水处理工程有限公司;BSA224S-CW电子天平,赛多利斯科学仪器(北京)有限公司;HH-S4恒温水浴锅,巩义市予华仪器有限责任公司;IMS-25全自动雪花制冰机,常熟市雪科电器有限公司;TD4-WS离心机,盐城市凯特实验仪器有限公司;L4物联智能紫外可见分光光度计、P901酸度计,上海佑仪仪器仪表有限公司;MIX-30S迷你混合仪,杭州米欧仪器有限公司;PBX-52电热恒温培养箱,上海博迅实业有限公司医疗设备厂;ZQLY-180N全温振荡培养箱,上海巴玖实业有限公司;迈瑞BS-430全自动生化分析仪,成都晟达亿新医疗科技有限公司。
1.3 实验方法
1.3.1 菊粉复配AAP结合胆酸盐能力的测定
参照于美汇等[14]的方法模拟人体胃肠道环境,分别采用甘氨胆酸钠和牛黄胆酸钠标准溶液,绘制胆酸盐标准曲线。探讨不同质量比例的菊粉复配AAP与胆酸盐结合能力。采用比色法对照甘氨胆酸钠和牛磺胆酸钠标准曲线进行测定,每个样品做3次平行实验,胆酸盐结合率按公式(1)、公式(2)计算:
甘氨胆酸钠结合率/%
(1)
牛磺胆酸钠结合率/%
(2)
1.3.2 菊粉复配AAP结合胆酸盐能力的测定
参照曹叶霞等[15]的方法,探讨不同质量比例的菊粉复配AAP对胰脂肪酶抑制率的测定。不同质量比例菊粉复配AAP对于脂肪酶活性抑制能力按公式(3)计算:
脂肪酶活性抑制率/%
(3)
1.3.3 动物实验
1.3.3.1 实验动物分组及干预
将70只KM雄性小鼠,在室内温度(25±5) ℃、湿润度(65±5)%、光照时间12 h/d的环境下饲养。适应1周后,其中正常组8只饲喂普通饲料,62只饲喂高脂饲料作模型组。每周称量体重,8周后,从高脂饲喂的小鼠中挑选体重高于正常组质量比20%的56只肥胖小鼠,即为造模小鼠。将造模成功的小鼠随机分为7组,高脂对照组、菊粉复配AAP质量比(5∶0,4∶1,3∶2,2∶3,1∶4,0∶5)剂量实验干预组,开始对小鼠进行灌胃干预,每组喂养及灌胃受试物剂量情况见表1,其中每组灌胃量为200 mg/(kg·d),实验期间小鼠自由摄食和饮水,每日进行灌胃干预,每周测量各组实验小鼠体重,实验干预喂养时长为期8周。
表1 不同比例菊粉复配AAP干预高脂饮食小鼠的分组
Table 1 Groups of mice with different proportions of inulin combined with AAP intervention on a high-fat diet
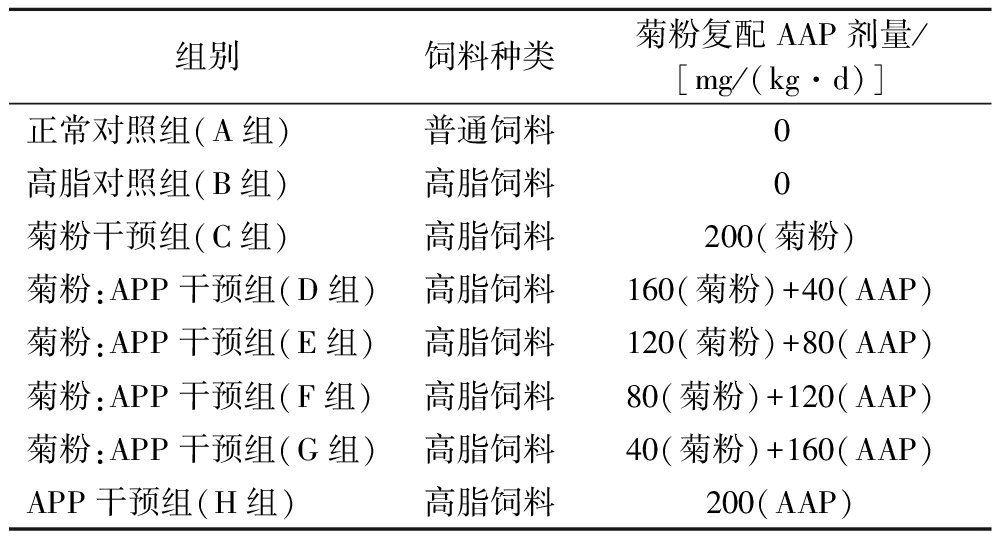
组别饲料种类菊粉复配AAP剂量/[mg/(kg·d)]正常对照组(A组)普通饲料0高脂对照组(B组)高脂饲料0菊粉干预组(C组)高脂饲料200(菊粉)菊粉:APP干预组(D组)高脂饲料160(菊粉)+40(AAP)菊粉:APP干预组(E组)高脂饲料120(菊粉)+80(AAP)菊粉:APP干预组(F组)高脂饲料80(菊粉)+120(AAP)菊粉:APP干预组(G组)高脂饲料40(菊粉)+160(AAP)APP干预组(H组)高脂饲料200(AAP)
1.3.3.2 体重及肝体比的测定
每周对小鼠的体重以及摄食量进行称重与记录。末次干预后,禁食12 h,摘取眼球并取血于洁净的1.5 mL的塑料尖底离心管中,以4 000 r/min离心15 min,分离血清并在4 ℃冰箱下储存。解剖取其肝脏,用滤纸吸干水分,对肝脏称重,并按公式(4)计算肝体比。
肝体比/%=肝脏质量/体重×100
(4)
1.3.3.3 血清生化指标的测定
取1.3.3.2节中所得血清立即送往全自动生化仪中测量总甘油三酯(total triglyceride,TG)、TC、HDL-C、LDL-C浓度。
1.3.3.4 肝脏油红染色
肝脏称重后立即放入多聚甲醛组织固定液中,委托武汉赛维尔生物科技有限公司进行脱水、包埋、油红染色、切片,光学显微镜下观察其组织形态及病理变化。
1.3.3.5 肠道菌群分析
用无菌离心管收集干预第8周末的小鼠粪便3~4粒,-80 ℃ 冰箱冷冻保藏。委托杭州联川生物技术股份有限公司对小鼠进行肠道菌群DNA提取、PCR 扩增及高通量测序技术检测。肠道菌群的基因组DNA用作扩增16S rRNA基因的模板。采用16S rDNA基因的V3~V4区域使用正向引物341F(5′-CCTACGGGNGGCWGCAG-3′)、反向引物805R(5′-GACTACHVGGGTATCTAATCC-3′)。
1.4 统计方法
实验数据均以“平均值±标准差”表示,采用 SPSS 22.0软件进行统计学分析,组间采用t检验,多组比较采用方差分析,肠道菌群结构统计数据采用GraphPad prism 9.5软件绘图。
2 结果与分析
2.1 菊粉复配AAP对甘氨胆酸钠、牛磺胆酸钠结合率结果
不同质量比例菊粉复配AAP对甘氨胆酸钠的结合率比较结果见电子版增强出版附图1(https://doi.org/10.13995/j.cnki.11-1802/ts.044256,下同),配制的不同质量比例菊粉复配AAP溶液均能与甘氨胆酸钠结合,随着复配质量比例的改变,甘氨胆酸钠的结合率呈现出先增高后降低的趋势,6种质量比例菊粉复配AAP对甘氨胆酸钠的结合率均为24%~42%,其中复配质量比例为2∶3(菊粉80 mg/L+AAP 120 mg/L)的结合率最高,可达到41.07%,菊粉对甘氨胆酸钠的直接结合作用较弱,由于菊粉主要通过物理吸附(氢键、疏水相互作用等)而非静电结合(缺乏带电基团),其结合效率显著低于带负电的AAP。两者复配后,甘氨酸钠结合率得以上升。
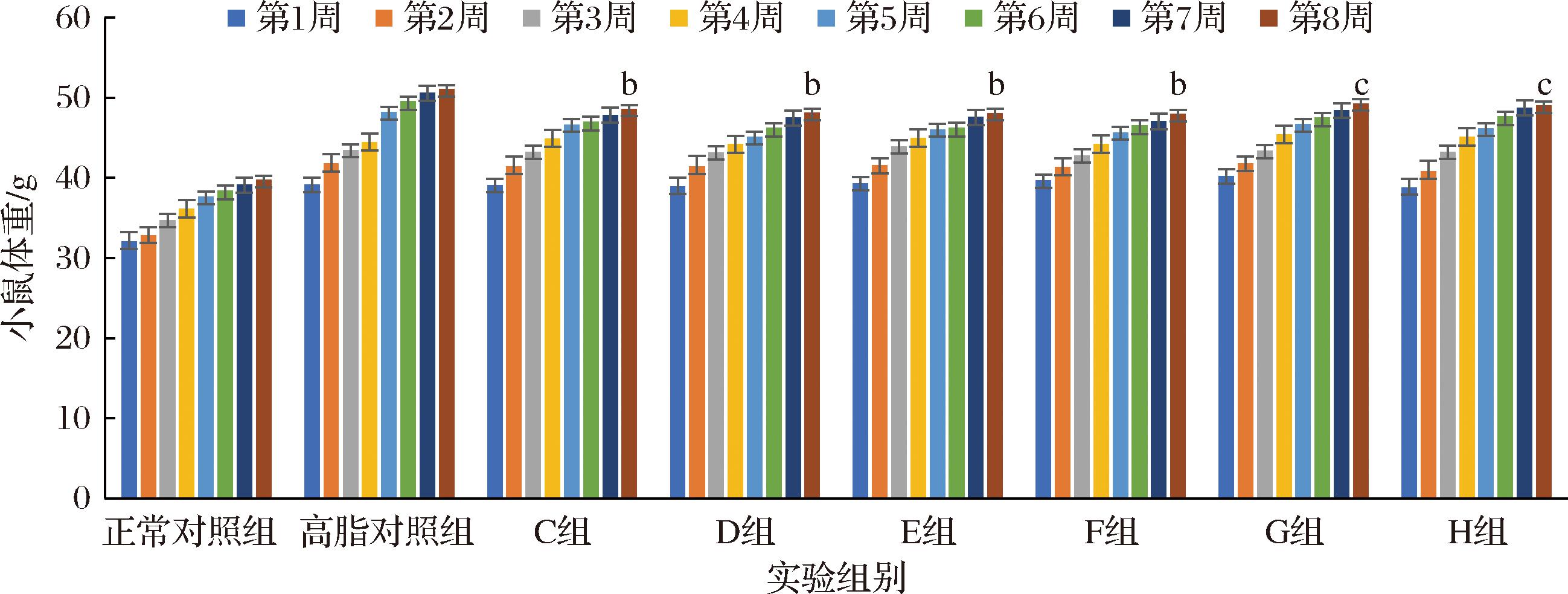
图1 菊粉复配AAP对小鼠体重的影响
Fig.1 Effects of inulin combined with AAP on mouse body weight
注:b表示与高脂对照组比较具有极显著差异(P<0.01);c表示与高脂对照组比较具有显著性差异(P<0.05)(图2同)。
不同质量比例菊粉复配AAP溶液均能与牛磺胆酸钠结合,由附图2可知,随着复配质量比例的改变,结合率呈现出先增高后降低的趋势,6种质量比例的最终结合能力依次为:2∶3>1∶4>0∶5>3∶2>4∶1>5∶0,复配质量比例2∶3的最终结合率达到38.31%。
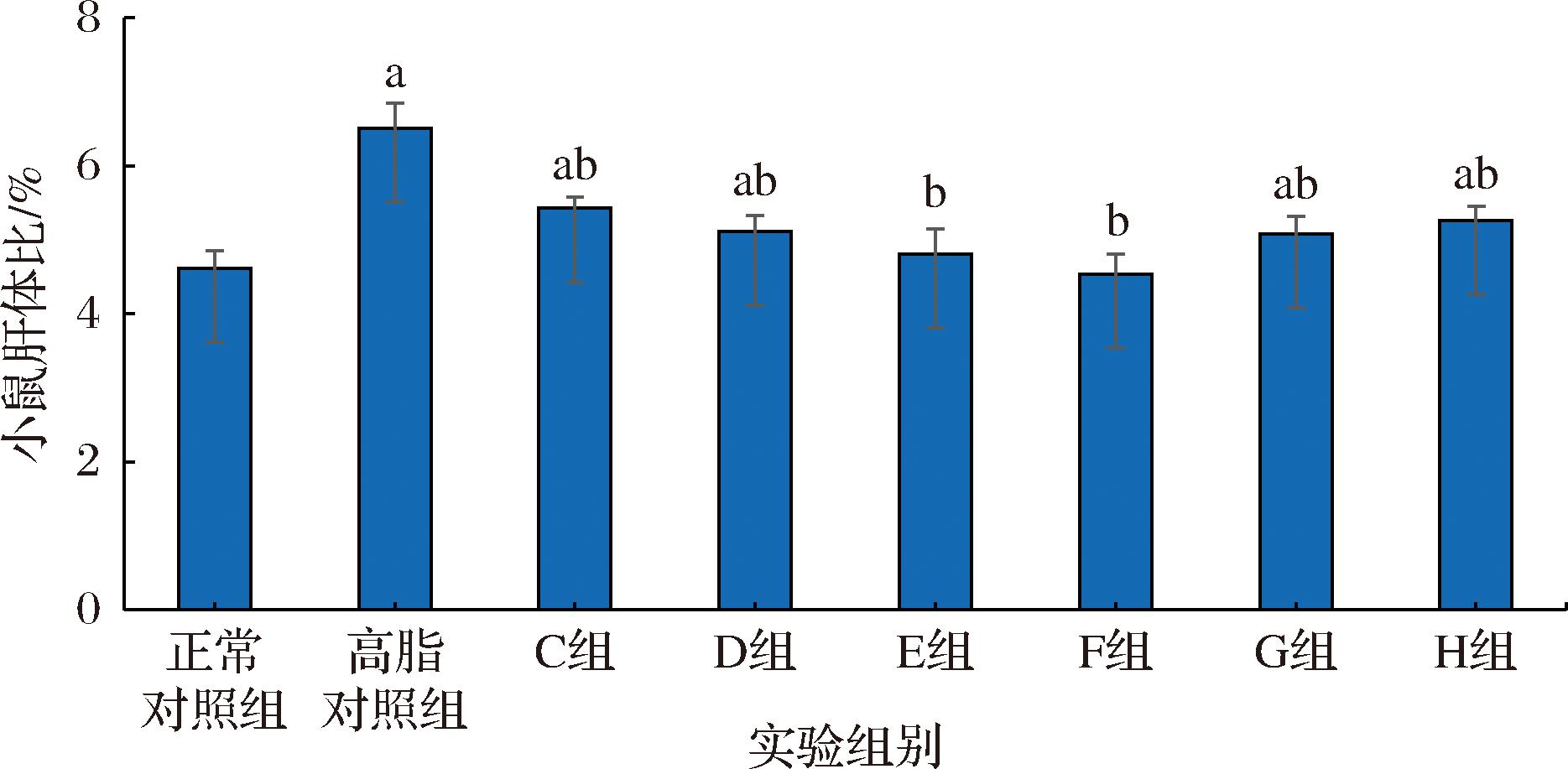
图2 菊粉复配AAP对小鼠肝体比的影响
Fig.2 Effects of inulin combined with AAP on liver-to-body ratio of mice
注:a表示与正常对照组比较具有极显著差异(P<0.01)。
2.2 菊粉复配AAP对脂肪酶抑制率结果
如附图3所示,当菊粉与 AAP的配比发生变化时,其对脂肪酶的抑制效果表现出先升高后趋于平缓趋势。在菊粉复配APP质量比例5∶0、4∶1、3∶2、2∶3范围内,随着APP的添加,脂肪酶抑制率呈现升高趋势。单一使用APP时,脂肪酶抑制率相对较高,抑制率达32.87%,但与菊粉复配AAP比例为2∶3和1∶4差异不大。可能是AAP质量的升高,导致高黏度包裹了脂肪滴,减少了酶与底物接触,从而间接降低了脂肪水解效率。
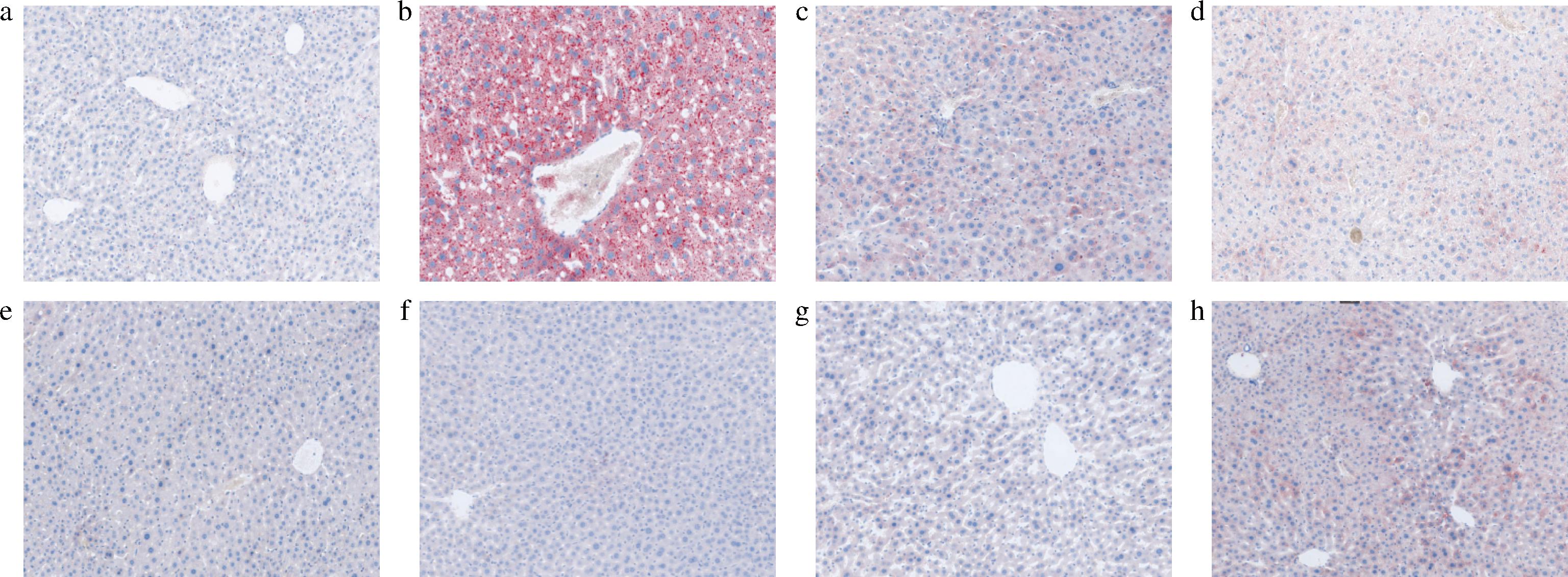
a-正常对照组(A组);b-高脂对照组(B组);c-C组;d-D组;e-E组;f-F组;g-G组;h-H组
图3 不同组别小鼠肝脏组织油红O染色结果(×10)
Fig.3 Oil red O staining results of liver tissue of mice in different groups
2.3 菊粉复配AAP对小鼠体重的影响
体重变化作为肥胖小鼠最直观的指标,各组结果如图1所示,各实验小鼠体重增量见附图4。干预8周后,与所有实验干预组(C~H)相比均存在显著性差异(P<0.05),其中干预组(C~F)存在极显著差异(P<0.01),说明菊粉、AAP及复配干预有效抑制高脂饮食诱导的小鼠体重增加,可能通过调节肠道菌群或抑制脂肪吸收减缓体重增长。随着AAP比例增加,体重增加量呈现先降低后升高的趋势,其中E组、F组体重增加量与正常对照组相比,无显著性差异,复配比例为2∶3时,增量更接近空白对照组,说明该比例复配协同抗肥胖作用较佳。
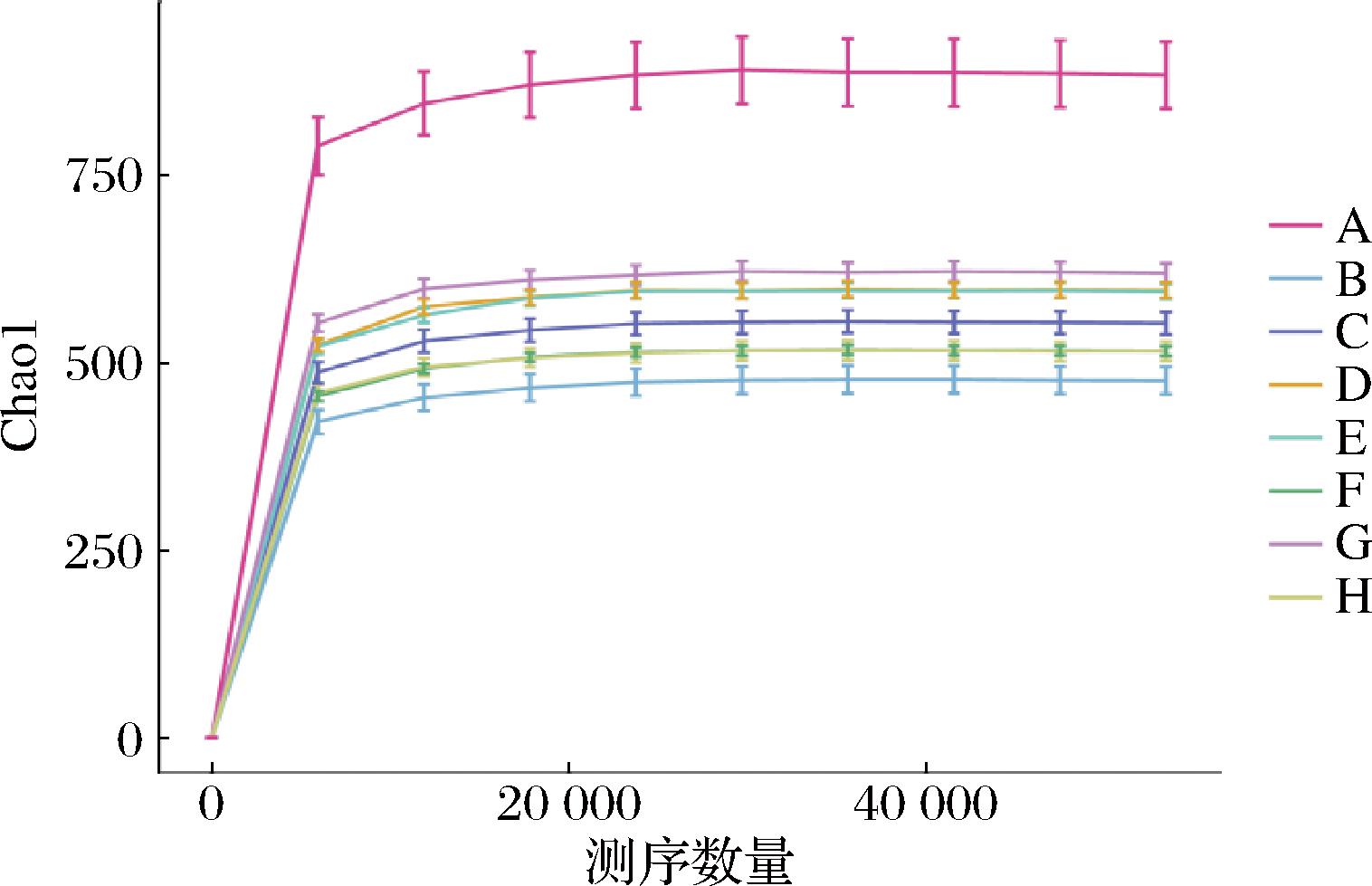
图4 不同组别样品的稀释曲线图
Fig.4 Dilution curves of different groups of samples
2.4 菊粉复配AAP对小鼠肝体比的影响
如图2所示,与正常对照组相比,高脂对照组的肝体比显著升高(P<0.01)。不同质量比例菊粉复配AAP实验组与高脂对照组相比,显著低于高脂对照组肝体比(P<0.01)。随着AAP比例增加,肝体比呈现先降低后升高的趋势,表明菊粉复配AAP相对单一喂养小鼠,对小鼠肝体比降低效果较好,其中E组、F组体重增加量与正常对照组相比,无显著性差异,当两者质量比例为2∶3表现出最显著的肝体比降低效果,说明该比例复配具有协同降低肝体比作用。
2.5 菊粉复配AAP对小鼠血清生化指标的影响
TG、TC、LDL-C、HDL-C作为高脂血症血脂异常的重要指标,主要由于脂质代谢紊乱所导致。如表2所示,与正常对照组,模型组高脂饮食显著增加了小鼠的TG、TC、LDL-C含量水平,显著降低了HDL-C含量水平(P<0.01),高脂对照组 (B) 的所有指标均与正常对照组 (A) 存在显著差异,符合高脂饮食模型的预期。与高脂对照组相比,各干预组经过菊粉、菊粉复配AAP干预后,血清TC、TG、LDL-C含量均极显著下降(P<0.01),HDL-C水平均显著升高(P<0.01)。
表2 菊粉复配AAP对小鼠小鼠血清脂质的影响
Table 2 Effects of inulin combined with AAP on serum lipids in mice
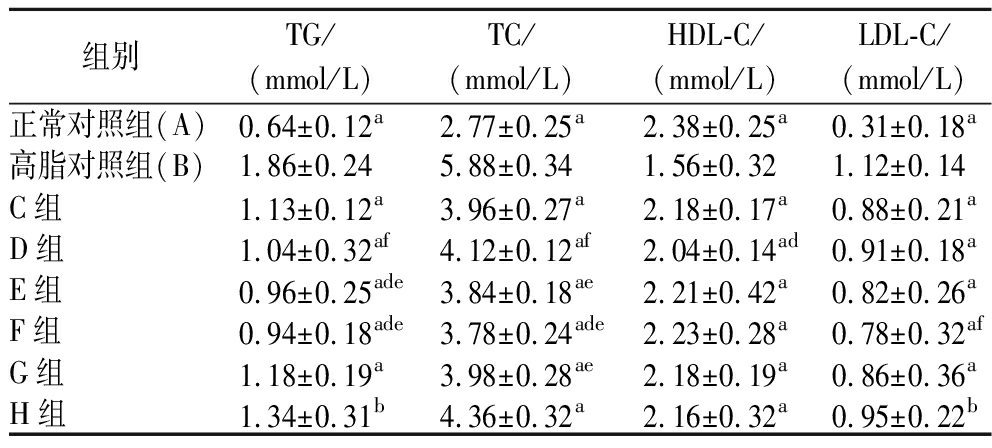
组别TG/(mmol/L)TC/(mmol/L)HDL-C/(mmol/L)LDL-C/(mmol/L)正常对照组(A)0.64±0.12a2.77±0.25a2.38±0.25a0.31±0.18a高脂对照组(B)1.86±0.245.88±0.341.56±0.321.12±0.14C组1.13±0.12a3.96±0.27a2.18±0.17a0.88±0.21aD组1.04±0.32af4.12±0.12af2.04±0.14ad0.91±0.18aE组0.96±0.25ade3.84±0.18ae2.21±0.42a0.82±0.26aF组0.94±0.18ade3.78±0.24ade2.23±0.28a0.78±0.32afG组1.18±0.19a3.98±0.28ae2.18±0.19a0.86±0.36aH组1.34±0.31b4.36±0.32a2.16±0.32a0.95±0.22b
注:a表示与高脂对照组比较具有极显著差异(P<0.01),b表示与高脂对照组比较具有显著性差异(P<0.05);c表示与C组比较具有极显著差异(P<0.01),d表示与C组比较具有显著性差异(P<0.05);e表示与H组比较具有极显著差异(P<0.01),f表示与H组比较具有显著性差异(P<0.05)。
菊粉、AAP复配干预与C组相比,E组和F组的TG水平, F组 的TC水平显著低于C组(P<0.05),其他组各血脂水平无显著差异。特别说明的 D组的HDL-C显著低于C组(P<0.05),可能是AAP质量比例不足导致的效果减弱。
菊粉、AAP复配干预与H组相比,E组和F组的TG水平极显著低于H组(P<0.01),D组的TG水平显著低于H组(P<0.05),G组的TG水平与H组无差异,可能AAP比例过高时,复配优势消失。复配组(D~G)的TC含量均显著或极显著低于H组,其中 E组和F组效果最优。
2.6 菊粉复配AAP对小鼠肝脏油红O染色的影响
高脂饮食的摄入会增加体内脂肪储存堆积,油红O染色结果如图3所示,正常对照组小鼠肝脏中未见明显红染脂滴,脂肪堆积不明显;B组小鼠肝脏中呈现大片的脂滴,脂肪堆积严重,可见弥漫性大小不等密集的橘红色脂肪滴,这与张廷婷等[12]对高脂饮食大鼠脂肪堆积情况描述一致。与B组比较,菊粉复配AAP不同比例干预组(D组、E组、F组、G组)小鼠肝脏中脂肪滴数量和体积均明显减少,脂肪堆积情况均有所缓解。C组、H组与B组比较,脂肪滴数量和体积均也有所减少,但没有复配干预组脂肪滴密度明显下降,染色变淡,细胞显现界限分明,其中E组、F组减脂效果较好,这与AAP改善高脂饮食诱导的大鼠肝脏脂质积累效果一致[12]。说明菊粉复配AAP可明显缓解高血脂小鼠肝脏中脂肪堆积。对预防或缓解小鼠脂肪肝的积累、形成具有一定的抑制作用。
2.7 菊粉复配AAP对小鼠肠道菌群结构的影响
2.7.1 α-多样性分析
稀释性曲线用来比较不同样本中物种的丰富度及评估样品的测序深度。若曲线急剧上升,表明测序数据量并未达到最佳;若曲线趋于平缓,则证明测序数据量已饱和。从图4可看出,小鼠肠道菌群的稀释曲线趋于平坦,测序数据量已经足够,更多的测序数据量只会产生少量新的扩增子序列变异体(amplicon sequence variant,ASV)数目,说明测序结果可反映样本中绝大多数的微生物信息。在测序深度相同的情况下,正常对照组的丰富度明显高于其他组,高脂组的丰富度最低。菊粉复配AAP组丰富度均高于高脂组,说明添加菊粉、AAP能够有效提高小鼠肠道菌群的丰富度,提高物种多样性,并且效果也均优于只添加菊粉组(C)、AAP(H),而菊粉复配AAP的比例(G组、E组、D组)效果最好,可提高物种多样性。
AAP、菊粉都能够一定程度上提高高脂饮食小鼠肠道菌群的微生物多样性。Alpha多样性通常用来衡量物种多样性及均匀度。其中,Chao1 指数用于衡量物种多样性,Shannon指数、Simpson 指数用于衡量物种均匀度。由图5可以看出:高脂对照组(B组)的Shannon指数显著低于正常对照组(A组),经过菊粉、AAP干预的组别Shannon指数升高,并且菊粉、AAP复配的(D组、E组、F组、G组)相对单一的菊粉、AAP干预效果更佳。
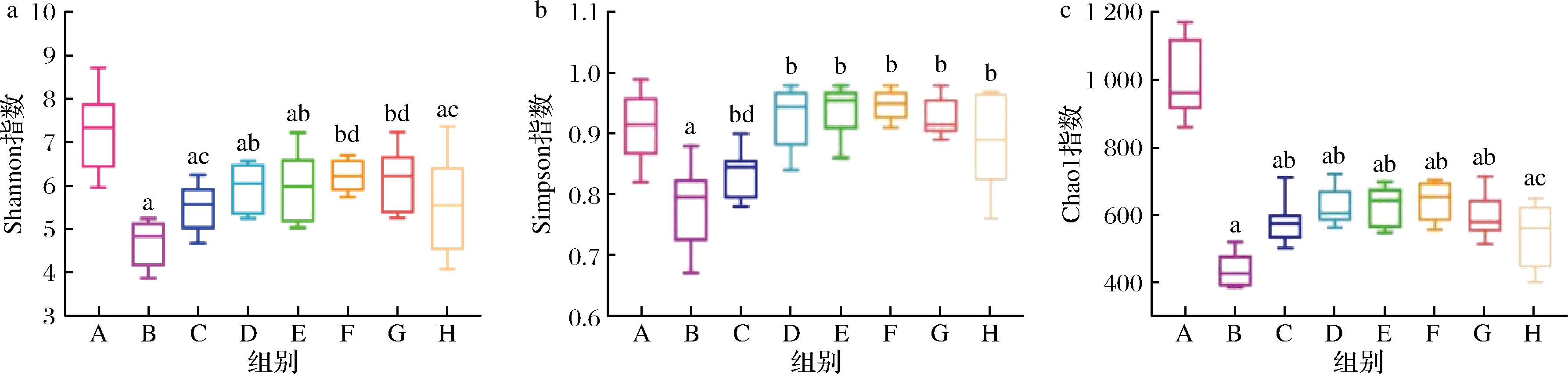
a-Shannon指数;b-Simpson指数;c-Chao1指数
图5 不同组别小鼠肠道菌群的Alpha多样性指数
Fig.5 Alpha diversity index of gut microbiota of mice in different groups
注:a表示与A组比较具有极显著差异(P<0.01);b表示与B组比较具有极显著差异(P<0.01);c表示与B组比较具有显著性差异(P<0.05);d表示与A组比较具有显著性差异(P<0.05)。
高脂对照组(B组)的Simpson指数显著低于正常对照组(A组),经过菊粉、AAP干预的组别Simpson指数升高,并且菊粉、AAP复配干预(D组、E组、F组、G组)相比于正常对照组(A组)没有明显差异性,两者复配比单一的菊粉、AAP(C组、H组)效果更佳。
高脂对照组(B组)的Chao1指数显著低于正常对照组(A组),经过菊粉、AAP干预的组别Chao1指数升高,并且菊粉、AAP复配干预(D组、E组、F组、G组)相比于正常对照组(A组)仍存在明显差异性,两者复配比单一的菊粉、AAP干预(C组、H组)效果更佳。菊粉、AAP具有抑制肠道菌群丰富度下降的能力,并使Chao1指数向A组靠拢,并能增加菌群的物种多样性。
2.7.2 Beta多样性分析
主坐标分析(principal coordinates analysis, PCoA),通过可视化的低维空间(通常是二维)重新排列样品,最大化展示样品之间的关系信息,不同组别小鼠肠道菌群的Beta多样性变化如图6。
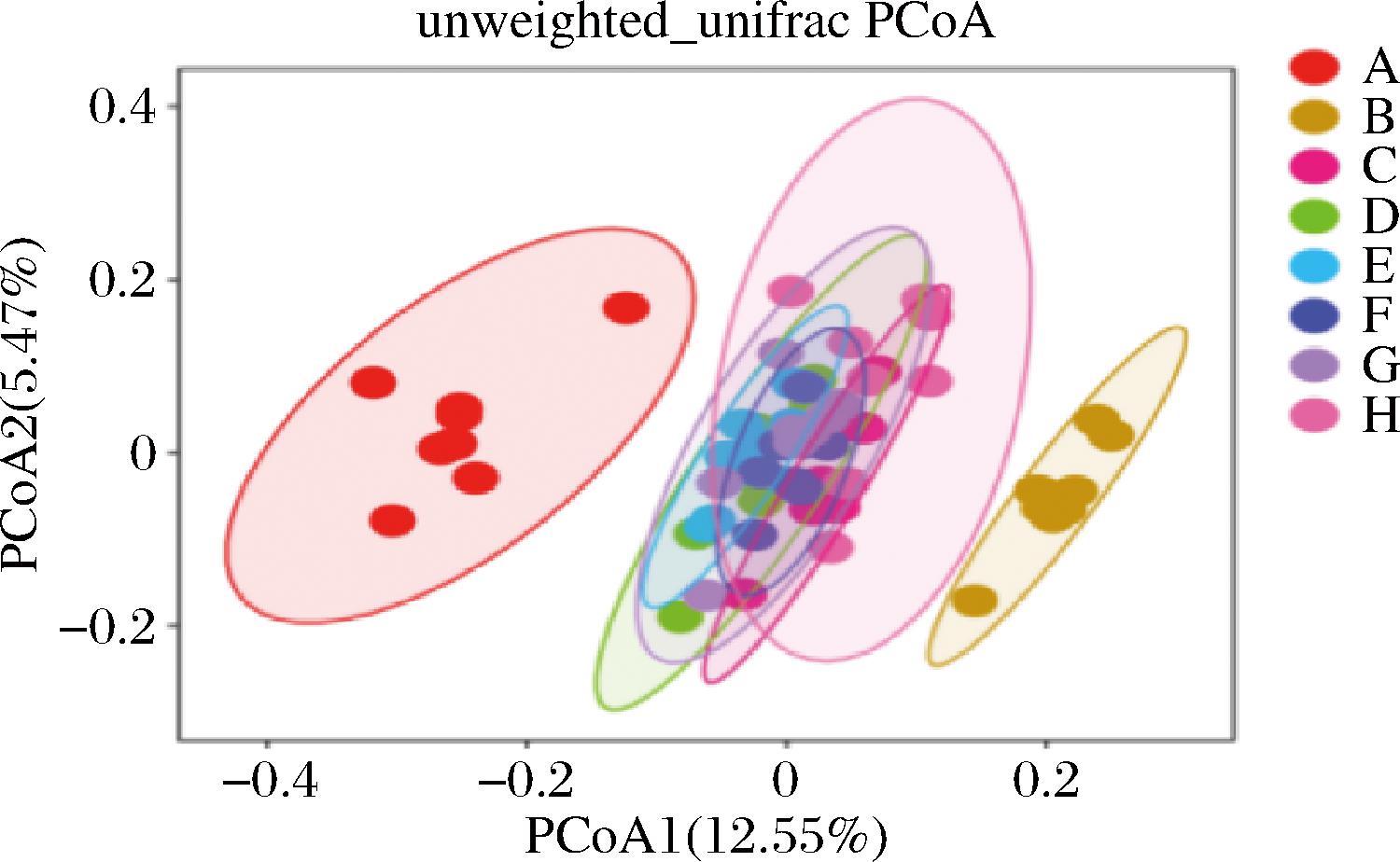
图6 不同组别小鼠肠道菌群的Beta多样性变化
Fig.6 Changes in beta diversity of gut microbiota in different groups of mice
图6结果显示,主坐标组合(PCoA1=12.55%,PCoA2=5.47%)贡献率最高。B组与A组在PCoA1/PCoA2上明显分离,说明高脂饮食显著改变小鼠肠道菌群结构,饲喂高脂饲料的小鼠在8周的饲养结束后粪便菌群发生了较大变化。干预组C~H组与B组、A组在PCoA1/PCoA2上也能明显分离,说明干预组可能部分恢复小鼠菌群结构。通过比较C组(纯菊粉)、复配组(如D~G组)、H组(纯AAP组)小鼠菌群分布,可以发现灌胃菊粉、AAP的小鼠菌群趋势偏向B组,而复配组(如D~G组)趋势更偏向A组,说明两者复配对菌群调节作用相比单独使用,对恢复肠道菌群结构较好,但复配比例对肠道菌群结构影响不显著。
2.7.3 小鼠肠道微生物菌落组成分析
饮食变化可以调节肠道菌群结构,导致疾病的发生或促进机体健康,小鼠肠道菌群结构在门水平的差异分别见图7。图7结果显示,实验组的主要肠道微生物类型包括厚壁菌门(Firmicutes)、拟杆菌门(Bacteroidetes)、变形菌门(Proteobacteria)和脱硫杆菌门(Desulfobacterota)等9个门结构。值得注意的是,细菌分类学分析表明,与正常对照组(A组)组相比,B组中厚壁菌门、脱硫杆菌门的相对丰度增加,而拟杆菌门的相对丰度减少,厚壁菌门与拟杆菌门的比例也有所增加。菊粉、AAP干预组(C组~H组)较B组厚壁菌门丰度减少,单一菊粉、AAP干预组较B组拟杆菌门丰度有所减少,但没有显著性差异,菊粉复配AAP干预组(D组、E组、G组、H组)拟杆菌门丰度显著升高,说明菊粉复配AAP可以缓解高脂饮食引发的菌群结构失调。
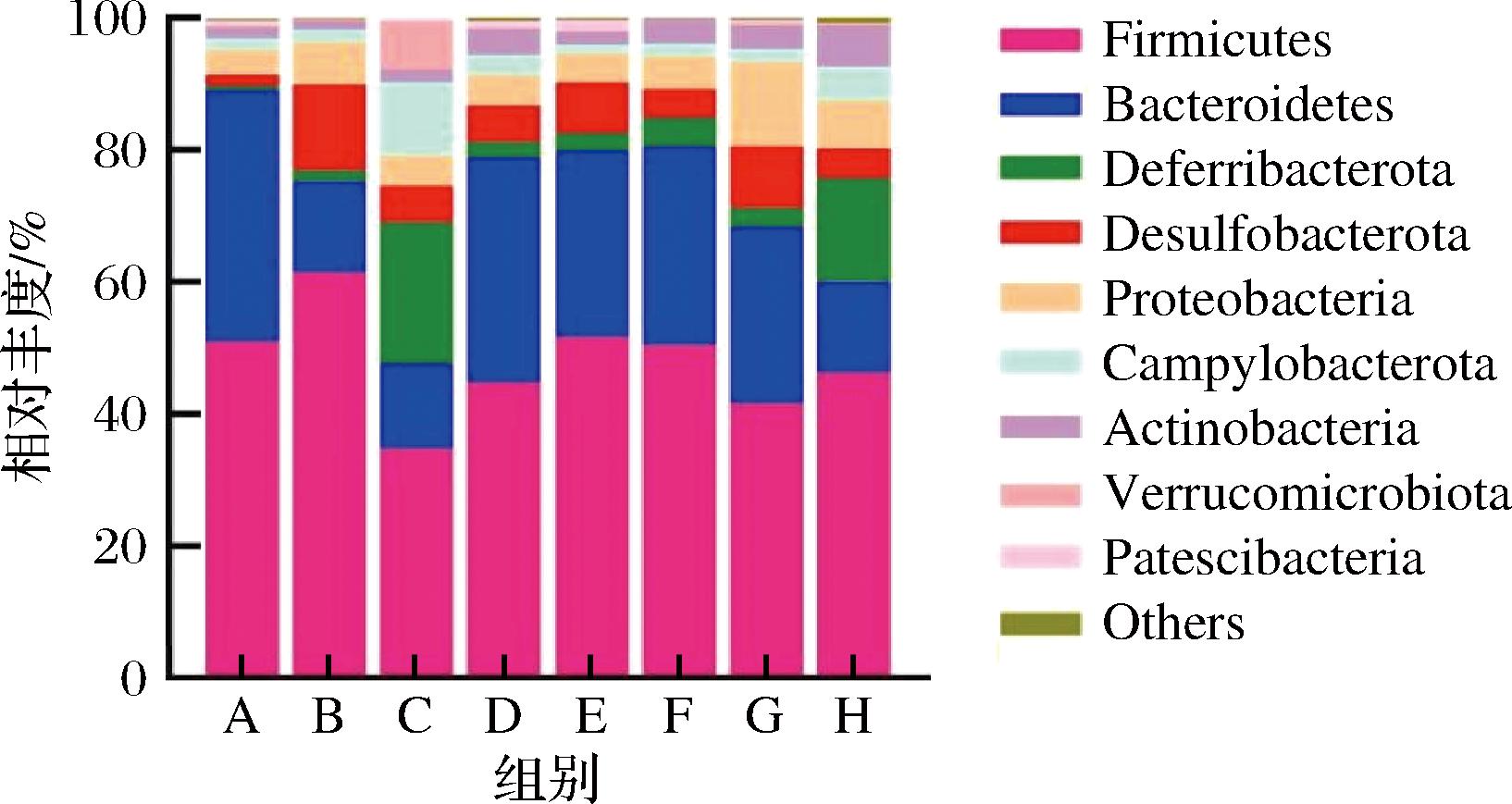
图7 小鼠肠道菌群结构在门水平的差异性
Fig.7 Differences in gut microbiota structure at the phylum level in mice
热图分析中的颜色梯度由蓝色到红色表示相对丰度由低到高。如图8所示,B组厚壁菌门、脱硫杆菌门丰度较高,无复配的C组、H组脱铁杆菌门(Deferribacterota)、弯曲杆菌门(Campylobacterota)、疣微菌门(Verrucomicrobiota)丰度有所提升,复配的F组、E组帕特西菌门(Patescibacteria)、弯曲杆菌门丰度较低。
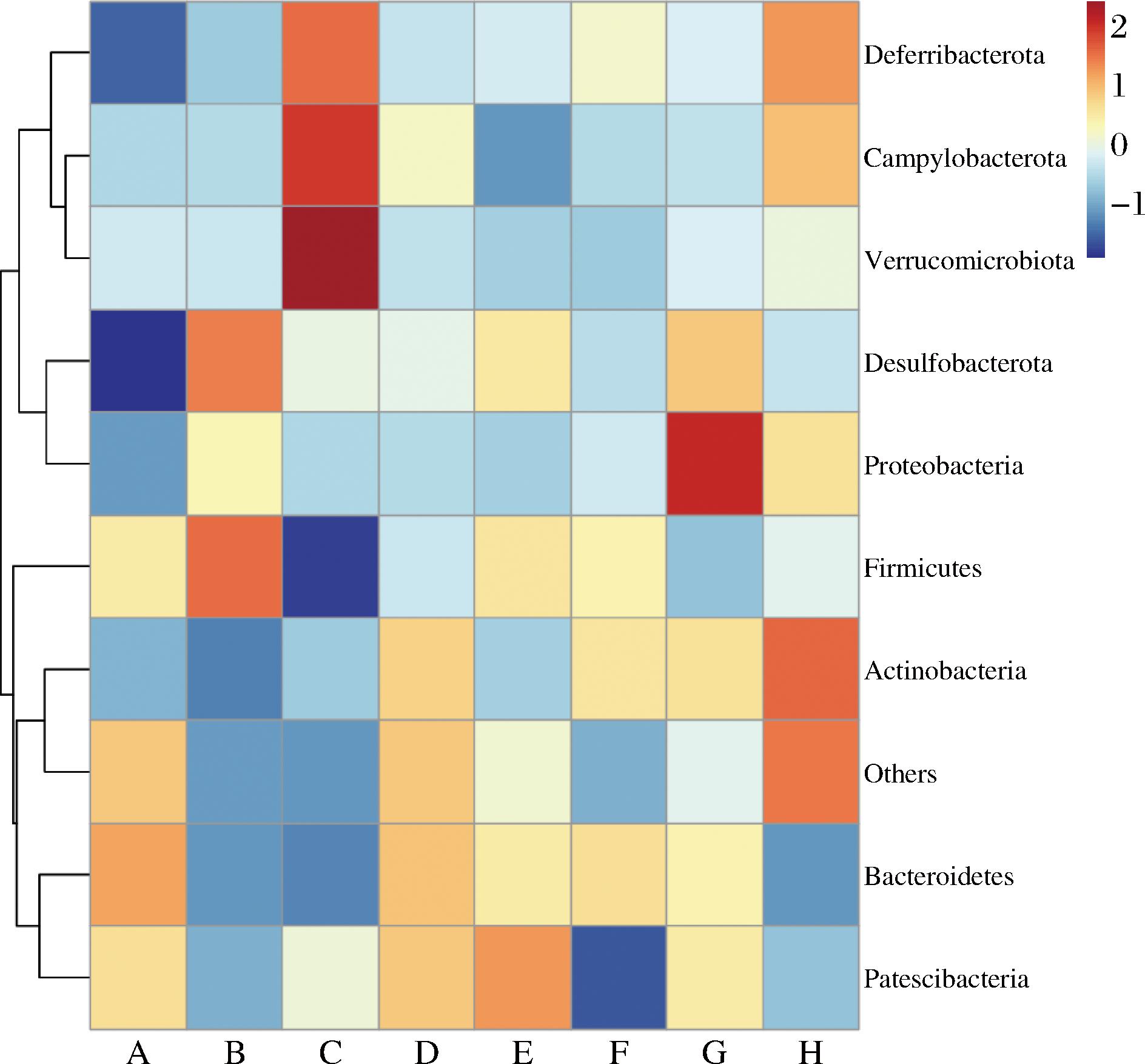
图8 门水平物种聚类分析热图
Fig.8 Heat map of horizontal species cluster analysis
通过分析丰度排名前30的细菌属水平柱状图,各组在属水平上分类学结果如图9。其中未分类的共有4个,分别为属于鼠杆菌科(Muribaculaceae_unclassified)、脱硫弧菌科(Desulfovibrionaceae_unclassified)、梭菌目(Clostridiales_unclassified)、厚壁菌门(Firmicutes_unclassified)。与A组相比,高脂对照B组乳杆菌属(Lactobacillus)、脱硫弧菌科(Desulfovibrionaceae_unclassified)、毛螺菌科-NK4A136(Lachnospiraceae_NK4A136)、脱硫弧菌属(Desulfovibrio)、螺杆菌属(Helicobacter)、志贺氏菌属(Escherichia-Shigella)、异杆菌属(Allobaculum)相对丰度升高。
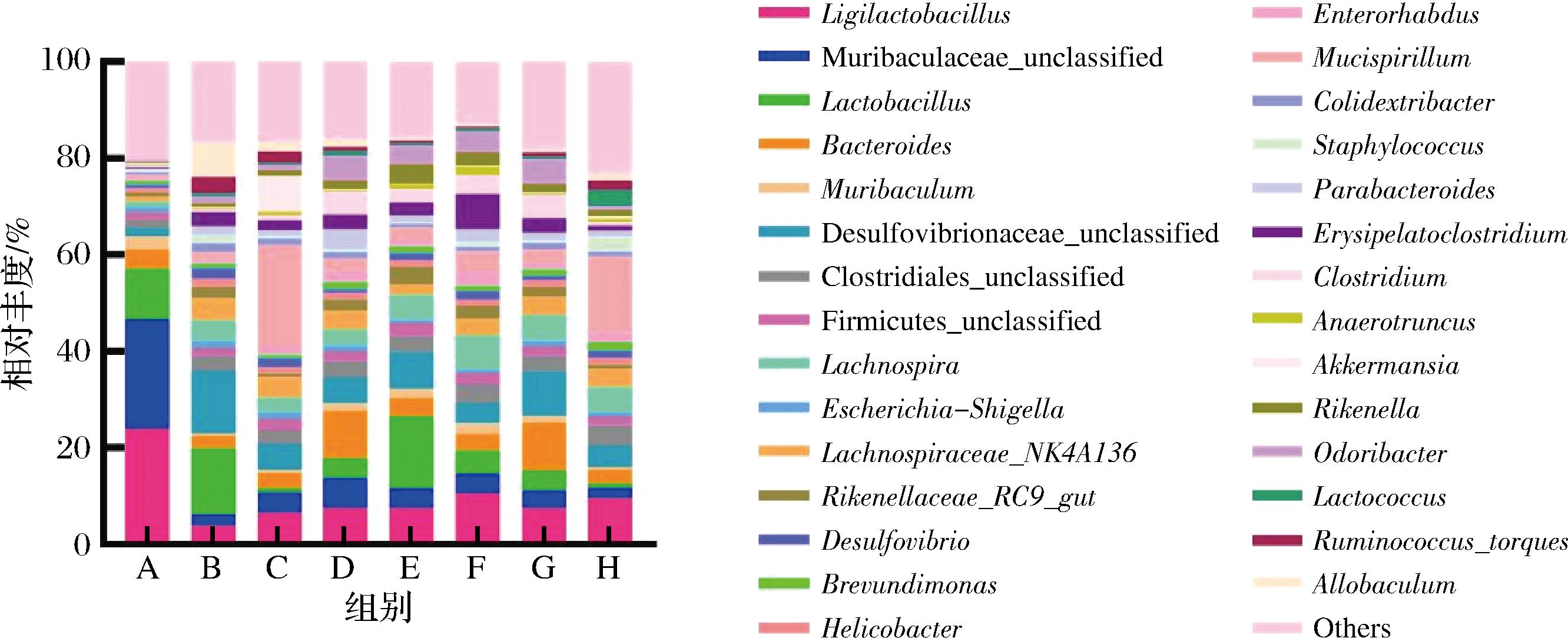
图9 小鼠肠道菌群结构在属水平的差异性
Fig.9 Differences in the structure of intestinal microbiota in mice at the genus level
与B组相比,C组粘螺菌属(Mucispirillum)、乳酸杆菌属-子属(Ligilactobacillus)、拟杆菌属(Bacteroides)、文肯菌属(Rikenella)、肠球菌属(Enterorhabdus)、肠属杆菌(Muribaculum)、艾克曼菌属(Akkermansia)相对丰度升高;H组粘螺菌属、乳酸杆菌属-子属、毛螺菌属(Lachnospira)、拟杆菌属、文肯菌属、肠球菌属、肠属杆菌、艾克曼菌属等菌属相对丰度显著升高,毛螺菌科-NK4A136、脱硫弧菌属、螺杆菌属、丹毒荚膜菌属(Erysipelatoclostridium)、志贺氏菌属等菌属丰度降低;复配组(C组~G组)粘螺菌属、鼠杆菌科、乳酸杆菌属-子属、拟杆菌属、杆菌属、文肯菌属、肠球菌属、梭菌属、副拟杆菌属、肠属杆菌(Muribaculum)等菌属相对丰度均升高,毛螺菌科-NK4A136、脱硫弧菌属、螺杆菌属、扭链瘤胃球菌(Ruminococcus_torques)、志贺氏菌属、异杆菌属、Colidextribacter相对丰度均降低。
3 讨论
血脂异常升高是心血管疾病的一个重要风险因素,长期高糖、高脂肪、低纤维素的饮食习惯,都是高血脂产生的重要原因。目前临床常用的降脂药物主要包括他汀类、胆固醇吸收抑制剂、贝特类、烟酸类以及新型靶向药物等,长期服用会出现肝毒性、肌病风险、胃肠道症状等风险[16]。菊粉作为一种天然的水溶性膳食纤维,可以通过调节肠道菌群结构改善糖脂代谢、抑制炎症反应。AAP具有降血脂、抗氧化等功能活性,可以一定程度提升高脂饮食条件下优势菌群的丰度,缓解炎症反应。
本研究结果表明,高脂饮食小鼠体重、肝体比显著升高,引起血清TC、TG、HDL-C显著升高,肝脏脂肪堆积严重。肝脏作为脂质代谢的关键场所,肝损伤和肝脏脂肪堆积导致肝功能障碍,进而发生脂质代谢异常。菊粉、AAP干预后,能够明显抑制高脂饮食小鼠体重的增长,能在一定程度上缓解肝损伤和肝脏脂肪堆积,从而可促进脂质代谢。不同比例菊粉、AAP复配干预较两者单独摄食,血清中TC、TG发生显著性降低,也可明显缓解高血脂小鼠肝脏中脂肪堆积。
饮食的改变可以调节肠道菌群结构,导致疾病的发生或促进健康。在本研究中,高脂饮食小鼠厚壁菌门/拟杆菌门比例升高,菊粉复配AAP在一定程度上改变了高脂饮食中优势菌群丰度的分布,有利于拟杆菌门生长而不利于厚壁菌门的生长,能够一定程度预防脂肪摄入引起菌群结构的改变。高脂饮食下变形菌门、脱硫杆菌门、异杆菌属相对丰度显著增加,而菊粉复配AAP干预效果呈现负相关。
在属水平上,高脂饮食小鼠脱硫弧菌科(Desulfovibrionaceae_unclassified)、脱硫弧菌属(Desulfovibrio)丰度升高,脱硫弧菌属的相对丰度与体重、TG水平和尿酸水平呈负相关,产生内源性H2S毒害肠道上皮细胞,造成肠道敏感性,引发溃疡性结肠炎。Colidextribacter作为肠道菌群的肥胖标志物,能发酵膳食纤维产生短链脂肪酸,参与胆汁酸的转化,影响脂肪消化和脂质代谢,高脂饮食小鼠该菌属丰度升高,机体肥胖常伴随着该菌丰度的升高[17],经过菊粉、AAP复配组干预显著降低了Colidextribacter丰度。扭链瘤胃球菌过度增殖会减少黏液层厚度,增加肠道通透性,也会致使脂多糖易位进入血液,激活TLR4/NF-κB通路,促进肝脏脂肪沉积和血脂异常[18]。经过菊粉、AAP复配组干预扭链瘤胃球菌丰度降低,可以增加黏液层厚度,降低肠道通透性,改善肠道屏障,起到对高脂饮食小鼠高脂血症的预防作用。
菊粉、AAP复配组干预致使拟杆菌属丰度升高,拟杆菌属可通过淀粉利用系统,致使其在竞争性肠道环境中具有优势,有助于附着在黏液聚糖上,多糖利用位点机制可使其参与邻近微生物的物种间交叉摄食,同时通过产生短链脂肪酸以维持稳态[19]。ZHU等[20]研究发现Muribaculaceae的核心代谢能力就是能够降解各类复杂多糖,通过糖酵解途径会产生短链脂肪酸,也可增加黏液蛋白基因的表达量和分泌再生,缓解结肠组织损伤并降低肠道通透性。本研究中菊粉、AAP复配组Muribaculaceae丰度升高,说明高脂饮食造成的小鼠肝重及肝指数上升,肝损伤可能与Muribaculaceae丰度降低有关,菊粉、黑木耳多糖复配提升其丰度进而改善肝损伤情况。
乳酸杆菌属可通过分泌乳酸、乙酸等短链脂肪酸,降低肠道pH,抑制病原菌生长,缓解高脂饮食引发的肠屏障损伤。丙酸可通过抑制羟甲基戊二酰辅酶A还原酶,减少内源性胆固醇生成,丁酸可激活单磷酸腺苷活化蛋白激酶通路,促进脂肪酸氧化,减少TG堆积,这些短链脂肪酸可增强肠道L细胞分泌胰高血糖素样肽-1,促进胰岛素分泌,间接改善脂代谢[21]。菊粉、AAP复配组乳酸杆菌属、杆菌属、副拟杆菌属、拟杆菌属等微生物丰度均升高,这些微生物都属于产短链脂肪酸菌,说明干预组可能通过富集产生短链脂肪酸的有益菌进而提高短链脂肪酸含量以预防高脂饮食大鼠体重增加、调节血脂异常的作用。
4 结论
本研究表明,在菊粉复配AAP比例为2∶3时,与甘氨胆酸钠、牛磺胆酸钠结合率最高,随着AAP占比的升高,两者复配对胰脂肪酶抑制率也会升高,高于复配比例2∶3时,抑制率变化不大。菊粉复配AAP能够显著降低高脂饮食小鼠的体重、肝体比,血清TC、TG、LDL-C含量均极显著下降,HDL-C水平均显著升高。小鼠肝脏中脂肪滴数量和体积均明显减少,均比单一菊粉、AAP干预效果明显,菊粉复配AAP比例为2∶3效果最佳。菊粉复配AAP降低了高脂饮食小鼠肠道厚壁菌门与拟杆菌门的比例,提高了乳酸杆菌属、杆菌属、副拟杆菌属、拟杆菌属等产生短链脂肪酸菌属相对丰度,降低了脱硫弧菌属、螺杆菌属、扭链瘤胃球菌、Colidextribacter相对丰度,改善了高脂饮食对肠道菌群的影响。
[1] 许同丽, 刘钦弘, 王寅初, 等.肥胖影响下高血压与高血脂相关联的分子机制研究进展[J].中国现代应用药学, 2024, 41(4):545-555.
XU T L, LIU Q H, WANG Y C, et al.Research progress in the molecular mechanism of the relationship between hypertension and hyperlipidemia under the influence of obesity[J].Chinese Journal of Modern Applied Pharmacy, 2024, 41(4):545-555.
[2] 王丹萍, 徐珒昭, 张晓航, 等.糖尿病与宿主肠道菌群的关系及饮食介导的菌群调控作用研究进展[J].食品科学, 2023, 44(15):379-389.
WANG D P, XU J Z, ZHANG X H, et al.Progress in understanding the relationship between diabetes and host intestinal microbiota and diet-mediated microbiota regulation[J].Food Science, 2023, 44(15):379-389.
[3] WANG Y, FEI Y Q, LIU L R, et al.Polygonatum odoratum polysaccharides modulate gut microbiota and mitigate experimentally induced obesity in rats[J].International Journal of Molecular Sciences, 2018, 19(11):3587.
[4] ZONG X, ZHANG H, ZHU L Y, et al.Auricularia auricula polysaccharides attenuate obesity in mice through gut commensal Papillibacter cinnamivorans[J].Journal of Advanced Research, 2023, 52:203-218.
[5] LIU N N, CHEN X F, SONG J N, et al.Hypoglycemic effects of Auricularia auricula polysaccharides on high fat diet and streptozotocin-induced diabetic mice using metabolomics analysis[J].Food &Function, 2021, 12(20):9994-10007.
[6] 李静雯, 刘春霞, 李姗姗, 等.膳食纤维通过肠道对胆汁酸代谢的调控机制研究进展[J].食品与发酵工业, 2025, 51(7):351-359.
LI J W, LIU C X, LI S S, et al.Research progress on the regulation mechanisms of dietary fiber on bile acid metabolism through the intestine[J].Food and Fermentation Industries, 2025, 51(7):351-359.
[7] WAN X H, GUO H, LIANG Y Y, et al.The physiological functions and pharmaceutical applications of inulin:A review[J].Carbohydrate Polymers, 2020, 246:116589.
[8] 韩薇, 贺稚非, 谢兆华, 等.菊粉的功能特性及其在肉制品中的应用研究进展[J].食品与发酵工业, 2022, 48(16):311-317.
HAN W, HE Z F, XIE Z H, et al.The functional analysis of inulin and its application in meat products[J].Food and Fermentation Industries, 2022, 48(16):311-317.
[9] 冯焱, 蒙爱, 魏思昂, 等.菊粉通过调节肠道菌群改善Ⅱ型糖尿病小鼠的认知功能障碍[J].动物营养学报, 2024, 36(11):7305-7319.
FENG Y, MENG A, WEI S A, et al.Inulin ameliorates cognitive dysfunction in type Ⅱ diabetic mice by regulating intestinal flora[J].Chinese Journal of Animal Nutrition, 2024, 36(11):7305-7319.
[10] LI L L, WANG Y T, ZHU L M, et al.Inulin with different degrees of polymerization protects against diet-induced endotoxemia and inflammation in association with gut microbiota regulation in mice[J].Scientific Reports, 2020, 10:978.
[11] 马晟, 罗先群, 黄雪星, 等.黑木耳多糖分离纯化及生物活性研究进展[J].微生物学通报, 2025, 52(5):1967-1986.
MA S, LUO X Q, HUANG X X, et al.Research progress in isolation, purification, and biological activities of Auricularia heimuer polysaccharides[J].Microbiology China, 2025, 52(5):1967-1986.
[12] 张廷婷, 赵文颖, 谢倍珍, 等.黑木耳及其多糖对高脂饮食大鼠的降血脂和肠道菌群调节作用[J].中国食品学报, 2021, 21(9):89-101.
ZHANG T T, ZHAO W Y, XIE B Z, et al.Effects of Auricularia auricula and its polysaccharides on hypolipidemic and regulating intestinal flora in high-fat diet rats[J].Journal of Chinese Institute of Food Science and Technology, 2021, 21(9):89-101.
[13] ZHAO R Q, CHENG N H, NAKATA P A, et al.Consumption of polysaccharides from Auricularia auricular modulates the intestinal microbiota in mice[J].Food Research International, 2019, 123:383-392.
[14] 于美汇, 赵鑫, 尹红力, 等.碱提醇沉黑木耳多糖体外和体内降血脂功能[J].食品科学, 2017, 38(1):232-237.
YU M H, ZHAO X, YIN H L, et al.In vitro and in vivo hypolipidemic effect of Auricularia auricular polysaccharides[J].Food Science, 2017, 38(1):232-237.
[15] 曹叶霞, 李慧卿, 尹爱萍, 等.韭菜提取物对胰脂肪酶抑制作用的研究[J].粮食与油脂, 2023, 36(4):141-144;159.
CAO Y X, LI H Q, YIN A P, et al.Study on the inhibitory effect of leek extracts on pancreatic lipase[J].Cereals &Oils, 2023, 36(4):141-144;159.
[16] 何嘉烽. 黑木耳多糖的降血脂作用及相关机制的初步探讨[D].广州:广东药科大学, 2019.
HE J F.Preliminary discussion on the hypolipidemic effect of auricularia auricula polysaccharides and its related mechanisms[D].Guangzhou:Guangdong Pharmaceutical University, 2019.
[17] SONG E J, SHIN N R, JEON S, et al.Lorcaserin and phentermine exert anti-obesity effects with modulation of the gut microbiota[J].Frontiers in Microbiology, 2023, 13:1109651.
[18] SCHAUS S R, VASCONCELOS PEREIRA G, LUIS A S, et al.Ruminococcus torques is a keystone degrader of intestinal mucin glycoprotein, releasing oligosaccharides used by Bacteroides thetaiotaomicron[J].mBio, 2024, 15(8):e00039-24.
[19] O-SULLIVAN I, NATARAJAN ANBAZHAGAN A, SINGH G, et al.Lactobacillus acidophilus mitigates osteoarthritis-associated pain, cartilage disintegration and gut microbiota dysbiosis in an experimental murine OA model[J].Biomedicines, 2022, 10(6):1298.
[20] ZHU Y Q, CHEN B R, ZHANG X Y, et al.Exploration of the Muribaculaceae family in the gut microbiota:Diversity, metabolism, and function[J].Nutrients, 2024, 16(16):2660.
[21] CHAMBERS E S, VIARDOT A, PSICHAS A, et al.Effects of targeted delivery of propionate to the human colon on appetite regulation, body weight maintenance and adiposity in overweight adults[J].Gut, 2015, 64(11):1744-1754.