皮肤是人体最大的器官,由表皮、真皮和皮下层组成,在温度调节、环境刺激检测以及保护身体免受外部压力源损伤方面起着关键作用[1]。紫外线是造成皮肤损伤的最主要环境因子,会损害皮肤的结构完整性和生理功能[2]。中波紫外线(ultraviolet B,UVB)是UV的重要组成部分,其波长介于290~320 nm,能够穿透大气层并抵达皮肤表皮层,是导致皮肤光损伤的主要因素[3-4]。短时过度或长期暴露于UVB辐射下,皮肤会出现干燥、皱纹及不规则色素沉着等特征,从而引发晒伤、色素沉着,甚至皮肤癌[5]。
UVB辐射会打破皮肤细胞微环境中的氧化还原稳态,进而诱发皮肤的氧化应激反应,这是UVB造成皮肤光损伤的开端[6]。UVB辐射诱发皮肤产生炎性细胞因子,进而引发皮肤炎症反应,使皮肤产生红斑与水肿[7]。这些炎性细胞因子能够进一步提升基质金属蛋白酶(matrix metalloproteinases,MMPs)的表达水平,促使I型胶原蛋白、弹性蛋白及透明质酸的分解,导致细胞外基质降解,最终引发皮肤水分流失并促进皱纹的形成[8]。因此,减轻氧化应激反应、遏制炎症因子的产生,抑制MMPs的过度表达是改善UVB造成皮肤光损伤的有效途径。
随着对皮肤生理机制的不断深入研究,皮肤代谢物引起了越来越多的关注。这些代谢物不仅影响着皮肤的外观和功能,还与多种皮肤疾病的发生和发展密切相关[9]。皮肤代谢产物源自皮肤细胞成分,如角质形成细胞、黑素细胞及成纤维细胞;也可来源于皮肤液体环境,包括汗液、皮脂和间质液[10]。皮肤代谢物种类繁多、功能各异。其中,氨基酸类代谢物对皮肤的功能和外观存在重要影响[11];脂质类代谢物在支持皮肤屏障功能、细胞信号传导和抗菌防御方面发挥关键性作用[12];脂肪酸类代谢物能够维持皮肤屏障完整性、调节皮肤免疫[13]。这些代谢产物在环境应激因素、药物作用、基因突变等的触发下产生变化,从而影响皮肤状态[5,14]。研究表明,UV辐射会降低脂质代谢从而增强免疫抑制;也会增加氨基酸代谢从而导致皮肤炎症[15]。在UVB诱导的人永生化表皮细胞(human immortalized keratinocytes,HaCaT)光损伤模型中,碳水化合物、氨基酸和谷胱甘肽代谢途径发生显著变化[16]。UVB诱导的人皮肤成纤维细胞(human foreskin fibroblast-1,HFF-1)体外光损伤模型研究显示,甘油磷脂与谷胱甘肽代谢是皮肤真皮区域应对UV损伤的重要途径[17]。可见,在皮肤UVB光损伤防护的研究中,皮肤代谢物及途径是较有价值的机制揭示切入点。
越来越多的研究表明,膳食中添加功能性成分可以保护皮肤免受UV光损伤[18]。天然植物多糖因其保湿性、美白性、抗氧化、抗炎、抗菌等功效在保护皮肤方面优势显著[19]。在缓解皮肤UV光损伤方面,天然多糖也展现了其潜在的应用价值。例如,口服羊栖菜多糖能够通过抑制MMPs的表达对UVB辐射的无毛昆明小鼠表现出显著的保护作用,并减少了UVB诱导的氧化应激[20]。口服黑加仑多糖抑制了UV辐射引起的皮肤脱水,并降低了小鼠皮肤组织中的IL-6和MMPs转录水平[21]。树莓多糖是从树莓果实中提取的多糖,多项研究表明,树莓多糖具备抗氧化、缓解疲劳、免疫调节及降低血脂等多重生物功能[22-24]。前期研究发现,树莓粗多糖(raspberry crude polysaccharides,RCP)能够通过降低炎症水平和缓解氧化应激来预防UVB对HaCaT造成的光损伤[25]。本研究以前期研究为基础,利用UVB诱导的BALB/c小鼠皮肤光损伤模型进一步在整体水平探究动物口服RCP对皮肤UVB光损伤的防护作用,并通过非靶向代谢组学筛选出响应这一过程的皮肤代谢产物及途径,为RCP在食品、保健品及口服美容等领域的进一步应用提供参考,也为其后续作用机理的深入研究奠定基础。
1 材料与方法
1.1 材料与试剂
树莓冷冻果,青海树莓农业产业化有限公司;BALB/c雌性小鼠,8周龄,北京华阜康生物科技股份有限公司[动物生产许可证为SCXK(京)2019-0008,使用许可证为SL-2023036];PBS,青海莱茵尔生物科技有限责任公司;超氧化物歧化酶(superoxide dismutase,SOD)(A001-3, WST-1法)检测试剂盒、过氧化氢酶(catalase,CAT)(A007-1-1,可见光法)检测试剂盒,南京建成生物技术研究所;IL-6、TNF-α、基质金属蛋白酶-3(matrix metalloproteinases-1,MMP-3)酶联免疫吸附测定试剂盒(enzyme linked-immuno-sorbent assay,ELISA),武汉伊莱瑞特生物科技股份有限公司;快速蛋白质定量试剂盒(BCA法),亚科因(武汉)生物技术有限公司。
1.2 仪器与设备
CBCL-24冷冻研磨仪,上海测博生物技术发展中心;1510酶标仪,赛默飞世尔仪器有限公司;L125紫外辐照计,深圳市林上科技有限公司;AB Triple TOF 6600质谱仪,SCIEX公司;1290 Infinity LC超高效液相色谱系统,安捷伦科技(中国)有限公司。
1.3 实验方法
1.3.1 RCP的制备
使用超声波辅助法提取[26]。将树莓果粉进行脱脂处理,随后加入乙醇进行回流处理。对经过上述处理的树莓果粉进行超声波提取,并离心得到上清液。随后,利用Sevage法除去蛋白质,将水溶液减压浓缩。并加入粮食酒精沉淀。将沉淀冷冻干燥,得到RCP。采用苯酚硫酸法测得RCP的多糖含量为(84.20±1.34)%[27],采用快速蛋白质定量试剂盒测得蛋白质含量为(8.60±4.32)%。
1.3.2 动物饲养与分组
BALB/c小鼠适应性喂养7 d后随机分为5组,每组8只。分别为CK组(不经UVB辐照);UVB模型组;经预实验确定RCP的剂量为口服低剂量组(100 mg/kg)、中剂量组(200 mg/kg)和高剂量组(400 mg/kg)。动物实验经青海大学科技伦理委员会批准,编号为SL-2023036。
1.3.3 UVB皮肤光损伤动物模型的建立
小鼠经背部毛发剃除处理后,采用隔日一次的UVB照射方案(每次于上午时段进行辐射)。通过观察各组小鼠表皮红斑、皱纹形成及角质层脱落等变化,评价UVB辐射对皮肤组织造成的损伤程度。在预实验中已确定最小红斑剂量(minimum erythema dose,MED)为60 mJ/cm2。每经过一个7 d的周期,辐照剂量在前一周的基础上增加1个MED,即第一周60 mJ/cm2;第二周120 mJ/cm2;第三周180 mJ/cm2;第四周240 mJ/cm2。除空白组小鼠外,其余各组小鼠均使用UVB辐照装置对背部皮肤进行辐照。在UVB照射前60 min,空白组和模型组小鼠均灌胃100 μL蒸馏水,RCP组小鼠灌胃100 μL不同剂量的RCP。
1.3.4 光损伤小鼠皮肤组织收集与保存
实验完成后,所有实验组的小鼠被实施禁食处理(持续12 h,期间保持饮水自由),随后采用体积分数为2%~4%的乙醚进行麻醉,并立即通过颈椎脱位法处死。从小鼠背部采集皮肤组织样本,剔除附着的脂肪组织,并使用PBS充分漂洗以去除残留血液。用吸水纸轻轻吸干样本表面水分,随即将其置于冻存管内,并保存在-80 ℃条件下,以备后续分析使用。
1.3.5 皮肤组织苏木精-伊红(hematoxylin-eosin,H&E)染色
将小鼠背部皮肤组织用质量分数为4%的多聚甲醛溶液固定,包埋在石蜡中,切片经H&E染色。采用数字切片扫描仪对切片进行图像采集。
1.3.6 UVB诱导的光损伤小鼠皮肤组织中生化指标的测定
取小鼠皮肤组织样本按料液比1∶9(g∶mL)加入PBS,使用冷冻研磨仪将混合物制备成质量分数为10%的皮肤组织匀浆,收集上清液。根据说明,采用ELISA试剂盒测定小鼠皮肤组织中MMP-3、IL-6和TNF-α的含量,使用微板法测定小鼠皮肤组织中SOD和CAT活力。
1.3.7 非靶向代谢组学分析
采用超高效液相色谱-串联飞行时间质谱联用仪检测样本中的代谢物。采用AB Triple TOF 6600质谱仪进行样本一级、二级谱图的采集。样品经Agilent 1290 Infinity LC超高效液相色谱系统分离后,用Triple TOF 6600质谱仪进行质谱分析,分别采用电喷雾电离(electrospray ionization,ESI)正离子和负离子模式进行检测。ESI源设置参数如下:雾化气辅助加热气1(Gas1):60,辅助加热气2(Gas2):60,气帘气 (CUR)30 psi,离子源温度600 ℃,喷雾电压(ISVF)±5 500 V(正负2种模式);一级质荷比检测60~1 000 Da,二级子离子质荷比检测25~1 000 Da,一级质谱扫描累积时间0.20 s/spectra,二级质谱扫描累积时间0.05 s/spectra;二级质谱采用数据依赖型采集模式(information dependent acquisition,IDA)获得,并且采用峰强度值筛选模式,去簇电压(declustering potential,DP)±60 V(正负2种模式),碰撞能量(35±15) eV。IDA设置如下:动态排除同位素离子范围:4 Da,每次扫描采集10个碎片图谱。
1.4 数据分析
采用GraphPad Prism 9.5.1软件,对实验数据进行单因素方差分析,所有数据均以“平均值±标准差”表示,P<0.05或P<0.01表示有统计学意义。使用联川生物云平台(https://www.omicstudio.cn/tool)的OmicStudio工具进行生物信息学分析。
2 结果与分析
2.1 RCP对UVB诱导的皮肤光损伤组织病理学的影响
根据H&E染色结果,空白组小鼠皮肤的角质层、表皮层、真皮层结构清晰(图1-a)。模型组小鼠表皮增厚明显,可见局部角化过度,真皮层可见纤维组织增生并伴有炎性细胞浸润,且真皮层与表皮层边界模糊(图1-b)。RCP低、中和高剂量组小鼠皮肤表皮增厚、局部角化过度现象均有缓解。同时,纤维组织增生得到抑制,炎性细胞浸润减少,真皮层与表皮层之间的界限变得更为清晰(图1-c~图1-e),且随着RCP剂量的升高改善效果越来越明显。
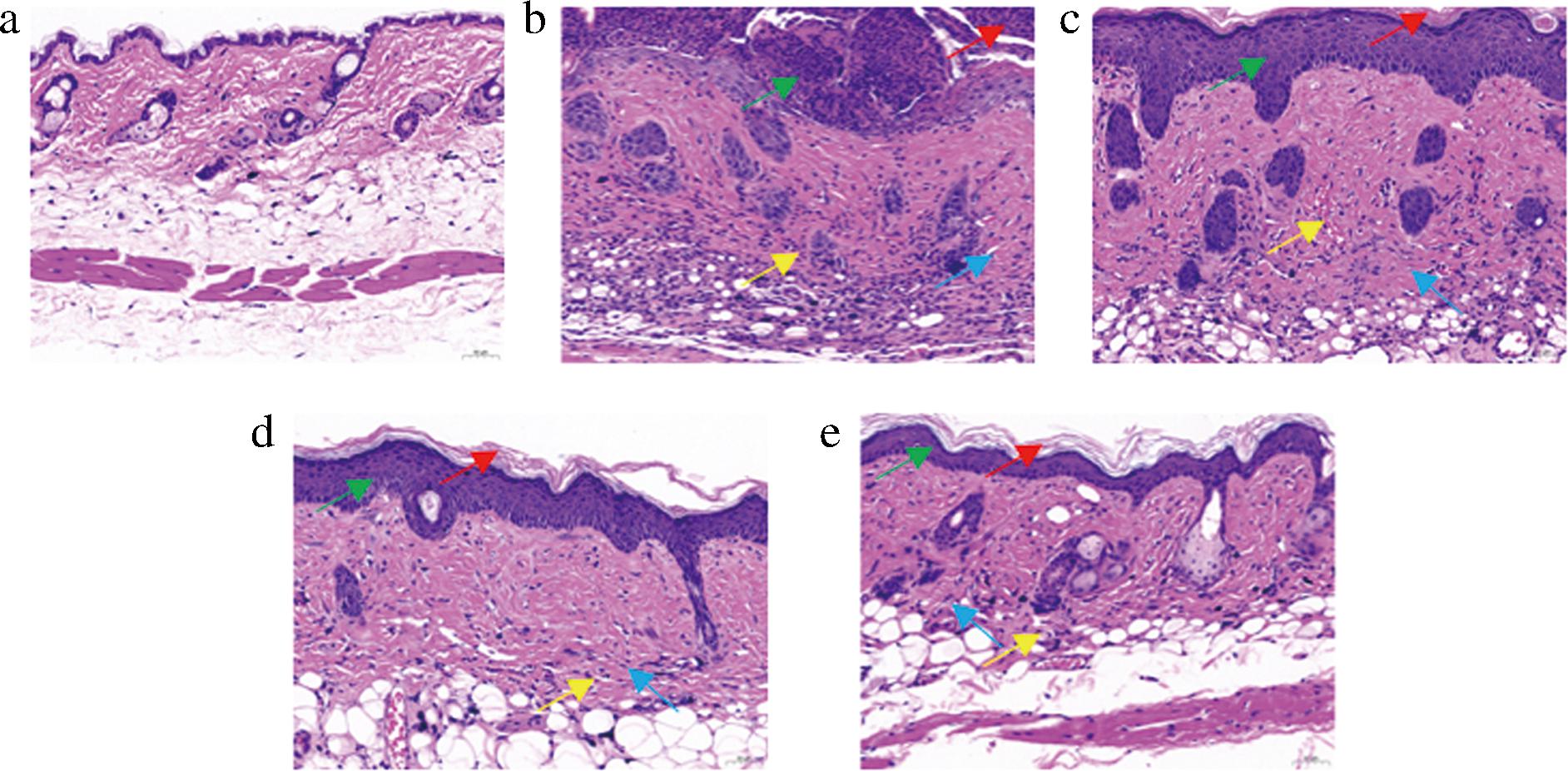
a-空白组;b-模型组;c-RCP低剂量组;d-RCP中剂量组;e-RCP高剂量组
图1 RCP对UVB诱导的光损伤小鼠皮肤组织病理学的影响
Fig.1 Effect of RCP on skin histopathology in UVB-induced photodamage of mice
注:表皮增厚(↑)角化过度(↑)淋巴细胞(↑)纤维组织增生(↑)。
2.2 RCP对UVB诱导的皮肤光损伤小鼠抗氧化酶活力的影响
为了评价RCP对UVB诱导的氧化应激的保护作用,测定了小鼠皮肤组织中抗氧化酶的活力,如图2所示。UVB组SOD和CAT活力极显著低于空白组(P<0.01),表明氧化损伤严重。与UVB组相比,低、中和高剂量的RCP均可极显著提高SOD和CAT的活力(P<0.01),且呈现剂量依赖效应。
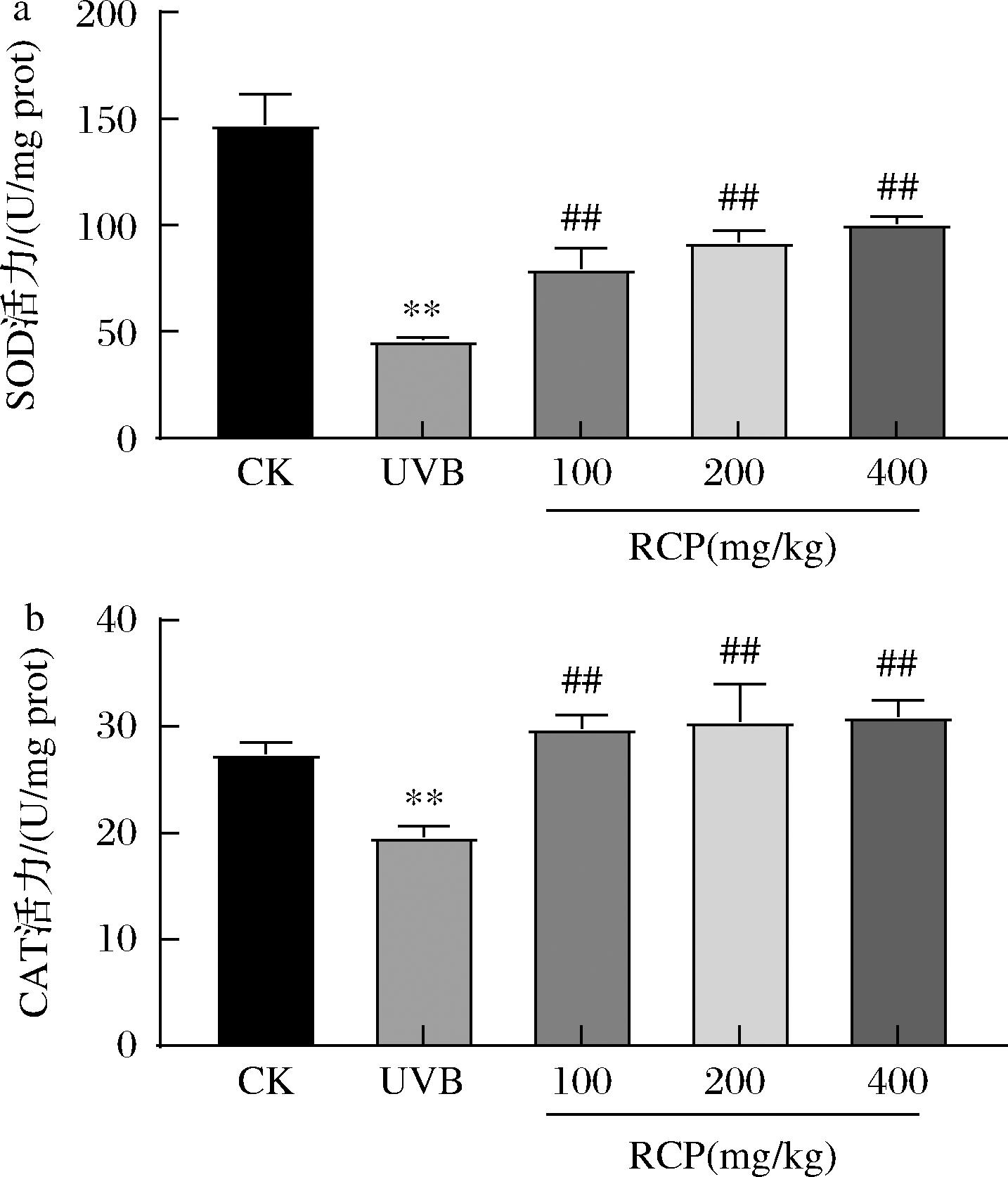
a-SOD;b-CAT
图2 RCP对UVB诱导的光损伤小鼠皮肤组织中抗氧化酶活力的影响
Fig.2 Effect of RCP on anti-oxidant enzyme activities in UVB-induced photodamaged mouse skin tissue
注:*表示模型组与空白组差异显著(P<0.05),**表示模型组与空白组的差异极显著(P<0.01);#表示RCP组与模型组的差异显著(P<0.05),##表示RCP组与模型组的差异极显著(P<0.01)(下同)。
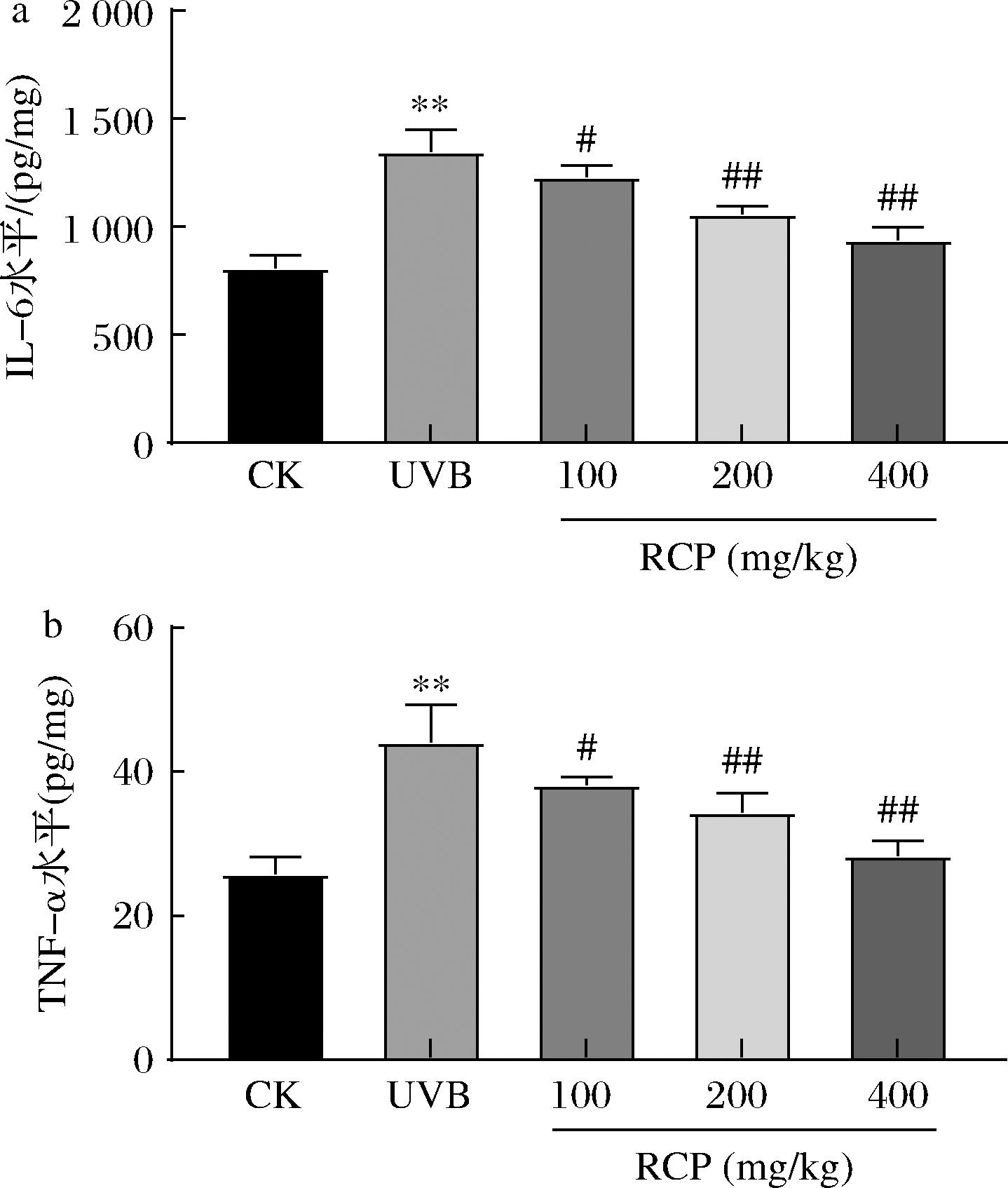
a-IL-6;b-TNF-α
图3 RCP对UVB诱导的光损伤小鼠皮肤组织中IL-6和TNF-α水平的影响
Fig.3 Effect of RCP on IL-6 and TNF-α levels in UVB-induced photodamaged mouse skin tissue
2.3 RCP对UVB诱导的皮肤光损伤小鼠的IL-6和TNF-α水平的影响
如图3所示,相较于空白组,UVB辐射极显著提高了皮肤中炎症因子TNF-α和IL-6的水平(P<0.01),与UVB组相比,RCP低剂量组显著降低了TNF-α和IL-6的水平(P<0.05);RCP中和高剂量组均极显著降低了TNF-α和IL-6的水平(P<0.01),且RCP对IL-6和TNF-α水平的降低作用呈剂量依赖性。该结果表明,UVB光损伤的皮肤中,RCP显示出良好的抗炎作用。
2.4 RCP对UVB诱导的皮肤光损伤小鼠MMP-3含量的影响
如图4所示,模型组MMP-3含量极显著升高(P<0.01),RCP中和高剂量组小鼠皮肤中MMP-3的含量显著低于UVB组(P<0.01)。说明,RCP能够通过降低MMP-3含量对UVB诱导的皮肤光损伤发挥保护作用。
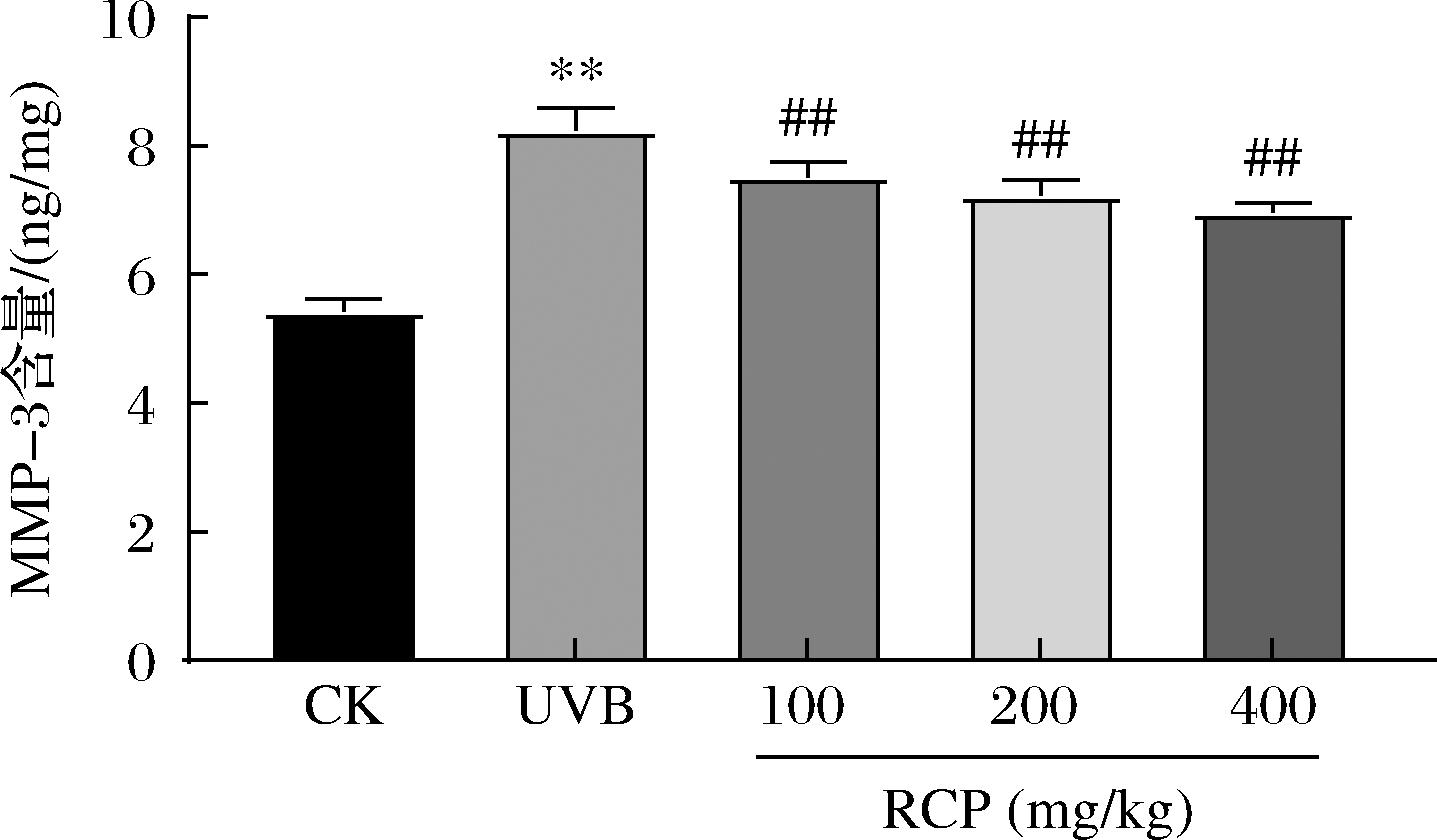
图4 RCP对UVB诱导的光损伤小鼠皮肤组织中MMP-3含量的影响
Fig.4 Effect of RCP on MMP-3 concentration in UVB-induced photodamaged mouse skin tissue
2.5 UVB诱导的皮肤光损伤小鼠皮肤代谢物分类
为进一步探究口服RCP对UVB诱导的皮肤光损伤的防护作用及其对皮肤代谢物的影响,对3组(空白组、UVB组、RCP组)小鼠背部皮肤组织进行了非靶向代谢组学分析。在空白组、UVB组和RCP组中共鉴定出1 654种代谢物,其中正离子模式鉴定出1 054种,负离子模式鉴定出599种。代谢物分类信息如图5所示,占比最高的前3类分别为有机酸及其衍生物(29.87%)、脂质及类脂分子(26.90%)和有机杂环化合物(9.07%)。
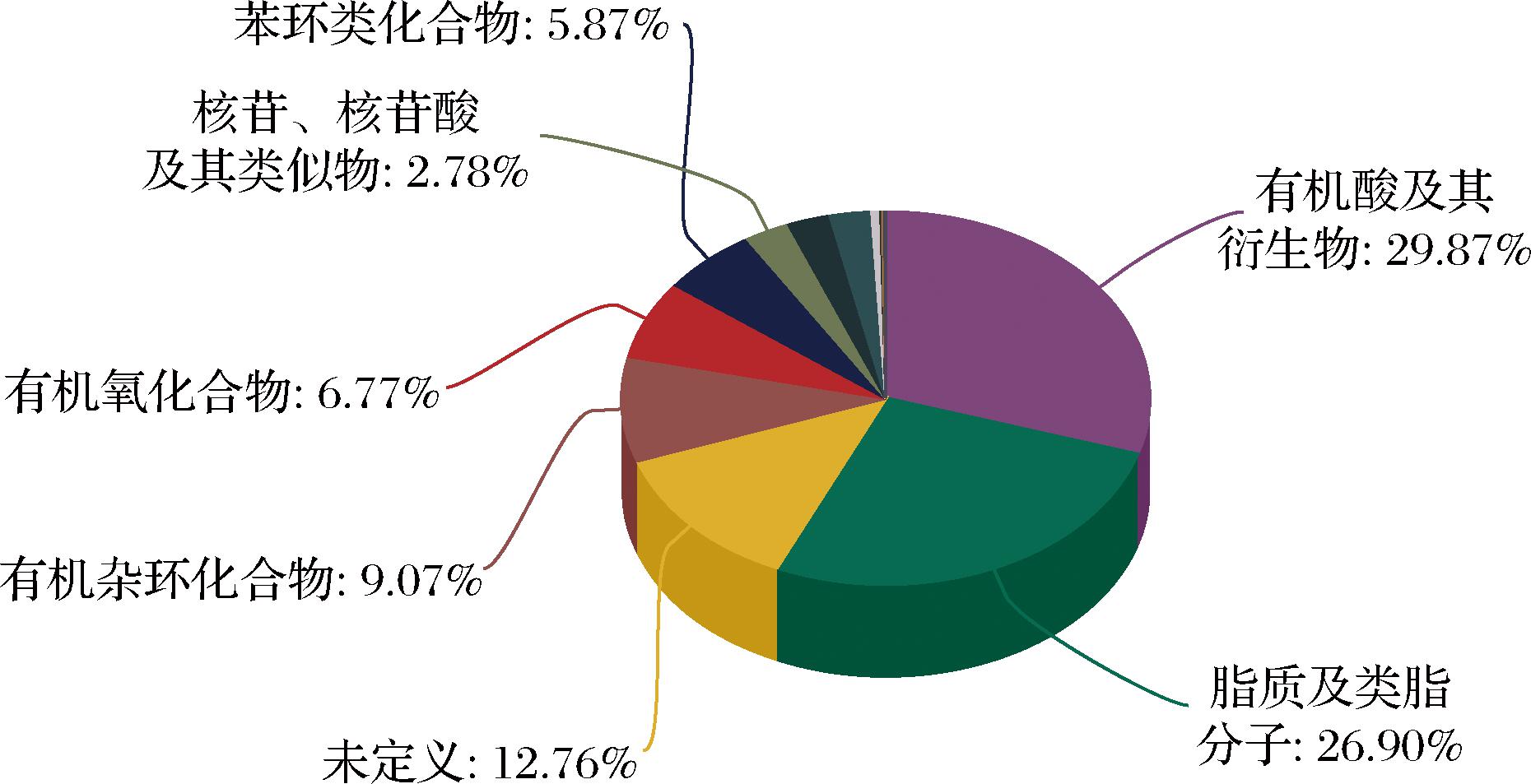
图5 UVB诱导的皮肤光损伤小鼠皮肤代谢物分类
Fig.5 Classification of skin metabolites in UVB-induced photodamage mice
2.6 RCP对UVB诱导的皮肤光损伤小鼠皮肤代谢产物的影响
采用主成分分析(principal component analysis,PCA)和偏最小二乘判别分析(partial least squares discriminant analysis,PLS-DA)对空白组、UVB组和RCP组(400 mg/kg)皮肤组织中代谢物进行分析。PCA和PLS-DA评分图显示,空白组和UVB组的样本明显分离,RCP组和UVB组也有明显的分离趋势(图6),且与UVB组相比,RCP组更接近空白组。表明与正常皮肤相比,UVB辐射导致明显的皮肤代谢异常,应用RCP后皮肤的异常代谢有所恢复,小鼠皮肤中的代谢物与正常皮肤更接近。
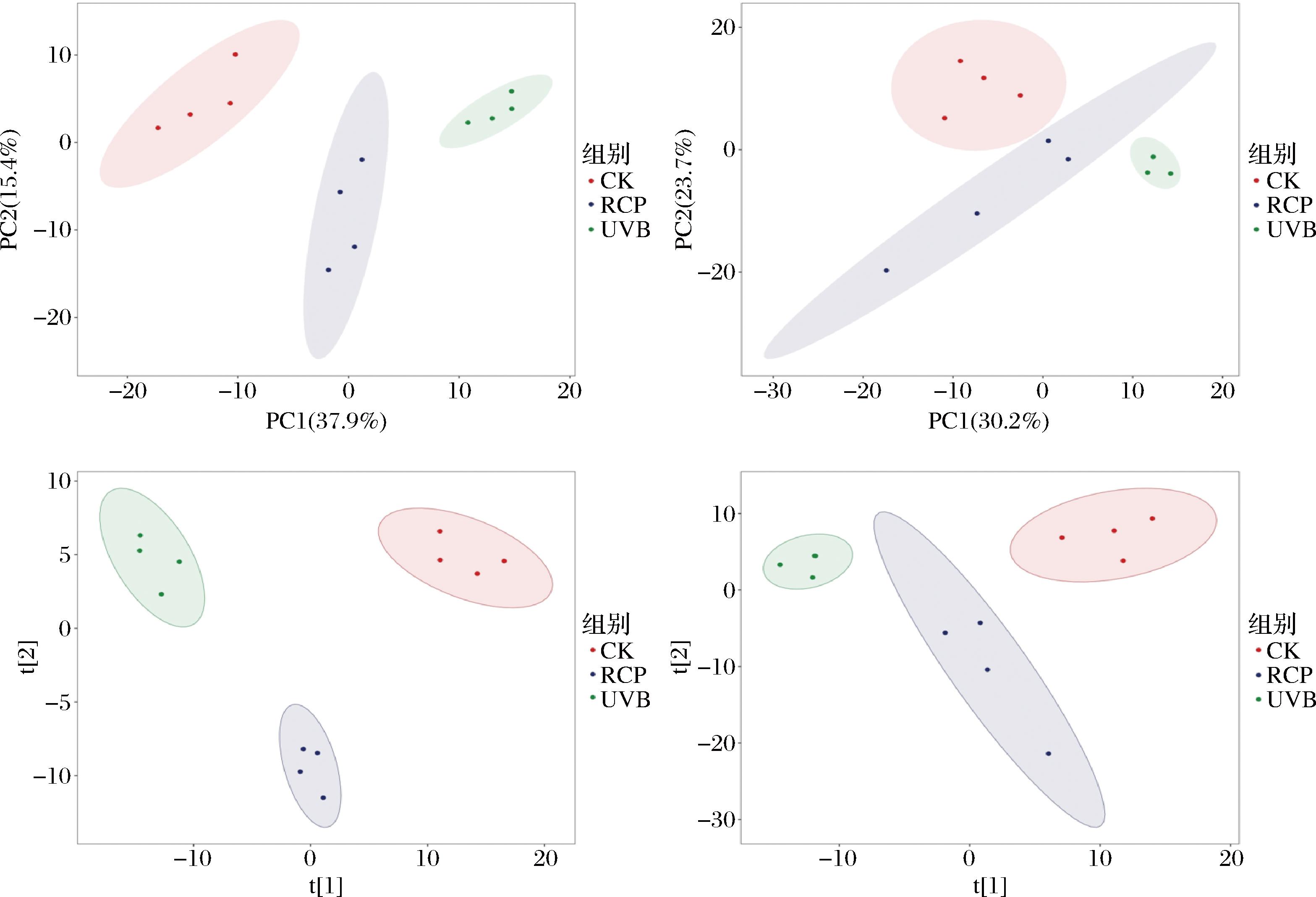
a-PCA-正离子;b-PCA-负离子;c-PLS-DA-正离子;d-PLS-DA-负离子
图6 RCP对UVB光损伤小鼠皮肤代谢产物的影响
Fig.6 The effect of RCP on skin metabolites in UVB-induced photodamage mice
2.7 UVB诱导的皮肤光损伤小鼠皮肤差异代谢产物鉴定
以P<0.05作为筛选标准在空白组、UVB组和RCP组间进一步筛选出58种差异代谢物。将P值从小到大排序,选取前20的差异代谢产物进行聚类热图分析(图7)。颜色越红表示代谢物相对表达量越高,越蓝表示代谢物相对表达量越低。在空白组中,原本高表达的代谢物经UVB辐射后表达量明显下降,而经过RCP处理后,其表达量又有所上升。相反,空白组中原本低表达的代谢物在UVB辐射后表达量明显上升,但在应用RCP后,其表达量又呈现下降趋势。以上结果表明,RCP干预能够改善UVB引起的小鼠皮肤代谢异常,使光损伤小鼠皮肤代谢物水平向空白组小鼠趋近。
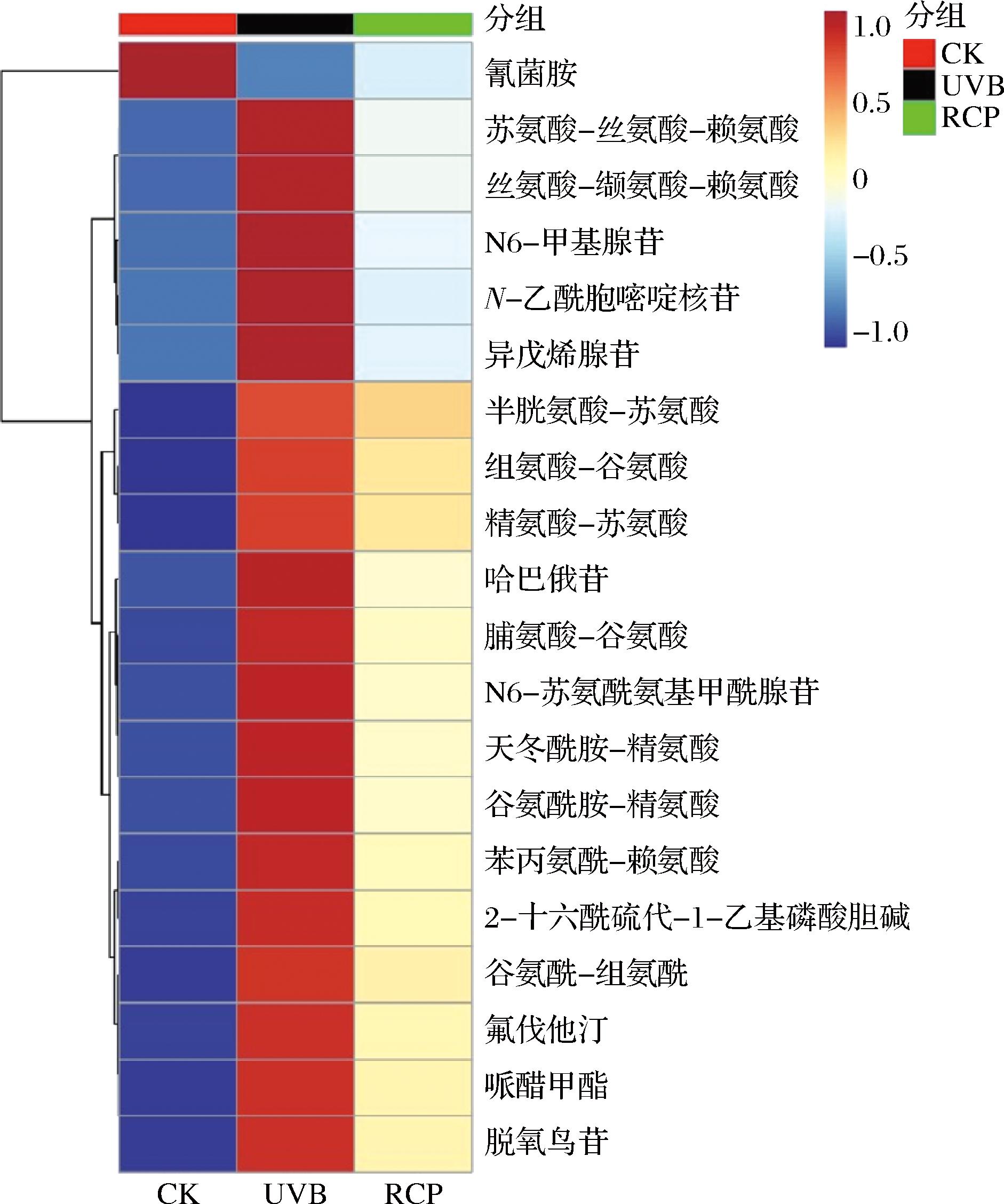
图7 差异代谢物聚类热图
Fig.7 Heatmap of differential metabolite clustering
2.8 差异代谢物的代谢通路分析
进一步对空白组与UVB组、UVB组与RCP组的差异代谢物进行KEGG通路富集分析,以P<0.05为标准筛选RCP干预UVB皮肤光损伤小鼠影响的代谢通路。由图8-a和图8-b可知,这些差异代谢物路最为显著。进一步将氨基酸代谢通路进行富集,主要富集到氨基酸代谢通路、癌症、碳水化合物代谢和心血管疾病等代谢通路上,其中以氨基酸代谢通析,涉及丙氨酸、天冬氨酸和谷氨酸代谢、组氨酸代谢、精氨酸生物合成和苯丙氨酸、酪氨酸和色氨酸生物合成途径,其中丙氨酸、天冬氨酸和谷氨酸代谢途径最为显著(图8-c)。以上结果表明,RCP干预可能通过影响光损伤小鼠皮肤中丙氨酸、天冬氨酸和谷氨酸代谢途径发挥其UVB防护作用。
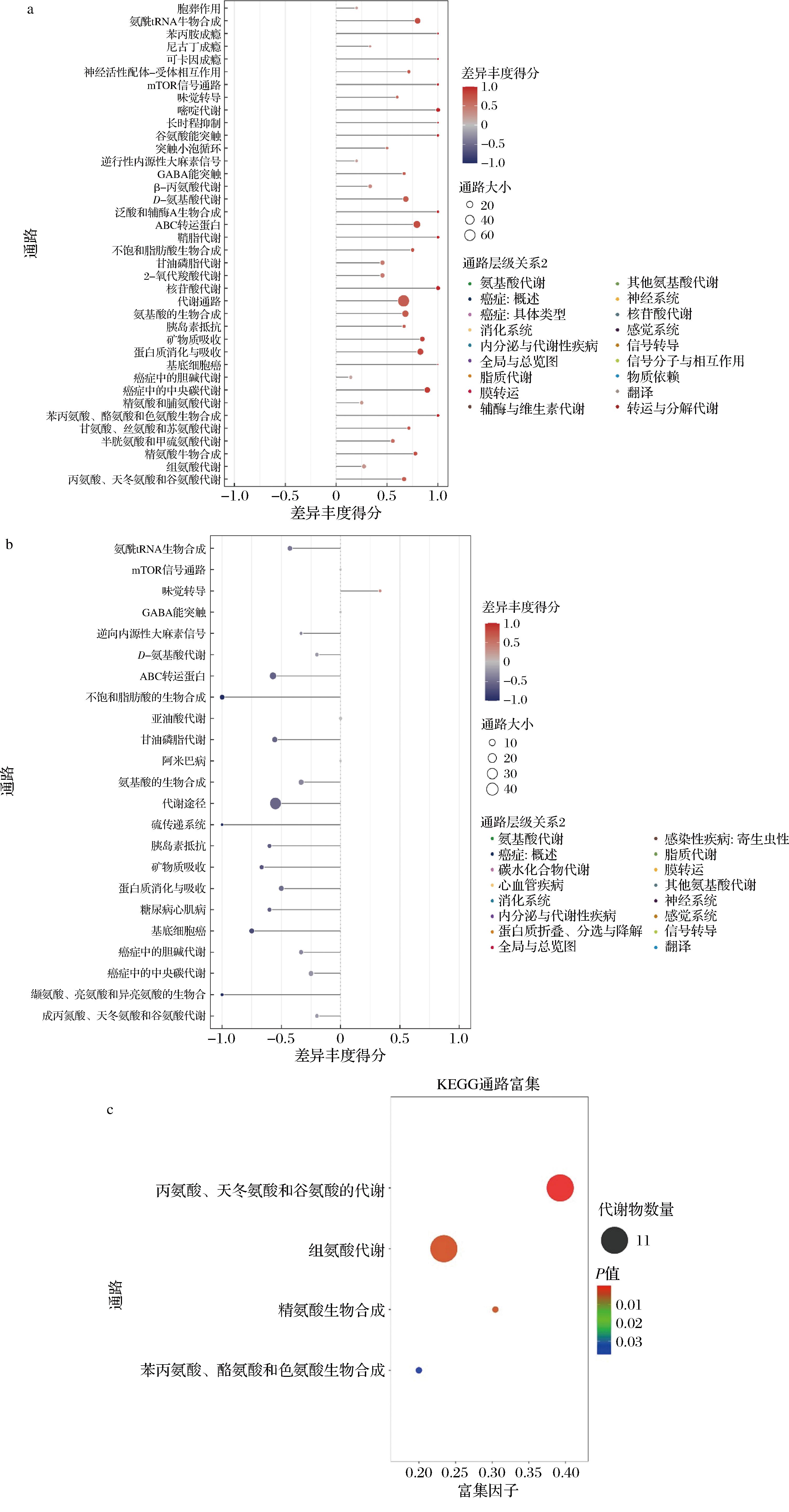
a-代谢通路分类(空白组vs UVB组);b-代谢通路分类(空白组vs RCP组);c-代谢通路富集
图8 差异代谢产物KEGG富集分析
Fig.8 Analysis of KEGG enrichment of differential metabolites
2.9 生化指标与差异氨基酸代谢物的相关性分析
对生化指标和丙氨酸、天冬氨酸和谷氨酸相关代谢物进行Pearson相关性层次聚类分析,见图9。丙氨酸与SOD呈显著正相关,DL-天冬酰胺、谷氨酸、L-谷氨酰胺和N-乙酰基-L-天冬氨酸与SOD呈显著负相关。以上结果表明,皮肤光损伤小鼠皮肤代谢物的改变与氧化应激密切相关。
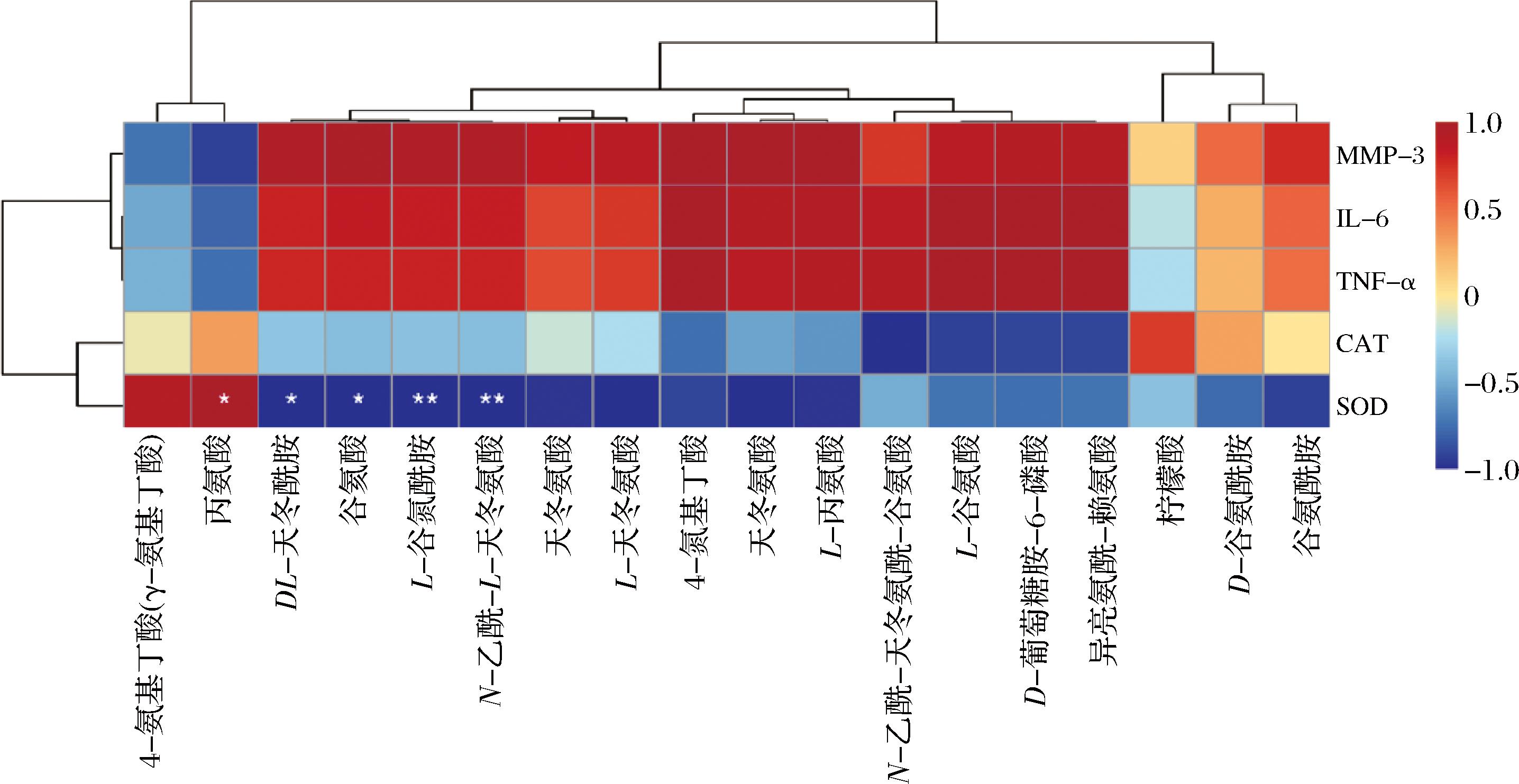
图9 生化指标与差异代谢物相关性分析
Fig.9 Correlation analysis of biochemical indicators with differential metabolites
3 结论与讨论
本研究中RCP的剂量范围(100、200、400 mg/kg)选择基于预实验的皮肤状态评估及同类天然产物的剂量依据。预实验结果显示,200、400 mg/kg剂量组均能显著改善UVB诱导的皮肤红斑和脱屑,且本研究剂量范围与其他天然产物的剂量具有可比性。例如,如羊栖菜多糖在UVB小鼠光损伤的剂量为200、400、600 mg/kg[20],红景天苷在UVB小鼠光损伤模型中的剂量为50、100、200 mg/kg[28],未成熟苹果提取物的剂量为100、200、400 mg/kg[29]。所以本研究选择100、200、400 mg/kg作为正式实验剂量。
UVB辐射会破坏体内的氧化-抗氧化平衡,引发氧化应激,导致皮肤光损伤及严重的氧化损伤,进而损伤皮肤屏障并引发皮肤炎症[30-31]。人体皮肤中的SOD、CAT等抗氧化酶对于抵御UVB辐射引起的氧化应激和维持体内氧化-还原平衡至关重要[32]。SOD家族特别是SOD3亚型的功能不仅局限于抗氧化防御,也参与免疫反应。研究表明,SOD通过清除超氧阴离子,抑制NF-κB通路的激活,减少IL-6和TNF-α等促炎因子的释放,从而减轻炎症反应[33]。SOD3作为哺乳动物SOD亚型之一,可能抑制CD4+ T细胞的早期激活,从而抑制其分化为Th2和Th17细胞[34]。SOD3还可通过减少IL-2、IL-4和IL-17细胞因子的分泌来控制Th2和Th17细胞的活化、增殖和分化[35]。进一步研究表明,SOD3处理通过在体外和体内抑制TLR2/p38/NF-κB信号轴和NLRP3炎性小体激活来抑制炎性细胞因子(TNF-α、IL-1β、IL-6和IL-8)的表达[36]。UVB辐射也会通过产生促炎细胞因子诱发皮肤的炎症反应。TNF-α可诱导产生下游炎症介质IL-6,这些炎症因子进一步介导表皮细胞的生长过程,从而导致表皮增生现象[37]。本研究H&E染色结果也显示,模型组小鼠表皮增厚明显并伴有炎性细胞浸润。上述炎症因子还可通过信号传导途径,增加MMPs的合成和分泌[38]。MMP-3是皮肤光损伤过程中导致细胞外基质降解的最重要MMPs之一,能够降解各种类型的细胞外基质并以促酶形式激活其他MMP的分泌,最终导致皮肤出现皱纹和松弛[39]。已有研究表明,植物多糖具有良好的抗氧化和抗炎活性,能够缓解UVB诱导的皮肤光损伤。例如石斛多糖能够通过提高抗氧化酶SOD和CAT的活力,缓解UVB诱导的皮肤光损伤昆明小鼠的氧化应激,此外,石斛多糖降低了炎症因子IL-6、TNF-α和MMP-3的表达[40]。在UVB诱导的小鼠皮肤光损伤模型中,水母雪莲多糖能够缓解UVB辐射诱导的表皮增厚和胶原纤维结构松散,提高SOD活力[41]。本研究结果显示,RCP缓解了皮肤光损伤小鼠的表皮增厚,纤维组织增生及炎性细胞浸润现象;增加了光损伤小鼠皮肤中SOD和CAT活力,并降低IL-6、TNF-α和MMP-3水平。能明显减轻UVB诱导的小鼠皮肤光损伤,与上述结果一致。
在小鼠皮肤组织非靶向代谢组学分析中,UVB组小鼠的代谢表型与健康小鼠有明显差异。RCP干预后,它们的表型接近空白组,表明RCP影响了皮肤光损伤小鼠的皮肤代谢。随后,对差异代谢物进行聚类、注释,共鉴定到58种差异代谢产物,且RCP改变了差异代谢物的表达量。KEGG富集分析结果显示,丙氨酸、天冬氨酸和谷氨酸代谢是RCP干预后差异最显著的代谢途径。相关性分析结果显示,丙氨酸与SOD呈显著正相关,DL-天冬酰胺、谷氨酸、L-谷氨酰胺和N-乙酰基-L-天冬氨酸呈显著负相关。说明这些代谢物可能在氧化应激方面起重要作用。丙氨酸作为疏水氨基酸更容易与脂质分子相互作用并形成厚膜。这可以保护可氧化脂质免受自由基或其他氧化性物质的直接攻击[42]。丙氨酸还可以提高酪氨酸酶的抑制活力,并具备破坏黑色生成的能力[43]。谷氨酸作为谷胱甘肽合成的前体在维持细胞的抗氧化防御系统方面至关重要,UVB辐射已被证明能抑制谷胱甘肽的合成过程,进而引发氧化应激反应,并加速角质形成细胞的凋亡[16]。谷氨酰胺是谷氨酸的一种衍生物,在维持皮肤结构完整性、促进水合作用及加速皮肤修复进程中扮演着核心角色,因此成为皮肤护理不可或缺的成分[44]。谷氨酰胺还能够生成抗氧化剂,有效抵御外界杂质对皮肤造成的损害[45]。此外,丙氨酸、天冬氨酸代谢可能与免疫抑制降低、表皮厚度增加和细胞浸润增加有关。在急性UVB辐射的小鼠皮肤代谢物中,观察到丙氨酸、天冬氨酸和谷氨酸代谢的增强,这与本研究结果一致。此外,丙氨酸、天冬氨酸代谢可能与免疫抑制降低、表皮厚度增加和细胞浸润增加有关[13]。
综上所述,RCP能够通过提高SOD和CAT的活力、降低IL-6、TNF-α和MMP-3的水平来缓解UVB诱导的BALB/c小鼠皮肤光损伤。同时,RCP或可通过调控丙氨酸、天冬氨酸及谷氨酸的代谢途径,有效减轻UVB引发的皮肤氧化应激反应,进而缓解UVB所致的皮肤光损伤。本研究提示RCP是一种有效缓解UVB皮肤光损伤的天然物质,为RCP的后续开发和利用提供了理论依据。同时,本研究也为后期从调节氨基酸代谢的角度进一步揭示RCP缓解皮肤UVB光损伤的作用机制奠定了研究基础。
[1] AHMAD UMAR S, TASDUQ S A.Integrating DNA damage response and autophagy signalling axis in ultraviolet-B induced skin photo-damage:A positive association in protecting cells against genotoxic stress[J].RSC Advances, 2020, 10(60):36317-36336.
[2] 郑雅文, 杨安全, 王菁, 等.蚌肉多糖的提取分离及对UVB损伤的修复作用[J].食品工业科技, 2024, 45(19):346-356.
ZHENG Y W, YANG A Q, WANG J, et al.Extraction and separation of Hyriopsis cumingii polysaccharide and the repairing effect on UVB damage[J].Science and Technology of Food Industry, 2024, 45(19):346-356.
[3] 王安娜, 方梦婕, 唐超, 等.丹参素对UVB诱导的皮肤光老化小鼠的保护作用和抗氧化机制研究[J].日用化学工业(中英文), 2024, 54(1):65-72.
WANG A N, FANG M J, TANG C, et al.Protective effect and antioxidant mechanism of danshensu on UVB-induced skin photoaging mice[J].China Surfactant Detergent &Cosmetics, 2024, 54(1):65-72.
[4] 黄菁霞, 沈伟花, 陈嘉志, 等.光甘草定包合物对中波紫外线诱导小鼠皮肤光损伤的保护作用[J].食品安全质量检测学报, 2024, 15(5):165-172.
HUANG J X, SHEN W H, CHEN J Z, et al.Protection of glabridin inclusion on middlewave ultraviolet radiation induced skin photo damage in mice[J].Journal of Food Safety &Quality, 2024, 15(5):165-172.
[5] PENG Z L, CHEN B B, ZHENG Q S, et al.Ameliorative effects of peptides from the oyster (Crassostrea hongkongensis) protein hydrolysates against UVB-induced skin photodamage in mice[J].Marine Drugs, 2020, 18(6):288.
[6] WANG S Y, YANG M F, YIN S G, et al.A new peptide originated from amphibian skin alleviates the ultraviolet B-induced skin photodamage[J].Biomedicine &Pharmacotherapy, 2022, 150:112987.
[7] LIN T Y, WU P Y, HOU C W, et al.Protective effects of sesamin against UVB-induced skin inflammation and photodamage in vitro and in vivo[J].Biomolecules, 2019, 9(9):479.
[8] CUI B N, WANG Y, JIN J H, et al.Resveratrol treats UVB-induced photoaging by anti-MMP expression, through anti-inflammatory, antioxidant, and antiapoptotic properties, and treats photoaging by upregulating VEGF-B expression[J].Oxidative Medicine and Cellular Longevity, 2022, 2022(1):6037303.
[9] MASUTIN V, KERSCH C, SCHMITZ-SPANKE S.A systematic review:Metabolomics-based identification of altered metabolites and pathways in the skin caused by internal and external factors[J].Experimental Dermatology, 2022, 31(5):700-714.
[10] ELPA D P, CHIU H Y, WU S P, et al.Skin metabolomics[J].Trends in Endocrinology &Metabolism, 2021, 32(2):66-75.
[11] CHEN C, HOU G X, ZENG C W, et al.Metabolomic profiling reveals amino acid and carnitine alterations as metabolic signatures in psoriasis[J].Theranostics, 2021, 11(2):754-767.
[12] ZHOU M, WANG H, YANG M, et al.Lipidomic analysis of facial skin surface lipids reveals an altered lipid profile in infant acne[J].The British Journal of Dermatology, 2020, 182(3):817-818.
[13] PATRA V, BORDAG N, CLEMENT Y, et al.Ultraviolet exposure regulates skin metabolome based on the microbiome[J].Scientific Reports, 2023, 13:7207.
[14] ROUX P F, ODDOS T, STAMATAS G.Deciphering the role of skin surface microbiome in skin health:An integrative multiomics approach reveals three distinct metabolite-microbe clusters[J].Journal of Investigative Dermatology, 2022, 142(2):469-479.e5.
[15] 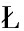 UCZAJ W, DO ROS
UCZAJ W, DO ROS RIO DOMINGUES M, DOMINGUES P, et al.Changes in lipid profile of keratinocytes from rat skin exposed to chronic UVA or UVB radiation and topical application of cannabidiol[J].Antioxidants, 2020, 9(12):1178.
RIO DOMINGUES M, DOMINGUES P, et al.Changes in lipid profile of keratinocytes from rat skin exposed to chronic UVA or UVB radiation and topical application of cannabidiol[J].Antioxidants, 2020, 9(12):1178.
[16] MANOSALVA C, BAHAMONDE C, SOTO F, et al.Linoleic acid induces metabolic reprogramming and inhibits oxidative and inflammatory effects in keratinocytes exposed to UVB radiation[J].International Journal of Molecular Sciences, 2024, 25(19):10385.
[17] YANG X Y, WANG J T, WANG H C, et al.Metabolomics study of fibroblasts damaged by UVB and BaP[J].Scientific Reports, 2021, 11:11176.
[18] GENG R X, KANG S G, HUANG K L, et al.Boosting the photoaged skin:The potential role of dietary components[J].Nutrients, 2021, 13(5):1691.
[19] 刘慧, 杨思佳, 任晗堃, 等.天然植物多糖的提取、分离及其在皮肤领域的研究进展[J].日用化学工业(中英文), 2024, 54(6):708-717.
LIU H, YANG S J, REN H K, et al.Extraction and separation of natural plant polysaccharides and its research progress in the field of skin[J].China Surfactant Detergent &Cosmetics, 2024, 54(6):708-717.
[20] YE Y H, JI D S, YOU L J, et al.Structural properties and protective effect of Sargassum fusiforme polysaccharides against ultraviolet B radiation in hairless Kun Ming mice[J].Journal of Functional Foods, 2018, 43:8-16.
[21] ASHIGAI H, KOMANO Y, WANG G Y, et al.Orally administered polysaccharide derived from blackcurrants (Ribes nigrum L.) improves skin hydration in ultraviolet-irradiated hairless mice[J].Journal of Nutritional Science and Vitaminology, 2018, 64(4):301-304.
[22] 田文慧, 杨永晶, 吴云, 等.树莓果肉多糖在1型糖尿病大鼠中的免疫调节和抗氧化活性研究[J].食品与发酵工业, 2020, 46(12):102-108.
TIAN W H, YANG Y J, WU Y, et al.Immune regulation and antioxidant activity of raspberry pulp polysaccharide through type 1 diabetic rats[J].Food and Fermentation Industries, 2020, 46(12):102-108.
[23] 李戈, 张烁.树莓果肉多糖提取工艺优化及其抗疲劳作用[J].食品研究与开发, 2023, 44(11):112-120.
LI G, ZHANG S.Extraction process optimization of raspberry (Rubus idaeus L.)pulp polysaccharide and anti-fatigue activity of the polysaccharide[J].Food Research and Development, 2023, 44(11):112-120.
[24] XIONG X M, LIU Z, CHE X C, et al.Chemical composition, pharmacological activity and development strategies of Rubus chingii:A review[J].Chinese Herbal Medicines, 2024, 16(3):313-326.
[25] 尹星星, 王学红, 田文慧, 等.树莓粗多糖对UVB诱导HaCaT细胞光损伤的防护作用[J].中国生物化学与分子生物学报, 2022, 38(10):1359-1369.
YIN X X, WANG X H, TIAN W H, et al.Protective effects of raspberry crude polysaccharides on UVB-induced photodamage in HaCaT cells[J].Chinese Journal of Biochemistry and Molecular Biology, 2022, 38(10):1359-1369.
[26] 赵红艳, 张鸭关, 陈德瑞.臭参粗多糖热水浸提工艺及抗氧化性研究[J].化学工程师, 2024, 38(10):90-94.
ZHAO H Y, ZHANG Y G, CHEN D R.Study on the extraction process and antioxidant properties of Codonopsis Pilosula polysaccharide[J].Chemical Engineer, 2024, 38(10):90-94.
[27] 王熙彤, 杨嘉祥, 王爱家, 等.微量苯酚-硫酸法快速测定西瓜翠衣多糖含量[J].食品安全质量检测学报, 2024, 15(22):204-210.
WANG X T, YANG J X, WANG A J, et al.Rapid determination of the polysaccharide content from Citrullus lanatus peel by micro-phenol-sulfuric acid method[J].Journal of Food Safety &Quality, 2024, 15(22):204-210.
[28] MEI M X, CAI R H, YU Q H, et al.Salidroside alleviates UVB-induced skin damage by inhibiting keratinocytes pyroptosis via the AQP3/ROS/GSDMD-N signaling pathway[J].Journal of Functional Foods, 2023, 107:105647.
[29] RIM P, KWANG K, KYOUNG L, et al.The protective effects of unripe apple (Malus pumila) extract on ultraviolet B-induced skin photoaging mouse model[J].Applied Sciences, 2023, 13(8):4788.
[30] GUO Y, KONG Y, SUN J, et al.Alleviation of ultraviolet-B radiation-induced photoaging using Saussurea medusa Maxim polysaccharide[J].Photochemistry and Photobiology, 2024, 100(3):622-632.
[31] ZHANG L X, GU W J, LIU T, et al.NDRG2 deficiency exacerbates UVB-induced skin inflammation and oxidative stress damage[J].Inflammation, 2025, 48(3):1313-1325.
[32] LONG Y L, WANG W J, ZHANG Y Y, et al.Photoprotective effects of Dendrobium nobile Lindl.polysaccharides against UVB-induced oxidative stress and apoptosis in HaCaT cells[J].International Journal of Molecular Sciences, 2023, 24(7):6120.
[33] CHEN Y Y, LIU X, LEI X J, et al.Premna microphylla Turcz pectin protected UVB-induced skin aging in BALB/c-nu mice via Nrf2 pathway[J].International Journal of Biological Macromolecules, 2022, 215:12-22.
[34] AGRAHARI G, SAH S K, BANG C H, et al.Superoxide dismutase 3 controls the activation and differentiation of CD4+T cells[J].Frontiers in Immunology, 2021, 12:628117.
[35] NGUYEN N H, TRAN G B, NGUYEN C T.Anti-oxidative effects of superoxide dismutase 3 on inflammatory diseases[J].Journal of Molecular Medicine, 2020, 98(1):59-69.
[36] NGUYEN C T, SAH S K, ZOUBOULIS C C, et al.Inhibitory effects of superoxide dismutase 3 on Propionibacterium acnes-induced skin inflammation[J].Scientific Reports, 2018, 8:4024.
[37] PRASEDYA E S, MARTYASARI N W R, ABIDIN A S, et al.Macroalgae Sargassum cristaefolium extract inhibits proinflammatory cytokine expression in BALB/c mice[J].Scientifica, 2020, 2020(1):9769454.
[38] SOL L, JOO K.The role of matrix metalloproteinase in inflammation with a focus on infectious diseases[J].International Journal of Molecular Sciences, 2022, 23(18):10546.
[39] FENG C, CHEN X L, YIN X Q, et al.Matrix metalloproteinases on skin photoaging[J].Journal of Cosmetic Dermatology, 2024, 23(12):3847-3862.
[40] LONG Y L, WANG W J, ZHANG Y Y, et al.Dendrobium nobile lindl polysaccharides attenuate UVB-induced photodamage by regulating oxidative stress, inflammation and MMPs expression in mice model[J].Photochemistry and Photobiology, 2023, 99(5):1269-1281.
[41] LUO H Q, YING N, ZHAO Q H, et al.A novel polysaccharide from Rubus chingii Hu unripe fruits:Extraction optimization, structural characterization and amelioration of colonic inflammation and oxidative stress[J].Food Chemistry, 2023, 421:136152.
[42] DENG Y J, HUANG L X, ZHANG C H, et al.Skin-care functions of peptides prepared from Chinese quince seed protein:Sequences analysis, tyrosinase inhibition and molecular docking study[J].Industrial Crops and Products, 2020, 148:112331.
[43] BOO Y C.Up- or downregulation of melanin synthesis using amino acids, peptides, and their analogs[J].Biomedicines, 2020, 8(9):322.
[44] WANG Z T, ZHAO F, XU C C, et al.Metabolic reprogramming in skin wound healing[J].Burns &Trauma, 2024, 12:tkad047.
[45] JANCIAUSKIENE S.The beneficial effects of antioxidants in health and diseases[J].Chronic Obstructive Pulmonary Diseases, 2020, 7(3):182-202.