α-L-鼠李糖苷酶(α-L-rhamnosidase,EC 3.2.1.40)通过水解鼠李糖分子中的糖苷键[1],产生游离的鼠李糖和相应的糖苷元[2]。该酶属于糖苷水解酶家族,已发现其存在于GH13、GH78和GH106[3-4]等多个家族,GH78是目前研究最多的家族[5]。α-L-鼠李糖苷酶来源于真菌[6]、细菌[7]及植物[8]等。在植物次生代谢物的合成和降解中[9],该酶通过水解黄酮类和甾醇类化合物中的鼠李糖[10],影响它们的生物活性[11]和稳定性。
由于其催化多种糖苷水解[12]的独特能力,α-L-鼠李糖苷酶已成为食品和医药等领域研究的热点[13],具有重要的应用前景。在食品工业中,α-L-鼠李糖苷酶通过水解风味前体中的糖苷键释放芳香化合物[14],增强水果加工品和酒类发酵产品的风味特征[15];也可去除某些糖苷类物质带来的苦味[16],改善饮料等食品的口感[17]。在医药行业,α-L-鼠李糖苷酶通过水解糖苷类化合物(如淫羊藿苷[18])释放具有生物活性的成分,发挥抗氧化[19]、抗炎[20]、抗癌[21]等药理作用。在临床应用中,利用α-L-鼠李糖苷酶水解作用,可实现药物的缓释和定向释放[22-23],优化药物治疗效果。
尽管多个物种来源的α-L-鼠李糖苷酶已被广泛研究且部分功能特性得到阐明[24],但在序列和结构特征方面的报道仍较少[25]。真菌是α-L-鼠李糖苷酶的重要来源,其中曲霉属[26]和青霉属[27]是主要的产酶菌。但现有研究大多集中于曲霉属来源的α-L-鼠李糖苷酶[28-29],针对青霉属来源α-L-鼠李糖苷酶的研究较少,这限制了对该酶家族结构多样性的全面理解。鉴于青霉属真菌在工业酶制剂和生物技术领域的重要性,深入探究青霉属来源α-L-鼠李糖苷酶的蛋白质结构显得尤为重要。本研究利用序列分析和结构预测等生物信息学方法,深入分析青霉属来源α-L-鼠李糖苷酶的蛋白结构和功能,可为理解其催化机制,实现其工业应用中的理性改造及性能优化提供理论支撑。
1 材料与方法
1.1 数据来源
在NCBI网站(https://www.ncbi.nlm.nih.gov)中以“(α-L-rhamnosidase)AND"Penicillium"”为搜索词检索来源于青霉的α-L-鼠李糖苷酶,以FASTA格式下载名称、来源和序列数据。
1.2 分析方法
通过ExPASy的ProtParam工具对α-L-鼠李糖苷酶进行理化性质分析;运用CELLO进行亚细胞定位预测;运用SignalP 6.0进行信号肽预测;运用MEGA11和iTOL工具构建进化树;运用MEME和Web CD-Search进行基序与结构域分析,通过TBtools-Ⅱ工具进行可视化;运用NetPhos进行磷酸化位点预测和分析;运用STRING进行蛋白质相互作用网络预测;运用SOPMA进行二级结构分析;运用SWISS-MODEL以同源建模法进行三级结构预测,通过PyMOL进行可视化。具体生物信息学分析工具见表1。
表1 生物信息学分析工具
Table 1 Bioinformatics analysis tools

工具名称网址功能ProtParamhttps://web.expasy.org/protparam/蛋白质的分子质量、理论等电点(isoelectric point,pI)、原子总数、不稳定指数、脂肪系数、总平均亲水性预测CELLOhttp://cello.life.nctu.edu.tw/蛋白质亚细胞定位预测SignalP 6.0https://services.healthtech.dtu.dk/services/SignalP-6.0/蛋白质信号肽预测MEGA11—蛋白质多序列比对与进化树构建iTOLhttps://itol.embl.de/进化树美化MEMEhttps://meme-suite.org/meme/蛋白质保守基序预测Web CD-Searchhttps://www.ncbi.nlm.nih.gov/Structure/cdd/cdd.shtml蛋白质保守结构域预测TBtools-Ⅱhttps://github.com/CJ-Chen/TBtools-II蛋白质保守基序与保守结构域的可视化NetPhos3.1https://services.healthtech.dtu.dk/services/NetPhos-3.1/蛋白质磷酸化位点预测STRINGhttp://string-db.org/蛋白质相互作用网络预测SOPMAhttps://npsa-prabi.ibcp.fr/cgi-bin/npsa_automat.pl page=/NPSA/npsa_sopma.html蛋白质二级结构预测SWISS-MODELhttps://swissmodel.expasy.org/蛋白质三级结构预测PyMOL—蛋白质三级结构可视化
2 结果与分析
2.1 序列数据分析与处理
在NCBI数据库中共检索到1 236条序列数据,其中未经过实验验证的数据有1 015条,经过实验验证的数据有221条。对221条经过实验验证的α-L-鼠李糖苷酶序列进行去重,得到136条未重复青霉来源的α-L-鼠李糖苷酶序列。根据来源对这些序列信息进行分类统计,分为44个种类,分别列于表2。
表2 α-L-鼠李糖苷酶来源
Table 2 Source of α-L-rhamnosidases
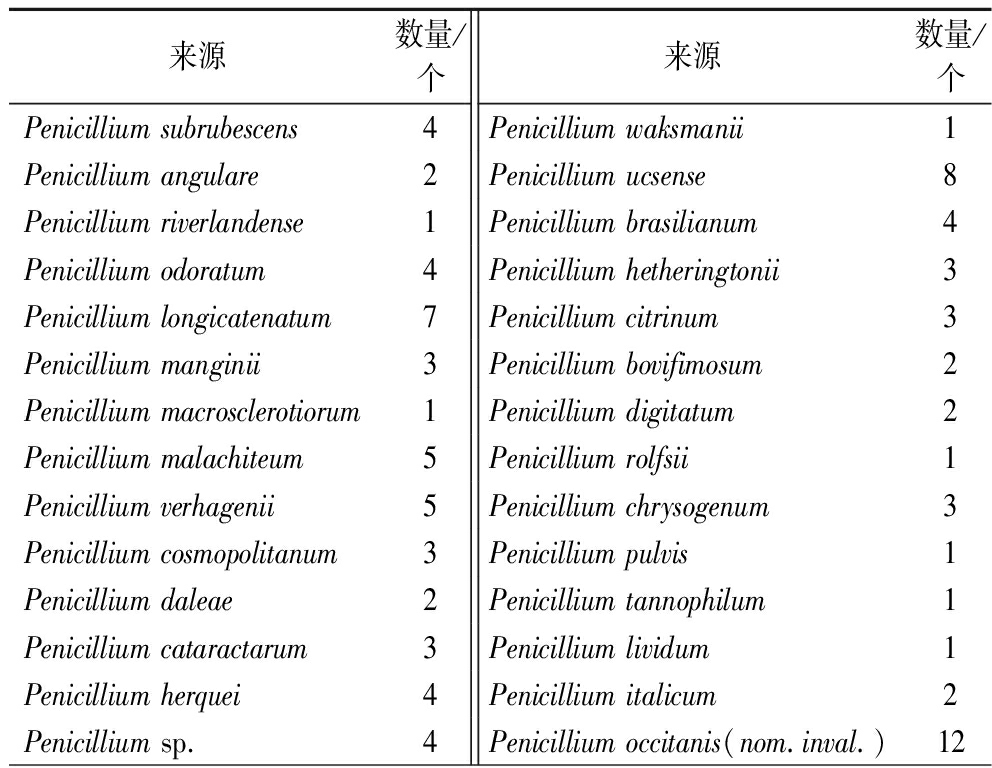
来源数量/个来源数量/个Penicillium subrubescens4Penicillium waksmanii1Penicillium angulare2Penicillium ucsense8Penicillium riverlandense1Penicillium brasilianum4Penicillium odoratum4Penicillium hetheringtonii3Penicillium longicatenatum7Penicillium citrinum3Penicillium manginii3Penicillium bovifimosum2Penicillium macrosclerotiorum1Penicillium digitatum2Penicillium malachiteum5Penicillium rolfsii1Penicillium verhagenii5Penicillium chrysogenum3Penicillium cosmopolitanum3Penicillium pulvis1Penicillium daleae2Penicillium tannophilum1Penicillium cataractarum3Penicillium lividum1Penicillium herquei4Penicillium italicum2Penicillium sp.4Penicillium occitanis(nom.inval.)12
续表2
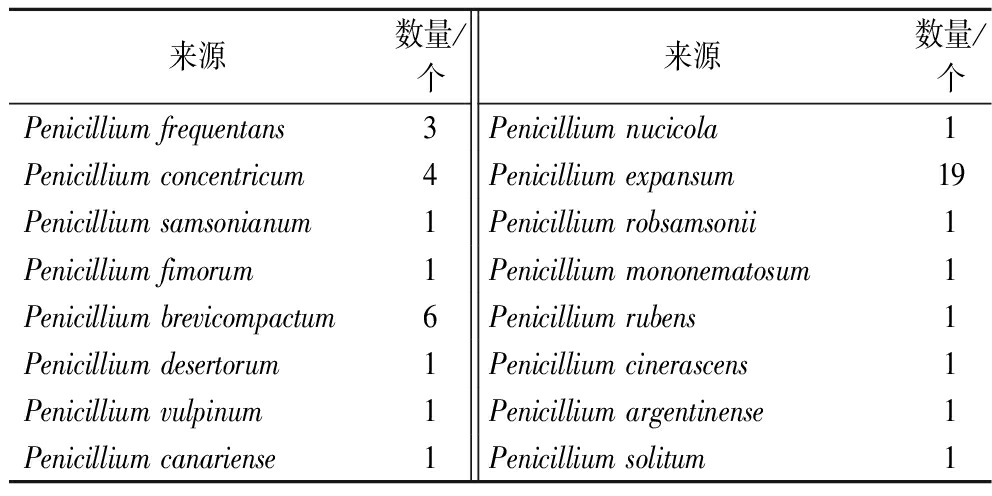
来源数量/个来源数量/个Penicillium frequentans3Penicillium nucicola1Penicillium concentricum4Penicillium expansum19Penicillium samsonianum1Penicillium robsamsonii1Penicillium fimorum1Penicillium mononematosum1Penicillium brevicompactum6Penicillium rubens1Penicillium desertorum1Penicillium cinerascens1Penicillium vulpinum1Penicillium argentinense1Penicillium canariense1Penicillium solitum1
2.2 理化性质分析
对136种α-L-鼠李糖苷酶进行理化性质分析,结果包括氨基酸数目、分子质量、pI、原子总数、不稳定指数、脂肪系数和总平均亲水性。其中,对氨基酸数目和分子质量进行统计,如图1所示。氨基酸数目分布在201~1 310(图1-a);分子质量分布在22.19~143.57 kDa(图1-b);136种α-L-鼠李糖苷酶的氨基酸和分子质量数目均呈现显著差异性。
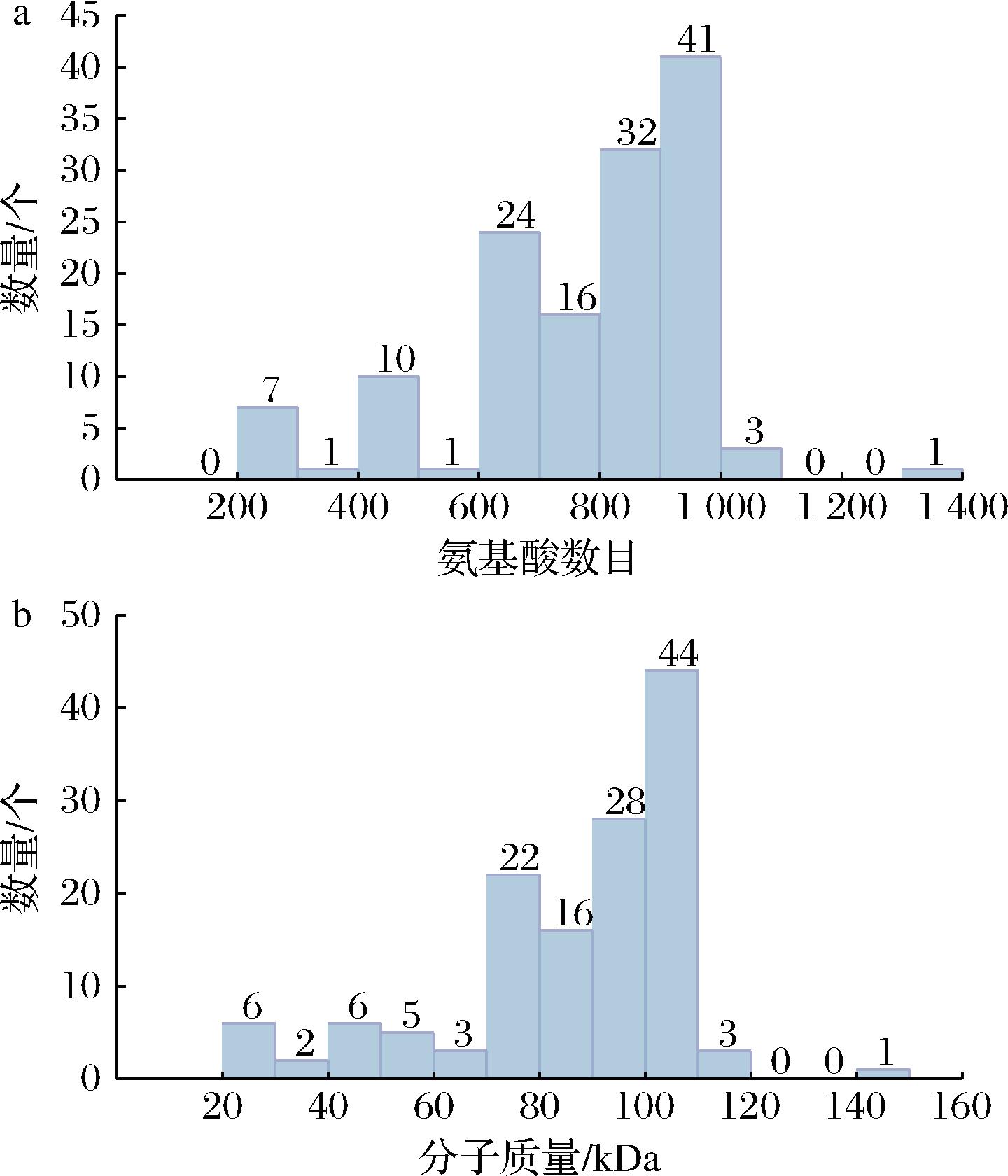
a-氨基酸数目分布图;b-分子质量分布图
图1 136种α-L-鼠李糖苷酶理化性质
Fig.1 Physicochemical properties of the 136 α-L-rhamnosidases
2.3 亚细胞定位分析
对136个α-L-鼠李糖苷酶的亚细胞定位预测结果进行统计分析,如图2所示。这些酶分布于7个不同区域,其中定位于质膜的酶数量最多,共53个,占比38.97%;其次是细胞外,42个,占比30.88%;细胞质中有35个,占比25.74%;分别有2个定位在叶绿体和溶酶体,占比各为1.47%;分别有1个定位在线粒体和细胞核,占比各为0.74%。这一分布特点表明α-L-鼠李糖苷酶大多为分泌型蛋白,主要参与细胞膜相关及胞外基质中的糖苷水解过程。
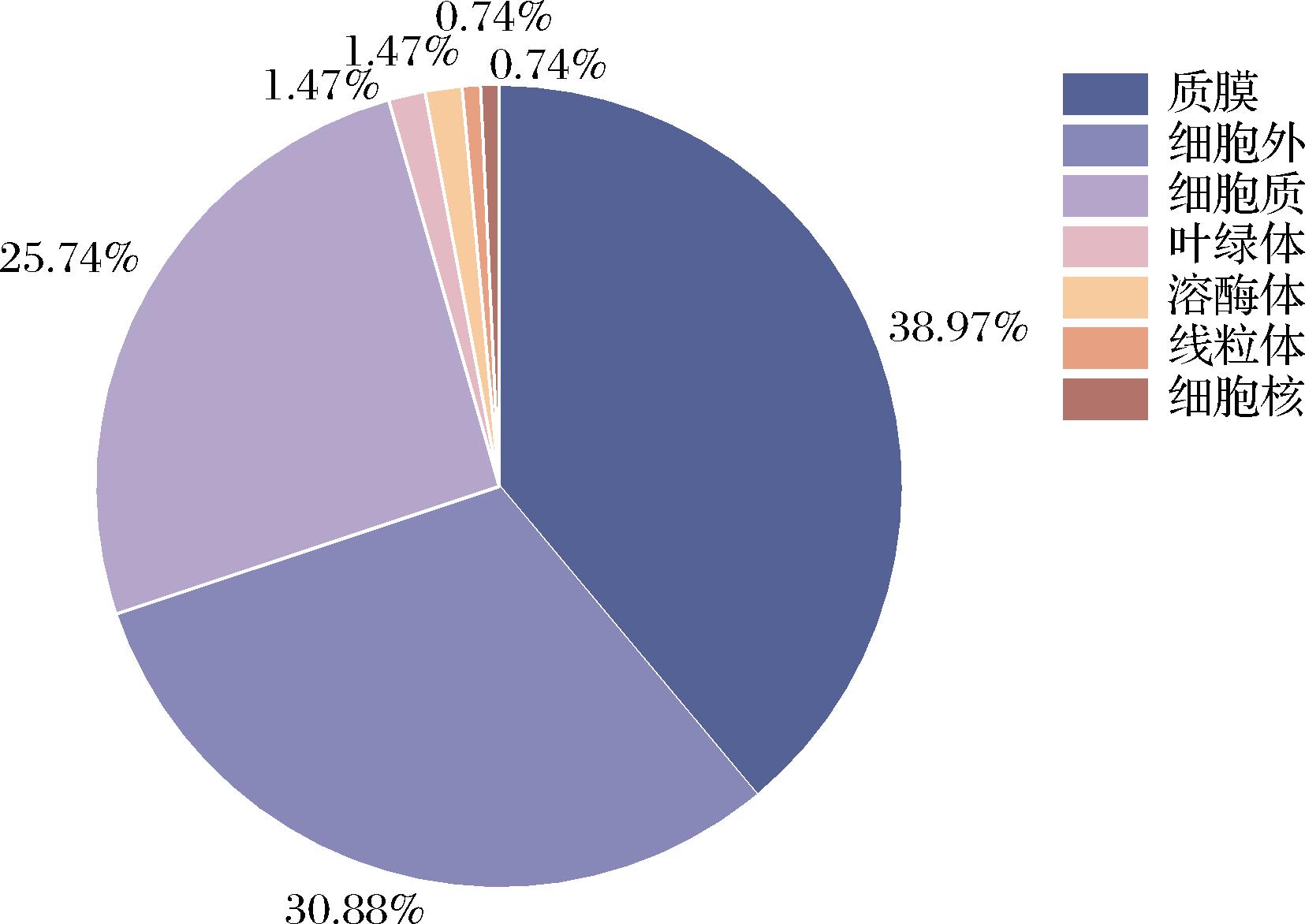
图2 136种α-L-鼠李糖苷酶亚细胞定位分布图
Fig.2 Subcellular localization distribution of the 136 α-L-rhamnosidases
2.4 信号肽预测
对136个α-L-鼠李糖苷酶进行信号肽预测分析。如表3所示,共有41个α-L-鼠李糖苷酶蛋白序列含有信号肽。这些序列的信号肽预测结果具有较高的可靠性,其存在可能性几乎都在90%以上。信号肽的切割位点位于第15~26个氨基酸之间,其中以第20个氨基酸附近为主要集中区域,表明该酶可能通过经典的分泌途径进行转运,且N端信号肽具有较高的序列保守性。
表3 α-L-鼠李糖苷酶信号肽分布
Table 3 Signal peptide distribution of α-L-rhamnosidases

序列ID可能性/%切割位点可能性/%XP_056998784.199.96ATA18-W19S97.57XP_056966435.199.98VVA18-D19K97.32XP_056966433.199.97CLA18-S19T97.41KAJ5652978.199.97VTA18-D19K97.72KAJ5652965.199.97CQG18-S19T97.53KAJ5727481.199.90VAA21-T22L78.03XP_057122805.199.85SEA22-A23A96.25KAF7736289.199.97VQQ20-D21N52.16KAF7714833.174.17AAA20-L21S38.03KAF7714263.199.98VLA20-T21E98.06XP_056485823.194.31SEA22-A23A88.98XP_057136664.199.98SIA22-D23T97.98XP_057088793.199.98SAA22-D23T96.85KAJ5514678.199.98SAA22-D23T97.01XP_057150027.199.98SSA22-D23T97.92XP_056815912.199.98SSA22-D23S97.79XP_056565682.199.98STA22-D23T97.99XP_056584918.199.98SVA21-E22T98.08KAJ6153173.199.98STA22-D23T97.99KAJ5842598.199.98STA22-D23T98.00KAJ5500354.199.98SVA22-D23T98.01KAJ5487727.199.98SNA22-D23T97.95KAJ5367698.199.98SSA22-D23S97.75KAJ5328223.199.98SSA22-D23S97.78XP_056805563.199.97AEA19-I20T88.88KAJ5354036.199.97AEA19-I20T92.22KAJ5322619.199.96AEA19-I20T91.58PCH01640.199.97AEA23-G24S90.76PCG89254.199.96SFG23-S24V83.27PCG89253.199.95VQS20-T21F97.38OKO89552.199.97VAG16-L17S97.14XP_056521215.199.98SVA22-E23G96.19KAF3391609.199.56LSA19-S20K55.30XP_016593924.199.98SVA22-D23T98.01XP_016600200.162.19CLA15-V16P59.95KZN92224.199.98VVA20-K21G97.94KGO76564.199.97SLA22-N23T97.99KGO73594.162.19CLA15-V16P59.95OOQ90343.199.97ATA21-K22G97.98OOQ89737.199.98EER25-N26P89.64OOQ89199.199.96GAA21-Q22S90.55
2.5 进化树分析
将136条α-L-鼠李糖苷酶序列在MEGA11中进行序列比对,采用邻位相连(neighbor-joining,NJ)方法构建进化树。如图3所示,根据进化关系,将所有序列划分为5个主要分支(Group Ⅰ~Group Ⅴ)。其中Group Ⅰ具有最大的遗传距离,表明该分支的蛋白可能经历了更长时间的独立进化,具有独特的结构和功能特性。Group Ⅱ和Group Ⅲ形成的大分支遗传距离最小,表明这些蛋白可能具有较近的共同祖先,且在进化过程中保持了较高的序列保守性。不同物种来源的序列以不同颜色的条带标记,结果显示α-L-鼠李糖苷酶具有广泛的物种来源,其中来源于扩展青霉(Penicillium expansum)(浅紫色条带标识)的序列数量最为丰富,广泛分布在Group Ⅱ、Group Ⅲ和Group Ⅴ中,并且同一节点中的蛋白具有相同的遗传距离,表明这些蛋白可能通过基因复制产生,在结构和功能上可能具有共同特性。分别以正方形、圆形、五角星表示理论pI、总平均亲水性(GRAVY值)、稳定性。当pI<7.00(指酸性蛋白)、GRAVY<0(指亲水蛋白)、II<40.00(指稳定蛋白)时,对应图形标记为空心,反之则为实心。结果显示除KAJ5703544.1、KAJ5569240.1、PCG88911.1、XP_056554983.1这4个蛋白的pI>7.00(表现为碱性蛋白)外,其余蛋白均表现为酸性(pI<7.00);除PCG89253.1之外,所有蛋白的GRAVY值均小于0(表现为亲水蛋白),与蔡雨晨等[30]总结出的曲霉来源α-L-鼠李糖苷酶的性质一致;77种蛋白的II<40.00(表现为稳定蛋白),59种蛋白的II>40.00(表现为不稳定蛋白)。结合信号肽预测结果,Group Ⅰ中的蛋白全部含有信号肽,其他含有信号肽的蛋白主要集中在Group Ⅲ,表明分泌能力可能是该蛋白家族进化分支形成的关键因素[31]。

图3 136种α-L-鼠李糖苷酶进化树
Fig.3 Phylogenetic tree of the 136 α-L-rhamnosidases
注:珊瑚粉色、橙色、绿色、蓝色、紫色依次为Group Ⅰ, Group Ⅱ, Group Ⅲ, Group Ⅳ和Group Ⅴ。
2.6 保守基序与结构域分析
选取来源于P.expansum的19条α-L-鼠李糖苷酶序列进行保守基序与结构域分析。如图4所示,19种α-L-鼠李糖苷酶蛋白总共含有10个保守基序,分别命名为Motif 1~Motif 10。其中,7个蛋白序列(KAJ5510232.1、XP_016597498.1、KGO48591.1、XP_016594907.1、KGO62521.1、XP_016597568.1、KGO64900.1)包含全部10个基序,并且这些基序在序列中的相对位置高度保守,表明它们具有复杂且多样的功能,且很可能来源于同一超家族,具有相似的三维结构。KAJ5500354.1和XP_016593924.1两个蛋白序列包含的基序数量最少,仅包含Motif 4和Motif 8两个基序。Motif 4和Motif 8在19个蛋白序列中均有出现,表明Motif 4和Motif 8是该酶的高度保守基序。Motif 4和Motif 8基序富集疏水性带电荷残基,部分侧链基团能与底物产生相互作用[32]。基序中的“GKSFYD”和“KYIT”等区域与某些激酶或ATP结合蛋白的保守序列具有相似性,推测这些区域可能参与辅因子结合。基序中还含有多个芳香族氨基酸,它们在催化中主要发挥亲核攻击作用[31]。因此Motif 4和Motif 8可能构成α-L-鼠李糖苷酶的活性中心或底物结合域的关键区域。结构域分析显示,19种α-L-鼠李糖苷酶蛋白共包含12种结构域。其中Bac_rhamnosid6H和Bac_rhamnosid6H superfamily结构域的出现频率最高。Bac_rhamnosid6H结构域是一种典型的糖苷水解酶超家族成员。其中,N端结构域通过保守的芳香族氨基酸特异性识别L-鼠李糖;核心催化域具有极高的序列保守性,含有典型的酸性氨基酸残基,负责水解α-1,6/α-1,2糖苷键;C端结构域则可能通过构象变化调节酶的稳定性。朱小冲等[33]的研究表明,多数鼠李糖苷酶的催化作用由酸性氨基酸残基实现。因此,Bac_rhamnosid6H结构域是介导α-L-鼠李糖苷酶底物结合与催化活性的关键功能单元。
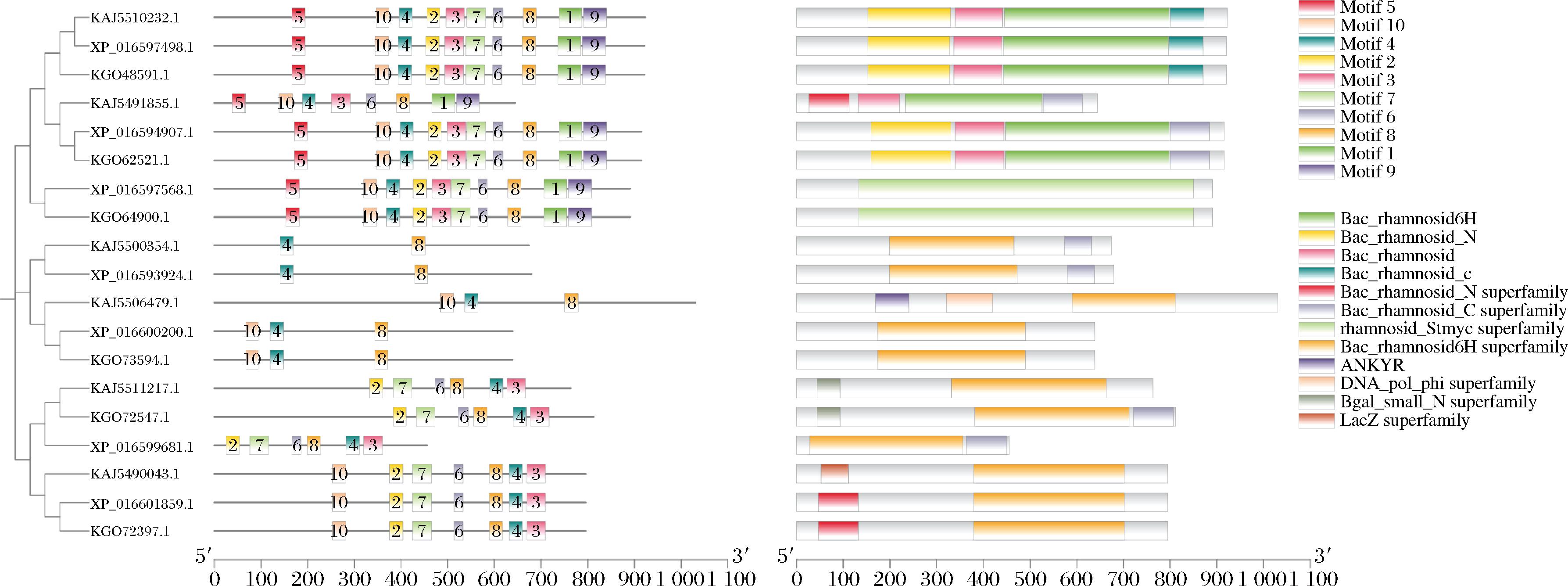
图4 19种α-L-鼠李糖苷酶基序与结构域
Fig.4 Motifs and domains of the 19 α-L-rhamnosidases
2.7 磷酸化位点预测
对来源于P.expansum的19种α-L-鼠李糖苷酶进行磷酸化位点预测。如图5所示,这些酶的磷酸化位点数量存在差异性。其中KAJ5491855.1蛋白的磷酸化位点总数目最少,为76个;KAJ5506479.1蛋白的磷酸化位点总数目最多,为172个。在具体的磷酸化位点分布中,丝氨酸的占比最高,为58.20%;苏氨酸的占比为32.25%;酪氨酸的占比仅为9.55%。这一分布特点表明该酶的磷酸化位点以丝氨酸为主。
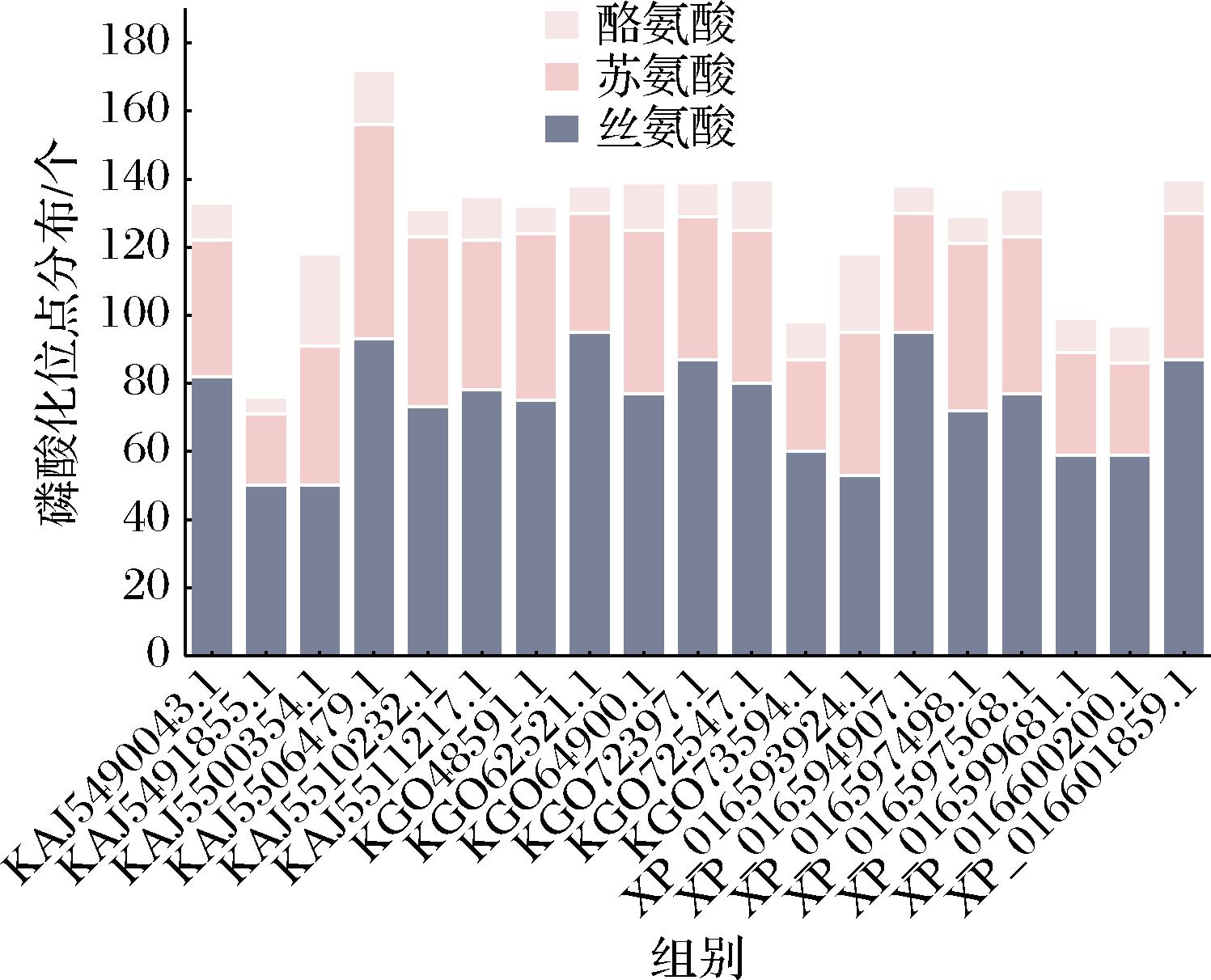
图5 19种α-L-鼠李糖苷酶磷酸化位点分布图
Fig.5 Phosphorylation site distribution of the 19 α-L-rhamnosidases
2.8 蛋白质相互作用网络预测
对来源于P.expansum的19种α-L-鼠李糖苷酶进行蛋白质相互作用网络预测(图6)。其中,XP_016599681.1蛋白(图中标记为PEX2_066970)的相互作用得分平均值最高,表明该蛋白的相互作用可信度最高。与XP_016599681.1(PEX2_066970)蛋白存在相互作用的蛋白质有PEX2_015530、PEX2_061850、PEX2_044270、PEX2_002620、PEX2_099310、PEX2_015670、PEX2_066980、PEX2_063870、PEX2_032050、PEX2_044090等;其中肾上腺皮质铁氧还蛋白(PEX2_044270)与该蛋白的相互作用强度最为显著。肾上腺皮质铁氧还蛋白是一种关键的铁硫蛋白,核心功能是作为电子传递载体参与类固醇激素的合成过程。基于这一相互作用网络,推测α-L-鼠李糖苷酶XP_016599681.1可能与肾上腺皮质铁氧还蛋白在类固醇激素合成中具有潜在的协同作用。
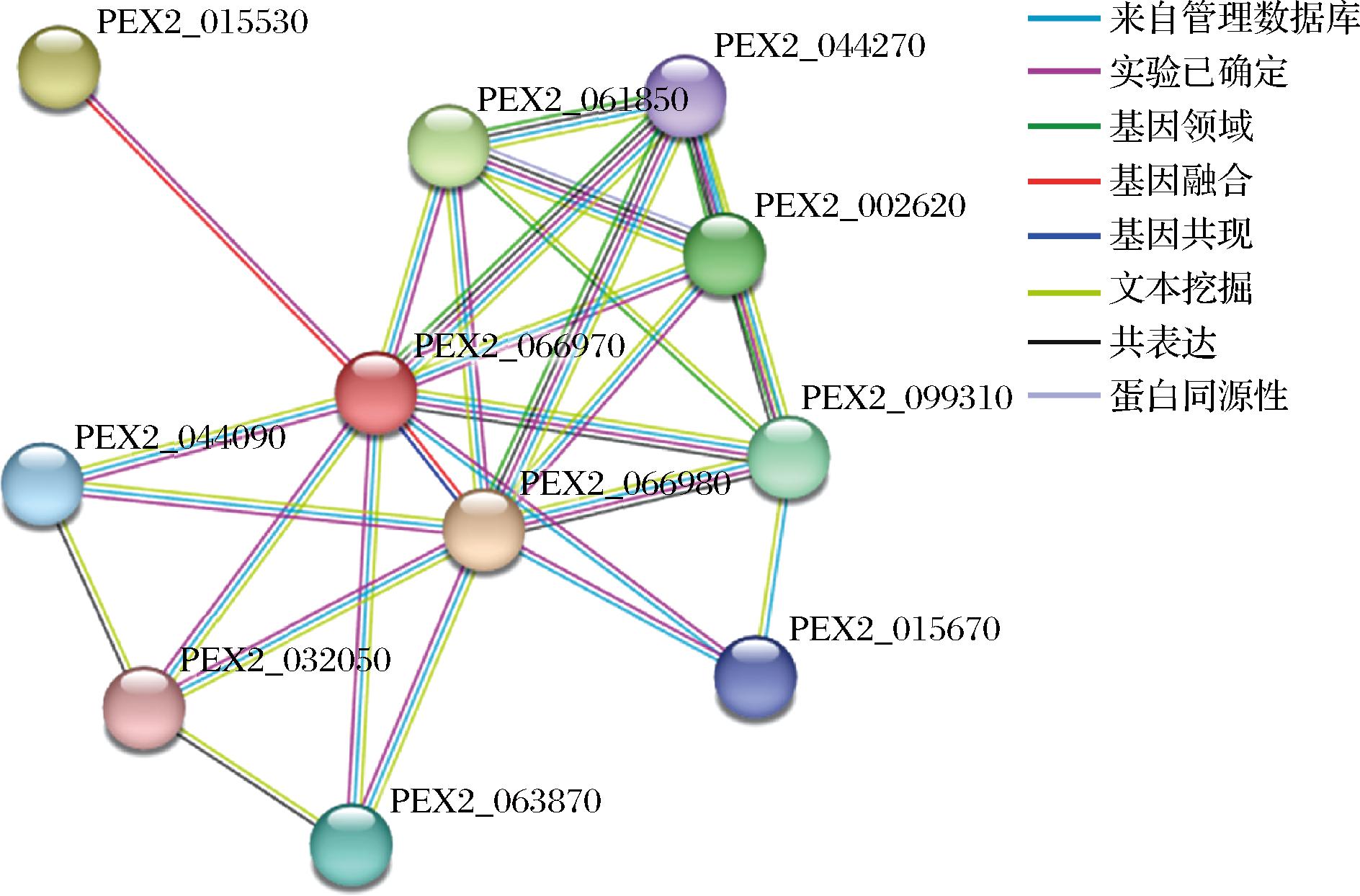
图6 α-L-鼠李糖苷酶XP_016599681.1蛋白质相互作用网络
Fig.6 Protein interaction network of α-L-rhamnosidase (XP_016599681.1)
2.9 二级结构预测
对来源于P.expansum的19种α-L-鼠李糖苷酶进行二级结构预测。如图7所示,这些酶都含有α-螺旋、延伸链、β-转角和无规则卷曲。α-螺旋的比例范围为22.54%~42.32%,平均占比为27.74%;延伸链的比例范围为13.16%~24.10%,平均占比为20.05%;β-转角的比例范围为3.29%~7.60%,平均占比为5.53%;无规则卷曲的比例范围为39.09%~49.85%,平均占比为46.69%。其中无规则卷曲占比最大,表明α-L-鼠李糖苷酶结构具有较高的柔韧性,这有助于其适应不同底物的结合需求而提高催化效率。19种α-L-鼠李糖苷酶蛋白中4种二级结构的占比规律与陈东启等[34]总结的黑曲霉来源的α-L-鼠李糖苷酶的二级结构规律一致。
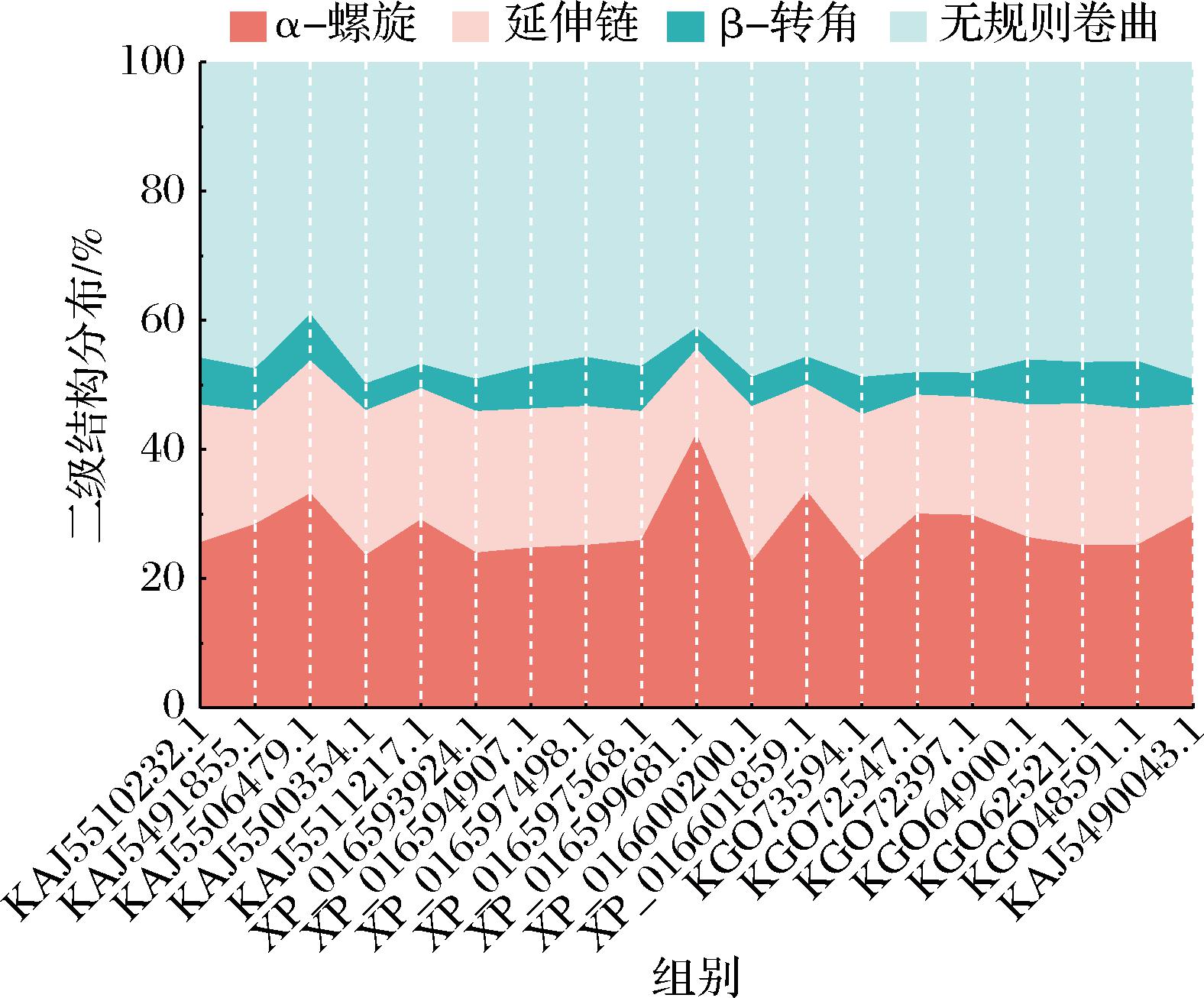
图7 19种α-L-鼠李糖苷酶二级结构分布图
Fig.7 Secondary structure distribution of the 19 α-L-rhamnosidases
2.10 三级结构预测
以同源建模法对来源于P.expansum的19种α-L-鼠李糖苷酶蛋白的三级结构进行预测。在建模过程中,XP_016593924.1蛋白的氨基酸序列与所选模板蛋白的序列一致性最高,达到90.29%,这表明该模板具有良好的适用性,可用于构建α-L-鼠李糖苷酶的三级结构模型。预测所得的三级结构模型如图8所示,该蛋白模型主要包含1个C端结构域和1个6型发夹糖苷酶结构域。C端结构域主要由β-折叠构成,推测可能存在碳水化合物结合结构域(carbohydrate binding module,CBM)三维结构,通过与L-鼠李糖配体形成氢键和范德华力提高复合物的稳定性,从而提高催化效率[35]。6型发夹糖苷酶结构域以α-螺旋为核心,通过螺旋束与无规则卷曲的相互作用维持其整体构象稳定性。短β-折叠与相邻α-螺旋形成特征性发夹结构,推测该区域可能构成酶的活性中心,形成底物结合口袋并参与催化反应。
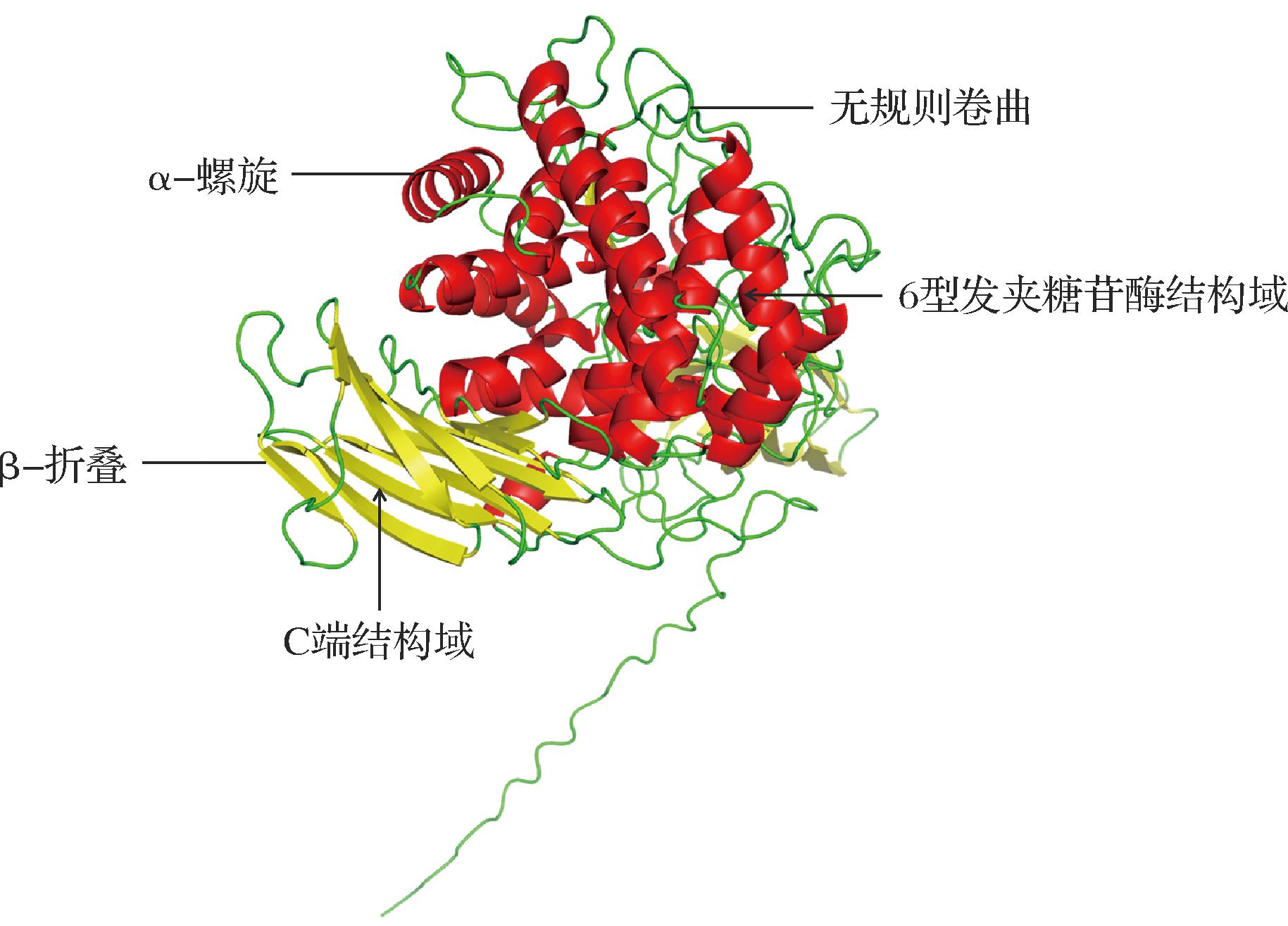
图8 α-L-鼠李糖苷酶XP_016593924.1蛋白三级结构
Fig.8 Tertiary structure of α-L-rhamnosidase (XP_016593924.1)
3 结论与讨论
本研究运用多种生物信息学工具,对从NCBI数据库中筛选出的136条青霉属来源的α-L-鼠李糖苷酶序列进行了系统性分析,揭示了该类酶的一系列关键特征。理化性质分析表明α-L-鼠李糖苷酶多为酸性、亲水且相对稳定的蛋白,氨基酸数目在201~1 310之间,分子质量在22.19~143.57 kDa范围,均呈现显著差异性。亚细胞定位预测显示这些酶主要分布在质膜和细胞外,功能上可能主要参与细胞膜相关的糖苷类物质的水解。信号肽分析显示共有41个α-L-鼠李糖苷酶蛋白序列含有信号肽,切割位点主要位于第15~26个氨基酸之间(集中于第20位附近),表明该酶通过经典的分泌途径完成转运。根据进化关系,α-L-鼠李糖苷酶序列划分为5个进化分支,其中Group Ⅰ有最大的遗传距离,推测Group Ⅰ中的蛋白具有独特的结构和功能适应性,与其他分支蛋白分化显著。来源于P.expansum的序列数量最为丰富,并且分布在不同的分支中,且同一节点中的蛋白具有相同的遗传距离,表明这些蛋白可能通过基因复制产生,在结构和功能上可能具有共同特性。
对P.expansum的19个α-L-鼠李糖苷酶进行保守性分析,鉴定出10个保守基序,其中Motif 4和Motif 8高度保守,Motif 4和Motif 8可能构成α-L-鼠李糖苷酶的活性中心或底物结合域的关键区域。结构域分析表明,Bac_rhamnosid6H和Bac_rhamnosid6H superfamily结构域出现的频率最高,Bac_rhamnosid6H结构域是介导α-L-鼠李糖苷酶底物结合与催化活性的关键功能单元。该酶的磷酸化位点主要以丝氨酸为主,其次是苏氨酸,酪氨酸位点最少。蛋白质相互作用网络预测显示,XP_016599681.1蛋白的相互作用可信度最高,其中与肾上腺皮质铁氧还蛋白的互作最为密切,表明该酶可能在铁代谢及类固醇激素合成中发挥作用。二级结构预测表明这些酶都含有α-螺旋、延伸链、β-转角和无规则卷曲,其中无规则卷曲占比最大(39.09%~49.85%),表明其结构具有较高的柔性,有利于适应多种底物的结合和催化。基于与模板高度一致(90.29%)的XP_016593924.1序列构建的三级结构模型主要包含1个C端结构域和1个6型发夹糖苷酶结构域。C端结构域主要由β-折叠构成,可能存在CBM三维结构,通过与L-鼠李糖配体形成氢键和范德华力提高复合物的稳定性,从而提高催化效率。6型发夹糖苷酶结构域区域可能构成酶的活性中心,形成底物结合口袋并参与催化反应。
综上所述,本研究深入解析了青霉属来源α-L-鼠李糖苷酶的序列、结构及潜在功能特征,为后续的功能验证、理性设计及工业应用奠定了重要的理论基础并提供了关键数据支持。
[1] WANG D Q, ZHENG P, CHEN P C, et al.Immobilization of alpha-L-rhamnosidase on a magnetic metal-organic framework to effectively improve its reusability in the hydrolysis of rutin[J].Bioresource Technology, 2021, 323:124611.
[2] LYU Y B, ZENG W Z, DU G C, et al.Efficient bioconversion of epimedin C to icariin by a glycosidase from Aspergillus nidulans[J].Bioresource Technology, 2019, 289:121612.
[3] ZHANG F, YOU S, HUANG T, et al.Dual promoter strategy enhances co-expression of α-L-rhamnosidase and enhanced fluorescent protein for whole-cell catalysis and bioresource valorization[J].Science of the Total Environment, 2020, 722:137865.
[4] LI B C, LI X, PENG B, et al.Improving rutin biotransformation efficiency of α-L-rhamnosidase from Bacteroides thetaiotaomicron VPI-5482 via targeted mutagenesis focused on general acid motif[J].Catalysts, 2024, 14(8):501.
[5] GE L, LIU Y Y, ZHOU F M, et al.Heterologous expression and characterization of a thermostable α-L-rhamnosidase from Thermoclostridium stercorarium subsp.thermolacticum DSM 2910 and its application in the biotransformation of rutin[J].Journal of Microbiology and Biotechnology, 2023, 33(11):1521-1530.
[6] YE H Y, LI X J, LI L Y, et al.Homologous expression and characterization of α-L-rhamnosidase from Aspergillus niger for the transformation of flavonoids[J].Applied Biochemistry and Biotechnology, 2022, 194(8):3453-3467.
[7] LU C N, DONG Y R, KE K X, et al.Modification to increase the thermostability and catalytic efficiency of α-L-rhamnosidase from Bacteroides thetaiotaomicron and high-level expression[J].Enzyme and Microbial Technology, 2022, 158:110040.
[8] XIE X, GUO Z W, CHEN B H, et al.Surface display and characterization of recombinant α-L-rhamnosidase from Emiliania huxleyi on Pichia pastoris[J].Bioorganic Chemistry, 2025, 155:108121.
[9] XIE J C, ZHAO J, ZHANG N, et al.Efficient production of isoquercitin, icariin and icariside II by a novel thermostable α-L-rhamnosidase PodoRha from Paenibacillus odorifer with high α-1, 6-/α-1, 2- glycoside specificity[J].Enzyme and Microbial Technology, 2022, 158:110039.
[10] LOU H H, LIU X Y, LIU S Y, et al.Purification and characterization of a novel α-L-rhamnosidase from Papiliotrema laurentii ZJU-L07 and its application in production of icariin from epimedin C[J].Journal of Fungi, 2022, 8(6):644.
[11] ZHANG S S, LU C N, CAO S P, et al.Efficient production of icariin and baohuoside I from Epimedium folium flavonoids by fungal α-L-rhamnosidase hydrolysing regioselectively the terminal rhamnose of epimedin C[J].Biotechnology for Biofuels and Bioproducts, 2023, 16(1):107.
[12] BAN Y L, YANG H W, JIANG J X, et al.A α-L-rhamnosidase from Echinacea purpurea endophyte Simplicillium sinense EFF1 and its application in production of Calceorioside B[J].International Journal of Biological Macromolecules, 2024, 270:132090.
[13] LUO C M, KE L F, HUANG X Y, et al.Efficient biosynthesis of prunin in methanol cosolvent system by an organic solvent-tolerant α-L-rhamnosidase from Spirochaeta thermophila[J].Enzyme and Microbial Technology, 2024, 175:110410.
[14] KUMAR D, YADAV S, YADAVA S, et al.An alkali tolerant α-L-rhamnosidase from Fusarium moniliforme MTCC-2088 used in de-rhamnosylation of natural glycosides[J].Bioorganic Chemistry, 2019, 84:24-31.
[15] FERREIRA-LAZARTE A, PLAZA-VINUESA L, DE LAS RIVAS B, et al.Production of α-rhamnosidases from Lactobacillus plantarum WCFS1 and their role in deglycosylation of dietary flavonoids naringin and rutin[J].International Journal of Biological Macromolecules, 2021, 193:1093-1102.
[16] BORZOVA N, GUDZENKO O, VARBANETS L.α-L-rhamnosidase from Penicillium tardum and its application for biotransformation of citrus rhamnosides [J].Applied Biochemistry and Biotechnology, 2022, 194(10):4915-4929.
[17] PENG C, LI R, NI H, et al.The effects of α-L-rhamnosidase, β-D-glucosidase, and their combination on the quality of orange juice[J].Journal of Food Processing and Preservation, 2021, 45(7):e15604.
[18] LI Q, GE L, ZHENG D Y, et al.Screening and characterization of a GH78 α-L-rhamnosidase from Aspergillus terreus and its application in the bioconversion of icariin to icaritin with recombinant β-glucosidase[J].Enzyme and Microbial Technology, 2022, 153:109940.
[19] WANG F Y, JIA J, SONG H H, et al.Icariin protects vascular endothelial cells from oxidative stress through inhibiting endoplasmic reticulum stress[J].Journal of Integrative Medicine, 2019, 17(3):205-212.
[20] EL-SHITANY N A, EID B G.Icariin modulates carrageenan-induced acute inflammation through HO-1/Nrf2 and NF-kB signaling pathways[J].Biomedicine &Pharmacotherapy, 2019, 120:109567.
[21] WU X L, KONG W C, QI X Y, et al.Icariin induces apoptosis of human lung adenocarcinoma cells by activating the mitochondrial apoptotic pathway[J].Life Sciences, 2019, 239:116879.
[22] SU J W, WU T, CAO S P, et al.Screening and characterization of a β-xylosidase from Bifidobacterium breve K-110 and its application in the biotransformation of the total flavonoids of Epimedium to icariin with α-L-rhamnosidase[J].Bioorganic Chemistry, 2023, 132:106364.
[23] CHENG L Y, ZHANG H, CUI H Y, et al.Efficient enzyme-catalyzed production of diosgenin:Inspired by the biotransformation mechanisms of steroid saponins in Talaromyces stollii CLY-6[J].Green Chemistry, 2021, 23(16):5896-5910.
[24] XIE J C, ZHANG S S, TONG X Y, et al.Biochemical characterization of a novel hyperthermophilic α-L -rhamnosidase from Thermotoga petrophila and its application in production of icaritin from epimedin C with a thermostable β-glucosidase[J].Process Biochemistry, 2020, 93:115-124.
[25] YOU S, ZHU L L, ZHANG S M, et al.Recyclable and efficient isoquercitrin production with whole-cell catalysis of improved GH78 α-L-rhamnosidase by domain truncation strategy[J].Industrial Crops and Products, 2023, 191:115945.
[26] SUN J, LI W J, LIAO H, et al.Adding sorbitol improves the thermostability of α-L-rhamnosidase from Aspergillus niger and increases the conversion of hesperidin[J].Journal of Food Biochemistry, 2022, 46(2):e14055.
[27] YADAV S, YADAVA S, YADAV K D S.α-L-rhamnosidase selective for rutin to isoquercitrin transformation from Penicillium griseoroseum MTCC-9224[J].Bioorganic Chemistry, 2017, 70:222-228.
[28] WANG D Q, ZHENG P, CHEN P C, et al.Engineering an α-L-rhamnosidase from Aspergillus niger for efficient conversion of rutin substrate[J].Biochemical Engineering Journal, 2022, 186:108572.
[29] WANG D Q, ZHENG P, CHEN P C, et al.Highly efficient enzymatic conversion of rutin to isoquercitrin and l-rhamnose using deep eutectic solvents[J].ACS Sustainable Chemistry &Engineering, 2020, 8(39):14905-14913.
[30] 蔡雨晨, 李孟泽, 李利君, 等.曲霉来源的α-L-鼠李糖苷酶结构特征规律分析[J].现代食品科技, 2021, 37(1):38-46;100.CAI Y C, LI M Z, LI L J, et al.Analysis of structural characteristics of α-L-rhamnosidase from Aspergillus species[J].Modern Food Science and Technology, 2021, 37(1):38-46;100.
[31] 巩建业, 吴喆瑜, 李利君, 等.GH78家族真菌α-L-鼠李糖苷酶分子系统进化关系分析[J].现代食品科技, 2017, 33(10):13-20.GONG J Y, WU Z Y, LI L J, et al.Analysis of evolutionary relationship of GH78 fungal α-L-rhamnosidase[J].Modern Food Science and Technology, 2017, 33(10):13-20.
[32] 吉亚茹. 多形拟杆菌α-L-鼠李糖苷酶资源挖掘及其结构分析[D].大同:山西大学, 2018.JI Y R.Discovery of novel α-L-rhamnosidases from Bacteroides thetaiotaomicron VPI-5482 and structural analysis[D].Datong:Shanxi University, 2018.
[33] 朱小冲, 唐双焱.α-L-鼠李糖苷酶特性简述及影响酶活的因素[J].生物工程学报, 2021, 37(8):2623-2632.ZHU X C, TANG S Y.Enzymatic properties of α-L-rhamnosidase and the factors affecting its activity:A review[J].Chinese Journal of Biotechnology, 2021, 37(8):2623-2632.
[34] 陈东启, 余勃, 陆豫.RACE法克隆黑曲霉NCU-317中α-L-鼠李糖苷酶基因与生物信息学分析[J].南昌大学学报(理科版), 2019, 43(5):489-496.CHEN D Q, YU B, LU Y.RACE cloning and bioinformatics analysis of α-L-rhamnosidase from Aspergillus niger NCU-317[J].Journal of Nanchang University (Natural Science), 2019, 43(5):489-496.
[35] 蔡雨晨, 曹博瀚, 巩建业, 等.真核α-L-鼠李糖苷酶的碳水化合物结合结构域功能架构分析[J].现代食品科技, 2020, 36(1):156-162;168.CAI Y C, CAO B H, GONG J Y, et al.Functional and structural analysis of carbohydrate-binding module of eukaryotic α-L-rhamnosidase[J].Modern Food Science and Technology, 2020, 36(1):156-162;168.