浓香型白酒是中国白酒的典型代表,以其独特的特点深受消费者青睐,在市场中占据主导地位[1]。浓香型白酒酿造过程中的风味物质主要来自于酿造原料及微生物代谢,其中微生物代谢是白酒风味的主要来源[2]。糟醅是窖池发酵系统中的重要组成部分,在微生物代谢与多种理化因素相互作用下分解其中的大分子物质,代谢产生浓香型白酒呈香呈味的前体物质[3]。因此,行业内对浓香型白酒糟醅及微生物的研究愈加重视。
目前对于窖池的探究聚焦在时间、空间维度微生物菌群演替规律及与理化指标的相关性研究,并揭示新、老窖池在浓香型白酒增香微生物多样性及风味物质生成维度的差异。HE等[4]研究表明,与新窖池相比,老窖池中拥有更丰富的菌属组成,老窖泥中各类微生物相互作用,形成完整的窖泥菌群代谢链,使得其生产的浓香型白酒风味更佳,品质更好。杨中元等[5]对不同窖龄窖池基酒风味及其空间变化规律展开研究,结果表明老窖池对风味物质生成的影响强于新窖,老窖池基酒风味物质浓度明显优于新窖。MU等[6]解释了窖泥在发酵过程中对糟醅微生物组装机制及糟醅微生物对风味物质形成的影响,对于揭示糟醅发酵机理具有促进作用。曾波等[7]展开新、老窖池发酵糟醅理化及微生物群落差异与风味物质的影响研究,揭示了新、老窖池发酵糟醅理化特性及微生物群落相关性及白酒风味差异机制,为白酒微生物资源的开发利用提供了有价值的参考。糟醅研究受地域限制,导致糟醅理化指标、微生物存在差异和独特的浓香型白酒风格,因此对于糟醅发酵机理及风味物质生成需进一步研究。
本研究对西北某酒厂浓香型白酒新、老窖池发酵周期内糟醅取样检测理化指标,并采用高通量测序技术探究发酵糟醅微生物变化规律,解析浓香型白酒新、老窖池发酵糟醅理化指标与微生物群落差异,结合Spearman相关性研究揭示发酵糟醅优势微生物间、优势微生物与理化指标的相关性,为后续解析新、老窖生产原酒风味物质的作用机理提供数据参考。
1 材料与方法
1.1 实验材料
窖池中微生物多样性与代谢活性通常在20~30年内变得稳定[8],本实验糟醅样品取自甘肃某酒厂以高粱、大米、糯米、小麦和玉米为原料进行酿造8年(新)、35年(老)的窖池,新窖池糟醅发酵周期为70 d,老窖糟醅发酵周期为80 d,取样时间为4月~6月。
1.2 实验仪器
5424R高温台式冷冻离心机,德国Eppendorf公司;A200全触控屏梯度PCR仪,杭州朗基科学仪器有限公司;GL-88B旋涡混合器,海门市其林贝尔仪器制造有限公司;DYY-6C电泳仪,北京市六一仪器厂;Illumina MiSeq测序仪,美国Illumina公司。
1.3 实验方法
1.3.1 糟醅取样
根据糟醅发酵温度变化规律,使用自制取样器采集浓香型白酒新(X组)、老窖池(L组)上、中、下层发酵糟醅样品,每层糟醅样本由3口窖池5个取样点样本均匀混合而成(图1)。收集新窖第0、3、5、7、11、15、19、23、30、37、44、57、70天糟醅样本,分别标记为X0、X3、X5、X7、X11、X15、X19、X23、X30、X37、X44、X57、X70;老窖较新窖增加第80天样本,分别标记为L0、L3、L5、L7、L11、L15、L19、L23、L30、L37、L44、L57、L70、L80。所采集的糟醅样本一部分用于理化指标检测,另一部分保存至-80 ℃冰箱,用于送检微生物多样性。
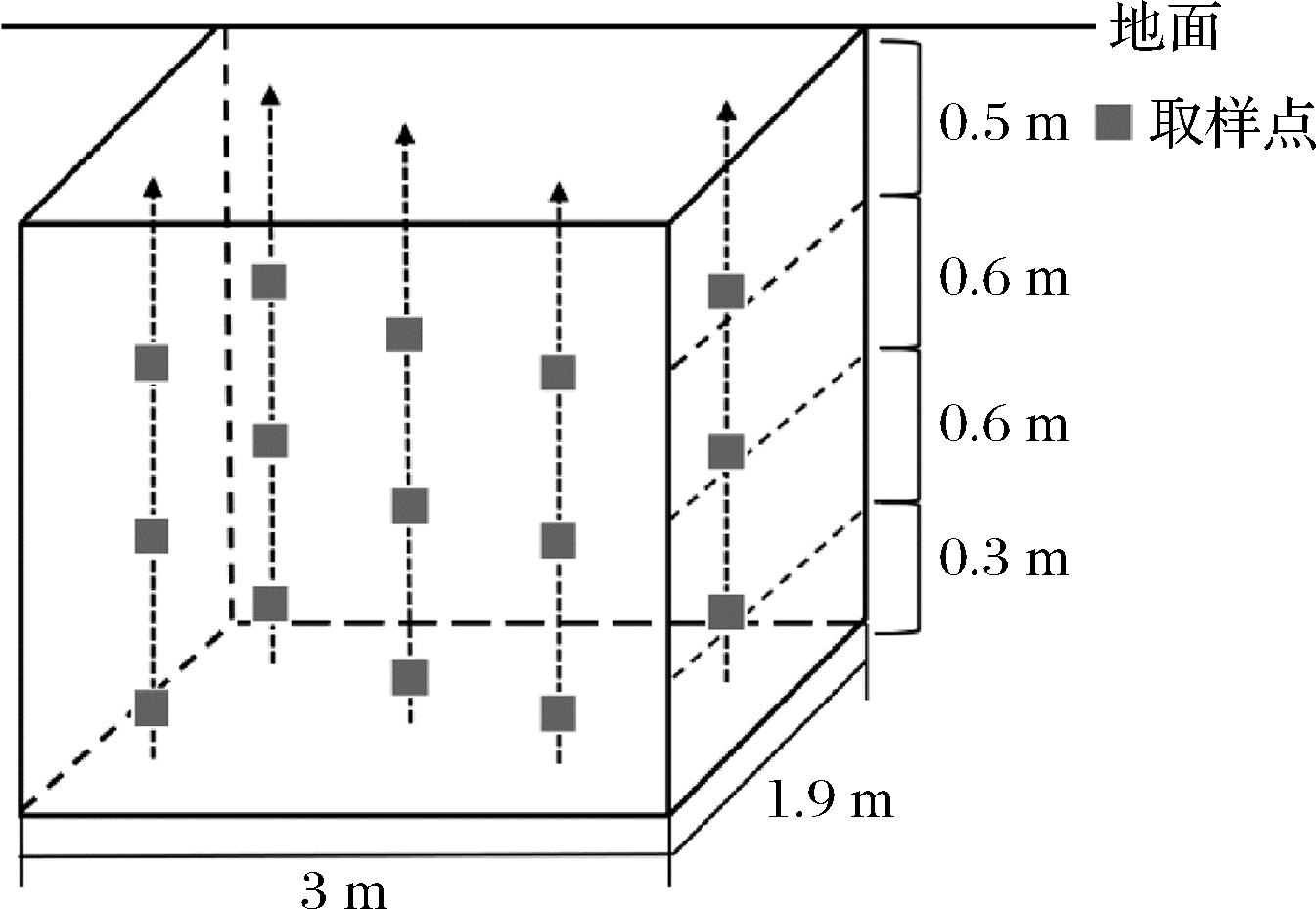
图1 糟醅取样示意图
Fig.1 Sampling diagram of fermented grains
1.3.2 糟醅理化指标检测
糟醅水分、酸度、淀粉含量、残糖含量、蒸馏酒精度检测参照王媚[9]的方法进行。
1.3.3 Illumina MiSeq高通量测序
根据实验要求提取糟醅样品基因组DNA,采用引物338F/806R和ITS1F/ITS2R[10]分别PCR扩增细菌16S DNA V3~V4和真菌ITS1的高变区基因序列,PCR扩增条件及体系参考WEI等[11]的方法。PCR扩增纯化后构建文库,进行Illumina MiSeq平台上机测序。测序后对序列质量进行质控,序列优化后进行操作分类单元(operational taxonomic units,OTU)聚类分析和物种分类学分析,对糟醅样品的OTU进行α-多样性指数分析。
1.4 数据分析
相关性热图通过在线平台https://www.chiplot.online/绘制,其他图表通过R软件绘制。
2 结果与分析
2.1 浓香型白酒新、老窖池发酵糟醅理化指标结果分析
水分是窖池发酵系统物质能量流动的载体,是发酵糟醅蒸馏时浓缩风味物质的主要参与者[12],水分通过影响窖池内固液发酵界面进而影响发酵糟醅物质循环。新、老窖糟醅水分随时间变化整体呈逐渐上升的趋势,发酵结束下层糟醅水分高于中、上层糟醅,与王媚等[13]研究结果一致。新窖糟醅水分由55.2%~57.6%升高至60.2%~68.6%(下层糟醅黄水浸泡),滴窖后糟醅水分恢复至正常出窖水平;老窖糟醅水分由56.5%~58.9%上升至60.9%~62.5%。发酵后期由于滴窖等工艺操作,使得发酵后期新窖上、中、下层糟醅和老窖上层糟醅水分含量明显下降(图2)。
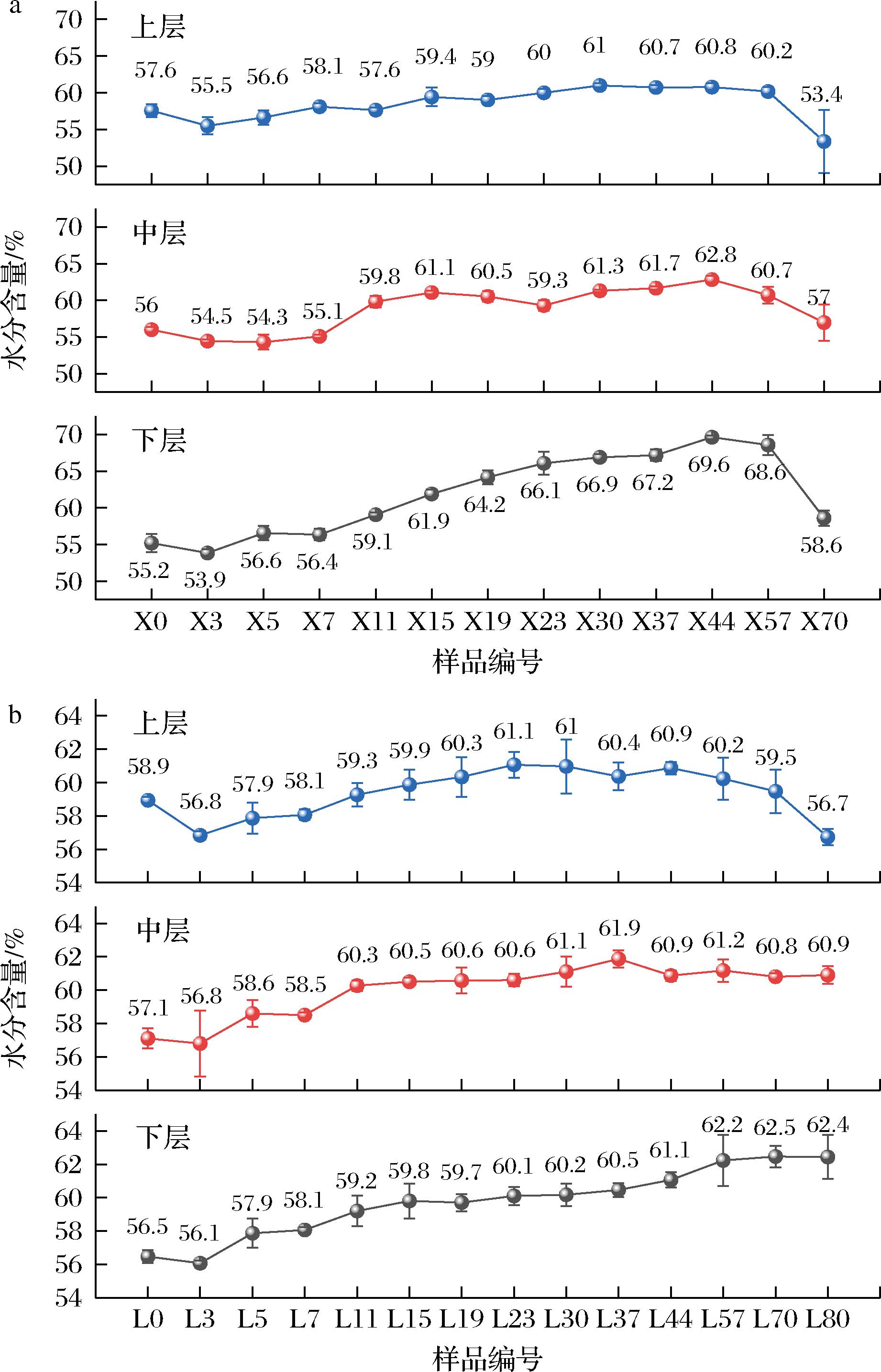
a-新窖池;b-老窖池
图2 发酵糟醅水分含量
Fig.2 Moisture content of fermented grains
酸是浓香型白酒呈味的主要物质,是酯类的合成前体,适宜的酸度有利于淀粉糊化糖化,抑制其他杂菌生长,并为酵母菌和霉菌提供营养进而促进风味物质生成,提升产酒质量[14]。伴随着发酵糟醅产酸微生物不断生长,新、老窖糟醅酸度在整个发酵过程中呈上升趋势,新窖糟醅酸度由1.5~1.7升高至2.3~3.4,老窖糟醅酸度由1.9~2.1升高至3.5~4.1,老窖糟醅酸度整体高于新窖(图3),与王乐等[15]的研究结果一致。
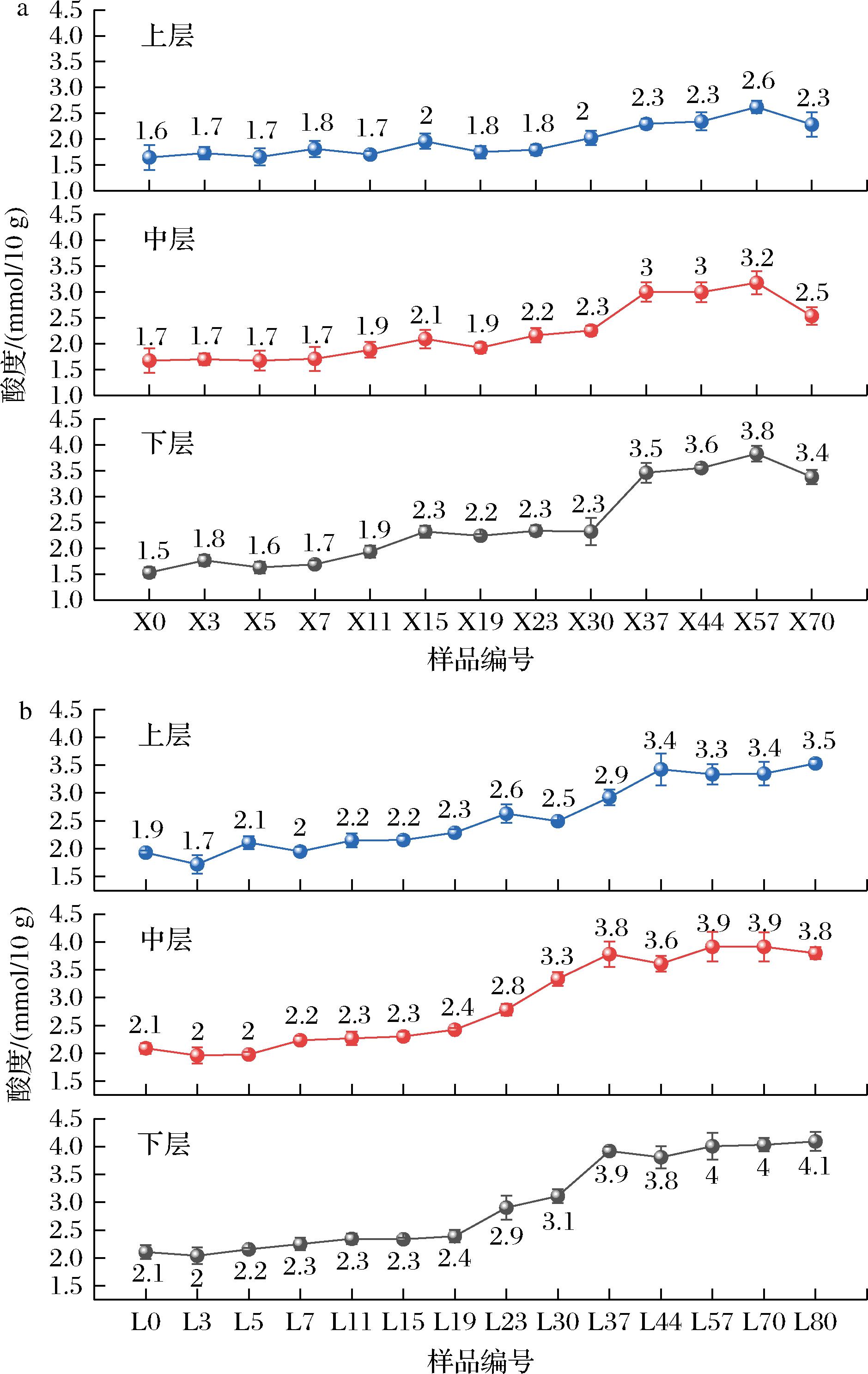
a-新窖池;b-老窖池
图3 发酵糟醅糟醅酸度
Fig.3 Acidity of fermented grains
淀粉是酿酒原粮中的主要成分,是微生物生长代谢和窖池升温的主要物质来源,淀粉分解后生成还原糖,经过酿酒微生物代谢产生酒精和其他风味成分[16]。新、老窖糟醅淀粉含量整体呈下降趋势,糟醅发酵正常。新窖糟醅淀粉含量从21.2%~21.9%下降至10.0%~10.9%,老窖糟醅淀粉含量从21.4%~22.3%下降至9.2%~13.6%(图4)。新窖淀粉利用率略高于老窖,这与窖池中糖化微生物代谢活跃程度相关,淀粉利用率不能直接说明新、老窖池出酒率和产酒质量,入窖前工艺控制和整体发酵情况均是影响淀粉消耗的重要因素[17]。
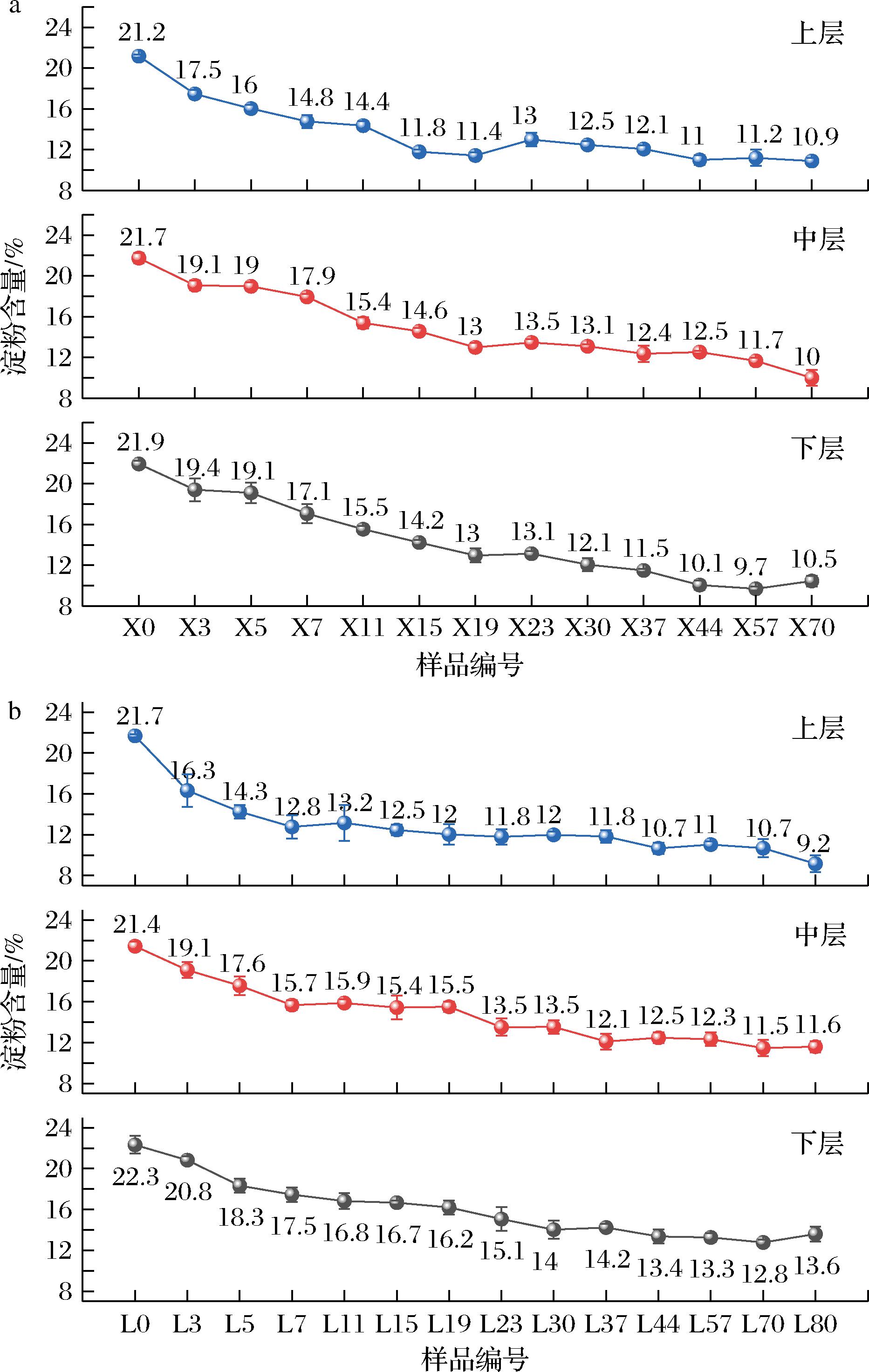
a-新窖池;b-老窖池
图4 发酵糟醅淀粉含量
Fig.4 Starch content of fermented grains
还原糖是淀粉转化为风味物质的中间产物,反映淀粉糖化与发酵程度的协调关系,发酵过程中新、老窖糟醅残糖含量整体呈下降趋势,新窖糟醅残糖含量由2.1%~2.8%降低至0.4%,老窖糟醅残糖含量从1.5%~2.6%下降至0.5%(图5),新、老窖池残糖变化规律较为相似,残糖含量越低,表明其利用消耗率越高,糟醅发酵较为正常[18]。
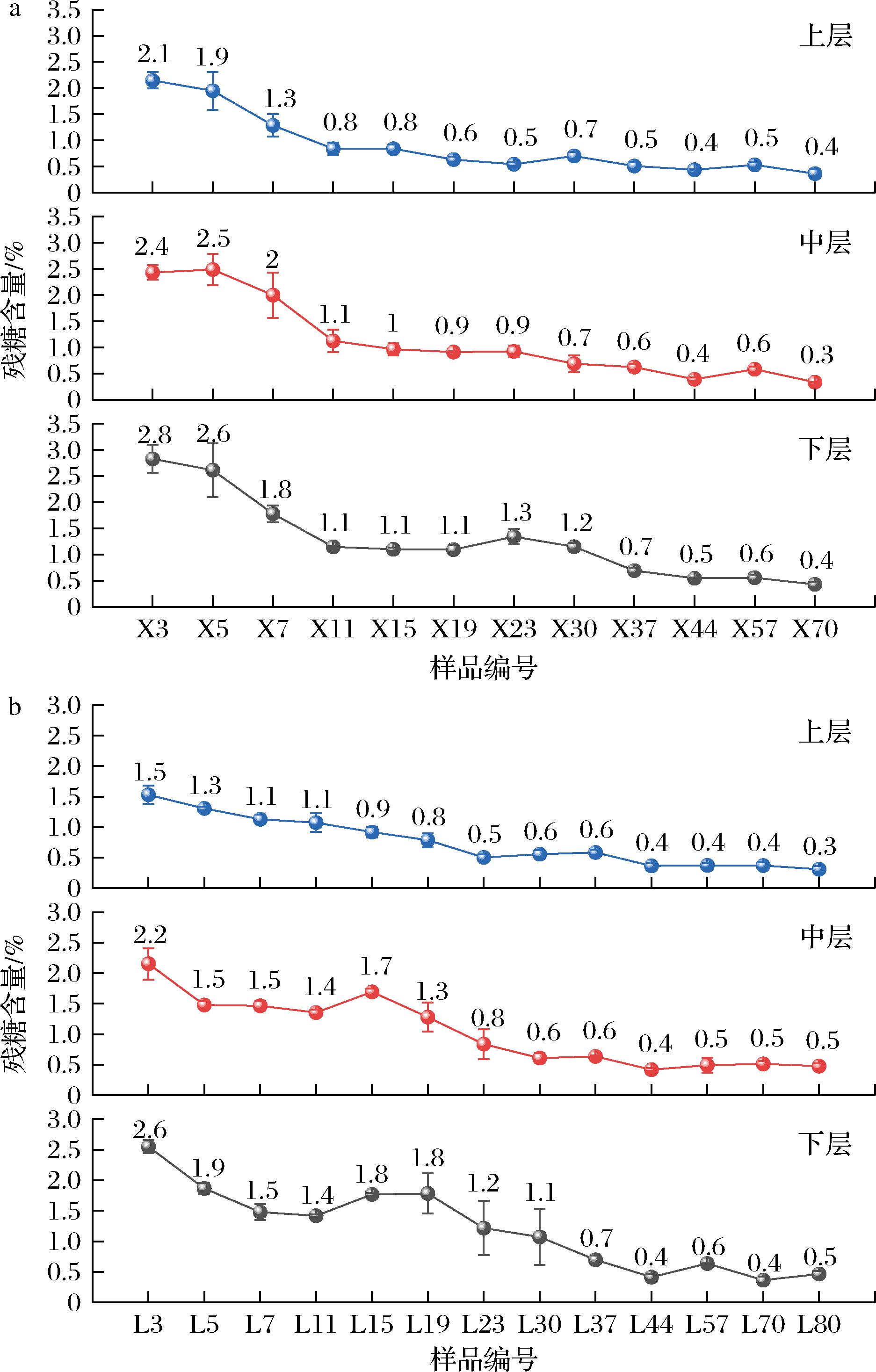
a-新窖池;b-老窖池
图5 发酵糟醅残糖含量
Fig.5 Residual sugar content of fermented grains
糟醅蒸馏酒精度主要反映糟醅发酵过程中酒精含量变化规律,新窖糟醅蒸馏酒精度从0.2%vol升高至2.4%vol~4%vol,老窖糟醅蒸馏酒精度从0.9%vol~1.2%vol升高至2%vol~3.8%vol(图6),新窖糟醅蒸馏酒精度在发酵前期上升幅度高于老窖,发酵中后期变化规律相近,这与窖池发酵前期大量生成酒精、发酵中后期醇酸酯化反应能力相关。由于重力的作用,下层糟醅酒精含量较中、上层丰富,其次下层糟醅蒸馏酒精度高于中、上层是由于蒸馏过程中收集到其他挥发性物质导致[19]。
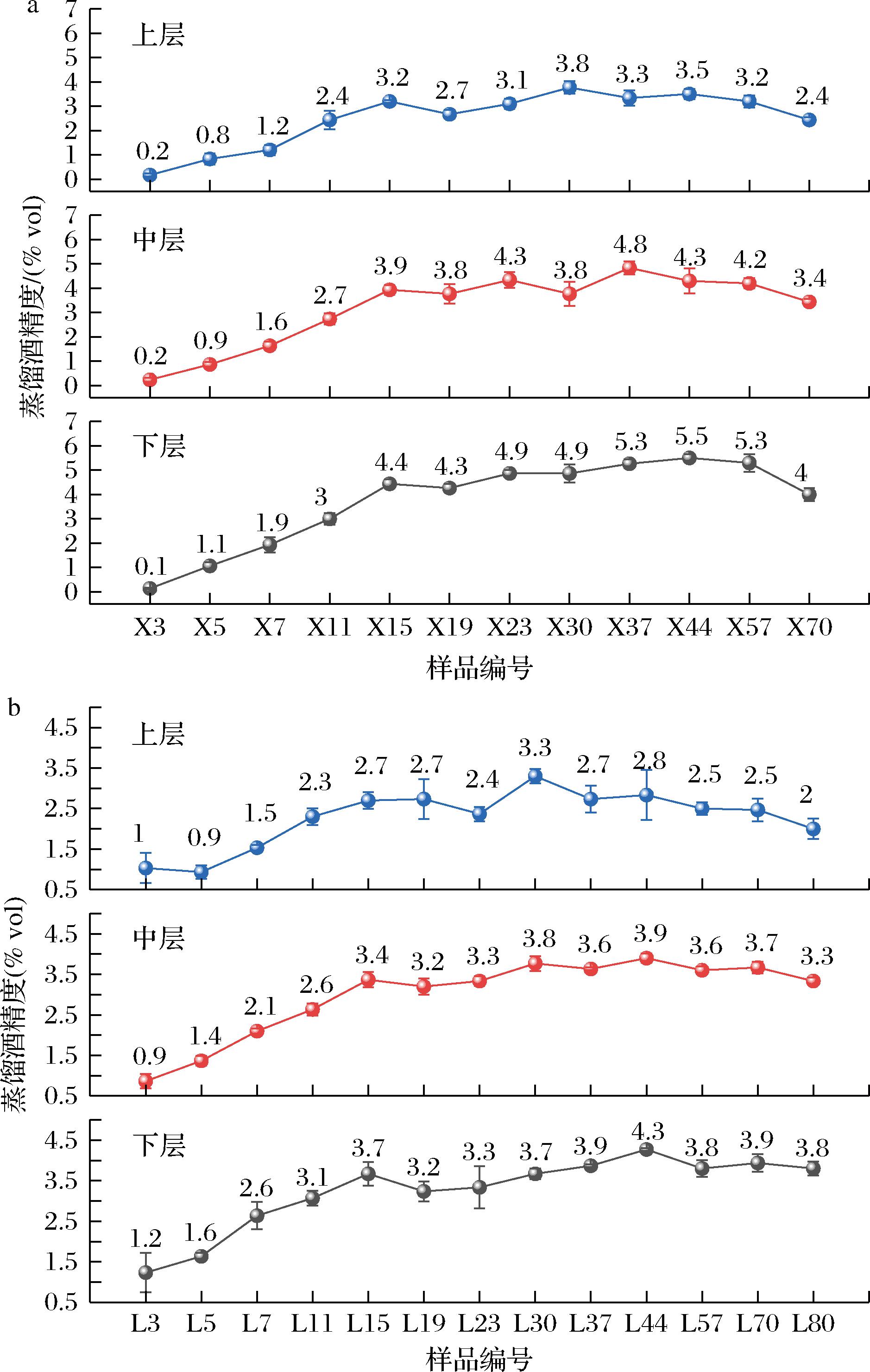
a-新窖池;b-老窖池
图6 发酵糟醅蒸馏酒精度含量
Fig.6 Alcoholic content of fermented grains
综上,新、老窖糟醅发酵前期水分呈增长趋势,后期微生物生化反应及工艺控制导致水分含量下降;酸度整体呈上升趋势,后期趋于稳定;前期霉菌、酵母菌比较活跃且可利用淀粉含量高,淀粉前期比后期消耗速度快,整体呈下降趋势;还原糖含量呈波动式下降;前期糟醅酒精含量增加,中后期部分酒精参与酯化反应或作为碳源被微生物利用,整体变化规律与酸度相近。由于白酒酿造产区差异性,甘肃地区糟醅水分、酸度、残糖含量低于泸州、宜宾地区,残余淀粉量高于泸州、宜宾地区,蒸馏酒精度相近[20]。正是由于产区地理位置条件、原料特性及发酵工艺不同导致浓香型白酒糟醅理化指标和微生物代谢的差异,形成不同产区浓香型白酒独特的风格,对认识不同产区糟醅发酵过程中的理化指标变化规律和提升产品品质具有重要的意义。
2.2 浓香型白酒新、老窖池发酵糟醅微生物菌群的α-多样性分析
α-多样性是反映特定生态系统内生物丰富度和多样性的综合指标,利用Chao 1和Shannon、Simpson指数分别进行评估[21]。新、老窖池发酵糟醅微生物菌群的α-多样性整体呈先增后减再增的变化趋势,并且细菌菌群的丰富度和多样性均高于真菌菌群,老窖糟醅样品中细菌群落多样性、物种丰富度优于新窖,真菌群落反之(图7)。发酵0~11 d细菌和真菌α-多样性大幅提高,表明大量微生物增殖生长,发酵11~30 d由于O2耗尽和酒精大量生成,超过大部分微生物耐受阈值,造成细菌和真菌α-多样性大幅下降,30 d以后由于发酵生境,厌氧微生物大量增殖使得细菌和真菌α-多样性再次升高。
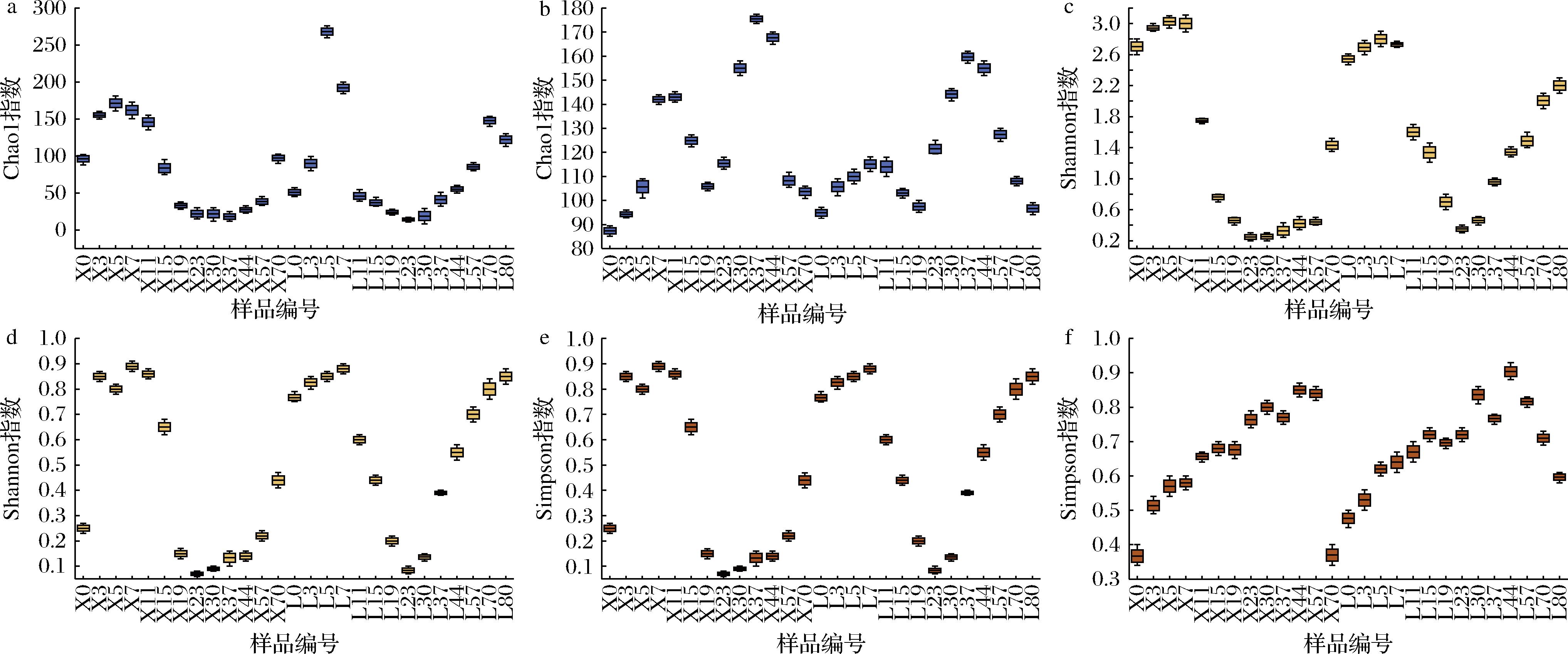
a-细菌Chao 1指数;b-真菌Chao 1指数;c-细菌Shannon指数;d-真菌Shannon指数;e-细菌Simpson指数;f-真菌Simpson指数
图7 发酵糟醅微生物α-多样性分析结果
Fig.7 Results of microbial α-diversity analysis of fermented grains
2.3 浓香型白酒新、老窖池发酵糟醅微生物菌群的β-多样性分析
2.3.1 细菌群落组成及演替
本研究将新、老窖糟醅样品中相对丰度>1%的微生物定义为优势微生物。基于高通量测序的序列数据分析表明新、老窖糟醅样品中细菌主要分布在20个门,厚壁菌门(Firmicutes)、变形菌门(Proteobacteria)、放线菌门(Actinobacteriota)、拟杆菌门(Bacteroidota)是新、老窖糟醅主要的优势细菌门(图8)。新、老窖糟醅门水平细菌群落变化规律相近,厚壁菌门(Firmicutes,47.7%~99.2%,55.1%~98.9%)占据主导地位。
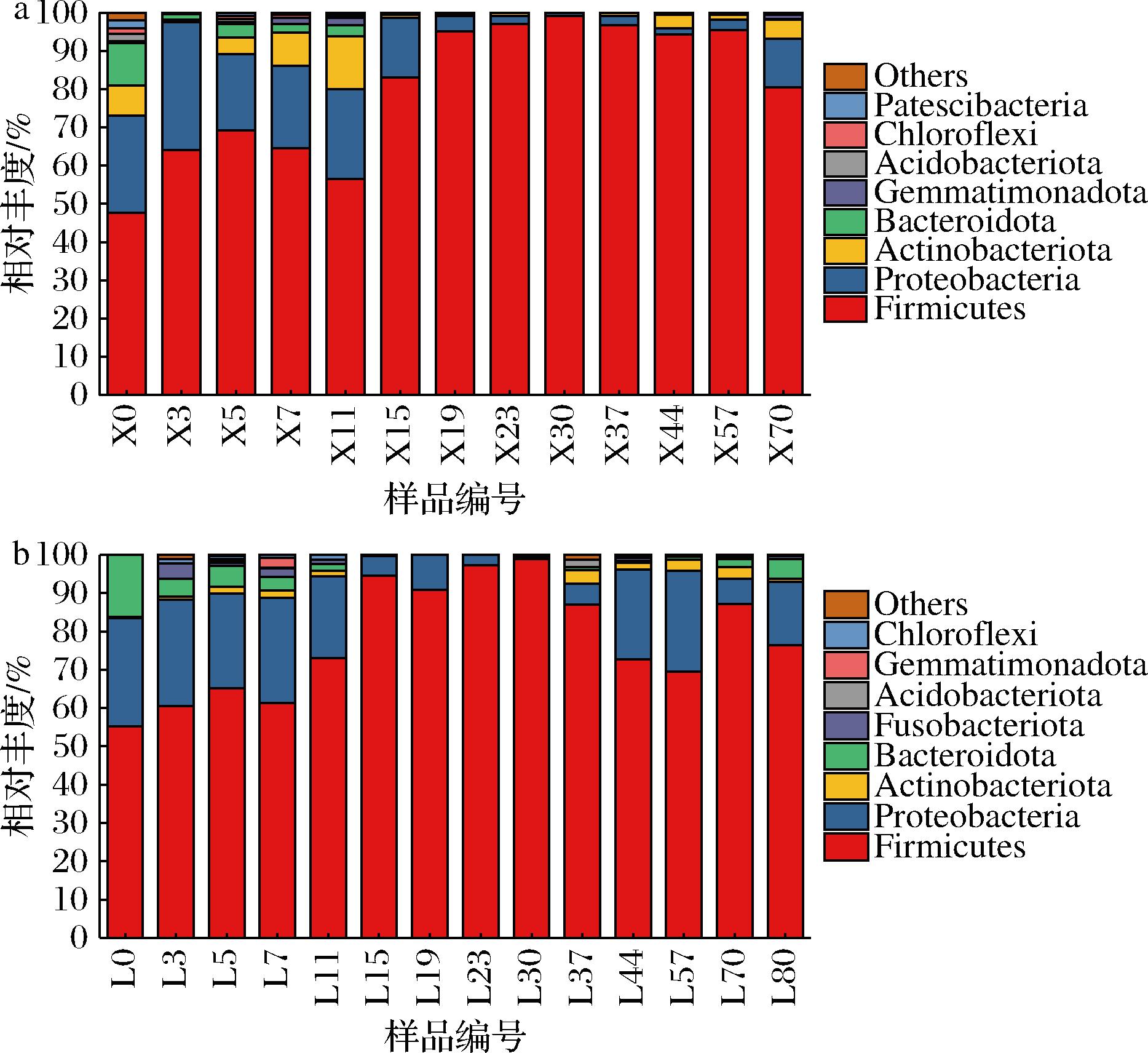
a-新窖池;b-老窖池
图8 发酵糟醅门水平细菌群落结构
Fig.8 Bacterial community structure at the phylum level of fermented grains
由图9-a可知,新窖发酵糟醅0~11 d以乳杆菌属(Lactobacillus,31.4%~58.1%)、醋酸菌属(Acetobacter,2.5%~57.2%)为主要优势菌属;15~70 d发酵糟醅细菌微生物以乳杆菌属(Lactobacillus,77.0%~99.1%)为主要优势菌属。由图9-b可知,老窖发酵糟醅0~11 d以乳杆菌属(Lactobacillus,14.5%~61.9%)、醋酸菌属(Acetobacter,1.1%~36.2%)、不动杆菌属(Acinetobacter,3.7%~22.4%)、高温放线菌属(Thermoactinomyces,3.2%~15.5%)为主要优势菌属;15~70 d发酵糟醅细菌微生物以乳杆菌属(Lactobacillus,48.8%~98.6%)为主要优势菌属。综上所述,新、老窖糟醅发酵过程中细菌微生物群落不断演替,乳杆菌属是发酵过程中绝对优势菌属,这与高江婧等[22]的研究结果一致。乳杆菌属、醋酸菌属在发酵前期能够快速产生乳酸、乙酸等有机酸,有效抑制其他杂菌生长,代谢产生的CO2有助于推进发酵环境从有氧到无氧的转变,醋酸菌属相对丰度下降。随着发酵的进行,糟醅酸度、酒精含量增加,含氧量降低,继而出现更耐酸、耐酒精、耐低含氧量的乳酸菌参与后续发酵过程[23]。
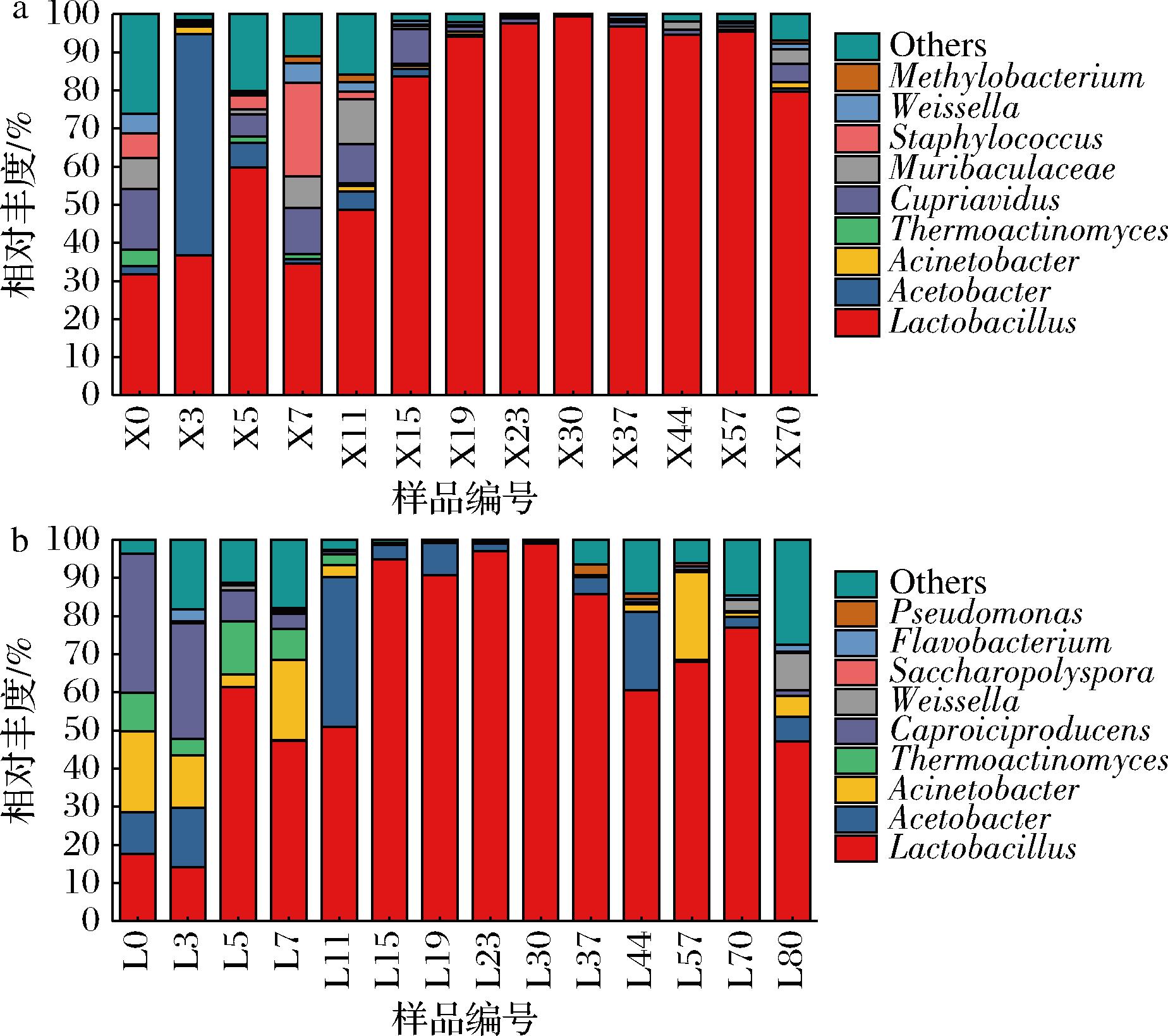
a-新窖池;b-老窖池
图9 发酵糟醅属水平细菌群落结构
Fig.9 Bacterial community structure at the genus level of fermented grains
2.3.2 真菌群落组成及演替
基于高通量测序的序列数据分析表明,新、老窖糟醅样品中真菌主要分布在12个门,新窖糟醅样品有2个优势真菌门,分别是子囊菌门(Ascomycota)和担子菌门(Basidiomycota);老窖糟醅样品有3个优势菌门,分别为子囊菌门(Ascomycota)、担子菌门(Basidiomycota)、真菌门(Fungi)(图10)。其中新窖糟醅发酵前中期门水平真菌群落由子囊菌门(75.2%~99.7%)占据主导地位,发酵后期由担子菌门(78.7%~93.1%)占据主导地位,而老窖糟醅门水平真菌群落发酵后期担子菌门相对丰度有所增长,但整个发酵过程仍以子囊菌门(48.4%~99.7%)占据主导地位。
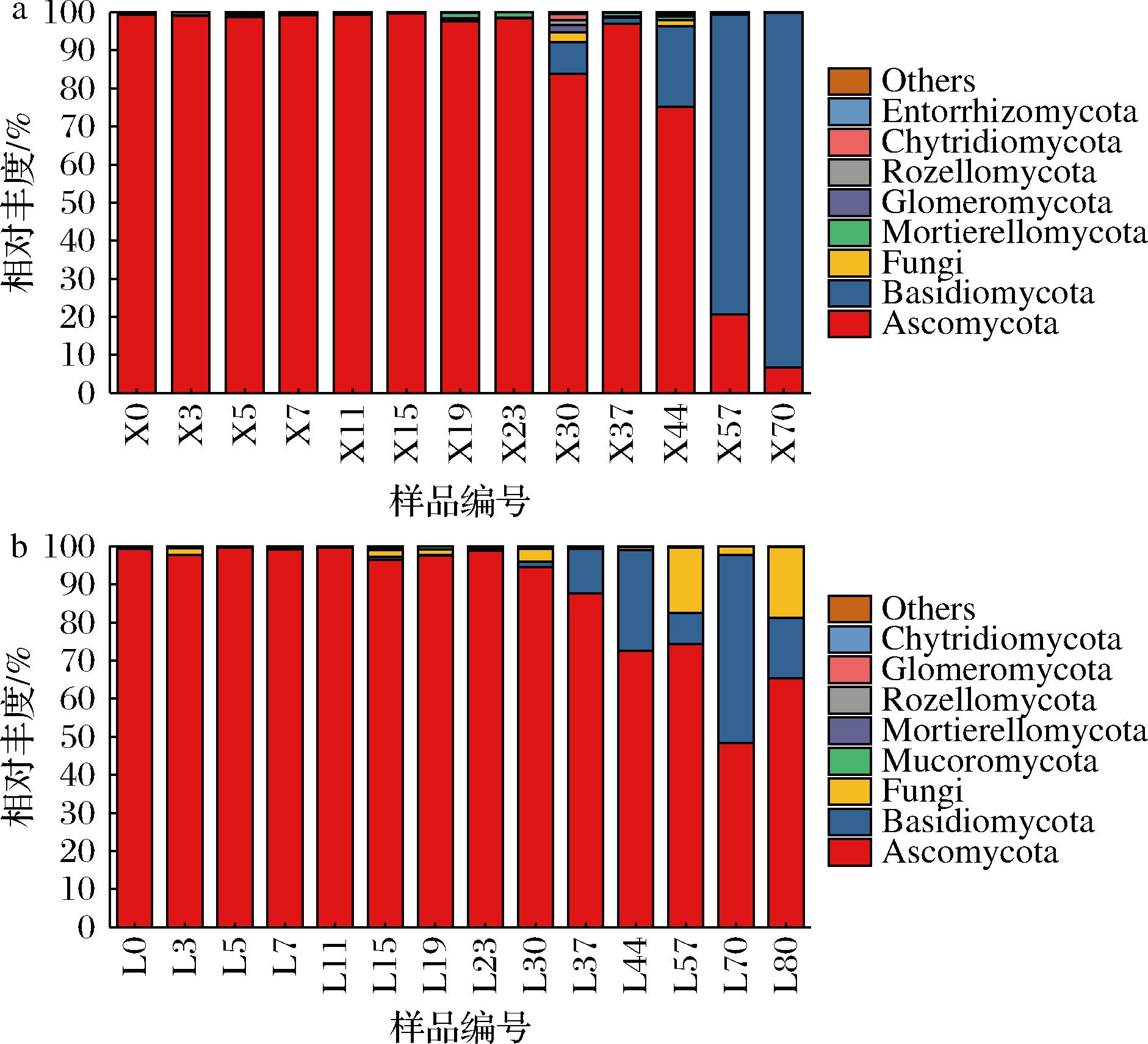
a-新窖池;b-老窖池
图10 发酵糟醅门水平真菌群落结构
Fig.10 Fungal community structure at the phylum level of fermented grains
由图11-a可知,新窖发酵糟醅0~37 d以嗜热真菌属(Thermomyces,46.6%~84.4%)、哈萨克斯坦酵母属(Kazachstania,3.6%~40.2%)、毕赤酵母属(Pichia,1.0%~8.5%)为主要优势菌属;44~70 d以担子菌酵母属(Apiotrichum,47.1%~97.5%)为主要优势菌属。由图11-b可知,老窖发酵糟醅0~44 d以嗜热真菌属(32.6%~78.4%)、哈萨克斯坦酵母属(2.9%~62.1%)为主要优势菌属;44~80 d真菌微生物群落较为丰富,以嗜热真菌属(5.9%~7.1%)、哈萨克斯坦酵母属(1.9%~5.1%)、担子菌酵母属(24.9%~47.7%)、青霉属(Penicillium,30.7%~36.1%)为主要优势菌。综上所述,新、老窖糟醅发酵过程中真菌微生物群落不断演替,嗜热真菌属、哈萨克斯坦酵母属是发酵前中期的主要优势菌属,担子菌酵母属是发酵后期的主要优势菌属,这与李宜伦[24]研究结果相近。嗜热真菌属和哈萨克斯坦酵母属在乳酸发酵过程中同化乳酸,水解葡萄糖醛糖苷作为异型发酵乳酸菌的代谢底物,促进其利用果糖产乙酸,并合成其他风味物质,初步推测这是新窖池的产酒量较高,而老窖风味更优的原因之一[25]。担子菌酵母属参与氨基酸、还原糖、高级脂肪酸、多元醇、矿物质等物质代谢过程,对于酯类前体物质合成具有正向作用,进而丰富白酒风味物质[26]。
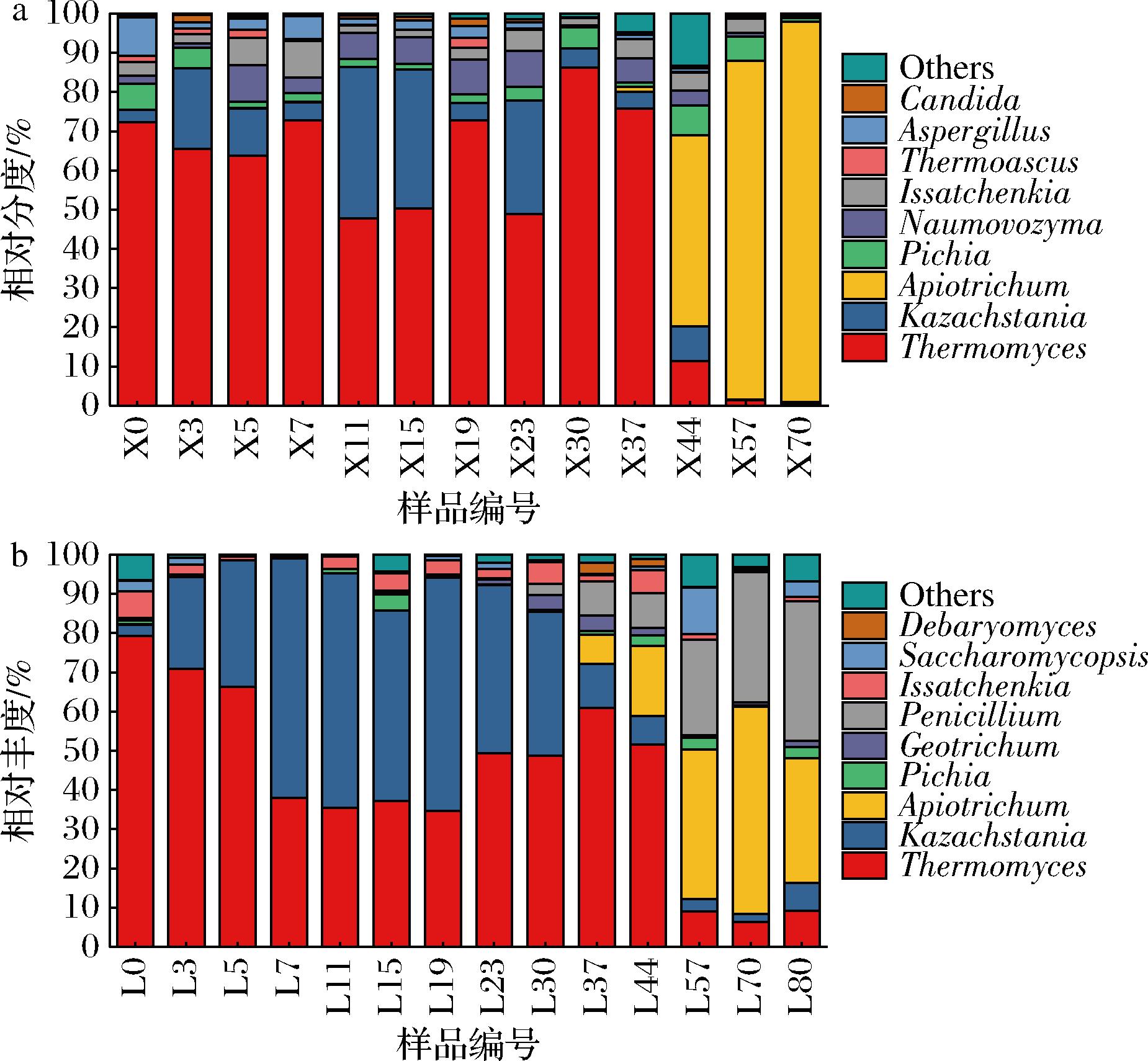
a-新窖池;b-老窖池
图11 发酵糟醅属水平真菌群落结构
Fig.11 Fungal community structure at the genus level of fermented grains
2.4 浓香型白酒新、老窖池发酵糟醅微生物菌群相关性分析
微生物多样性及演替决定其复杂的相互作用关系和多样化的代谢规律,本文基于Spearman相关性热图分析评估新、老窖池中优势微生物属间的相互作用关系(图12),多数优势微生物表现出较强的属间作用关系,维持微生物之间的演替和代谢平衡,驱动整个发酵过程[27]。新窖池优势真菌与细菌之间的正相关较强,老窖池反之,其中微生物相互作用呈正相关的结果表明发酵过程中具有明显的协同作用,反之呈负相关的结果具有明显的抑制作用[28]。由图12-a可知,新窖糟醅发酵过程中,曲霉属(Aspergillus)与高温放线菌属(Thermoactinomyces)呈高度显著正相关(P<0.001),与贪铜菌属(Cupriavidus)、魏斯氏菌属(Weissella)呈极显著正相关(P<0.01),与葡萄球菌属(Staphylococcus)呈显著正相关(P<0.05),与乳杆菌属(Lactobacillus)呈极显著负相关(P<0.01),研究表明曲霉属、高温放线菌属与魏斯氏菌属是新窖池中的主要优势菌属,共同推进发酵环境微生物群的组装,而乳杆菌属在演替过程中具有较强的竞争力,在整个发酵过程中占据主要地位。由图12-b可知,老窖糟醅发酵过程中微生物相互作用更加复杂,东方伊萨酵母属(Issatchenkia)和魏斯氏菌属呈高度显著负相关(P<0.001),与扣囊覆膜酵母属(Saccharomycopsis)呈显著负相关(P<0.05);德巴利酵母属(Debaryomyces)与假单胞菌属(Pseudomonas)呈极显著正相关(P<0.01),与乳杆菌属呈显著正相关(P<0.05),与己酸菌属(Caproiciproducens)呈极显著负相关(P<0.01);地霉属(Geotrichum)与假单胞菌属呈显著正相关(P<0.05),与高温放线菌属呈显著极负相关(P<0.01),与己酸菌属(Caproiciproducens)呈显著负相关(P<0.05);青霉菌属(Penicillium)与高温放线菌属呈显著极负相关(P<0.01);毕赤酵母属(Pichia)与醋酸菌属(Acetobacter)呈显著正相关(P<0.05),与邱显平等[29]研究结果相近,老窖池组的微生物网络具有更高的聚集程度,微生物群落的共存关系更加复杂。综上,新、老窖微生物群在窖池环境长时间的筛选下逐渐稳定,但新窖内的微生物相关性在老窖中不尽相同,与窖龄息息相关。
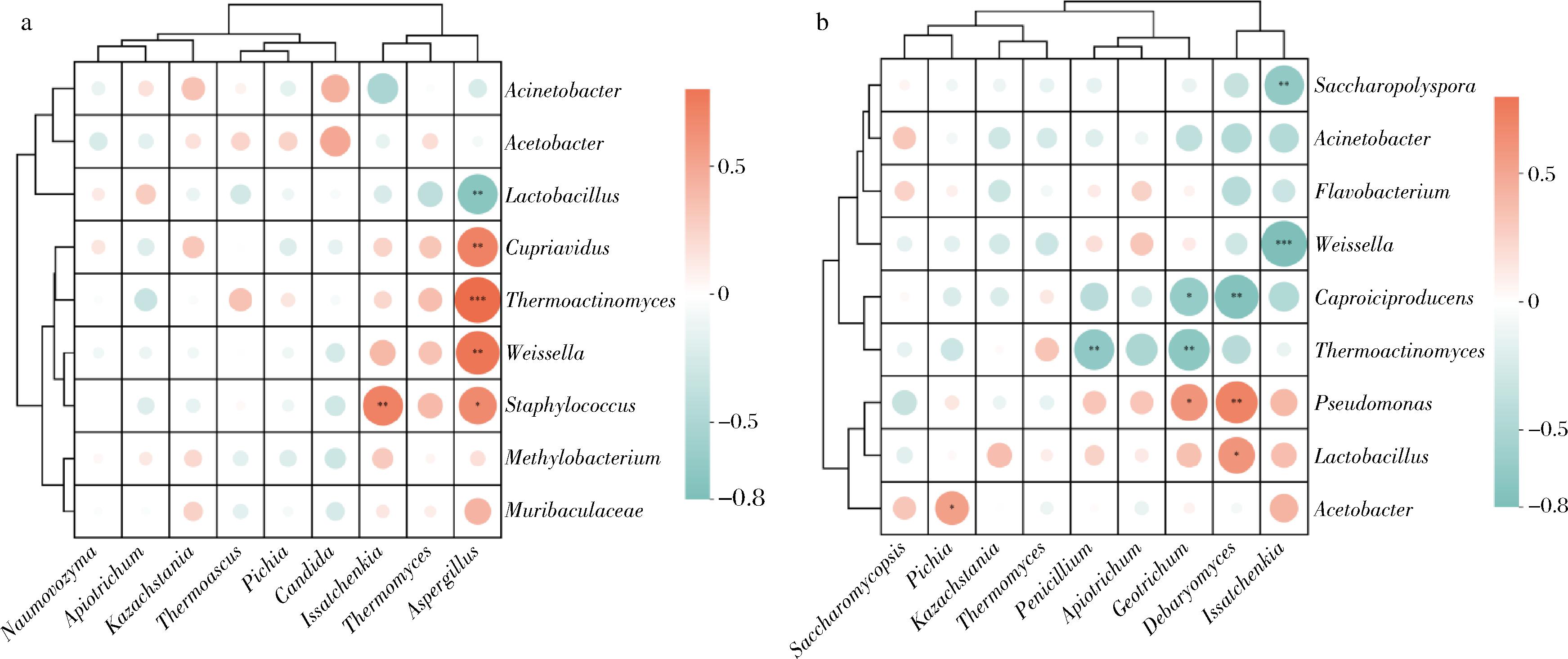
a-新窖池;b-老窖池
图12 发酵糟醅属水平优势微生物相关性分析
Fig.12 Correlation analysis of dominant microorganisms at the genus level of fermented grains
注:*表示P<0.05呈现显著相关,**表示P<0.01呈现显著相关,***表示P<0.001呈现显著相关,下同。
2.5 浓香型白酒新、老窖池发酵糟醅理化指标与微生物菌群相关性分析
浓香型白酒糟醅发酵过程中理化和微生物群落相互作用,为了揭示糟醅发酵过程中理化因素对于微生物群落演替影响,本文用热图展现了理化与优势微生物属间Spearman相关性,结果如图13所示,新、老窖糟醅微生物聚为相关性相反的2类,一类是与淀粉、还原糖消耗有关,另一类与有机酸、水、酒精生成有关。由图13-a可知,新窖池发酵糟醅中扣囊覆膜酵母属、醋酸菌属(Acetobacter)、高温放线菌属、嗜热真菌属、曲霉属与淀粉、残糖含量呈极显著正相关(P<0.05),表明以上微生物对淀粉、还原糖利用转化作用较强,对淀粉分解、还原糖转化具有正向作用,DU等[30]研究表明随着上述微生物丰度增加,与淀粉代谢、糖酵解相关酶类表达水平上调,不断将淀粉、还原糖转化为酒精。担子菌酵母属与淀粉、残糖含量呈显著负相关(P<0.05),乳杆菌属与淀粉含量呈显著负相关(P<0.05),乳杆菌属与酒精度、水分、酸度呈显著正相关(P<0.05),担子菌酵母属与酸度呈显著正相关(P<0.05),表明乳杆菌属与担子菌酵母属在发酵过程中促进酸度、水分、酒精生成,MU等[31]研究表明糟醅中乳酸脱氢酶的高表达积累了大量乳酸和乙酸,使糟醅酸度在发酵过程中不断升高,并且乳杆菌属对淀粉代谢和糖酵解代谢过程中酶的表达存在抑制作用。扣囊覆膜酵母属、醋酸菌属、高温放线菌属与酒精度、水分、酸度呈显著负相关(P<0.05),噬热子囊菌属、曲霉属、贪铜菌属(Cupriavidus)、嗜热真菌属与酸度呈显著负相关(P<0.05),上述优势微生物与酒精度、水分、酸度呈负相关,原因在于发酵过程中伴随糟醅发酵酒精、酸度增加,对大部分不耐受微生物产生抑制作用甚至使其丰度减少,影响其正常生长代谢作用[32]。由图13-b可知,老窖池发酵糟醅中己酸菌属、高温放线菌属、嗜热真菌属与淀粉含量呈显著正相关(P<0.05),嗜热真菌属、哈萨克斯坦酵母属(Kazachstania)与残糖含量呈显著正相关(P<0.05)。地霉属(Geotrichum)、担子菌酵母属、青霉菌属与淀粉、残糖含量呈显著负相关(P<0.05)。嗜热真菌属、哈萨克斯坦酵母属在发酵前中期占据优势地位,对淀粉、还原糖转化作用比较明显,这也解释了发酵前期淀粉、还原糖含量下降较快的原因[33]。伴随着淀粉、还原糖被消耗,酒精、有机酸和水不断生成,地霉属、担子菌酵母属、青霉菌属、德巴利酵母属与酸度和酒精度呈显著正相关(P<0.05),地霉属、德巴利酵母属、乳杆菌属、假单胞菌属与水分呈显著正相关(P<0.05),上述微生物主要以酒精生成、酯类物质合成为主,丰富所产白酒风味物质含量[34]。己酸菌属、高温放线菌属、嗜热真菌属与酸度呈显著负相关(P<0.05),高温放线菌属、己酸菌属、不动杆菌属、黄杆菌属(Flavobacterium)与水分呈显著负相关(P<0.05),高温放线菌属、己酸菌属与酒精度含量呈显著负相关。综上,新窖糟醅发酵过程中的理化指标对真菌群落的影响较小,而老窖反之;水分、酸度、淀粉、还原糖含量和蒸馏酒精度可作为调控糟醅微生物的指标,间接调控微生物代谢途径以实现浓香型白酒风味物质的合成。
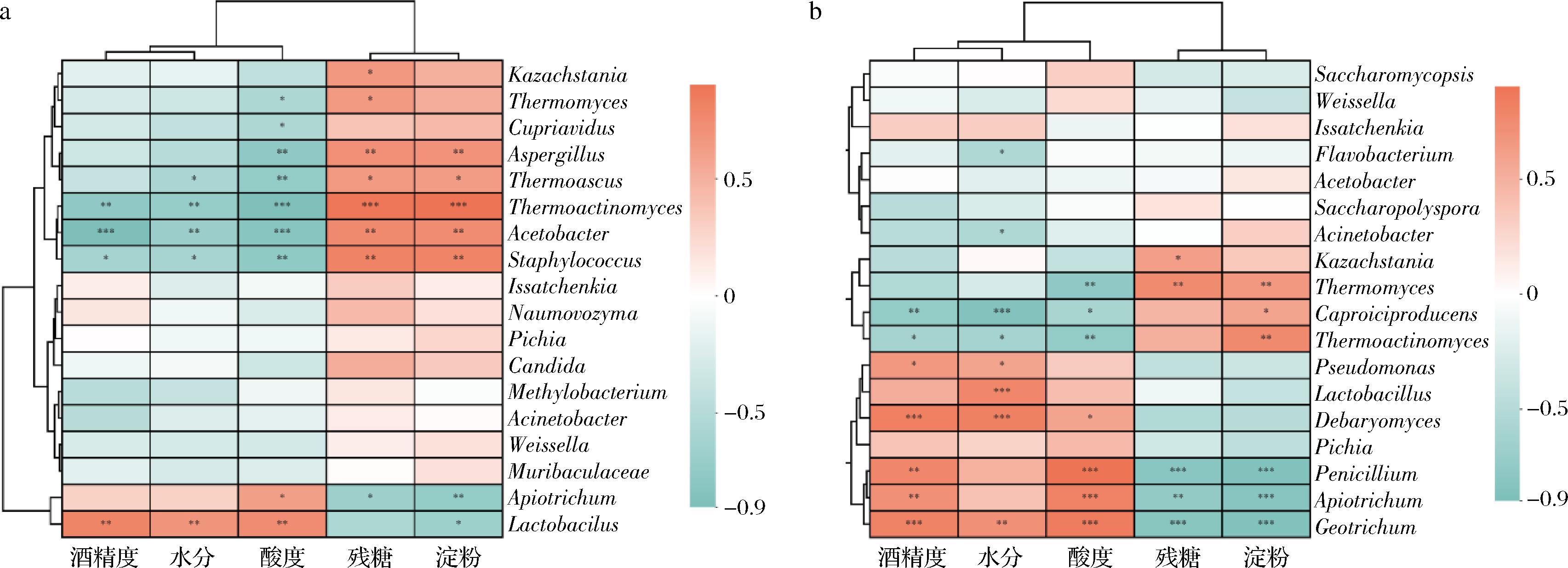
a-新窖池;b-老窖池
图13 发酵糟醅理化与优势微生物属相关性分析
Fig.13 Correlation analysis between the physicochemical indexes and the dominant microbial genera of fermented grains
3 结论
通过对浓香型白酒新、老窖池整个发酵周期的糟醅取样检测分析,新、老窖池糟醅理化指标变化规律较为相近。高通量技术解析新、老窖发酵糟醅微生物结果表明新、老窖糟醅发酵过程中微生物群落不断演替,乳杆菌属(Lactobacillus)是整个发酵过程最主要的优势细菌属,嗜热真菌属(Thermomyces)、哈萨克斯坦酵母属(Kazachstania)是发酵前、中期的主要优势真菌属,担子菌酵母属(Apiotrichum)是发酵后期的主要优势真菌属。相关性分析结果表明,新、老窖池糟醅中优势微生物间存在不同程度的联系,糟醅优势微生物与淀粉、还原糖的代谢和有机酸、水和酒精生成聚类相反,新窖糟醅发酵过程中的理化指标对真菌群落的影响较小,而老窖反之。后续研究以新、老窖生产的原酒风味物质为重点,结合糟醅理化指标和微生物数据,深入探究理化指标与优势微生物对浓香型白酒风味物质形成的影响,为揭示浓香型白酒发酵机理提供科学依据。
[1] HE Y X, LIU Z P, QIAN M, et al.Unraveling the chemosensory characteristics of strong-aroma type Baijiu from different regions using comprehensive two-dimensional gas chromatography-time-of-flight mass spectrometry and descriptive sensory analysis[J].Food Chemistry, 2020, 331:127335.
[2] CHAI L J, ZHANG J Y, GAO T, et al.Seasonality shapes the microbiota and metabolome of strong-flavor Baijiu during fermentation and affects its flavor characteristics[J].Food Bioscience, 2024, 62:105534.
[3] HUANG Z G, ZENG B, DENG J, et al.Succession of microbial community structure in fermented grains during the fermentation of strong-flavor Baijiu and its impact on the metabolism of acids, alcohols, and esters[J].Food Science and Biotechnology, 2024, 33(15):3501-3513.
[4] HE G Q, GAO L, DENG Y, et al.Microbial succession in different years of pit mud from a distillery in Sichuan for Nong-Xiang Baijiu fermentation[J].Food Science and Biotechnology, 2024, 33(13):3083-3092.
[5] 杨中元, 杨岱霖, 郭辉祥, 等.新老窖池窖内风味物质水平空间分布的差异性分析[J].酿酒科技, 2025(11):28-32.YANG Z Y, YANG D L, GUO H X, et al.Difference analysis of horizontal spatial distribution of flavor substances in new and old pits[J].Liquor-Making Science &Technology, 2025(11):28-32.
[6] MU Y, HUANG J, ZHOU R Q, et al.Response and assembly of abundant and rare taxa in Zaopei under different combination patterns of Daqu and pit mud:From microbial ecology to Baijiu brewing microecosystem[J].Food Science and Human Wellness, 2024, 13(3):1439-1452.
[7] 曾波, 饶家权, 邹永芳, 等.浓香型白酒酒醅发酵过程中微生物群落结构演替及其与理化指标相关性[J].食品科学, 2024, 45(7):111-118.ZENG B, RAO J Q, ZOU Y F, et al.Structural succession of microbial communities in fermented grains for nongxiangxing Baijiu during the fermentation process and its correlation with physicochemical indicators[J].Food Science, 2024, 45(7):111-118.
[8] MU Y, HUANG J, ZHOU R Q, et al.Exploring the response patterns of strong-flavor Baijiu brewing microecosystem to fortified Daqu under different pit ages[J].Food Research International, 2022, 155:111062.
[9] 王媚. 浓香型白酒糟醅窖内外发酵动态因子的初步研究[D].贵阳:贵州大学,2015.WANG M.A preliminary study of dynamic factors inside and outside of the cellar when grains were fermentated of Luzhou-flavor liquor [D].Guiyang:Guizhou University, 2015.
[10] 胡晓龙, 王康丽, 余苗, 等.浓香型酒醅微生物菌群演替规律及其空间异质性[J].食品与发酵工业, 2020, 46(10):66-73.HU X L, WANG K L, YU M, et al.Microbial community succession pattern and spatial heterogeneity in fermented grains of strong-flavor Baijiu[J].Food and Fermentation Industries, 2020, 46(10):66-73.
[11] WEI H W, WANG L H, HASSAN M, et al.Succession of the functional microbial communities and the metabolic functions in maize straw composting process[J].Bioresource Technology, 2018, 256:333-341.
[12] 李召, 朱立宁.通过跑窖和降低入窖水分恢复窖泥功能[J].现代食品, 2022, 28(14):99-102.LI Z, ZHU L N.Restore pit mud function by running the cellar and reducing the moisture in the cellar[J].Modern Food, 2022, 28(14):99-102.
[13] 王媚, 邱树毅, 潘玲玲, 等.浓香型白酒容器及窖池发酵糟醅动态因子变化及白酒品质研究[J].中国酿造, 2023, 42(4):53-58.WANG M, QIU S Y, PAN L L, et al.Dynamic factors change of fermented grains and quality of strong-flavor Baijiu fermented in containers and pits[J].China Brewing, 2023, 42(4):53-58.
[14] 李义, 邓杰, 张娟, 等.大曲白酒发酵中不同入窖酸度对糟醅微生物群落结构的影响[J].现代食品科技, 2023, 39(7):68-74.LI Y, DENG J, ZHANG J, et al.Effects of mash acidity on the microbial community structure of fermenting grains during the brewing of Daqu Baijiu[J].Modern Food Science and Technology, 2023, 39(7):68-74.
[15] 王乐, 魏功, 郭逸臻, 等.北方浓香型白酒发酵过程中不同空间层次糟醅理化指标及风味物质的变化[J].中国酿造, 2024, 43(3):63-71.WANG L, WEI G, GUO Y Z, et al.Changes of physicochemical indexes and flavor substances of fermented grains at different spatiallevels during Northern strong-flavor Baijiu fermentation[J].China Brewing, 2024, 43(3):63-71.
[16] 李嵩博, 唐朝臣, 陈峰, 等.中国粒用高粱改良品种的产量和品质性状时空变化[J].中国农业科学, 2018, 51(2):246-256.LI S B, TANG C C, CHEN F, et al.Temporal and spatial changes in yield and quality with grain Sorghum variety improvement in China[J].Scientia Agricultura Sinica, 2018, 51(2):246-256.
[17] 宋瑞滨, 邵泽良, 宋军, 等.多粮浓香型白酒连续超长发酵期生产工艺探讨[J].酿酒, 2020, 47(1):105-112.SONG R B, SHAO Z L, SONG J, et al.Discussion on production technology of multi-grain Luzhou-flavor liquor during continuous and super-long fermentation period[J].Liquor Making, 2020, 47(1):105-112.
[18] 张霞, 王中凯, 郑佳, 等.浓香型白酒发酵过程中酒醅理化指标变化规律研究[J].酿酒科技, 2021(10):53-56.ZHANG X, WANG Z K, ZHENG J, et al.Change rules of physicochemical indexes of fermented grains in the production process of Nongxiang Baijiu[J].Liquor-Making Science &Technology, 2021(10):53-56.
[19] YAN S B, WANG S C, WEI G G, et al.Investigation of the main parameters during the fermentation of Chinese Luzhou-flavour liquor[J].Journal of the Institute of Brewing, 2015, 121(1):145-154.
[20] 杨娜, 周文, 舒学香, 等.四川浓香型白酒糟醅理化因子的产区特征解析[J].酿酒, 2023, 50(6):62-66.YANG N, ZHOU W, SHU X X, et al.Characteristics on physicochemical factors in fermented grains of Luzhou flavor Baijiu from Sichuan different production areas[J].Liquor Making, 2023, 50(6):62-66.
[21] 翟磊, 刘瑞娜, 张京涛, 等.浓香型白酒窖池中细菌群落结构的研究[J].食品与发酵工业, 2023, 49(13):78-84.ZHAI L, LIU R N, ZHANG J T, et al.Bacterial community structure of cellars in strong-flavor Baijiu[J].Food and Fermentation Industries, 2023, 49(13):78-84.
[22] 高江婧, 任聪, 刘国英, 等.浓香型白酒酒醅风味物质和微生物菌群结构随发酵时间的变化规律[J].食品与发酵工业, 2019, 45(20):1-6.GAO J J, REN C, LIU G Y, et al.Dynamic changes of flavor compounds and microbial community in fermented grains of Chinese strong aroma-type Baijiu during fermentation[J].Food and Fermentation Industries, 2019, 45(20):1-6.
[23] FAN J Y, CHEN J, DU G C, et al.Mechanism of lactic acid synthesis during strong-flavor Baijiu fermentation revealed by transcriptomic analysis[J].Food Bioscience, 2024, 58:103780.
[24] 李宜伦. 使用年限对浓香型白酒车间中微生物和糟醅代谢差异的影响[D].无锡:江南大学,2022.LI Y L.The impact of the usage times on the differences of microbiota and metabolic activity in the strong-flavor Baijiu workshop [D].Wuxi:Jiangnan University, 2022.
[25] CORSETTI A, LAVERMICOCCA P, MOREA M, et al.Phenotypic and molecular identification and clustering of lactic acid bacteria and yeasts from wheat (species Triticum durum and Triticum aestivum) sourdoughs of Southern Italy[J].International Journal of Food Microbiology, 2001, 64(1-2):95-104.
[26] QUAN S K, WANG Y, RAN M F, et al.Contrasting the microbial community and non-volatile metabolites involved in ester synthesis between Qing-flavor Daqu and Nong-flavor Daqu[J].Journal of Bioscience and Bioengineering, 2023, 136(3):213-222.
[27] ZHUANSUN W W, XU J, LI Z Q, et al.Dynamic changes in the microbial community, flavour components in Jiupei of a novel Maotai-Luzhou-flavoured liquor under various daqu blending modes and their correlation analysis[J].LWT, 2022, 172:114167.
[28] LI H H, QIN D, WU Z Y, et al.Characterization of key aroma compounds in Chinese Guojing sesame-flavor Baijiu by means of molecular sensory science[J].Food Chemistry, 2019, 284:100-107.
[29] 邱显平, 黄桥, 杨静, 等.浓香型白酒在新、老窖池发酵过程中酒醅微生物群落结构差异分析[J].中国酿造, 2024, 43(1):50-56.QIU X P, HUANG Q, YANG J, et al.Differences of microbial community structure in fermented grains during strong-flavor Baijiu fermentationin new and old pits[J].China Brewing, 2024, 43(1):50-56.
[30] DU R B, WU Q, XU Y.Chinese liquor fermentation:Identification of key flavor-producing Lactobacillus spp.by quantitative profiling with indigenous internal standards[J].Applied and Environmental Microbiology, 2020, 86(12):e00456-20.
[31] MU Y, HUANG J, ZHOU R Q, et al.Bioaugmented Daqu-induced variation in community succession rate strengthens the interaction and metabolic function of microbiota during strong-flavor Baijiu fermentation[J].LWT, 2023, 182:114806.
[32] LI X Y, DU C Y, ZHAO Y F, et al.Differences in microbial communities among different types of Zaopei and their effects on quality and flavor of Baijiu[J].Food Research International, 2024, 197:115224.
[33] XU S S, ZHANG M Z, XU B Y, et al.Microbial communities and flavor formation in the fermentation of Chinese strong-flavor Baijiu produced from old and new Zaopei[J].Food Research International, 2022, 156:111162.
[34] DUAN Z F, WU Y F, ZHANG C N, et al.Comparison of fungal communities and flavour substances in surface and inner layers of fermented grains during stacking fermentation of sauce-flavour Baijiu[J].Journal of Bioscience and Bioengineering, 2023, 136(4):295-303.