中国酿酒葡萄产业近年来发展迅速,其种植面积持续扩大,已成为全球重要的生产国之一[1]。新疆作为中国西北部的核心产区,凭借独特的光热资源与地理优势,酿酒葡萄种植规模与产量长期位居全国前列。然而,该地区广袤的地域特征与复杂的气候条件,如干旱、盐碱化、冬季严寒等生态限制,对产业的可持续发展提出了严峻挑战[2]。因此,负载量对葡萄的生长发育及果实品质形成具有关键调控作用。适宜的负载量能够平衡树体营养分配,优化光合产物的积累与转运,而负载量过高或过低均可能引发树体生理失衡[3-4]。当负载量过大时,植株有限的养分资源被过量果实竞争性消耗,导致叶片光合速率下降、果实发育受阻,具体表现为单粒重降低、可溶性固形物含量减少以及糖酸比下降[5-6]。许多研究表明,适宜的负载量不仅能够调节酿酒葡萄的生长、物候期和产量,还会显著影响其果实的品质特征,如糖分、酸度、单宁、花色苷、白藜芦醇以及香气[7-8]等成分。这些变化不仅对葡萄酒的质量产生作用,还可能影响其颜色、口感等感官特性[9-10]。然而,当前研究大多聚焦于负载量对葡萄生长和果实品质的影响,对于负载量如何作用于葡萄果实中的代谢物以及相关代谢过程、代谢途径的探讨则相对较少。
代谢组学是指对生物体中所有代谢物的分析,并可同时测量给定生物系统中的所有代谢物[11-12]。从生物样本中可检测和筛选出来具有生物学意义和统计学差异的代谢差异物,可识别不同样本之间理化性质的差异,也是品质调控的重要衡量指标[13-14]。因此,代谢组学的研究对提高食品品质具有重要意义[15]。近年来,代谢组学方法已应用于蓝莓[16]、番茄[17]、蔓越莓[18]等果蔬上,但是在酿酒葡萄方面的研究较少。ZHANG等[19],采用超高效液相色谱串联质谱(ultra-performance liquid chromatography-tandem mass spectrometry, UPLC-MS/MS)方法研究了中国5个产地的葡萄和葡萄酒的代谢差异。共计94种花青素和78种非花青素酚类化合物,表明平均高温和平均低温与一些酚类化合物呈正相关,而降水量、相对湿度和大气压力与一些花青素和黄酮醇呈负相关。VANDERWEIDE等[20]通过代谢组学研究证实,在葡萄生育前期实施人工摘叶处理可显著促进果实花色苷与黄酮醇的生物合成,该发现为优化酚类物质积累的栽培技术提供了理论依据。章智钧等[21]通过非靶向代谢组学技术,探讨了不同砧穗组合对‘赤霞珠’葡萄果皮代谢物的影响,揭示了通过影响多个代谢通路的合适的砧穗组合,近而改变葡萄果皮中多酚类物质(如花色苷)及有机酸(如柠檬酸和苹果酸)的合成。这些变化有助于优化葡萄酒的色泽、口感以及抗氧化性能。
本研究利用UHPLC-MS/MS技术的广靶代谢组学,分析了不同负载量下酿酒葡萄‘马瑟兰’果实代谢物质,包括主成分分析和正交偏最小二乘法(orthogonal partial least squares-discriminant analysis,OPLS-DA)等多元统计分析方法,筛选出不同负载量葡萄代谢差产物并对其相关通路进行分析,探究代谢物对葡萄品质的影响,以期筛选出较为合适的负载量。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
品种为新疆焉耆天塞酒庄酿酒葡萄‘马瑟兰’(Marselan),其双亲是赤霞珠(Cabernet Sauvignon)和黑歌海娜(Grenache Noir)。本实验以新疆焉耆回族自治县天塞酒庄葡萄园为实验地(42.03°N,86.23°E),马瑟兰葡萄为实验对象,定植于2016年,南北行向,3.5 m行距,75 cm株距,架势为多主蔓散形,树势基本一致,采取滴灌方式浇灌。该地区属于中温带干旱大陆气候,四季明显,日照充足,且昼夜温差可达到15 ℃。地理位置上,酒庄一侧靠近博斯腾湖,三面被山脉环绕,海拔约1 100米。该地无霜期长达180 d,空气干燥且清新,非常适合酿酒葡萄的生长。
选择生长发育良好、长势大致一致的‘马瑟兰’葡萄植株,每15株为一个负载量处理。新梢密度10条/m,每梢果穗数为1穗/条(T1);新梢密度10条/m,每梢果穗数为2穗/条(T2);新梢密度15条/m,每梢果穗数为1穗/条(T3);新梢密度15条/m,每梢果穗数为2穗/条(T4); 对照组(未经疏穗处理)。每个处理15株葡萄,每个处理3个重复。
于2025年8月23日开始,在焉耆天塞葡萄园实验田内采样,采样时间为上午9~12 h,每个处理随机采收35穗无病害的葡萄并带回实验室。每个处理选择10穗测定‘马瑟兰’外观品质指标,随机从果穗串上、中、下部位选取其中100粒左右,随后将果实放入-80 ℃冰箱中保存。
1.1.2 试剂
甲醇、乙腈、乙酸、异丙醇、超纯水,均为色谱纯,德国CNW Technologies公司。
1.2 仪器与设备
Vanquish超高效液相、Stellar高灵敏度质谱、Heraeus Fresco17离心机,赛默飞世尔科技有限公司;PS-60AL超声仪,深圳市雷德邦电子有限公司;JXFSTPRP-24匀浆机,上海净信科技有限公司;LGJ-10C冷冻干燥机,四环福瑞科仪科技发展有限公司;WZ-1110/ATC手持式阿贝折射糖度计,四环福瑞科仪科技发展有限公司。
1.3 实验方法
1.3.1 成熟指标测定
可溶性固形物:随机取30粒马瑟兰果实,用研钵磨碎混匀,使用手持式阿贝折射糖度计测定。还原糖:用斐林直接滴定法测定葡萄果实中的含量(单位mg/g)。总酸:采用酸碱滴定法测定葡萄中总酸的含量(单位mg/g)。使用pH计测定葡萄果汁pH值。
1.3.2 样品制备
样品经冷冻干燥后,在研磨仪中以60 Hz,30 s进行粉碎。称取25 mg粉末,置于2 mL离心管中,加入1 mL甲醇/水混合溶液(体积比4∶1,含内标)。放入3.2 mm的钢珠2颗,先涡旋振荡30 s,再以45 Hz匀浆4 min,冰水浴中超声波处理5 min;上述匀浆与超声波处理步骤重复3次。之后将样品置于-40 ℃冰箱静置1 h。待样品恢复至4 ℃时,经12 000 r/min离心15 min后,取上清液经0.22 μm滤膜过滤,并转入进样瓶备用。每个样本各取等体积溶液混合制备质控(quality control, QC)样品,用于后续检测。
1.3.3 色谱条件
目标化合物的分离采用Vanquish超高效液相色谱系统(Thermo Fisher Scientific),配备UPLC Kinetex C18色谱柱(2.1 mm×50 mm,2.6 μm)。流动相A为体积分数0.01%乙酸的水溶液,流动相B为乙腈与异丙醇按1∶1配比的混合液。色谱柱恒温保持在25 ℃,自动进样器设定为4 ℃,进样体积2 μL,流速控制在0.3 mL/min。
1.3.4 质谱条件
检测采用Stellar QqLIT质谱仪(Thermo Fisher Scientific),使用加热电喷雾离子化(H-ESI)源,并在PRM模式下进行分析。
2 结果与分析
2.1 不同负载量‘马瑟兰’成熟期理化指标
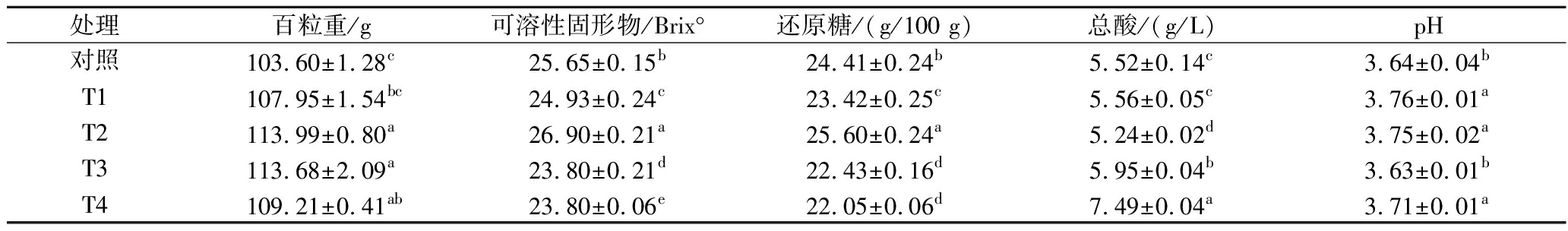
由表1可知,经过疏穗处理的百粒重均显著高于对照组(P<0.05),T2处理的百粒重最高,为113.90 g;各处理之间可溶性固形物均有显著性差异,对照组、T2处理组显著高于其他处理组;还原糖含量与可溶性固形物含量成正比,T2处理组还原糖含量显著高于其他处理组,T4处理组最低,表明适当的疏穗能够提高还原糖的含量;T3、T4处理组的总酸含量相比其他处理组较高,这就导致pH的指标显著低于其他处理组。综上所述,同一地域进行疏穗的葡萄果实成熟度较未疏穗的成熟度更好,对糖酸的影响更大。
表1 不同负载量‘马瑟兰’葡萄成熟期理化指标
Table 1 Physicochemical indicators of ‘Marselan’ grape ripening at different yield levels
处理百粒重/g可溶性固形物/Brix°还原糖/(g/100 g)总酸/(g/L)pH对照103.60±1.28c25.65±0.15b24.41±0.24b5.52±0.14c3.64±0.04bT1107.95±1.54bc24.93±0.24c23.42±0.25c5.56±0.05c3.76±0.01aT2113.99±0.80a26.90±0.21a25.60±0.24a5.24±0.02d3.75±0.02aT3113.68±2.09a23.80±0.21d22.43±0.16d5.95±0.04b3.63±0.01bT4109.21±0.41ab23.80±0.06e22.05±0.06d7.49±0.04a3.71±0.01a
注:不同小写字母表示差异显著(P<0.05)。
2.2 离子色谱图分析
通过总离子流图(图1)可大致看到样本出峰和响应情况。各QC样品的峰面积与保留时间具有较好的一致性,表明质谱平台运行稳定,所得实验数据可靠性较高。
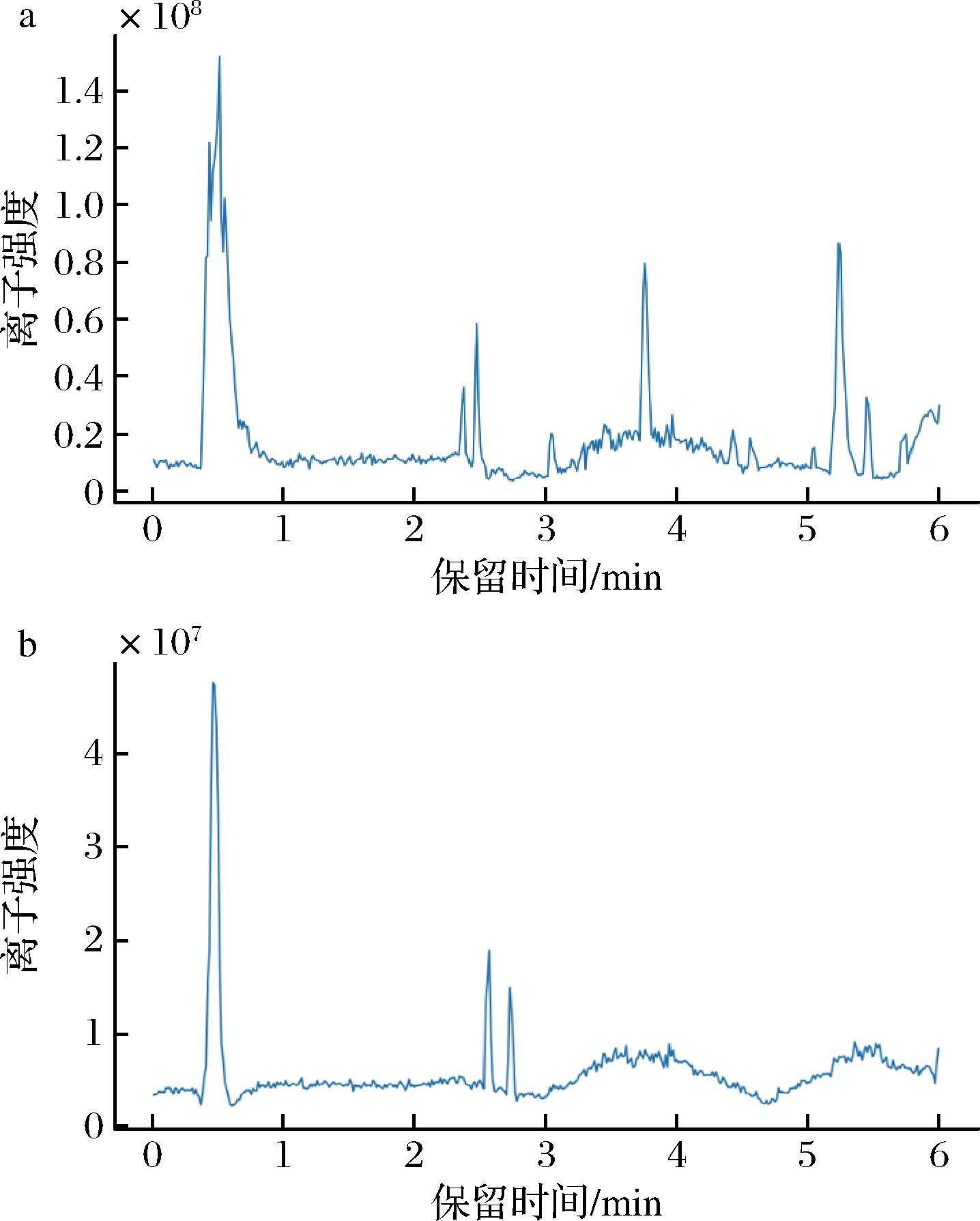
a-正离子模式;b-负离子模式
图1 葡萄QC样品总离子流图
Fig.1 Total ion chromatography of grape QC sample
2.3 不同负载量下葡萄差异代谢物HMDB聚类分析
如图2所示,对“马瑟兰”葡萄果实进行代谢组分析,共检出8大类代谢物5 192种。其中,占比前三代谢物为:莽草酸及苯丙酸类共1 133种(黄酮类、酚酸等)、脂肪酸1 127种(脂肪酸酯、甘油酯等),萜类1 057种(单萜类、甾体等)。其次为生物碱 786种(色氨酸生物碱、酪氨酸生物碱等),聚酮 352种(色酮、芳香聚酮等),氨基酸及短肽298种(氨基酸、二肽等)以及其他类301种。
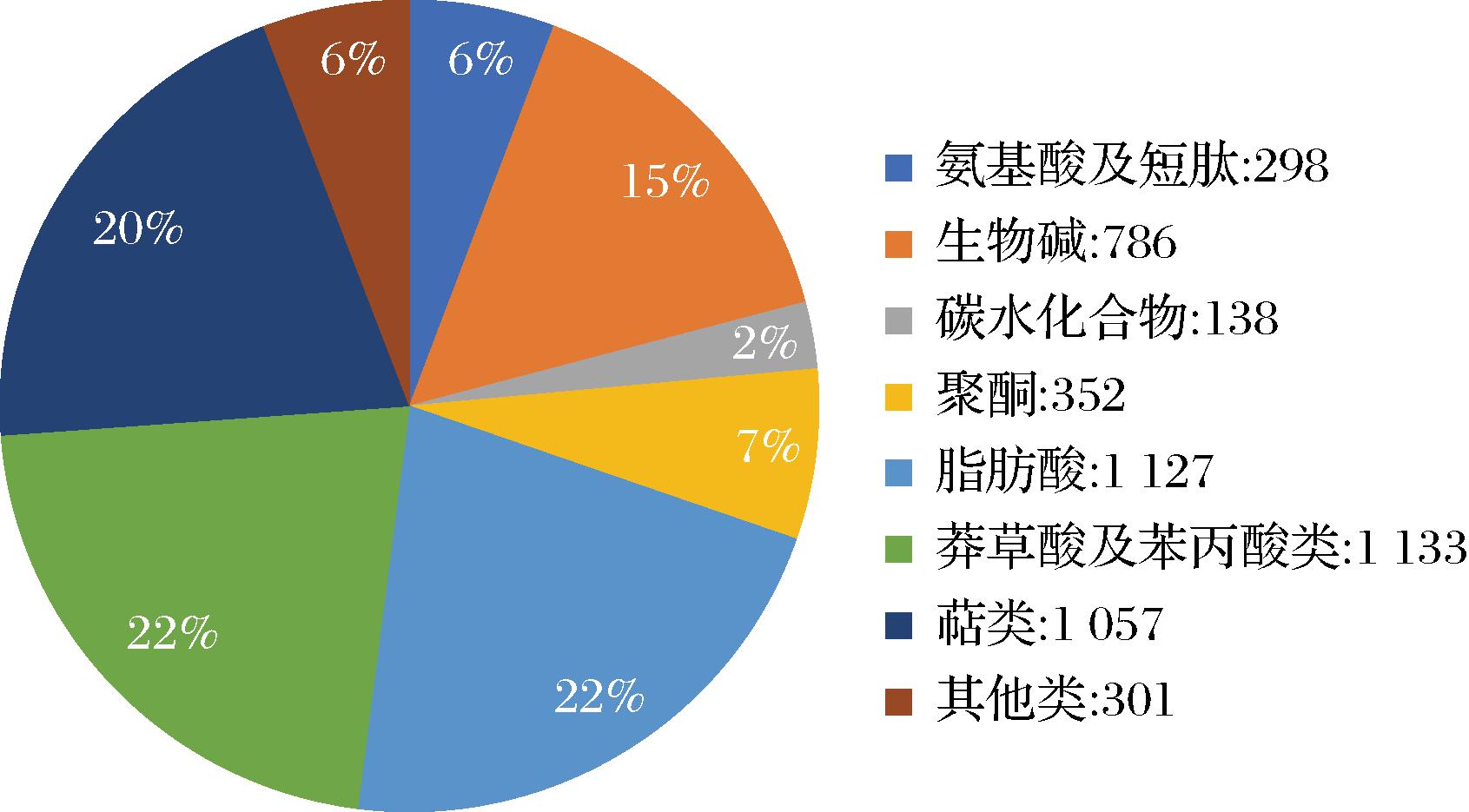
图2 ‘马瑟兰’葡萄果实代谢物分类统计
Fig.2 Metabolite classification statistics for ‘Marselan’ grape fruit
2.4 不同负载量下葡萄差异代谢物韦恩分析
韦恩图能够展示出代谢集间代谢物数量的改变,表明不同负载量实验各阶段诱导的代谢物变化。如图3所示,对照vs T1代谢数目为2 371、对照vs T2代谢数目为761、对照vs T3代谢数目为1 173、对照vs T4代谢数目为1 257。其中有178种代谢物为各比较组的共同差异代谢物,对照vs T1中独有的代谢物有1 054种,对照vs T2中独有的代谢物有123种,对照vs T3中独有的代谢物有218种,对照vs T4中独有的代谢物有304种。表明,不同负载量下的比较组独有代谢物数目呈现出先上升后下降的趋势。
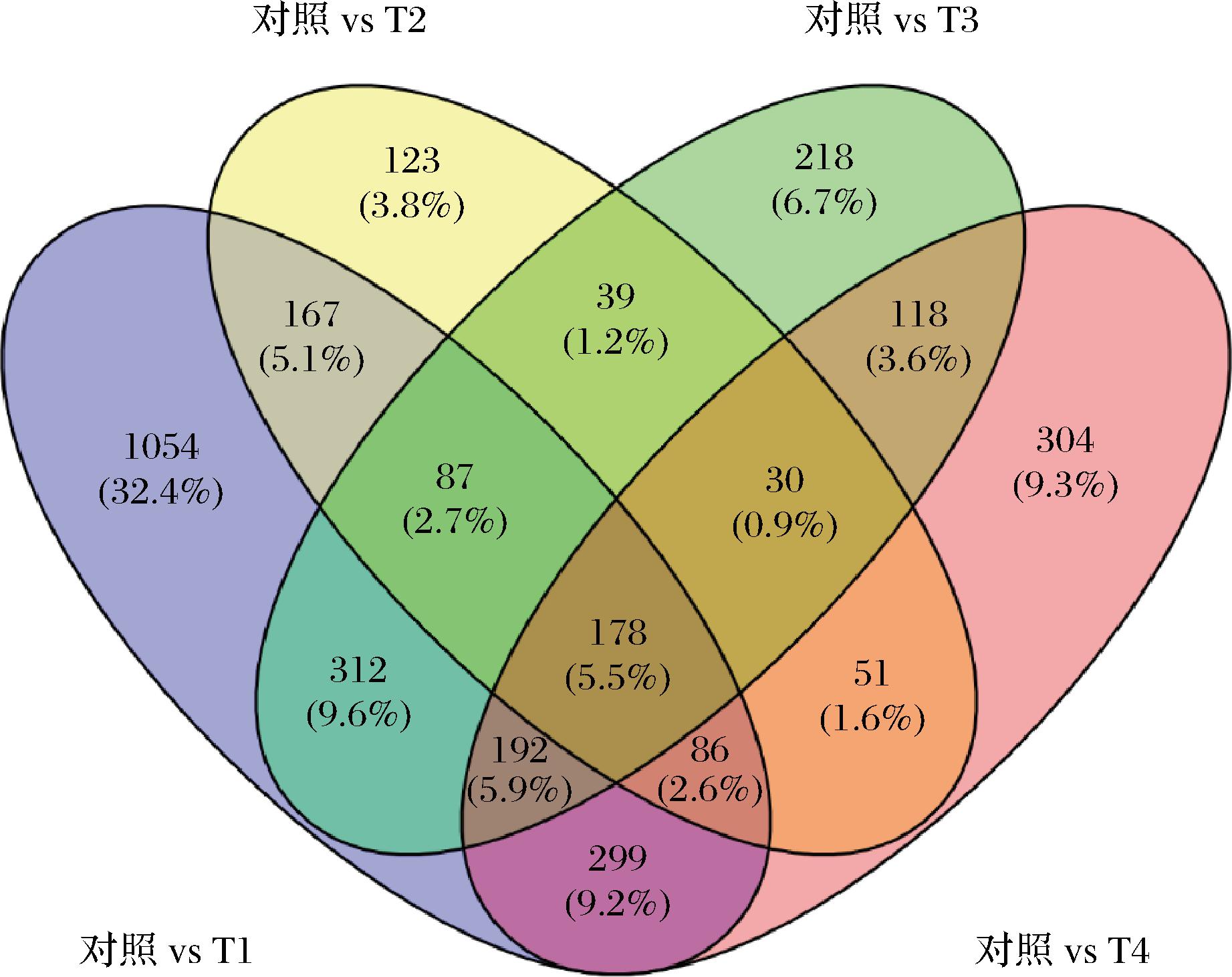
图3 ‘马瑟兰’葡萄果实差异代谢物韦恩图
Fig.3 Wine-type metabolite Venn diagram for ‘Marselan’ grape fruit variants
2.5 不同负载量‘马瑟兰’葡萄的化学型差异
主成分分析是一种将多个相关变量转化为一组线性不相关变量的统计方法。通过对不同负载量葡萄代谢物进行主成分分析(图4-a),结果表明所有样本均位于95%置信区间内。其中,第一主成分(PC1)能够解释数据集48.6%的总变异性,而第二主成分(PC2)解释了21.5%的变异性。因此,前2个主成分解释了数据集总变异性的70.1%,说明对照、T1、T2、T3和T4处理组之间的代谢物表现出显著的差异性。与主成分分析不同,聚类热图能够直观地展示不同负载量葡萄中代谢物表达量的聚类关系。如图4-b所示的树形图中,可以清晰地观察到,与对照组相比,T1、T2、T3和T4处理组的代谢数据呈现出明显的分离趋势,且存在显著差异。
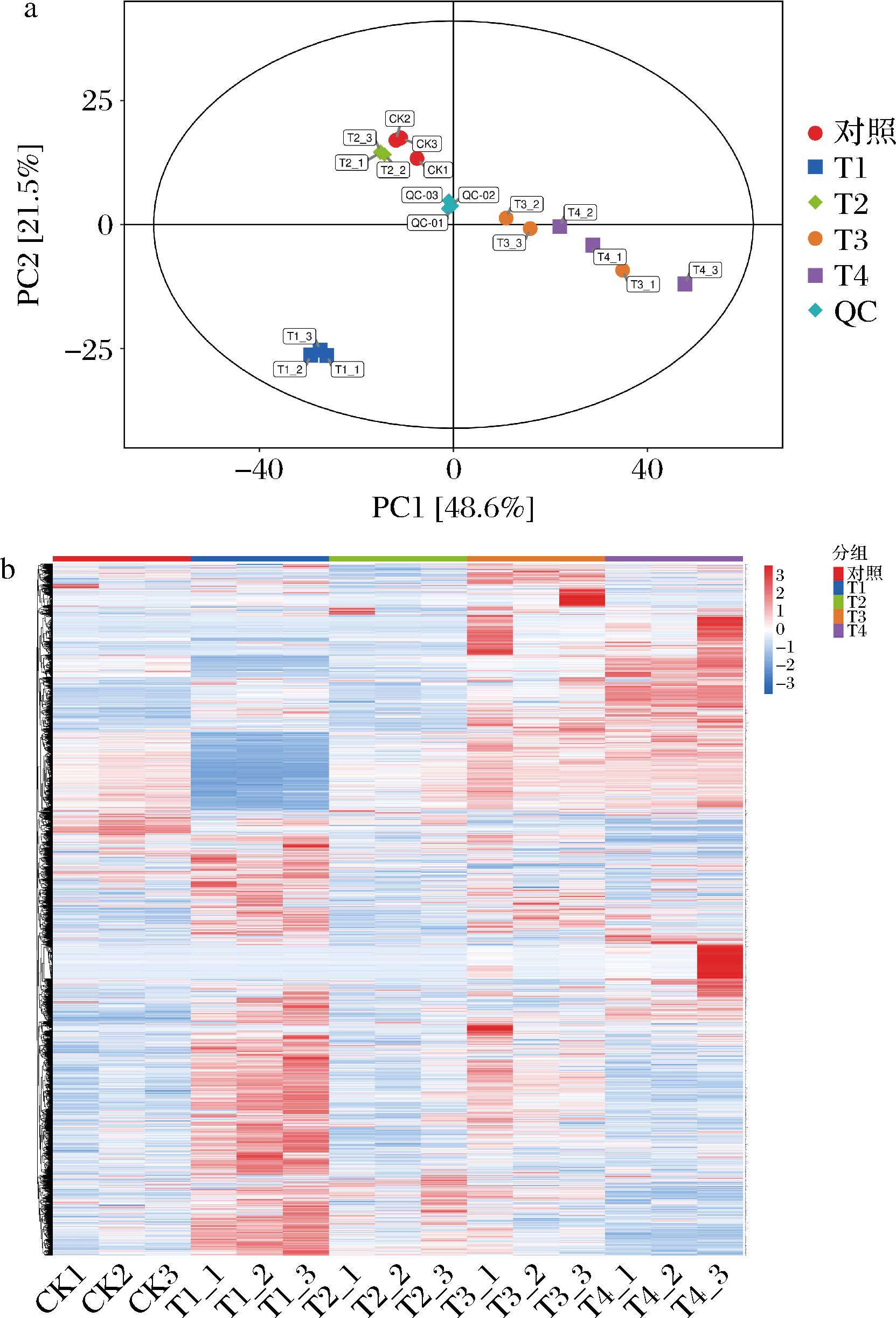
a-主成分分析得分图;b-聚类分析图
图4 不同负载量‘马瑟兰’葡萄的主成分分析得分图和聚类分析图
Fig.4 PCA score plot and cluster analysis diagram of ‘Marselan’ grapes under different load levels
2.6 基于OPLS-DA模型的判定
OPLS-DA能够剔除与分组无关的正交成分,从而将非正交与正交部分分别解析,更有助于精准揭示代谢物组间的差异及其与实验处理之间的关联。采用SIMCA软件对数据第一主成分进行OPLS-DA建模分析。为了解不同负载水平下葡萄的代谢差异,对5种处理条件下的样品进行了全面的代谢组学对比研究。分别为对照vs T1、对照vs T2、对照vs T3、对照vs T4,随后对数据进行建模与置换检验。结果如图5所示,4组样品均分布在置信区间两侧,且各组样本全部在95%置信区间范围内,说明组间代谢物差异显著,判别效果可靠,可用于后续差异代谢物的筛选与分析。
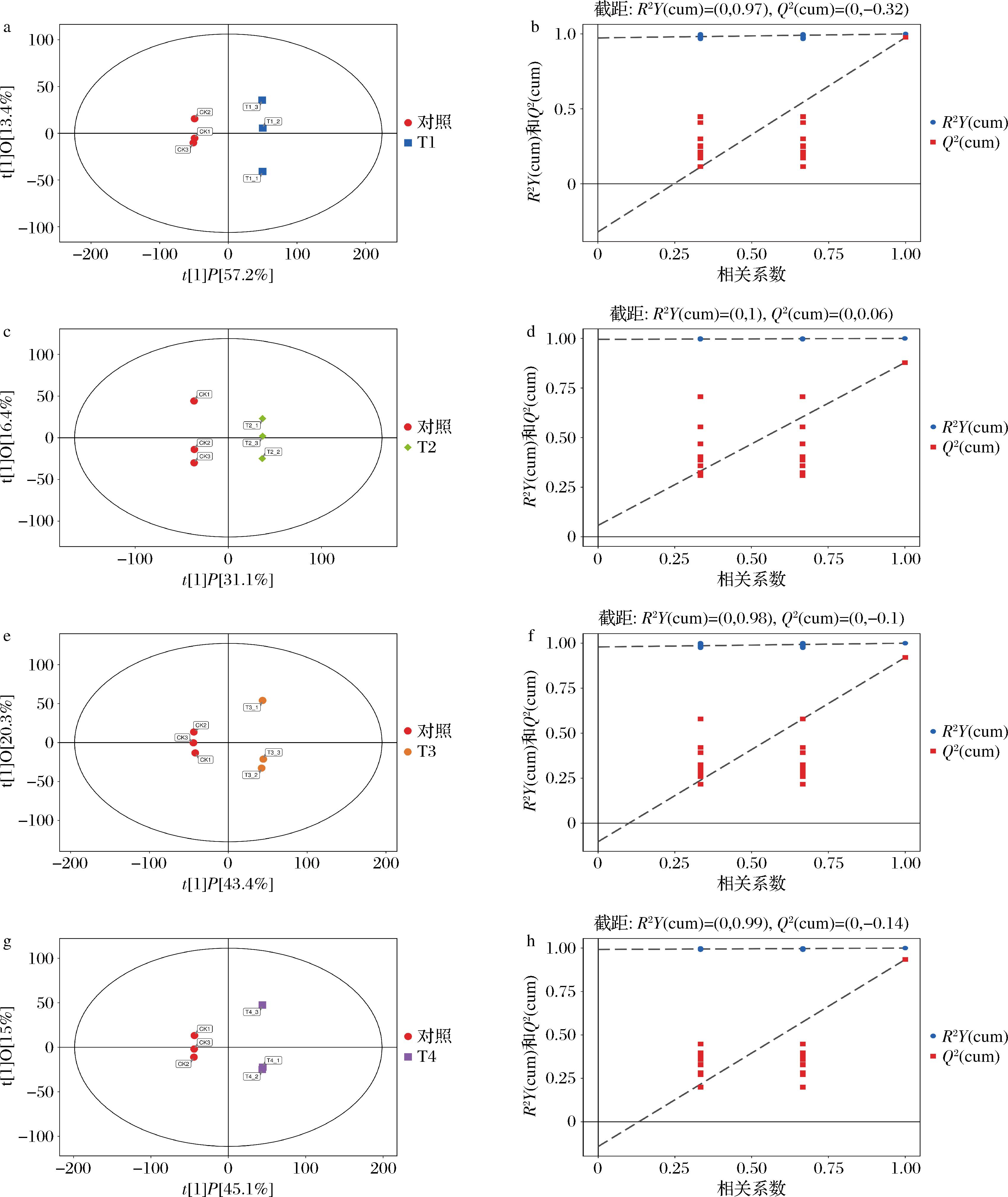
A、C、E、G分别为对照vs T1、对照vs T2、对照vs T3、对照vs T4的OPLS-DA得分图;B、D、F、H分别为对照vs T1、对照vs T2、对照vs T3、对照vs T4的置换检验分析图
图5 不同负载量下‘马瑟兰’葡萄代谢物的OPLS-DA得分图和置换检验分析图
Fig.5 OPLS-DA score plots and replacement test analysis plots of ‘Marselan’ grape metabolites under different loadings
根据置换检验图显示,所有组的R2和Q2值符合预期变化趋势。Q2值低于原始Q2值,说明模型没有出现过拟合现象,且具备很好的稳定性。综上所述,这4组原始模型验证了OPLS-DA模型对样本间差异的准确性和可靠性,可进一步筛选差异代谢物。
2.7 不同负载量的‘马瑟兰’葡萄差异代谢物筛选
根据OPLS-DA模型中第一主成分的变量投影重要性(VIP>1)、学生t检验结果(P<0.05)以及差异倍数>2和差异倍数<1/2设定筛选条件,对分组样品的差异代谢物进行鉴别。图6所示的火山图中,散点大小与VIP值成正比,点越大表示其在模型中的贡献越高;其中,红色点代表显著上调代谢物,蓝色点为显著下调代谢物,灰色点则为无显著差异的代谢物。由火山图可知,与CK相比,T1样品中有1 113种代谢物存在显著差异,其中上调436种,下调677种;T2与CK比较共鉴定180种差异代谢物,包括上调50种,下调130种;T3相较于CK有369种差异代谢物存在显著差异,其中上调265种,下调104种;T4与CK之间共有581种差异代谢物,其中上调467种,下调124种。这表明疏穗处理显著影响(P<0.05)‘马瑟兰’葡萄果实的代谢物积累特征。结果表明,不同负载量‘马瑟兰’葡萄差异代谢物数量呈现出波动趋势,T1和T4处理的‘马瑟兰’葡萄上调差异物较多。通过合理的对‘马瑟兰’留穗的数量的增加,其差异代谢物上调物质出现先增长后降低的趋势,下调物质出现先上升后下降的趋势。
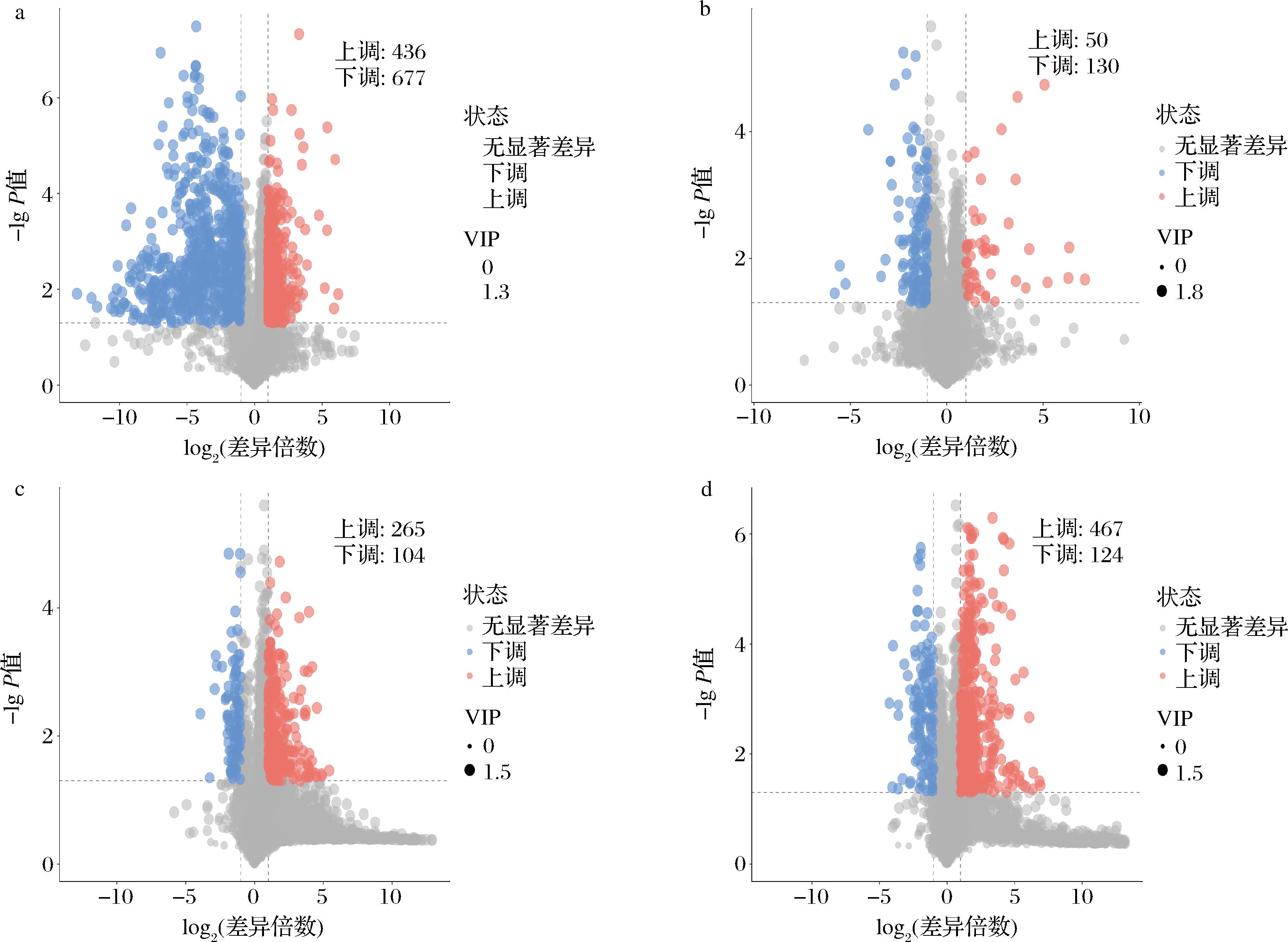
a-T1 vs对照;b-T2 vs对照;c-T3 vs对照;d-T4 vs对照
图6 不同负载量下‘马瑟兰’葡萄差异代谢物火山图
Fig.6 Volcano plots of differential metabolites in ‘Marselan’ grapes under varying load levels
根据OPLS-DA模型VIP>1、P<0.05、差异倍数>2或差异倍数<1/2的标准对4个处理组进行共同显著差异物的筛选[22]。如表2所示,共筛选出9种上调差异代谢物和2种下调差异代谢物。检测出4个处理组共同上调差异物有2种,是虎杖苷和白皮杉醇,都属于茋类。其中虎杖苷在对照vs T1、对照vs T2、对照vs T3和对照vs T4分别上调10.15倍、2.03倍、3.88倍、9.91倍,白皮杉醇在对照vs T1、对照vs T2、对照vs T3和对照vs T4分别上调11.38倍、2.39倍、2.01倍、18.39倍。它们是葡萄中重要的酚类化合物,尤其在酿酒葡萄中,茋类物质对葡萄的质量、风味和酒的口感有重要影响。茋类物质是葡萄酒涩味的主要来源之一,高浓度的茋类会增加葡萄酒的涩感,这是由于茋类分子与蛋白质、酚类化合物及其他分子的结合,造成口感上的收敛[23]。T1、T4处理组中显著上调的物质是异式大黄苷(茋类)分别上调3.35倍、3.88倍。T1、T2处理组中显著上调的物质是表没食子酸酯(黄酮类)分别上调2.47倍、2.72倍、鲁望桔内酯(香豆素类)分别上调62.98倍、33.85倍。T3、T4处理组的显著上调物质是白藜芦醇(茋类)分别上调2.99倍、12.44倍,假荆芥内酯(单萜类)分别上调2.17倍、3.32倍和龙胆三糖(糖类)分别上调2.07倍、3.54倍。T1处理显著降低了芒柄花黄素(异黄酮类)0.17倍和3-O-乙酰基短叶松素(黄酮类)0.30倍,这一变化受到葡萄生长发育阶段和负载量的调控。在疏穗处理下,葡萄的光合产物主要用于糖分的积累,而非酚类化合物的合成。因此,黄酮类物质的合成被抑制,从而导致它们在葡萄中的含量显著减少。
表2 不同负载量‘马瑟兰’葡萄显著差异代谢化合物表
Table 2 Metabolic compounds showing significant differences in ‘Marselan’ grapes under different yield levels

序号代谢物名称变化类型分子式大类组别FC值1虎杖苷上调C20H22O8茋类对照/T1/T2/T3/T410.15、2.03、3.88、9.912白皮杉醇上调C14H12O4茋类对照/T1/T2/T3/T411.38、2.39、2.01、18.393异式大黄苷上调C21H24O9茋类对照/T1/T43.35、3.884表没食子酸酯上调C22H18O11黄酮类对照/T1/T22.47、2.725鲁望桔内酯上调C15H14O4香豆素类对照/T1/T262.98、33.856白藜芦醇上调C14H12O3茋类对照/T3/T42.99、12.447假荆芥内酯上调C10H14O2单萜类对照/T3/T42.17、3.328龙胆三糖上调C18H32O16糖类对照/T3/T42.07、3.549白皮杉醇上调C14H12O4茋类对照/T3/T42.01、18.3910芒柄花黄素下调C16H12O4异黄酮类对照/T10.17113-O-乙酰基短叶松素下调C17H14O6黄酮类对照/T10.30
2.8 不同负载量下‘马瑟兰’葡萄差异代谢物的通路富集
如图7所示,通过KEGG数据库对对照、T1、T2、T3和T4 5个处理差异代谢物质进行KEGG通路富集分析和KEGG通路分类。对照vs T1中主要涉及7大代谢途径,主要是氨基酸代谢(精氨酸和脯氨酸代谢、赖氨酸降解、丙氨酸、天冬氨酸和谷氨酸代谢、酪氨酸代谢、色氨酸代谢、赖氨酸的生物合成和苯丙氨酸、酪氨酸和色氨酸的生物合成),次生代谢物的生物合成(茋类化合物、二苯基庚烷类化合物以及姜辣素的生物合成和植物次生代谢产物的生物合成过程)、碳水化合物代谢(三羧酸循环和丙酮酸代谢)、能量代谢(硫代谢)、氨基酸的生物合成、磷脂代谢和其他氨基酸代谢;对照vs T2中涉及5大代谢途径,主要是次级代谢(类黄酮和黄酮的生物合成、苯丙素类化合物的生物合成),氨基酸代谢(苯丙氨酸、酪氨酸和色氨酸的生物合成以及色氨酸代谢),脂质代谢(角质、木栓质和蜡质的生物合成),核苷酸代谢(DNA和RNA合成)以及辅酶和维生素代谢(叶酸代谢);对照vs T3中涉及6大代谢途径,主要是次级代谢(茋类化合物、二苯基庚烷类化合物和姜辣素的生物合成、黄酮和黄烷醇的生物合成),氨基酸代谢(苯丙氨酸、酪氨酸和色氨酸的生物合成、苯丙氨酸代谢、赖氨酸降解和色氨酸代谢)和核苷酸代谢(DNA和RNA合成)等;对照vs T4中涉及4大代谢途径,主要是次级代谢(茋类化合物、二苯基庚烷类化合物和姜辣素的生物合成,黄酮和黄烷醇的生物合成),脂质代谢(不饱和脂肪酸的生物合成和甘油磷脂代谢),氨基酸代谢(苯丙氨酸、酪氨酸和色氨酸的生物合成和色氨酸代谢),辅酶因子和维生素的代谢(辅酶Q及萜类喹酮类物质的生物合成)。在上述具有显著差异的代谢通路中,对‘马瑟兰’进行疏穗处理,其中影响最显著的代谢通路是黄酮类和类黄酮生物合成、苯丙氨酸、酪氨酸和色氨酸的生物合成和三羧酸循环。
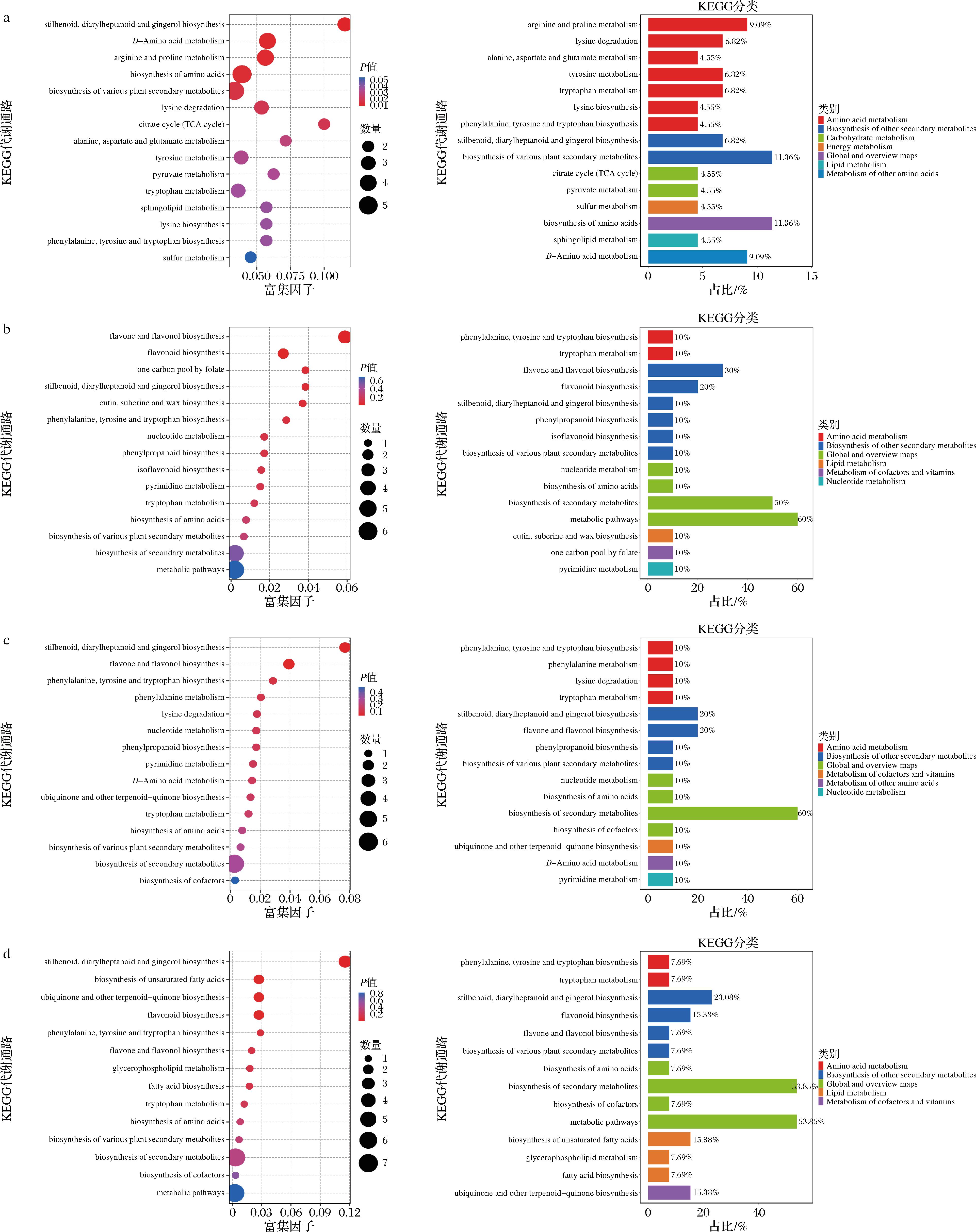
a-对照vs T1;b-对照vs T2;c-对照vs T3;d-对照vs T4
图7 不同负载量下‘马瑟兰’葡萄差异代谢物的KEGG富集分析图和差异代谢物的KEGG富集分类图
Fig.7 KEGG enrichment analysis diagram of differential metabolites in ‘Marselan’ grapes under varying load conditions and KEGG enrichment classification diagram of differential metabolites
注:phenylalanine, tyrosine and tryptophan biosynthesis(苯丙氨酸、酪氨酸和色氨酸生物合成)、phenylalanine metabolism(苯丙氨酸代谢)、tyrosine metabolism(酪氨酸代谢)、tryptophan metabolism(色氨酸代谢)、lysine biosynthesis(赖氨酸生物合成)、lysine degradation(赖氨酸降解)、arginine and proline metabolism(精氨酸和脯氨酸代谢)、alanine, aspartate and glutamate metabolism(丙氨酸、天冬氨酸和谷氨酸代谢)、biosynthesis of amino acids(氨基酸生物合成)、D-amino acid metabolism(D-氨基酸代谢)、metabolism of other amino acids(其他氨基酸代谢)、pyrimidine metabolism(嘧啶代谢)、nucleotide metabolism(核苷酸代谢)、phenylpropanoid biosynthesis(苯丙烷类生物合成)、flavonoid biosynthesis(黄酮类生物合成)、flavone and flavonol biosynthesis(黄酮与黄酮醇生物合成)、isoflavonoid biosynthesis(异黄酮生物合成)、stilbenoid, diarylheptanoid and gingerol biosynthesis(芪类化合物、二芳基庚烷类和姜酚生物合成)、biosynthesis of various plant secondary metabolites(多种植物次生代谢产物生物合成)、biosynthesis of secondary metabolites(次生代谢产物生物合成)、metabolic pathways(代谢通路)、biosynthesis of cofactors(辅因子生物合成)、ubiquinone and other terpenoid-quinone biosynthesis(泛醌及其他萜醌类生物合成)、one carbon pool by folate(叶酸介导的一碳代谢库)、cutin, suberine and wax biosynthesis(角质素、木栓质和蜡生物合成)、biosynthesis of unsaturated fatty acids(不饱和脂肪酸生物合成)、fatty acid biosynthesis(脂肪酸生物合成)、glycerophospholipid metabolism(甘油磷脂代谢)、sphingolipid metabolism(鞘脂代谢)、citrate cycle (TCA cycle)(柠檬酸循环(TCA循环/三羧酸循环))、pyruvate metabolism(丙酮酸代谢)、sulfur metabolism(硫代谢)。
本实验中虎杖苷、白皮杉醇、异式大黄苷等茋类含量较高,这与苯丙氨酸代谢通路密切相关,苯丙氨酸作为植物体内的重要氨基酸,是许多次生代谢物(如黄酮、花青素、茋类等)的前体。虎杖苷和白藜芦醇都源自苯丙氨酸代谢通路。在葡萄中,苯丙氨酸通过苯丙氨酸解氨酶等关键酶催化转化为不同的黄酮类化合物[24]。白皮杉醇和异式大黄苷是通过苯丙氨酸进一步转化而来的化合物,参与黄酮醇类的合成,对葡萄的抗氧化性、抗病虫害等有显著影响。通过苯丙氨酸代谢通路,这些茋类化合物的合成也会受到酪氨酸的影响,尤其是在葡萄成熟期,酪氨酸的转化在苯丙氨酸、黄酮类物质的合成中起着重要作用。虽然这些茋类化合物本身并非三羧酸循环的直接产物,但其合成过程与该循环密切相关。三羧酸循环作为细胞内关键的能量代谢途径,为酚类化合物与黄酮类物质的合成提供了所需的ATP与其他能量中间体。以白藜芦醇和白皮杉醇为例,其生物合成需大量能量,主要来自三羧酸循环所生成[25]。通过三羧酸循环,葡萄植物能够生成供酚酸类及黄酮类物质合成所需的高能磷酸键,从而促进这些次级代谢物的积累与转化。
3 结论与讨论
本研究旨在探讨不同负载量对‘马瑟兰’葡萄差异代谢物的影响,采用UPLC-MS/MS广靶向代谢组学技术,鉴定了8大类5 192种代谢物。通过OPLS-DA得分图和模型概览验证了模型的稳定性和可靠性,依据VIP>1、P<0.05、FC>2及FC<1/2的标准筛选出显著差异代谢物,共识别出11种显著差异代谢物,包括9种上调物质和2种下调物质。对这些代谢物进行代谢通路分析后,发现茋类、香豆素类和糖类物质主要表现为上调,而黄酮类物质则以下调为主。表明,经过疏穗处理的葡萄能够促进黄酮类和类黄酮生物合成,苯丙氨酸、酪氨酸和色氨酸的生物合成和三羧酸循环,从而改善‘马瑟兰’葡萄的品质。
结合疏穗处理后的‘马瑟兰’葡萄理化性质,结果表明T2和T3处理的百粒重较大,提示这些处理下葡萄的生长较为充分,可为次生代谢物的合成提供了更多的营养物质,从而促进茋类化合物的积累,茋类能够影响葡萄的风味和葡萄酒的口感。许多茋类化合物具有抗氧化、抗炎、抗菌等作用,这些特性有助于葡萄酒的口感平衡和口腔回味[26]。糖分的增加为茋类物质的合成提供了足够的能量。然而,高糖分也可能造成糖类与黄酮类物质合成的竞争,导致芒柄花黄素和3-O-乙酰基短叶松素的合成受到影响。苯丙氨酸代谢途径在T2和T3处理中可能更多地将中间产物转化为糖分,从而抑制黄酮类物质的合成。T2处理下葡萄的可溶性固形物含量最高,表明糖分积累较为显著。白皮杉醇和虎杖苷属于黄酮类物质。白皮杉醇为黄酮醇类化合物,而虎杖苷则为抗氧化相关的类白藜芦醇化合物。它们的合成途径依赖于查尔酮合酶、查尔酮异构酶和二氢黄酮醇还原酶等关键酶的催化[27]。糖分的积累对黄酮类物质的合成具有重要作用,葡萄中的糖类(如可溶性固形物和还原糖)为黄酮合成通路提供了能量和底物支持。同时T4处理下总酸含量较高,酸度的增加可能抑制了某些黄酮类物质(如芒柄花黄素和3-O-乙酰基短叶松素)的合成。
本实验成功鉴定出了‘马瑟兰’葡萄4种疏穗处理的特征标志物,揭示了疏穗对‘马瑟兰’葡萄影响的代谢机制,不仅对生长发育和果实大小进行研究,还深入到了果实的代谢物组成与积累规律,尤其在糖、酸、酚类、黄酮类等成分的变化上,为酿酒葡萄负载量的选择提供理论依据,为未来酿酒葡萄负载量控制对代谢物积累的研究提供了新视角。
[1] 赵向豪, 刘亚茹, 孙慧.新疆葡萄酒产业集群发展策略研究[J].中国酿造, 2025, 44(1):298-302.ZHAO X H, LIU Y R, SUN H.Study on the development strategy of Xinjiang wine industry cluster[J].China Brewing, 2025, 44(1):298-302.
[2] 王敏, 韩守安, 刘旭鹏, 等.新疆葡萄产业发展现状分析[J].新疆农业科学, 2024, 61(S1):127-130.WANG M, HAN S A, LIU X P, et al.The current development status of the grape industry in Xinjiang[J].Xinjiang Agricultural Sciences, 2024, 61(S1):127-130.
[3] 葛谦, 张媛珂, 闫玥, 等.不同采收期下负载量对赤霞珠葡萄及葡萄酒品质的影响[J].食品科学, 2025, 46(3):128-137.GE Q, ZHANG Y K, YAN Y, et al.Effect of crop load on the quality of Cabernet Sauvignon grapes and wines at different harvest times[J].Food Science, 2025, 46(3):128-137.
[4] 张峰玮, 张军翔.负载量对赤霞珠葡萄酒挥发性物质的影响[J].江苏农业科学, 2018, 46(1):146-150.ZHANG F W, ZHANG J.X.Effect of crop load on the volatile compounds of Cabernet Sauvignon wine[J].Jiangsu Agricultural Sciences, 2018, 46(1):146-150.
[5] 李秀杰, 李晨, 翟衡, 等.不同负载量对夏黑葡萄果实品质的影响[J].山东农业科学, 2015, 47(8):42-45.LI X J, LI C, ZHAI H, et al.Effects of different loading amounts on fruit quality of Summer Black grape[J].Shandong Agricultural Sciences, 2015, 47(8):42-45.
[6] 张峰玮.“厂”字整形下不同负载量对葡萄果实和葡萄酒品质的影响[D].银川:宁夏大学,2016.ZHANG F.W.Influence of different crop loads under the “Factory” shape on grape fruit and wine quality[D].Yinchuan:Ningxia University, 2016.
[7] 王明洁, 鲁会玲, 肖丽珍, 等.负载量对酿酒葡萄公酿1号果实品质的影响[J].中国果树, 2023(11):99-103.WANG M J, LU H L, XIAO L Z, et al.Effect of loading capacity on fruit quality of wine grape ‘Gongniang 1’[J].China Fruits, 2023(11):99-103.
[8] 宫磊, 王珊, 苏玲, 等.不同负载量及花穗整形方式对‘户太八号’葡萄果实品质的影响[J].中国果树, 2020(2):81-83.GONG L, WANG S, SU L, et al.Effects of different fruit loads and different ways of flower thinning on fruit quality of ‘Hutai 8’ grape[J].China Fruits, 2020(2):81-83.
[9] 冯学梅, 梁玉文, 李阿波, 等.宁夏贺兰山东麓酿酒葡萄产量控制对果实品质及葡萄酒质量的影响[J].宁夏农林科技, 2020, 61(10):6-9.FENG X M, LIANG Y W, LI A B, et al.Effects of grape yield control on fruit quality and wine quality in eastern foothills of Helan Mountain in Ningxia[J].Ningxia Journal of Agriculture and Forestry Science and Technology, 2020, 61(10):6-9.
[10] 孙浈育, 刘万好, 肖慧琳, 等.负载量对‘马瑟兰’果实及葡萄酒品质的影响[J].中外葡萄与葡萄酒, 2022(2):60-64.SUN Z Y, LIU W H, XIAO H L, et al.Effects of crop load on fruit and wine quality of’Marselan’Grapevine[J].Sino-Overseas Grapevine &Wine, 2022(2):60-64.
[11] CAI W C, WANG Y R, HOU Q C, et al.Rice varieties affect bacterial diversity, flavor, and metabolites of Zha-chili[J].Food Research International, 2021, 147:110556.
[12] HE C L, PENG B, ZHANG D S, et al.Comparative analysis of strong-flavor Baijiu and brandy:Volatile and nonvolatile metabolic compounds identified using non-targeted metabolomics[J].European Food Research and Technology, 2025, 251(6):1225-1239.
[13] YANG B H, HE S, LIU Y, et al.Transcriptomics integrated with metabolomics reveals the effect of regulated deficit irrigation on anthocyanin biosynthesis in Cabernet Sauvignon grape berries[J].Food Chemistry, 2020, 314:126170.
[14] LIANG L, LI Y H, MAO X J, et al.Metabolomics applications for plant-based foods origin tracing, cultivars identification and processing:Feasibility and future aspects[J].Food Chemistry, 2024, 449:139227.
[15] SAVOI S, SANTIAGO A, ORDU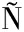 A L, et al.Transcriptomic and metabolomic integration as a resource in grapevine to study fruit metabolite quality traits[J].Frontiers in Plant Science, 2022, 13:937927.
A L, et al.Transcriptomic and metabolomic integration as a resource in grapevine to study fruit metabolite quality traits[J].Frontiers in Plant Science, 2022, 13:937927.
[16] LI Y P, LI H F, WANG S Y, et al.Metabolomic and transcriptomic analyses of the flavonoid biosynthetic pathway in blueberry (Vaccinium spp.)[J].Frontiers in Plant Science, 2023, 14:1082245.
[17] CAI W Q, JIANG P F, LIU Y, et al.Distinct changes of taste quality and metabolite profile in different tomato varieties revealed by LC-MS metabolomics[J].Food Chemistry, 2024, 442:138456.
[18] WANG Y F, VORSA N, DE B HARRINGTON P, et al.Nontargeted metabolomic study on variation of phenolics in different cranberry cultivars using UPLC-IM-HRMS[J].Journal of Agricultural and Food Chemistry, 2018, 66(46):12206-12216.
[19] ZHANG L, WANG Z X, ZHANG C, et al.Metabolomics analysis based on UHPLC-QqQ-MS/MS to discriminate grapes and wines from different geographical origins and climatological characteristics[J].Food Chemistry, 2024, 22:101396.
[20] VANDERWEIDE J, MEDINA-MEZA I G, FRIONI T, et al.Enhancement of fruit technological maturity and alteration of the flavonoid metabolomic profile in merlot (Vitis vinifera L.) by early mechanical leaf removal[J].Journal of Agricultural and Food Chemistry, 2018, 66(37):9839-9849.
[21] 章智钧, 刘怀锋, 孙军利, 等.非靶向代谢组学对赤霞珠果皮不同砧穗组合差异代谢物的分析[J].食品科学, 2020, 41(24):22-30.ZHANG Z J, LIU H F, SUN J L, et al.Analysis of differential metabolites in Cabernet Sauvignon skins from different rootstock-scion combinations by non-targeted metabolomics[J].Food Science, 2020, 41(24):22-30.
[22] 范蕊, 王文文, 王腾斌, 等.基于非靶向代谢组学分析不同发酵时期新疆沙棘酵素代谢产物的差异[J].食品与发酵工业, 2025, 51(10):167-176.FAN R, WANG W W, WANG T B, et al.Difference of enzyme metabolites in Xinjiang seabuckthorn during different fermentation periods based on non-targeted metabolomics[J].Food and Fermentation Industries, 2025, 51(10):167-176.
[23] MCRAE J M, KENNEDY J A.Wine and grape tannin interactions with salivary proteins and their impact on astringency:A review of current research[J].Molecules, 2011, 16(3):2348-2364.
[24] MARANT B, CROUZET J, FLOURAT A L, et al.Key-enzymes involved in the biosynthesis of resveratrol-based stilbenes in Vitis spp.A review[J].Phytochemistry Reviews, 2025, 24(1):461-481.
[25] MU H Y, LI Y, YUAN L, et al.MYB30 and MYB14 form a repressor-activator module with WRKY8 that controls stilbene biosynthesis in grapevine[J].The Plant Cell, 2023, 35(1):552-573.
[26] HASAN M, BAE H.An overview of stress-induced resveratrol synthesis in grapes:Perspectives for resveratrol-enriched grape products[J].Molecules, 2017, 22(2):294.
[27] LI C Y, CHEN L F, FAN Q, et al.Weighted gene co-expression network analysis to explore hub genes of resveratrol biosynthesis in exocarp and mesocarp of ‘summer black’ grape[J].Plants, 2023, 12(3):578.