乳酸菌(lactic acid bacteria,LAB)是一类能够通过发酵碳水化合物产生大量乳酸的革兰氏阳性细菌的统称,在食品工业中具有重要的应用价值[1]。LAB作为传统发酵食品的发酵剂在食品发酵过程中发挥着关键作用。在发酵过程中,LAB代谢产生有机酸、氨基酸、小分子肽和其他风味化合物,并产生过氧化物和细菌素以及其他天然抗菌物质,赋予发酵产品特殊的风味和营养价值。SINGRACHA等[2]研究发现LAB与酵母协同发酵可以增强酱油醪中挥发性风味物质合成。李秀娟等[3]研究证实,将从酱油发酵酱醅中筛选出的戊糖片球菌(Pediococcus pentosaceus)回添至低盐固态酱油发酵体系,可显著提升成品酱油的氨基酸态氮含量、总氮含量以及香气成分总数。此外,PORTO等[4]研究也证明了P.pentosaceus在发酵应用(如花椒素)中具有抑制杂菌污染及作为益生菌补充剂的功能。发酵食品通过调节肠道菌群平衡、维持生理稳态以及清除活性氧等机制在预防多种疾病方面表现出独特优势[5]。
在发酵食品体系中,NaCl是常用的食品添加剂之一,对酱料、泡菜等产品的质地和风味形成具有重要影响。研究表明在这些发酵产品中的NaCl高浓度会引起对微生物的盐胁迫,不仅影响微生物生长动力学,还会改变产品特性[6]。在长期的进化过程中,LAB进化出了压力感应系统和压力防御系统,能够承受恶劣的条件和环境突变,能够在不利环境条件下维持生存[7]。这些细菌以特定的方式对压力做出反应,这些适应机制可能导致菌株表型和生理特性的改变,进而影响其抗氧化能力等关键功能特性。LUO等[8]的研究发现,240 mg/mL NaCl溶液引发的渗透胁迫抑制细菌生长和发酵活性,并导致菌株结构和功能特性的显著变化。
在前期的研究中,从120 mg/mL NaCl溶液的传统古法酱油中分离得到戊糖片球菌RP-24。该菌展现出优异的耐盐性与抗菌活性,具备作为功能性食品发酵剂的潜力。然而现有研究表明,盐浓度变化会显著影响戊糖片球菌的生理状态,进而影响发酵效率及益生特性[9]。基于上述研究背景,本研究拟以P.pentosaceus RP-24为研究对象,系统评估其在不同NaCl浓度环境下,细胞生理特性的变化情况以及细胞表面结构的改变。通过对P.pentosaceus RP-24的生长性能、表观形貌、DPPH自由基清除能力、ABTS阳离子自由基清除能力、表面疏水性、自聚集能力、亚硝酸盐降解能力的研究,进一步探究盐浓度对P.pentosaceus生长的影响机制。本研究为了解P.pentosaceus在盐胁迫环境的生理适应机制和功能性低盐发酵食品的研发提供理论基础。
1 材料与方法
1.1 材料和试剂
古法酿制酱油(120 mg/mL NaCl浓度、未灭菌的生酱油),广西壮族自治区钦州市钦南区菜市场;MRS肉汤、MRS琼脂,青岛高科技工业园海博生物有限公司;牛胆盐,国药集团化学试剂有限公司;FeSO4,山东科源生化有限公司;增强革兰氏染色液、ABTS、DPPH,上海源叶生物科技有限公司;NaCl,上海麦克林生化科技有限公司;二甲苯,四川西陇科学有限公司。其他试剂均为国产分析纯。
1.2 仪器与设备
SJ-CJ-2FD超净工作台,苏洁医疗器械江苏有限公司;SPX-2508SH-II生化培养箱,上海新苗医疗器械制造有限公司;Synergy H1多功能微孔板检测仪,BioTek Instruments公司;BSA223S电子分析天平,赛多利斯科学仪器北京有限公司;IS-RSDA小型台式恒温振荡器,苏州捷美电子有限公司;Sigma 360扫描电镜,德国卡尔·蔡司股份公司。
1.3 实验方法
1.3.1 LAB培养和生长量的测定
参考张甜等[10]的实验方法并稍作调整,将纯菌株P.pentosaceus RP-24菌株以1%的接种量分别转接至NaCl质量浓度为0、40、80 mg/mL 和120 mg/mL 的MRS液体培养基中,37 ℃培养14 h。随后,以2 h为时间间隔连续取样,在600 nm波长处测定菌液吸光度值。由于菌株在含有120 mg/mL NaCl的培养基中培养14 h后的OD600值未超过0.2,生长缓慢,因此在后续实验分析中不使用该浓度。
1.3.2 产酸性
菌株活化后离心得到菌体,将菌体用MRS液体培养基重悬,调节菌悬液在600 nm处的光密度至1.0。以2%的接种量依次接种至NaCl质量浓度为0、40、80 mg/mL的MRS液体培养基中。37 ℃培养,以2 h为时间间隔,在14 h内连续测定菌液pH以评估其在不同质量浓度NaCl条件下的产酸情况。
1.3.3 亚硝酸盐降解能力
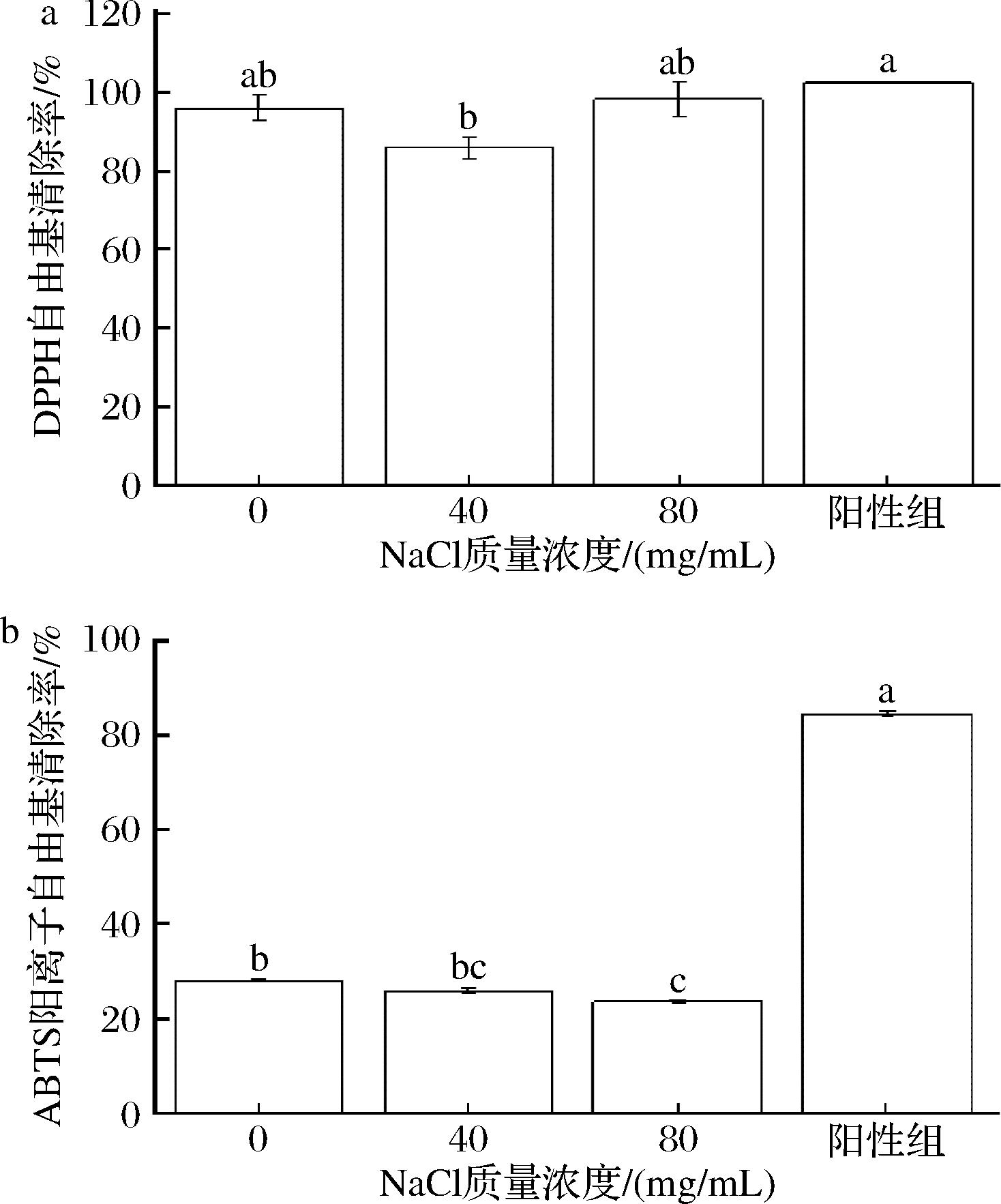
参考丁娟芳等[11]的实验方法并稍作调整,菌株活化后离心收集菌体,将菌体重悬于MRS液体培养基中,调节至OD600=1.0。以2%接种量分别接种至含有250 mg/L NaNO2的MRS液体培养基中,培养基NaCl质量浓度分别为0、40 mg/mL和80 mg/mL。于37 ℃条件下培养24 h,测定培养前后培养液中的亚硝酸盐含量。亚硝酸盐含量的测定采用GB/T 5009.33—2025《食品安全国家标准 食品中亚硝酸盐与硝酸盐的测定》中盐酸萘乙二胺分光光度法。菌株对亚硝酸盐降解率如公式(1)所示:
亚硝酸盐降解率![]()
(1)
式中:A0,初始亚硝酸盐质量浓度,mg/L;A1,培养后亚硝酸盐质量浓度,mg/L。
1.3.4 菌株表观形态的测定
制备扫描电镜样品,将菌株分别接种于NaCl质量浓度为0、40 mg/mL和80 mg/mL的MRS培养基中,于37 ℃条件下培养2 h。取2 mL不同NaCl浓度培养的菌液离心,弃去上清液,用PBS(pH 7.4)洗涤菌体2次沿管壁缓慢加入4 ℃预冷的2.5%(体积分数)戊二醛固定液,然后于4 ℃冰箱保存过夜。对样品喷金后在高真空条件下,通过电子束扫描样品表面,收集二次电子信号,形成样品表面的微观形貌图像。
1.3.5 体外抗氧化活性的测定
1.3.5.1 制备LAB发酵上清液待测液
将菌株以1%的接种量分别接种于NaCl质量浓度为0、40、80 mg/mL的MRS培养基中,37 ℃培养24 h。培养结束后,将样品在 4 ℃、8 000 r/min离心10 min,收集发酵上清液作为待测液。以1 mg/mL抗坏血酸为阳性对照。
1.3.5.2 DPPH自由基清除率的测定
参考MU等[12]的实验方法并稍作调整,将1 mL待测液和1 mL DPPH溶液(0.2 mmol/L无水乙醇),室温下避光反应30 min,4 ℃、8 000 r/min离心10 min,收集上清液,于517 nm处测定吸光度的变化。DPPH自由基清除率的计算如公式(2)所示:
DPPH自由基清除率![]()
(2)
式中:Ai,1 mL DPPH溶液和1 mL待测液混合液的吸光度;Aj,1 mL乙醇和1 mL待测液混合液的吸光度;Ac,1 mL DPPH溶液和1 mL生理盐水混合液的吸光度。
1.3.5.3 ABTS阳离子自由基清除的测定
参考张乃珣等[13]的方法并稍作调整,将ABTS阳离子自由基溶液(7 mmol/L)与过硫酸钾溶液(2.45 mmol/L)混合制成ABTS阳离子自由基清储备液,在黑暗中放置14 h后将该溶液用无水乙醇稀释至OD734=0.7制成ABTS阳离子自由基工作液。将0.15 mL待测液与2 mL ABTS阳离子自由基工作液混匀,室温避光反应6 min后,4 ℃、8 000 r/min离心10 min,收集上清液,在734 nm处测定吸光度。ABTS阳离子自由基清除率的计算如公式(3)所示:
ABTS阳离子自由基清除率![]()
(3)
式中:As,0.15 mL待测液和2 mL ABTS阳离子自由基工作液混合液的吸光度;Ab,0.15 mL蒸馏水和2 mL ABTS阳离子自由基工作液混合液的吸光度。
1.3.6 自聚集性、表面疏水性的测定
1.3.6.1 待测溶液的预处理
参考ZHAO等[14]的方法并稍作修改,将菌株以1%的接种量分别接种于NaCl质量浓度为0、40、80 mg/mL 的MRS培养基,37 ℃培养24 h后,5 000 r/min离心10 min,弃去上清液,菌体用磷酸盐缓冲液(pH 7.2)洗涤2次后重悬于缓冲液,并将OD600调整到0.5,涡旋混合10 s后获得待测溶液。
1.3.6.2 细胞自聚集性的测定
取待测溶液分别静置2 h和4 h,随后在600 nm波长下测定其吸光度,分别记为At1和At2。菌株的自聚集率的计算如公式(4)所示:
自聚集率![]()
(4)
式中:At代表At1或At2。At1,静置2 h时重悬液的吸光度;At2,静置4 h时重悬液的吸光度;A0,静置前重悬液的吸光度。
1.3.6.3 细胞疏水性的测定
将待测溶液与二甲苯以1∶1的体积比例混合,涡旋振荡20 min,随后静置30 min使其充分分层。在600 nm波长下测定水相溶液的吸光度,记为Ai。菌株疏水率的计算如公式(5)所示:
细胞疏水率![]()
(5)
式中:Ai,水相溶液吸光度;A0,混合前重悬液的吸光度。
1.3.7 数据处理
所有实验均进行3次重复,结果以“平均值±标准差”表示。采用SPSS 26软件对结果进行单因素方差分析。显著性检验采用Tukey检验,显著性差异设为P<0.05。数据分析使用Origin 2021b完成。
2 结果与分析
2.1 P.pentosaceus RP-24的生长情况
如表1所示,在NaCl质量浓度为0 mg/mL和40 mg/mL时,P.pentosaceus RP-24的生长呈现出典型的LAB生长特征:在接种后的4 h内微生物生长缓慢,4 h后进入对数生长期,生长速度明显加快,随后在12~14 h达到稳定期,吸光度值趋于平稳。80 mg/mL NaCl菌株RP-24培养14 h后的生长量显著小于对照组(P<0.05),但随着时间的变化,菌株RP-24呈现缓慢生长的趋势(P<0.05)。这一趋势与WU等[15]的研究一致,与对照组相比,40 mg/mL 和80 mg/mL NaCl浓度下降低了副干酪乳酪杆菌LN-1的最大生物量。120 mg/mL NaCl培养下的菌株在14 h后的OD600值为0.153,显著低于其他样品(P<0.05),表明在120 mg/mL NaCl显著影响P.pentosaceus RP-24的生长。以上现象可能是由于在低盐度条件下,P.pentosaceus RP-24可以通过调节细胞 内的渗透压平衡来适应中等盐度环境,但在高盐条件下这种调节机制达到极限从而生长缓慢。ZAMFIR等[16]研究发现魏斯氏菌38.2在80、90、100 mg/mL NaCl质量浓度条件下菌液的OD600值分别为1.5、0.7和0.6,说明LAB随NaCl浓度增大而生长缓慢。基于以上发现,后续实验将重点研究P.pentosaceus RP-24在0、40、80 mg/mL NaCl质量浓度条件下的生理特性变化以评估菌株特性的变化。
表1 不同NaCl浓度下戊糖片球菌RP-24生长情况
Table 1 Growth of P.pentosaceus RP-24 under different NaCl concentrations
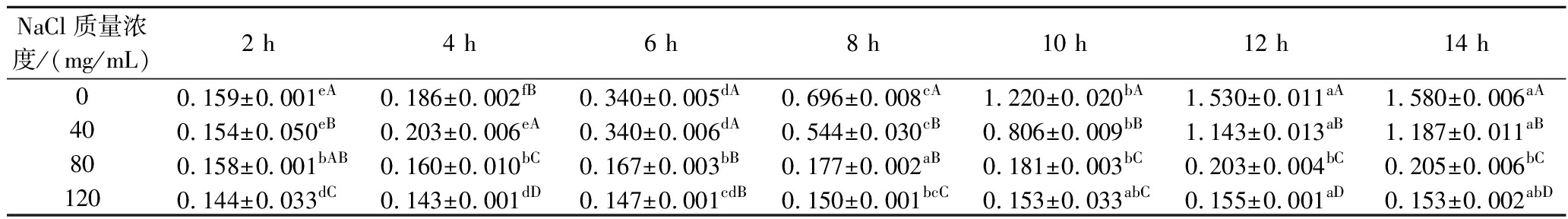
NaCl质量浓度/(mg/mL)2 h4 h6 h8 h10 h12 h14 h00.159±0.001eA0.186±0.002fB0.340±0.005dA0.696±0.008cA1.220±0.020bA1.530±0.011aA1.580±0.006aA400.154±0.050eB0.203±0.006eA0.340±0.006dA0.544±0.030cB0.806±0.009bB1.143±0.013aB1.187±0.011aB800.158±0.001bAB0.160±0.010bC0.167±0.003bB0.177±0.002aB0.181±0.003bC0.203±0.004bC0.205±0.006bC1200.144±0.033dC0.143±0.001dD0.147±0.001cdB0.150±0.001bcC0.153±0.033abC0.155±0.001aD0.153±0.002abD
注:不同的小写字母表示同一行内的显著差异(P<0.05),不同的大写字母表示同一列内的显著差异(P<0.05)。
2.2 产酸性和亚硝酸盐降解能力
P.pentosaceus的产酸性是其在发酵工业中的重要特性之一,其生长过程中发酵液pH值的变化直接影响发酵食品的风味、质地和保质期。如图1-a所示,P.pentosaceus RP-24在不同NaCl浓度条件下的产酸特性呈现阶段性变化。在培养的前4 h内,菌株的产酸速率较为缓慢,这可能与菌株在初始阶段的适应期有关。在4~12 h期间,P.pentosaceus RP-24在0 mg/mL 和40 mg/mL NaCl质量浓度环境下表现出显著的产酸趋势,pH值下降至4.1~4.4。该现象可能是由于此时菌株进入对数生长期,菌体数量迅速增加,代谢活性增强,乳酸等有机酸的产量显著提升,符合酱油发酵前期的快速酸化需求,并能抑制大部分杂菌污染。在培养12 h之后,各盐度条件下的pH值变化趋于平缓,此时菌株产酸速率趋于平缓。这一结果与忻晓庭等[17]的研究一致,其菌株JLSC2-6发酵的泡菜在12 h时pH值降至3.54,之后保持稳定。值得注意的是,P.pentosaceus RP-24在40 mg/mL NaCl质量浓度条件下孵育14 h后,pH值显著高于对照组和80 mg/mL NaCl质量浓度条件下的pH值,表明适当的NaCl质量浓度能够有效提高菌株的产酸活性。这一趋势与ZHANG等[9]的研究结果一致,发现发酵粘液乳杆菌R6在20、40 mg/mL NaCl质量浓度下的发酵液pH值显著低于0、60 mg/mL NaCl质量浓度下的pH值(P<0.05)。这种现象可能与P.pentosaceus RP-24在低盐胁迫下通过增加糖酵解产生更多丙酮酸有关,这些丙酮酸进一步转化为乳酸和乙酸,从而导致发酵液pH值升高。而高浓度盐度引起的渗透应激可能严重抑制碳水化合物的主动运输,阻碍菌株的发酵过程,进而抑制其生长并降低产酸活性[18]。如图1-b所示,P.pentosaceus RP-24降解亚硝酸盐的能力随着培养条件中盐度的升高呈现逐渐减弱的趋势。在0 mg/mL NaCl质量浓度条件下,菌株RP-24的亚硝酸盐降解率达到(7.93±0.23)%。在40、80 mg/mL NaCl质量浓度条件下菌株RP-24对亚硝酸盐降解率分别为(5.06±0.41)%和(4.21±0.94)%。随着NaCl质量浓度增大,菌株RP-24的亚硝酸盐降解能力显著下降(P<0.05)。这一现象与李世文等[19]的实验结果一致,其研究中利用植物乳植杆菌在不同NaCl浓度下发酵酸笋,亚硝酸盐的降解率随着培养条件中NaCl质量浓度的增加而降低。综上可知,适当的NaCl质量浓度能增强P.pentosaceus RP-24的产酸性能,但是降亚硝酸盐能力受到影响。
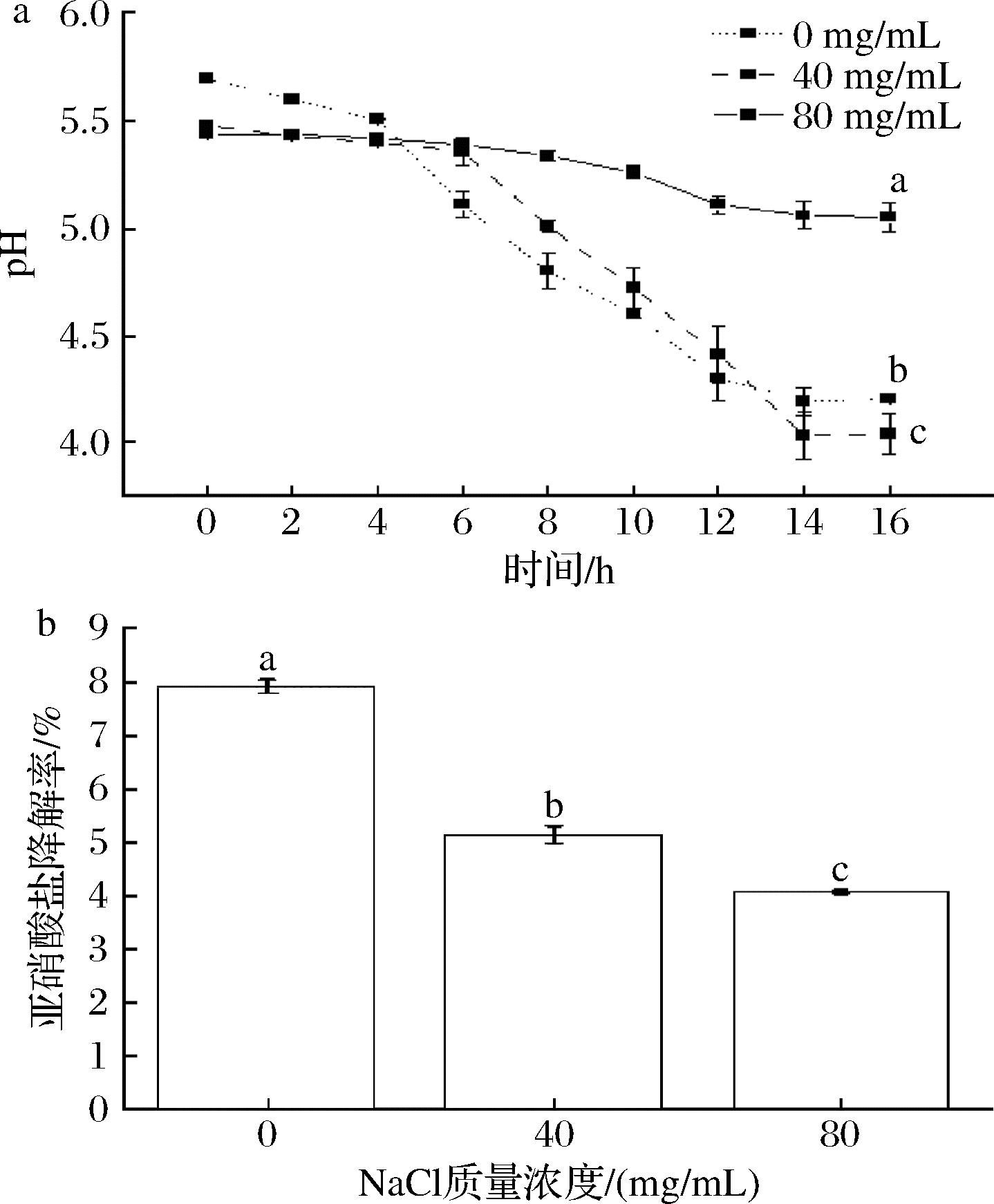
a-pH值的变化趋势;b-亚硝酸盐的降解率
图1 不同盐度条件下P. pentosaceus RP-24生长过程中的pH变化与亚硝酸盐降解率
Fig.1 Changes in pH and nitrite degradation rate during the growth of P. pentosaceus RP-24 under different salinity conditions
注:不同的小写字母表示样品间存在统计学的显著性差异,P<0.05,下同。
2.3 P.pentosaceus RP-24的表面形态分析
如图2-a所示,不添加NaCl时,菌株呈现典型的四联球形态,表面存在突起结构,符合P.pentosaceus的形态特征。与图2-a相比,在40 mg/mL NaCl质量浓度下,细胞表面突起显著减少(图2-b),表明中等盐度环境可能抑制细胞壁代谢或分泌活动,导致表面结构简化。进一步结合图2-a与图2-c分析,当NaCl质量浓度增加至80 mg/mL时,P.pentosaceus RP-24细胞表面突起基本消失,证实高盐环境对细胞壁结构产生显著破坏,可能引发表面层蛋白脱落或代谢活动深度抑制。以上现象与WANG等[20]的研究相似,魏斯氏菌在含有350 mg/mL NaCl培养基培养后,细胞表面出现皱褶并形成孔洞,导致细胞内蛋白物质泄露,进一步证实了高盐环境对P.pentosaceus RP-24细胞结构的破坏性影响。此外,DUBEY等[21]研究证实,P.pentosaceus GS4的表面层蛋白对其细胞黏附功能具有关键作用。综上所述,NaCl质量浓度增加导致P.pentosaceus RP-24表面结构趋于光滑,可能改变其表层蛋白,进而影响菌株的自聚集能力与细胞表面疏水性。本研究为阐释NaCl质量浓度梯度下戊糖片球菌益生特性的变化机制提供了形态学依据。

a-0 mg/mL;b-40 mg/mL;c-80 mg/mL
图2 P.pentosaceus RP-24在不同NaCl质量浓度下的扫描电镜形态
Fig.2 Scanning electron micrographs of P.pentosaceus RP-24at different mass concentrations of NaCl
2.4 P.pentosaceus RP-24的抗氧化性
如图3-a所示,在40 mg/mL和80 mg/mL NaCl质量浓度条件下,P.pentosaceus RP-24发酵上清液对DPPH自由基的清除率均高达90%以上,与对照组相比无显著差异(P<0.05),表明其在不同NaCl质量浓度下均表现出优异的抗氧化性能。这种特性不仅有助于清除食品体系中的自由基,还可能通过抑制脂质过氧化等途径延长发酵食品的货架期。值得注意的是,P.pentosaceus RP-24在80 mg/mL NaCl质量浓度条件下表现出最强的DPPH自由基清除能力。ZHANG等[9]的研究发现P.pentosaceus R1的上清液在0~40 mg/mL NaCl质量浓度范围内对DPPH自由基的清除活性达到50%,而在60 mg/mL NaCl下清除活性下降至30%左右。如图3-b所示,与对照组相比,不同NaCl浓度下P.pentosaceus RP-24发酵上清液对ABTS阳离子自由基的清除率无显著变化(P<0.05),清除率范围为(23.13±0.17)%至(28.48±0.15)%。然而,随着NaCl浓度增加,RP-24上清液对ABTS阳离子自由基的清除活性呈现下降趋势,表明80 mg/mL NaCl对菌株清除ABTS阳离子自由基的能力产生了一定的抑制作用。以上结果表明P.pentosaceus RP-24对DPPH和ABTS两类自由基的清除率相差较大。与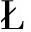 EPECKA等[22]的研究趋势一致,鼠李糖乳酪杆菌GG菌株对于DPPH自由基和ABTS阳离子自由基的清除率分别为24.12%、6.73%。这可能是由于菌株培养24 h后产生的乳酸导致发酵上清液处于低pH环境[23]。DPPH自由基清除主要依赖氢原子供体,低pH环境可能促进菌株分泌的某些酸性代谢物(如有机酸)的质子化,增强其提供氢原子的能力,从而显著提升DPPH清除率。ABTS阳离子自由基清除更依赖于电子转移机制,低pH可能改变发酵上清液中抗氧化成分的电荷状态或构象,使其电子转移效率降低。
EPECKA等[22]的研究趋势一致,鼠李糖乳酪杆菌GG菌株对于DPPH自由基和ABTS阳离子自由基的清除率分别为24.12%、6.73%。这可能是由于菌株培养24 h后产生的乳酸导致发酵上清液处于低pH环境[23]。DPPH自由基清除主要依赖氢原子供体,低pH环境可能促进菌株分泌的某些酸性代谢物(如有机酸)的质子化,增强其提供氢原子的能力,从而显著提升DPPH清除率。ABTS阳离子自由基清除更依赖于电子转移机制,低pH可能改变发酵上清液中抗氧化成分的电荷状态或构象,使其电子转移效率降低。
a-DPPH自由基的清除率;b-ABTS阳离子自由基的清除率
图3 不同NaCl浓度培养后菌株RP-24的抗氧化特性变化
Fig.3 Changes in antioxidant properties of P.pentosaceus RP-24 after cultivation at different mass concentrations of NaCl
2.5 P.pentosaceus RP-24的自聚集性、表面疏水性
如图4-a所示,P.pentosaceus RP-24的自聚集能力随孵育时间的延长而显著增强,4 h的自聚集率明显高于2 h的结果(P<0.05)。值得注意的是,菌株RP-24在40 mg/mL NaCl质量浓度条件下表现出最强的自聚集能力,孵育4 h后自聚集率达到(53.27±0.19)%,显著优于0 mg/mL和80 mg/mL NaCl质量浓度条件下的自聚集率(P<0.05)。这一趋势与REID等[24]的研究结果一致,实验菌株在20、40 mg/mL NaCl条件下培养3 h后,自聚集率显著高于0、60 mg/mL NaCl质量浓度胁迫下的结果(P<0.05)。研究表明,细胞的自聚集现象可能是微生物对盐度胁迫的直接反应,其机制可能与细胞壁组分(如脂磷壁酸和蛋白质)的表达或构象变化有关[20]。此外,P.pentosaceus的细胞表面疏水性是评估其黏附上皮细胞能力的重要指标,能够反映菌株在肠道环境中的定植潜力。较强的疏水性有助于菌株在宿主肠道黏膜表面的黏附[25]。如图4-b所示,P.pentosaceus RP-24在不同NaCl浓度条件下的细胞疏水性变化趋势与自聚集变化趋势基本一致。在40 mg/mL NaCl质量浓度条件下,菌株的细胞疏水率达到(11.31±0.12)%,显著高于0、80 mg/mL NaCl质量浓度条件下的疏水率(P<0.05)。结合菌株表面形态的实验结果分析,适量的盐度环境可能使细胞突起减少可能暴露疏水基团,从而增强P.pentosaceus RP-24的自聚集性和疏水性。但高盐度环境导致P.pentosaceus RP-24细胞的表面蛋白大量脱落,导致黏附位点丧失,从而自聚集性降低。
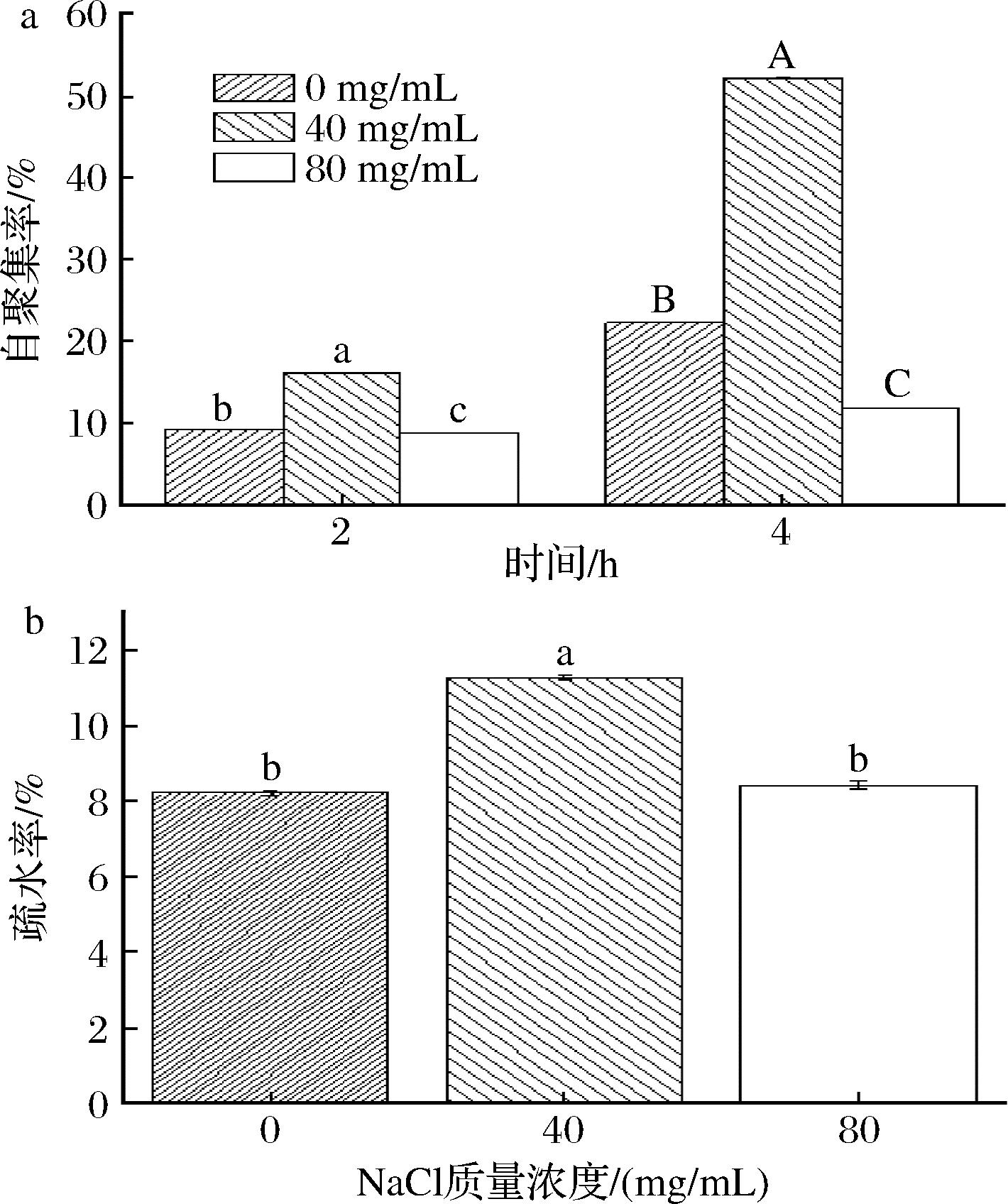
a-自聚集率;b-疏水率
图4 不同NaCl浓度培养后菌株RP-24的自聚集性和表面疏水性变化
Fig.4 Changes of self-aggregation and surface hydrophobicity of strain RP-24 after culture with different salt concentrations
注:图中不同的大小写字母表示组内样品间存在统计学的显著性差异(P<0.05)。
3 结论
本研究揭示了不同NaCl浓度对P.pentosaceus RP-24生理特性及益生功能的显著影响。在40 mg/mL NaCl浓度条件下,该菌株表现出最优的综合性能,包括良好的生长能力、产酸能力、强抗氧化活性、高自聚集性及表面疏水性。然而,高盐环境显著抑制其生长和代谢活动,导致细胞表面结构损伤、疏水性下降,进而削弱其益生功能。本研究为开发基于P.pentosaceus的低盐发酵食品提供了重要的科学依据,也为理解乳酸菌在食品基质中的适应性提供了新视角。未来研究可深入探究P.pentosaceus RP-24在低盐发酵食品基质中的应用效果及其对产品品质的影响,并评估该菌株在不同NaCl浓度条件下的长期贮存稳定性。
[1] MEDINA L M, PÉREZ-RODR GUEZ F.Lactic acid bacteria:An inexhaustible source of scientific knowledge and food innovation[J].Foods, 2025, 14(5):858.
GUEZ F.Lactic acid bacteria:An inexhaustible source of scientific knowledge and food innovation[J].Foods, 2025, 14(5):858.
[2] SINGRACHA P, NIAMSIRI N, VISESSANGUAN W, et al.Application of lactic acid bacteria and yeasts as starter cultures for reduced-salt soy sauce (moromi) fermentation[J].LWT, 2017, 78:181-188.
[3] 李秀娟, 王夫杰, 鲁绯, 等.一株戊糖片球菌在低盐固态酱油工艺中的应用[J].食品科学, 2011, 32(9):251-256.LI X J, WANG F J, LU F, et al.Application of a Pediococcus pentosaceus strain in low-salt solid-state fermentation of soy sauce[J].Food Science, 2011, 32(9):251-256.
[4] PORTO M C W, KUNIYOSHI T M, AZEVEDO P O S, et al.Pediococcus spp.An important genus of lactic acid bacteria and pediocin producers[J].Biotechnology Advances, 2017, 35(3):361-374.
[5] GUO P L, WANG W J, XIANG Q, et al.Engineered probiotic ameliorates ulcerative colitis by restoring gut microbiota and redox homeostasis[J].Cell Host &Microbe, 2024, 32(9):1502-1518.e9.
[6] NDIAYE A, FLISS I, FILTEAU M.High-throughput characterization of the effect of sodium chloride and potassium chloride on 31 lactic acid bacteria and their co-cultures[J].Frontiers in Microbiology, 2024, 15:1328416.
[7] SERRAZANETTI D I, GUERZONI M E, CORSETTI A, et al.Metabolic impact and potential exploitation of the stress reactions in lactobacilli[J].Food Microbiology, 2009, 26(7):700-711.
[8] LUO X, LI M, ZHANG H N, et al.Comparative proteomic analysis of three Lactobacillus plantarum strains under salt stress by iTRAQ[J].Journal of the Science of Food and Agriculture, 2021, 101(8):3457-3471.
[9] ZHANG H, WANG Q, LIU H T, et al.In vitro growth performance, antioxidant activity and cell surface physiological characteristics of Pediococcus pentosaceus R1 and Lactobacillus fermentum R6 stressed at different NaCl concentrations[J].Food &Function, 2020, 11(7):6376-6386.
[10] 张甜, 丁真真, 刘艳全, 等.具有抑菌活性乳酸菌的分离、鉴定及其生长特性研究[J].中国酿造, 2024, 43(2):119-124.ZHANG T, DING Z Z, LIU Y Q, et al.Isolation, identification and growth characteristics of lactic acid bacteria with antibacterial activity[J].China Brewing, 2024, 43(2):119-124.
[11] 丁娟芳, 杨嘉, 朱淑云, 等.扬州酱菜中降解亚硝酸盐乳酸菌的筛选、鉴定及性能研究[J].中国酿造, 2018, 37(12):87-91.DING J F, YANG J, ZHU S Y, et al.Screening, identification and characteristic of nitrite degradating lactic acid bacteria from Yangzhou pickles[J].China Brewing, 2018, 37(12):87-91.
[12] MU G Q, GAO Y, TUO Y F, et al.Assessing and comparing antioxidant activities of lactobacilli strains by using different chemical and cellular antioxidant methods[J].Journal of Dairy Science, 2018, 101(12):10792-10806.
[13] 张乃珣, 尹红力, 赵鑫, 等.红松多酚与真菌多糖联合清除ABTS自由基活性比较[J].北京林业大学学报, 2016, 38(10):104-111.ZHANG N X, YIN H L, ZHAO X, et al.Combined ABTS radical scavenging activity of Pinus koraiensis polyphenols with fungus polysaccharides[J].Journal of Beijing Forestry University, 2016, 38(10):104-111.
[14] ZHAO J Y, ZHAO J S, ZANG J H, et al.Isolation, identification, and evaluation of lactic acid bacteria with probiotic potential from traditional fermented sour meat[J].Frontiers in Microbiology, 2024, 15:1421285.
[15] WU R N, WU Z X, ZHAO C Y, et al.Identification of lactic acid bacteria in Suancai, a traditional Northeastern Chinese fermented food, and salt response of Lactobacillus paracasei LN-1[J].Annals of Microbiology, 2014, 64(3):1325-1332.
[16] ZAMFIR M, GROSU-TUDOR S S.Stress response of some lactic acid bacteria isolated from Romanian artisan dairy products[J].World Journal of Microbiology and Biotechnology, 2014, 30(2):375-384.
[17] 忻晓庭, 刘大群, 张程程, 等.我国特色发酵蔬菜降解亚硝酸盐菌株的筛选鉴定及应用[J].浙江农业学报, 2021, 33(2):335-345.XIN X T, LIU D Q, ZHANG C C, et al.Screening, identification and application of high efficient nitrite degrading functional strains in Chinese characteristic fermented vegetables[J].Acta Agriculturae Zhejiangensis, 2021, 33(2):335-345.
[18] 杨雄州, 姚国强, 于洁, 等.工业微生物在渗透胁迫下的应激反应及保护措施[J].微生物学报, 2022, 62(11):4176-4187.YANG X Z, YAO G Q, YU J, et al.Response of industrial microorganisms to osmotic stress and countermeasures[J].Acta Microbiologica Sinica, 2022, 62(11):4176-4187.
[19] 李世文, 伊奎鑫, 唐云, 等.食盐浓度对植物乳杆菌发酵酸笋品质的影响[J].世界竹藤通讯, 2024, 22(5):91-95.LI S W, YI K X, TANG Y, et al.Effect of salt concentration on quality of sour bamboo shoot fermented with Lactobacillus plantarum[J].World Bamboo and Rattan, 2024, 22(5):91-95.
[20] WANG A L, DU Q Q, LI X M, et al.Intracellular and extracellular metabolic response of the lactic acid bacterium Weissella confusa under salt stress[J].Metabolites, 2024, 14(12):695.
[21] DUBEY V, MISHRA A K, GHOSH A R.Cell adherence efficacy of probiotic Pediococcus pentosaceus GS4 (MTCC 12683) and demonstrable role of its surface layer protein (Slp)[J].Journal of Proteomics, 2020, 226:103894.
[22] 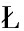 EPECKA A, SZYMA
EPECKA A, SZYMA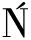 SKI P, OKO
SKI P, OKO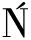 A, et al.Antioxidant activity of environmental lactic acid bacteria strains isolated from organic raw fermented meat products[J].LWT, 2023, 174:114440.
A, et al.Antioxidant activity of environmental lactic acid bacteria strains isolated from organic raw fermented meat products[J].LWT, 2023, 174:114440.
[23] MENG C Y, XIE J W, CHEN J Q, et al.Fermentation of Pediococcus pentosaceus JC30 improves phytochemical, flavor characteristics and antioxidant activity of mulberry leaves[J].Molecules, 2025, 30(8):1703.
[24] REID E, LIU X R, JUDD S J.Effect of high salinity on activated sludge characteristics and membrane permeability in an immersed membrane bioreactor[J].Journal of Membrane Science, 2006, 283(1-2):164-171.
[25] LIU C, XUE W J, DING H, et al.Probiotic potential of Lactobacillus strains isolated from fermented vegetables in Shaanxi, China[J].Frontiers in Microbiology, 2021, 12:774903.