酱腌芥菜作为我国传统发酵食品的重要代表,凭借独特的风味和丰富的营养价值深受消费者喜爱[1-2]。然而,在加工、贮藏及流通过程中,由腐败微生物引发的品质劣变问题严重制约了其产业规模化发展。尤其在开放式的自然发酵环境下,腐败菌群(如芽孢杆菌属、不动杆菌属、毕赤酵母属等)易通过代谢活动分解营养物质并产生异味物质,导致产品酸败、质构软烂及货架期缩短[3-6]。传统化学防腐剂(如苯甲酸钠、山梨酸钾)虽能有效抑制腐败菌增殖,但长期使用可能引发潜在的食品安全风险,如残留毒性及耐药菌株的产生[7-9]。近年来,随着消费者对天然、健康食品需求的提升,天然防腐剂因其安全性高、副作用小等优势成为研究热点。然而,单一天然防腐剂通常面临抑菌谱窄、作用浓度高或稳定性不足等瓶颈问题[10]。基于此,通过复配天然防腐剂,有望突破单一防腐剂的局限性,从而开发出高效、广谱且稳定的新型防腐体系,这已成为食品保鲜领域的重要研究方向。
目前,围绕天然防腐剂抑菌机理研究多集中于单一成分对微生物细胞膜、细胞壁及代谢酶的靶向作用。例如,ε-聚赖氨酸通过静电作用破坏细胞膜磷脂双分子层的完整性,导致胞内物质外泄[11];壳聚糖凭借阳离子特性干扰细菌细胞壁肽聚糖的合成[12];乳酸链球菌素可特异性结合细菌细胞膜上的脂质Ⅱ,抑制细胞壁合成并引发孔洞形成[13];而肉桂醛则通过疏水作用穿透细胞膜,干扰膜蛋白功能并诱导活性氧积累[13-14]。然而,复配防腐剂的协同抑菌机制仍不清晰,尤其是不同成分在组合后对腐败菌细胞结构及生理功能的综合影响尚未系统阐明。此外,天然防腐剂在实际应用中的稳定性易受温度、pH及盐质量浓度等环境因素干扰,明确其适用条件对酱腌芥菜工业化生产至关重要。
前期研究通过高通量测序和传统培养法,分离、纯化和鉴定出酱腌芥菜的主要腐败菌为贝莱斯芽孢杆菌和鲍曼不动杆菌,并通过抑菌实验结合响应面优化确定复配天然防腐剂最佳配比。在此研究基础上,通过测定细胞膜渗透性、通透性、细胞壁完整性及抗氧化酶等指标,探究复配防腐剂对菌体结构的破坏路径及代谢途径;其次,结合扫描电镜观察细菌超微形态变化,直观揭示防腐剂对菌体结构的物理损伤效应;最后,系统评估温度、pH及盐质量浓度对复配防腐剂稳定性的影响,为其在酱腌芥菜加工中的实际应用提供理论支撑。
1 材料与方法
1.1 材料与试剂
贝莱斯芽孢杆菌(Bacillus velezensis)、鲍曼不动杆菌(Acinetobacter baumannii),从湖南海霸食品有限公司提供的酱腌芥菜中分离纯化,经分子生物学方法鉴定。
ε-聚赖氨酸(食品级),捷恒生物科技有限公司;乳酸链球菌素(食品级),河南中辰生物科技有限公司;壳聚糖(食品级),河南万邦化工科技有限公司;肉桂醛(食品级),武汉拉那白医药化工有限公司;苯甲酸钠(食品级),武汉有机实业有限公司;山梨酸钾(食品级),山东昆达生物科技有限公司;乙酸、盐酸、NaOH(分析纯),国药集团化学试剂有限公司;葡萄糖(分析纯),天津市大茂化学试剂厂;碱性磷酸酶(alkaline phosphatase,AKP)试剂盒、过氧化氢酶(catalase,CAT)试剂盒、超氧化物歧化酶(superoxide dismutase,SOD)试剂盒,南京建成生物工程研究所;2.5%戊二醛固定液(电镜专用),飞净生物科技有限公司;麦氏比浊管,比克曼生物科技有限公司;营养琼脂培养基、LB肉汤培养基、磷酸盐缓冲溶液(phosphate buffered saline,PBS),青岛海博生物技术有限公司。
1.2 仪器与设备
HVA-85全自动压力蒸汽灭菌锅,江苏肯尔菲实验仪器贸易有限公司;BIOsafe12生物安全柜,上海力申科学仪器有限公司;LRH-250生化培养箱,上海一恒科技有限公司;DKZ-450B电热恒温振荡水槽,上海森信实验仪器有限公司;H1850高速台式离心机,湘仪离心机仪器有限公司;SJ-142电导率仪,上海仪电科学仪器股份有限公司;RT-2100C酶标分析仪,深圳雷杜生命科学股份有限公司;UV-2600紫外可见分光光度计,岛津仪器(苏州)有限公司。
1.3 实验方法
1.3.1 菌悬液的制备
用无菌接种环刮取细菌接种至营养琼脂培养基中37 ℃培养24 h,将活化后的菌种用无菌PBS配制成细菌浓度1×105 CFU/mL的菌悬液,备用。
1.3.2 复配防腐剂的制备
a)天然防腐剂组:将4种天然防腐剂进行复配,质量浓度分别为ε-聚赖氨酸180 μg/mL、乳酸链球菌素102 μg/mL、壳聚糖121 μg/mL和肉桂醛100 μg/mL。
b)化学防腐剂组:依据GB 2760—2024《食品安全国家标准 食品添加剂使用标准》,以腌渍的蔬菜最大允许使用量(均为1.0 g/kg)添加苯甲酸钠和山梨酸钾(添加质量比1∶1)。
1.3.3 复配防腐剂对细胞膜渗透性的影响
根据文献[15]的方法并修改。将受试菌分别接入到LB肉汤培养基中恒温摇床37 ℃培养12 h后,吸取菌液60 mL,平均分装在2个50 mL离心管中,离心(8 000 r/min、5 min)收集菌体,用PBS冲洗3次,过滤得到菌液,实验组添加复配天然防腐剂,化学防腐剂为阳性对照组,添加质量浓度同1.3.2节,同时设立未添加防腐剂的空白对照组。放置于37 ℃恒温水浴摇床培养,每隔2 h吸取4 mL菌液,6 000 r/min离心10 min,取上清液分别测定260、280 nm波长处的吸光值。
1.3.4 复配防腐剂对细胞膜通透性的影响
根据文献[16]的方法并修改。将受试菌接入到LB肉汤培养基中37 ℃培养12 h后,5 000 r/min离心10 min,收集菌体,用质量分数5%葡萄糖溶液洗涤至菌液的相对电导率与质量分数5%葡萄糖溶液的相对电导率相当,此菌液为等渗菌液。向质量分数5%葡萄糖溶液中分别加入复配天然防腐剂和化学防腐剂,混匀后4 000 r/min离心5 min,取上清液测其相对电导率记为L1。取等渗菌液分别加入2种防腐剂,37 ℃下培养6 h,每1 h取出菌悬浮液5 mL,4 000 r/min离心5 min后取上清液测定相对电导率,记为L2。将等渗菌液在沸水浴中煮沸5 min,冷却后离心,取上清液测定相对电导率记为L0。相对电导率按照公式(1)计算:
(1)
式中:E,相对电导率,%;L0,等渗菌液在沸水浴中煮沸后上清液的电导率,mS/cm;L1,向质量分数5%葡萄糖溶液中加入2种防腐剂,上清液的电导率,mS/cm;L2,等渗菌液加入2种防腐剂,上清液的电导率,mS/cm。
1.3.5 复配防腐剂对细胞壁完整性的影响
根据文献[17]的方法并修改。将受试菌分别接入到LB肉汤培养基中恒温摇床37 ℃培养12 h后,取30 mL菌悬液5 000 r/min离心5 min收集菌体,并用PBS重悬至1×107 CFU/mL,分别加入复配天然防腐剂和化学防腐剂,37 ℃振荡恒温培养,于0、4 h取样,4 000 r/min离心5 min,取上清液,参照AKP试剂盒说明方法测其酶活力。
1.3.6 复配防腐剂对过氧化氢酶和超氧化物歧化酶酶活力的影响
根据文献[18]的方法并修改。将受试菌分别接入到LB肉汤培养基中恒温摇床37 ℃培养12 h后,取30 mL菌悬液5 000 r/min离心5 min后收集菌体,并用PBS重悬至1×107 CFU/mL,分别加入复配天然防腐剂和化学防腐剂,37 ℃振荡恒温培养4 h取样,4 000 r/min离心5 min。吸取上清液,参照过氧化氢酶和超氧化物歧化酶试剂盒说明方法测其酶活力。
1.3.7 复配防腐剂对细胞形态的影响
根据文献[19]的方法并修改。首先将待测菌株接种于LB液体培养基中,在37 ℃恒温培养箱中进行24 h活化培养。培养完成后,使用高速离心机以8 000 r/min离心10 min收集菌体,随后用无菌PBS洗涤2次以去除培养基残留。采用比浊法将菌悬液浓度调整为1×107 CFU/mL,分别加入复配天然防腐剂和化学防腐剂,将处理后的菌悬液置于37 ℃恒温振荡培养箱中培养4 h,再次以8 000 r/min离心10 min收集菌体,并用PBS洗涤3次以去除残留物质。样品制备阶段采用2.5%(体积分数)戊二醛溶液于4 ℃条件下进行固定过夜处理。固定完成后,依次使用30%、50%、70%、90%(体积分数)及无水乙醇进行梯度脱水处理,每个浓度梯度处理15 min。脱水后的样品经临界点干燥仪干燥后,通过离子溅射仪进行镀金处理以增强样品导电性。最终使用扫描电子显微镜观察细菌超微结构形态变化。
1.3.8 相对抑菌活性的测定
使用酶标仪测定相对抑菌活性:向细胞培养板的每孔中加入50 μL的LB培养基,再向细胞培养板的每孔中加入配好的复配防腐剂100 μL,然后向每孔中加入50 μL菌悬液,将细胞培养板放入37 ℃恒温培养箱中培养12 h。培养完成后,测定12 h的OD630。每组实验3次平行。根据相对抑菌活性判断不同因素对复配天然防腐剂抑菌活性的稳定性影响。相对抑菌活性的测定按照公式(2)计算:
相对抑菌活性![]()
(2)
1.3.9 温度对复配防腐剂抑菌活性的影响
复配防腐剂分别在-20、40、60、80、100 ℃下处理30 min,121 ℃高温高压处理20 min,然后冷却至室温,以未处理的复配防腐剂作为对照组(相对抑菌活性为100%),使用酶标仪测定吸光值,研究不同温度对复配防腐剂抑菌活性的影响。
1.3.10 pH处理对复配防腐剂抑菌活性的影响
复配防腐剂分别用0.1 mol/L的HCl溶液和NaOH溶液调节pH值至2.0、3.0、4.0、5.0、6.0、7.0、8.0室温处理4 h,调回pH至中性(6.5~7.5),以未处理的复配防腐剂作为对照组(相对抑菌活性为100%),然后用酶标仪测定吸光值,研究不同pH值对复配防腐剂抑菌活性的影响。
1.3.11 盐质量浓度对复配防腐剂抑菌活性的影响
配制质量浓度分别为1.0、2.0、3.0、4.0、5.0、6.0 mg/mL的NaCl溶液,加入复配天然防腐剂,室温处理4 h后,以未处理的复配防腐剂作为对照组(相对抑菌活性为100%),然后用酶标仪测定吸光值,研究不同盐的质量浓度对复配防腐剂抑菌活性的影响。
1.3.12 数据处理
使用SciDAVis 2.9.2软件进行数据处理。
2 结果与分析
2.1 复配防腐剂对细胞膜渗透性的影响
基于核酸(最大吸收峰260 nm)与蛋白质(最大吸收峰280 nm)的紫外吸收特性,可以通过检测OD260和OD280值的变化量,来评估细胞膜渗透性的破坏程度[20]。因此可通过该方法来评估防腐剂作用后贝莱斯芽孢杆菌和鲍曼不动杆菌核酸和蛋白质内容物的泄漏情况。如图1所示,相比于0 h,贝莱斯芽孢杆菌菌液经过8 h处理后,未添加防腐剂组OD260和OD280数值变化量仅为0.002;化学防腐剂组OD260和OD280变化量分别为0.026和0.112;而天然防腐剂组OD260和OD280变化量分别提升至0.096和0.153,表明天然防腐剂的添加对细胞膜的破坏大于化学防腐剂。如图2所示,相比于0 h,鲍曼不动杆菌菌液经过8 h处理后,未添加防腐剂组OD260和OD280变化量维持在0.001;化学防腐剂组OD260和OD280变化量分别为0.118和0.137;而天然防腐剂组OD260和OD280变化量分别高达0.188和0.193,表明天然防腐剂的添加对细胞膜的破坏也大于化学防腐剂。综上,根据数值变化量可知,天然防腐剂相比于化学防腐剂和未添加防腐剂处理组对贝莱斯芽孢杆菌和鲍曼不动杆菌细胞膜渗透性破坏程度更大,可诱导胞内蛋白质和核酸物质大量泄漏。此外,ZHAO等[21]通过检测OD260值及胞外蛋白质含量变化,证实了抑菌活性成分可引发不可逆的细胞膜损伤,导致胞内核酸、蛋白质等大分子物质异常外泄。从作用机制层面分析,天然防腐剂可能通过改变细胞膜通透性,破坏细胞内稳态,干扰微生物正常代谢活动,最终实现抑菌目的[22]。
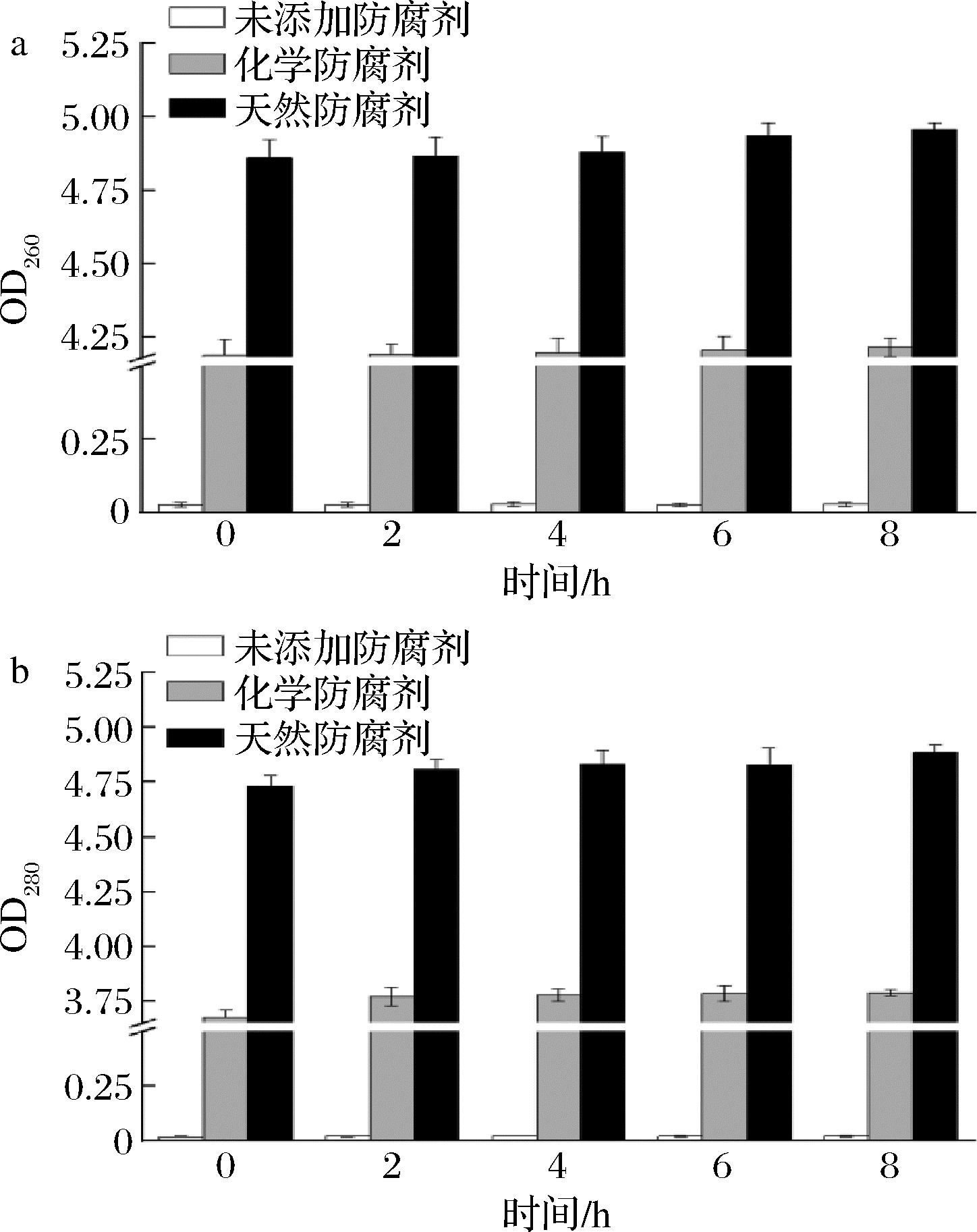
a-核酸;b-蛋白质
图1 防腐剂对贝莱斯芽孢杆菌核酸和蛋白质泄漏的影响
Fig.1 Effects of preservative on nucleic acid and protein leakage in Bacillus velezensis
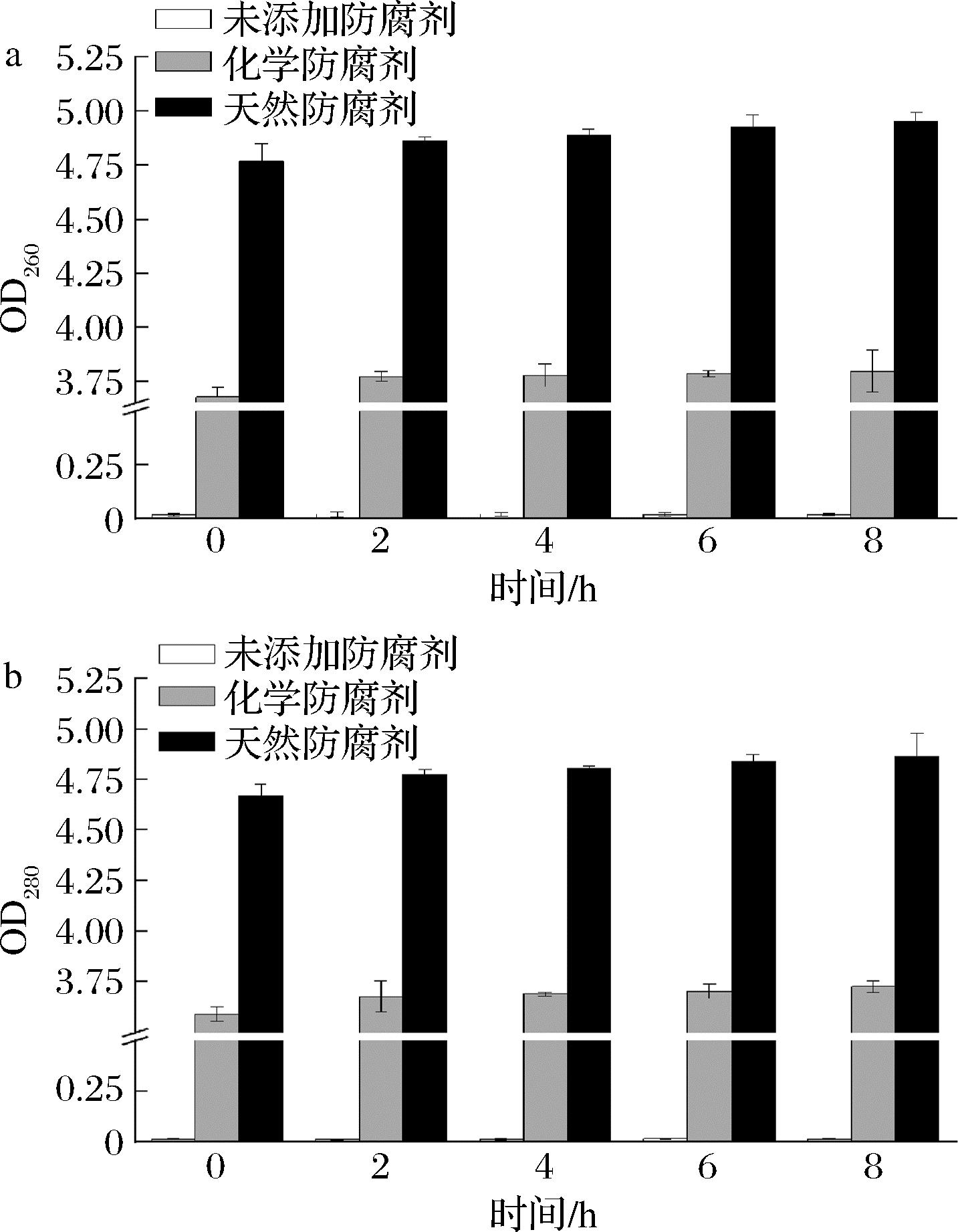
a-核酸;b-蛋白质
图2 防腐剂对鲍曼不动杆菌核酸和蛋白质泄漏的影响
Fig.2 Effects of preservative on nucleic acid and protein leakage in Acinetobacter baumannii
2.2 复配防腐剂对细胞膜通透性的影响
细胞膜作为细菌选择通透性屏障,通过K+、Na+、H+等离子的跨膜运输调控能量代谢、渗透压平衡及物质转运[23]。防腐剂通过破坏细胞膜通透性促使电解质异常外流,因此,可通过菌液相对电导率的变化来反映细胞膜通透性改变。如图3所示,天然防腐剂处理后的2种细菌均显示出比化学防腐剂和未添加防腐剂处理组更高的相对电导率值,并在0~2 h呈现出快速上升的趋势,此后逐渐趋于平缓。天然防腐剂处理贝莱斯芽孢杆菌5 h后相对电导率达到11.16%,相比于化学防腐剂处理组提高了1.27倍。而天然防腐剂处理鲍曼不动杆菌6 h后相对电导率达到3.7%,相比于化学防腐剂处理组提高了2.25倍。说明本实验复配天然防腐剂较化学防腐剂对2种菌的抑菌效果更好。许超群等[16]研究发现2种天然防腐剂协同处理4种细菌相对电导率值在0~2 h显著增加之后趋于平缓,与本实验中复配天然防腐剂的抑菌现象相似。
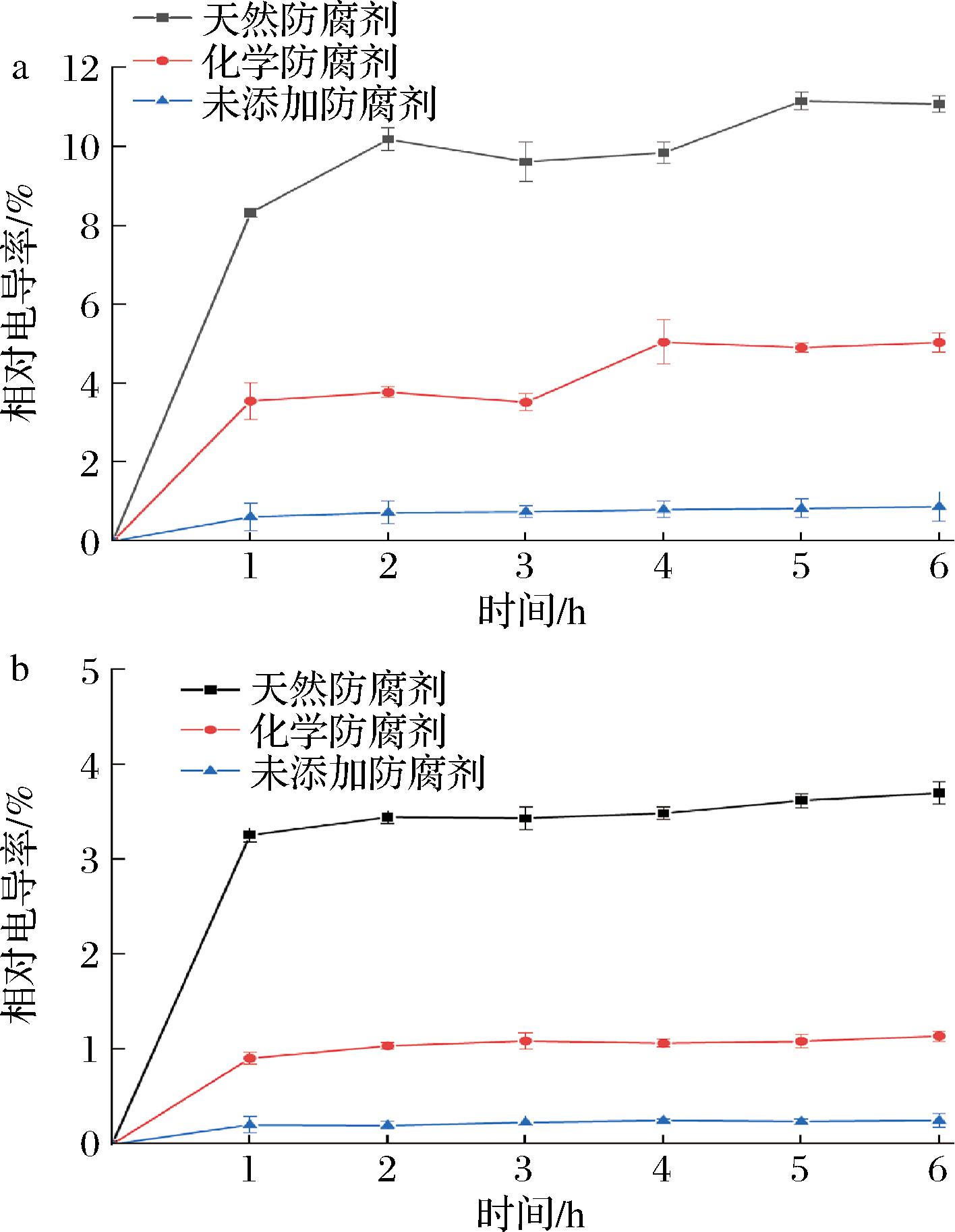
a-贝莱斯芽孢杆菌;b-鲍曼不动杆菌
图3 防腐剂对腐败菌相对电导率的影响
Fig.3 Effect of preservative on the relative electrical conductivity of spoilage bacteria
2.3 复配防腐剂对细胞壁完整性的影响
AKP主要存在于微生物细胞膜或细胞壁外表面,当细胞壁结构完整性受损时,AKP可通过破损的细胞壁外泄至胞外环境[24]。因此,可通过检测胞外AKP活力的动态变化来反映复配防腐剂对目标菌株细胞壁结构的破坏程度及其作用强度[25]。如图4所示,与未添加防腐剂和化学防腐剂比较,天然防腐剂处理组的AKP活力高于未添加防腐剂和化学防腐剂对照组。当处理4 h后,天然防腐剂处理贝莱斯芽孢杆菌和鲍曼不动杆菌AKP活力达到0.633、0.762金氏单位/100 mL,相比于化学防腐剂处理组分别提高了3.4%和9.2%。可见,复配天然防腐剂对腐败菌细胞壁具有一定的破坏作用,可使腐败菌中的AKP从菌体释放到体外。黄伟英等[26]研究发现,壳聚糖和ε-聚赖氨酸作用肉食杆菌后,使处理组AKP含量高于空白对照组,表明防腐剂破坏了细胞壁的完整性。
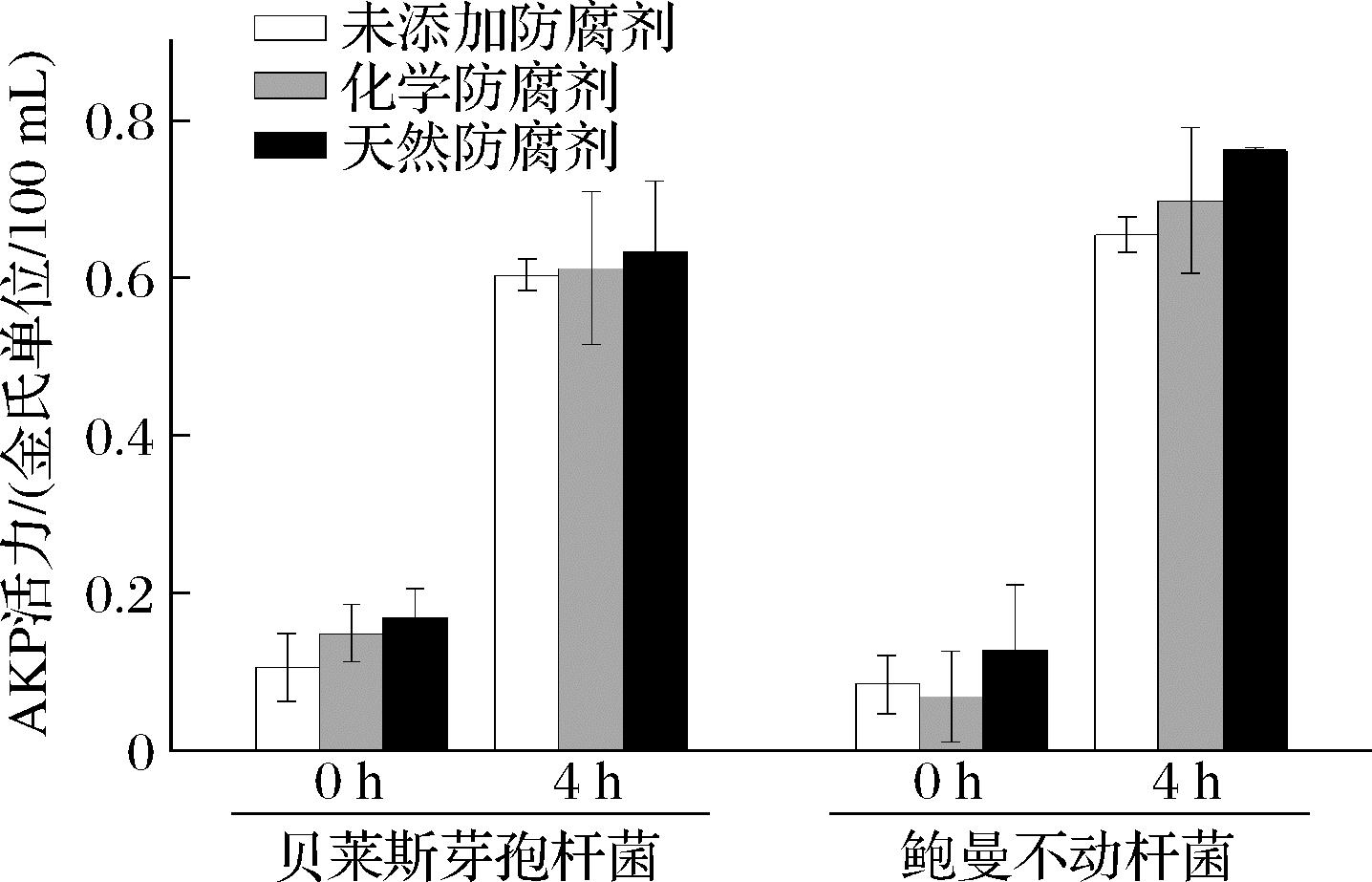
图4 防腐剂对腐败菌AKP活力的影响
Fig.4 Effect of preservatives on alkaline phosphatase enzyme activities in spoilage bacteria
2.4 复配防腐剂对CAT活力的影响
CAT是细胞内源性抗氧化防御体系的关键酶[27]。如图5所示,天然防腐剂和化学防腐剂处理组的CAT活力均低于未添加防腐剂对照组。在4 h时,经天然防腐剂处理的贝莱斯芽孢杆菌和鲍曼不动杆菌CAT活力分别为0.904、1.333 U/mL,相较于未添加防腐剂的对照组,酶活力分别下降了38.95%和26.69%。CAT活力的下降表明菌体膜系统受到损伤,进而影响细胞正常的生长代谢过程[28],由此可见,天然防腐剂对腐败菌CAT活力具有显著影响。也可能是因为复配天然防腐剂削弱了菌体自身清除过氧化物的能力,加剧氧自由基的积累[29],导致酶活力被抑制,最终造成菌体自身防御机能降低而消亡。葛文沛等[30]研究同样发现,经抑菌剂处理的菌体CAT活力较空白对照组呈现明显降低趋势;相关研究进一步指出,乳酸链球菌素的存在可使腐败菌CAT活力受到抑制[31]。
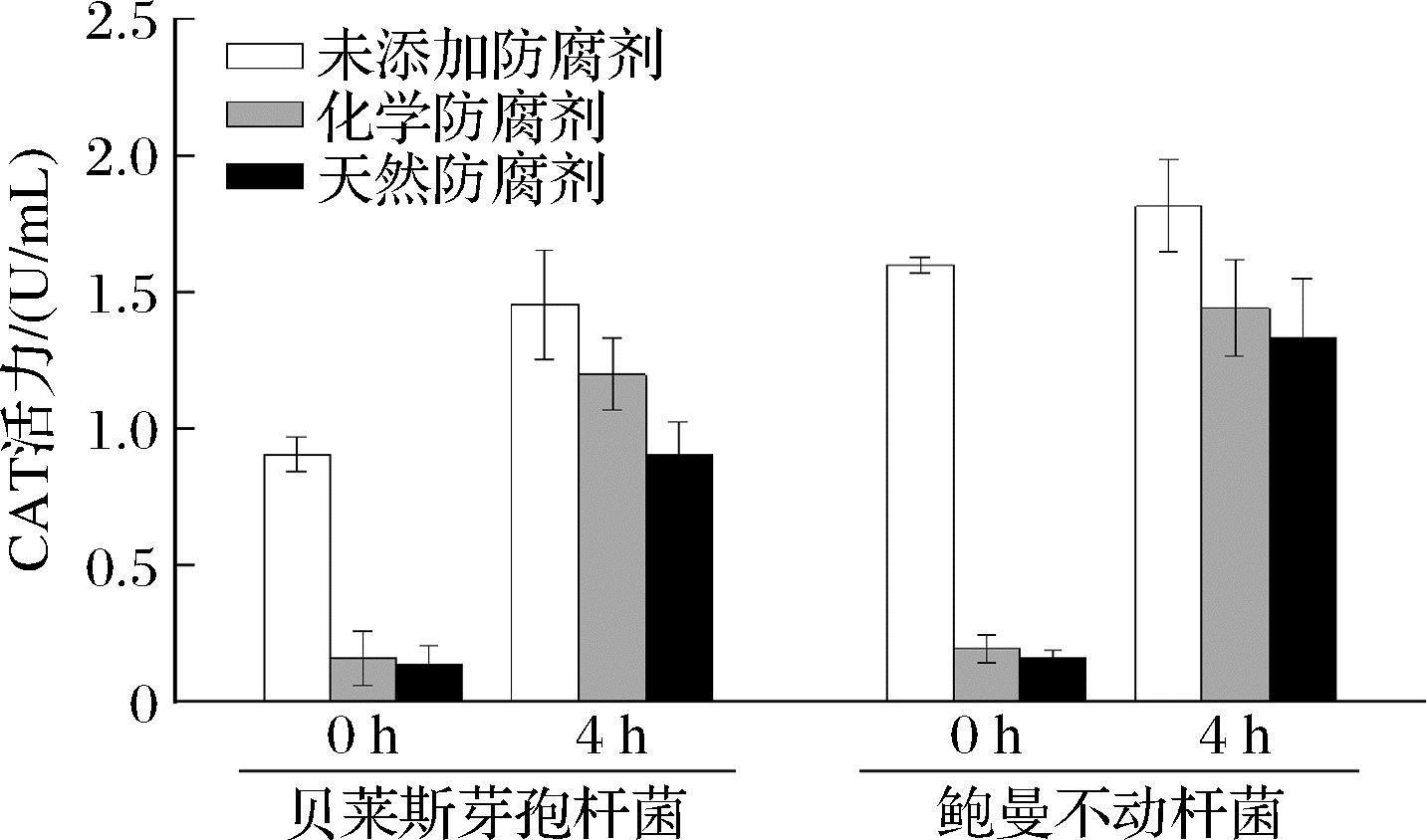
图5 防腐剂对腐败菌CAT活力的影响
Fig.5 Effect of preservatives on CAT activities in spoilage bacteria
2.5 复配防腐剂对SOD活力的影响
SOD是生物体内关键的抗氧化酶,通过高效清除超氧自由基保护细胞免受氧化损伤[32]。如图6所示,天然防腐剂处理组的SOD活力均高于化学防腐剂和未添加防腐剂对照组。在0~4 h,天然防腐剂处理的菌体SOD活力均明显升高;在4 h时,天然防腐剂处理的贝莱斯芽孢杆菌和鲍曼不动杆菌SOD活力达到18.41、17.28 U/mL,分别比未添加防腐剂处理组的SOD活力提高了35.27%和20.59%。由此可见,添加天然防腐剂处理对腐败菌SOD活力具有显著影响。陈山乔等[33]研究表明,盐脱氮枝芽孢杆菌经复配抑菌剂处理后,其SOD活力较空白对照组提高了62.7%。可能是腐败菌受到天然防腐剂的损害,通过胁迫作用导致菌体超氧阴离子自由基代谢平衡被破坏,引起SOD活力升高[34]。
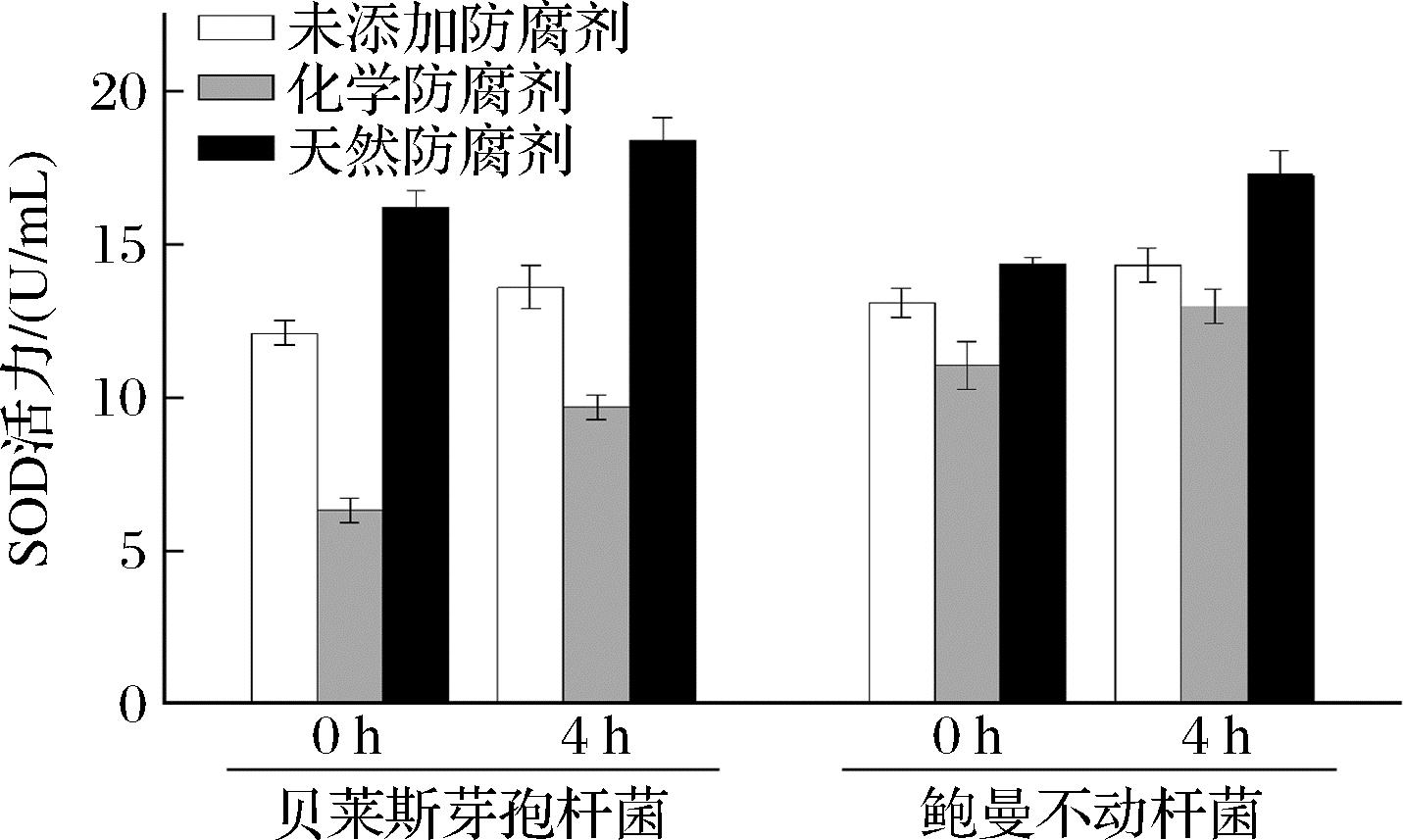
图6 防腐剂对腐败菌SOD活力的影响
Fig.6 Effect of preservatives on SOD activities in spoilage bacteria
2.6 复配防腐剂对细胞形态的影响
通过扫描电镜对腐败菌进行形态观察,可较为直观地看到防腐剂作用后对贝莱斯芽孢杆菌和鲍曼不动杆菌细胞形态的变化。如图7所示,空白对照组(图7-a和图7-d)细胞表面完整无损、形态饱满且轮廓清晰,没有出现细胞破损和内容物溢出等现象;加入化学防腐剂处理(图7-b和图7-e)后菌体出现少量坍塌,并出现小部分孔洞以及微量内容物外泄等受损情况;然而当加入天然防腐剂处理(图7-c和图7-f)后菌体出现大量褶皱凹陷,并出现大面积孔洞以及大量内容物外泄和出现空化现象。相比于化学防腐剂处理组,天然防腐剂处理组的变化则更为明显,可以清晰看出菌体形态遭到更严重的破坏。这种情况可能是天然防腐剂通过破坏贝莱斯芽孢杆菌和鲍曼不动杆菌的细胞壁膜结构,引发胞内物质外泄,导致其丧失维持细胞正常代谢的功能及细胞内容物保护作用,最终致使菌体形态发生显著改变[35]。

a-贝莱斯芽孢杆菌空白对照组;b-贝莱斯芽孢杆菌化学防腐剂处理组;c-贝莱斯芽孢杆菌天然防腐剂处理组;d-鲍曼不动杆菌空白对照组;e-鲍曼不动杆菌化学防腐剂处理组;f-鲍曼不动杆菌天然防腐剂处理组
图7 防腐剂处理后的细菌微观形态图
Fig.7 Microscopic morphology of bacteria after preservative treatment
2.7 不同因素对复配天然防腐剂抑菌活性的影响
2.7.1 温度对复配防腐剂抑菌活性的影响
酱腌芥菜的加工及杀菌过程可能需要加热,因此需要考察温度对复配天然防腐剂抑菌活性的影响。如图8所示,复配防腐剂对贝莱斯芽孢杆菌和鲍曼不动杆菌在-20~80 ℃和-20~60 ℃处理30 min相对抑菌活性与对照组相比没有显著性差异(P>0.05)。复配防腐剂经高温100 ℃处理 30 min,121 ℃高温高压处理20 min后,对贝莱斯芽孢杆菌的相对抑菌活性分别为85.7%、83.1%;对鲍曼不动杆菌的相对抑菌活性分别为89.0%、85.0%。表明复配天然防腐剂具备良好的热稳定性。这种良好的热稳定性可能源于以下因素:ε-聚赖氨酸由25~35个L-赖氨酸残基构成,等电点为9,即便在100~120 ℃的高温高压条件下,仍能维持较长的聚合物链长度,进而具备较高的热稳定性[36]。杨志彩等[37]通过抑菌活性实验证实,乳酸链球菌素具有良好的热稳定性。郑铁生等[38]的研究显示,经过60~100 ℃以及121 ℃高温处理的壳聚糖,对金黄色葡萄球菌和大肠杆菌的抑菌活性无显著性影响。袁瑶等[39]的研究也发现,肉桂醛具有较好的热稳定性。
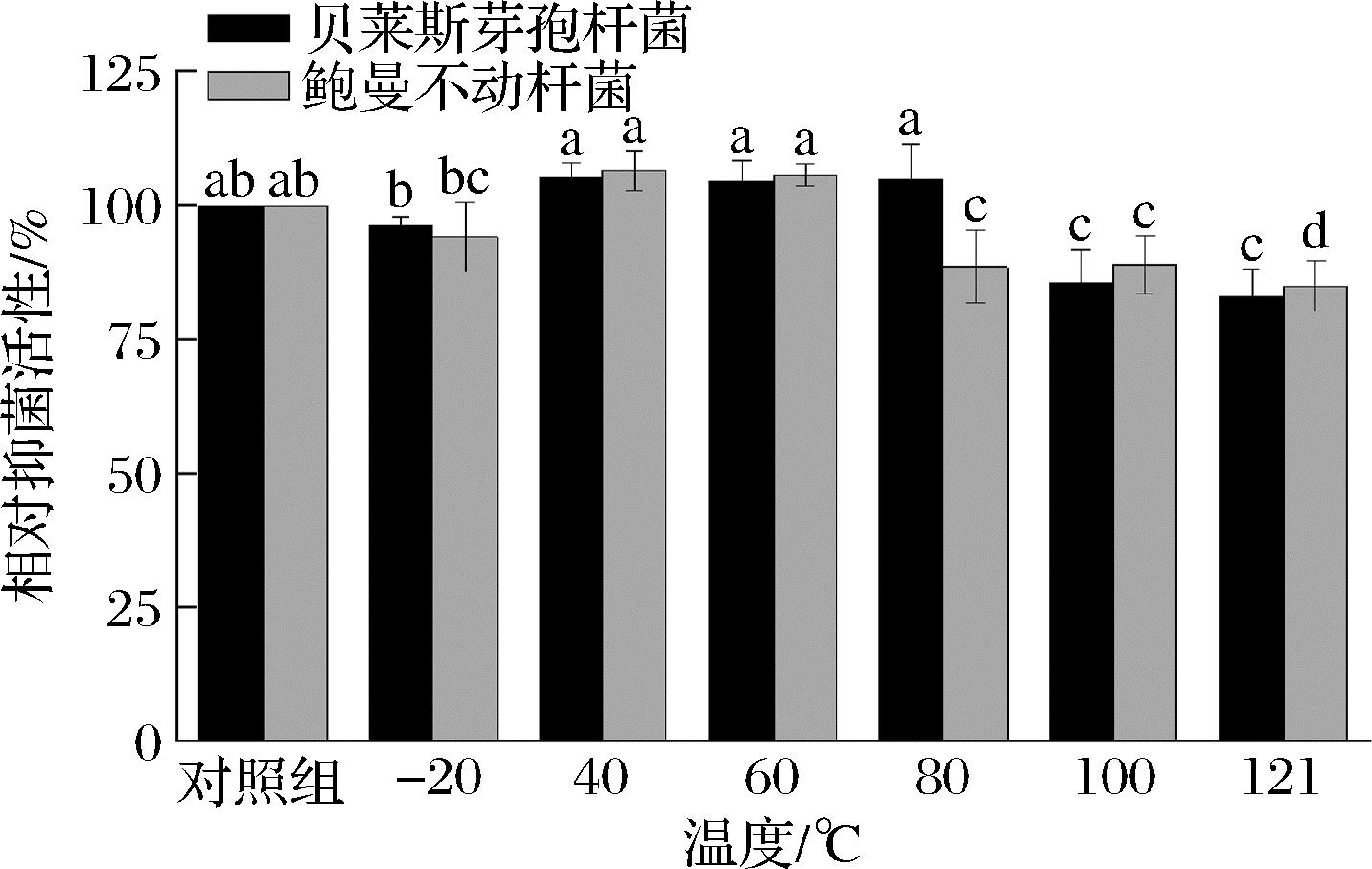
图8 温度对防腐剂抑菌活性的影响
Fig.8 Effect of temperature on the antibacterial activity of preservatives
注:同一指标字母不同表示差异显著(P<0.05)(下同)。
2.7.2 pH处理对复配防腐剂抑菌活性的影响
不同的食品存在不同的酸碱性环境,为了探究不同pH值对复配天然防腐剂抑菌活性的影响,选择常见的酱腌芥菜酸碱性范围(pH值为2~8)进行实验,结果如图9所示。当pH值为3~5和7时,复配天然防腐剂对腐败菌的相对抑菌活性没有显著影响(P>0.05);当pH 6时,复配天然防腐剂对贝莱斯芽孢杆菌和鲍曼不动杆菌的相对抑菌活性比对照组分别提高了11.07%和19.63%;当pH>7时,复配天然防腐剂的相对抑菌活性降低。结果表明复配天然防腐剂适用于偏酸性的环境。酱腌芥菜属于偏酸性食品,而本研究中复配天然防腐剂在偏酸性条件下抑菌效果比碱性条件下抑菌效果好,可能还存在酸与复配天然防腐剂的协同抑菌效应[40]。
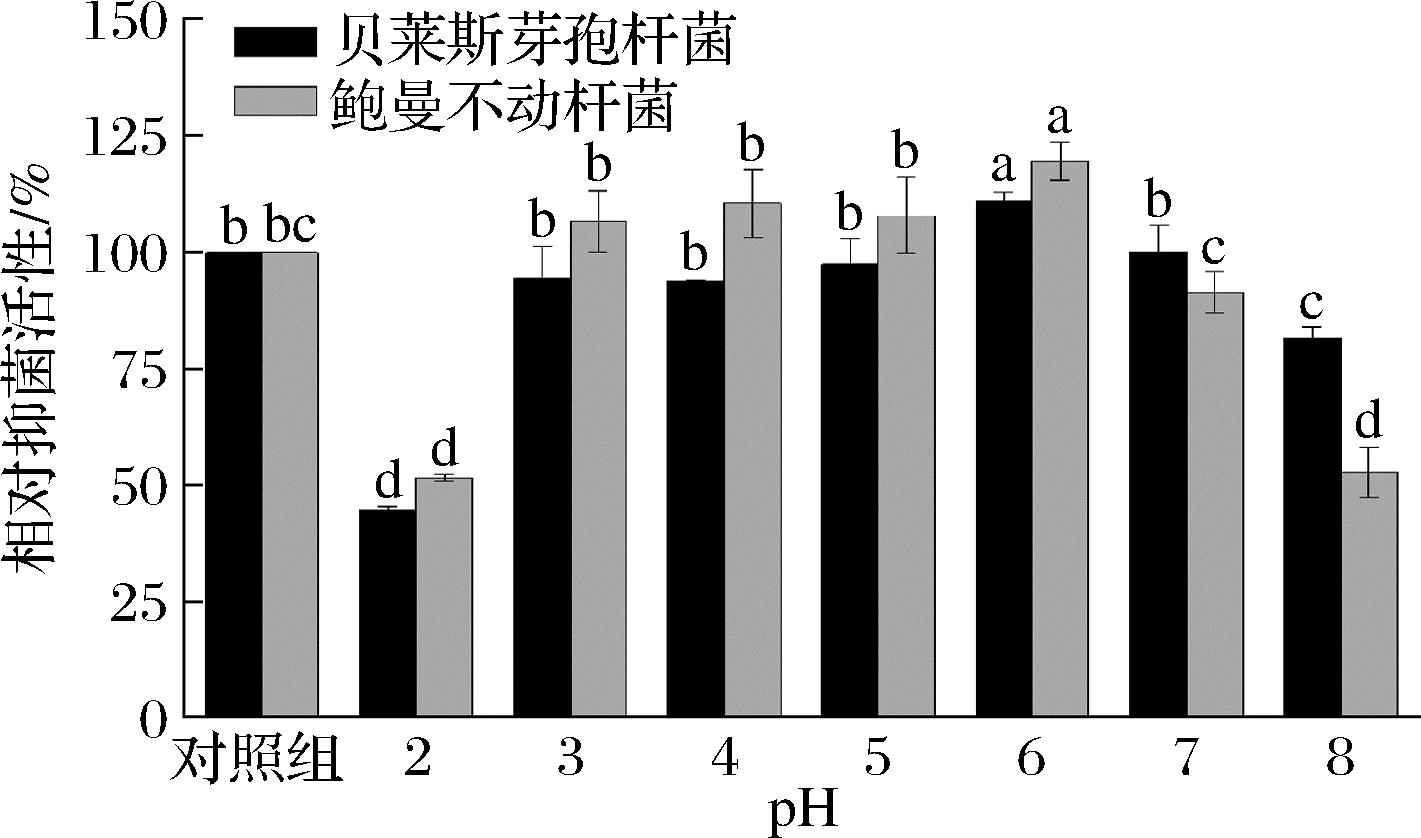
图9 pH值对防腐剂抑菌活性的影响
Fig.9 Effect of pH value on the antibacterial activity of preservatives
2.7.3 盐质量浓度对复配防腐剂抑菌活性的影响
通过梯度调节NaCl质量浓度(0~6.0 mg/mL),来考察盐质量浓度变化对复配天然防腐剂抑菌活性的影响,结果如图10所示。当NaCl质量浓度<4.0 mg/mL时,复配天然防腐剂对腐败菌的相对抑菌活性没有显著性影响(P>0.05);当NaCl质量浓度达到6.0 mg/mL时,复配天然防腐剂对贝莱斯芽孢杆菌和鲍曼不动杆菌的相对抑菌活性分别为72.23%和80.07%。结果表明,适当盐质量浓度对复配天然防腐剂抑菌效果没有显著影响,但盐质量浓度过高则会影响防腐剂抑菌效果。可能是因为金属Na+通过静电引力与菌体表面带负电的磷脂双分子层发生电荷中和,形成离子扩散层,导致细菌素活性肽的正电结构域与菌膜间的静电吸引势能降低,从而削弱其跨膜吸附效率,致使抑菌活性下降[41]。与杜旭婷等[42]研究结果相似。
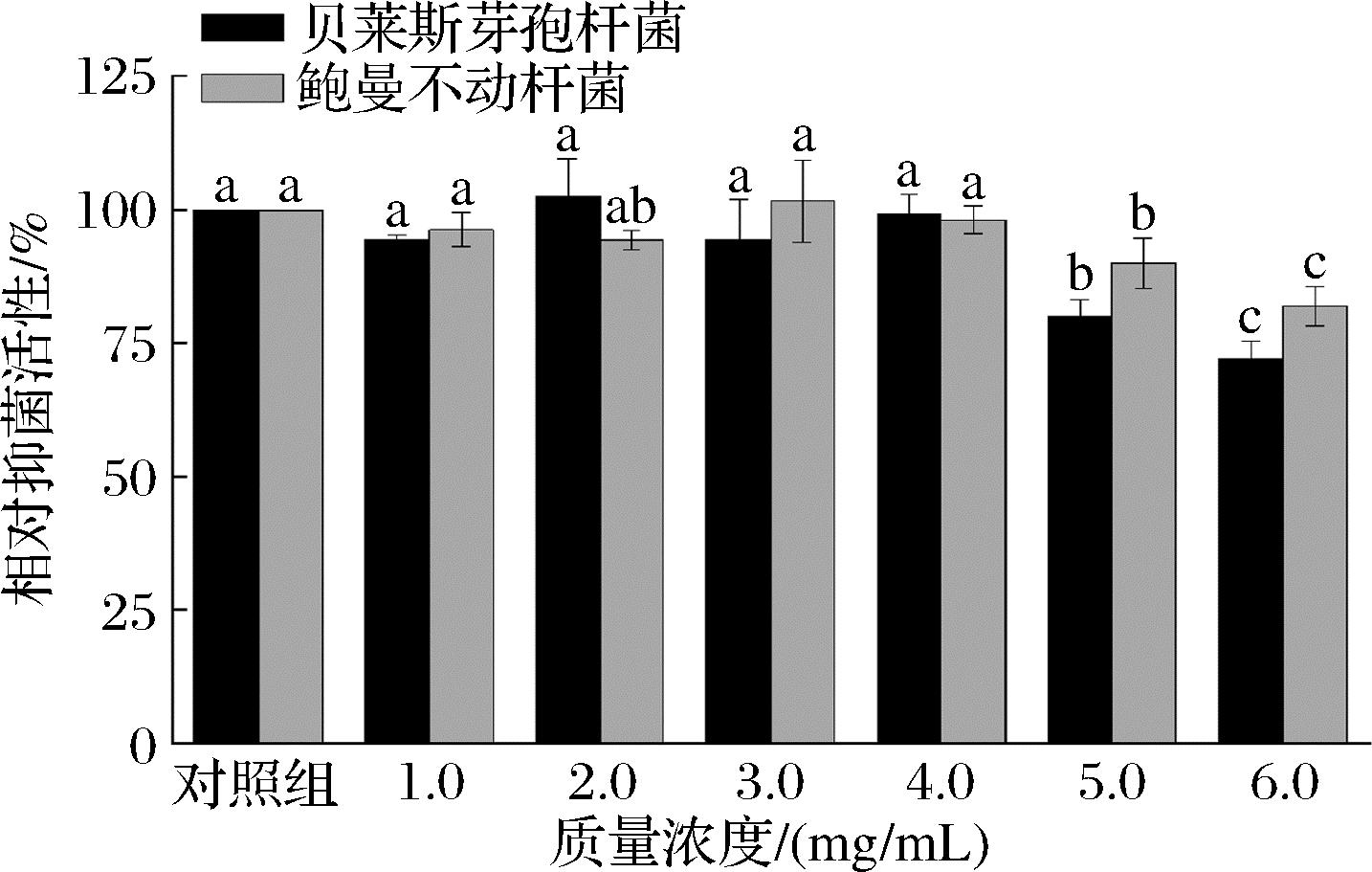
图10 盐质量浓度对防腐剂抑菌活性的影响
Fig.10 Effect of salt mass concentration on the antibacterial activity of preservatives
3 结论
本研究探讨了复配天然防腐剂对贝莱斯芽孢杆菌、鲍曼不动杆菌的抑菌机理及其稳定性。结果表明,复配天然防腐剂通过协同作用显著破坏腐败菌的细胞结构并抑制其代谢活性。具体而言,复配天然防腐剂处理组相较于化学防腐剂及空白对照组,细胞膜完整性受损更严重。此外,复配天然防腐剂破坏了细胞壁结构,使胞外AKP活力升高,并通过抑制CAT活力下降和诱导SOD活力升高,加剧菌体氧化应激,导致代谢失衡。扫描电镜观察显示,复配天然防腐剂处理组菌体表面出现大面积孔洞和内容物外泄,形态损伤程度显著高于化学防腐剂组。复配天然防腐剂在稳定性方面,-20~80 ℃时热稳定性良好,100 ℃处理30 min后相对抑菌活性仍保持83%以上;当pH值为3~5和7时,对腐败菌的相对抑菌活性没有显著影响(P>0.05),能适应酱腌芥菜低pH特性;盐质量浓度≤4 mg/mL时相对抑菌活性无显著影响(P>0.05)。该研究证实,复配天然防腐剂通过多靶点破坏菌体结构并干扰代谢通路,同时具备良好的环境适应性,为酱腌芥菜工业化生产中天然防腐体系的应用提供了理论依据,对减少化学防腐剂依赖、提升食品安全性具有重要意义。
[1] 赖慧婷, 刘伟, 罗艺璇, 等.发酵芥菜中微生物多样性及风味研究进展[J].食品工业, 2025, 46(3):247-252.LAI H T, LIU W, LUO Y X, et al.Advances in research on microbial diversity and flavor substances in fermented mustard[J].The Food Industry, 2025,46(3):247-252.
[2] ZHANG C C, ZHANG J M, LIU D Q.Biochemical changes and microbial community dynamics during spontaneous fermentation of Zhacai, a traditional pickled mustard tuber from China[J].International Journal of Food Microbiology, 2021, 347:109199.
[3] 敖晓琳, 蔡义民, 夏姣, 等.引起泡菜“生花”腐败微生物的分离鉴定[J].食品科学, 2013, 34(21):204-208.AO X L, CAI Y M, XIA J, et al.Isolation and identification of spoilage microorganisms from Sichuan pickles[J].Food Science, 2013, 34(21):204-208.
[4] 唐睿. 腌制华容大叶芥菜微生物多样性分析[D].长沙:湖南农业大学, 2021.TANG R.Analysis on microbial diversity of pickled Huarong Daye mustard[D].Changsha:Hunan Agricultural University, 2021.
[5] WU R N, YU M L, LIU X Y, et al.Changes in flavour and microbial diversity during natural fermentation of Suan-Cai, a traditional food made in Northeast China[J].International Journal of Food Microbiology, 2015, 211:23-31.
[6] 蔡炯, 迟原龙, 汪冬冬, 等.腐败四川泡菜菌相构成及主要腐败菌特性分析[J].食品科技, 2017, 42(1):279-283.CAI J, CHI Y L, WANG D D, et al.Microflora and characteristics of main spoilage microorganisms in putrid Sichuan pickle[J].Food Science and Technology, 2017, 42(1):279-283.
[7] SONI A, SMITH J, THOMPSON A, et al.Microwave-induced thermal sterilization- A review on history, technical progress, advantages and challenges as compared to the conventional methods[J].Trends in Food Science &Technology, 2020, 97:433-442.
[8] 任彩霞, 王立霞, 丁毅.西安市售酱腌菜中防腐剂和糖精钠的检测与分析[J].保鲜与加工, 2022, 22(8):76-81.REN C X, WANG L X, DING Y.Determination and analysis of preservatives and saccharin sodium content in commercial pickles in Xi’an[J].Storage and Process, 2022, 22(8):76-81.
[9] WANG D, MA Y, SUN X, et al.Effect of dense phase carbon dioxide treatment on physicochemical and textural properties of pickled carrot[J].CyTA-Journal of Food, 2019, 17(1):988-996.
[10] 曹兆玉. 食品中天然防腐剂的研究进展[J].食品安全导刊, 2024(27):147-149.CAO Z Y.Research progress of natural preservatives in food[J].China Food Safety Magazine, 2024(27):147-149.
[11] 姚惠芳, 李文娟, 孟哲, 等.ε-聚赖氨酸的抑菌机理及其在果蔬保鲜中应用研究进展[J].现代食品, 2023, 29(23):20-22.YAO H F, LI W J, MENG Z, et al.Research progress in ε-polylysine:Antibacterial mechanism and application in preservation of fruits and vegetables[J].Modern Food, 2023, 29(23):20-22.
[12] 张鹏敏, 王文秀, 孙剑锋, 等.壳聚糖/姜黄素光动力复合涂膜对金黄色葡萄球菌的抑菌效果及机理[J].食品科学, 2024, 45(6):233-243.ZHANG P M, WANG W X, SUN J F, et al.Antibacterial effect and mechanism of chitosan/curcumin composite photodynamic coating on Staphylococcus aureus[J].Food Science, 2024, 45(6):233-243.
[13] 陈楷珊, 蔡郭瀚, 陈相宇, 等.中药提取物小檗碱和肉桂醛的抑菌活性进展综述[J].工业微生物, 2024, 54(4):164-166.CHEN K S, CAI G H, CHEN X Y, et al.A review on the antibacterial activity of traditional Chinese medicine extracts berberine and cinnamaldehyde[J].Industrial Microbiology, 2024, 54(4):164-166.
[14] CHEN X H, LIU P P, LUO X F, et al.Study on the antibacterial activity and mechanism of Cinnamaldehyde against Methicillin-resistant Staphylococcus aureus[J].European Food Research and Technology, 2024, 250(4):1069-1081.
[15] 杜金婷, 张雁, 李雁, 等.茶皂素对食源性腐败酵母的抑菌能力及作用机理[J].现代食品科技, 2022, 38(5):118-125;327.DU J T, ZHANG Y, LI Y, et al.Antibacterial activity and mechanism of tea saponin against foodborne spoilage yeasts[J].Modern Food Science and Technology, 2022, 38(5):118-125;327.
[16] 许超群, 陈飞平, 梁旭茹, 等.肉桂醛与ε-聚赖氨酸盐酸盐的抑菌活性及其协同抑菌机制初探[J].现代食品科技, 2023, 39(7):24-31.XU C Q, CHEN F P, LIANG X R, et al.Preliminary investigation of the antimicrobial activities and synergies of cinnamaldehyde and ε-polylysine hydrochloride[J].Modern Food Science and Technology, 2023, 39(7):24-31.
[17] 王志新, 刘丹丹, 贾紫伟, 等.爱媛类芽孢杆菌抗菌肽对扩展青霉孢子的抑制作用机制[J].食品科学, 2023, 44(15):19-27.WANG Z X, LIU D D, JIA Z W, et al.Antimicrobial mechanism of antimicrobial peptide from Paenibacillus ehimensis against Penicillium expansum spores [J].Food Science, 2023, 44(15):19-27.
[18] MOTAVALLIHAGHI S, KHODADADI I, GOUDARZI F, et al.The role of Acanthamoeba castellanii (T4 genotype) antioxidant enzymes in parasite survival under H2O2-induced oxidative stress[J].Parasitology International, 2022, 87:102523.
[19] 陈小敏, 黄泽璇, 谭礼浩, 等.表没食子儿茶素没食子酸酯对食源性致病菌抑菌机理及应用研究[J].食品与机械, 2024, 40(8):127-134.CHEN X M, HUANG Z X, TAN L H, et al.Study on the inhibitory mechanism of epigallocatechin gallate against foodborne pathogens and its application[J].Food &Machinery, 2024, 40(8):127-134.
[20] 宁亚维, 杨坤, 何建卓, 等.基于细胞膜损伤的蔗糖月桂酸酯对金黄色葡萄球菌的作用机制[J].食品科学, 2019, 40(5):38-44.NING Y W, YANG K, HE J Z, et al.Sucrose laurate exerts antibacterial activity against Staphylococcus aureus by destroying the cell membrane[J].Food Science, 2019, 40(5):38-44.
[21] ZHAO M M, BAI J W, BU X Y, et al.Microwave-assisted aqueous two-phase extraction of phenolic compounds from Ribes nigrum L.and its antibacterial effect on foodborne pathogens[J].Food Control, 2021, 119:107449.
[22] 高娟娟, 贾丽艳, 畅盼盼, 等.枯草芽孢杆菌细菌素A32的抑菌机理研究[J].中国食品学报, 2021, 21(10):56-64.GAO J J, JIA L Y, CHANG P P, et al.Studies on the inhibition mechanism of bacteriocin A32 producing by Bacillus subtilis[J].Journal of Chinese Institute of Food Science and Technology, 2021, 21(10):56-64.
[23] DIAO W R, HU Q P, ZHANG H, et al.Chemical composition, antibacterial activity and mechanism of action of essential oil from seeds of fennel (Foeniculum vulgare Mill.)[J].Food Control, 2014, 35(1):109-116.
[24] WANG F, WEI F Y, SONG C X, et al.Dodartia orientalis L.essential oil exerts antibacterial activity by mechanisms of disrupting cell structure and resisting biofilm[J].Industrial Crops and Products, 2017, 109:358-366.
[25] SHENG J W, LIU D M, JING L, et al.Striatisporolide A, a butenolide metabolite from Athyrium multidentatum (Doll.) Ching, as a potential antibacterial agent[J].Molecular Medicine Reports, 2019, 20(1):198-204.
[26] 黄伟英, 刘晓婷, 关玉凤, 等.壳聚糖和ε-聚赖氨酸对肉食杆菌抑菌机制初步研究[J].食品工业科技, 2024, 45(5):144-152.HUANG W Y, LIU X T, GUAN Y F, et al.Preliminary study on the mechanism of chitosan and ε-polylysine inhibition against Carbibacterium divergens[J].Science and Technology of Food Industry, 2024, 45(5):144-152.
[27] BARREIRO D S, OLIVEIRA R N S, PAULETA S R.Bacterial peroxidases-Multivalent enzymes that enable the use of hydrogen peroxide for microaerobic and anaerobic proliferation[J].Coordination Chemistry Reviews, 2023, 485:215114.
[28] 陈雪琴, 赵圆圆, 张珍, 等.肉桂精油的化学成分分析及其对沙门氏菌细胞膜损伤机制的研究[J].食品与发酵工业, 2022, 48(14):24-32.CHEN X Q, ZHAO Y Y, ZHANG Z, et al.Analysis of cinnamon essential oil composition and its mechanism of cell membrane damage in Salmonella enterica[J].Food and Fermentation Industries, 2022, 48(14):24-32.
[29] JIANG Z Y, NI L X, LI X L, et al.Mechanistic insight into the inhibitory effect of artemisinin sustained-release inhibitors with different particle sizes on Microcystis aeruginosa[J].Environmental Science and Pollution Research, 2022, 29(58):87545-87554.
[30] 葛文沛, 王洪玲, 崔欣然, 等.茄腐镰刀菌拮抗菌株M1的抑菌机理及其促生作用研究[J].中国酿造, 2024, 43(10):142-148.GE W P, WANG H L, CUI X R, et al.Antibacterial mechanism and growth-promoting effects of antagonistic strain M1 against Fusarium solani[J].China Brewing, 2024, 43(10):142-148.
[31] 黄伟英, 叶红雨, 刘晓婷, 等.乳酸链球菌素对肉食杆菌和腐生葡萄球菌的抑菌机制研究[J].食品安全质量检测学报, 2023, 14(14):95-104.HUANG W Y, YE H Y, LIU X T, et al.Study on the antibacterial mechanism of Nisin against carnivorous bacteria and saprophytic Staphylococcus[J].Journal of Food Safety and Quality, 2023, 14(14):95-104.
[32] MONTLLOR-ALBALATE C, COLIN A E, CHANDRASEKHARAN B, et al.Extra-mitochondrial Cu/Zn superoxide dismutase (Sod1) is dispensable for protection against oxidative stress but mediates peroxide signaling in Saccharomyces cerevisiae[J].Redox Biology, 2019, 21:101064.
[33] 陈山乔, 孙志栋.Nα-月桂酰-L-精氨酸乙酯盐酸盐与山梨酸钾对榨菜的协同保鲜及诱导致腐菌的氧化应激作用[J].现代食品科技, 2020, 36(10):125-132.CHEN S Q, SUN Z D.Synergistic actions of Nα-lauroyl-L-arginine ethyl ester hydrochloride and potassium sorbate in preserving pickled mustard tubers and inducing oxidative stress against spoilage bacteria[J].Modern Food Science and Technology, 2020, 36(10):125-132.
[34] ZHANG H H, HATOKO M, YIN D R, et al.Antibacterial activity and biocompatibility of nanoporous titanium doped with silver nanoparticles and coated with N-acetyl cysteine[J].Journal of Hard Tissue Biology, 2018, 27(4):351-358.
[35] 石成龙, 汪锡武, 李安琪, 等.ε-聚赖氨酸对阪崎克罗诺杆菌细胞结构与生物被膜形成的影响[J].生物技术通报, 2022, 38(9):147-157.SHI C L, WANG X W, LI A Q, et al.Effect of ε-polylysine on the cell structure and biofilm formation of Cronobacter sakazakii[J].Biotechnology Bulletin, 2022, 38(9):147-157.
[36] YANG J, PUNIA BANGAR S, KHAN M R, et al.Biopolymer-based packaging films/edible coatings functionalized with ε-polylysine:New options for food preservation[J].Food Research International, 2024, 187:114390.
[37] 杨志彩, 郭舒阳, 李素云, 等.不同环境因素和食品基质对Nisin抑制单增李斯特菌活性的影响[J].食品与发酵工业, 2022, 48(12):209-214.YANG Z C, GUO S Y, LI S Y, et al.Effects of environmental factors and food matrices on the inhibitory activity of Nisin against Listeria monocytogenes[J].Food and Fermentation Industries, 2022, 48(12):209-214.
[38] 郑铁生, 王亚娜, 宗爱萍.壳聚糖天然抗菌的活性及其稳定性[J].商场现代化, 2005(11):188-189.ZHENG T S, WANG Y N, ZONG A P.Natural antibacterial activity and stability of chitosan[J].Market Modernization, 2005(11):188-189.
[39] 袁瑶, 文雨晴, 石一凡, 等.15种植物精油添加剂热稳定性和体外抑菌作用研究[J].畜牧与兽医, 2019, 51(5):70-76.YUAN Y, WEN Y Q, SHI Y F, et al.The thermal stability and antibacterial effect of 15 plant essential oil additives[J].Animal Husbandry and Veterinary Medicine, 2019, 51(5):70-76.
[40] THOMAS L V, WIMPENNY J W.Investigation of the effect of combined variations in temperature, pH, and NaCl concentration on nisin inhibition of Listeria monocytogenes and Staphylococcus aureus[J].Applied and Environmental Microbiology, 1996, 62(6):2006-2012.
[41] 刘国荣, 宋振芹, 郜亚昆, 等.食品加工环境因素对双歧杆菌细菌素BB04抑菌作用的影响[J].食品工业科技, 2016, 37(2):125-129;137.LIU G R, SONG Z Q, GAO Y K, et al.Effect of environmental factors in food processing on the inhibitory actvity of bifidocin BB04[J].Science and Technology of Food Industry, 2016, 37(2):125-129;137.
[42] 杜旭婷, 岳子尧, 董晶, 等.食品加工、贮藏对乳杆菌源抗菌肽抑菌活性的影响及安全性评价[J].中国食品学报, 2024, 24(1):110-118.DU X T, YUE Z Y, DONG J, et al.Effect of food processing and preservation on antimicrobial activity of Lactobacillus-derived antimicrobial peptide and its safety evaluation[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(1):110-118.