棉籽糖蜜是棉籽蛋白加工过程中产生的一种黑褐色的废液,其中含有丰富的蔗糖、粗蛋白、粗脂肪等营养物,以及棉子糖和水苏糖等低聚糖益生元,具有作为饲料添加剂的潜力,亦可提取益生元应用于动物养殖或者人类保健食品行业,但由于其成分中含有大量的游离棉酚(free gossypol,FG),限制了其直接使用[1]。已有研究表明游离棉酚具有细胞神经类毒性,过量摄入后,会刺激胃黏膜,引发胃肠炎,产生氧化应激反应,造成肝损伤,引发生殖功能障碍等中毒现象[2]。因此,如何实现棉籽糖蜜中游离棉酚脱除是实现其安全利用的前提。
目前棉籽糖蜜(加工废液)处理,绝大多数企业将其作为工业废水进行简单处理后排放,这不但造成了资源的浪费,同时也增加了环境污染风险。另外一些研究人员使用物理和化学的方法对其中低聚糖进行提取后用于食品行业,从而实现其资源化利用,但提取过程中仍然会产生大量废弃物,形成二次污染[1]。国内外目前关于利用微生物来实现游离棉酚降解的研究较多,绝大多数集中在棉籽粕和棉籽壳等材料,并且研究结果表明利用生物发酵法脱除游离棉酚不但高效、安全,而且发酵后还能提升饲料的营养和品质[3]。杨文婷[4]比较了棉酚降解酶和益生菌对棉粕中游离棉酚降解率的影响,结果表明棉酚降解酶对棉籽粕中游离棉酚降解率高于益生菌。屯妮萨·麦提赛伊迪[5]使用平菇(Pleurotus ostreatus)降解棉籽壳中游离棉酚,显著降低了棉籽壳中游离棉酚的同时提高了粗蛋白含量。ASHAYERIZADEH等[6]使用酵母菌、芽孢杆菌和乳酸菌复合发酵棉籽粕,不仅可以显著降低游离棉酚含量,而且提高了饲料的饲用品质。但是,目前关于利用益生菌发酵棉籽糖蜜的研究尚未见报道。
合生元是一种由益生菌以及可促进益生菌生长的活性物质共同构成的混合物,并且两者之间具有互补或者协同作用[7]。张娜[8]发现植物乳植杆菌在肠道中利用低聚糖代谢,可促进自身在肠道的定植,显著提高结肠短链脂肪酸水平,同时添加低聚糖可以促进植物乳植杆菌的生长,增加该菌发酵乳冷藏期的活菌数,增强抗氧化和蛋白质水解能力。大量研究已经表明合生元产品应用于畜禽养殖或者人体健康均具有提高免疫、改善肠道菌群、提高抗氧化能力等有益作用[9-11]。因此,本研究拟筛选出能够以棉籽糖蜜为唯一营养源,具有高效降解其中游离棉酚,同时能够对低聚糖具有较高保留能力的益生菌,以期一步法实现棉籽糖蜜向低聚糖合生元产品转化,为棉籽糖蜜资源化利用提供技术参考。
1 材料与方法
1.1 材料
1.1.1 棉籽糖蜜
棉籽糖蜜购自新疆泰昆集团昌吉饲料有限责任公司,其主要成分如电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.042297,下同)所示。
表1 菌株对棉籽糖蜜中游离棉酚降解能力测定
Table 1 Determination of the degradation ability of each strain to free gossypol in cottonseed processing wastewater
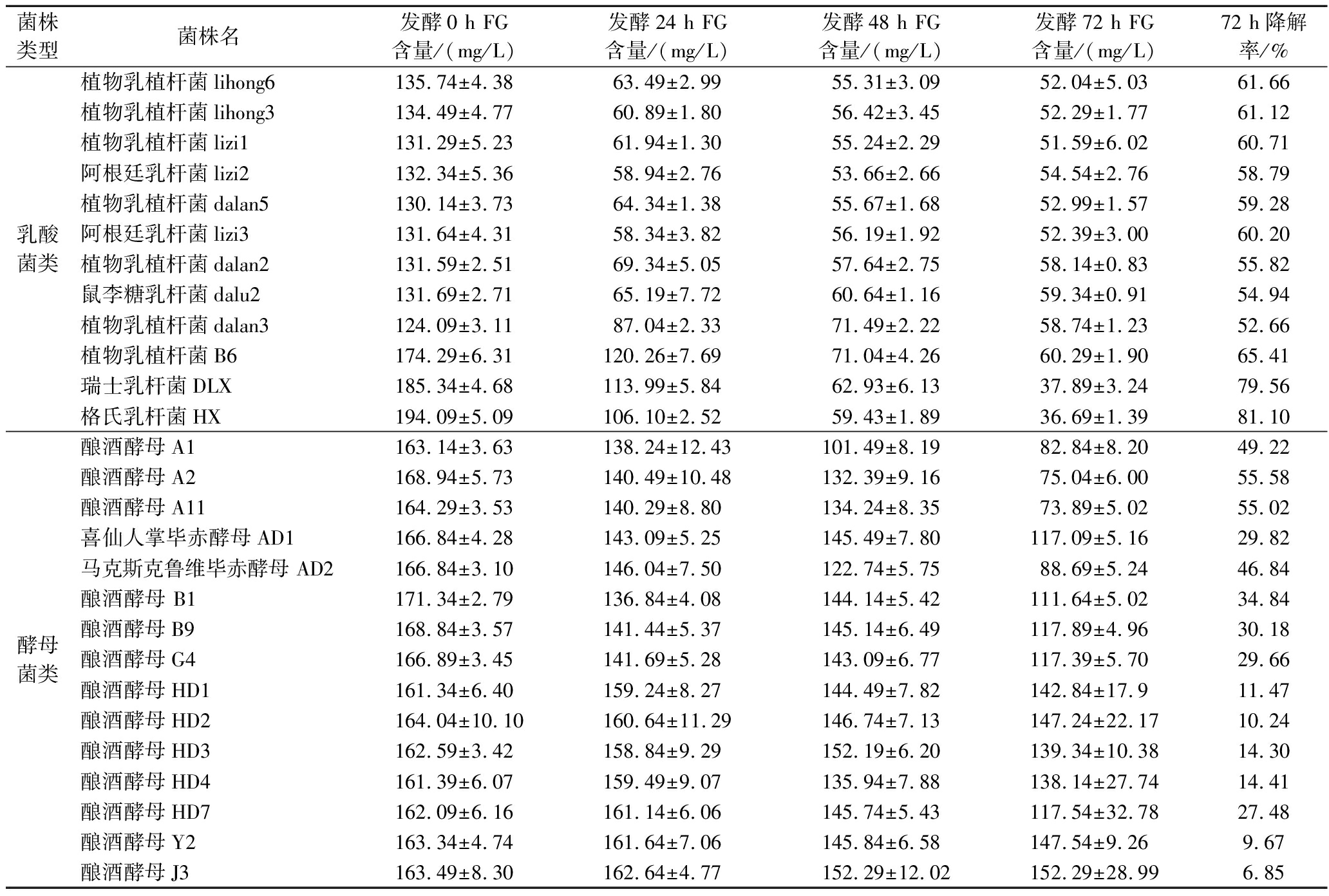
菌株类型菌株名发酵0 h FG含量/(mg/L)发酵24 h FG含量/(mg/L)发酵48 h FG含量/(mg/L)发酵72 h FG含量/(mg/L)72 h降解率/%乳酸菌类植物乳植杆菌lihong6135.74±4.3863.49±2.9955.31±3.0952.04±5.0361.66植物乳植杆菌lihong3134.49±4.7760.89±1.8056.42±3.4552.29±1.7761.12植物乳植杆菌lizi1131.29±5.2361.94±1.3055.24±2.2951.59±6.0260.71阿根廷乳杆菌lizi2132.34±5.3658.94±2.7653.66±2.6654.54±2.7658.79植物乳植杆菌dalan5130.14±3.7364.34±1.3855.67±1.6852.99±1.5759.28阿根廷乳杆菌lizi3131.64±4.3158.34±3.8256.19±1.9252.39±3.0060.20植物乳植杆菌dalan2131.59±2.5169.34±5.0557.64±2.7558.14±0.8355.82鼠李糖乳杆菌dalu2131.69±2.7165.19±7.7260.64±1.1659.34±0.9154.94植物乳植杆菌dalan3124.09±3.1187.04±2.3371.49±2.2258.74±1.2352.66植物乳植杆菌B6174.29±6.31120.26±7.6971.04±4.2660.29±1.9065.41瑞士乳杆菌DLX185.34±4.68113.99±5.8462.93±6.1337.89±3.2479.56格氏乳杆菌HX194.09±5.09106.10±2.5259.43±1.8936.69±1.3981.10酵母菌类酿酒酵母A1163.14±3.63138.24±12.43101.49±8.1982.84±8.2049.22酿酒酵母A2168.94±5.73140.49±10.48132.39±9.1675.04±6.0055.58酿酒酵母A11164.29±3.53140.29±8.80134.24±8.3573.89±5.0255.02喜仙人掌毕赤酵母AD1166.84±4.28143.09±5.25145.49±7.80117.09±5.1629.82马克斯克鲁维毕赤酵母 AD2166.84±3.10146.04±7.50122.74±5.7588.69±5.2446.84酿酒酵母 B1171.34±2.79136.84±4.08144.14±5.42111.64±5.0234.84酿酒酵母B9168.84±3.57141.44±5.37145.14±6.49117.89±4.9630.18酿酒酵母G4166.89±3.45141.69±5.28143.09±6.77117.39±5.7029.66酿酒酵母HD1161.34±6.40159.24±8.27144.49±7.82142.84±17.911.47酿酒酵母HD2164.04±10.10160.64±11.29146.74±7.13147.24±22.1710.24酿酒酵母HD3162.59±3.42158.84±9.29152.19±6.20139.34±10.3814.30酿酒酵母HD4161.39±6.07159.49±9.07135.94±7.88138.14±27.7414.41酿酒酵母HD7162.09±6.16161.14±6.06145.74±5.43117.54±32.7827.48酿酒酵母Y2163.34±4.74161.64±7.06145.84±6.58147.54±9.269.67酿酒酵母J3163.49±8.30162.64±4.77152.29±12.02152.29±28.996.85
1.1.2 菌种来源
益生菌包括乳酸菌类12株,酵母菌类15株,具体菌种信息如电子版增强出版附表2所示,所有菌株均来自新疆维吾尔自治区农业科学院微生物所菌种资源保藏库。
表2 供试菌株的溶血活性
Table 2 Hemolytic activity of the test strains
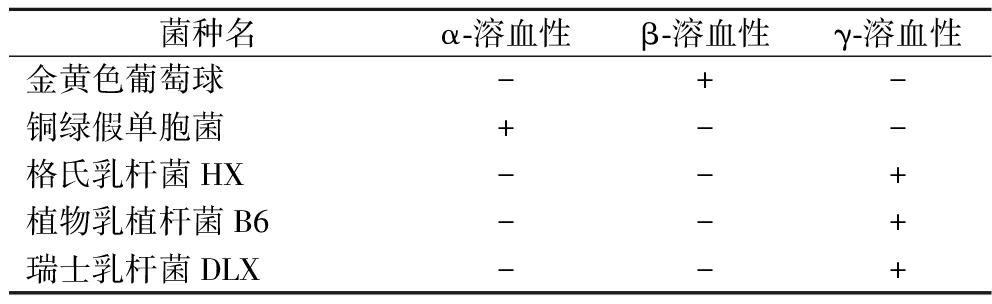
菌种名α-溶血性β-溶血性γ-溶血性金黄色葡萄球-+-铜绿假单胞菌+--格氏乳杆菌HX--+植物乳植杆菌B6--+瑞士乳杆菌DLX--+
注:+为阳性;-为阴性。
1.1.3 主要试剂和仪器
MgSO4、NaCl、KH2PO4、NaHCO3,天津市鑫铂特化工有限公司;植物棉子糖酶联免疫试剂盒、植物水苏糖酶联免疫试剂盒,上海市科桥生物有限公司。哥伦比亚血琼脂培养基、NA培养基、MRS培养基、YPD培养基,青岛海博生物技术有限公司。
Epoch微孔板分光光度计,美国博腾仪器有限公司;4120600型pH计,上海雷磁仪器厂;MA104E 30697417电子分析天平,瑞士梅特勒-托利多集团;LRH-250电热恒温培养箱,上海一恒科学仪器有限公司;HH-2电热恒温水槽,上海博讯实业有限公司;2-16R台式高速低温离心机,湖南赫西仪器装备有限公司;T600A紫外/可见分光光度计,英国柏诺集团;SW-CJ-2D双人净化工作台,浙江孚夏医疗科技有限公司。
1.1.4 培养基
棉籽糖蜜筛选培养基(g/L):棉籽糖蜜60、MgSO4 0.5、NaCl 1、KH2PO4 1,pH值调至6.0±0.2。乳酸菌类种子液培养使用MRS培养基,酵母菌类种子液培养使用YPD培养基。
1.2 游离棉酚降解菌株筛选
1.2.1 游离棉酚降解实验设计
将待筛选的27株菌使用其对应的培养基进行种子活化后,按照体积分数5%接种至棉籽糖蜜筛选培养基中,乳酸菌类37 ℃静置培养72 h,酵母菌类30 ℃、150 r/min振荡培养72 h。
1.2.2 游离棉酚检测
采用间苯三酚法[12]对益生菌发酵不同时间后发酵液中游离棉酚含量进行检测,根据发酵液发酵前后游离棉酚的含量变化计算棉酚降解率,筛选出游离棉酚降解率高的菌株进行后续实验,按照公式(1)计算游离棉酚降解率。
游离棉酚降解率![]()
(1)
式中:C0,0 h时发酵液中游离棉酚含量,mg/L;C1,72 h时发酵液中游离棉酚含量,mg/L。
1.3 菌株安全性检测
1.3.1 溶血实验
将供试菌株调至OD600nm=0.5的菌悬液,将悬液点接在哥伦比亚血琼脂平板上,37 ℃(乳酸菌)或者30 ℃(酵母菌类)培养24 h,观察溶血圈的形成情况,若产生和铜绿假单胞菌一样的草绿色溶血圈则为α溶血,若产生和金黄色葡萄球菌一样的透明圈则为β溶血,无溶血圈则为不溶血[13]。
1.3.2 菌株耐药性检测
在培养基上均匀涂布活化后的供试菌悬液,将青霉素、四环素、亚胺培南、万古霉素、利福平、克林霉素和阿莫西林7种抗生素药敏片放置于平板上,每组设置3个重复,37 ℃培养24 h,观察并记录抑菌圈大小,根据抑菌圈大小判定耐药性。
1.4 低聚糖保留能力
1.4.1 棉子糖保留率
参照植物棉子糖酶联免疫试剂盒法进行标准曲线的绘制及发酵液中棉子糖含量的测定,按公式(2)计算棉子糖保留率。
棉子糖保留率![]()
(2)
式中:C2,0 h时发酵液中棉子糖含量,mg/L;C3,72 h时发酵液中棉子糖含量,mg/L。
1.4.2 水苏糖保留率
参照植物水苏糖酶联免疫试剂盒法进行标准曲线的绘制及发酵液中水苏糖含量的测定,按公式(3)计算水苏糖保留率。
水苏糖保留率![]()
(3)
式中:C4,0 h时发酵液中水苏糖含量,mg/L;C5,72 h时发酵液中水苏糖含量,mg/L。
1.5 发酵性能分析
1.5.1 最适生长温度测定
将供试菌株以体积分数5%的接种量接种于灭菌的棉籽糖蜜培养基中,然后将接种好的培养基分别置于20、25、30、37、42 ℃的摇床内,150 r/min培养24 h,取样,测定波长于600 nm处吸光度(OD600nm值),每组设置3个重复。
1.5.2 生长曲线测定
将供试菌株以体积分数5%的接种量接种于灭菌的棉籽糖蜜培养基中。在0、2、4、6、8、10、12、14、16、18、20、22、24 h取样,测定波长于600 nm处吸光度(OD600nm值),每组设置3个重复,以培养时间为横坐标,OD600nm值为纵坐标,绘制生长曲线。同时采用稀释梯度培养法对培养至0、12、24 h的活菌数进行测定,每组设定3个重复。
1.5.3 产酸能力测定
将供试菌株以体积分数5%的接种量接种于灭菌的棉籽糖蜜培养基中。在0、2、4、6、8、10、12、14、16、18、20、22、24 h取样,测定其pH值,每组设定3个重复,同时在0、12、24、36、48、60、72 h取样,使用GB 12456—2021《食品安全国家标准 食品中总酸的测定(含第1号修改单)》方法测发酵液的总酸含量。以培养时间为横坐标,pH值和总酸含量作为纵坐标,绘制产酸曲线。
1.6 益生性能分析
1.6.1 菌株抑菌能力测定
按照吴慧昊等[14]的方法,将大肠杆菌、金黄色葡萄球菌和沙门氏菌分别涂布于NA固体培养基上,将150 μL供试菌液加入在平板内打好的孔,盖上平皿,将平皿置于4 ℃冰箱扩散,之后放入37 ℃恒温培养箱培养24 h,观察小孔周围抑菌圈直径。
1.6.2 菌株耐酸和耐胆盐能力测定
将活化后的菌液(初始活菌数108 CFU/mL)按体积分数5%接入MRS肉汤培养基中,37 ℃培养24 h 后。取1 mL菌液分别接种至9 mL的MRS培养基(用1 mol/L的盐酸调节pH值分别为2、3、4;或者加入牛胆盐分别至质量分数的0.5%和1%),37 ℃静置培养4 h,分别在0、4 h用平板计数法测定活菌数,每组设置3个重复。存活率按公式(4)计算:
存活率![]()
(4)
式中:N0和Nt分别代表菌株处理前(0 h)和处理后(4 h)的菌落数。
1.7 菌株发酵棉籽糖蜜代谢物的测定
1.7.1 发酵液样品前处理
取100 μL样本置于EP管中,加入400 μL体积分数80%甲醇水溶液;涡旋振荡,冰浴静置5 min,15 000×g、4 ℃离心20 min;取一定量的上清液加质谱级水稀释至甲醇体积分数为53%;15 000×g、4 ℃离心20 min,收集上清液,进样至液相色谱-质谱联用仪进行分析。
1.7.2 色谱质谱条件
液相条件:色谱柱HypersilGoldcolumn(C18)。流动相A为0.1%甲酸,流动相B为甲醇。进样量2 μL,流速0.2 mL/min。梯度洗脱程序为:0~1.5 min,98% A;1.5~3 min,98%~15% A;3~10 min,15%~0% A;10~10.1 min,0%~98% A;10.1~11 min,98% A;11~12 min,98% A。
1.7.3 质谱条件
扫描范围选择m/z 100~1 500。ESI源的设置如下:喷雾电压3.5 kV;鞘气流速35 psi;辅助气流速10 L/min;离子传输管温度320 ℃;离子导入射频电平60;辅助气加热器温度350 ℃;极性为positive、negative;MS/MS二级扫描为数据依赖性扫描。
1.7.4 数据分析
原始质谱数据通过ProteoWizard软件转换为mzXML格式,先采用XCMS进行峰提取及峰定量,通过保留时间、质荷比等参数,对于不同样本进行峰对齐;然后根据设置10 ppm质量偏差及加合离子等信息与高质量二级谱图数据库进行比对,进行代谢物鉴定。随后用blank样本去除背景离子,最后得到代谢物的鉴定和相对定量结果。数据处理部分基于Linux操作系统(CentOS 6.6)以及软件R、Python进行。使用使用KEGG数据库(https://www.genome.jp/kegg/pathway.html)、HMDB数据库(https://hmdb.ca/metabolites)对鉴定到的代谢物进行注释。
2 结果与分析
2.1 游离棉酚降解菌株筛选
如表1所示,72 h内乳酸菌游离棉酚降解率均高于酵母菌,其中格氏乳杆菌HX、植物乳植杆菌B6和瑞士乳杆菌DLX对游离棉酚降解率较高,都为乳酸菌菌株,降解率分别达到81.10%、65.4%和79.56%,优于吴慧昊等[15]发现的乳酸菌对棉籽粕中游离棉酚降解率。
2.2 安全性评价
2.2.1 溶血性实验
如表2所示,与质控菌金黄色葡萄球菌(Staphylococcus aureus)和铜绿假单胞菌(Pseudomonas aeruginosa)相比,3株菌均未出现溶血现象,具有生物安全性。
2.2.2 药敏实验结果
如表3所示,格氏乳杆菌HX对利福平、万古霉素、阿莫西林、亚胺培南、青霉素、四环素敏感,仅对克林霉素中度敏感;植物乳植杆菌B6对利福平、阿莫西林、亚胺培南、青霉素、克林霉素敏感,对万古霉素和四环素中度敏感;瑞士乳杆菌DLX对这7种抗生素均敏感。本研究的3株菌株对大部分抗生素都敏感,说明其生物安全较高。
表3 供试菌株对七类抗生素药敏性判定结果
Table 3 Drug sensitivity of the tested strains to seven kinds of antibiotics
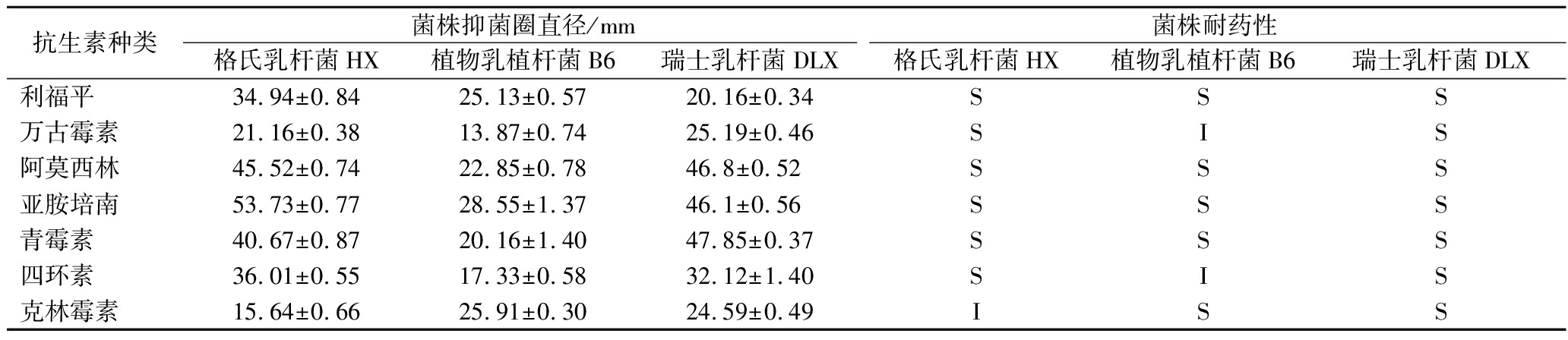
抗生素种类菌株抑菌圈直径/mm菌株耐药性格氏乳杆菌HX植物乳植杆菌B6瑞士乳杆菌DLX格氏乳杆菌HX植物乳植杆菌B6瑞士乳杆菌DLX利福平 34.94±0.8425.13±0.5720.16±0.34SSS万古霉素21.16±0.3813.87±0.7425.19±0.46SIS阿莫西林45.52±0.7422.85±0.7846.8±0.52SSS亚胺培南53.73±0.7728.55±1.3746.1±0.56SSS青霉素 40.67±0.8720.16±1.4047.85±0.37SSS四环素36.01±0.5517.33±0.5832.12±1.40SIS克林霉素15.64±0.6625.91±0.3024.59±0.49ISS
注:R-耐药;I-中度敏感;S-敏感。
2.3 低聚糖保留能力
如表4所示,格氏乳杆菌HX发酵棉籽糖蜜72 h对棉子糖和水苏糖均具有最高的保留能力分别达到了77.63%和95.74%,瑞士乳杆菌DLX对这2种低聚糖保留能力最弱。
表4 供试菌株低聚糖保留能力
Table 4 Retention ability of oligosaccharide of the test strains
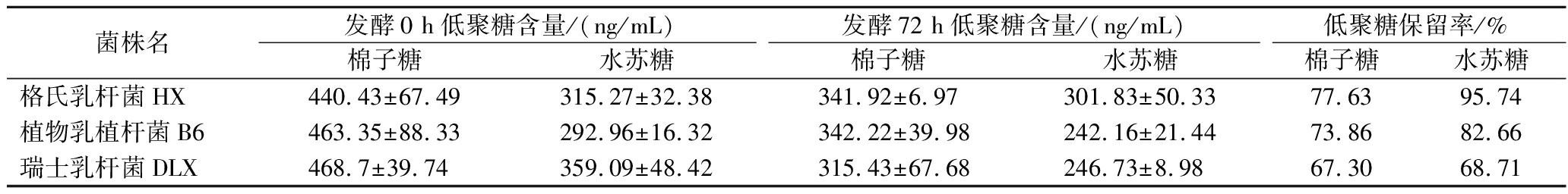
菌株名发酵0 h低聚糖含量/(ng/mL)发酵72 h低聚糖含量/(ng/mL)低聚糖保留率/%棉子糖水苏糖棉子糖水苏糖棉子糖水苏糖格氏乳杆菌HX440.43±67.49315.27±32.38341.92±6.97301.83±50.3377.6395.74植物乳植杆菌B6463.35±88.33292.96±16.32342.22±39.98242.16±21.4473.8682.66瑞士乳杆菌DLX468.7±39.74359.09±48.42315.43±67.68246.73±8.9867.3068.71
2.4 发酵性能
3株菌能够在20~42 ℃条件下生长,其中37 ℃为最佳生长温度。另外,3株菌在42 ℃时菌能生长,其中HX生物量最高(图1-a)。3株菌的生长趋势较为一致,0~2 h延滞期(0 h活菌数在1×107 CFU/mL在水平),4~8 h进入对数生长期(8 h活菌数108 CFU/mL水平),12~20 h生物量趋于平稳(活菌数达到109 CFU/mL)(图1-b)。菌株发酵过程pH变化曲线如图1-c所示,植物乳植杆菌B6发酵液的pH下降最快,发酵4~14 h时呈线型下降趋势;格氏乳杆菌HX和瑞士乳杆菌DLX pH值变化趋势一致,8~20 h的pH值开始下降。可滴定总酸结果显示,3株菌随着培养时间的增加总酸呈现出增加趋势,其中植物乳植杆菌B6产总酸量最小并且随着培养时间增加增加量最低,而格氏乳杆菌HX产总酸能力最强,并且24~60 h间呈现出线性增加趋势(图1-d)。经产酸能力的测定,3株菌都表现出良好的产酸性能,丰富的有机酸可以降低肠道pH,使有害微生物的繁殖受到抑制,促进益生菌的增殖,激发动物的食欲,增加采食量,减轻腹泻等问题[16]。
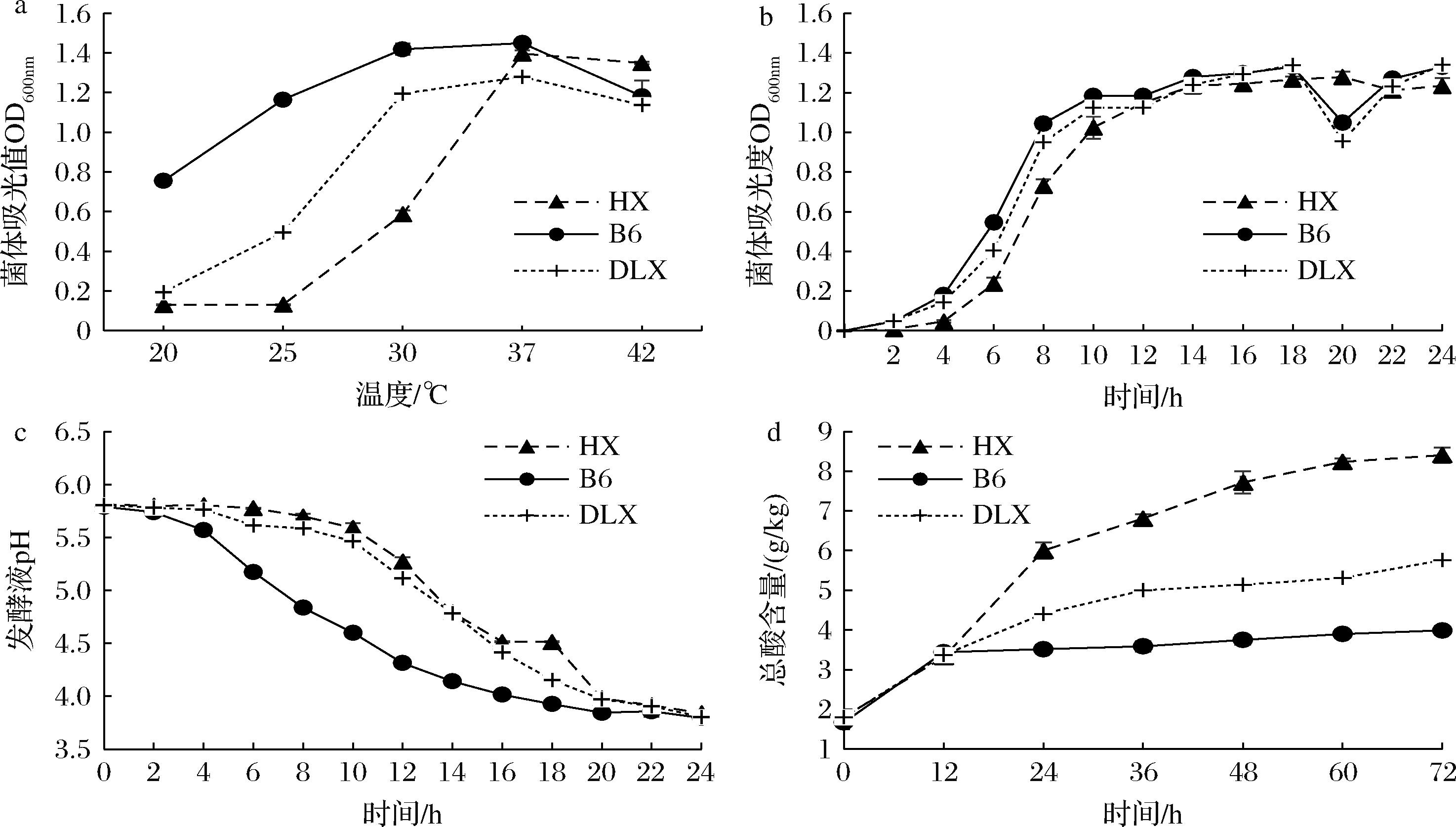
a-最适生长温度;b-生长曲线;c-发酵过程pH变化;d-发酵过程总酸含量变化
图1 供试菌株最适温度,生长曲线及产酸能力
Fig.1 Optimum temperature, growth curve, and acid production capacity of the tested strains
2.5 菌株益生性能
2.5.1 菌株抑菌能力检测
由表5可知,瑞士乳杆菌DLX对金黄色葡萄球菌的抑菌能力最强,其抑菌圈达到了(20.44±1.62) mm,植物乳植杆菌B6对大肠杆菌和沙门氏菌的抑菌能力最强;格氏乳杆菌HX对这3种病原菌的抑菌圈大小均显著低于植物乳植杆菌B6和瑞士乳杆菌DLX。
表5 供试菌株对3株病原菌的抑菌能力
Table 5 Antibacterial ability of the tested strains against three pathogens
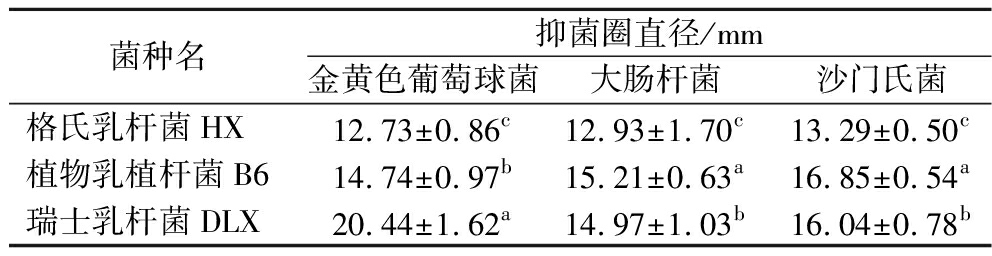
菌种名抑菌圈直径/mm金黄色葡萄球菌大肠杆菌沙门氏菌格氏乳杆菌HX12.73±0.86c12.93±1.70c13.29±0.50c植物乳植杆菌B614.74±0.97b15.21±0.63a16.85±0.54a瑞士乳杆菌DLX20.44±1.62a14.97±1.03b16.04±0.78b
注:同列字母不同为差异极显著(P<0.01)。
2.5.2 菌株耐酸和耐胆盐能力
如图2-a所示。随着pH值的降低,菌株的存活率也随之下降,所有菌株在pH值为4的条件下,存活率都能达到50%以上,其中格氏乳杆菌HX在此环境下生长旺盛,其存活率达到116%;在pH值为3的环境下,3株菌的存活率有一定下降,其中格氏乳杆菌HX对低酸环境的耐受较强,在pH值为3时,菌株存活率仍达到94%,而植物乳植杆菌B6和瑞士乳杆菌DLX对低酸环境耐受力较差,其存活率分别降至55.07%和24.65%;当pH值降至2时,仅有格氏乳杆菌HX存活率在70%以上,其余2株菌的存活率都降至50%以下。格氏乳杆菌HX这一株乳酸菌表现出了较强的耐酸能力。如图2-b所示,3株菌都能耐受质量分数为0.5%和1%的胆盐环境,在质量分数0.5%的胆盐环境中,3株乳酸菌的存活率都达到了60%以上,格氏乳杆菌HX、植物乳植杆菌B6和瑞士乳杆菌DLX的存活率分别为60.08%、76.49%和72.67%。其中植物乳植杆菌B6表现出了较强的胆盐耐受能力。在质量分数1%胆盐环境中,3株菌的存活率都出现了一定下降,格氏乳杆菌HX、植物乳植杆菌B6、瑞士乳杆菌DLX的存活率分别为56.47%、62.36%和72.48%。其中植物乳植杆菌B6存活率下降最为明显。
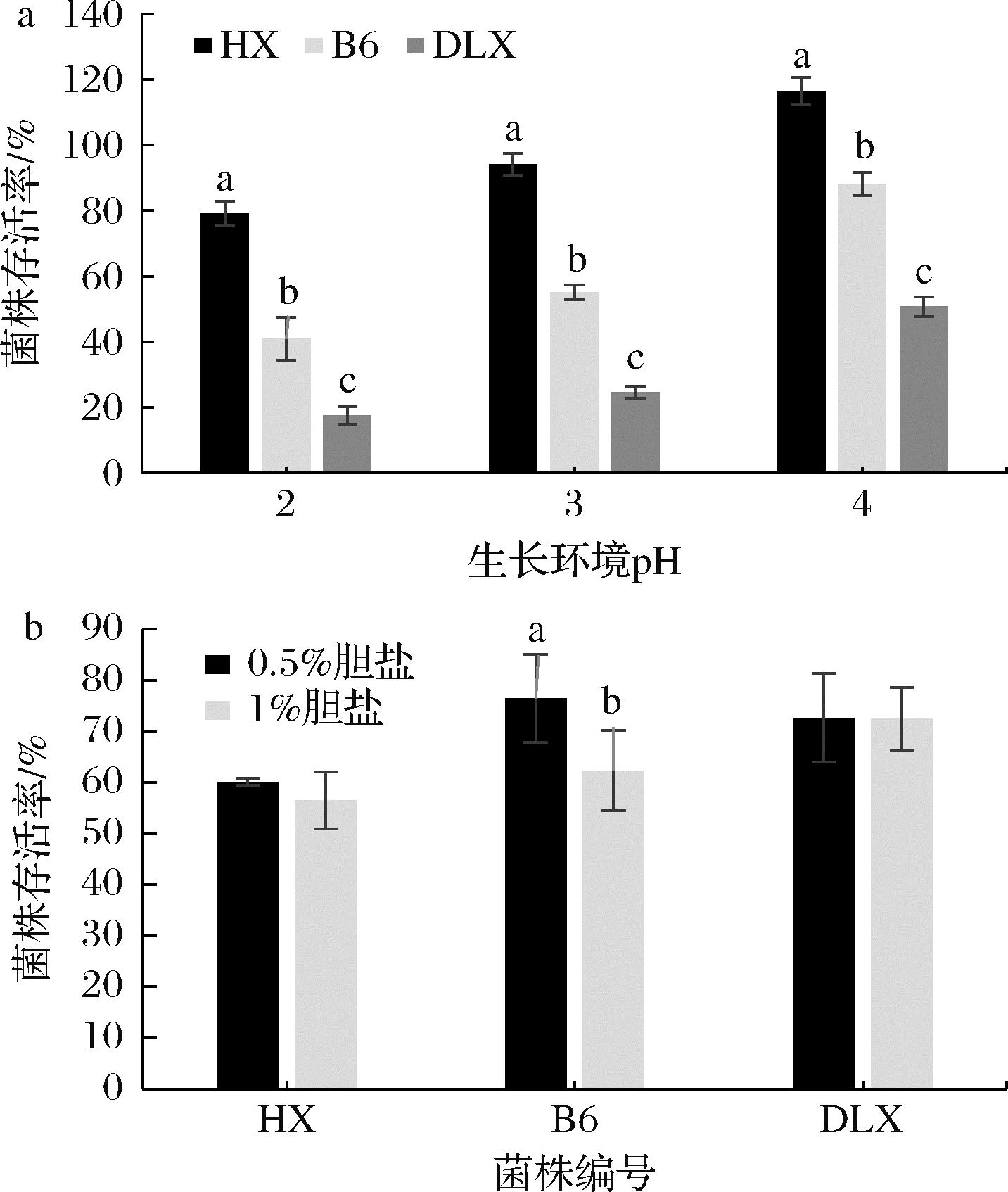
a-耐酸能力;b-耐胆盐能力
图2 供试菌株耐酸和耐胆盐能力
Fig.2 Acid and bile salt tolerance abilities of the tested strains
注:不同字母为差异极显著(P<0.01)。
2.6 菌株HX发酵棉籽糖蜜代谢组学分析
2.6.1 主要代谢物及其含量
利用液相色谱-质谱联用仪对菌株HX发酵棉籽糖蜜中代谢物成分进行鉴定,共鉴定出1 969种代谢物,包括脂质和类脂分子(421种)占总含量的35.41%,其次是有机杂环化合物(479种)占总含量的19.98%、苯类化合物199种(11.24%)、有机氮化合物49种(8.33%)、有机酸及其衍生物382种(8.19%)、有机氧化物125种(4.68%)、生物碱及其衍生物106种(4.06%)、苯丙类化合物和聚酮类化合物134种(3.93%)(电子增强出版附表3)。研究发现发酵液中相对含量较高的化合物均与消炎、抗氧化、促消化、提高免疫等功能相关。例如,所有代谢物中含量最高的是脂肪酰类中的Crepenynic acid(3.59%),作为一种天然的抗氧化剂成分,其对肾有保护作用[17];其次,顺式9-十八碳烯酰胺和油酸酰胺具诱导动物产生生理性睡眠和镇静的作用[18-19]。异戊烯醇脂中的桉油烯醇具有抗菌消炎作用[20];有机氮化合物中的Hexadecasphinganine具有抗氧化活性,对肾脏有保护作用[21],胆碱类化合物可以提高抗氧化能力、免疫机能及修复肝脏损伤[22];吲哚萘啶生物碱中的Luotonin C类物质对人类癌细胞系具有选择杀伤力,特别是对白血病P-388细胞有较强的杀伤力[23]。此外,哈尔满碱类物质具有较强的抗氧化能力和抗凝血活性[24];黄酮类化合物具有改善肠道健康、促生长、抗炎、清除自由基、抗氧化和提高动物免疫力的功能[25]。
2.6.2 菌株HX发酵棉籽糖蜜代谢物KEGG通路富集
如图3-a所示,正离子模式下HX发酵棉籽糖蜜溶液涉及34条代谢通路,主要包括全局和概况图谱(global and overview maps)、氨基酸代谢(amino acid metabolism)、外源物质生物降解与代谢(xenobiotics biodegradation and metabolism)、其他次生代谢物的合成和化学结构转换图谱(biosynthesis of other secondary metabolites)。如图3-b所示,负离子模式下HX发酵棉籽糖蜜溶液涉及30条代谢通路,主要包括全局和概况图谱(global and overview maps)、氨基酸代谢(amino acid metabolism)、其他次生代谢物的合成(biosynthesis of other secondary metabolites)、碳水化合物代谢(carbohydrate metabolism)和化学结构转换图谱(chemincal structure transformation maps)。
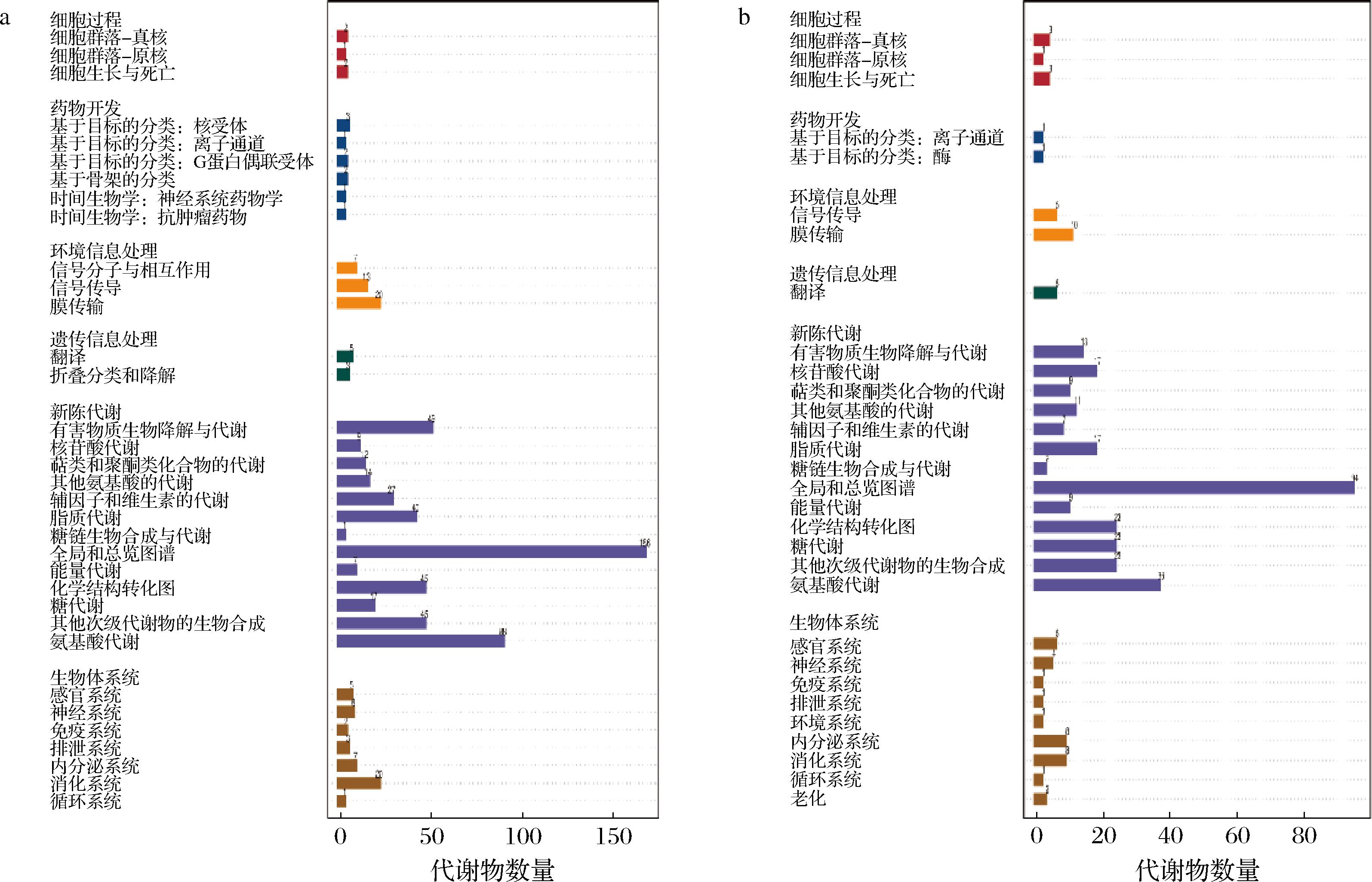
a-正离子模式;b-负离子模式
图3 代谢物KEGG通路分析
Fig.3 Metabolite KEGG pathway analysis
2.6.3 HX发酵棉籽糖蜜溶液代谢物HMDB代谢物分类图
图4-a显示了正离子模式下HX发酵棉籽糖蜜溶液HMDB种类饼图代谢物组分,HX发酵的棉籽糖蜜溶液代谢物以有机杂环化合物(24.45%)、脂类及类脂质(21.49%)和有机酸及其衍生物(19.50%)为主要类别;图4-b显示,负离子模式下HX发酵的棉籽糖蜜溶液代谢物以脂类及类脂质(20.82%)、有机酸及其衍生物(19.24%)、有机氧化物(15.51%)为主要类别。
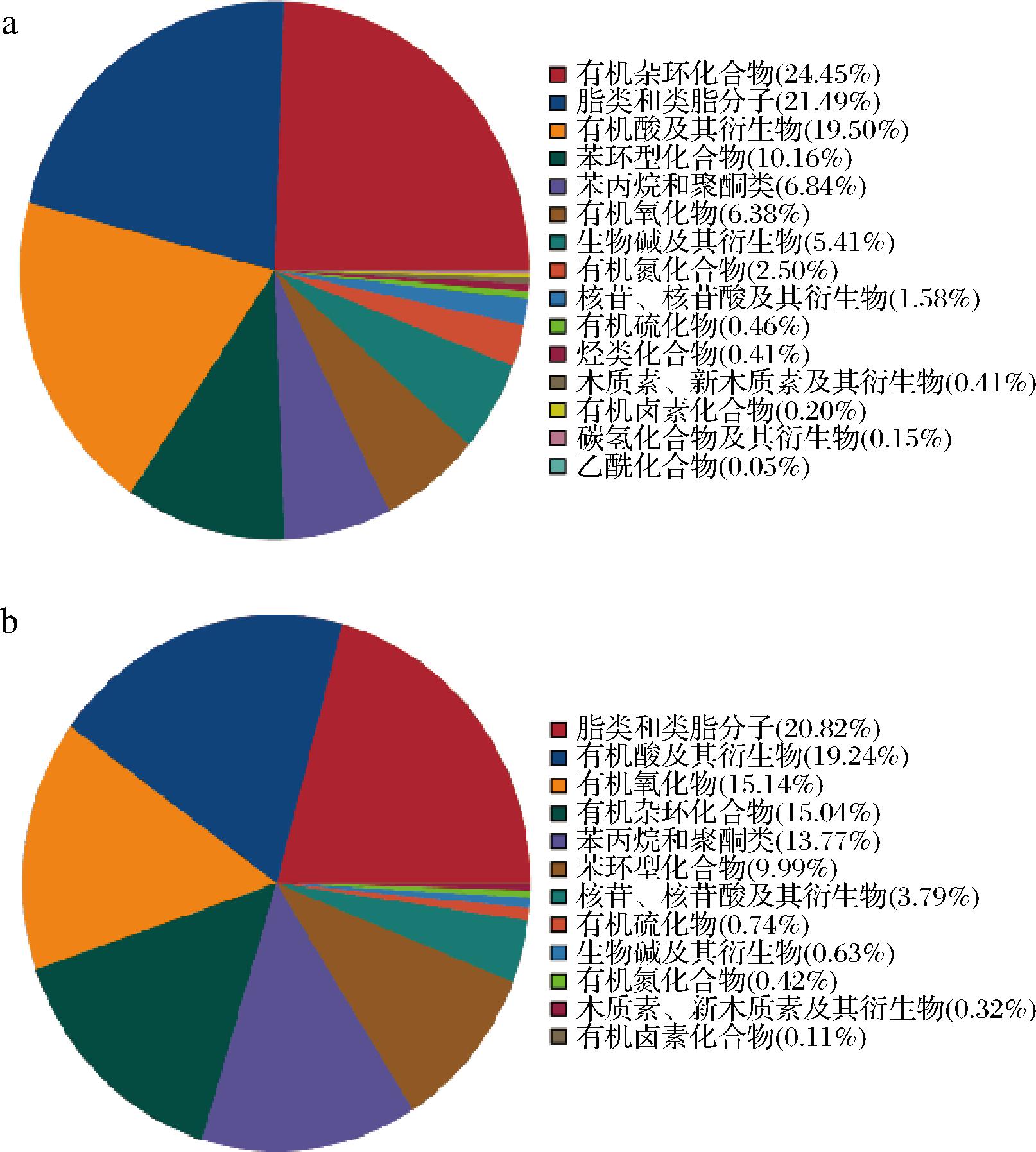
a-正离子模式;b-负离子模式
图4 HMDB数据库中代谢物中的分类
Fig.4 Classification of metabolites in HMDB database
3 结论
格氏乳杆菌HX菌株具有安全、发酵性能和益生性能优良,其发酵棉籽糖蜜后能够产生大量活性代谢物,能够一步发酵法实现棉籽糖蜜转化。
[1] 康嘉伟. 棉籽加工废液中棉籽糖提取工艺研究[D].石河子:石河子大学, 2022.KANG J W.Study on extraction technology of raffinose from cottonseed processing waste liquid[D].Shihezi:Shihezi University, 2022.
[2] GADELHA I C N, FONSECA N B S, OLORIS S C S, et al.Gossypol toxicity from cottonseed products[J].The Scientific World Journal, 2014, 2014:231635.
[3] 薄晓培, 吕淑平, 聂利红, 等.棉花副产品利用研究进展[J].农产品加工, 2024(13):103-107.BO X P, LYU S P, NIE L H, et al.Research progress in the utilization of cotton by-products[J].Farm Products Processing, 2024(13):103-107.
[4] 杨文婷. 棉酚降解酶与益生菌对棉粕生物脱毒效果的比较研究[D].石河子:石河子大学, 2020.YANG W T.A comparative study of gossypol degradation enzymes andprobiotics on detoxification of cottonseed meal[D].Shihezi:Shihezi University, 2020.
[5] 屯妮萨·麦提赛伊迪.真菌糙皮侧耳(Pleurotus ostreatus)降解棉籽壳木质纤维素和游离棉酚的作用及其机制的初步研究[D].乌鲁木齐:新疆农业大学, 2019.TUNISA MATTHIESAYEDI.Preliminary study on the effect and mechanism of degradation of lignocellulose and free gossypol in cottonseed hulls by Pleurotus ostreatus[D].Urumqi:Xinjiang Agricultural University, 2019.
[6] ASHAYERIZADEH A, JAZI V, REZVANI M R, et al.An investigation into the influence of fermented cottonseed meal on the productive performance, egg quality, and gut health in laying hens[J].Poultry Science, 2024, 103(5):103574.
[7] MARCO M L, SANDERS M E, G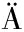 NZLE M, et al.The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on fermented foods[J].Nature Reviews Gastroenterology &Hepatology, 2021, 18(3):196-208.
NZLE M, et al.The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on fermented foods[J].Nature Reviews Gastroenterology &Hepatology, 2021, 18(3):196-208.
[8] 张娜. 植物乳杆菌ZDY2013与功能性低聚糖协同改善小鼠结肠炎研究及其发酵乳制备[D].南昌:南昌大学, 2022.ZHANG N.Synergistic improvement of colitis in mice with Lactobacillus plantarum ZDY2013 combined with functional oligosaccharides and its preparation for milk fermentation[D].Nanchang:Nanchang University, 2022.
[9] KAZU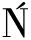 B, MA
B, MA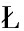 ACZEWSKA J, KAZU
ACZEWSKA J, KAZU K, et al.Dietary administration of β-1, 3/1, 6-glucan and Lactobacillus plantarum improves innate immune response and increases the number of intestine immune cells in roach (Rutilus rutilus)[J].BMC Veterinary Research, 2020, 16(1):216.
K, et al.Dietary administration of β-1, 3/1, 6-glucan and Lactobacillus plantarum improves innate immune response and increases the number of intestine immune cells in roach (Rutilus rutilus)[J].BMC Veterinary Research, 2020, 16(1):216.
[10] LALITSURADEJ E, SIRILUN S, SITTIPRAPAPORN P, et al.The effects of synbiotics administration on stress-related parameters in Thai subjects:A preliminary study[J].Foods, 2022, 11(5):759.
[11] SERGEEV I N, ALJUTAILY T, WALTON G, et al.Effects of synbiotic supplement on human gut microbiota, body composition and weight loss in obesity[J].Nutrients, 2020, 12(1):222.
[12] 郑清梅, 温茹淑, 韩春艳.间苯三酚法快速测定棉粕中游离棉酚的方法研究[J].饲料工业, 2010, 31(3):42-44.ZHENG Q M, WEN R S, HAN C Y.Study on rapid determination of free gossypol in cotton meal by phloroglucinol method[J].Feed Industry, 2010, 31(3):42-44.
[13] 李倜, 胡昕, 张潇月, 等.圈养大熊猫肠道乳酸菌分离及益生特性[J].微生物学通报, 2023, 50(9):4063-4077.LI T, HU X, ZHANG X Y, et al.Isolation and probiotic characteristics of lactic acid bacteria from intestinal tract of giant panda in captivity[J].Microbiology China, 2023, 50(9):4063-4077.
[14] 吴慧昊, 牛锋, 陈珊珊, 等.高效降亚硝酸盐乳酸菌的驯化复筛及菌株鉴定[J].食品科学, 2016, 37(19):160-165.WU H H, NIU F, CHEN S S, et al.Screening and identification of nitrite-degrading lactic acid bacteria[J].Food Science, 2016, 37(19):160-165.
[15] 吴慧昊, 舒文秀, 刘梓琦, 等.脱除游离棉酚乳酸菌的分离鉴定及益生性能研究[J].微生物学杂志, 2022, 42(3):36-43.WU H H, SHU W X, LIU Z Q, et al.Isolation, identification and probiotic performance of Lactobacillus capable of gossypol removal[J].Journal of Microbiology, 2022, 42(3):36-43.
[16] 尹苗,陈希文,王聪,等.酸化剂的作用机制及在畜禽健康养殖中的应用[J].黑龙江畜牧兽医,2022(20):31-35 YIN M, CHEN X W, WANG C, et al.Action mechanism of acidifier and its application in healthy livestock and poultry breeding[J].Heilongjiang Animal Science and Veterinary Medicine, 2022(20):31-35.
[17] SANTOS P, BUSTA L, YIM W C, et al.Structural diversity, biosynthesis, and function of plant falcarin-type polyacetylenic lipids[J].Journal of Experimental Botany, 2022, 73 (9):2889-2904.
[18] CRAVATT B F, PROSPERO-GARCIA O, SIUZDAK G, et al.Chemical characterization of a family of brain lipids that induce sleep[J].Science, 1995, 268(5216):1506-1509.
[19] YANG J Y, WU C F, SONG H R.Studies on the sedative and hypnotic effects of oleamide in mice[J].Arzneimittel-Forschung, 1999, 49(8):663-667.
[20] MUFTI A, FERIANI A, CONTRERAS M D M, et al.Ephedra alata seeds confer kidney protection against early life exposure to acephate by regulating oxidative insult and activating autophagy[J].Life, 2023, 13(12):2254.
[21] 徐心雨, 武之绚, 鲍梦圆, 等.胆碱的生理功能及其对鱼脂肪代谢的调控机制[J].饲料研究, 2023, 46(6):137-141.XU X Y, WU Z X, BAO M Y, et al.Physiological functions of choline and its regulatory mechanism on fat metabolism in fish[J].Feed Research, 2023, 46(6):137-141.
[22] DAS S, PATRA A, MANDAL A, et al.Choline chloride induces growth performance of Indian major carps and air-breathing fish species with an outcome of quality food-fish under a semi-intensive culture system:A biochemical investigation[J].ACS Omega, 2022, 7(17):14579-14590.
[23] LIANG J L, CHA H C, JAHNG Y.Recent advances in the studies on luotonins[J].Molecules, 2011, 16(6):4861-4883.
[24] MOURA D J, RICHTER M F, BOEIRA J M, et al.Antioxidant properties of beta-carboline alkaloids are related to their antimutagenic and antigenotoxic activities[J].Mutagenesis, 2007, 22(4):293-302.
[25] 林春草, 陈大伟, 戴均贵.黄酮类化合物合成生物学研究进展[J].药学学报, 2022, 57(5):1322-1335.LIN C C, CHEN D W, DAI J G.Advances of synthetic biology of flavonoids[J].Acta Pharmaceutica Sinica, 2022, 57(5):1322-1335.