复合发酵技术通过组合具有不同代谢性能的菌株,显著提高了发酵效率,促进了风味物质和营养物质的形成[1]。相较于单菌发酵,复合发酵具有加快酸化进程、产生丰富风味化合物、提升感官品质和延长产品保质期等多方面优势[2]。乳酸乳球菌因其独特的代谢特性和益生功能,已被广泛应用于新型复合发酵剂开发[3-4]。菌株互作会对发酵乳制品产生多方面影响,主要表现在代谢网络重构提高发酵效率,包括提升碳源利用效率和缩短发酵周期[5];塑造独特风味特征,形成丰富且平衡的风味物质,提升产品整体感官品质[6];增强产品营养功能,促进维生素合成、生物活性肽释放和功能性脂类物质积累,提高发酵乳的营养价值和健康功效[7]。
作为复合发酵体系中的关键物质,氨基酸不仅是菌株生长的重要营养源,还显著影响发酵过程和产品品质,同时作为菌株互作的物质基础和风味前体物质[8-9]。不同乳酸菌菌株之间存在明显的氨基酸代谢互补关系,表现为某些菌株能够分泌特定氨基酸,而其他菌株则可以利用这些氨基酸促进自身生长[10]。例如,嗜热链球菌嗜热亚种能产生组氨酸等氨基酸,为乳酸乳球菌的生长提供必要的营养物质,形成典型的营养互补关系,而乳酸乳球菌则进一步将中间产物转化为关键风味化合物[6]。特别是支链氨基酸的代谢,在乳制品中产生醛类、醇类和酯类等重要风味物质。基于氨基酸代谢互作机制的菌株筛选已成为开发高效复合发酵剂的重要策略。通过分析不同乳酸菌菌株的氨基酸代谢特性,筛选出具有互补代谢模式的菌株组合,显著提高了发酵乳的风味品质和功能特性[11]。氨基酸代谢互作的分子机制研究是解析复合发酵体系的关键。近期通过研究代谢组学分析揭示,乳酸菌间的氨基酸交换不仅涉及直接的营养互补,还包括复杂的信号分子网络调控,这些信号分子如吲哚衍生物和短链脂肪酸可调节菌株间的代谢活动和基因表达[12]。Transwell共培养系统作为研究微生物代谢互作的有效工具,可在菌体不直接接触的情况下研究代谢物交换。结合代谢组学分析,可全面揭示菌株间的代谢互作网络,为复合发酵剂的定向设计提供科学依据[13]。
前期研究结果表明,相较于其他乳酸乳球菌和商业发酵剂的复合发酵、单一商业发酵剂发酵,商业发酵剂与乳酸乳球菌(Lactococcus lactis NGD8)的复合发酵组合能够产生具有最佳理化特性和感官品质的发酵乳制品。基于前期基因组规模代谢模型的预测分析揭示,商业发酵剂菌株与NGD8之间可能存在氨基酸代谢互补的协同关系。本研究通过氨基酸缺陷型培养基分析发酵剂菌株的氨基酸缺陷型和Transwell培养板,分析在有无商业发酵剂菌株条件下NGD8的生长情况以及非靶向代谢物的差异性,进而验证复合发酵过程中存在的氨基酸互作关系。本研究结果将为复合发酵剂的定向设计和优化提供科学依据和理论支持,对提升发酵乳制品的品质和功能特性具有重要意义。
1 材料与方法
1.1 实验菌株
本研究所使用的5株乳酸乳球菌菌株均取自江南大学食品生物技术中心,分别为FDRS7B2、FDNGD8B1、FDRB23B5、FDRB30B9、FDRB40B4。商业发酵剂菌株包含唾液链球菌嗜热亚种(Streptococcus salivarius subsp. thermophilus CS)和德氏乳杆菌保加利亚亚种(Lactobacillus delbrueckii subsp. bulgaricus CL)。
1.2 材料与试剂
乳糖、抗坏血酸、KH2PO4、K2HPO4、MgCl2、CaCl2、NaCl、CuSO4、CoCl2、MnSO4、FeCl2、ZnSO4、脯氨酸、苯丙氨酸、色氨酸、甲硫氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甘氨酸、丝氨酸、苏氨酸、半胱氨酸、酪氨酸、天冬氨酸、谷氨酸、赖氨酸、精氨酸、组氨酸、对氨基苯甲酸、生物素、腺嘌呤、鸟嘌呤、尿嘧啶、吡哆醇、泛酸、烟酸、黄嘌呤、天冬酰胺、谷氨酰胺,国药集团化学试剂有限公司;2×Taq Plus MasterMix、ddH2O,康为世纪生物科技股份有限公司;RT-qPCR引物,上海生工有限公司。YO-MIX 300商业发酵剂,丹尼斯克;安佳脱脂乳粉,恒天然集团;细菌基因组DNA提取试剂盒、溶菌酶溶液(20 mg/mL)、RNase A(100 mg/mL),北京天根生化科技有限公司;M17肉汤培养基,北京索莱宝科技有限公司。
本研究所用培养基及其配方如下,灭菌条件为115 ℃,20 min。
LM17液体培养基(g/L):在M17肉汤培养基中添加乳糖5。
LM17固体培养基(g/L):在LM17液体培养基中添加琼脂15。
化学成分确定培养基(chemically defined medium,CDM)培养基(g/L):乳糖5、乙酸钠1、柠檬酸铵6、抗坏血酸0.5、KH2PO4 3、K2HPO4 2.5、MgCl2 0.2、CaCl2 0.05、CuSO4 0.001、CoCl2 0.002 5、MnSO4 0.028、FeCl2 0.005、ZnSO4 0.005、脯氨酸0.68、苯丙氨酸0.28、色氨酸0.05、甲硫氨酸0.12、丙氨酸0.24、缬氨酸0.33、亮氨酸0.48、异亮氨酸0.22、甘氨酸0.18、丝氨酸0.34、苏氨酸0.23、半胱氨酸0.25、酪氨酸0.29、天冬氨酸0.46、谷氨酸0.4、赖氨酸0.44、精氨酸0.13、组氨酸0.15、对氨基苯甲酸0.01、生物素0.01、腺嘌呤0.01、鸟嘌呤0.01、尿嘧啶0.01、吡哆醇0.007、泛酸0.002、烟酸0.001、黄嘌呤0.01、天冬酰胺0.35、谷氨酰胺0.39。
1.3 仪器与设备
CT65A全自动立式蒸汽灭菌器,上海伯能仪器有限公司;ME3002E电子天平,梅特勒-托利多公司;Bio-Rad S1000 PCR仪,美国Bio-Rad公司;电动磁力搅拌器,德国IKA公司;Centrifuge 5424 R小型台式高速离心机,德国Eppendorf公司;Protect-1 FD洁净工作台,Trace 1300液相色谱/质谱联用仪,美国Thermo Fisher Scientific公司;TA-XTPlus质构分析仪,英国Stable Micro Systems公司;Transwell培养板(0.4 μm孔径聚酯膜小室,无菌),美国Corning Incorporated公司。
1.4 实验方法
1.4.1 复合培养中菌株的绝对定量
采用定量聚合酶链式反应(quantitative polymerase chain reaction,qPCR)技术测定发酵体系中发酵剂菌株的活菌数。标准曲线构建方案如下:首先将培养至平台期的菌株进行梯度稀释(10-1~10-6),并将各稀释度样品(100 μL)涂布于LM17固体培养基上,并在30 ℃恒温培养箱中倒置培养48 h,同时从相应稀释度样品中提取细菌基因组DNA。以提取的DNA为模板,使用特异性引物进行PCR扩增,引物列表如表1所示。PCR反应程序包括:94 ℃预变性2 min;随后进行30个循环,每个循环包括94 ℃变性30 s、58~60 ℃退火30 s及72 ℃延伸30 s;最后72 ℃终延伸2 min。通过将平板计数获得的活菌数(CFU/mL)为横坐标与相应的循环阈值(cycle threshold,Ct)为纵坐标构建标准曲线。
表1 PCR引物列表
Table 1 List of PCR primers
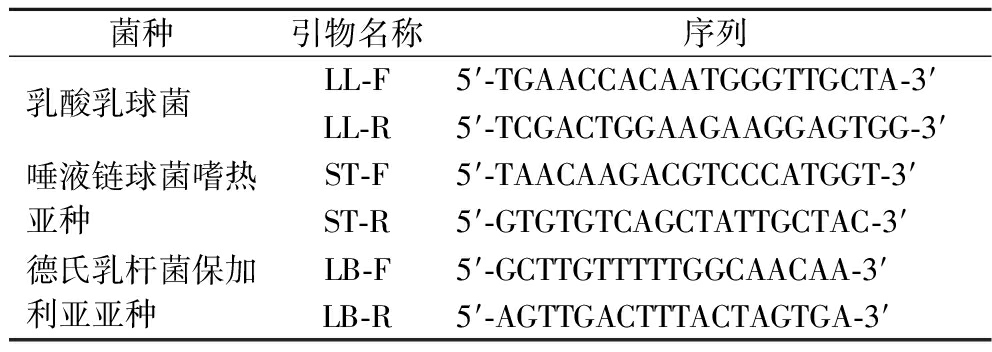
菌种引物名称序列乳酸乳球菌LL-F5′-TGAACCACAATGGGTTGCTA-3′LL-R5′-TCGACTGGAAGAAGGAGTGG-3′唾液链球菌嗜热亚种ST-F5′-TAACAAGACGTCCCATGGT-3′ST-R5′-GTGTGTCAGCTATTGCTAC-3′德氏乳杆菌保加利亚亚种LB-F5′-GCTTGTTTTTGGCAACAA-3′LB-R5′-AGTTGACTTTACTAGTGA-3′
取1 mL发酵乳样品,提取其中的细菌基因组DNA。提取的DNA经定量后,按照与标准曲线构建相同的qPCR反应体系和条件进行扩增。将获得的Ct值代入标准曲线,计算得到发酵体系中菌株的活菌数(CFU/mL)。
1.4.2 培养液中非靶向代谢组学分析
发酵乳样品4 ℃、10 000 r/min离心5 min分离获得液相部分。取上清液100 μL与400 μL甲醇∶乙腈混合液(1∶1,体积比)在离心管中充分混合。样品经涡旋振荡后进行冷沉淀(-20 ℃,1 h),随后在4 ℃条件下以15 000 r/min离心15 min。所得提取物经旋转蒸发仪浓缩至干,并用200 μL乙腈∶水混合液(1∶1,体积比)重新溶解。经剧烈混合和离心(15 000 r/min,15 min,4 ℃)后,处理好的提取物转移至进样瓶用于后续分析。质量控制样品则通过等体积混合所有样品制备而成。
代谢组学分析采用Dionex UltiMate 3000超高效液相色谱系统结合Q EXACTIVE高分辨质谱仪进行,同时采用正、负离子电喷雾电离模式[14]。色谱分离使用Acquity BEH C18色谱柱。流动相由A相(体积分数为0.1%甲酸水溶液)和B相(乙腈)组成。梯度洗脱程序(流速0.3 mL/min):0~1 min,5% B;1~5 min,50%~60% B;5~8 min,60%~100% B;8~11 min,100% B;11~14 min,60%~100% B;14~15 min,50%~60% B;最后在5% B条件下平衡15~18 min。进样体积5 μL,分析时间12 min。质谱参数设置如下:喷雾电压3.5 kV,脱溶剂温度 350 ℃,全扫描分辨率为70 000 FWHM,质量扫描范围70~1 050 m/z。数据依赖性M2S,采集使用35 000分辨率和1×105的AGC。
1.4.3 发酵剂菌株氨基酸缺陷型分析
基于CDM培养基构建了一系列单一氨基酸缺陷型培养基,具体包括:以CDM为对照组,分别构建缺少丙氨酸(Ala-)、甘氨酸(Gly-)、天冬氨酸(Asp-)、谷氨酸(Glu-)、精氨酸(Arg-)和苯丙氨酸(Phe-)的6种氨基酸缺陷型培养基,其余成分与CDM保持一致。培养基配制完成后,采用超声波处理以确保培养基成分充分溶解,随后通过0.22 μm水系滤膜进行除菌过滤,最终将过滤后的培养基在4 ℃无菌条件下保存备用。将菌株NGD8、CS和CL按照2%(体积分数)比例接种活化3代,以下6种菌株组合按2%(体积分数)接种量分别接种于上述6种氨基酸营养缺陷型培养基中:
1)NGD8单菌株(N);
2)CS单菌株(S);
3)CL单菌株(L);
4)NGD8∶CS(SN)=1∶1(菌株浓度比);
5)NGD8∶CL(LN)=1∶1(菌株浓度比);
6)NGD8∶CS∶CL(SLN)=1∶1∶1(菌株浓度比)。
将接种后的培养液置于30 ℃恒温培养箱中培养12 h,培养结束后提取培养液中DNA,采用qPCR的方法测定各组合中NGD8、CS和CL的活菌数。在特定氨基酸缺乏条件下,比较单菌培养与混菌培养体系中目标菌株的生长情况。若混菌培养条件下目标菌株的活菌数显著高于单菌培养,则表明共培养体系中的伴随菌株能够通过代谢互作机制弥补培养基中特定氨基酸的缺乏,从而促进目标菌株的生长,证实菌株间存在氨基酸代谢互补关系。
1.4.4 Transwell培养板探究互作机制
采用12孔Transwell培养板,构建了上层小室和下层大室分隔的共培养体系。上室体积500 μL,下室体积1 500 μL。将分别接种后的Transwell培养板置于30 ℃恒温培养箱中培养12 h。培养结束后,收集下层大室中NGD8培养液。采用qPCR法测定各组合中下层大室NGD8的活菌数,并利用LC-MS技术对下层大室中NGD8培养液进行非靶向代谢组学分析。
1.5 数据处理
实验数据统计分析借助GraphPad Prism 9.1与SPSS 25.0软件进行。色谱数据经Compound Discover 3.2软件处理,VIP评分计算利用SIMCA软件完成,数据可视化通过OmicStudio在线工具(https://www.omicstudio.cn/tool)实现。实验结果以“平均值±标准差”表示。
2 结果与分析
2.1 菌株的氨基酸缺陷型分析
如图1所示,对NGD8、CS和CL在不同氨基酸缺陷型培养基条件下进行绝对定量分析表明,CS和CL在混菌培养后的活菌数显著降低(P<0.05)或保持稳定,这可能是由于菌株间的营养竞争、代谢产物抑制或生态位重叠导致的相互抑制作用[15]。然而,NGD8菌株在不同氨基酸缺陷型培养基中的活菌数呈现显著升高趋势(P<0.05),这一现象表明混菌培养条件下商业发酵剂菌株(CS和CL)可能通过分泌特定氨基酸或其他代谢物等方式促进了NGD8的生长。
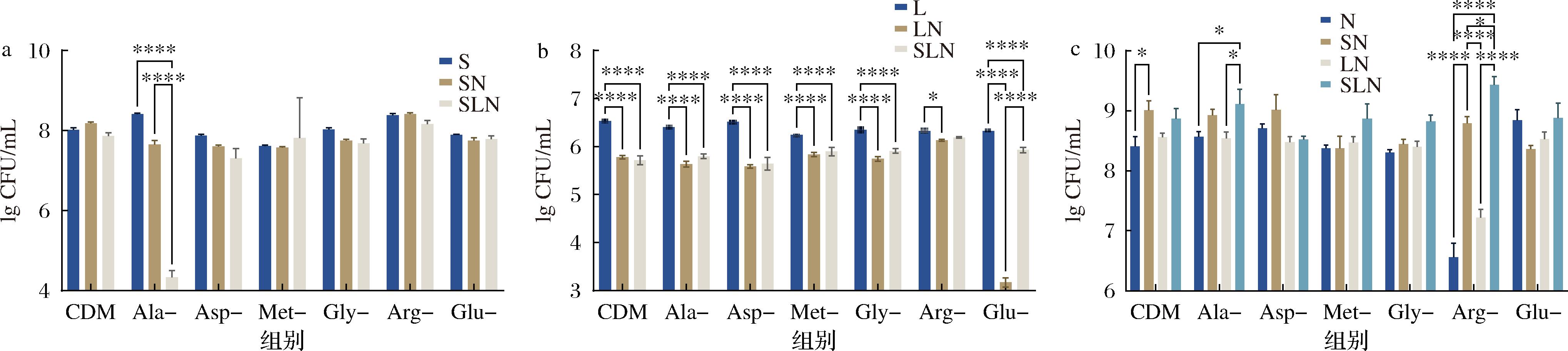
a-CS;b-CL;c-NGD8
图1 不同氨基酸缺陷培养基中CS、CL和NGD8菌株的生长情况
Fig.1 Growth of CS, CL, and NGD8 strain in different kinds of amino acid-deficient media
注:*P<0.05,**P<0.01,***P<0.001,****P<0.000 1(下同)。
在丙氨酸缺陷型(Ala-)培养基中,SLN组中NGD8的活菌数达到9.11 lg CFU/mL显著高于N组(8.56 lg CFU/mL),这一结果表明,在丙氨酸缺乏的环境中,NGD8自身生长受到一定限制,而商业发酵剂菌株(CS和CL)的存在能够显著改善其生长情况。同时,SLN组中NGD8菌数显著高于LN组(P<0.05),表明CS在丙氨酸代谢互作中发挥了关键作用。这一结果与先前报道的嗜热链球菌嗜热亚种具有较高丙氨酸合成能力的发现相符,证实了商业发酵剂菌株能够通过提供丙氨酸促进NGD8的生长[16]。最显著的互作效应出现在精氨酸缺陷型(Arg-)培养基中,在缺乏精氨酸的条件下,N组中NGD8的菌数与接种时基本一致(6.91 lg CFU/mL),表明精氨酸对NGD8的生长至关重要,是其不可或缺的营养元素。相较于N组,在SN组中NGD8活菌数显著提高至8.79 lg CFU/mL(P<0.000 1),SLN组达到9.43 lg CFU/mL(P<0.000 1),LN组达到7.22 lg CFU/mL(P<0.05),这与先前研究报道的乳酸菌间精氨酸代谢互作现象一致[17],证实了精氨酸代谢在NGD8与商业发酵剂菌株互作中的核心地位。
通过上述实验分析不同组合在各氨基酸缺陷型培养基中的菌株生长情况,确定了3种主要的氨基酸代谢互作模式:1)丙氨酸代谢互作主要发生在NGD8与CS和CL混菌培养中(A-SLN);2)精氨酸代谢互作存在于NGD8与CS混菌培养中(G-SN);3)精氨酸代谢互作存在于NGD8与CS和CL混菌培养中(G-SLN)。
2.2 丙氨酸、精氨酸营养缺陷下菌株互作关系的验证
为了进一步验证上述实验中观察到的NGD8与商业发酵剂菌株(CS、CL)间的代谢互作模式,并排除直接菌体接触因素的影响,本研究采用Transwell培养板验证了上述实验中3种氨基酸互作模式,实验设计如图2所示。
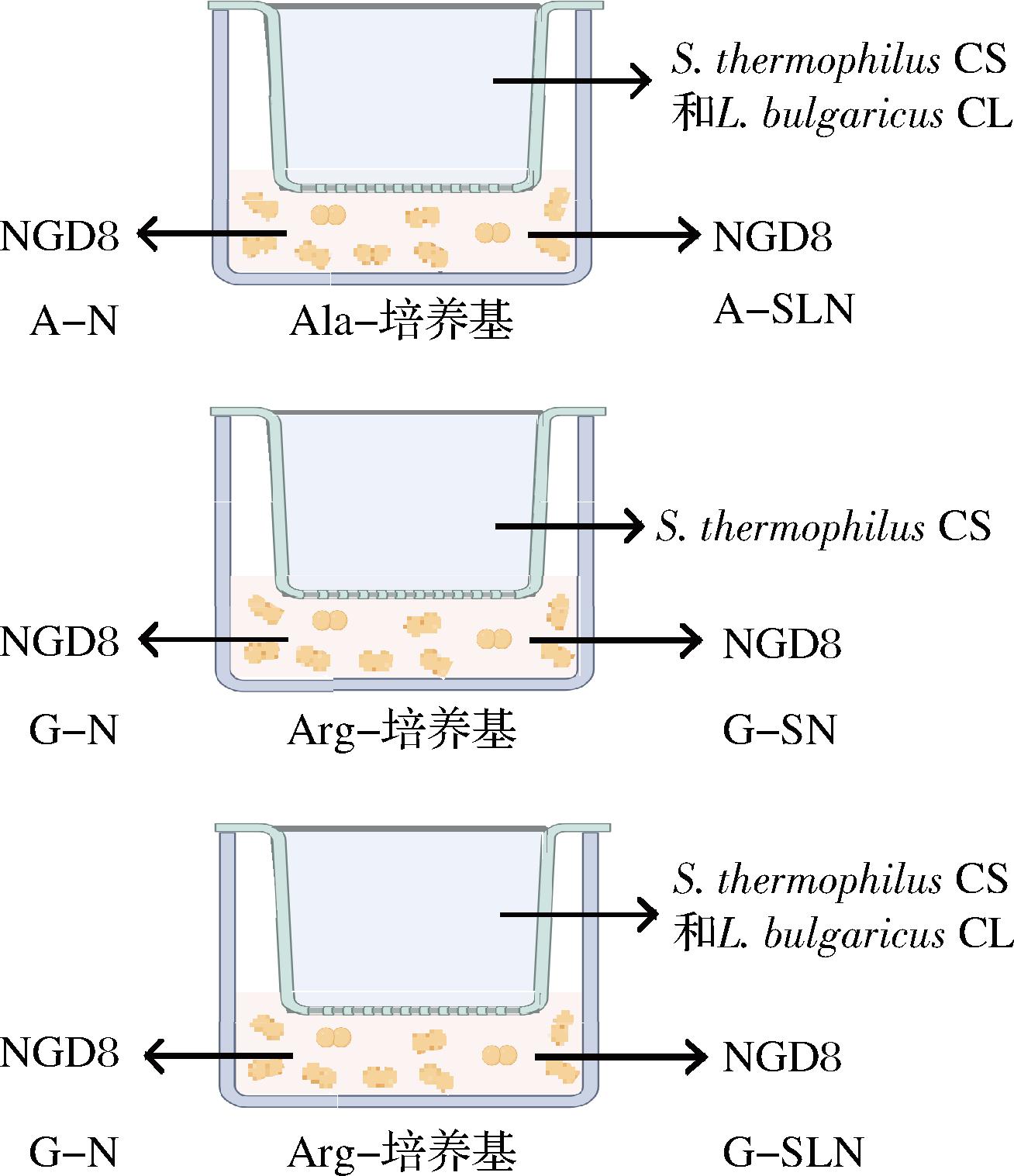
图2 用于探究氨基酸互作关系的Transwell共培养设计
Fig.2 Transwell co-culture design for investigating amino acid interaction relationships
在Ala-培养基中,上层小室有无CS和CL条件下(A-N和A-SLN),下层大室培养液中NGD8的动态生长过程,如图3-a所示。随着培养时间延长,2组差异逐渐显著:6 h时,A-SLN组中NGD8活菌数达到7.64 lg CFU/mL,显著高于A-N组的7.31 lg CFU/mL(P<0.01);12 h时,A-SLN组中NGD8活菌数进一步增至9.43 lg CFU/mL,而A-N组仅为8.67 lg CFU/mL(P<0.000 1)。这一结果表明,虽然菌体之间不能直接接触,但商业发酵剂菌株(CS和CL)的代谢物能够促进NGD8的生长。图3-b显示了在Arg-培养基中上层小室有无CS(G-N和G-SN)或有无CS和CL(G-N和G-SLN)条件下,下层大室培养液中NGD8的动态生长过程。6 h时,G-SN组(6.91 lg CFU/mL)和G-SLN组(7.05 lg CFU/mL)的NGD8活菌数显著高于G-N组(6.08 lg CFU/mL)(P<0.000 1);12 h时,差异进一步扩大,G-SN组达到7.44 lg CFU/mL,G-SLN组达到7.46 lg CFU/mL,均显著高于G-N组的6.18 lg CFU/mL(P<0.000 1)。已有研究证明,嗜热链球菌嗜热亚种通过精氨酸双水解酶途径产生鸟氨酸等代谢物,这一过程不仅是嗜热链球菌嗜热亚种维持自身生长的关键机制,还对其生态系统中的其他乳酸菌产生影响,乳酸菌能够有效利用鸟氨酸进一步合成多种功能性代谢产物,包括胞外多糖和短链脂肪酸,进而提升发酵食品的质地、增强风味特性以及提高整体营养价值[18]。
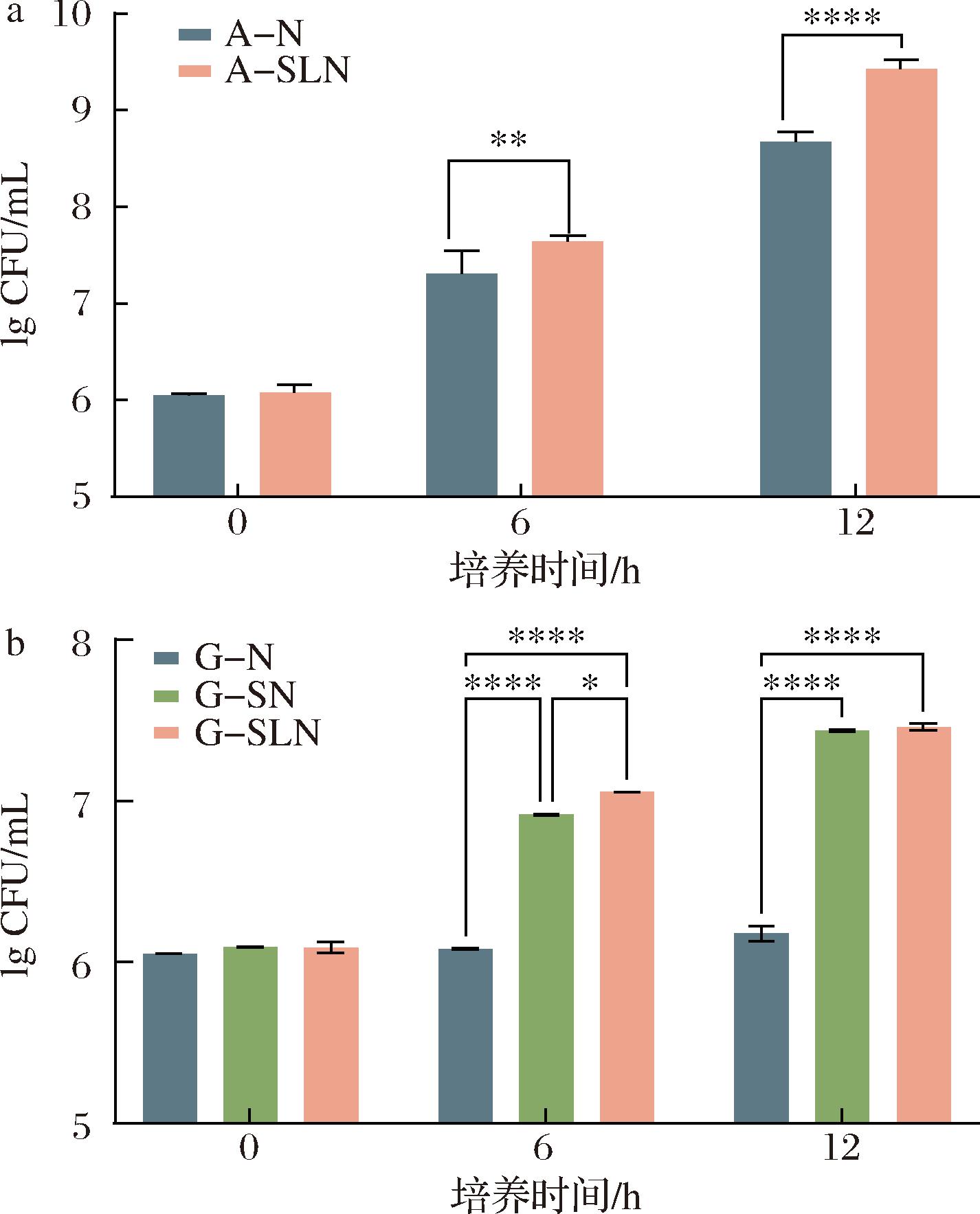
a-在Ala-培养基中,NGD8在上层小室有无商业发酵剂菌株(CS和CL)情况下菌液的动态生长过程;b-在Arg-培养基中,NGD8在上层小室有无商业发酵剂菌株(CS或CS和CL)情况下菌液的动态生长过程
图3 Transwell板下层大室中NGD培养液的生长情况
Fig.3 Growth of NGD8 culture medium in the lower chamber of the Transwell plate
2.3 乳酸乳球菌NGD8利用商业发酵剂菌株代谢产物的分析
进一步对Transwell下室培养液进行非靶向代谢物分析,将上层小室中有无相应的商业发酵剂菌株进行对比,分析下层大室中NGD8培养液的差异代谢物。
如图4所示,采用偏最小二乘判别分析(partial least squares discriminant analysis,PLS-DA)在Ala-培养基条件下进行分析,结果表明,有无商业发酵剂组的代谢物呈现显著分离状态,证实2组样本间存在明显的代谢差异。火山图分析进一步揭示,N-甲基烟酰胺和精氨酸等代谢物在下层大室NGD8培养液中显著上调,通路富集分析表明尿素循环、赖氨酸降解和天冬氨酸代谢通路被显著富集,这表明上室商业发酵剂菌株可能通过分泌精氨酸等氮源化合物和代谢中间体,为下层大室中的NGD8提供丙氨酸缺乏环境下所需的替代性营养物质[19]。此外,作为尿素循环的关键中间体,上调的精氨酸为NGD8生长提供了重要的氮源来源。此外,甘氨酸和丝氨酸等小分子氨基酸代谢通路的富集进一步说明,商业发酵剂菌株可能通过提供这些小分子氨基酸或其前体物质,有效地帮助NGD8补偿培养环境中丙氨酸的缺乏,从而促进其生长。
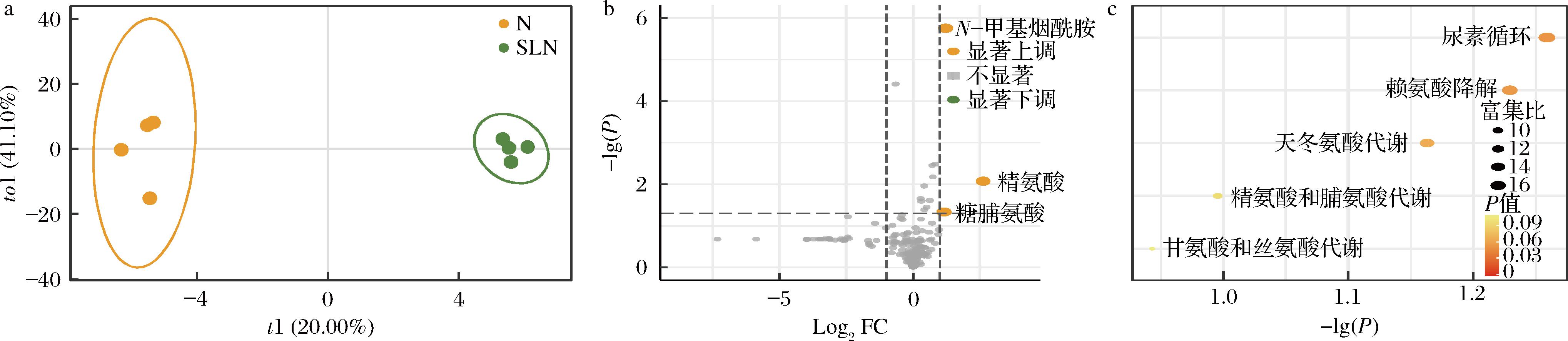
a-PLS-DA得分图;b-差异代谢物火山图;c-代谢通路分析
图4 在Ala-培养基中,Transwell板下层大室NGD8培养液(A-SLN)非靶向代谢组学分析
Fig.4 In Ala-medium, NGD8 culture medium in the lower chamber of the Transwell plate(A-SLN)
在Arg-培养基中,进一步探究上层小室中CS的存在对下层大室NGD8的影响(图5)。PLS-DA模型结果清晰地展示了2组样本在代谢谱上的显著区分,证实商业发酵剂中CS的添加引起了下室NGD8代谢网络的变化。G-N和G-SN的差异代谢物分析表明,下层大室NGD8培养液中棕榈酰乙醇胺、酪氨酸和羟基苯甲醛等代谢物发生显著变化,这反映了上室CS通过代谢物交换引起下室NGD8脂质代谢和芳香族氨基酸代谢网络的重构[20]。通路富集分析显示甲状腺激素合成和儿茶酚胺生物合成通路被显著激活,揭示了NGD8通过酪氨酸相关代谢途径应对精氨酸缺乏的分子机制。
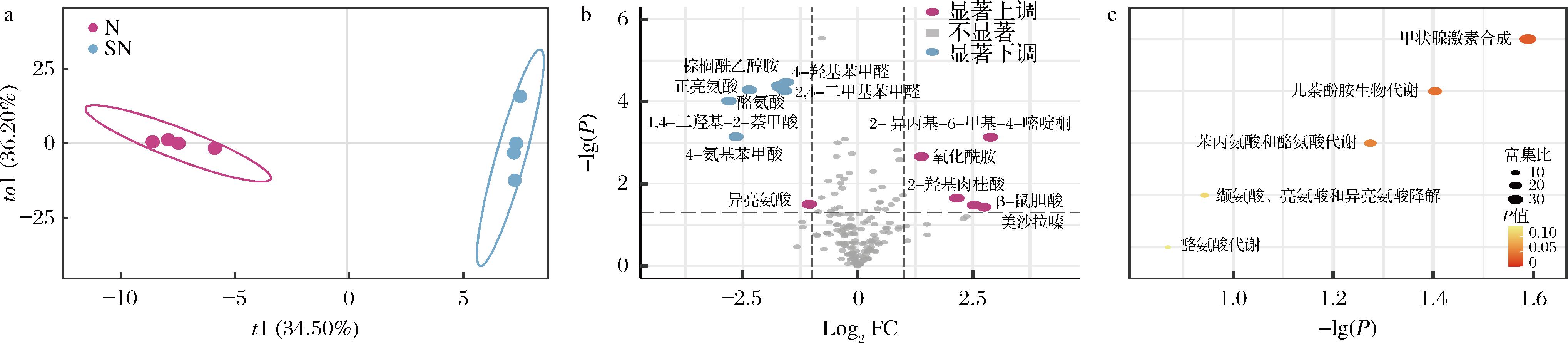
a-PLS-DA得分图;b-差异代谢物火山图;c-代谢通路分析
图5 在Arg-培养基中,Transwell板下层大室NGD8培养液(G-SN)非靶向代谢组学分析
Fig.5 In Arg-medium, NGD8 culture medium in the lower chamber of the Transwell plate(G-SN)
如图6所示,上层小室中商业发酵剂菌株(CS和CL)对下层NGD8菌株代谢产生了显著影响。在G-SLN培养体系中,下室NGD8培养液中酪氨酸的上调现象可通过转氨基作用为细胞提供必需的氮源,同时产生的α-酮酸可直接进入中心碳代谢途径。这一代谢交叉调控机制与KODURU等[21]关于乳酸菌氨基酸代谢的研究结果相一致。通过比较G-N和G-SLN两种培养模式发现,微生物间的代谢互作呈现出更为复杂且精细的调控模式。代谢组学分析揭示,2,6-二甲基吡嗪、吲哚乳酸和糖精氨酸等差异代谢物在下室NGD8中显著上调,表明上室混合菌株通过协同作用强化了下室NGD8的芳香族氨基酸代谢和吲哚衍生物合成通路。苯丙氨酸和酪氨酸代谢通路的显著富集进一步验证了这一发现,这些芳香族氨基酸及其代谢产物不仅作为精氨酸缺乏条件下的替代氮源,还可能参与构建复杂的细胞间信号传导网络。特别是作为色氨酸代谢的重要产物,吲哚乳酸在细菌间信号传导中发挥着关键的调控作用,可能是微生物群落间代谢互作的重要媒介分子。
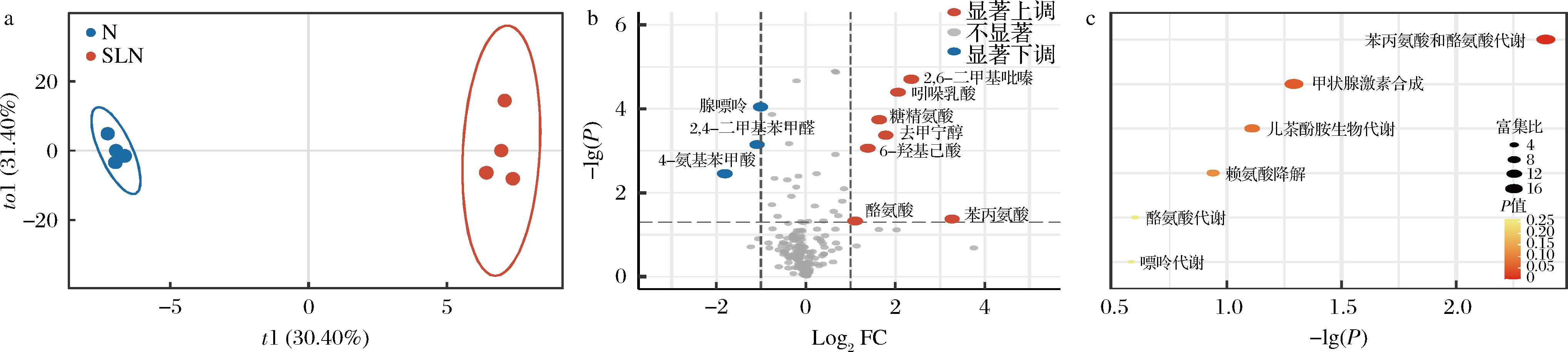
a-PLS-DA得分图;b-差异代谢物火山图;c-代谢通路分析
图6 在Arg-培养基中,Transwell板下层大室NGD8培养液(G-SLN)的非靶向代谢组学分析
Fig.6 In Arg-medium, NGD8 culture medium in the lower chamber of the Transwell plate(G-SLN)
上述实验共同揭示了NGD8与商业发酵剂菌株(CS和CL)在氨基酸缺乏条件下复杂的代谢互补机制。在实际发酵乳生产过程中,这种精细的代谢物交换网络相互影响,共同塑造发酵环境。
3 结论
通过氨基酸缺陷型分析和Transwell验证实验,揭示了复合发酵体系中氨基酸互作的核心作用。利用氨基酸缺陷型培养基实验确定了3种主要氨基酸代谢互作模式:丙氨酸代谢互作(A-SLN)和精氨酸代谢互作(G-SN、G-SLN)。通过Transwell实验,揭示了NGD8与商业发酵剂菌株之间存在显著的氨基酸代谢互补:在丙氨酸缺陷型培养基中,上室商业菌株通过代谢物交换引起下室NGD8代谢网络重构;在精氨酸缺陷型培养基中,CS诱导NGD8脂质代谢和芳香族氨基酸代谢重组,当CS和CL菌株共同存在时增强了NGD8的芳香族氨基酸代谢和吲哚衍生物合成通路。
[1] KESER G, OZCAN T.Cross-over fermentation dynamics and proteomic properties of acid gels with indigenous Lactobacillus spp.isolated from cheeses[J].Food Microbiology, 2025, 128:104700.
[2] BANKOLE A O, IRONDI E A, AWOYALE W, et al.Application of natural and modified additives in yogurt formulation:Types, production, and rheological and nutraceutical benefits[J].Frontiers in Nutrition, 2023, 10:1257439.
[3] KONDROTIENE K, ZAVISTANAVICIUTE P, AKSOMAITIENE J, et al.Lactococcus lactis in dairy fermentation:Health-promoting and probiotic properties[J].Fermentation, 2023, 10(1):16.
[4] KELLEHER P, BOTTACINI F, MAHONY J, et al.Comparative and functional genomics of the Lactococcus lactis taxon;insights into evolution and niche adaptation[J].BMC Genomics, 2017, 18(1):267.
[5] YAN S K, HUANG P, YU L L, et al.Metabolomic analysis reveals Ligilactobacillus salivarius CCFM 1266 fermentation improves dairy product quality[J].Food Research International, 2024, 188:114309.
[6] MELKONIAN C, ZORRILLA F, KJ☞RBØLLING I, et al.Microbial interactions shape cheese flavour formation[J].Nature Communications, 2023, 14:8348.
[7] ADEYEMO S M, AWOJOBI K O, OGUNLUSI E D.Biosynthesis of enzymes in fermented foods by lactic acid bacteria and possible use as bio-preservative in fermented milk[J].Journal of Advances in Biology &Biotechnology, 2018, 19(3):1-11.
[8] ZIESACK M, GIBSON T, OLIVER J K W, et al.Engineered interspecies amino acid cross-feeding increases population evenness in a synthetic bacterial consortium[J].mSystems, 2019, 4(4):e00352-19.
[9] YAN X, LI S, TU T Y, et al.Free amino acids identification and process optimization in greengage wine fermentation and flavor formation[J].Journal of Food Science, 2023, 88(3):988-1003.
[10] MARIN K, KR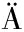 MER R.Amino acid transport systems in biotechnologically relevant bacteria[M].Amino Acid Biosynthesis~Pathways, Regulation and Metabolic Engineering.Berlin, Heidelberg:Springer, 2007:289-325.
MER R.Amino acid transport systems in biotechnologically relevant bacteria[M].Amino Acid Biosynthesis~Pathways, Regulation and Metabolic Engineering.Berlin, Heidelberg:Springer, 2007:289-325.
[11] LIU C, BI Y P, MA D Y, et al.Optimization of asparagus juice co-fermented with lactic acid bacteria and yeast,and the flavor components analysis of the products[J].Food and Fermentation Industries, 2023.
[12] JIANG L, SHEN S W, ZUO A T, et al.Characterizing flavor development in low-salt Chinese horse bean-chili paste through integrated metabolomics and metagenomics[J].Food Chemistry, 2025, 463:141076.
[13] RAVIKRISHNAN A, BLANK L M, SRIVASTAVA S, et al.Investigating metabolic interactions in a microbial co-culture through integrated modelling and experiments[J].Computational and Structural Biotechnology Journal, 2020, 18:1249-1258.
[14] WU R, CHEN J Y, ZHANG L S, et al.LC/MS-based metabolomics to evaluate the milk composition of human, horse, goat and cow from China[J].European Food Research and Technology, 2021, 247(3):663-675.
[15] QIAO Y Z, HUANG Q W, GUO H Y, et al.Nutrient status changes bacterial interactions in a synthetic community[J].Applied and Environmental Microbiology, 2024, 90(1):e0156623.
[16] ARIOLI S, DELLA SCALA G, REMAGNI M C, et al.Streptococcus thermophilus urease activity boosts Lactobacillus delbrueckii subsp.bulgaricus homolactic fermentation[J].International Journal of Food Microbiology, 2017, 247:55-64.
[17] PESSIONE A, LAMBERTI C, PESSIONE E.Proteomics as a tool for studying energy metabolism in lactic acid bacteria[J].Molecular BioSystems, 2010, 6(8):1419-1430.
[18] SASAKI M, KODAMA Y, SHIMOYAMA Y, et al.Aciduricity and acid tolerance mechanisms of Streptococcus anginosus[J].The Journal of General and Applied Microbiology, 2018, 64(4):174-179.
[19] SHIMIZU K, MATSUOKA Y.Feedback regulation and coordination of the main metabolism for bacterial growth and metabolic engineering for amino acid fermentation[J].Biotechnology Advances, 2022, 55:107887.
[20] GAO Y, SKOWYRA M L, FENG P Q, et al.Protein import into peroxisomes occurs through a nuclear pore-like phase[J].Science, 2022, 378(6625):eadf3971.
[21] KODURU L, KIM Y, BANG J, et al.Genome-scale modeling and transcriptome analysis of Leuconostoc mesenteroides unravel the redox governed metabolic states in obligate heterofermentative lactic acid bacteria[J].Scientific Reports, 2017, 7:15721.