2型糖尿病(type 2 diabetes mellitus,T2DM)是一种全球性代谢疾病,严重威胁全球数亿人口的健康[1]。根据国际糖尿病联合会( international diabetes federation,IDF)的数据,中国成人患糖尿病人数最多,占全球糖尿病患者的1/4,高达1.43亿人,患病率约为12%[2]。预计到2050年,全球将有13.1亿糖尿病患者[3]。T2DM可导致各种并发症,损害心血管系统、内分泌系统、神经系统和泌尿系统等组织器官[4],已成为世界范围内导致死亡的主要慢性疾病之一。目前,T2DM的治疗策略包括生活方式的改变和口服降糖药物,如双胍类、钠-葡萄糖共转运抑制剂、磺酰脲类、α-葡萄糖苷酶抑制剂和二肽基肽酶-4抑制剂等[5]。然而,这些抗糖尿病药物通常具有副作用,包括体重增加、低血糖和心力衰竭等,限制了它们的长期使用[6]。因此,迫切需要寻找新的,更安全、更有效的抗糖尿病产品进行早期预防和治疗。
近年来,功能性食品已成为预防和治疗包括T2DM在内的慢性代谢性疾病的有效策略。这些食物除了提供基本营养外,还富含生物活性物质,帮助机体调节代谢途径并改善生理功能,从而提供健康益处。药食同源植物兼具食用属性和药用价值,含有多种活性成分,如皂苷、黄酮类化合物、多酚、多糖等,并且这些成分已被证明具有广泛的生物活性,包括抗炎、抗氧化和预防糖尿病等特性[1],因此,药食同源植物是功能性食品的重要构成部分。黄精饮料由西伯利亚黄精、玉竹和枸杞3种药食同源植物组成,富含生物碱、皂苷和多糖等生物活性物质,具有降血糖、降血脂、抗氧化和抗糖尿病的作用[7-8]。菊苣是一种兼具食用和药用双重功能的植物,食用发酵菊苣可显著降低空腹血糖、糖化血红蛋白和胰岛素抵抗水平,同时减轻胰岛素靶器官的炎症反应[1]。此外,研究发现黄芪中的黄酮类化合物可以有效预防糖尿病中的氧化损伤,同时延缓糖尿病并发症的发生与发展[9]。由此可见,药食同源植物是功能性食品原料的宝贵来源。
荷叶是一种著名的药食同源植物,其具有良好的风味和营养特性,既可以用作食品原料,也可以用作食品辅料进行食品加工[10]。荷叶中含有丰富的活性化合物,包括生物碱、黄酮类化合物、单宁和精油等,具有抗肥胖、抗糖尿病、抗氧化、抗炎、肾脏保护和神经调节等作用[11]。荷叶茶冲剂已被证实具有调节糖脂代谢的作用,这是因为荷叶在冲泡过程中,多糖、黄酮类化合物和生物碱等生物活性成分会被热水提取出来[12]。这些活性成分通过调节肠道菌群,促进有益代谢产物产生,并通过血液循环到达肝脏,激活胰岛素信号,调节糖脂代谢,从而减轻肝脏、肾和胰腺损伤[12]。这些特性表明,荷叶有望成为辅助治疗糖尿病的潜在原料。基于此,本研究采用热浸提法提取荷叶汁,将浸提液与牛奶一起共同发酵制备荷叶酸奶,测定荷叶酸奶的抗氧化活性、α-淀粉酶和α-葡萄糖苷酶抑制率,旨在为荷叶的综合利用和荷叶相关食品的研究开发提供新的思路。
1 材料与方法
1.1 材料与试剂
荷叶粉,昆明轩庆生物科技有限公司;300型丹尼斯克酸奶发酵剂,丹尼斯克(中国)有限公司;脱脂奶粉(蛋白质32.9 g/100 g),恒天然商贸(上海)有限公司;MRS培养基、MC琼脂培养基,北京陆桥技术股份有限公司;可溶性淀粉、α-葡萄糖苷酶、α-淀粉酶、过硫酸钾,上海麦克林生化科技股份有限公司;1-二苯基-2-三硝基苯肼(DPPH),天津希恩思生化科技有限公司;2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(ABTS),上海笛柏生物科技有限公司;总抗氧化能力(total antioxidant capacity,T-AOC)检测试剂盒,北京索莱宝科技有限公司。
1.2 仪器设备
Synergy H1酶标仪,美国基因公司;MCR302模块化旋转与界面流变仪,奥地利安东帕公司;TA.XT Plus质构仪,英国Stable Micro Systems公司;C-Nose电子鼻,上海保圣实业发展有限公司;PHS-320 pH计,成都世纪方舟科技有限公司;GHP-9080恒温培养箱,上海齐欣科学仪器有限公司。
1.3 实验方法
1.3.1 荷叶粉浸提液的制备
称取适量的荷叶粉,按1∶10(g∶mL)的料液比加入适量体积的纯净水,搅拌混合均匀后,在85 ℃水浴锅中浸提1.5 h,用纱布或滤网过滤得到荷叶粉浸提液,取澄清液备用[13]。
1.3.2 酸奶的制备
将脱脂乳粉按照1∶10(g∶mL)加入纯净水和10%(质量分数)荷叶粉浸提液,对照组不添加浸提液,使用纯净水替代,白砂糖添加量为7%。然后45 ℃水浴30 min,均质,95 ℃灭菌5 min,冷却至42 ℃,随后加入0.2 g/L的酸奶发酵剂,搅拌均匀后分装至无菌杯中,放置于42 ℃恒温培养箱中发酵,直至可滴定酸度(titratable acid,TA)达到70 °T后,取出置于4 ℃冰箱中冷藏18~24 h进行后熟,待测定相关理化指标。
1.3.3 pH值和TA测定
使用pH计测定酸奶pH值。参照GB 5009.239—2016《食品安全国家标准 食品酸度的测定》测定酸奶的TA。即称取10.00 g酸奶样品,使用0.1 mol/L NaOH溶液进行滴定。根据NaOH溶液的消耗量计算TA。
1.3.4 活菌数的测定
参考GB 4789.35—2023《食品安全国家标准 食品微生物学检验 乳酸菌检验》测定酸奶中乳杆菌属和唾液链球菌嗜热亚种活菌数。将酸奶样品在无菌操作台中依次进行10倍梯度稀释,吸取100 μL适当稀释度样品溶液于固体培养基上涂布均匀,37 ℃培养箱培养48~72 h,选择菌落数为30~300的稀释度计算菌落总数,乳酸菌活菌数为乳杆菌属和唾液链球菌嗜热亚种活菌计数之和。
1.3.5 持水力的测定
持水力的测定参照ZHOU等[14]的方法略作修改,称取10.00 g酸奶样品,采用4 000 r/min离心10 min,除去上清液后,称量沉淀质量,并按公式(1)计算持水力:
持水力![]()
(1)
1.3.6 质构的测定
参考董闯等[15]的方法略作修改,使用P/36R探头,采用50%形变量,5 g触发力,压缩停留5 s。测试速度1.0 mm/s。
1.3.7 流变特性的测定
使用模块化旋转与界面流变仪测定酸奶的流变特性,平板探头直径为50 mm,应变设置为0.5%,频率范围0.1~10 Hz,剪切速率0.1-1~1 000-1,测试温度25 ℃,每组测3次生物平行[16]。
1.3.8 电子鼻的测定
准确称取10.00 g酸奶样品于顶空瓶中,加盖密封,45 ℃水浴平衡30 min后进行检测。清洗时间120 s,测定时间60 s,流速400 mL/min。电子鼻共有10个不同的传感器,每个传感器对应的敏感物质如表1所示。
表1 电子鼻传感器阵列
Table 1 Electronic nose sensor array

序号传感器敏感物质1S1芳香成分、苯类2S2氮氧化合物3S3芳香成分、氨类
续表1

序号传感器敏感物质4S4氢化物5S5短链烷烃芳香成分6S6甲基类物质7S7硫化合物8S8醇类、醛类9S9芳香成分、有机硫化物10S10长链烷烃
1.3.9 α-淀粉酶抑制率的测定
称取适量样品离心,吸取上清液,使用PBS(pH 6.8)稀释2.5倍,取500 μL稀释样品溶液与500 μL α-淀粉酶溶液(5 U/mL)涡旋混匀,再加入500 μL PBS缓冲液,37 ℃水浴10 min;随后加入500 μL可溶性淀粉溶液(10 mg/mL),37 ℃继续反应10 min;最后加入1 500 μL DNS显色剂(DNS显色剂配置:称取182.0 g酒石酸钠加入500 mL热水中,再加入2 moL/L NaOH溶液262 mL和6.3 g 3,5二硝基水杨酸,然后再加入5.0 g苯酚和5.0 g Na2SO3,充分混匀,定容至1 L,棕色瓶中贮存7~10 d后使用。),沸水浴中加热5 min终止反应,迅速冷却后,加水稀释30倍,在波长540 nm处测定吸光值[17]。每组测3次平行,按照公式(2)计算:
抑制率![]()
(2)
式中:A,加酶不加样品管吸光度值;B,不加酶不加样品管吸光度值;C,加酶加样品管吸光度;D,不加酶加样品管吸光度值。
1.3.10 α-葡萄糖苷酶抑制率的测定
取适量酸奶样品离心,吸取上清液,使用PBS稀释1.5倍。将1.2 mL稀释样品溶液、1.2 mL葡萄糖苷酶溶液(0.25 U/mL)和1.2 mL PBS涡旋混匀,37 ℃恒温培养10 min,然后加入1.2 mL预先37 ℃保温的α-D-吡喃葡萄糖苷溶液(5 mmol/L),37 ℃条件下继续反应30 min。反应完成后,加入3.6 mL Na2CO3(0.20 mol/L)终止反应,在波长405 nm处测定吸光值[18],按照公式(2)计算。
1.3.11 T-AOC的测定
分别称取2.5 g荷叶酸奶和对照酸奶于10 mL离心管中,加入5 mL无水乙醇,充分混匀后,在5 000 r/min条件下离心30 min,收集上清液用于抗氧化能力测定。
1.3.11.1 DPPH自由基清除率测定[18]
称取7.9 mg的DPPH粉末溶于无水乙醇,混匀定容到100 mL,配制成浓度为0.2 mmol/L DDPH溶液。然后将2 mL提取液与2 mL DPPH溶液混匀,室温下避光反应30 min,5 000 r/min离心10 min,取上清液于517 nm测定吸光度值。DPPH自由基清除率按照公式(3)计算:
DPPH自由基清除率![]()
(3)
式中:C,样品溶液与DPPH溶液混合后测定的吸光度值;B,无水乙醇和样品混合后的吸光度值;A,无水乙醇和DPPH混合后的吸光度值。
1.3.11.2 ABTS阳离子自由基清除率测定[18]
将5 mmol/L过硫酸钾和14 mmol/L ABTS溶液体积比1∶1混合,置于黑暗中孵育12~16 h得到母液,用无水乙醇将母液进行稀释,吸光度在734 nm下维持在0.700±0.020。取0.5 mL上清液,加入4.0 mL ABTS溶液,混匀,避光放置20 min,在734 nm下测得的吸光度为B;无水乙醇作为空白对照,测定吸光度记为A。ABTS阳离子自由基清除率按照公式(4)计算:
ABTS阳离子自由基清除率![]()
(4)
式中:A,无水乙醇与ABTS溶液混合后测定的吸光度值;B,上清液样品和ABTS混匀后的吸光度值。
1.3.11.3 T-AOC检测
根据T-AOC检测试剂盒(FRAP法)说明书,测定酸奶的总抗氧化能力。
1.4 数据处理
采用SPSS 22.0中的t检验及One-way ANOVA中的Tunky进行显著性分析,试验结果以“平均值±标准差”表示,采用Graphpad Prism 8.0.6绘图,每组3个平行。
2 结果与分析
2.1 荷叶酸奶发酵过程中pH和TA的变化
如图1所示,在整个发酵过程中pH显著性降低,TA显著性上升(P<0.05)。发酵第5 h,荷叶酸奶的TA达到(70.96±0.88)°T,而对照组TA仅达到(60.28±0.79)°T。随着发酵进行,对照酸奶6 h TA值达到(74.60±0.72) °T[14]。由此可见,荷叶在一定程度上促进酸奶发酵,缩短发酵时间。
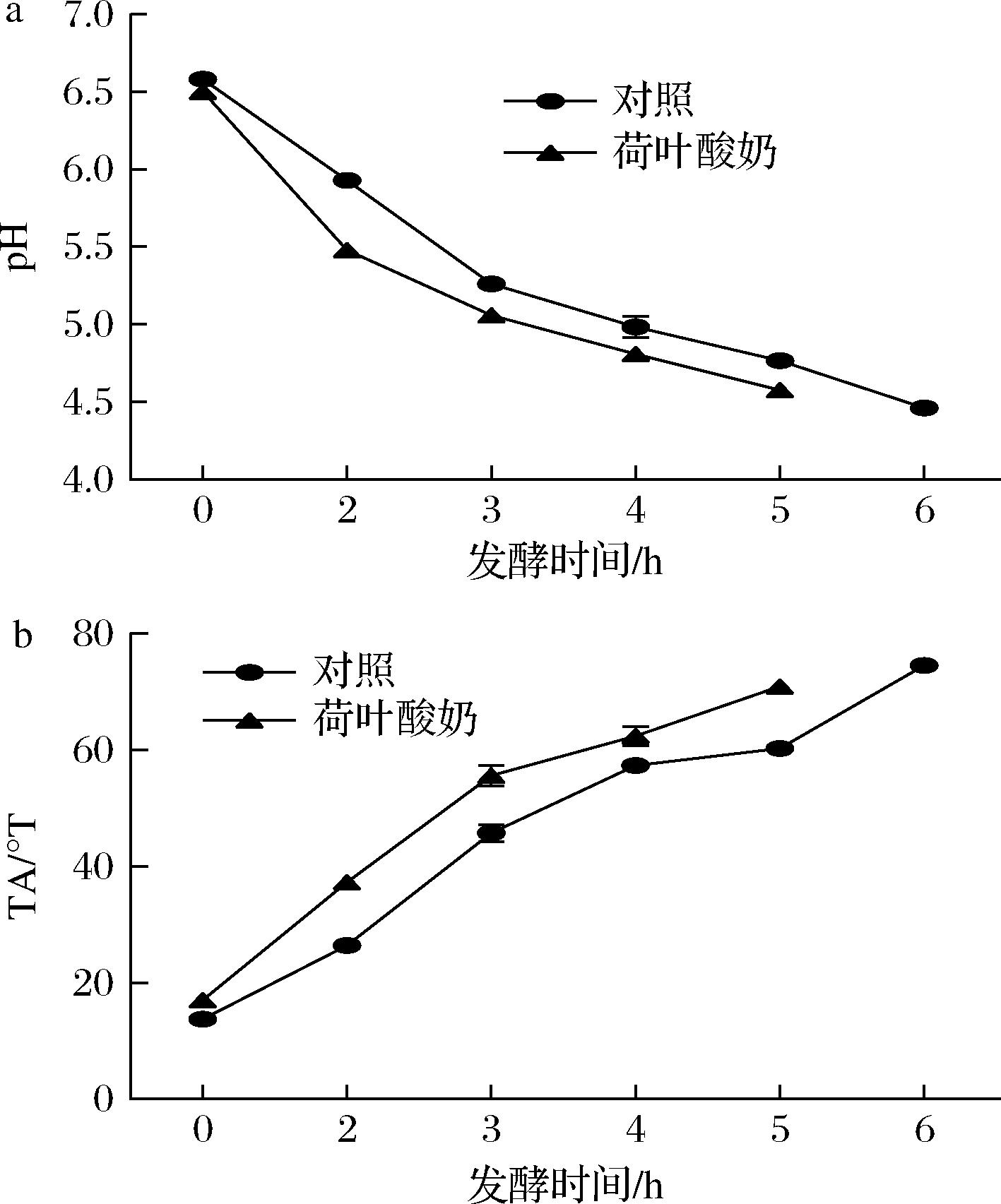
a-pH值;b-TA
图1 酸奶发酵过程中pH和TA的变化
Fig.1 Changes of pH and TA during yogurt fermentation
2.2 荷叶酸奶贮藏过程中pH和TA的变化
酸奶贮藏过程中,pH的降低和TA的升高在一定程度上会影响产品品质,缩短保质期。贮藏过程中酸奶保持适当的酸度尤为重要。通常,TA为70~110 °T是消费者可以接受的酸度[19]。图2-a~图2-b是2组酸奶贮藏过程中pH和TA的变化,在整个贮藏过程中,pH值呈下降趋势。相反,TA呈上升趋势。贮藏结束时,对照酸奶TA达到(91.85±1.62)°T,荷叶酸奶TA为(90.28±0.89)°T,2组之间无显著性差异(P >0.05),TA均在消费者可接受范围内。
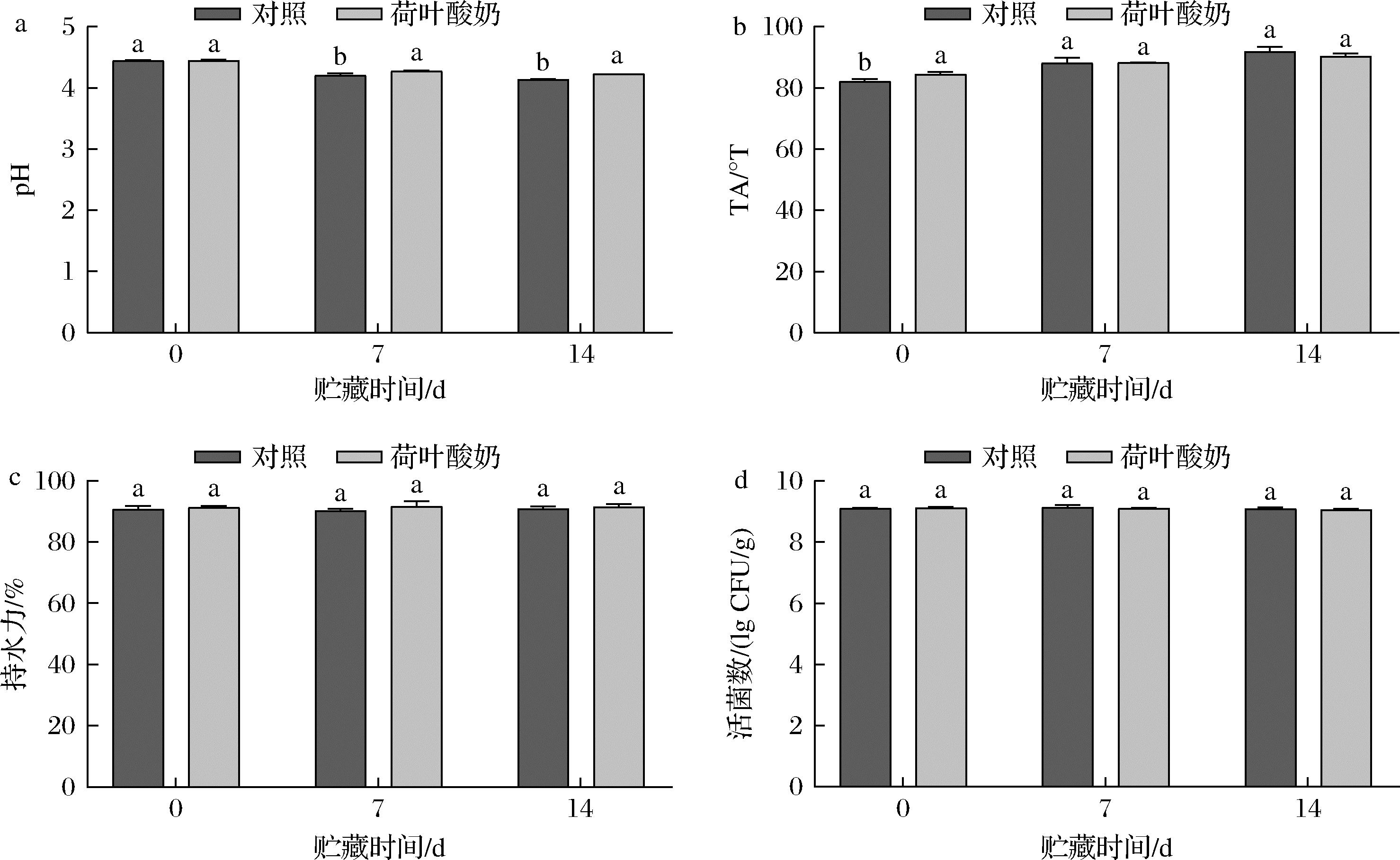
a-pH值;b-TA;c-持水力;d-活菌数
图2 酸奶贮藏过程中理化特性变化
Fig.2 Changes of physicochemical properties of yogurt during storage
注:不同小写字母表示2组之间具有显著性差异(P<0.05,图6、图7同)。
2.3 荷叶酸奶贮藏过程中持水力分析
持水力是影响酸奶保质期和消费者接受度的重要因素。如图2-c所示,贮藏初期,对照酸奶持水力为90.71%,荷叶酸奶持水力为91.24%。贮藏14 d后,对照酸奶持水力为90.81%,荷叶酸奶持水力为91.47%,2组之间持水力无显著性变化(P>0.05)。这意味着荷叶的添加不会影响酸奶的持水能力。
2.4 荷叶酸奶贮藏过程中活菌数变化
乳酸菌的存活能力是酸奶贮藏过程中的一个关键指标。如图2-d所示,贮藏第0天,对照酸奶的活菌数为9.10 lg CFU/g,荷叶酸奶的活菌数为9.11 lg CFU/g,2组之间活菌数无显著性差异(P>0.05)。在整个贮藏过程中,酸奶的活菌数没有发生显著性变化。贮藏结束,对照组酸奶活菌数为9.08 lg CFU/g,荷叶酸奶活菌数为9.05 lg CFU/g,2组间差异不显著(P>0.05)。说明荷叶的添加不会影响酸奶贮藏过程中活菌数的变化,具有良好的稳定性。
2.5 荷叶酸奶贮藏过程中质地分析
硬度是酸奶的一个重要质地特性。由图3-a可知,荷叶酸奶硬度值显著低于对照酸奶(P<0.05)。贮藏初期,对照酸奶和荷叶酸奶的硬度值分别为235.73 N和207.83 N。随着贮藏时间的延长,2组酸奶硬度值显著性增加(P<0.05),贮藏结束时,2组酸奶的硬度值分别为278.70 N和232.98 N。与对照组相比,荷叶酸奶的硬度值降低16.40%。这表明,荷叶的添加可能会影响酸奶的凝胶网络,降低其硬度。但是荷叶的添加对酸奶的弹性、内聚力和回弹性无显著性影响(P>0.05),对胶着性和咀嚼性具有显著性影响(P<0.05)。总之,荷叶的添加对酸奶贮藏稳定性无显著性影响(P>0.05)。
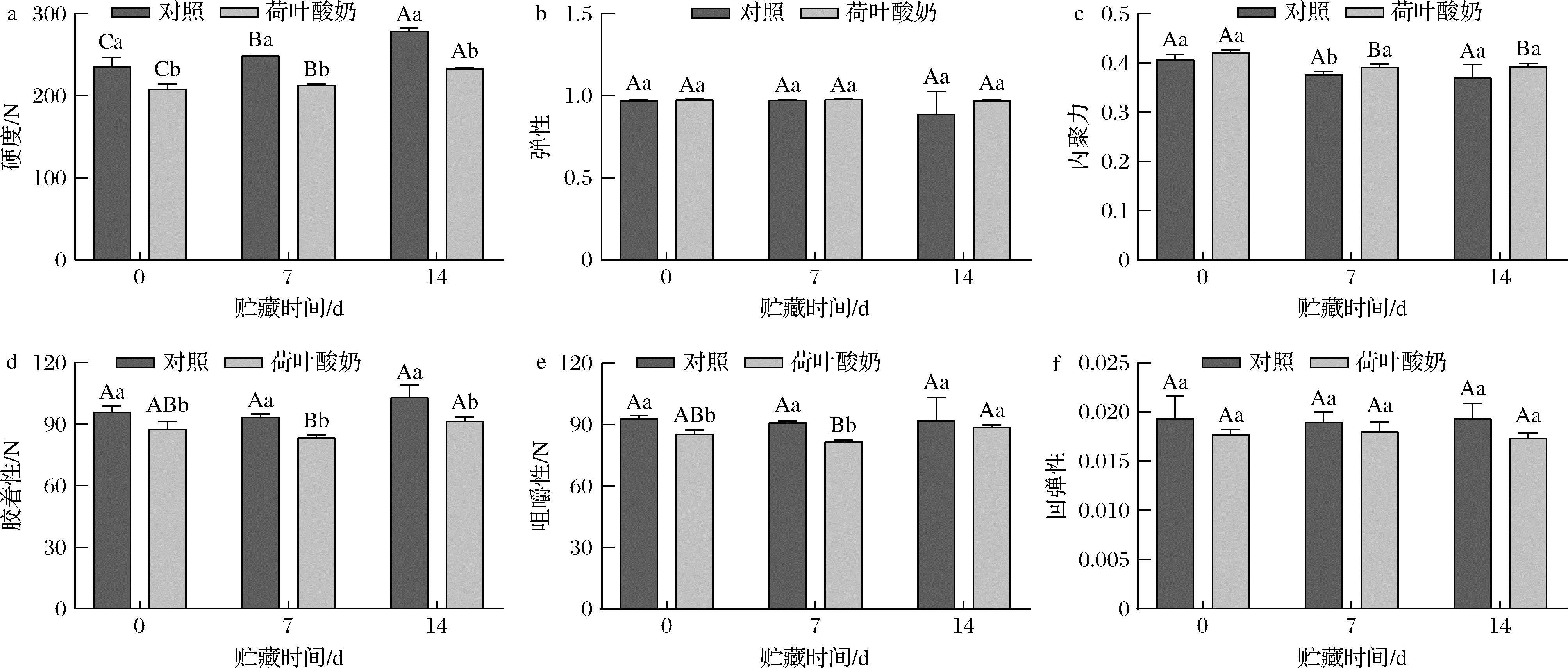
a-硬度;b-弹性;c-内聚力;d-胶着性;e-咀嚼性;f-回弹性
图3 酸奶贮藏过程中质构变化
Fig.3 Texture changes of yogurt during storage
注:不同大写字母表示贮藏期间组内具有显著性差异,不同小写字母表示2组之间具有显著性差异(P<0.05)(下同)。
2.6 荷叶酸奶流变学特性分析
酸奶的质地特性是影响消费者对产品接受度的重要因素,理想的酸奶应具有黏稠、均匀且细腻的质地[20]。由图4-a和图4-b可知,2组酸奶样品的储能模量和损耗模量均以频率依赖的方式增加,且荷叶酸奶高于对照酸奶。此外,如图4-c所示,荷叶酸奶的损耗正切值大于对照酸奶,并随着频率的增加而增加,但2组酸奶的损耗正切值均小于1,这表明其蛋白质网络结构良好,酸奶分子流动性低,产品均具有弹性的固体样特性[20]。如图4-d所示,2组酸奶样品的表观黏度随着剪切速率的增加而降低,表现出假塑性行为。在整个剪切速率范围内,荷叶酸奶与对照酸奶黏度无显著性差异(P>0.05)。
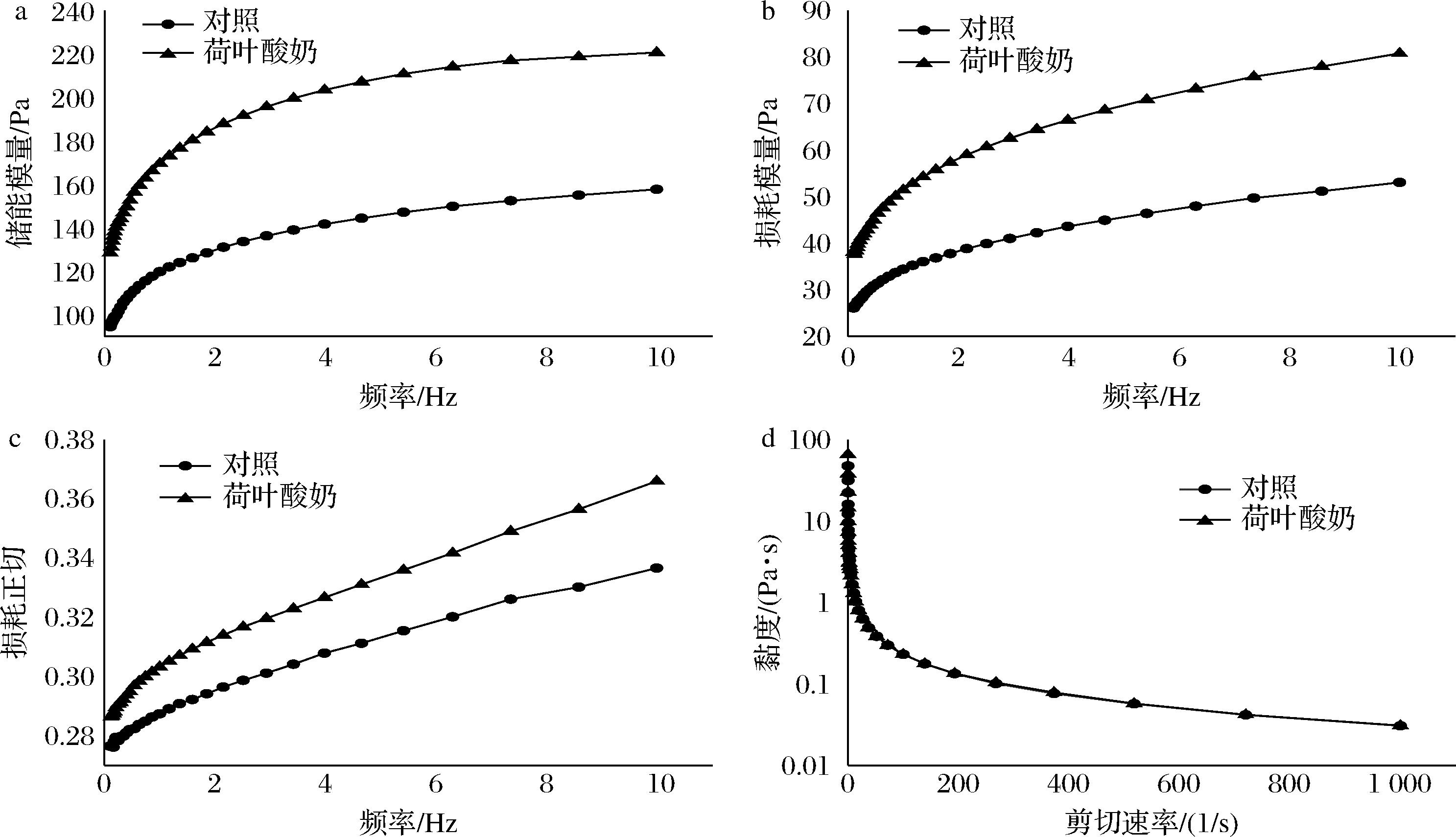
a-储能模量;b-损耗模量;c-损耗正切;d-黏度
图4 酸奶流变学特性
Fig.4 Rheological properties of yogurt
2.7 荷叶酸奶电子鼻分析
图5-a是酸奶的电子鼻雷达图,电子鼻共有10个传感器,每个传感器对酸奶风味成分的敏感程度各不相同,其中S1~S3和S7~S10传感器的响应值较高,表明酸奶中芳香成分、醇类、醛类、硫化物等物质含量较高。这些传感器所响应的化合物已经涵盖了酸奶中常见的大多数挥发性化合物,即硫化物、醇类、醛类和酮类[21]。值得注意的是,除传感器S3(芳香成分和氨类)外,荷叶酸奶的其他传感器响应值均低于对照酸奶,这表明荷叶酸奶与对照酸奶的香气成分明显不同。进一步使用主成分分析观察2组酸奶样品间是否发生聚类,如图5-b所示,2组酸奶样本相互分离,同一组样本聚集在一起,PC1和PC2的贡献率分别为97.0%和2.4%,总贡献率为99.4%。说明2组酸奶的香气成分具有明显差异,荷叶的添加显著改变酸奶的香气组成。
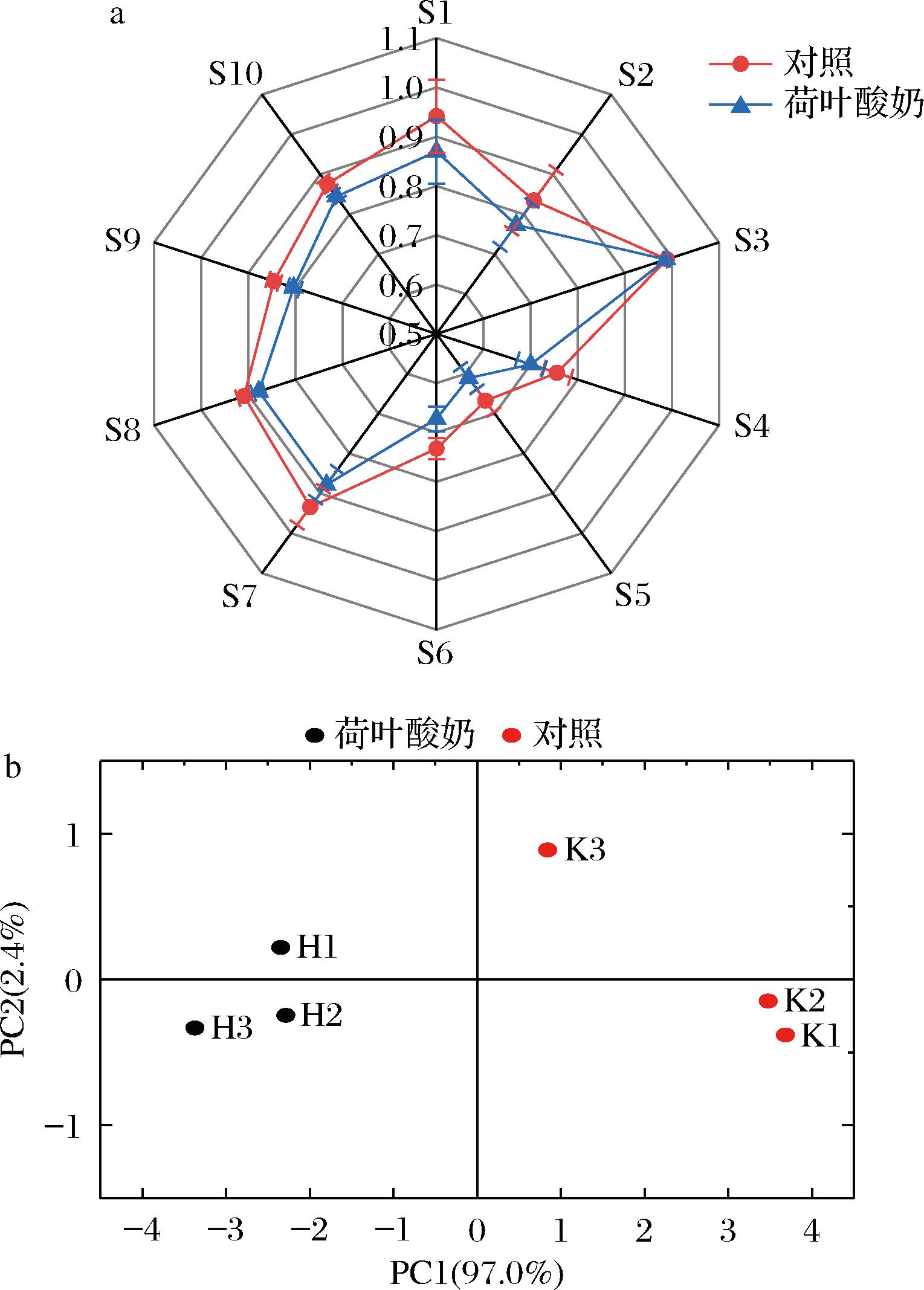
a-电子鼻雷达图;b-主成分分析
图5 酸奶电子鼻分析
Fig.5 Electronic nose analysis of yogurt
2.8 荷叶酸奶对α-淀粉酶和α-葡萄糖苷酶抑制作用
糖尿病是由胰岛素分泌缺陷、胰岛素抵抗或两者兼具引起的一种严重代谢性疾病,餐后高血糖是T2DM的典型表现[22]。α-淀粉酶和α-葡萄糖苷酶是碳水化合物消化中涉及的关键酶,通过抑制α-淀粉酶和α-葡萄糖苷酶活性来延迟葡萄糖吸收速率是调节血糖水平的有效方法[23]。如图6所示,荷叶酸奶对α-淀粉酶和α-葡萄糖苷酶的抑制率分别为46.37%和25.72%,显著性高于对照组(P<0.05)。表明荷叶酸奶具有良好的酶活性抑制能力。相关体内实验证明,荷叶中的多糖、黄酮类化合物和生物碱对糖脂代谢具有协同作用[12]。
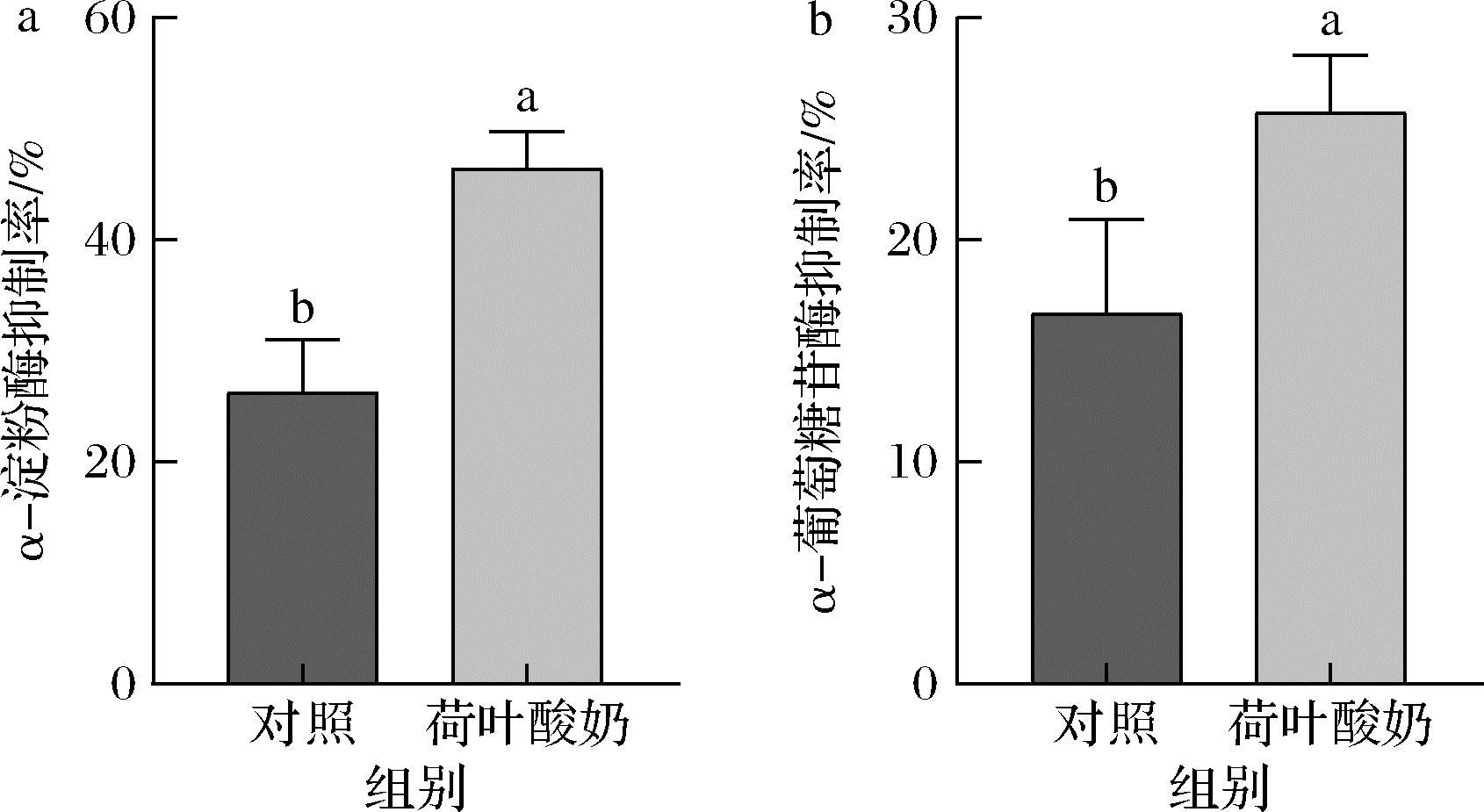
a-α-淀粉酶抑制率;b-α-葡萄糖苷酶抑制率
图6 酸奶对α-淀粉酶和α-葡萄糖苷酶活性的影响
Fig.6 Effects of yogurt on the activities of α-amylase and α-glucosidase
2.9 荷叶酸奶抗氧化活性
荷叶富含黄酮类化合物和生物碱等活性物质,其提取物具有显著的体外抗氧化活性,对多种自由基表现出优异的清除作用,在食品和制药领域表现出显著的应用潜力[24]。荷叶粉在熟猪肉冷藏期间可减少其氧化,并维持颜色的稳定[25]。如图7为荷叶酸奶的抗氧化活性,与对照组相比,荷叶酸奶的DPPH、ABTS阳离子自由基清除率和T-AOC显著性升高(P<0.05),对照组酸奶DPPH、ABTS阳离子自由基清除率和T-AOC分别为57.31%、51.33%和0.33 μmol/mL,而荷叶酸奶分别为96.01%、90.10%和1.19 μmol/mL。这些结果表明,荷叶酸奶具有良好的抗氧化活性。
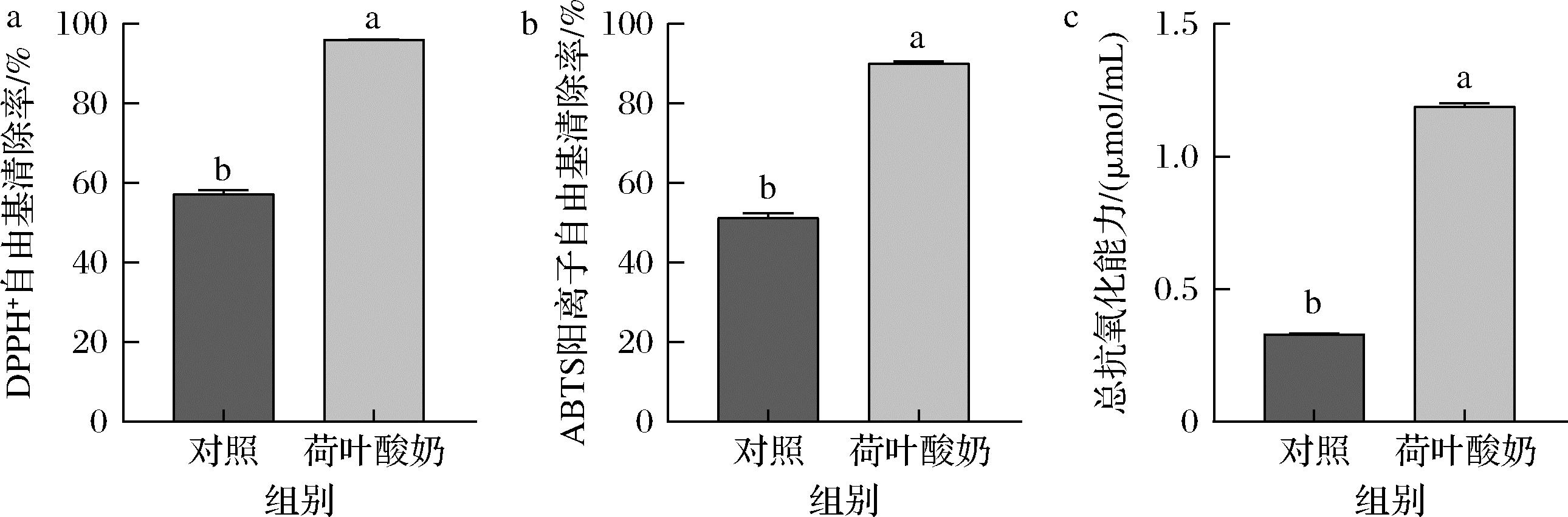
a-DPPH自由基清除率;b-ABTS阳离子自由基清除率;c-总抗氧化能力
图7 酸奶抗氧化活性
Fig.7 Antioxidant activity of yogurt
3 结论与讨论
本研究结果表明,荷叶酸奶具有理想酸奶的质地特性,并带有荷叶的清香味。贮藏期间稳定性良好,具有良好的持水力,乳酸菌活菌数保持在109 CFU/g,可滴定酸度和pH均在消费者可接受范围内。抗氧化活性、α-淀粉酶和α-葡萄糖苷酶抑制率显著性高于对照组,具有较强的抗氧化作用和酶抑制活性。该研究有利于提高荷叶的附加值,同时为荷叶产品开发提供理论依据。未来将进一步开展动物和人体试验,探究其在体内的降血糖作用,明晰其降血糖的机制,解析物质-通路-功效之间的相互作用关系。
[1] FANG S S, LIANG J Q, LI K, et al.Unraveling the mechanisms of fermented chicory root in alleviating hyperglycemia in type 2 diabetes mellitus:Based on in vivo experiments and network pharmacological study[J].Food Bioscience, 2025, 71:107043.
[2] XU Y, LU J L, LI M, et al.Diabetes in China part 2:Prevention, challenges, and progress[J].The Lancet Public Health, 2024, 9(12):e1098-e1104.
[3] 2021 DIABETES COLLABORATORS G B D.Global, regional, and national burden of diabetes from 1990 to 2021, with projections of prevalence to 2050:A systematic analysis for the Global Burden of Disease Study 2021[J].Lancet, 2023, 402(10397):203-234.
[4] GE Q, CHEN L, CHEN K P.Treatment of diabetes mellitus using iPS cells and spice polyphenols[J].Journal of Diabetes Research, 2017, 2017:5837804.
[5] WANG Y J, MA J X, TONG Y P, et al.Antidiabetic effects and mechanisms of Cyclocarya paliurus leaf flavonoids via PIK3CA[J].Journal of Functional Foods, 2024, 113:106031.
[6] CORTEZ-NAVARRETE M, PÉREZ-RUBIO K G, DE J ESCOBEDO-GUTIÉRREZ M.Role of fenugreek, cinnamon, Curcuma longa, berberine and Momordica charantia in type 2 diabetes mellitus treatment:A review[J].Pharmaceuticals, 2023, 16(4):515.
[7] YANG T T, ZHOU W T, XU W Q, et al.Modulation of gut microbiota and hypoglycemic/hypolipidemic activity of flavonoids from the fruits of Lycium barbarum on high-fat diet/streptozotocin-induced type 2 diabetic mice[J].Food &Function, 2022, 13(21):11169-11184.
[8] RUAN M X, AI Q L, CAO G C, et al.Study on the active ingredients and molecular mechanisms of Polygonatum sibiricum beverage in the intervention of type 2 diabetes mellitus based on UPLC-MS, network pharmacology and experimental validation[J].Journal of Functional Foods, 2025, 127:106762.
[9] LI J, HUANG Y Q, ZHAO S, et al.Based on network pharmacology to explore the molecular mechanisms of Astragalus membranaceus for treating T2 diabetes mellitus[J].Annals of Translational Medicine, 2019, 7(22):633.
[10] SHARMA B R, GAUTAM L N S, ADHIKARI D, et al.A comprehensive review on chemical profiling of Nelumbo nucifera:Potential for drug development[J].Phytotherapy Research, 2017, 31(1):3-26.
[11] WANG Z Y, CHENG Y, ZENG M M, et al.Lotus (Nelumbo nucifera Gaertn.) leaf:A narrative review of its phytoconstituents, health benefits and food industry applications[J].Trends in Food Science &Technology, 2021, 112:631-650.
[12] SONG Y X, KE Y, LIN L Z, et al.Comparison of in vivo glycolipid metabolism regulation pathway of lotus leaf polysaccharide and its combination with flavonoids and alkaloids:Effectiveness of high-pressure homogenization-assisted dual enzyme extraction[J].Food Bioscience, 2024, 61:104618.
[13] 孙敏. 荷叶山楂酸奶的配方研究[J].安徽农业科学, 2017,45(35):75-77.SUN M.Research on the recipe of lotus leaf and hawthorn yogurt[J].Journal of Anhui Agricultural Science, 2017,45(35):75-77.
[14] ZHOU X, WANG H W, WANG C, et al.Improvement of brown yogurt quality by Lactiplantibacillus plantarum S58 and oat β-glucan:Physicochemical properties, sensory quality, and metabolic changes[J].Food Bioscience, 2024, 62:105308.
[15] 董闯, 周小波, 祝亚辉, 等.不同处理方式对牦牛乳及酸奶理化性质的影响[J].食品与发酵工业, 2025,51(14):97-105.DONG C, ZHOU X B, ZHU Y H, et al.Effects of different treatments on physicochemical properties of yak milk and yogurt[J].Food and Fermentation Industries, 2025, 51(14):97-105.
[16] 赵晓, 杜琨, 张媛.菊粉对合生元酸奶质构、流变学特性和微观结构的影响[J].食品工业科技, 2023,44(01):72-77.ZHAO X, DU K, ZHANG Y.Effect of inulin on the texture, rheological properties, and microstructure of synbiotic yogurt[J].Science and Technology of Food Industry, 2023, 44(1):72-77.
[17] 买尔哈巴·艾合买提, 曹英, 崔卫东, 等.乳酸菌发酵驼乳工艺优化及抑制α-淀粉酶和α-葡萄糖苷酶活性的研究[J].中国乳业, 2022(8):97-107.MAIERHABA A, CAO Y, CUI W D, et al.Process optimization and inhibition of alpha-amylase and alpha-glucosidase activities in camel milk fermentation by lactic acid bacteria[J].China Dairy, 2022(8):97-107.
[18] BAO T, WANG Y, LI Y T, et al.Antioxidant and antidiabetic properties of Tartary buckwheat rice flavonoids after in vitro digestion[J].Journal of Zhejiang University:Science B, 2016, 17(12):941-951.
[19] SUDUN, WULIJIDELIGEN, ARAKAWA K, et al.Interaction between lactic acid bacteria and yeasts in airag, an alcoholic fermented milk[J].Nihon Chikusan Gakkaiho, 2013, 84(1):66-74.
[20] ZHANG X, YANG J J, ZHANG C, et al.Effects of Lactobacillus fermentum HY01 on the quality characteristics and storage stability of yak yogurt[J].Journal of Dairy Science, 2022, 105(3):2025-2037.
[21] CHENG H F.Volatile flavor compounds in yogurt:A review[J].Critical Reviews in Food Science and Nutrition, 2010, 50(10):938-950.
[22] XU L N, LI Y, DAI Y, et al.Natural products for the treatment of type 2 diabetes mellitus:Pharmacology and mechanisms[J].Pharmacological Research, 2018, 130:451-465.
[23] SANTOS C M M, PROENÇA C, FREITAS M, et al.2-Styrylchromones as inhibitors of α-amylase and α-glucosidase enzymes for the management of type 2 diabetes mellitus[J].Medicinal Chemistry Research, 2024, 33(4):600-610.
[24] LIU C L, XU F R, ZHANG Q, et al.Ultrasound-assisted enzyme extraction of total flavonoids from lotus leaf (Nelumbo nucifera Gaertn.) and its antioxidant activity[J].LWT, 2025, 215:117224.
[25] CHOE J H, JANG A, LEE E S, et al.Oxidative and color stability of cooked ground pork containing Lotus leaf (Nelumbo nucifera) and barley leaf (Hordeum vulgare) powder during refrigerated storage[J].Meat Science, 2011, 87(1):12-18.