作为膳食纤维、维生素及多种生物活性化合物(如酚类物质)的独特来源,水果对维持人体健康、预防心血管疾病、癌症及延缓衰老具有关键作用[1]。其中,膳食纤维等聚糖组分不仅可以调节肠道菌群,通过发酵产生短链脂肪酸、芳香族乳酸,以及合成B族维生素等人体不可或缺的营养组分[2],进而促进人体各种生理功能,包括调控肠道微生态平衡、预防各种慢性疾病等[3]。水果中的多酚、类黄酮是药食两用成分,对人体健康提供了不可或缺的营养和特殊功能组分,但通常不能被人体直接消化利用,降低了其功效作用[4]。肠道微生物发酵可以提高它们的生物可利用性,通过生物转化产生特殊生理功能的效应分子[5],譬如释放黄酮类、糖苷类、多酚类等活性成分。
近几十年来,益生菌在食品、医药、生物技术中被广泛利用,尤其在乳制品中。然而,目前益生菌发酵非乳制品越来越受欢迎[6],其中以富含多酚、类黄酮的植物基原料为首选,利用特殊功能的乳酸菌菌株进行体外发酵,提升水果维生素、矿物质、多酚等各组分的生物利用度[7],增强抗氧化活性[8]和降血糖活性[9]。此外,益生菌发酵会产生乙醛、乙醇和二乙酰等挥发性风味物质[10],赋予发酵果汁独特的感官风味。因此,发酵特色果蔬,生产富含营养和特殊功能的饮料或者后生元产品,成为目前极具市场潜力的发展方向[11]。
新疆是我国重要的水果产区,发展果品的深加工前景广阔。南疆引种的新兴杂交水果——杏李,目前规模化种植面积已超万亩,其色泽亮丽,富含多酚、维生素、氨基酸等生物活性物质,含糖高于传统李、杏,经济价值显著[12]。然而,杏李作为季节性水果,鲜果供应期短,残次果经济价值低,影响其经济效益和附加值。本研究采用当地人源的肠道益生菌——副干酪乳酪杆菌(Lacticaseibacillus paracasei) FMBL L23249 FJX(具有降血糖功效,已获批专利)为发酵剂,以杏李(风味玫瑰)为原料,通过单因素及响应面(response surface methodology,RSM)试验优化发酵工艺,分析比较了杏李果汁发酵前后的理化参数(活菌数、可溶性固形物、总糖含量、pH、总酸含量)、功能成分含量(总酚、总黄酮、花青素)、抗氧化与降血糖活性(ABTS阳离子自由基、DPPH自由基、羟自由基的清除能力与α-淀粉酶、α-葡萄糖苷酶的抑制率)、模拟胃肠道消化特性(酚类物质的释放量)、色度、风味及感官特征,为进一步开发高附加值的益生菌发酵杏李果汁产品奠定基础。
1 材料与方法
1.1 材料与仪器
杏李(Prunus domestica×armeniaca),市售;L. paracasei FMBL L23249 FJX(具有发酵潜力与降血糖功效,已获批专利CN117535185A、CN119524022A),食品生物技术中心筛选保藏。
蛋白胨、牛肉膏、酵母提取物、葡萄糖、吐温80、K2HPO4、乙酸钠、柠檬酸二铵、MgSO4·7H2O、MnSO4·7H2O、琼脂,天津光复精细化工研究所;DPPH、ABTS,北京伊诺凯科技有限公司;酪蛋白胨,英国Oxoid公司;NaNO2、Al(NO3)3、芦丁、福林酚、没食子酸,国药集团化学试剂有限公司;α-葡萄糖苷酶、α-淀粉酶、对硝基苯基-β-D-吡喃葡萄糖苷(p-nitrophenyl-β-D-glucopyranoside,PNPG),上海源叶生物科技有限公司。
BS224S万分之一天平,美国Mettler Toledo公司;SW-CJ-IBU超净工作台,上海沪净医疗器械有限公司;E500A厌氧培养箱,英国DWS公司;pH计、手持式数字折光仪、WSC-2S测色色差计,上海博讯医疗生物仪器公司;EON酶标仪,BIOTEK有限公司;5977A气相色谱-质谱联用仪,安捷伦科技有限公司。
1.2 实验方法
1.2.1 发酵杏李果汁的制备
杏李→清洗、去核→榨汁→抽滤→调配→灭菌→接种→发酵→杏李果汁
操作关键点:挑选无腐烂的杏李,洗净、去核,加入3倍质量的蒸馏水,搅打成匀浆,由300目的纱布过滤,加入质量浓度为50 g/L的葡萄糖和90 g/L的酪蛋白溶液进行调配。将FMBL L23249 FJX活化至二代,洗涤3次,用生理盐水重悬为1.0×107 CFU/mL的菌悬液,接种至灭菌后的杏李果汁中,进行发酵。
1.2.2 单因素试验
以发酵杏李果汁的总酚含量为评价指标,设定灭菌温度95 ℃、接种量3%、发酵温度37 ℃、发酵时间24 h为基础发酵条件。改变单一条件,考察灭菌温度(80、85、90、95、100、105、110 ℃)、接种量(0%、1%、2%、3%、4%、5%、6%,体积分数)、发酵温度(31、33、35、37、39、41、43 ℃)和发酵时间(6、12、18、24、30、36、42 h)对发酵杏李果汁中总酚含量的影响。
1.2.3 杏李果汁发酵过程中生物功能成分检测
1.2.3.1 总酚含量的测定
采用福林酚法测定总酚含量,没食子酸标准曲线方程为Y=0.010 8X+0.074 3,R2=0.999 2。
1.2.3.2 总黄酮含量的测定
采用亚硝酸钠-硝酸铝比色法测定总黄酮含量,芦丁标准曲线方程为Y=2.538 6X-0.000 1,R2=0.998 3。
1.2.3.3 总花青素含量的测定
采用pH示差法测定,取1 mL样品稀释10倍,用缓冲溶液(pH 1.0、4.5)定容至10 mL,避光反应50 min(pH 1.0)和80 min(pH 4.5)后,在510、700 nm波长下测定吸光值,根据公式(1)计算。
花青素含量![]()
(1)
式中:A,吸光值,(A510 nm·pH 1.0-A700 nm·pH 1.0)-(A510 nm·pH 4.5-A700 nm·pH 4.5);ε,26 900;DF,稀释因子;M,449.2;L,比色皿长度,cm。
1.2.4 中心组合(central composite design,CCD)试验设计
根据单因素试验结果,以最优灭菌温度、接种量、发酵温度和发酵时间为中心点,果汁的总酚含量为响应值,进行4因素5水平的分析试验,每组试验重复3次,CCD试验关键变量的水平与编码见表1。
表1 试验设计因素与水平
Table 1 Factors and levels for CCD
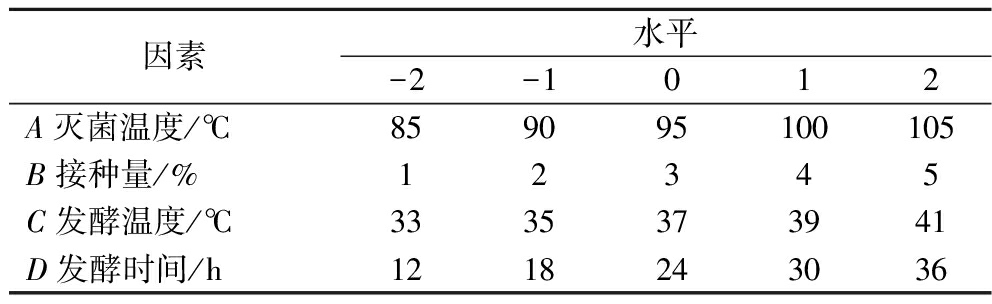
因素水平-2-1012A灭菌温度/℃859095100105B接种量/%12345C发酵温度/℃3335373941D发酵时间/h1218243036
1.2.5 RSM分析
利用RSM对发酵杏李果汁过程中自变量对因变量的影响进行统计建模。应用Design-Expert 13.0软件对CCD试验数据进行分析,将其拟合于二阶多项式模型[公式(2)]中。为了以图形方式理解独立参数对响应的行为,获得了3D等高线图。进一步分析该模型,最终得到最高总酚含量的理论最优发酵条件。
(2)
i,j=1,2,…,k
i≠j
式中:Y,预测总酚值;β0,截距;xi、xj分别为不同因素;βi、βii、βij,对应自变量系数。
1.2.6 基本理化性质的测定方法
活菌数的测定:参照GB 4789.35—2023《食品安全国家标准 食品微生物学检验 乳酸菌检验》,采用平板稀释法测定。可溶性固形物:使用手持式数字折光仪对样品进行测定。总糖含量的测定:采用苯酚-硫酸法测定。pH值的测定:使用pH计对样品进行测定。总酸含量的测定:按GB/T 12456—2021《食品安全国家标准 食品中总酸的测定(含第1号修改单)》测定,结果以苹果酸计。
1.2.7 色泽的测定
利用校准后的色差仪测定,记录亮度值(L*)、红度值(a*)和黄度值(b*)。每组样品做3个平行实验,根据公式(3)计算总色差(ΔE)。
(3)
式中:L*、a*和b*为发酵组果汁的色差测定值,![]() 和
和![]() 为未发酵组果汁的色差测定值。
为未发酵组果汁的色差测定值。
1.2.8 抗氧化活性的测定
1.2.8.1 ABTS阳离子自由基清除能力的测定
根据CELE等[13]的方法,将ABTS溶液(7.4 mmol/L)和过硫酸钾溶液(2.6 mmol/L)按1∶1(体积比)混合,避光反应12 h,将其稀释至734 nm处吸光度值为(0.70±0.02),用作ABTS工作液。取800 μL工作液加入40 μL样品,避光反应20 min,于734 nm处测量样品吸光度值As。空白组以蒸馏水代替样品,对照组以蒸馏水代替ABTS,分别测得吸光度为Ab和Ac,ABTS阳离子自由基清除率计算如公式(4)所示。
ABTS阳离子自由基清除率![]()
(4)
1.2.8.2 DPPH自由基清除能力的测定
参照CELE等[13]的方法,取0.1 mL的样品与3.9 mL DPPH溶液(0.025 g/L)混合均匀,避光反应30 min,于515 nm处测定其吸光度值为Bs。用无水乙醇替代果汁,测得吸光度为Bc,作为空白对照组,DPPH自由基清除率计算如公式(5)所示。
DPPH自由基清除率![]()
(5)
1.2.8.3 羟自由基清除能力
根据易翠平等[14]的方法稍作修改,取1 mL样品,加入1 mL FeSO4溶液(9 mmol/L)、水杨酸溶液(9 mmol/L)、H2O2溶液(8.8 mmol/L)混匀(A1),37 ℃恒温水浴30 min,在510 nm处测定吸光度。蒸馏水代替样品为A0,蒸馏水代替H2O2溶液为A2,羟自由基清除率计算如公式(6)所示。
羟自由基清除率![]()
(6)
1.2.9 发酵杏李果汁体外降血糖活性的测定
1.2.9.1 发酵杏李果汁α-淀粉酶的抑制活性
将250 μL样品与α-淀粉酶(1 mg/mL)等体积混合,37 ℃反应10 min;加入500 μL可溶性淀粉(1.5%),37 ℃反应15 min。加入1 mL DNS溶液,于沸水中反应5 min,用PBS稀释20倍后静置30 min,于540 nm处测定吸光度值。以PBS为α-淀粉酶和样品的空白对照,根据公式(7)计算α-淀粉酶活性抑制率。
α-淀粉酶酶抑制率![]()
(7)
式中:A,样品组吸光度;B,样品空白组吸光度(不含α-淀粉酶溶液);C,对照组吸光度(不含样品溶液);D,空白组吸光度(不含样品和α-淀粉酶溶液)。
1.2.9.2 发酵杏李果汁对α-葡萄糖苷酶的抑制活性
将100 μL样品与200 μL的0.25 U/mL α-葡萄糖苷酶混合,37 ℃反应10 min,加入100 μL PNPG溶液(5 mmol/L)于37 ℃反应30 min,加入100 μL的Na2CO3溶液(0.2 mol/L)终止反应。于405 nm处测定吸光度值,以PBS为α-葡萄糖苷酶和样品的空白对照,根据公式(8)计算α-葡萄糖苷酶活性抑制率。
α-葡萄糖苷酶抑制率![]()
(8)
式中:A,样品组吸光度;B,样品空白组吸光度(不含α-葡萄糖苷酶溶液);C,对照组吸光度(不含样品溶液);D,空白组吸光度(不含样品和α-葡萄糖苷酶溶液)。
1.2.10 体外模拟胃肠道消化
1.2.10.1 体外模拟胃消化
取10 mL 0.01 mol/L HCl溶液,加入0.2 g胃蛋白酶和1 g NaCl,用微孔滤膜过滤,为模拟胃液备用。试验分为模拟胃消化组、空白对照组(除样品外,均由生理盐水代替)和胃酸对照组(以盐酸代替模拟胃液)。取1 mL样品,稀释20倍,用盐酸(1 mol/L)调节pH值至2.0,加入4 mL模拟胃液,避光置于恒温水浴振荡器中,于37 ℃模拟胃消化1.5 h,分别在0、0.5、1、1.5 h时吸取样品,测定总酚含量。
1.2.10.2 体外模拟肠消化
取1.9 g牛胆盐,0.3 g胰蛋白酶,将其加入120 mL 0.1 mol/L 的NaHCO3溶液,用微孔滤膜过滤,为模拟肠液备用。吸取1.5 h的模拟胃消化后的样品,用1 mol/L的NaHCO3溶液调节pH值至7.2。试验分为模拟肠消化组(加入4 mL模拟肠液)和空白对照组(加入4 mL 0.1 mol/L的NaHCO3溶液),避光置于恒温水浴振荡器中,于37 ℃模拟肠消化1.5 h,分别在0、0.5、1、1.5 h时吸取样品,测定总酚含量。
1.2.11 发酵杏李果汁气味成分的检测
1.2.11.1 感官评价
石河子大学食品生物技术中心的26名成员(11名男性和15名女性,年龄20~42岁)组成训练有素的评估小组,对样品进行感官分析。小组成员每次评价会收到装在透明品尝杯中且有3位随机数字编号的样品,并在感官室中对果汁的颜色、香气、果味、花香、发酵味、酸度、甜度、苦味和总体可接受性进行评价。按照9分制享乐量表进行评价(范围从“1-极度不喜欢”到“9-极度喜欢”,中间为“5-既不喜欢也没有不喜欢”)。对每个样品进行一式三份的感官评价。
1.2.11.2 顶空固相微萃取-气相色谱质谱联用(headspace solid-phase microextraction coupled with gas chromatography-mass spectrometry,HS-SPME-GC-MS)
采用HS-SPME技术,取5 mL样品于25 mL顶空瓶中,加入1 g NaCl,加入5 μL 0.1 mg/mL的2-甲基-3-庚酮作为内标,加入1 cm转子。35 ℃条件下,以80 r/min的转速平衡20 min,插入老化后的萃取头(50 μm)30 min,将其在进样口(250 ℃)热解吸7 min进行物质分离鉴定。
色谱条件:采用无分流模式,Agilent HP-innowax色谱柱(30 m×250 μm,0.25 μm);升温程序:40 ℃保持5 min,5 ℃/min升温至120 ℃保持10 min,再以8 ℃/min升温至220 ℃保持5 min;载气为99.999%He,流速1.6 mL/min。
质谱条件:采用电子电离(electron impact,EI)模式,电子能量70 eV,离子源温度230 ℃,离子扫描范围30~350 m/z。
1.3 数据处理
采用R语言进行方差分析与显著性分析,利用Design-Expert 13软件进行CCD试验设计与RSM分析,用Graphpad Prism 10.1.2软件绘图。数据为3次重复试验的平均值,以“平均数±标准差”表示,P<0.05表示差异显著。
2 结果与分析
2.1 单因素试验
由图1-a可知,随着灭菌温度不断升高,发酵杏李果汁中的总酚含量显著上升(P<0.05),灭菌温度达到95 ℃时,总酚含量达到峰值(567.267 mg/L)。研究报道,高温破坏杏李果汁原有的细胞结构,细胞壁中的酚类化合物得以释放,导致果汁中总酚含量提升[15]。但灭菌温度超过95 ℃后,总酚含量显著下降(P<0.05),温度过高会导致部分热敏性的酚类化合物损失。由图1-b可知,接种量对发酵杏李果汁的总酚含量影响显著(P<0.05),随接种量的增加总酚含量先升高后降低。当接种量为3%时总酚含量达到最大值(566.932 mg/L),显著高于接种量为0的果汁(334.475 mg/L)。说明益生发酵有助于结合态酚类化合物转化为游离态,提高了总酚含量。此外,发酵温度对杏李果汁的总酚含量也产生显著影响(P<0.05),发酵温度为37 ℃时,总酚含量达到峰值(568.860 mg/L)(图1-c)。发酵温度过高会导致益生菌生长抑制、发酵体系中的酶变性失活,导致酚类物质的释放受到抑制。图1-d显示,在42 h的发酵过程中,24 h时总酚含量达到最高569.599 mg/L,随后急剧下降(P<0.05)。在发酵前期(0~24 h),益生菌的生长促进生物转化,释放酚类化合物;而发酵后期(24~48 h),酚类化合物可能发生氧化、聚合或降解等反应,导致总酚含量降低。因此,杏李果汁的最适灭菌温度为95 ℃,接种量3%,发酵温度37 ℃,发酵时间24 h。
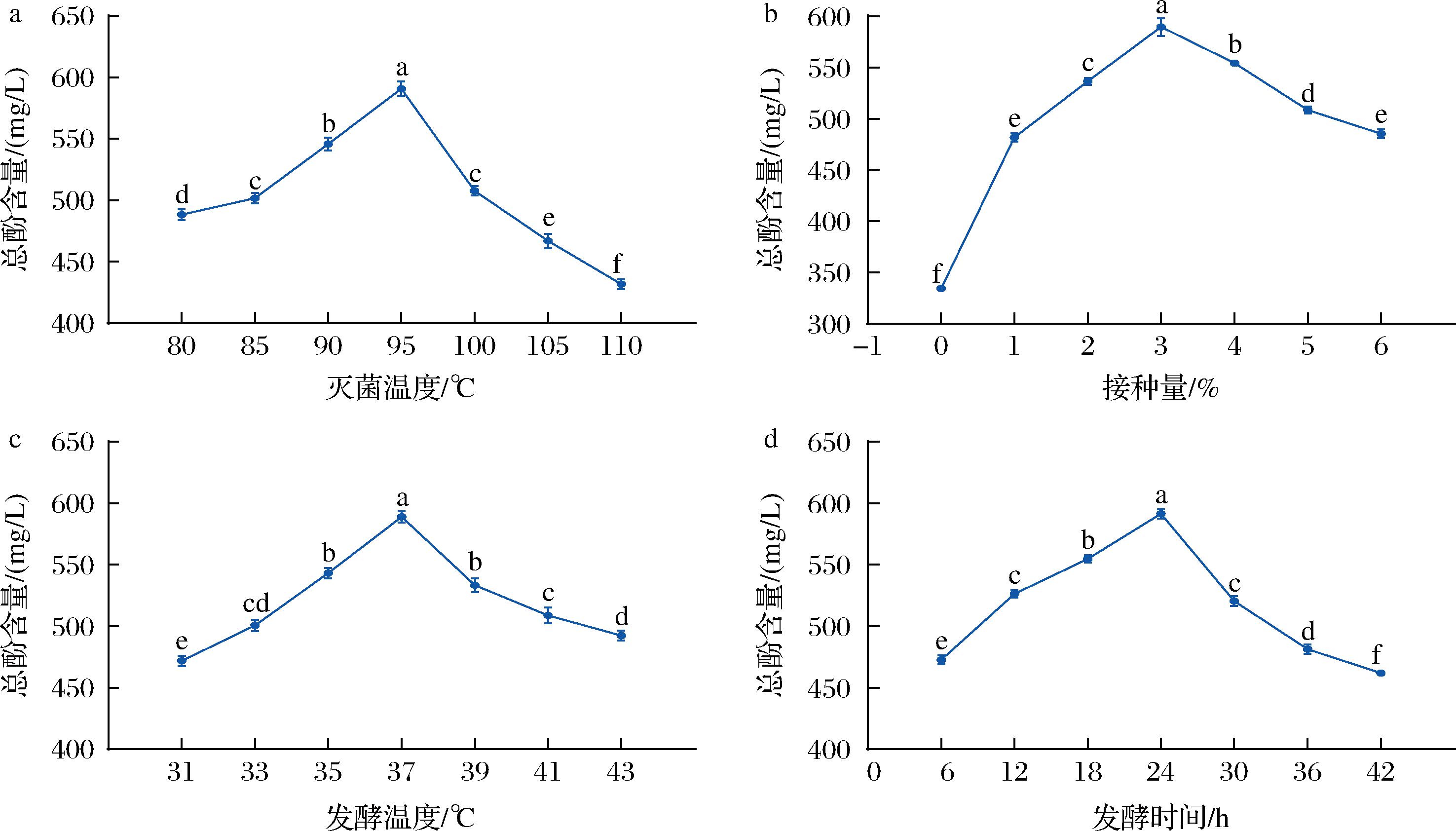
a-灭菌温度;b-接种量;c-发酵温度;d-发酵时间
图1 单因素对发酵杏李果汁中总酚含量的影响
Fig.1 Effect of single factor on total phenol content in fermented pluot juice
注:不同小写字母表示差异显著(P<0.05),下同。
2.2 CCD与RSM试验分析
CCD试验结果如电子版增强出版附表1所示(https://doi.org/10.13995/j.cnki.11-1802/ts.043529,下同)。对试验数据进行多元回归拟合,建立总酚含量(Y)对灭菌温度(A)、接种量(B)、发酵温度(C)、发酵时间(D)的回归模型,回归方程为:Y=581.10-10.69A-10.07B+7.61C-10.76D+7.15AB-10.69AC+6.32AD+6.64BC-3.15BD+8.26CD-25.36A2-22.27B2-19.40C2-21.24D2,模型的相关系数R2=0.957 0。模型的方差分析如附表2所示,二次回归模型极显著(F值=23.83,P<0.000 1);回归方程与实验数据的拟合效果较好(失拟项不显著);模型具有较高的可信度和精确度,能精确预测实验值[16]。不同工艺下二次回归模型中的单项因素对响应值(Y)的影响顺序为灭菌温度(A)=发酵时间(D)>接种量(B)>发酵温度(C)。由P值可知,4个因素及其二次项A2、B2、C2、D2对总酚含量的影响极显著(P<0.000 1);交互项AB、CD的影响显著,AC的影响极显著。
各因素交互作用的RSM图如附图1所示,灭菌温度与接种量及发酵温度与发酵时间的交互作用对总酚含量有显著影响,灭菌温度与发酵温度的交互作用对总酚含量有极显著影响,与方差分析的结果一致。经Design Expert 13软件分析,最优发酵工艺为灭菌温度93.435 ℃、接种量2.769%、发酵温度37.381 ℃、发酵时间22.524 h,预测总酚含量为585.990 mg/L。因工艺的实操性,将其调整为灭菌温度93 ℃、接种量2.8%、发酵温度37 ℃、发酵时间23 h。在最优发酵条件下,重复进行3次验证实验,得到发酵杏李果汁的总酚含量为572.634 mg/L,与预测值的相对误差仅为2.332%。
2.3 发酵过程中理化指标的变化
如图2-a所示,菌株在8~23 h内呈指数增长,23 h时达到最大值9.46 lg CFU/mL,表明杏李果汁可以作为其生长和繁殖的良好载体。可溶性固形物(图2-b)和总糖含量(图2-c)分别由8.77 °Bx和222.40 mg/mL下降至7.83 °Bx和175.13 mg/mL,显示菌株在发酵过程中对糖的活跃利用。发酵初期,碳水化合物被水解为葡萄糖和果糖提供了代谢底物,支持菌体快速增殖;而随着菌株生长进入稳定期,糖耗速率趋缓,菌株代谢达到稳态期[17]。此外,pH值明显下降(4.83降至3.93),总酸含量增加(0.33 g/100 mL增至0.44 g/100 mL)(图2-d、图2-e)。酸性环境不仅提升了果汁的感官风味,也可能通过抑制杂菌生长延长产品保质期。因此,L. paracasei FMBL L23249 FJX能够在杏李果汁中实现较高水平的增殖和代谢活性,发酵过程中糖的降解与酸的积累相互协调,体现出其在植物基基质中应用的可行性和功能潜力[18]。
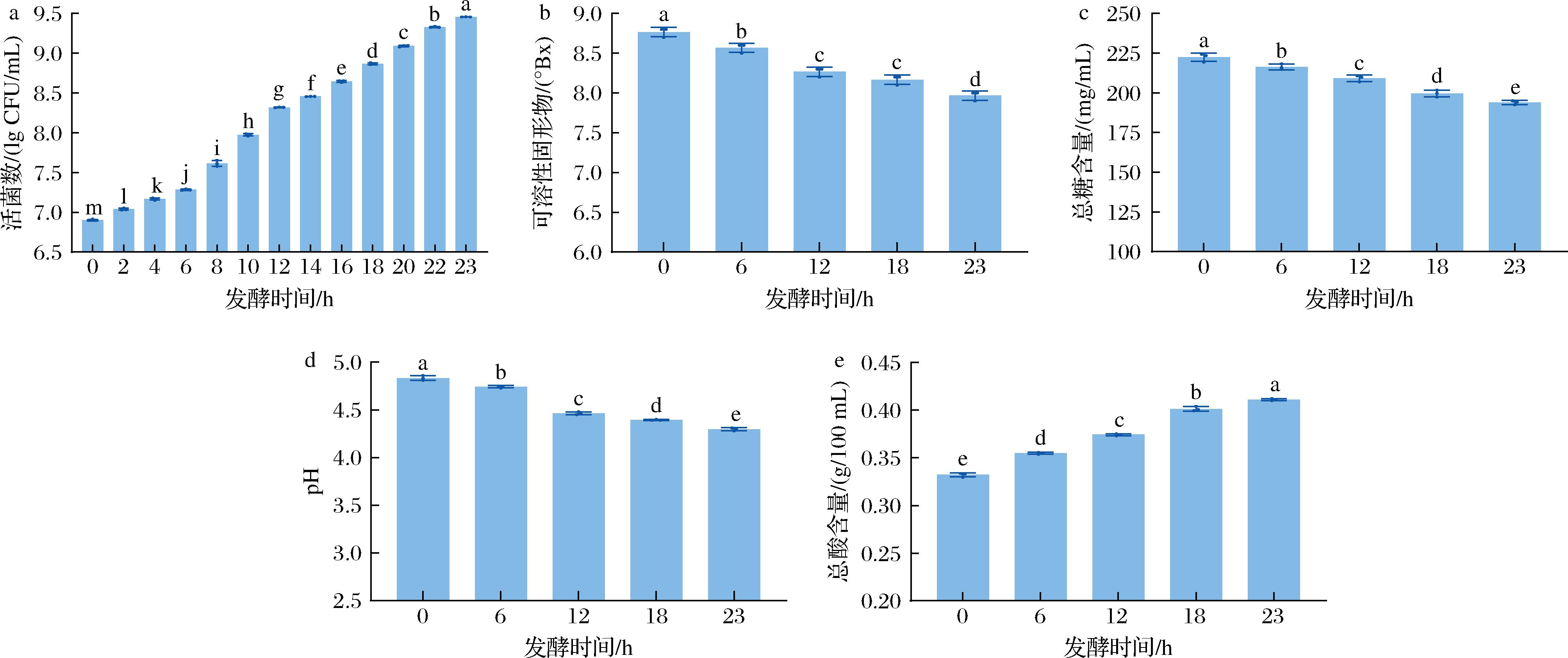
a-活菌数;b-可溶性固形物;c-总糖含量;d-pH;e-总酸含量
图2 杏李果汁发酵过程中活菌数、可溶性固形物、总糖含量、pH和总酸含量的变化
Fig.2 Changes in the number of viable bacteria, soluble solids, total sugar content, pH and total acid content of pluot juice during fermentation
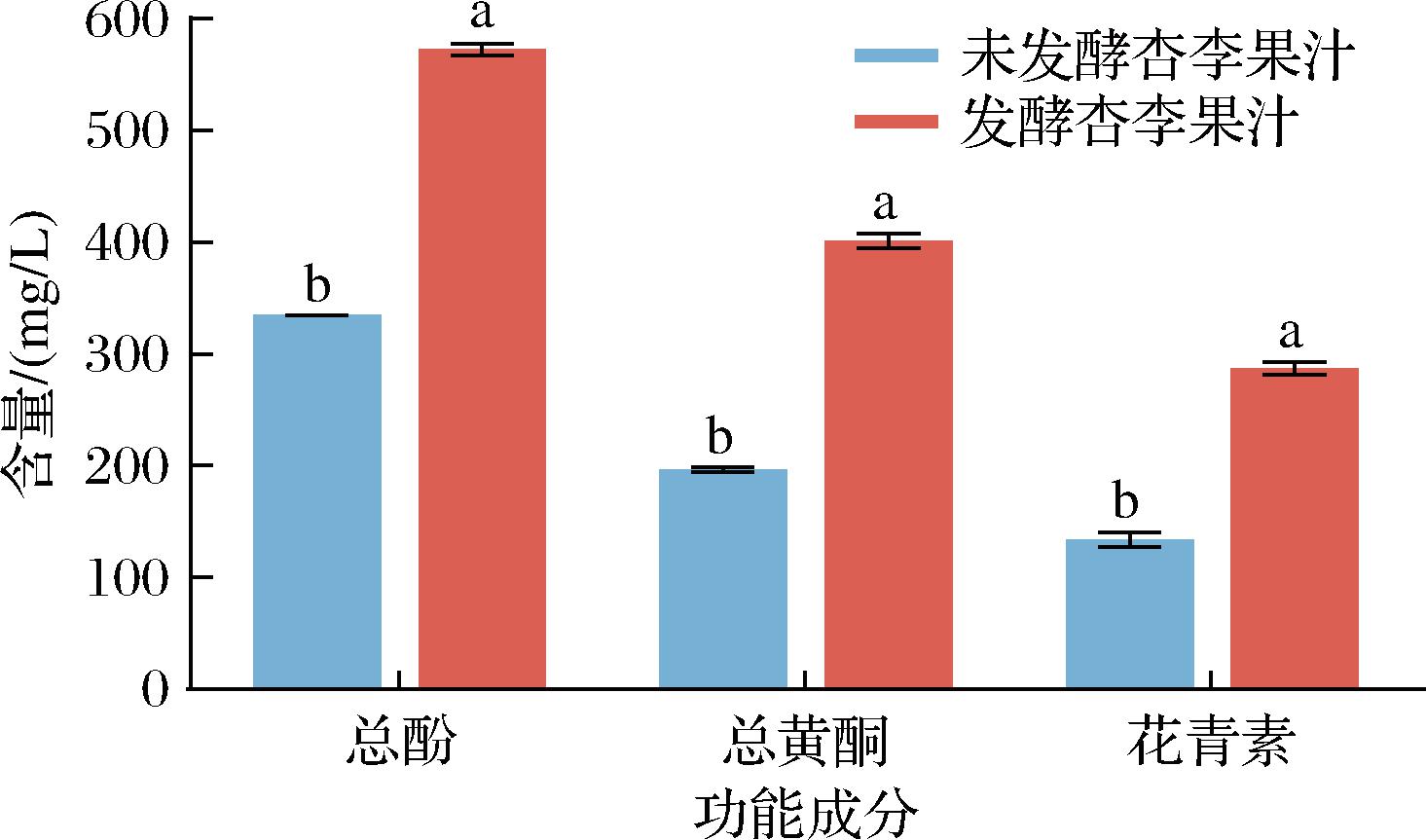
图3 发酵前后杏李果汁功能成分的变化
Fig.3 Changes in functional components of pluot juice before and after fermentation
注:a,b表示发酵与未发酵组间存在显著性差异(P<0.05)。
2.4 杏李果汁发酵前后功能成分的变化
杏李富含多酚、花青素和类黄酮,经L. paracasei FMBL L23249 FJX发酵后,杏李果汁的总酚、总黄酮与花青素含量分别由334.48、196.43、133.76 mg/L显著提升(P<0.05)至572.63、401.21、287.22 mg/L,表明益生菌发酵能够有效促进总酚、总黄酮与花青素的释放和积累。在益生菌的发酵过程中,所产生的酸性代谢产物可有效降低体系pH值,从而抑制部分活性物质的降解;能够产生酚酸脱羧酶,驱动结合酚转化为小分子酚类物质;还能产生微生物酶促进花青素和类黄酮从膳食纤维中的复杂形式释放成易溶形式[19]。值得注意的是,与部分已有研究中报道的结果不同,本文发现杏李果汁经L. paracasei FMBL L23249 FJX发酵后,总黄酮与花青素含量显著上升(P<0.05)。LI等[20]在蓝莓果汁发酵研究中指出,乳酸菌发酵过程中花青素含量呈现下降趋势,主要归因于乳酸菌代谢产生的酶类对花青素结构的降解作用;另有研究[21]在对红枣果汁发酵的分析中也发现,部分酚类物质在发酵过程中发生转化或降解,导致其含量减少。与上述结果相比,本研究中黄酮和花青素含量的上调可能与菌株特异的代谢通路有关,如糖苷水解酶或相关酶系对植物细胞壁中结合型酚类物质的释放,或花青素前体物质的富集转化所致。此外,杏李果汁本身富含多酚前体物质,其在发酵过程中可能通过糖苷水解或其他酶促反应释放为可测定形式。L. paracasei FMBL L23249 FJX可能通过调节发酵环境pH值及氧化还原状态,提高了花青素的稳定性和生物可及性。益生菌发酵杏李果汁中多种因素发挥协同作用,增强了杏李果汁中活性物质的生物利用度。以上结果表明,乳酸菌发酵对多酚类活性成分的影响具有菌株依赖性和基质特异性,提示在筛选发酵菌株时应充分考虑其对功能成分的保留与转化能力,以实现目标营养品质的提升。
2.5 杏李果汁发酵前后抗氧化与降血糖活性的变化
水果中的酚类物质具有较强的抗氧化能力,在益生菌的发酵过程中,菌株可以代谢酚类化合物中的糖苷键,释放具有更高抗氧化活性的游离苷元等代谢物,从而增强果汁的清除自由基能力[21]。如图4-a所示,副干酪乳酪杆菌发酵前,杏李果汁对ABTS阳离子、DPPH及羟自由基的清除率分别为76.84%、31.13%和34.26%;发酵后,清除率分别提升至95.84%、59.76%和63.17%,提升幅度分别为24.73%、91.97%和84.38%,抗氧化活性显著增强(P<0.05)。如图4-b所示,发酵显著提高了果汁对α-淀粉酶和α-葡萄糖苷酶的抑制率(P<0.05),分别由发酵前的63.71%和49.20%提升至81.62%和66.27%,增幅分别为1.35和1.28倍。研究表明,益生菌发酵会促进功能性代谢物的释放,增强对2种酶的活性抑制,延缓碳水化合物的水解和吸收,从而对血糖水平调节具有积极作用[22]。因此,L. paracasei FMBL L23249 FJX发酵不仅显著提升了杏李果汁的抗氧化能力,也增强了其潜在的降血糖功能,表明其作为功能性发酵饮品有较高的开发价值。
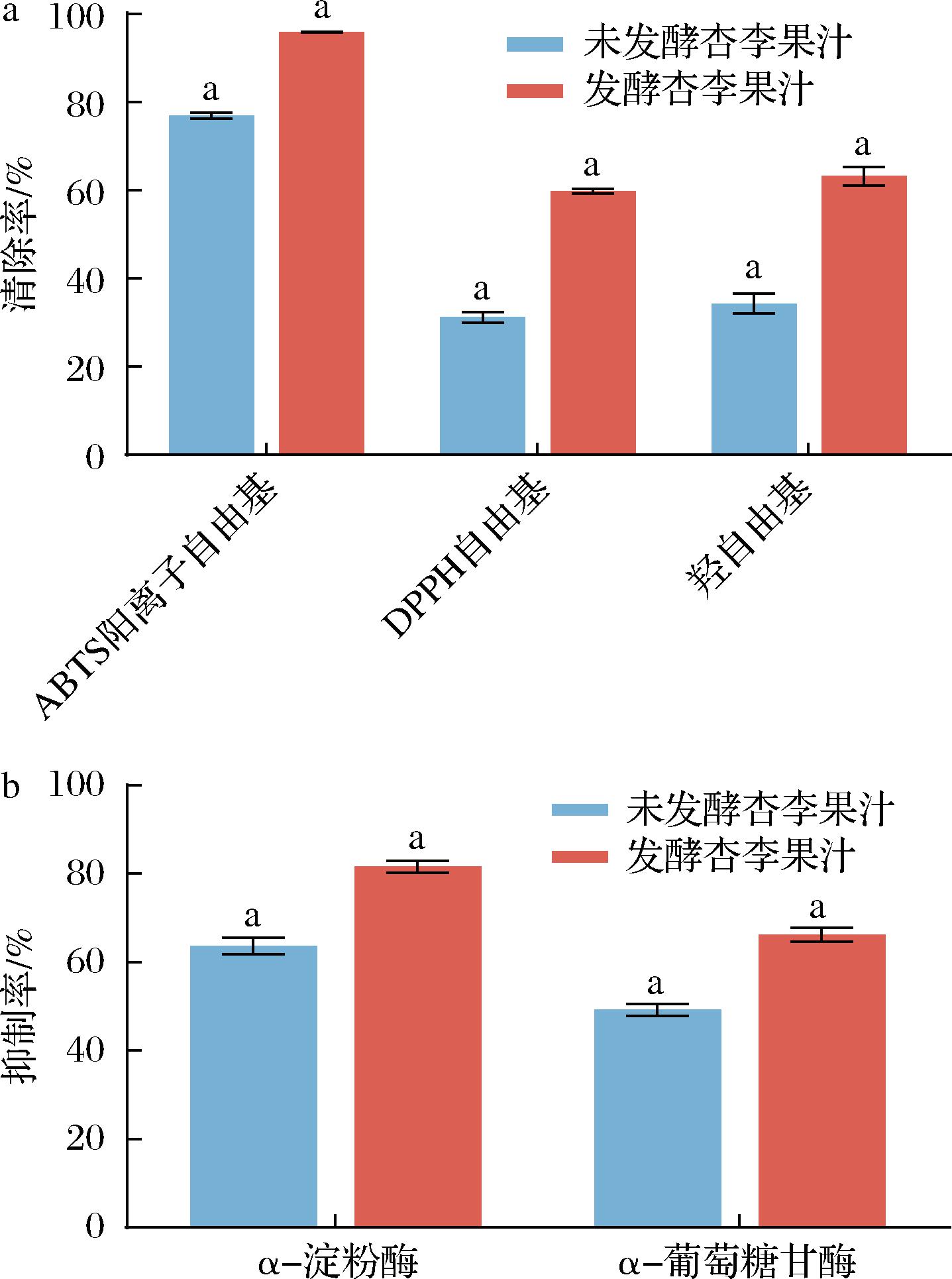
a-抗氧化活性;b-降血糖活性
图4 发酵前后杏李果汁体外抗氧化与降血糖活性的变化
Fig.4 Changes in antioxidant and hypoglycemic activities of pluot juice before and after fermentation in vitro
2.6 体外模拟消化中发酵杏李果汁酚类物质的释放
发酵前后的杏李果汁在体外模拟胃、肠道消化过程中的总酚含量变化如图5所示。在空白组中,发酵与未发酵果汁的总酚含量均显著降低,未发酵杏李果汁的下降率为22.28%,而发酵果汁仅为7.95%,表明发酵产生的酸性环境有助于多酚的稳定。在胃酸组和胃消化组中,总酚含量均呈显著上升趋势,说明胃酸与胃蛋白酶均可促进酚类化合物的释放。消化1.5 h后,未发酵果汁的总酚含量由246.46 mg/mL上升至256.71 mg/mL,而发酵果汁的总酚含量由消化前(531.79 mg/mL)显著提升至571.79 mg/mL。在模拟肠消化实验中,发酵与未发酵杏李果汁的总酚含量均呈先升后降的趋势,且肠消化组显著高于空白组。模拟肠消化1 h时,发酵果汁的总酚含量提升至589.81 mg/L,1.5 h时略有降低(578.26 mg/L),但仍显著高于未发酵果汁(239.83 mg/L)。综合胃、肠道模拟消化,发酵果汁总酚含量较初始(531.79 mg/mL)提高1.09倍,较未发酵果汁消化后(239.83 mg/L)提升了2.41倍,表明益生菌发酵后的杏李果汁,通过模拟胃肠道消化,酚类物质不仅可以保持稳定性,而且释放能力略有提升。
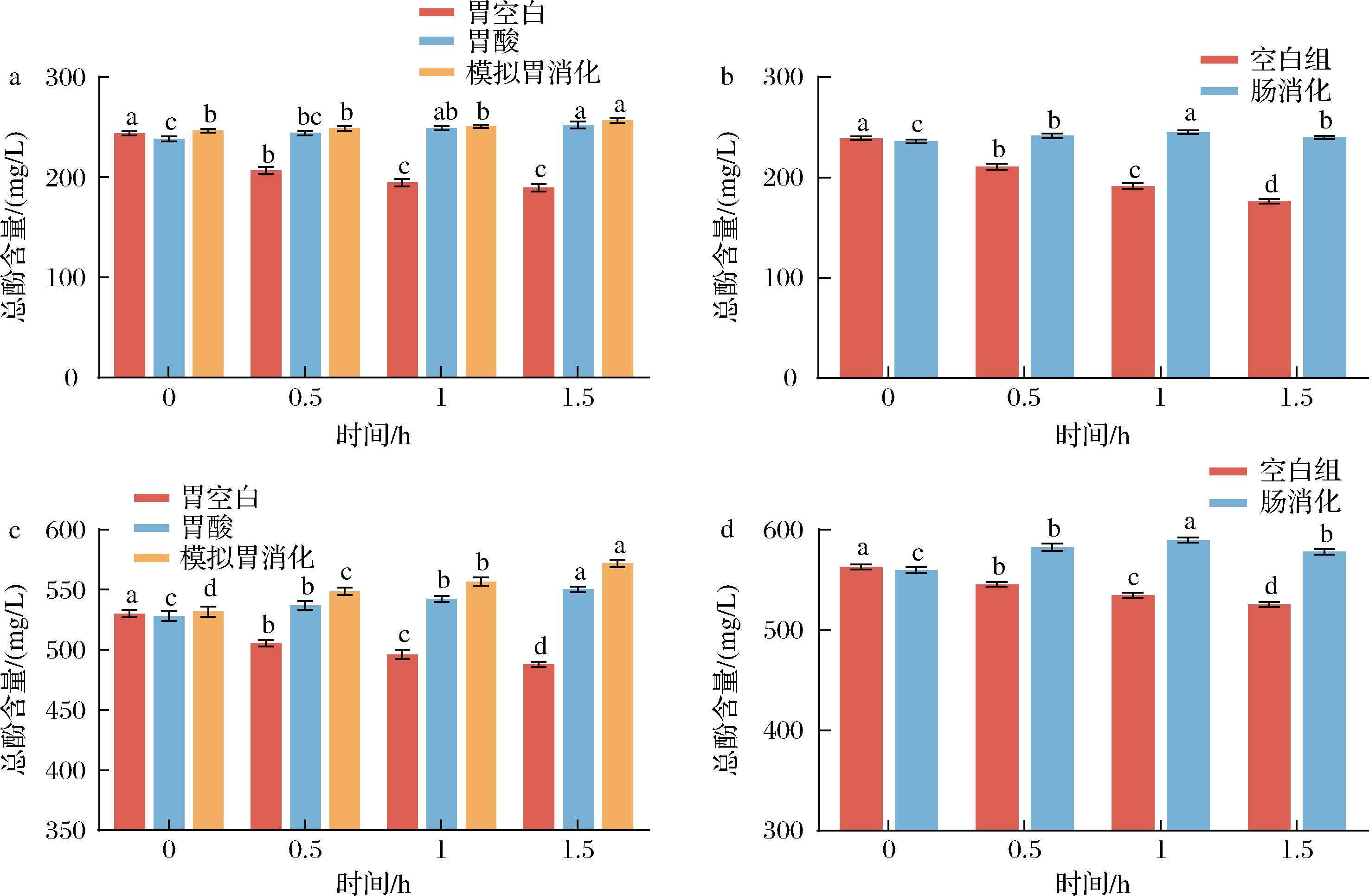
a-模拟胃消化过程中未发酵杏李果汁中总酚的含量变化;b-模拟肠道消化过程中未发酵杏李果汁中总酚的含量变化;c-模拟胃消化过程中发酵杏李果汁中总酚的含量变化;d-模拟肠道消化过程中发酵杏李果汁中总酚的含量变化
图5 模拟胃、肠道消化过程中未发酵与发酵杏李果汁中总酚的含量变化
Fig.5 Changes in total phenolic content in fermented and unfermented pluot juice during simulated gastric and intestinal digestion
注:a,b,c,d表示发酵过程中果汁中的总酚含量存在显著性差异(P<0.05)
2.7 发酵后杏李果汁的色度与感官评价
如图6-a所示,发酵前后杏李果汁的L*、a*、b*值均为正数,但发酵引起了显著的色差(ΔE>5)。具体来看,发酵后果汁的L*值和a*值增加,b*值降低,果汁颜色由橙黄转变为更明亮的红色。这与L. paracasei FMBL L23249 FJX在发酵过程中产生乳酸、乙酸等酸性代谢产物,改变果汁的pH值,进而影响花青素等天然色素的稳定性与显色行为有关。在感官评价方面(图6-b),发酵后的杏李果汁在颜色、香气、酸度、果味、花香味和发酵味等维度评分显著提高(P<0.05),而苦味和甜度评分有所下降。总体可接受度也高于未发酵果汁,说明发酵提升了风味的丰富度与协调性。L. paracasei FMBL L23249 FJX在实验室前期的基因组测序与注释中识别到与苹果酸乳酸发酵(malolactic fermentation,MLF)相关的功能基因(mleS、mleA),表明其具备MLF能力,能够将苹果酸代谢为乳酸,从而减少刺激性有机酸,进一步改善果汁的口感与稳定性[23]。
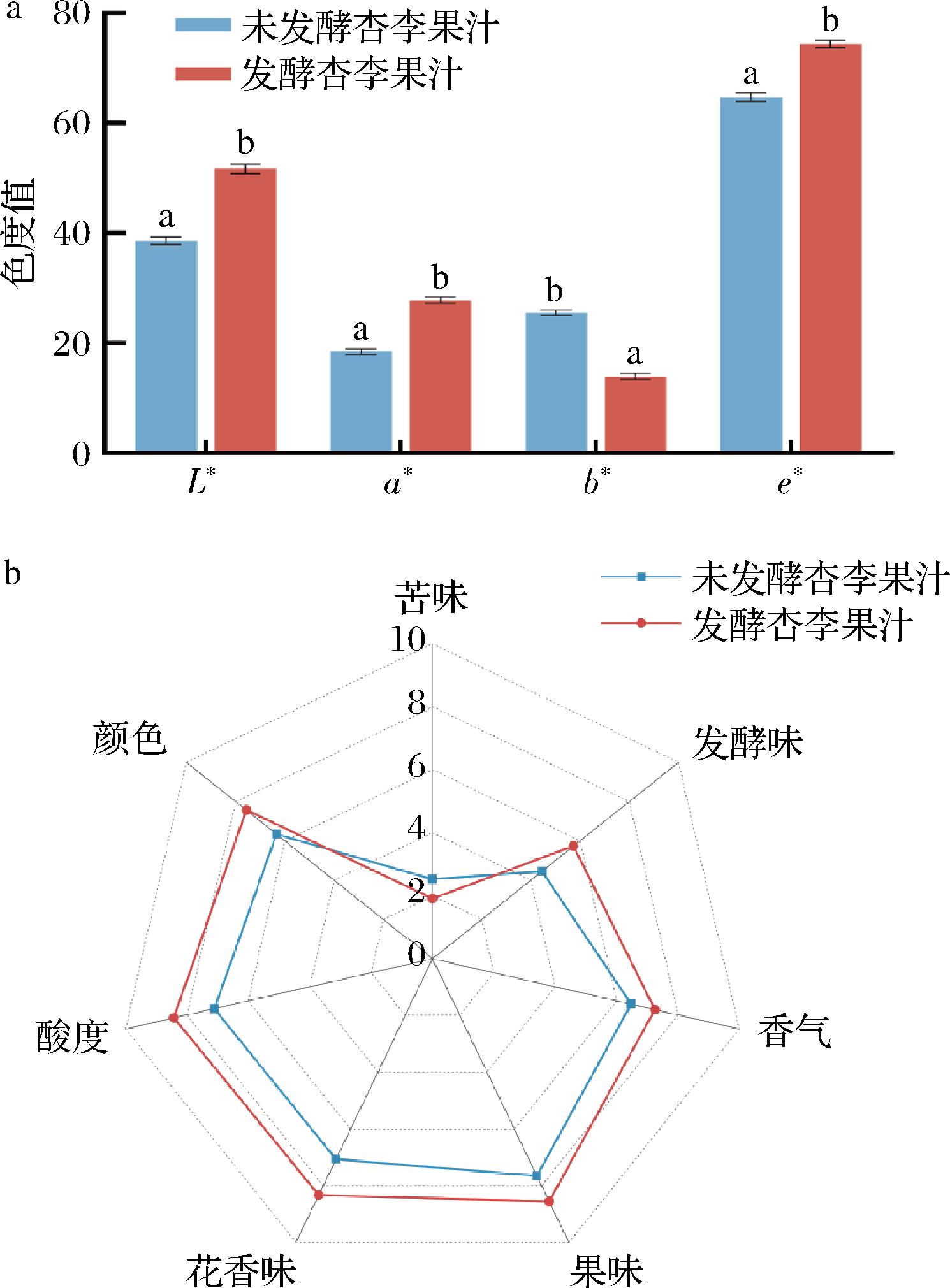
a-色度;b-感官喜好度评价
图6 发酵前后杏李果汁色度与感官喜好度评价的变化
Fig.6 Changes in color and sensory preference evaluation of pluot juice before and after fermentation
2.8 基于GC-MS的挥发性风味物质分析
风味是评估果汁感官品质的关键指标,其特征主要由挥发性化合物构成。基于HS-SPME-GC-MS技术对发酵前后杏李果汁的风味成分进行分析,共检测到60种挥发性化合物(附表3和图7),包括醇类(21种)、醛类(21种)、酮类(4种)、酸类(6种)、酯类(7种)和酚类(1种)。发酵前后果汁中的挥发性物质由26种增加至45种,总含量由5 132.66 μg/kg升至9 337.39 μg/kg,L. paracasei FMBL L23249 FJX发酵显著增强了果汁中风味物质的复杂性和浓郁度。果汁中丰富的挥发性化合物,呈现出相互协调的香气物质,赋予了果汁浓郁而独特的风味[24]。发酵后醛类和酸类物质含量显著上升,占总挥发性成分的62.08%,其中苯甲醛和壬醛赋予发酵果汁茉莉、玫瑰和柑橘类香气;辛酸、甲酸环己酯和甲酸丁酯增强了果味和酸味。醛类物质是水果的主要挥发性物质,给果汁带来了清新果香;酸类物质是果汁发酵中的副产物,有助于提升果汁整体风味的协调性[25]。醇类物质主要通过氨基酸降解和丙酮酸代谢合成,赋予果汁醇甜、花香、果香馥郁的味道和口感[26]。发酵后一些不良风味醇类物质消失或含量下降,如2-丁基-1-辛醇和2-壬醇的消失有助于青草、土壤等不良风味的去除;而2-乙基己醇和正辛醇含量的提升,增强了果香与花香,使整体风味更为清爽宜人。因此,L. paracasei FMBL L23249 FJX发酵不仅增加了芳香类挥发性物质的种类和含量,去除了部分不良风味物质,有效改善了杏李果汁的感官风味特征。
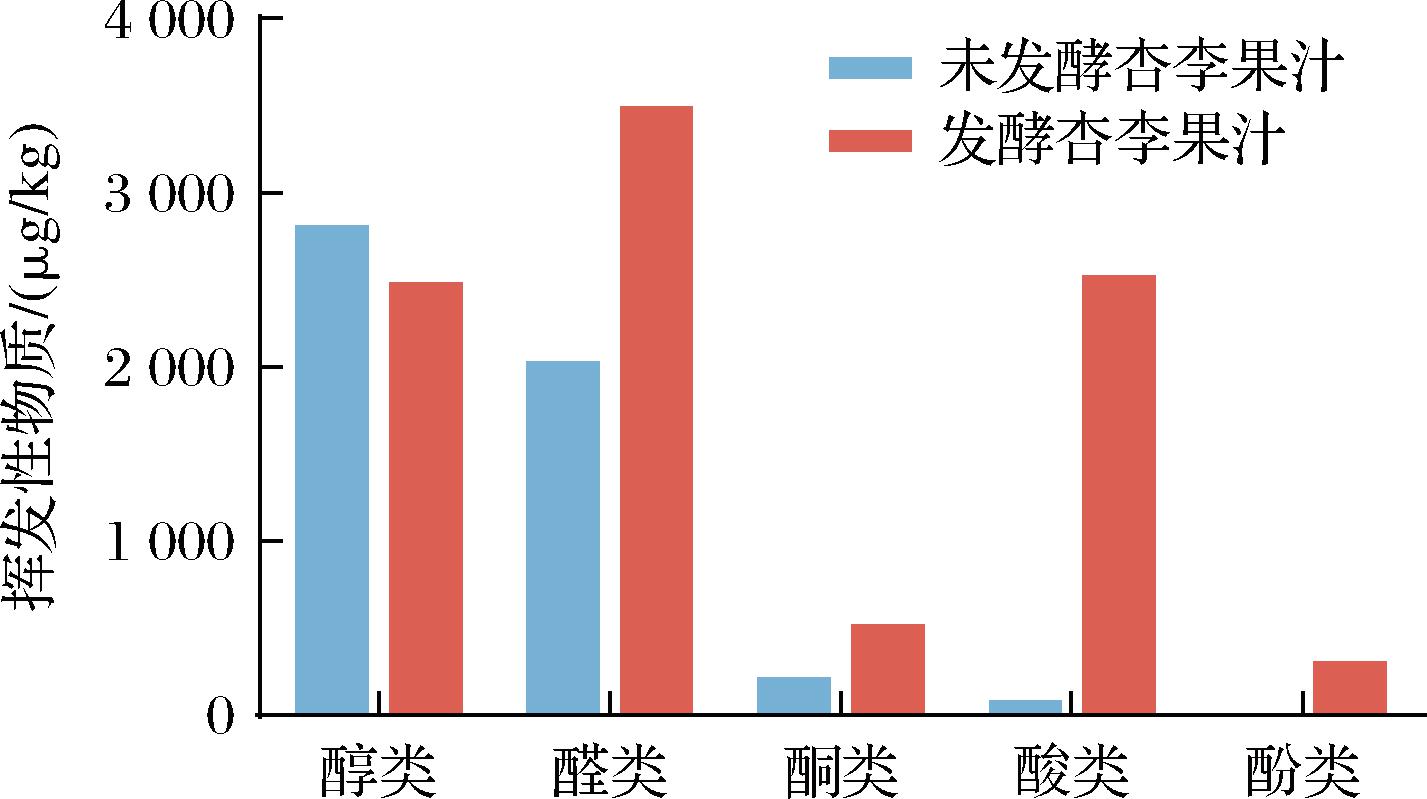
图7 杏李果汁发酵前后挥发性化合物浓度的变化
Fig.7 Changes in volatile compounds concentrations in pluot juice before and after fermentation
3 结论
本研究为促进高附加值杏李产品的开发,采用新疆本地人源的益生菌——副干酪乳酪杆菌(Lacticaseibacillus paracasei) FMBL L23249 FJX发酵杏李果汁,通过单因素与RSM试验对发酵工艺进行了优化,确定最优发酵条件为:灭菌温度93 ℃、接种量2.8%、发酵温度37 ℃、发酵时间23 h,总酚含量提升至572.634 mg/L,提升幅度为71.20%。比较发酵前后果汁理化性质、功能成分、体外抗氧化和降血糖活性,评价其增效作用。结果显示,发酵后,杏李果汁中的活菌数与总酸含量显著提高,pH值、可溶性固形物和总糖含量显著降低;总黄酮与花青素含量分别显著提升至401.21 mg/L和287.22 mg/L;抗氧化与降血糖活性也显著增强,对ABTS阳离子自由基、DPPH自由基和羟自由基的清除率分别为95.84%、59.76%和63.17%,对α-淀粉酶与α-葡萄糖苷酶的抑制率分别为81.62%和66.27%,较发酵前分别提高1.35倍和1.28倍;经胃、肠道模拟消化后,发酵杏李果汁中的总酚含量达到578.26 mg/L,较消化前(531.79 mg/mL)提升了1.09倍,较未发酵果汁消化后(239.83 mg/L)提升了2.41倍,表明在其消化过程中酚类物质具有良好的稳定性与释放能力。GC-MS共鉴定出60种挥发性化合物(未发酵果汁26种、发酵杏李果汁45种),其中醇类21种、醛类21种、酮类4种、酸类6种、酯类7种和酚类1种,总含量由5 132.66 μg/kg提升至9 337.39 μg/kg,尤其是醛、酸类物质的种类和含量显著增加。感官评价结果显示,发酵果汁在色泽、香味和口感方面均优于未发酵果汁。本研究结果为新疆杏李残次果的高值化利用与功能性发酵果汁的研发奠定了基础,对促进新疆南疆杏李产业的发展具有重要意义。
[1] RENDA G,  ÖHRETO
ÖHRETO LU D.Fruit juices:Chemical compositions and health benefits[J].Phytochemistry Reviews, 2025, 24(3):2175-2202.
LU D.Fruit juices:Chemical compositions and health benefits[J].Phytochemistry Reviews, 2025, 24(3):2175-2202.
[2] AL-MADBOLY L A, YAGI A, KABBASH A, et al.Microbiota-derived short chain fatty acids in fermented Kidachi aloe promote antimicrobial, anticancer, and immunomodulatory activities[J].BMC Microbiology, 2023, 23(1):240.
[3] GONÇALVES A C, NUNES A R, FLORES-FÉLIX J D, et al.Cherries and blueberries-based beverages:Functional foods with antidiabetic and immune booster properties[J].Molecules, 2022, 27(10):3294.
[4] HADJ SAADOUN J, CALANI L, CIRLINI M, et al.Effect of fermentation with single and co-culture of lactic acid bacteria on okara:Evaluation of bioactive compounds and volatile profiles[J].Food &Function, 2021, 12(7):3033-3043.
[5] YUAN Y H, MU D D, GUO L, et al.From flavor to function:A review of fermented fruit drinks, their microbial profiles and health benefits[J].Food Research International, 2024, 196:115095.
[6] CATHARINA WEIS C M S, GONÇALVES G C V, SANCHES F L, et al.Water-soluble vegetable extract of cashew nut (Anacardium occidentale L.) fermented with water kefir:Development and characterization[J].Food and Humanity, 2024, 2:100307.
[7] GUO W L, CHEN M X, CUI S M, et al.Effects of Lacticaseibacillus casei fermentation on the bioactive compounds, volatile and non-volatile compounds, and physiological properties of barley beverage[J].Food Bioscience, 2023, 53:102695.
[8] WU C Y, LI T L, QI J, et al.Effects of lactic acid fermentation-based biotransformation on phenolic profiles, antioxidant capacity and flavor volatiles of apple juice[J].LWT, 2020, 122:109064.
[9] WANG X W, HAN M Z, ZHANG M N, et al.In vitro evaluation of the hypoglycemic properties of lactic acid bacteria and its fermentation adaptability in apple juice[J].LWT, 2021, 136:110363.
[10] JI G Y, LIU G P, LI B, et al.Influence on the aroma substances and functional ingredients of apple juice by lactic acid bacteria fermentation[J].Food Bioscience, 2023, 51:102337.
[11] SAUD S, TANG X J, FAHAD S.The consequences of fermentation metabolism on the qualitative qualities and biological activity of fermented fruit and vegetable juices[J].Food Chemistry:X, 2024, 21:101209.
[12] 杨路宽, 李红洲, 王振兴, 等.6个品种李果实品质差异性分析[J].食品安全质量检测学报, 2025, 16(8):267-275.YANG L K, LI H Z, WANG Z X, et al.Analysis of fruit quality differences among 6 kinds of Prunus salicina L.varieties[J].Journal of Food Safety &Quality, 2025, 16(8):267-275.
[13] CELE N P, AKINOLA S A, MANHIVI V E, et al.Influence of lactic acid bacterium strains on changes in quality, functional compounds and volatile compounds of mango juice from different cultivars during fermentation[J].Foods, 2022, 11(5):682.
[14] 易翠平, 张思颉, 肖锦湘, 等.米糠发酵液的抗氧化活性及其对秀丽隐杆线虫寿命的影响[J].食品与发酵工业, 2025, 51(21):70-75.YI C P, ZHANG S J, XIAO J X, et al.Antioxidant activity of rice bran fermentation broth and its effect on the longevity of Caenorhabditis elegans[J].Food and Fermentation Industries, 2025, 51(21):70-75.
[15] BARBA F J, MARIUTTI L R B, BRAGAGNOLO N, et al.Bioaccessibility of bioactive compounds from fruits and vegetables after thermal and nonthermal processing[J].Trends in Food Science &Technology, 2017, 67:195-206.
[16] RUSSO G L, LANGELLOTTI A L, VERARDO V, et al.Bioconversion of cheese whey and food by-products by Phaeodactylum tricornutum into fucoxanthin and n-3 lc-PUFA through a biorefinery approach[J].Marine Drugs, 2023, 21(3):190.
[17] MIAO W, LI N, WU J L.Food-polysaccharide utilization via in vitro fermentation:Microbiota, structure, and function[J].Current Opinion in Food Science, 2022, 48:100911.
[18] LORN D, NGUYEN T K C, HO P H, et al.Screening of lactic acid bacteria for their potential use as aromatic starters in fermented vegetables[J].International Journal of Food Microbiology, 2021, 350:109242.
[19] SEPTEMBRE-MALATERRE A, REMIZE F, POUCHERET P.Fruits and vegetables, as a source of nutritional compounds and phytochemicals:Changes in bioactive compounds during lactic fermentation[J].Food Research International, 2018, 104:86-99.
[20] LI S J, TAO Y, LI D D, et al.Fermentation of blueberry juices using autochthonous lactic acid bacteria isolated from fruit environment:Fermentation characteristics and evolution of phenolic profiles[J].Chemosphere, 2021, 276:130090.
[21] LI T L, JIANG T, LIU N, et al.Biotransformation of phenolic profiles and improvement of antioxidant capacities in jujube juice by select lactic acid bacteria[J].Food Chemistry, 2021, 339:127859.
[22] ZHOU M, JOHNSTON L J, WU C D, et al.Gut microbiota and its metabolites:Bridge of dietary nutrients and obesity-related diseases[J].Critical Reviews in Food Science and Nutrition, 2023, 63(18):3236-3253.
[23] TIAN M B, HU R Q, LIU Z L, et al.The pH adjustment of Vitis amurensis dry red wine revealed the evolution of organic acids, volatomics, and sensory quality during winemaking[J].Food Chemistry, 2024, 436:137730.
[24] WANG D W, DENG Y N, ZHAO L, et al.GABA and fermented litchi juice enriched with GABA promote the beneficial effects in ameliorating obesity by regulating the gut microbiota in HFD-induced mice[J].Food &Function, 2023, 14(18):8170-8185.
[25] SHENG J, SHAN C H, LIU Y Y, et al.Comparative evaluation of the quality of red globe grape juice fermented by Lactobacillus acidophilus and Lactobacillus plantarum[J].International Journal of Food Science &Technology, 2022, 57(4):2235-2248.
[26] JIANG X H, LU Y Y, LIU S Q.Effects of pectinase treatment on the physicochemical and oenological properties of red dragon fruit wine fermented with Torulaspora delbrueckii[J].LWT, 2020, 132:109929.