低聚半乳糖(galactooligosaccharides,GOS)是一种功能性低聚糖,具有促进有益菌生长、改善肠道健康等重要生理活性[1-2],在功能性食品、婴幼儿配方奶粉、环境保护与特殊新材料创新等方面具有重要应用价值[3],预计其全球市场至2033年的年增长率约为6%[4]。随着健康食品市场的快速发展,对高效生产GOS的乳糖酶需求日益增长。GOS最初通过分离提取方法获得,发展至今酶促合成已成为其主要制备方法。其中,具有高效转苷活性的乳糖酶是GOS生物制备的关键。乳糖酶(β-半乳糖苷酶,EC 3.2.1.23)是一类重要的糖苷水解酶,广泛分布于微生物、植物和动物中,多数以其催化乳糖水解为葡萄糖和半乳糖的功能而被发现或鉴定[5-6]。已有研究揭示,部分乳糖酶分子具有转糖苷活性,可将乳糖分子中的半乳糖基转移至受体乳糖分子上,由此实现GOS的酶促催化合成[7]。可见,乳糖酶的高效转苷活性决定了该酶在GOS制备中的价值并推动其相关应用的创建。
提升包括乳糖酶在内的工业重要酶制剂的催化性能,是酶工程研究领域的重要内容。传统策略主要集中在筛选高活性菌种、改善发酵工艺及优化反应条件等方面[8]。随着结构生物学和计算生物学的发展,基于酶分子结构的理性设计已成为提升工业重要酶制剂催化性能的新途径[9]。已有研究表明,酶分子底物通道的空间构象对酶的催化性能具有重要影响,底物通道作为连接酶表面与活性中心的关键通路,其结构特性直接影响底物的识别、转运及产物释放效率[10]。优化底物通道结构能够有效提高酶的催化效率,如血红素蛋白酶[11]、纤维素酶[12]等。
本课题组对乳糖酶的前期研究表明,理性微调催化产物葡萄糖通道结构并促进其释放可以显著提高乳糖酶的催化效率[13]。本研究以提高乳糖酶催化性能为目标,从其乳糖底物通道结构入手,探究乳糖酶BglD分子中底物通道的结构特征及其对催化性能的影响。通过分子对接和计算模拟,分析乳糖酶BglD底物口袋内衬氨基酸残基的空间构象和功能特性,识别关键功能位点,并通过定点突变技术对底物通道进行优化设计,以揭示乳糖酶底物通道结构与催化性能之间的关联机制,为通过酶分子进化技术提升乳糖酶催化性能,进而促进GOS高效制备和相关产业发展提供理论基础和技术支持。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株、质粒及引物
本研究所涉及的菌种和质粒均为实验室保藏,分别为枯草杆菌(Bacillus subtilis)WB600、地衣芽胞杆菌(Bacillus licheniformis)CBBD302和质粒pHY-WZX[14]。通过PCR扩增获得突变体V377S基因所用突变引物上、下游分别为V377S-f(5′-TAACGCCATTCGTAGCACACACAATCCAG-3′)和V377S-r(5′-CTGGATTGTGTGTGCTACGAATGGCGTTA-3′),基因全长引物上、下游分别为BglD-F(5′-GCTGGATCCAGCAAGACTACCTCCGCTGCTG-3′)和BglD-R(5′-AGGAGTGACGGTGAAAACAGAAG-3′),由生工生物工程(上海)股份有限公司通过化学合成获得。
1.1.2 试剂与培养基
胰蛋白胨、酵母粉,英国Oxoid公司;NaCl、CaCl2、(NH4)2SO4,中国国药集团化学试剂有限公司;硫酸卡那霉素,上海生物工程有限公司;豆饼粉,北京鸿润宝顺科技有限公司;乳糖,美国Sigma-Aldrich公司。
LB培养基(10 g/L胰蛋白胨,5 g/L酵母粉,10 g/L NaCl),用于B.subtilis和B.licheniformis及其转化子的培养,必要时在培养基中添加终质量浓度为20 μg /mL硫酸卡那霉素。发酵培养基[25 g/L豆饼粉,40 g/L乳糖,0.3 g/L CaCl2,3 g/L (NH4)2SO4],用于重组B.licheniformis异源酶的制备。
1.2 仪器与设备
Column SuperdexTM 200 Increase 10/300 GL型凝胶过滤层析柱,美国GE Healthcare公司;SBA-40X型生物传感仪,山东省科学院生物研究所;Shodex RI-201H型检测器,日本Shoko Science公司;1260型HPLC系统,美国Agilent公司;Sugar-PakTM Ⅰ Column型钙型阳离子交换柱,美国Waters公司;YMC-Pack NH2型氨基柱,日本YMC公司。
1.3 实验方法
1.3.1 乳糖酶分子结构模拟
通过蛋白质建模服务器SWISS-MODEL(https://swissmodel.expasy.org/)进行乳糖酶同源性建模,将相似度最高的晶体结构作为模型,预测构建突变体乳糖酶模型。利用ClustalW软件进行氨基酸序列比对,标记活性位点及保守序列[15]。运用AutoDockTools软件模拟乳糖酶与底物的分子对接情况[16]。通过通道预测软件CAVER分析底物运输通道的详细特征,预测底物和产物通道[17]。通过PyMOL软件分析获得可视化的乳糖酶及其突变体结构[18]。
1.3.2 分子克隆及定点突变
本研究所采用的分子克隆操作,均按照实验室常规方法进行[19]。定点突变采用重叠PCR技术完成[20]。乳糖酶及其突变体基因的扩增产物克隆至pHY-WZX载体中,经化学转化法将重组质粒转化入B.subtilis WB600中,经确认正确的重组质粒再电转入表达宿主B.licheniformis CBBD302中,获得重组菌,进行乳糖酶及其突变体的异源表达。
1.3.3 乳糖酶突变体的制备与纯化
将重组菌接种至装有50 mL LB液体培养基的三角瓶中,于37 ℃、200 r/min振荡培养16 h,制备种子液。按10%接种量将种子液接种至发酵培养基中,在相同条件下继续培养120 h。发酵结束后,8 000 r/min离心10 min,收集上清液,即为粗酶液。
粗酶液经50%~60%饱和(NH4)2SO4溶液分级沉淀后,收集沉淀并重新溶解于适当缓冲液中。进一步采用凝胶过滤层析柱进行蛋白纯化。纯化后的酶液经SDS-PAGE(分离胶12%,浓缩胶5%)验证纯度,并采用Bradford法测定蛋白浓度[21]。
1.3.4 酶学性质及动力学参数测定
乳糖酶活力测定参照文献[8]的方法。以100 g/L的乳糖溶液为底物,在40 ℃和pH 6.0条件下反应20 min,沸水浴10 min终止反应。使用生物传感仪测定生成的葡萄糖含量并计算乳糖酶活力。乳糖酶活力定义为:在检测条件下,每分钟催化产生1 μmol葡萄糖的酶量定义为一个酶活力单位(U)。
乳糖酶突变体的酶促动力学参数测定在50~300 mmol/L乳糖溶液中进行,按照上述方法测定酶活力,以1/V对1/S绘制动力学曲线,并计算获得酶的动力学参数Km、Vmax、kcat和kcat/Km。
1.3.5 GOS酶促合成与糖谱分析
以10 g/L乳糖为底物,加酶量5 U/g乳糖,在pH 6.0、40 ℃条件下,反应12 h后,置沸水浴加热10 min终止反应。反应过程中定时取样,使用配备有检测器的HPLC系统和双色谱柱法检测产物谱(GB/T 1903.27—2022《食品安全国家标准 食品营养强化剂 低聚半乳糖》)。色谱分析采用双柱互补检测策略。钙型阳离子交换柱分析条件:流动相采用超纯水,流速0.5 mL/min,柱温80 ℃,检测器温度40 ℃;氨基柱分析条件:流动相为体积分数为70%的乙腈,流速1.0 mL/min,柱温35 ℃,检测器温度40 ℃。以相关物质浓度变化反映GOS生成及乳糖消耗情况,按照公式(1)及公式(2)计算并绘制时间-产物(底物)浓度曲线。
ρ1=ρ2-ρ3-ρ4-ρ5
(1)
ρ6=ρ7-ρ5
(2)
式中:ρ1,GOS质量浓度,g/L;ρ2,总糖质量浓度,g/L;ρ3,半乳糖质量浓度,g/L;ρ4,葡萄糖质量浓度,g/L;ρ5,剩余乳糖质量浓度,g/L;ρ6,消耗乳糖质量浓度,g/L;ρ7,初始乳糖质量浓度,g/L。
2 结果与讨论
2.1 乳糖酶BglD乳糖底物通道的结构特征解析
以B.circulans来源的乳糖酶(SMTL ID:8q2 h.1.A)为模板,构建出BglD的3D构型(图1-a)。进一步与肺炎链球菌(Streptococcus pneumoniae)来源的BgaA[22]、B.circulans ATCC 31382来源的BgaD-D[23]和两歧双歧杆菌(Bifidobacterium bifidum)来源的BbgⅢ[24]进行氨基酸序列比对分析(图1-b),确认其催化三联体Glu447、Tyr511和Glu532组成及其结构特征。在该酶的催化三联体所在区域含有1个构型及大小适宜的底物口袋样结构,其中氨基酸残基Arg185、His379、Glu447、Glu532、Trp570和Glu601能够与底物乳糖直接产生氢键相互作用(图1-a)。以此为基准起点,进一步分析该酶分子内的乳糖底物通道,发现该酶分子内存在2个乳糖底物通道(分别命名为通道T1和通道T2),皆为8个β折叠组成的桶状结构,并被8个α螺旋所包围。其中,通道T2在结构上明显存在一段狭窄区,这一结构特征可能是影响该酶分子内乳糖转运速率的限定因素。
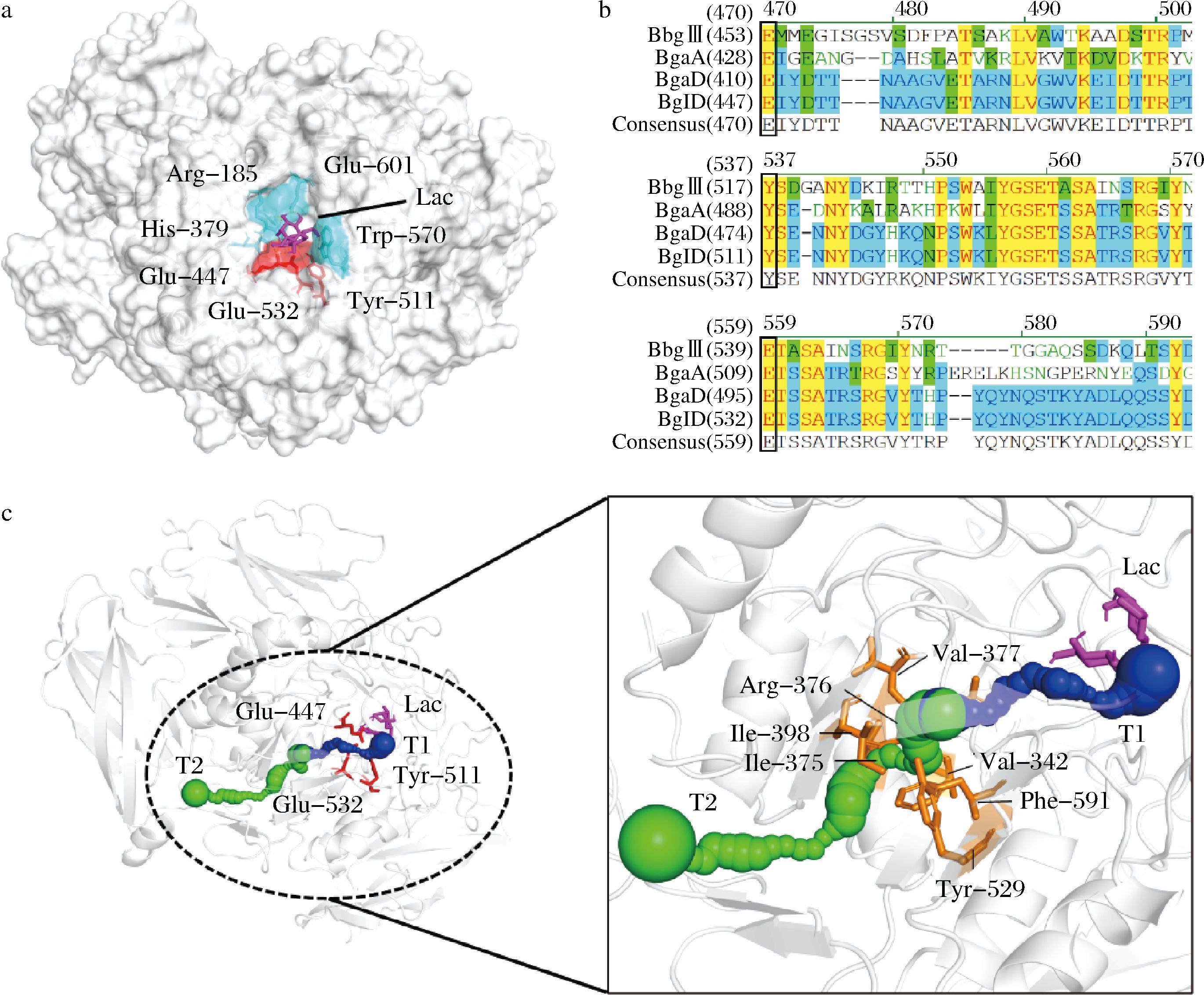
a-乳糖酶BglD三级结构及活性位点;b-氨基酸序列比对(方框内为催化三联体的保守氨基酸残基);c-乳糖酶分子内底物通道关键内衬氨基酸残基组成与分布
图1 乳糖酶BglD三级结构及其乳糖底物通道分析
Fig.1 Analysis of tertiary structure of lactase BglD and its lactose substrate tunnels
已有研究揭示,酶分子内底物/产物通道的结构优化可显著改变其催化性能。通过将特定酶分子内产物通道中瓶颈氨基酸残基突变为侧链较小的氨基酸后,可降低产物释放过程中遇到的阻力,由此显著提高酶活性[11, 25];定点突变一氧化碳脱氢酶分子中通道瓶颈氨基酸残基Ala559后实现对该酶分子内气体通道的结构微构优化,大幅度降低该酶的氧敏感性[26];通过系统改造细胞色素P450酶的活性位点、底物进入通道和水通道等关键部位,成功增强了该酶对长链烷烃碳氢键活化反应的催化能力[27];通过对酶底物/产物进出通道中特定氨基酸残基的理性设计,还可以显著消除酶促过程中常见的底物抑制效应[28]。因此,定向修改乳糖酶分子内通道T2的狭窄区,有可能提升该酶的催化性能。为此,进一步分析获得了该狭窄区的内衬氨基酸组成(图1-c),主要包括:Val342、Ile375、Arg376、Val377、Ile398、Tyr529和Phe591,作为后续通道T2结构改造的基础。
2.2 乳糖酶BglD底物通道T2区域的结构优化与突变体设计
针对底物通道T2狭窄区域关键内衬氨基酸残基,进行了模拟饱和突变后的结构变化分析。结果显示,底物通道T2狭窄区关键内衬氨基酸残基Val342、Ile375、Arg376、Val377、Ile398、Tyr529和Phe591突变后,仅V377S在未显著改变底物结合局部结构特征的前提下,有效改善底物T2通道狭窄区结构,其瓶颈半径增加11.68%,意味着有可能以更高效率实现底物转运(图2、表1)。此外,V377S突变后,通道T2的长度及曲率有所增大,但能量消耗和通道通量未发生明显变化。该突变未对底物通道T1的结构特征产生影响。进一步分析了V377S突变后关键构象的可能改变,结果显示该突变使酶分子与乳糖的结合构象发生了轻度变化(图2-b,图2-e),酶分子与底物乳糖相互作用的氨基酸残基由7个增加为8个,氢键数量由12个减少至10个(图2-c,图2-f),自由结合能由-4.13 kcal/mol降低至-4.24 kcal/mol,表明突变后活性中心对乳糖底物的亲和力提高,有利于提升该酶的催化效率。为此,就V377S突变可能带来的相关酶学性质变化,进行进一步实验分析。
表1 乳糖酶突变体V377S的底物通道参数
Table 1 Substrate tunnel parameters of mutant V377S
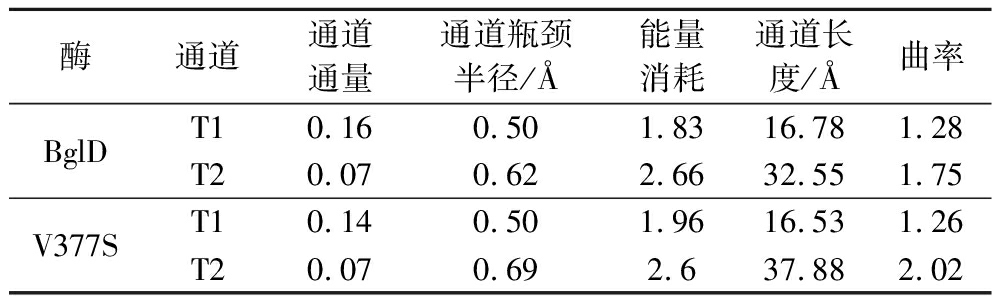
酶通道通道通量通道瓶颈半径/Å能量消耗通道长度/Å曲率BglDT10.160.501.8316.781.28T20.070.622.6632.551.75V377ST10.140.501.9616.531.26T20.070.692.637.882.02
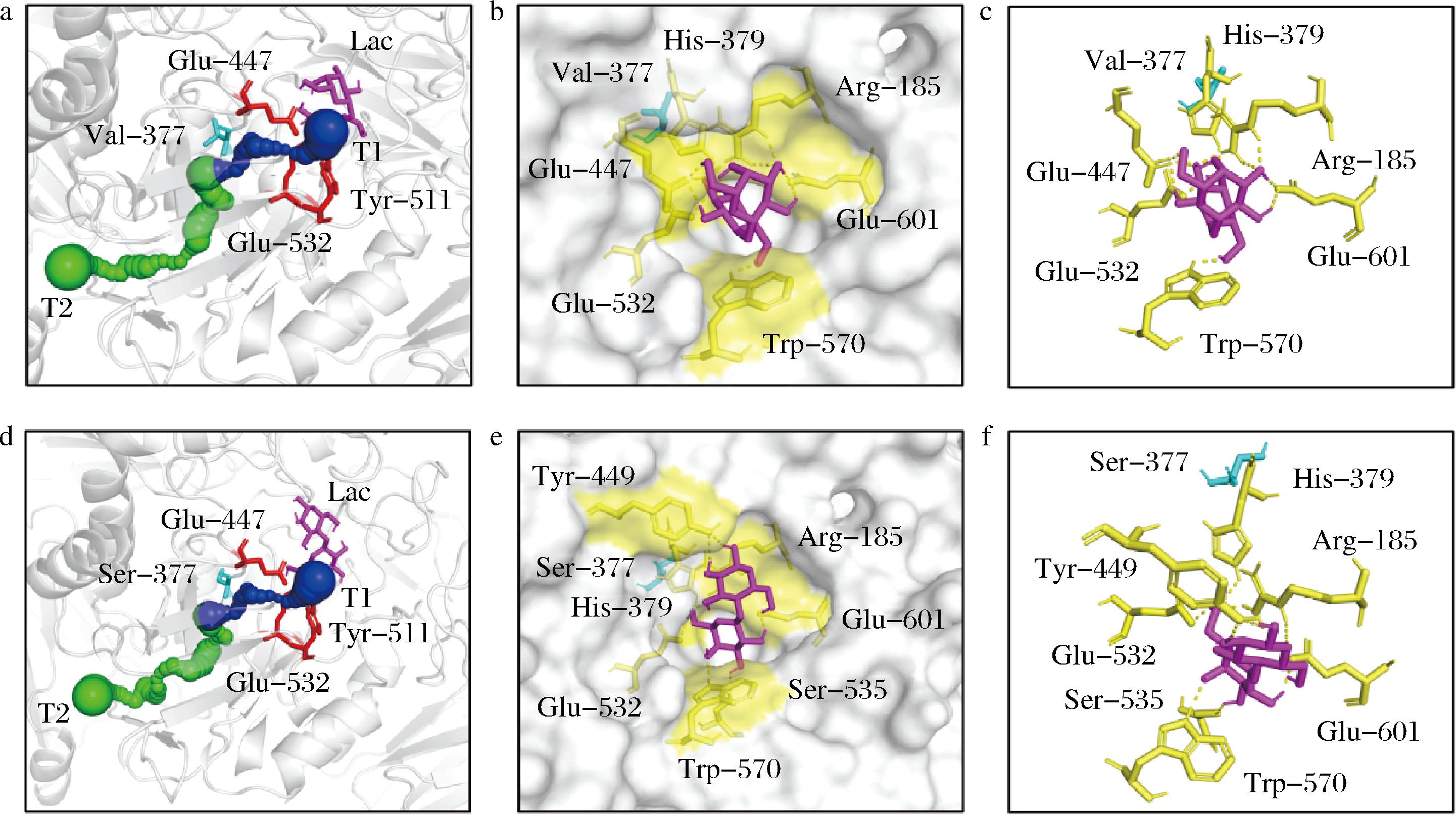
a-BglD底物通道;b-BglD底物结合口袋;c-BglD底物结合构象;d-V377S底物通道;e-V377S底物结合口袋;f-V377S底物结合构象
图2 乳糖酶突变体V377S的结构变化
Fig.2 Structural changes in mutant V377S
2.3 突变体V377S的创建及其催化特征解析
2.3.1 突变体V377S的创建、制备与纯化
通过定点突变技术在乳糖酶BglD中引入V377S突变,并在pHY-WZX介导下于B.licheniformis CBBD302中进行异源表达[14]。对发酵粗酶液进行酶活力测定,酶活力为75.74 U/mL,表明突变体V377S成功在B.licheniformis CBBD302中表达。对粗酶液进行纯化,SDS-PAGE分析显示,样品在约90 kDa位置呈现单一条带,证明突变体V377S被成功纯化(图3)。突变体V377S的比酶活力为135.83 U/mg,较野生型BglD提高17.95%(表2),提示其单位酶分子的催化效率增强。
表2 乳糖酶突变体V377S的比酶活力及酶促动力学参数
Table 2 Specific activities and kinetics parameters of mutant V377S

酶比酶活力/(U/mg)Km/(mmol/L)Vmax/(mmol/min)kcat/(s-1)kcat/Km/[L/(mmol·s)]BglD115.16110.241.3322.920.21V377S135.8379.421.7235.090.44
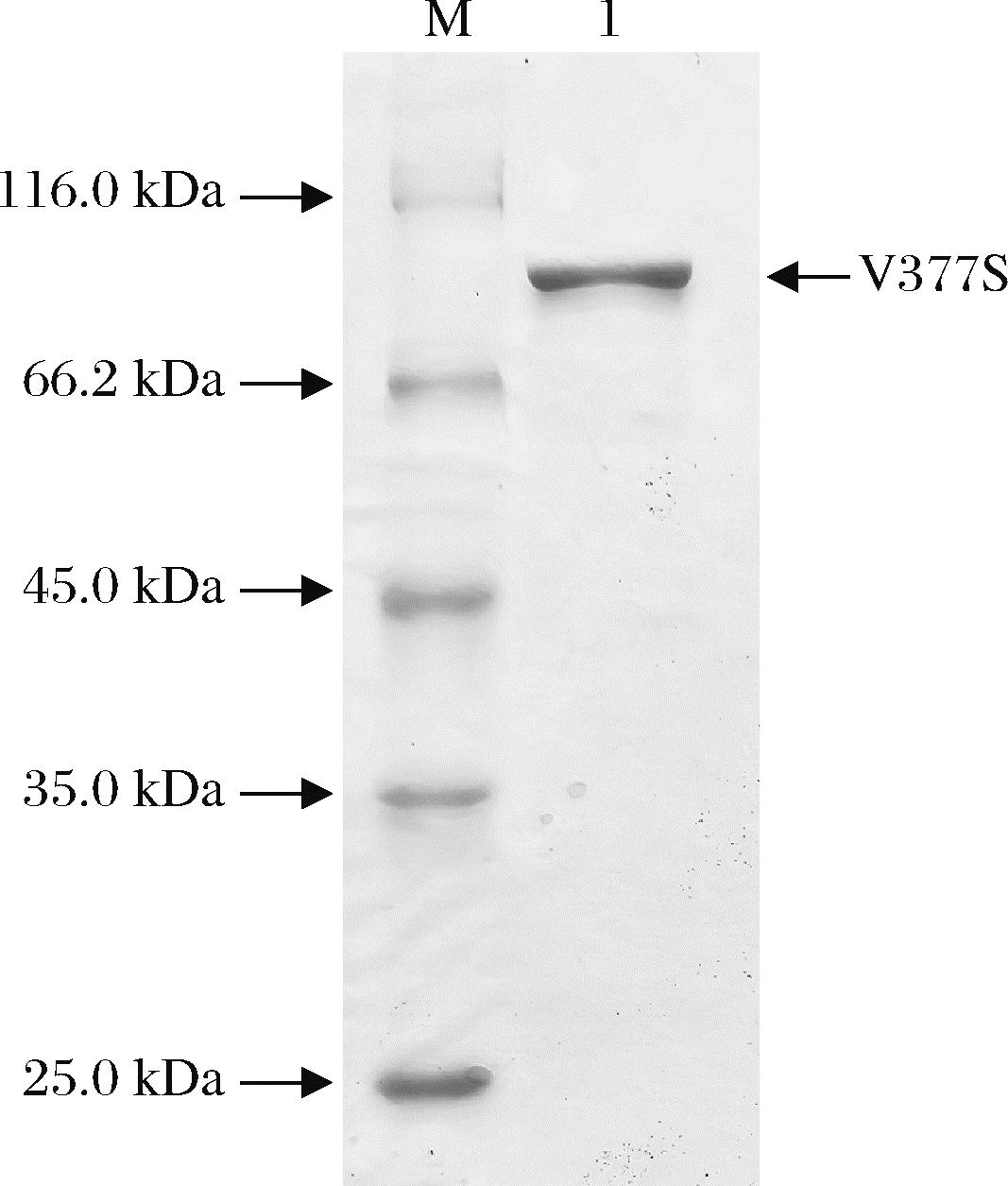
M-蛋白标准分子质量;1-乳糖酶突变体V377S。
图3 乳糖酶突变体V377S的SDS-PAGE分析
Fig.3 SDS-PAGE analysis of mutant V377S
2.3.2 突变体V377S酶促动力学特征变化
对突变体V377S的酶促动力学参数进行了分析,结果显示,其Km值降低了27.96%(表2),表明V377S突变后酶分子对底物的亲和力得到显著提升,表示在相同的底物浓度下,V377S相较于野生型更容易与底物形成酶-底物复合物,从而加快酶促反应进程。突变体V377S的kcat相较于野生型提高了53.10%(表2),表明当底物乳糖与突变体V377S的催化位点结合时,在单位时间内催化底物转化效率增强。底物亲和力(Km)增强和催化常数(kcat)提升,使得突变体V377S的催化效率(kcat/Km)较野生型提升了109.52%(表2)。这意味着当酶促反应在非饱和底物浓度下进行时(底物浓度低于Km),V377S识别并结合底物,然后将其转化为产物的能力大大提升。
这表明V377S突变不仅优化了底物转移效率,还改善了活性位点的微环境,有利于底物向产物的高效转化。综上所述,通过理性微调乳糖酶分子内部底物通道狭窄区的关键氨基酸残基,成功实现了酶催化效率的显著提升。现有研究揭示,酶分子内气态底物通道[26]、液态底物通道[27, 29]、水通道[27]、产物转运通道[11, 25, 28-30]等的微结构优化,显著提升了相关酶分子的催化性能。本研究针对乳糖酶底物通道狭窄区的微调所获得的结果,与上述通道结构优化提升酶催化效率的研究发现相互印证,进一步强化了酶分子通道工程在提高酶催化性能中的重要性。
2.3.3 突变体V377S催化合成GOS的动力学表征
进一步对突变体V377S催化乳糖合成GOS过程进行了系统分析,结果汇总于图4和表3。在相同反应条件下,突变体V377S在催化GOS合成过程中展现出显著优势,主要体现在以下两个方面:
表3 乳糖酶突变体V377S催化合成GOS的过程参数
Table 3 Process parameters of GOS synthesis catalyzed by mutant V377S
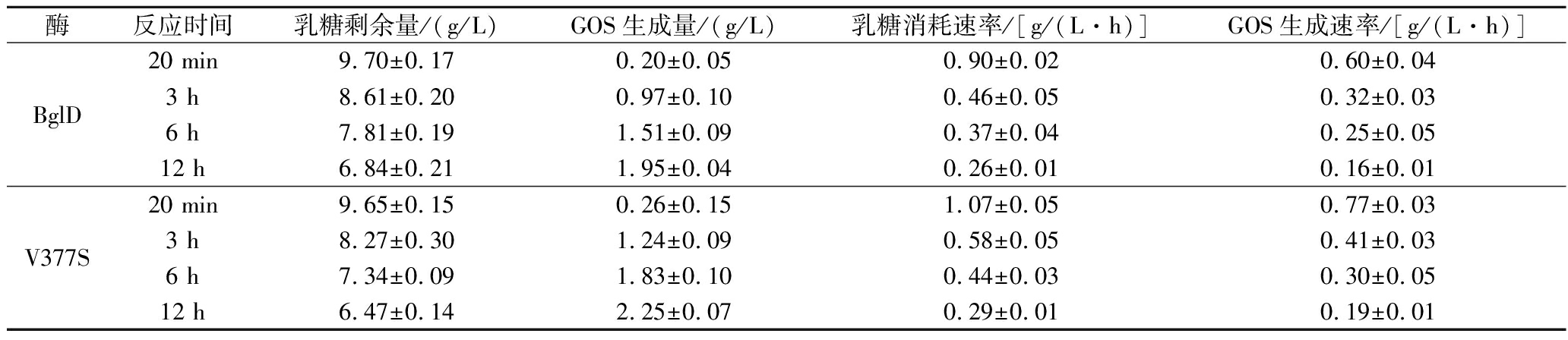
酶反应时间乳糖剩余量/(g/L)GOS生成量/(g/L)乳糖消耗速率/[g/(L·h)]GOS生成速率/[g/(L·h)]BglD20 min9.70±0.170.20±0.050.90±0.020.60±0.043 h8.61±0.200.97±0.100.46±0.050.32±0.036 h7.81±0.191.51±0.090.37±0.040.25±0.0512 h6.84±0.211.95±0.040.26±0.010.16±0.01V377S20 min9.65±0.150.26±0.151.07±0.050.77±0.033 h8.27±0.301.24±0.090.58±0.050.41±0.036 h7.34±0.091.83±0.100.44±0.030.30±0.0512 h6.47±0.142.25±0.070.29±0.010.19±0.01
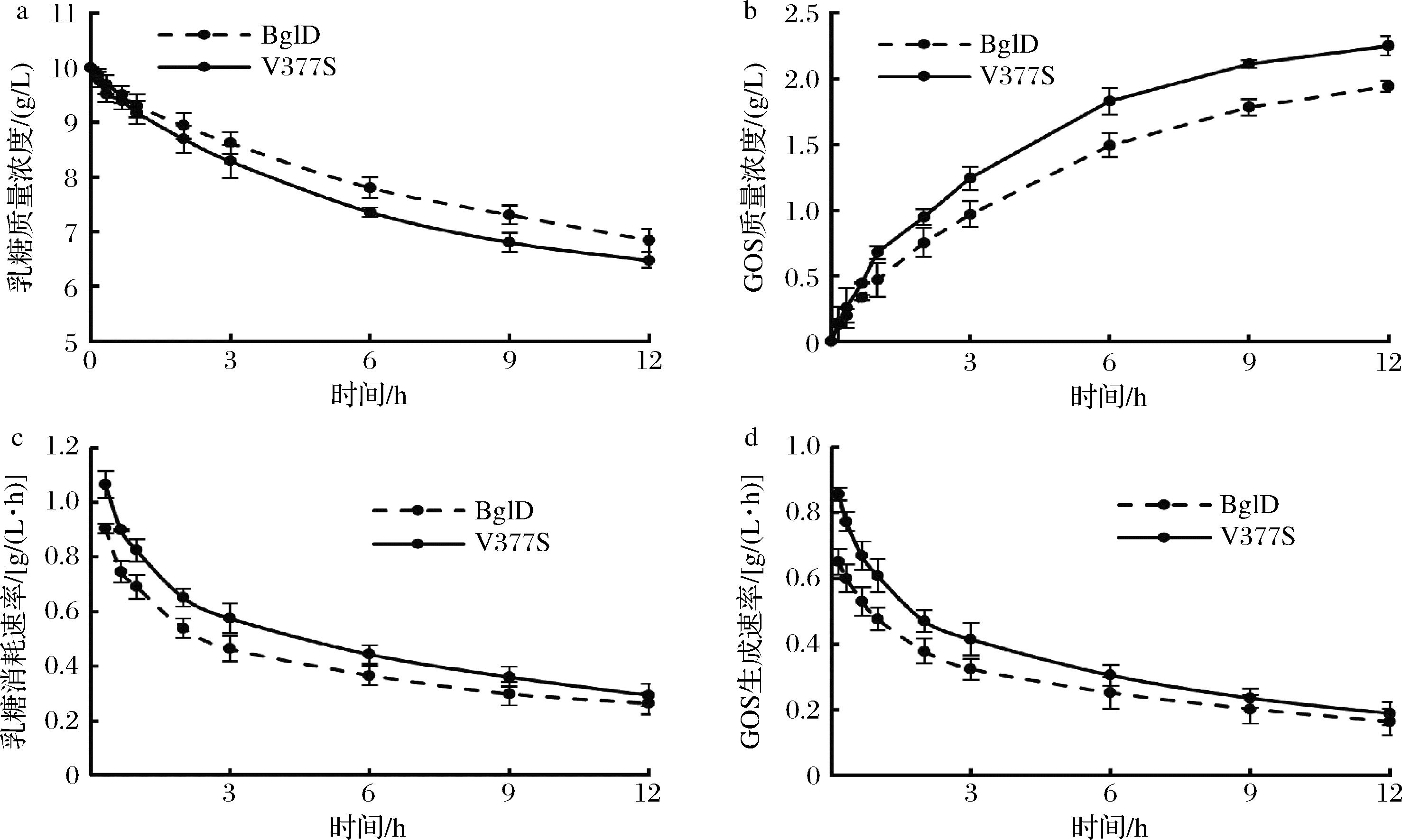
a-乳糖质量浓度变化;b-GOS质量浓度变化;c-乳糖消耗速率变化;d-GOS合成速率变化
图4 乳糖酶突变体V377S催化乳糖合成GOS反应过程
Fig.4 Synthesis process of GOS catalyzed by mutant V377S
一是底物转化效率得到明显提升。与野生型BglD相比,突变体V377S催化底物乳糖转化为GOS的转化率提高了15.38%,底物消耗率增加了11.71%,同时终反应体系中剩余乳糖量降低了5.41%(图4-a,图4-b)。这一结果与前述酶动力学参数变化相符,证实了V377S突变通过改善底物通道微环境明显增强了该酶对底物的利用效率。
二是催化GOS合成效率得到显著改善。与野生型BglD相比,突变体V377S表现出更高的反应初速度,在反应进程中GOS合成速率最高提升28.33%,乳糖消耗率最高提升26.09%(图4-c,图4-d)。这表明V377S突变不仅加快了反应速率,而且维持了较高的转化效率,这与其kcat/Km值提升109.52%的结果相符。因此,通过定向优化底物通道狭窄区微结构获得的新酶分子,具有更优异的催化乳糖合成GOS的能力。
当前,工业上通过乳糖酶催化合成GOS面临2个主要挑战:一是反应后剩余大量未转化底物,二是在低浓度乳糖条件下GOS合成效率低下。本研究所构建的V377S突变体提高了底物亲和力,显著降低了反应体系剩余底物量,这使其在低浓度乳糖条件下可能具有独特应用优势。这一改良酶分子为GOS生物制备工艺优化提供了新选择,特别适用于低乳糖浓度应用场景,为后续低成本、高效率GOS生产技术的开发奠定了基础。此方向的应用潜力及工艺参数优化将是未来深入研究的重点内容。
3 结论
本研究基于对乳糖酶分子结构的深入分析,系统阐明了其底物通道的分子结构基础,成功识别出限制底物转运的关键瓶颈区域及其内衬氨基酸残基。通过对乳糖底物通道结构的理性设计与优化,并采用定点突变手段扩展其底物通道中的狭窄区域,获得了对底物乳糖亲和力明显增强的突变体V377S,其比酶活力提高了17.95%,催化效率提高了近1.1倍,催化乳糖合成GOS时的底物转化效率、GOS合成效率等均得到显著提升,且GOS生成量提高15.38%,底物乳糖消耗量提高了5.41%。所获得的新酶分子有望在多种原材料(如乳清及其超滤透析液、稀乳清、乳制品加工废液以及低乳糖乳制品等)中实现更高效的GOS合成。特别是在乳糖含量较低的原料背景下,该突变体将有助于扩大原料来源、提升资源利用效率、简化工艺流程并降低生产成本。本研究建立的通道工程策略不仅适用于乳糖酶,还可为相关酶分子的改造提供参考,有助于拓展功能性低聚糖生产在食品工业中的应用前景。
[1] MEI Z J, YUAN J Q, LI D D.Biological activity of galacto-oligosaccharides:A review[J].Frontiers in Microbiology, 2022, 13:993052.
[2] CAI Y, GILBERT M S, GERRITS W J J, et al.Galacto-oligosaccharides alleviate lung inflammation by inhibiting NLRP3 inflammasome activation in vivo and in vitro[J].Journal of Advanced Research, 2022, 39:305-318.
[3] SOUZA A F C E, GABARDO S, DE JESUS SILVA COELHO R.Galactooligosaccharides:Physiological benefits, production strategies, and industrial application[J].Journal of Biotechnology, 2022, 359:116-129.
[4] MARKET DATA FORECAST INC.Global galacto-oligosaccharides (GOS) market size, share, trends &growth forecast report-segmented by application (food &beverages, dietary supplements), product (syrup, powder), and region(North America, Europe, Asia-Pacific, Latin America, Middle East and Africa)-global industry analysis, size, share, growth, trends and forecast 2025 to 2033[R].(2025-04) [2025-08-21].https://www.marketdataforecast.com/market-reports/galacto-oligosaccharide-market.
[5] DAMIN B I S, KOVALSKI F C, FISCHER J, et al.Challenges and perspectives of the β-galactosidase enzyme[J].Applied Microbiology and Biotechnology, 2021, 105(13):5281-5298.
[6] AMBROGI V, BOTTACINI F, MAC SHARRY J, et al.Bifidobacterial β-galactosidase-mediated production of galacto-oligosaccharides:Structural and preliminary functional assessments[J].Frontiers in Microbiology, 2021, 12:750635.
[7] DE ALBUQUERQUE T L, DE SOUSA M, GOMES E SILVA N C, et al.β-Galactosidase from Kluyveromyces lactis:Characterization, production, immobilization and applications - a review[J].International Journal of Biological Macromolecules, 2021, 191:881-898.
[8] 赵继华, 牛丹丹, MCHUNU N P, 等.高转苷活性乳糖酶快速筛选方法的建立与初步应用[J].食品与发酵工业, 2020, 46(7):17-20.ZHAO J H, NIU D D, MCHUNU N P, et al.Establishment and preliminary application of a rapid screening method for high transglycosylation activity β-galactosidase[J].Food and Fermentation Industries, 2020, 46(7):17-20.
[9] ZHOU L, TAO C M, SHEN X L, et al.Unlocking the potential of enzyme engineering via rational computational design strategies[J].Biotechnology Advances, 2024, 73:108376.
[10] KINGSLEY L J, LILL M A.Substrate tunnels in enzymes:Structure-function relationships and computational methodology[J].Proteins, 2015, 83(4):599-611.
[11] MENG S Q, AN R P, LI Z Y, et al.Tunnel engineering for modulating the substrate preference in cytochrome P450BsβHI[J].Bioresources and Bioprocessing, 2021, 8(1):26.
[12] LU Z H, LI X Z, ZHANG R, et al.Tunnel engineering to accelerate product release for better biomass-degrading abilities in lignocellulolytic enzymes[J].Biotechnology for Biofuels, 2019, 12(1):275.
[13] ZHAO J H, NIU D D, LIU J Q, et al.Enhancing β-galactosidase performance for galactooligosaccharides preparation via strategic glucose re-tunneling[J].International Journal of Molecular Sciences, 2024, 25(22):12316.
[14] NIU D D, ZUO Z R, SHI G Y, et al.High yield recombinant thermostable alpha-amylase production using an improved Bacillus licheniformis system[J].Microbial Cell Factories, 2009, 8:58.
[15] RAKOTOHARISOA R V, SEIFINOFEREST B, ZARIFI N, et al.Design of efficient artificial enzymes using crystallographically enhanced conformational sampling[J].Journal of the American Chemical Society, 2024, 146(14):10001-10013.
[16] MORRIS G M, HUEY R, LINDSTROM W, et al.AutoDock4 and AutoDockTools4:Automated docking with selective receptor flexibility[J].Journal of Computational Chemistry, 2009, 30(16):2785-2791.
[17] STOURAC J, VAVRA O, KOKKONEN P, et al.Caver Web 1.0:Identification of tunnels and channels in proteins and analysis of ligand transport[J].Nucleic Acids Research, 2019, 47(W1):W414-W422.
[18] DELANO W L.The PyMOL Molecular Graphics System[J].Proteins Structure Function and Bioinformatics, 2002, 30:442-454
[19] 诸葛健, 王正祥.工业微生物实验技术手册[M].北京:中国轻工业出版社, 1994.ZHUGE J, WANG Z X.Handbook of industrial microbiology experimental techniques[M].Beijing:China Light Industry Press, 1994.
[20] 杨林, 王柳月, 李慧美, 等.改进的多片段重叠延伸PCR制作基因多位点突变[J].中国生物工程杂志, 2019, 39(8):52-58.YANG L, WANG L Y, LI H M, et al.An improved multiple-site mutation method by multi-fragment overlap extension PCR[J].China Biotechnology, 2019, 39(8):52-58.
[21] KIELKOPF C L, BAUER W, URBATSCH I L.Bradford assay for determining protein concentration[J].Cold Spring Harbor Protocols, 2020, 2020(4):102269.
[22] SINGH A K, PLUVINAGE B, HIGGINS M A, et al.Unravelling the multiple functions of the architecturally intricate Streptococcus pneumoniae β-galactosidase, BgaA[J].PLoS Pathogens, 2014, 10(9):e1004364.
[23] ISHIKAWA K, KATAOKA M, YANAMOTO T, et al.Crystal structure of β-galactosidase from Bacillus circulans ATCC 31382 (BgaD) and the construction of the thermophilic mutants[J].The FEBS Journal, 2015, 282(13):2540-2552.
[24] MOROZ O V, BLAGOVA E, LEBEDEV A A, et al.Multitasking in the gut:The X-ray structure of the multidomain BbgIII from Bifidobacterium bifidum offers possible explanations for its alternative functions[J].Acta Crystallographica.Section D, Structural Biology, 2021, 77(Pt 12):1564-1578.
[25] KONG X D, YUAN S G, LI L, et al.Engineering of an epoxide hydrolase for efficient bioresolution of bulky pharmaco substrates[J].Proceedings of the National Academy of Sciences of the United States of America, 2014, 111(44):15717-15722.
[26] KIM S M, LEE J, KANG S H, et al.O2- tolerant CO dehydrogenase via tunnel redesign for the removal of CO from industrial flue gas[J].Nature Catalysis, 2022, 5(9):807-817.
[27] TAHER M, DUBEY K D, MAZUMDAR S.Computationally guided bioengineering of the active site, substrate access pathway, and water channels of thermostable cytochrome P450, CYP175A1, for catalyzing the alkane hydroxylation reaction[J].Chemical Science, 2023, 14(48):14316-14326.
[28] KOKKONEN P, BEIER A, MAZURENKO S, et al.Substrate inhibition by the blockage of product release and its control by tunnel engineering[J].RSC Chemical Biology, 2021, 2(2):645-655.
[29] HOSSAIN M, DODDA S R, DAS S, et al.Catalytic tunnel engineering of thermostable endoglucanase of GH7 family (W356C) from Aspergillus fumigatus gains catalytic rate[J].Enzyme and Microbial Technology, 2025, 187:110632.
[30] MA D, CHENG Z Y, HAN L C, et al.Structure-oriented engineering of nitrile hydratase:Reshaping of substrate access tunnel and binding pocket for efficient synthesis of cinnamamide[J].International Journal of Biological Macromolecules, 2024, 254:127800.