泡菜是我国著名的传统发酵蔬菜食品,历史悠久。以四川泡菜为代表的发酵蔬菜制品,主要采用蔬菜为基础原料,经过食盐或盐水腌渍发酵而成[1]。泡菜富含以乳酸菌和酵母菌为主的微生物菌群,风味酸爽、营养丰富,深受消费者喜爱。泡菜原料表面和环境中携带的微生物利用原料中的营养物质进行生长代谢,从而产生泡菜独特的风味。
风味是衡量发酵食品品质的重要指标,是泡菜新产品开发和消费者选购的重要参考。泡菜发酵过程中微生物种群结构、多样性及其代谢特征在风味物质的合成与转化中具有显著影响[2]。泡菜的风味形成还受到工艺、原料等多种因素影响,使自然发酵泡菜风味品质难以稳定[3]。工业上通过高盐、低温、防腐剂等措施来延缓泡菜过酸、软化和腐败[4-7],这种通过扰动提升传统发酵食品的风味和质量的方法具有重要意义。物理扰动是影响泡菜风味品质的重要因素。传统四川泡菜成熟后会将其取出,然后补充新鲜蔬菜、香辛料、食盐和冷开水等,搅拌混匀,连续多轮发酵,每轮发酵都保持泡菜体系盐浓度的相对平衡,实现泡菜风味的相对稳定。古代航海时期,船员普遍采用传统发酵工艺制备泡菜以应对长期航行中蔬菜缺少的问题,现代营养学分析表明,泡菜不仅能为船员补充维生素C等必需营养素,还具有促进消化吸收的功能[8]。泡菜随着船的颠簸而处于振荡环境,这种振荡环境可能有利于泡菜风味稳定,防止菌体沉淀。此外,生物扰动也是影响泡菜风味品质的关键因素。乳酸菌是泡菜发酵中主要的微生物,研究表明,乳酸菌可以耐受高酸度的环境,并在发酵后期产生丰富的乳酸[9]。泡菜发酵过程常采用接种乳酸菌来强化发酵,加快泡菜成熟。有研究表明,酵母菌对泡菜的香气和风味有一定的贡献[10],但更多研究报道表明,一部分酵母菌会导致泡菜“生花”和腐败变质[11-14]。泡菜制作环境不卫生或管理不当,易使泡菜液界面“生花”长膜,这一现象多与膜醭毕赤酵母污染有关,会损害泡菜的感官与风味。
复杂的扰动因素,影响着泡菜微生物生长代谢,继而造就了不同的风味品质,是自然发酵泡菜产品风味品质不稳定的主要原因。动态跟踪、模拟扰动过程中微生物数量、品质特征和风味成分的演变是调控泡菜风味品质的关键。目前有关振荡和强化接种毕赤酵母扰动处理对泡菜发酵过程风味品质影响的研究还未见报道。
综上,本研究旨在用连续式振荡模拟物理扰动、接种膜醭毕赤酵母1CF3模拟生物扰动,在密封与通气条件下分析泡萝卜理化特征参数及风味化合物。采用高效液相色谱法研究泡菜中的有机酸和糖醇关键滋味物质,采用顶空固相微萃取-气相色谱-质谱(headspace solid-phase microextraction combined with gas chromatography-mass spectrometry,HS-SPME-GC-MS)联用技术结合气味活性值(odor activity value,OAV)和偏最小二乘判别分析(partial least squares discriminant analysis,PLS-DA)确定泡菜的风味成分和关键香气化合物。以期为提高泡菜的风味和品质提供参考。
1 材料与方法
1.1 材料与试剂
白萝卜、小米椒、生姜、花椒、食盐、蔗糖,市售;膜醭毕赤酵母(Pichia membranifaciens) 1CF3,一种从泡菜中筛选出的好氧型酵母菌,四川东坡中国泡菜产业技术研究院菌种库;MRS培养基、马铃薯葡萄糖琼脂,北京陆桥技术股份有限公司;D-苹果酸、L-乳酸、琥珀酸、乙酸、甲酸、乙醇、葡萄糖和果糖标准品,上海源叶生物科技有限公司;NaCl(分析纯)、NaOH(分析纯)、乙腈(色谱纯)、H2SO4(色谱纯),成都市科隆化学品有限公司。
1.2 仪器与设备
GCMS-TQ8040型气相色谱质谱联用仪、LC-2030型高效液相色谱仪,日本岛津公司;V-1800PC型分光光度计,上海美谱达仪器有限公司;雷磁PHS-3C pH计,上海仪电科学仪器股份有限公司;LC-MS-M1型磁力搅拌器,上海力辰邦西仪器科技有限公司;THZ-C-1型全温振荡器,苏州市培英实验设备有限公司;ESJ200-4A型电子天平,沈阳龙腾电子有限公司;TG-16型高速离心机,四川蜀科仪器有限公司;SW-CJ-1FD超净工作台,江苏苏净集团有限公司。
1.3 实验方法
1.3.1 菌种活化
将实验室保藏的膜醭毕赤酵母1CF3接种于马铃薯葡萄糖液体培养基中,28 ℃下培养48 h,使菌体浓度达到107~108 CFU/mL。马铃薯葡萄糖液体培养基(g/L):马铃薯200,葡萄糖20,121 ℃灭菌20 min。
1.3.2 泡菜的制备与预处理
采用传统四川泡菜的制作方法,参考陈功[15]的方法,并稍作修改。新鲜萝卜清洗干净后晾干,切成1~2 cm的块状,加入2 L玻璃坛中;按照料水质量比1∶1.5添加凉开水,再加入质量分数为5%的食盐、1%的蔗糖、0.5%的小米椒、0.5%的生姜和0.1%的花椒(以料水总质量计)后搅拌均匀,共制备18坛泡菜,分为6个实验组,包括自然发酵(NF)、通气发酵(NF+O)、100 r/min振荡密封发酵组(S)、100 r/min振荡通气发酵组(S+O)、接种膜醭毕赤酵母1CF3密封发酵组(P)、接种膜醭毕赤酵母1CF3通气发酵组(P+O),其中发酵6 d后接种膜醭毕赤酵母1CF3,接种量为1×106CFU/mL。密封发酵采用坛沿加水密封,通气发酵用2层纱布密封玻璃坛坛口,最后于25 ℃发酵。
采用三点取样法分别于发酵0、3、6、9、12 d随机抽取上、中、下层等体积的泡菜液样品,充分混合后作为代表性样品立即进行微生物数量、pH值、总酸含量分析,剩余样品贮藏在-20 ℃待后续分析。
1.3.3 pH值的测定
参考GB 5009.237—2016《食品安全国家标准 食品pH值的测定》,使用pH计测定。
1.3.4 总酸含量的测定
参考GB 12456—2021《食品安全国家标准 食品中总酸的测定(含第1号修改单)》中pH电位法,用0.05 mol/L盐酸标准滴定溶液反滴定至pH 8.2,总酸含量以乳酸计。
1.3.5 微生物数量的测定
参考GB 4789.35—2023《食品安全国家标准 食品微生物学检验 乳酸菌检验》和GB 4789.15—2016《食品安全国家标准 食品微生物学检验 霉菌和酵母计数》对乳酸菌和酵母菌菌落总数进行测定。
1.3.6 有机酸、还原糖和乙醇含量的测定
使用HPLC对泡菜液中的有机酸(苹果酸、琥珀酸、乳酸、乙酸、甲酸)、还原糖(葡萄糖、果糖)和乙醇含量进行测定,参考WANG等[16]的方法稍作修改。取泡菜液2 mL,加入10 mL的超纯水稀释混匀,经200 W超声波处理30 min,12 000 r/min离心10 min后取上清液,上清液经0.22 μm滤膜过滤后上机分析。色谱柱为Carbomix H-NP(7.8 mm×300 mm,10 μm),流动相为2.5 mmol/L H2SO4溶液,柱温55 ℃,流速0.6 mL/min,进样量10 μL,采用紫外检测器(波长210 nm)和示差折光检测器(25 ℃)检测。
1.3.7 挥发性风味物质分析
采用HS-SPME-GC-MS对泡菜液中挥发性风味物质进行测定,参考汪冬冬[17]的方法并进行修改。
样品前处理:在15 mL顶空进样瓶中量取2 mL萝卜泡菜液,加入5 μL内标溶液(0.5 μg/mL 的4-甲基-2-戊醇,溶于甲醇),充分混匀并密封。样品在40 ℃水浴恒温条件下平衡30 min后,将预老化的SPME纤维插入瓶口进行30 min的顶空吸附,随后于250 ℃下热解析5 min。每个样品重复测定2次。
GC条件:采用不分流进样模式,进样口温度设定为250 ℃,进样温度为40 ℃。使用氦气(He)作为载气,流速1.2 mL/min,总流量50 mL/min。色谱柱初始温度设置为40 ℃,随后以16 ℃/min的速率升至75 ℃,保持0 min;然后以2 ℃/min的速率升至94 ℃,保持1 min;再以2 ℃/min的速率升至110 ℃,保持1 min;再以3 ℃/min的速率升至122 ℃,保持1 min;再以2 ℃/min的速率升至130 ℃,保持1 min;再以2 ℃/min的速率升至136 ℃,保持1 min;再以2 ℃/min的速率升至143 ℃,保持1 min;最后以6 ℃/min的速率升至200 ℃,保持5 min。
MS条件:电子轰击离子源,电子能量70 eV,离子源温度230 ℃;接口温度250 ℃;检测器电压0.1 kV;扫描方式为全扫描,扫描质量范围为 35.00~350.00 amu。
定性和定量分析:挥发性风味成分的鉴定基于色谱峰对应的质谱图,并利用NIST17及FFNSC 1.3质谱数据库进行比对,筛选保留匹配度高于80%的化合物作为有效识别结果。半定量分析采用4-甲基-2-戊醇(0.5 μg/mL,溶于甲醇)作为内标物,假设其响应因子为1,进而估算各挥发性组分的相对质量分数。
OAV分析:OAV为物质的质量分数与阈值的比值,按公式(1)计算:
(1)
式中:C,挥发性风味物质的质量分数,mg/kg;T,挥发性风味物质阈值,mg/kg。
1.3.8 数据处理
采用SPSS 22.0软件进行ANOVA分析,多重比较采用最小显著差异(least significant difference,LSD)算法,P>0.05表示差异不显著,0.01<P<0.05表示差异显著,P<0.01表示差异极显著。采用SIMCA 14.1软件进行主成分分析和PLS-DA。
2 结果与分析
2.1 pH值和总酸含量的动态变化
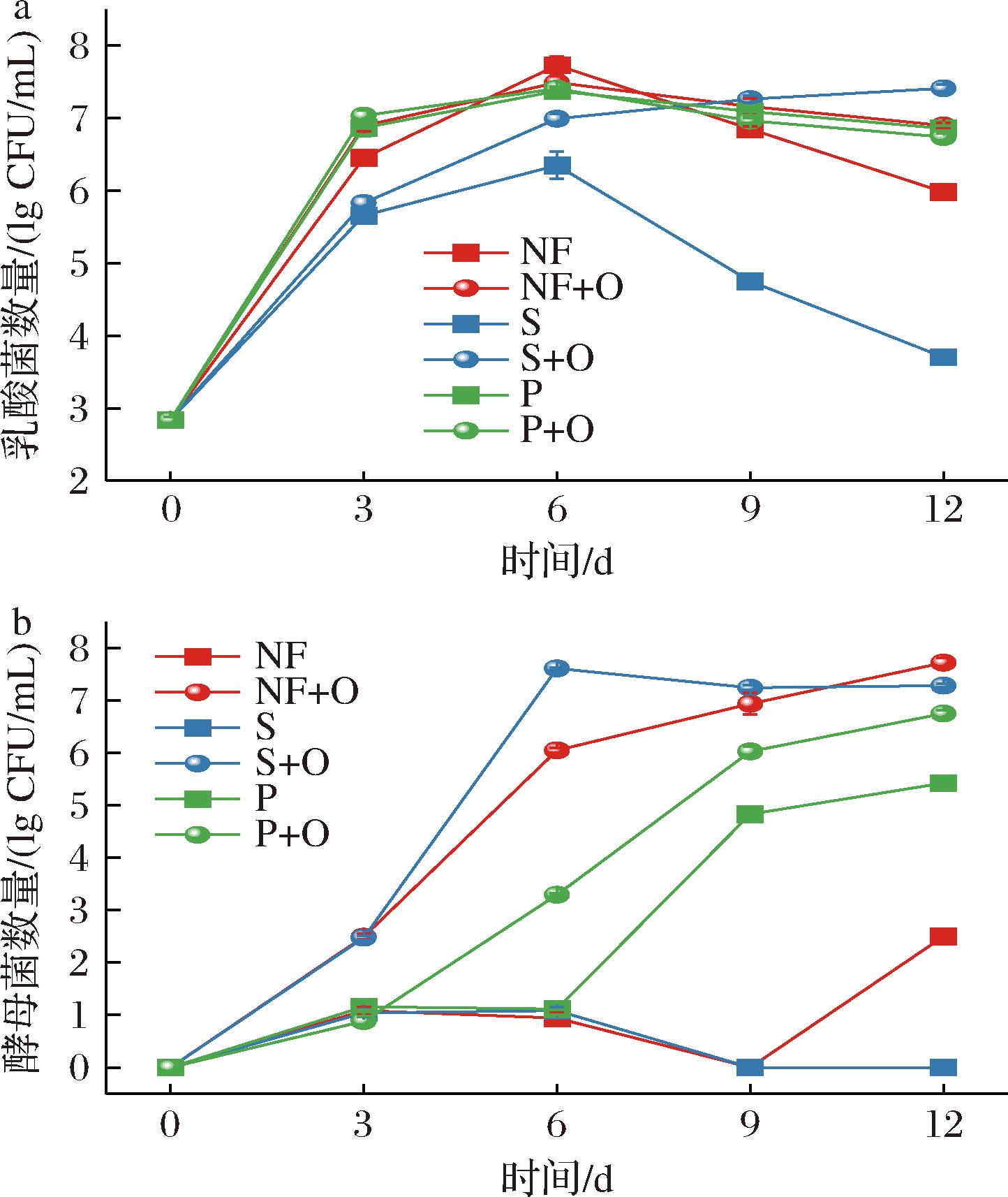
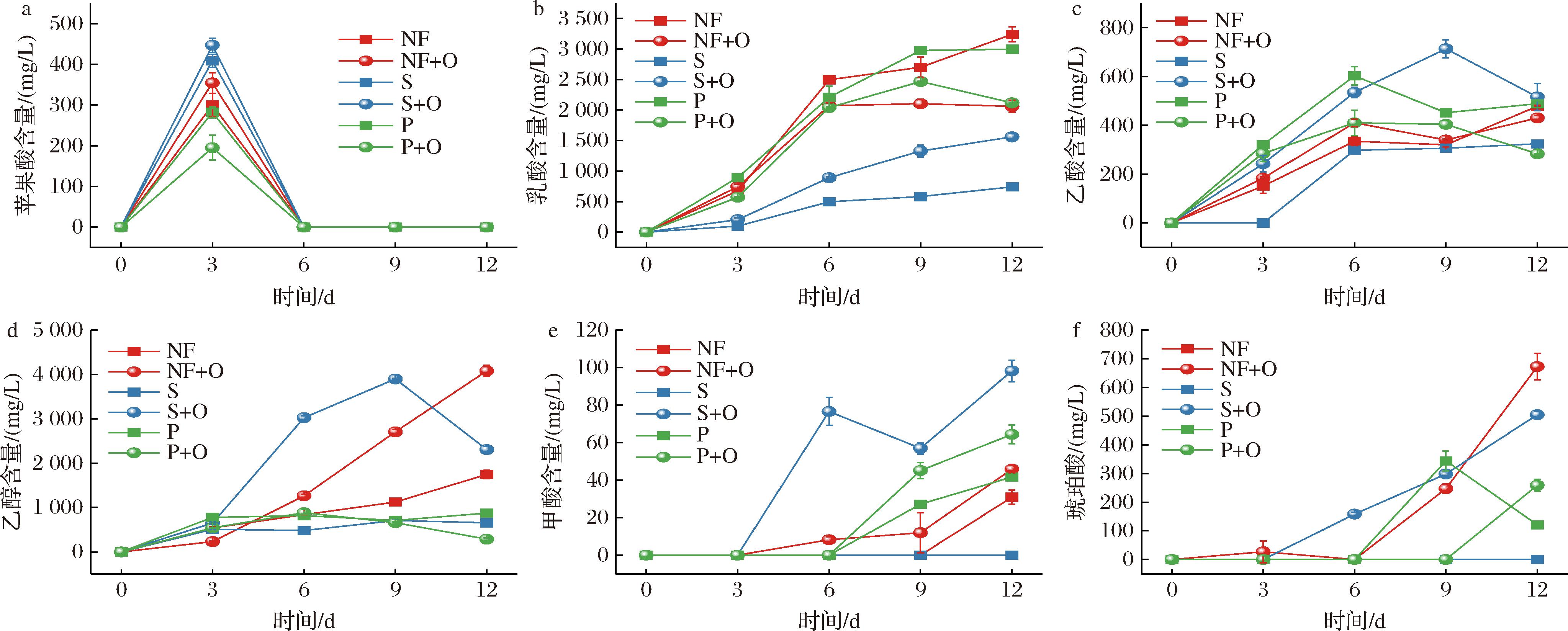
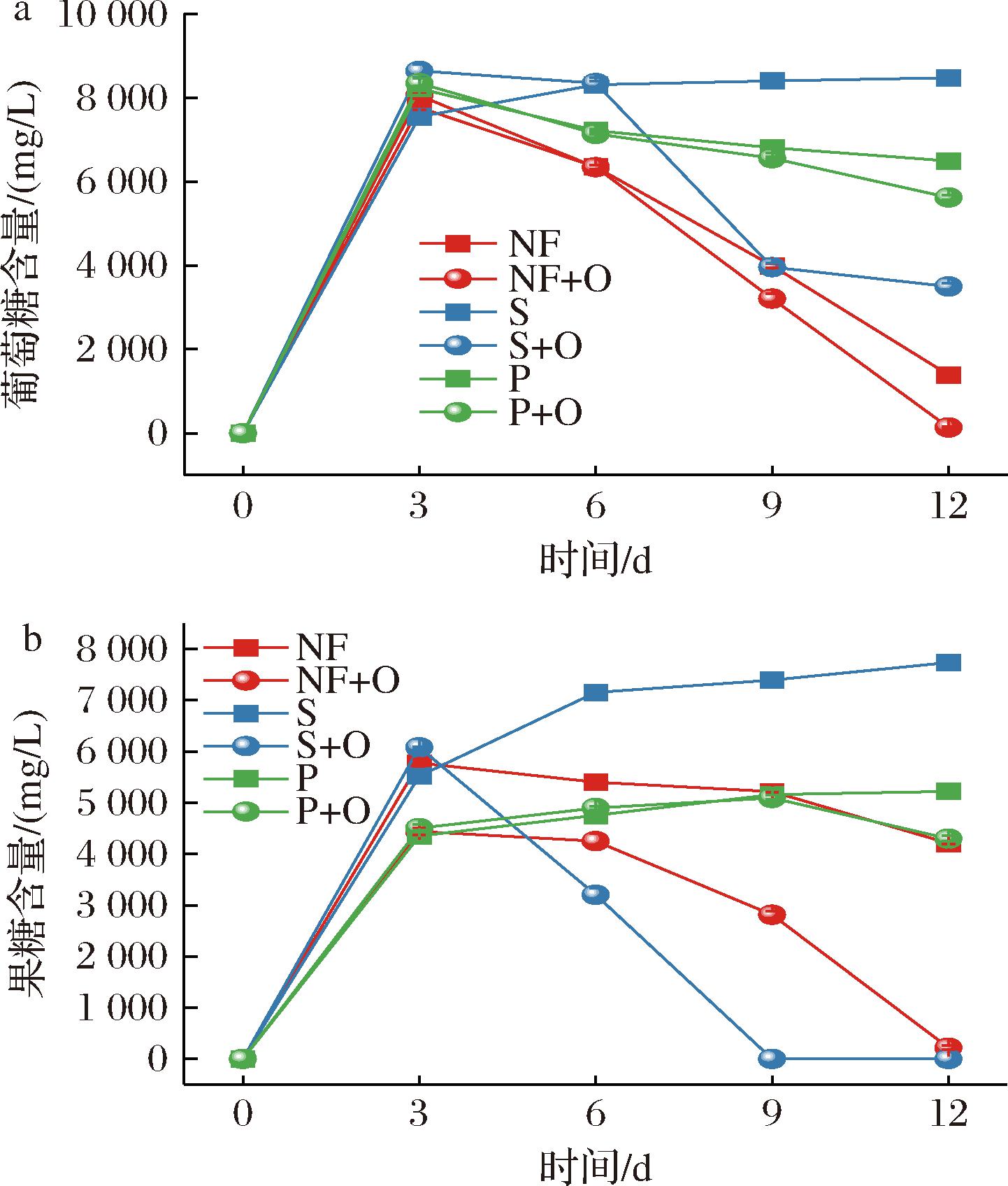
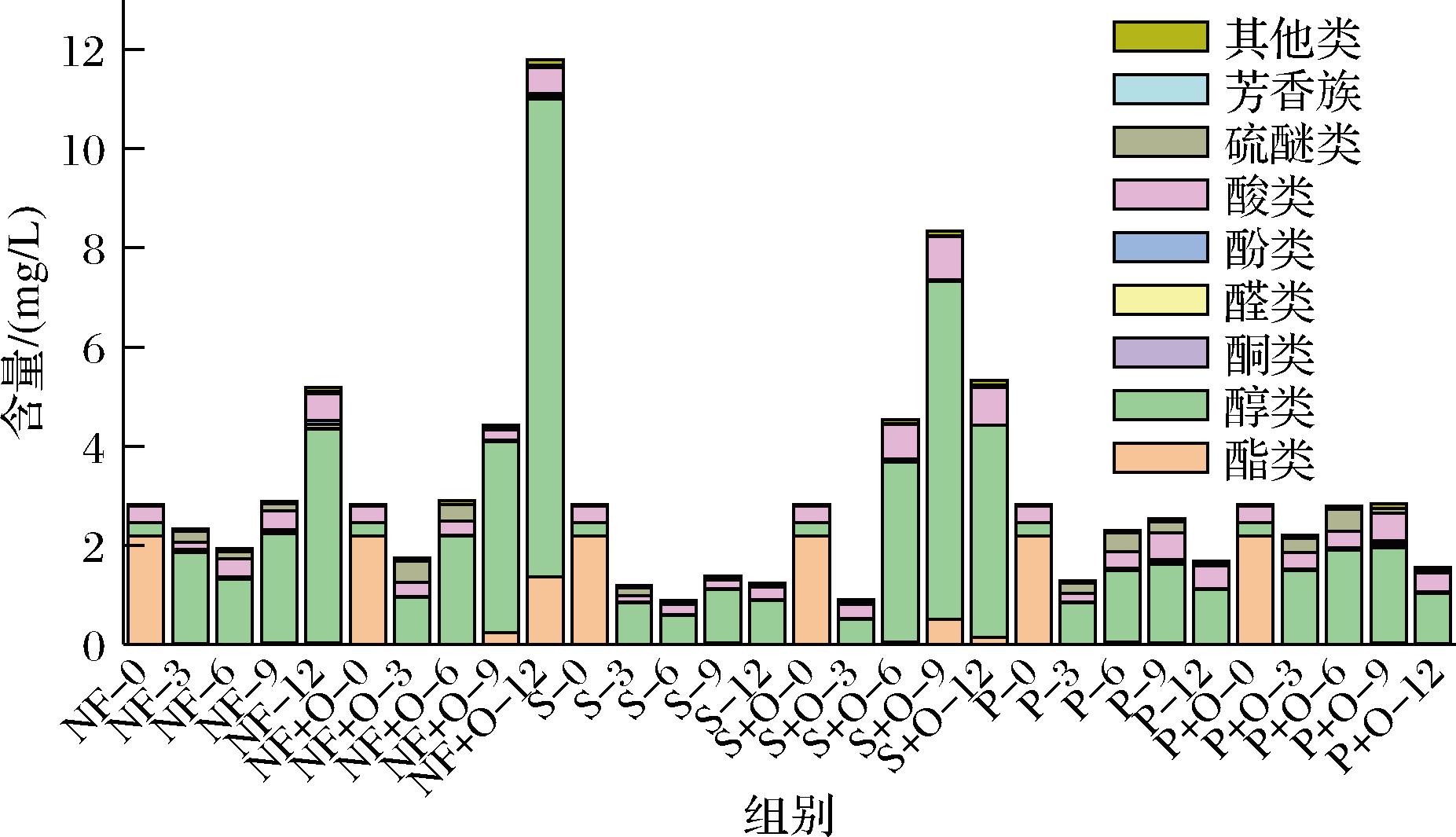
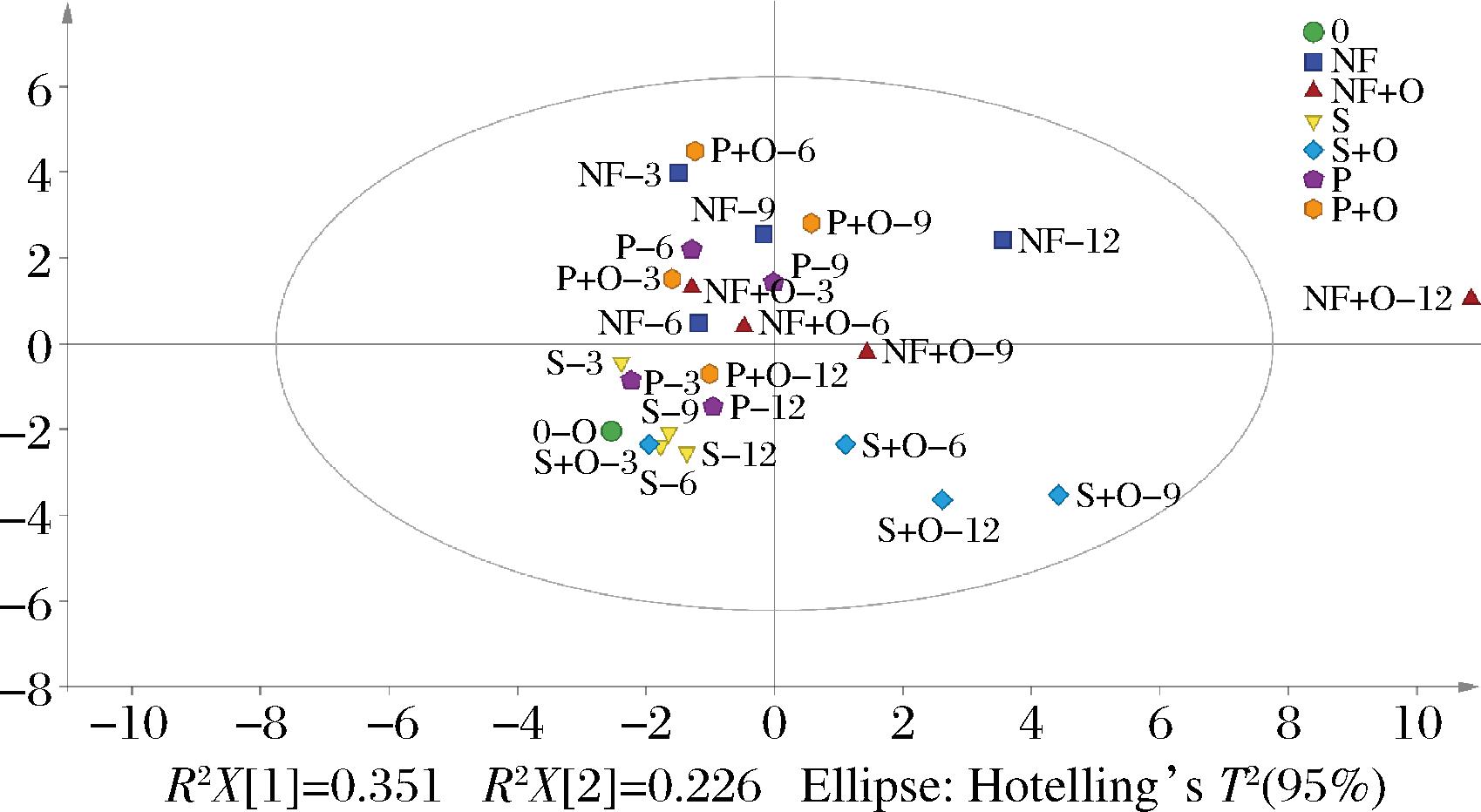
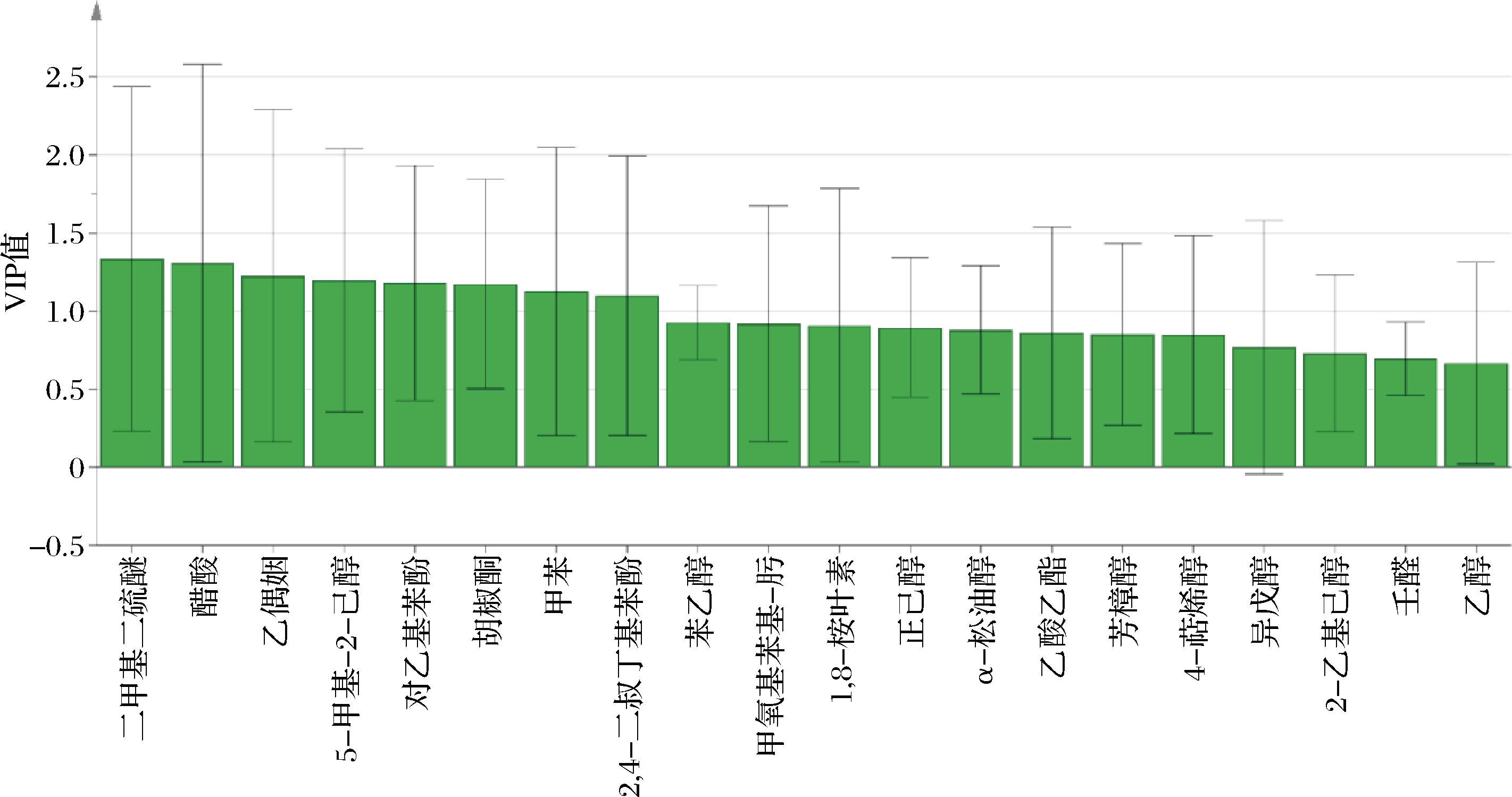
pH值和总酸是泡菜发酵过程中的重要参考指标,也是反映泡菜中微生物代谢活动情况的综合参数[18]。如图1所示,泡菜液中总酸整体呈现不断积累,pH值逐渐降低的趋势。发酵初期(0~3 d)pH值由6.25迅速降低至4.5以下,发酵中后期pH值下降速度减缓,从小到大依次为NF a-pH值;b-总酸含量 图1 不同处理组在发酵过程中萝卜泡菜液总酸和pH值 Fig.1 Total acidity and pH of radish Paocai liquid during fermentation under different treatments 如图2-a所示,泡菜液中的乳酸菌活菌数在发酵前期迅速上升,在中后期开始缓慢下降,除S+O组外,其余发酵组乳酸菌活菌数在6 d时达到峰值,数量大小呈现NF>NF+O>P、P+O>S,S组和NF组在发酵6 d时的乳酸菌活菌数存在极显著差异(P<0.01),分别为(6.35±0.19)、(7.73±0.12) lg CFU/mL。同在发酵中后期(6~12 d)S组的乳酸菌活菌数急剧下降,在发酵后期(12 d)时仅为(3.70±0.08) lg CFU/mL,此时NF组的乳酸菌活菌数为(5.98±0.11) lg CFU/mL,在发酵12 d时S组的乳酸菌活菌数极显著低于NF组(P<0.01)。说明在100 r/min振荡密封条件下,泡菜液中的乳酸菌无法进行正常的生长繁殖。有研究发现,振荡时流体剪切力可能对细菌的生长有一定影响[21]。因此振荡时流体剪切力也可能对乳酸菌的生长产生影响。 a-乳酸菌;b-酵母菌 图2 不同处理组在发酵过程中萝卜泡菜液乳酸菌数量和酵母菌数量 Fig.2 Lactic acid bacteria and yeast counts in radish Paocai liquid during fermentation under different treatments 如图2-b所示,在整个发酵期间,NF+O组和S+O组的酵母菌数量均极显著高于NF组(P<0.01)。其中NF+O组的酵母菌活菌数的峰值出现在12 d时,为(7.72±0.09) lg CFU/mL。说明通气后泡菜中的酵母菌无法被抑制而大量繁殖。接种膜醭毕赤酵母后,P组与P+O组的酵母菌活菌数迅速上升,在12 d时2组酵母菌活菌数都达到峰值,分别为(5.43±0.03) lg CFU/mL和(6.75±0.06) lg CFU/mL,且均极显著高于NF组(P<0.01)。 在9~12 d时,P+O组酵母菌活菌数极显著高于P组(P<0.01)。说明接种膜醭毕赤酵母后,膜醭毕赤酵母利用营养物质大量繁殖,且通气条件下更适合膜醭毕赤酵母生长繁殖。 泡菜中的有机酸含量在很大程度上体现了其发酵动态,是评估其风味表现与成熟度的核心指标[22]。5种有机酸和乙醇含量变化如图3所示。 a-苹果酸;b-乳酸;c-乙酸;d-乙醇;e-甲酸;f-琥珀酸 图3 不同处理组在发酵过程中萝卜泡菜液有机酸和乙醇含量 Fig.3 Organic acid and ethanol contents in radish Paocai liquid during fermentation under different treatments 苹果酸主要来源于泡菜原料本身[23],发酵初期原料中的苹果酸在食盐渗透作用下溢出到泡菜液中,其中S组与S+O组含量较高,超过400 mg/L,均极显著高于NF组(P<0.01),一方面与发酵程度弱有关,另一方面振荡加速了苹果酸从原料中的溢出。随着泡菜发酵的进行,苹果酸被快速消耗,同时乳酸菌可以通过脱氢反应将苹果酸转化为乳酸[24]。 乳酸具有柔和的酸味,是泡菜中主要的有机酸[25]。各发酵组中的乳酸在发酵过程中呈现上升趋势,且在12 d时达到最高含量,其中NF组的乳酸含量达到了(3 240.78±122.15) mg/L,均显著高于其余各组(P<0.05),S组乳酸含量最低,仅为(741.23±17.77) mg/L,在整个发酵过程中S组的乳酸含量均显著低于其余发酵组(P<0.05)。在12 d时,乳酸含量从大到小依次为NF组、P组、P+O组、NF+O组、S+O组、S组,且在整个发酵过程中也大致保持这个趋势。自然发酵乳酸积累较多,振荡发酵乳酸积累较少。说明振荡导致乳酸菌无法生长繁殖,从而导致乳酸积累较少。 乙酸带有愉快的酸香味,可以增加泡菜风味的浓郁程度,也可与相应的醇反应生成酯类物质[26]。各组中乙酸含量总体呈上升趋势,在发酵后期有所波动。NF+O组、S+O组等在发酵初期至中期表现出乙酸的持续上升,尤其是S+O组,其乙酸的质量浓度在9 d达到最高值(713.95±37.05) mg/L。P组和P+O组的乙酸含量在后期明显下降,可能与其他发酵代谢物的生成(如乳酸)和酸度的变化有关,抑制了乙酸的进一步生成。 乙醇与酵母菌的代谢有关,并且乳酸菌在厌氧条件下进行异型发酵会产生乳酸和乙醇[27]。NF+O组乙醇含量逐步上升,在12 d达到了(4 076.41±124.86) mg/L,极显著高于NF组(P<0.01)。S+O组乙醇含量在整个发酵过程中也逐步上升,在6 d和9 d时有较大的上升,并且在12 d时仍保持在较高水平。说明通气处理使酵母菌大量繁殖代谢产生了过量的乙醇。P组和P+O组乙醇含量在6 d后与NF组相比极显著较低(P<0.01),乙醇生成量的减少可能是由于膜醭毕赤酵母与部分产乙醇微生物之间存在竞争作用,进而抑制了乙醇的产生。 甲酸随发酵进行呈上升趋势,主要分布在NF+O、S+O、P和P+O组中,其中在12 d时S+O组甲酸含量最高,达到了(98.24±5.70) mg/L。甲酸具有刺鼻的味道,常出现在腐败食品中,虽然气味难闻,但仍被认为是食品中重要的风味成分。琥珀酸有较浓的苦咸味[28],在NF+O、S+O和P+O组中,琥珀酸含量随着发酵的进行不断上升。而P组中琥珀酸含量则呈现先升后降的趋势。 乳酸与乙酸是泡菜中最主要的有机酸组分,主要来源于乳酸菌对糖类物质的代谢产物[29]。在发酵过程中,这些有机酸的大量生成不仅构成泡菜酸味的核心,同时在调控整体风味感知中亦发挥重要作用,有机酸的组成及其浓度是影响泡菜风味与品质的重要参数。 在泡菜的发酵体系中,葡萄糖和果糖为主要还原糖,主要通过蔗糖的水解作用以及原料细胞质组分的溢出释放产生。这些糖类物质作为微生物代谢所需的基本碳源,驱动有机酸类风味代谢产物(如乳酸和乙酸)的形成[30]。 如图4所示,在发酵过程中,NF+O组和NF组的葡萄糖消耗尤为显著,特别是NF+O组,在较短时间内完全消耗。说明微生物大量利用葡萄糖进行生长代谢从而导致葡萄糖被迅速消耗,NF组和NF+O组的微生物代谢活性较强。NF+O组和S+O组的果糖消耗尤为显著,其中S+O组在短时间内完全消耗。这可能是由于通气处理导致泡菜出现杂菌且大量繁殖消耗碳源。S+O组在葡萄糖消耗上的速度较慢,而果糖的消耗较为显著,可能与外源性有机酸对微生物代谢途径的影响有关。而S组葡萄糖和果糖都未消耗,可能是振荡处理导致微生物代谢活性弱,未能充分利用碳源导致的。P组与P+O组的葡萄糖和果糖消耗较为稳定。 a-葡萄糖;b-果糖 图4 不同处理组在发酵过程中萝卜泡菜液葡萄糖和果糖的含量 Fig.4 Glucose and fructose contents in radish Paocai liquid during fermentation under different treatments 2.5.1 挥发性风味物质种类与含量 利用HS-SPME-GC-MS分析不同处理组发酵过程中萝卜泡菜液的挥发性风味物质,总计检测出34种风味成分,其中NF组32种、NF+O组32种、S组22种、S+O组27种、P组26种、P+O组28种。不同处理发酵过程中萝卜泡菜液挥发性成分种类及相对含量变化如图5所示,共包括10种酯类物质、2种硫醚类物质、2种酸类物质、14种醇类物质、1种酮类物质、1种醛类物质、2种酚类物质、1种芳香化合物及1种其他物质。萝卜泡菜发酵前后挥发性风味物质含量结果见电子版增强出版附表1(https://doi.org/10.13995/jcnki.11-1802/ts.043478,下同),亚油酸甲酯、反油酸乙酯、亚麻酸乙酯、甲基反油酸等在萝卜泡菜发酵前含量相对较高,经过自然发酵后,产生的大量醇类物质和一部分酸类物质,还有少量的酯类、酮类、醛类和硫醚类物质,主要有乙酸乙酯、α-松油醇、异戊醇、2-乙基己醇、4-萜烯醇、乙醇和醋酸。S组与P组经过发酵后产生了部分醇类物质和少量酸类物质,总体风味物质含量减少,并且主体风味物质,如2-乙基己醇、4-萜烯醇、乙醇和醋酸等物质,含量都低于自然发酵。经通气发酵后产生了大量的醇类、部分酸类、酯类物质和少量酮类、醛类和硫醚类物质,与自然发酵组对比发现,通气发酵组的风味物质种类并没有太大变化,但是一部分物质的含量却显著高于自然发酵组,比如乙酸乙酯、异戊醇、2-乙基己醇、苯乙醇和乙醇等。S+O组经发酵后,酯类、醇类和酸类物质也显著高于S组,主要有乙酸乙酯、异戊醇、2-乙基己醇、乙偶姻、苯乙醇、乙醇和醋酸等物质。 图5 不同处理组发酵过程中萝卜泡菜液挥发性成分种类及相对含量变化 Fig.5 Classification and relative content of volatile components in radish Paocai liquid during fermentation under different treatments 不同处理组中挥发性风味物质种类各有差异,其中S组挥发性风味物质种类和含量较少,这与振荡处理导致微生物受到抑制有关,从而发酵产生的风味物质种类和含量较少。NF+O组和S+O组挥发性风味物质含量更多的原因可能是通气处理导致好氧微生物活性增强,发酵产生了大量的醇类风味物质。P组与P+O组则是因为接种膜醭毕赤酵母后与泡菜中原有的微生物竞争,使部分泡菜微生物活性降低,导致发酵产生的风味物质种类减少。 2.5.2 OAV分析 泡菜中挥发性风味物质对整体香气的贡献不仅受其种类和含量影响,还与其气味阈值密切相关。一般认为,OAV>1的化合物对香气具有显著贡献,通常被视为关键风味物质。不同处理组发酵12 d时萝卜泡菜液的关键挥发性风味物质及OAV结果由附表2所示。11种关键挥发性风味物质OAV差异较大,其中NF组关键风味物质OAV高于其他组,S组OAV>1的关键风味物质仅有异戊醇和二甲基二硫醚,正己醇、乙偶姻、芳樟醇、1,8-桉叶素、壬醛、4-乙基苯酚和二甲基三硫醚在NF组中OAV较高,在S组和P组中OAV较低。NF+O组中乙偶姻、芳樟醇、壬醛和二甲基三硫醚的OAV均低于NF组。异戊醇和乙酸乙酯对NF+O组的风味贡献很大。 2.5.3 多元统计分析 采用主成分分析方法进一步对不同处理组萝卜泡菜发酵过程中的主体风味成分进行差异分析,如图6所示,第一主成分贡献率为35.1%,第二主成分贡献率为22.6%,累计贡献率达到57.8%。从图中组别类型来看,NF和P组相近,表明风味物质整体相似,S+O组与其他组距离较远,表明风味差异大。从发酵过程来看,S组样品相对较聚集,说明发酵偏弱,发酵前后风味差异小。其余泡菜组经发酵后样品间距离远,风味差异大。NF组和P组在发酵6~9 d时样品相距较近,表明风味相似,在12 d时样品相距较远,表明在发酵后期风味差异大。而通气组(NF+O)在第12天时与NF样品相距较远,说明风味差异较大。 图6 不同处理组萝卜泡菜发酵过程中的挥发性风味物质主成分分析 Fig.6 Principal component analysis of volatile flavor compounds during fermentation of radish Paocai under different treatments 采用PLS-DA方法对发酵12 d的萝卜泡菜液在不同处理条件下的挥发性组分进行模式识别分析,并通过变量投影重要性(variable importance in projection,VIP)值筛选差异性挥发物质。一般认为,当化合物的VIP值≥1时,其在样品区分及风味特征构建中具有较强代表性与贡献度。结果如图7所示,筛选出VIP值≥1的化合物8种,从大到小依次为二甲基二硫醚、醋酸、乙偶姻、5-甲基-2-己醇、对乙基苯酚、胡椒酮、甲苯和2,4-二叔丁基苯酚。 图7 基于PLS-DA分析不同处理组在12 d时泡菜液中的挥发性风味物质VIP图 Fig.7 VIP plot of volatile flavor compounds in Paocai liquid under different treatments at day 12 based on PLS-DA 二甲基二硫醚具有洋葱的香气,其香气阈值低,低浓度时具有令人愉悦的香味,是泡萝卜的主要风味物质[31],二甲基二硫醚的含量随着发酵时间而降低。醋酸具有柔和的酸味,在12 d时S组中与NF组相比醋酸含量较低,对风味有显著影响。乙偶姻具有强烈的奶油香气,其中NF组和S+O组中乙偶姻含量较高。5-甲基-2-己醇具有果香和青草的芳香气味,是NF+O组中特有的风味物质。对乙基苯酚具有强烈的木香、粉香、烟熏香,并有轻微的甜香香气,主要分布在NF组和NF+O组中。胡椒酮具有辛辣的味道,是由辅料带来的,在所有样品中都有少量分布。甲苯具有强烈的水果味和苦味,是NF+O组中独有的风味物质。2,4-二叔丁基苯酚具有强烈的辛辣气味,是NF组中独有的风味物质。 通过振荡和接种膜醭毕赤酵母(Pichia membranifaciens)模拟泡菜在发酵过程中受到的扰动,同时结合密封及通气2种处理方式发酵泡菜,分析泡菜发酵过程中pH值、总酸、微生物数量、有机酸和挥发性风味物质的变化规律,探究多因素扰动下泡菜风味品质的变化。结果表明,振荡导致泡菜中的乳酸菌无法进行正常的生长代谢,从而使泡菜发酵速度变慢。通气处理和接种膜醭毕赤酵母后泡菜的总酸含量会出现一定程度的下降,并且会使泡菜品质发生劣变。乳酸菌与膜醭毕赤酵母生长具有拮抗作用,乳酸菌在发酵过程中产生大量的酸,使pH值下降,从而能够抑制膜醭毕赤酵母的生长。通过HS-SPME-GC-MS技术共检测出34种挥发性风味物质,通过OAV分析筛选出11种OAV>1的挥发性风味物质,采用PLS-DA和VIP模型筛选出8种差异挥发性风味物质。挥发性风味物质分析结果表明,振荡发酵的泡菜液中挥发性风味物质的种类与含量更少,通气发酵后泡菜液中醇类物质更多,接种膜醭毕赤酵母后泡菜液中的挥发性风味物质种类更少。主成分分析结果表明振荡发酵、通气发酵和接种膜醭毕赤酵母发酵的泡菜与自然发酵的泡菜风味差异较大。振荡、通气和接种膜醭毕赤酵母均会导致泡菜风味变差。 [1] 陈功. 中国泡菜的品质评定与标准探讨[J].食品工业科技, 2009, 30(2):335-338.CHEN G.Quality evaluation and standard discussion of Chinese pickle[J].Science and Technology of Food Industry, 2009, 30(2):335-338. [2] 张锡茹, 关慧, 邢少华, 等.泡菜微生物演替与风味物质变化的研究进展[J].食品科学, 2021, 42(23):294-305.ZHANG X R, GUAN H, XING S H, et al.Advances in research on microbial succession and flavor changes in pickles[J].Food Science, 2021, 42(23):294-305. [3] 张晓, 夏延斌.泡菜风味及其影响因素研究进展[J].中国调味品, 2012, 37(3):32-35;58.ZHANG X, XIA Y B.Research on the pickle’s flavor and factors which effect it[J].China Condiment, 2012, 37(3):32-35;58. [4] 曾瑞. 复合精油微胶囊的制备及在低盐泡菜防腐中的应用[D].武汉:武汉轻工大学, 2024.ZENG R.Preparation of compound essential oil microcapsules and their application in the preservation of low-salt pickles[D].Wuhan:Wuhan Polytechnic University, 2024. [5] 张越. 植物精油天然防腐剂制备及其在发酵蔬菜中的应用研究[D].南昌:南昌大学, 2023.ZHANG Y.Preparation of plant essential oil as natural preservatives and their application in fermented vegetables[D].Nanchang:Nanchang University, 2023. [6] WANG X Y, SONG G, HE Z, et al.Effects of salt concentration on the quality of Paocai, a fermented vegetable product from China[J].Journal of the Science of Food and Agriculture, 2021, 101(15):6202-6210. [7] GE L H, HUANG Y L, LI X, et al.Temperature-driven divergence in molecular distribution and microbial invasion and the associated texture softening during dual-phase fermentation of Paocai[J].Food Chemistry, 2024, 457:140171. [8] 李文斌, 唐中伟, 宋敏丽.韩国泡菜营养价值与保健功能的最新研究[J].农产品加工(学刊), 2006(8):83-84;102.LI W B, TANG Z W, SONG M L.The up to date returns of nutritive value and health protection of corea pickled vegetable[J].Academic Periodical of Farm Products Processing, 2006(8):83-84;102. [9] 郑超, 侯信哲, 陈天花, 等.乳酸菌在蔬菜发酵中的作用机制研究进展[J].中国调味品, 2024, 49(8):205-210.ZHENG C, HOU X Z, CHEN T H, et al.Research progress of action mechanism of lactic acid bacteria in fermentation of vegetables[J].China Condiment, 2024, 49(8):205-210. [10] 王雅利, 赵楠, 葛黎红, 等.酵母菌对发酵萝卜品质的影响[J].食品与发酵工业, 2024, 50(24):68-75.WANG Y L, ZHAO N, GE L H, et al.Effect of yeast on quality of fermented radish[J].Food and Fermentation Industries, 2024, 50(24):68-75. [11] KIM J Y, KIM J, CHA I T, et al.Community structures and genomic features of undesirable white colony-forming yeasts on fermented vegetables[J].Journal of Microbiology, 2019, 57(1):30-37. [12] FAN Z Y, DENG W Q, LI X B, et al.Effect of air exposed storage on quality deterioration and microbial succession of traditional Sichuan Paocai[J].LWT, 2022, 154:112510. [13] AO X L, YAN J L, CHEN C, et al.Isolation and identification of the spoilage microorganisms in Sichuan homemade Paocai and their impact on quality and safety[J].Food Science &Nutrition, 2019, 7(9):2939-2947. [14] ZHANG F, TANG Y, REN Y, et al.Microbial composition of spoiled industrial-scale Sichuan Paocai and characteristics of the microorganisms responsible for Paocai spoilage[J].International Journal of Food Microbiology, 2018, 275:32-38. [15] 陈功. 中国泡菜加工技术[M].北京:中国轻工业出版社, 2011.CHEN G.Processing Technology of Chinese Pickles[M].Beijing:China Light Industry Press, 2011. [16] WANG D D, CHEN G, TANG Y, et al.Study of bacterial community succession and reconstruction of the core lactic acid bacteria to enhance the flavor of Paocai[J].International Journal of Food Microbiology, 2022, 375:109702. [17] 汪冬冬. 发酵温度对甘蓝泡菜细菌和风味的影响及其关联性研究[D].雅安:四川农业大学, 2020.WANG D D.Study on the correlation between fermentation temperature, bacterial community and flavor in cabbage pickles[D].Ya’an:Sichuan Agricultural University, 2020. [18] 汤春梅, 喻淋英, 闵锡祥, 等.四川泡菜生产中微生物多样性与发酵条件优化研究[J].农产品加工, 2024(14):31-37.TANG C M, YU L Y, MIN X X, et al.Analysis on quality safety control measures of production and processing in pickle enterprises[J].Farm Products Processing, 2024(14):31-37. [19] 钱杨, 吴李川, 许童桐, 等.不同空气暴露条件下四川泡菜的品质变化及产植物细胞壁降解酶微生物分析[J].食品工业科技, 2020, 41(13):128-133;147.QIAN Y, WU L C, XU T T, et al.Analysis of quality changes and plant cell wall degrading enzymes producing microorganism in Sichuan pickle under different air exposure conditions[J].Science and Technology of Food Industry, 2020, 41(13):128-133;147. [20] 黄玉立, 葛黎红, 马思尧, 等.乳酸菌与酵母菌互作对萝卜泡菜发酵进程及风味品质的影响[J].中国酿造, 2024, 43(4):197-202.HUANG Y L, GE L H, MA S Y, et al.Effect of the interaction between lactic acid bacterium and yeast on the fermentation process and flavor quality of radish Paocai[J].China Brewing, 2024, 43(4):197-202. [21] 魏焱, 吕锦, 孔敏, 等.振荡频率对变形链球菌生长及黏附的影响[J].现代临床医学, 2012, 38(6):456-458.WEI Y, LÜ J, KONG M, et al.Effects of shaking frequency in growth and adhesion behaviour of Streptococcus mutans[J].Journal of Modern Clinical Medicine, 2012, 38(6):456-458. [22] 黄岩. 多轮发酵豇豆泡菜中生物胺变化规律及其菌株产胺特性研究[D].雅安:四川农业大学, 2023.HUANG Y.Study on the variation of biogenic amines and amine-producing strains in multi-round fermented cowpea pickles[D].Ya’an:Sichuan Agricultural University, 2023. [23] 黄存辉, 朴泓洁, 金清, 等.肠膜明串珠菌发酵对四川泡菜中有机酸生成的影响[J].食品科技, 2018, 43(6):23-28.HUANG C H, PIAO H J, JIN Q, et al.Effects of Leuconostoc mesenteroides fermentation on production of organic acids in Sichuan pickle[J].Food Science and Technology, 2018, 43(6):23-28. [24] 潘海燕, 徐岩, 赵光鳌.苹果酸乳酸发酵的研究进展[J].食品与发酵工业, 2003, 29(11):75-80.PAN H Y, XU Y, ZHAO G A.Progression of malolactic fermentation[J].Food and Fermentation Industries, 2003, 29(11):75-80. [25] 史梅莓, 伍亚龙, 吕鹏军, 等.不同乳酸菌接种发酵对泡白菜理化特征及风味的影响[J].食品与发酵工业, 2024, 50(1):80-88.SHI M M, WU Y L, LYU P J, et al.Effect of different lactic acid bacteria inoculation fermentation on the physicochemical characteristics and flavor of Chinese cabbage pickles[J].Food and Fermentation Industries, 2024, 50(1):80-88. [26] 张入玉. 同/异型发酵乳酸菌筛选及其发酵青菜头缓解结肠炎作用研究[D].重庆:西南大学, 2024.ZHANG R Y.Screening of homo/heterofermentative lactic acid bacteria and their alleviating effects on colitis by fermenting Brassica juncea var.tsatsai[D].Chongqing:Southwest University, 2024. [27] 刘璞, 吴祖芳, 翁佩芳.榨菜腌制品风味研究进展[J].食品研究与开发, 2006, 27(1):158-161.LIU P, WU Z F, WENG P F.Advances of study on flavor of pickled mustard tuber[J].Food Research and Development, 2006, 27(1):158-161. [28] 魏雯丽. 四川工业豇豆泡菜微生物群落结构分析及风味代谢的研究[D].成都:四川大学, 2021.WEI W L.Analysis of microbial community structure and flavor metabolism in industrial fermented cowpea pickles in Sichuan[D].Chengdu:Sichuan University, 2021. [29] 吴昕怡, 朱志妍, 田浩, 等.正交试验设计结合CRITIC、熵权-TOPSIS法研究复配精油对泡菜发酵过程中品质的影响[J].中国调味品, 2025, 50(1):120-126;146.WU X Y, ZHU Z Y, TIAN H, et al.Effects of compound essential oils on the quality of pickles during fermentation based on orthogonal design and CRITIC-entropy-TOPSIS method[J].China Condiment, 2025, 50(1):120-126;146. [30] HUANG Y L, GE L H, LAI H M, et al.Seasonal alteration of environmental condition-driven shift in microbiota composition, physicochemical attributes and organic compound profiles in aged Paocai brine during intermittent back-slopping fermentation[J].Food Bioscience, 2022, 50:102111. [31] 刘树文. 合成香料技术手册[M].北京:中国轻工业出版社, 2009.LIU S W.Handbook of Synthetic Fragrance Technology[M].China Light Industry Press, 2009.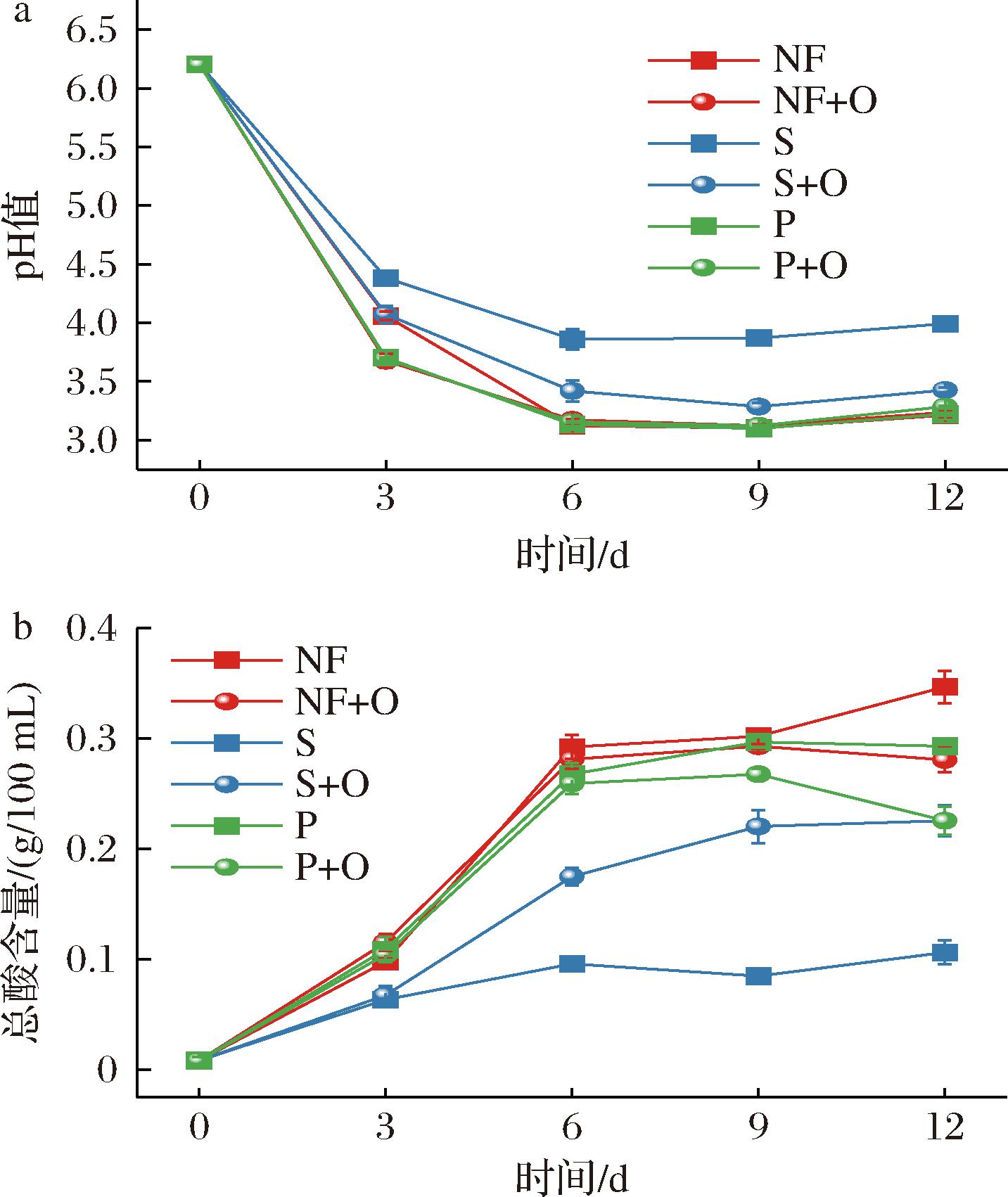
2.2 乳酸菌和酵母菌数量的动态变化
2.3 有机酸和乙醇的动态变化
2.4 还原糖的动态变化
2.5 挥发性风味物质分析
4 结论