四川酸菜作为川菜文化的重要组成部分,其独特的酸香滋味、风味与营养价值深受消费者喜爱。四川酸菜广泛用于各种菜肴中,如酸菜鱼。2022年中国酸菜鱼预制菜市场规模达到103.9亿元,增长态势显著,间接表明四川酸菜的需求量也日益增加[1]。四川酸菜生产逐渐从小规模作坊制作向工业化、规模化生产转变。随着工业化生产规模的扩大,人工接种发酵被认为可以缩短发酵周期、稳定发酵蔬菜产品品质[2]。已有研究多数探讨乳酸菌接种发酵对酸菜品质的影响,例如LEE等[3]、张楠笛等[4]、刘玉凌等[5]均采用多种乳酸菌复合接种,改善酸菜的品质。
然而,相关直投式乳酸菌发酵的研究表明,接种乳酸菌发酵其风味不及自然发酵醇厚,这表明其他微生物群落对酸菜风味仍然至关重要[6]。酵母菌是酸菜微生物体系中的另一典型群体,张文娟等[7]探究酿酒酵母与混合乳酸菌联合发酵对萝卜泡菜品质的影响,结果表明,酿酒酵母可以促进乳酸菌的生长繁殖,促进酸菜中酯类等风味物质的产生,提升酸菜的风味与品质。陈偲等[8]选取植物乳植杆菌J05和酿酒酵母Y21发酵传统泡菜,结果表明,二者可以相互促进生长,泡菜发酵周期短、还原性糖与亚硝酸盐含量较低。目前对酵母菌与乳酸菌联合发酵对酸菜发酵过程中的品质影响仍较为缺乏。
异常威克汉姆酵母(Wickerhamomyces anomalus)是中国白酒酿造中最重要的酯生产菌株之一[9],库德里阿兹威氏毕赤酵母(Pichia kudriavzevii)是一种非糖霉菌酵母,以其增强发酵食品中香气质量的能力而闻名[10]。前期研究探索发现植物乳植杆菌与肠膜明串珠菌对泡菜发酵影响大[6,11],因此,本研究为探究酵母菌与乳酸菌协同发酵对酸菜发酵过程中风味及品质的影响,分别采用W.anomalus与P.kudriavzevii联合植物乳植杆菌(Lactiplantibacillus plantarum)和肠膜明串珠菌(Leuconostoc mesenteroides)发酵,测量酸菜发酵过程中pH值、总酸、质构特性、亚硝酸盐含量、总酯含量、微生物菌落数、氨基酸、有机酸及挥发性成分的变化,并通过主成分分析(principal component analysis,PCA)进一步明确挥发性风味的差异,为工业化生产酸菜的安全性及提升产品品质提供理论依据。
1 材料与方法
1.1 材料与试剂
小叶芥菜、泡菜盐与白砂糖,重庆北碚区永辉超市。L.plantarum(保藏编号:CCTCC M 2025931 VZZ10)、 L.mesenteroides(保藏编号:CCTCC M 2025932 VZZ427)、W.anomalus(保藏编号:CCTCC M 2025930 MZL06),中国典型培养物保藏中心,P.kudriavzevii,西南大学食品科学学院实验室。
NaOH、NaNO2、四硼酸钠、亚铁氰化钾、乙酸锌、对氨基苯磺酸、盐酸萘乙二胺、硫酸、乙酸钠、KH2PO4,成都科龙化工试剂厂;MRS培养基、孟加拉红琼脂、营养琼脂,北京路桥技术股份有限公司;异硫氰酸苯酯、NaH2PO4、酚酞、三乙胺、正己烷、醋酸、磷酸、庚酸甲酯、甲醇、乙腈,重庆钛新化工有限公司。
1.2 仪器与设备
GCMS-QP2010气相色谱质谱联用仪、LC20A高效液相色谱仪,日本岛津公司;PB-10精密pH计,德国Sartorius公司;H1MG酶标仪,美国BioTek公司;CT325K230物性测定仪,美国Brookfield公司;HH-4恒温水浴锅,常州澳华仪器有限公司;5810台式高速离心机,德国Eppendorf公司。
1.3 实验方法
1.3.1 酸菜的制备
酸菜制备工艺:新鲜芥菜→清洗→称重→加入4%(质量分数)的糖与7%(质量分数)的盐配置的糖盐水[m(酸菜)∶m(糖盐水)=1∶2]→调整酸菜水盐度使最终盐度稳定在7%(质量分数)→接菌发酵(L.plantarum接种量为1×108 CFU/mL,L.mesenteroides接种量为1×106 CFU/mL,W.anomalus与P.kudriavzevii接种量为1×105 CFU/mL)→25 ℃恒温发酵[12]。
取第0、2、4、6、8天的酸菜进行分析。设置4个试验组,分别为复配乳酸菌与W.anomalus混合接种发酵 (L+W)、复配乳酸菌与P.kudriavzevii混合接种发酵(L+P)、复配乳酸菌(L.plantarum与L.mesenteroides)接种发酵(L0)、自然发酵(N0)。实时测量质构特性、微生物菌落数和挥发性成分。在酸菜发酵第 0、2、4、6、8 天分别取样,存放于-80 ℃冰箱保存,待测。
1.3.2 pH值和总酸含量的测定
取25 g酸菜与水混合制成匀浆,pH计测定pH值。加入适量纯水,搅碎后沸水浴加热30 min,中途摇动2~3次,结束后冷却至室温,定容后用标准碱液进行滴定得到总酸含量。
1.3.3 质构特性的测定
参考钱杨等[13]的方法,取芥菜样品根茎长宽约25 mm、厚10 mm的样品置于质构仪下进行质构测定。质构测定参数:探头TA44,测试速率1 mm/s,压缩量50%,压缩力7 g。
1.3.4 亚硝酸盐含量的测定
参考GB 5009.33—2025《食品安全国家标准 食品中亚硝酸盐与硝酸盐的测定》,采用盐酸萘乙胺法进行测定。
1.3.5 总酯含量的测定
参考唐蓉等[14]的方法,取50 mL发酵液置入250 mL回流瓶中,加入酚酞指示剂,用0.1 mol/L的NaOH标准溶液滴定至微红色,加入25 mL 0.1 mol/L的NaOH标准溶液,沸水浴回流皂化0.5 h,冷却至室温后立即用0.1 mol/L的硫酸标准溶液滴定,得到总酯含量。
1.3.6 微生物菌落数的测定
参照GB 4789.35—2023 《食品安全国家标准 食品微生物学检验 乳酸菌检验》、GB 4789.15—2016《食品安全国家标准 食品微生物学检验 霉菌和酵母计数》的方法分别进行乳酸菌、酵母菌计数。
1.3.7 游离氨基酸含量的测定
参考经骐源等[12]的方法,略作修改。
氨基酸提取:取烘干粉碎后的酸菜,用0.1 mol/L 盐酸溶解,超声波处理40 min,盐酸定容至25 mL,过滤后取上清液待衍生化处理。
衍生:取上清液200 μL,分别加入衍生剂A(精确量取异硫氰酸苯酯250 μL,用乙腈定容至10 mL)和衍生剂B(精确量取三乙胺1.4 mL,用乙腈定容至10 mL)各100 μL,室温暗处孵育1 h,加200 μL正己烷萃取2次,每次10 min,吸取下层溶液与800 μL水混合,过0.22 μm滤膜。
色谱条件:C18氨基酸专用分析柱(250 mm×4.6 mm,5 μm),流动相A为50 mmol/L无水醋酸钠(pH 6.5),流动相B为甲醇乙腈混合液(甲醇、乙腈、水的体积比为20∶60∶20),流速0.8 mL/min,检测波长254 nm,柱温35 ℃,进样量20 μL,梯度洗脱:0~39 min,100%~95% A;39~40 min,51%~0% A;40~50 min,0% A;50~51 min,0%~95% A;51~60 min,95% A。
1.3.8 有机酸含量的测定
参考经骐源等[12]的方法,略作修改。
有机酸提取:称取5 g酸菜匀浆,加入15 mL 80%(体积分数)乙醇-水溶液,75 ℃水浴0.5 h,纯水定容至25 mL,9 000 r/min离心30 min,准确吸取上清液,经0.22 μm滤膜过滤后待测定。
色谱条件:C18色谱柱(250 mm×4.6 mm,5 μm),紫外检测器,流动相A为0.01 mol/L NaH2PO4-H2O(NaH2PO4和H2O的体积比为3∶97,pH 2.8),流动相B为甲醇,波长210 nm,柱温35 ℃。
1.3.9 挥发性物质成分的分析
参考汪冬冬等[15]的方法,略作修改。准确称取5 g酸菜匀浆于15 mL顶空进样瓶中,加1 g NaCl和5 μL的庚酸甲酯(17.58 g/L)混匀、密封。于75 ℃条件下平衡45 min,将萃取头插入进样瓶中萃取20 min,取出萃取头插入GC-MS进样口解吸5 min。
GC条件:DB-5MS色谱柱(30 m×0.25 mm,0.25 μm);升温程序:初始温度40 ℃,保持3 min,以5 ℃/min速率升至150 ℃,保持3 min,再以10 ℃/min速率升至230 ℃,保持2 min;载气He,流速0.8 mL/min,不分流进样。MS条件:电离方式为电子电离,离子源温度230 ℃,四极杆温度150 ℃,接口温度250 ℃,能量70 eV;质量扫描范围25~450 m/z。
定性和定量分析:由GC-MS得到的色谱图,经计算机在标准谱库NIST 8.0中比对检索,选取相似度>80(最大值为100)的物质进行定性分析,并准确地鉴定出各样品的挥发性成分,同时采用庚酸甲酯(17.58 g/L)为内标进行半定量分析,得到各组分的质量浓度。
1.4 数据处理
采用Excel软件对实验数据统计分析并处理;采用Origin软件绘制图表与PCA作图,并用SPSS软件分析数据之间的差异显著性,P<0.05为具有显著差异;每组质构测定重复8次,其余实验每组重复3次。
2 结果与分析
2.1 不同酵母菌与乳酸菌协同发酵对酸菜pH值与总酸的影响
由图1-a可知,发酵过程中,各组酸菜在发酵第0~6天pH值均显著下降(P<0.05),而后逐渐平稳。L0组pH值全程低于其他组,但发酵结束时,4组pH值为3.21~3.32,组间差异不显著(P>0.05)。如图1-b所示,发酵第0~2天,L+W组、L+P组与N0组总酸含量增长缓慢,第2~8天显著上升(P<0.05)。值得注意的是,L0组最终总酸含量达到(5.10±0.16)g/kg,显著高于其他3组(3.5~3.7 g/kg)(P<0.05)。这与酵母菌和乳酸菌之间的拮抗作用有关,一方面二者存在对脂肪酸与还原糖的竞争关系,不同程度影响各自细胞生长,抑制乳酸菌产酸;另一方面,酵母菌代谢产生的乙醇与乳酸进行酯化反应生成乳酸乙酯,直接降低酸菜中的总酸含量[16-17]。这表明试验的酵母菌与乳酸菌的相互作用有助于缓解发酵过程中乳酸菌继续发酵的过度产酸,从而提升产品品质,延长保质期。
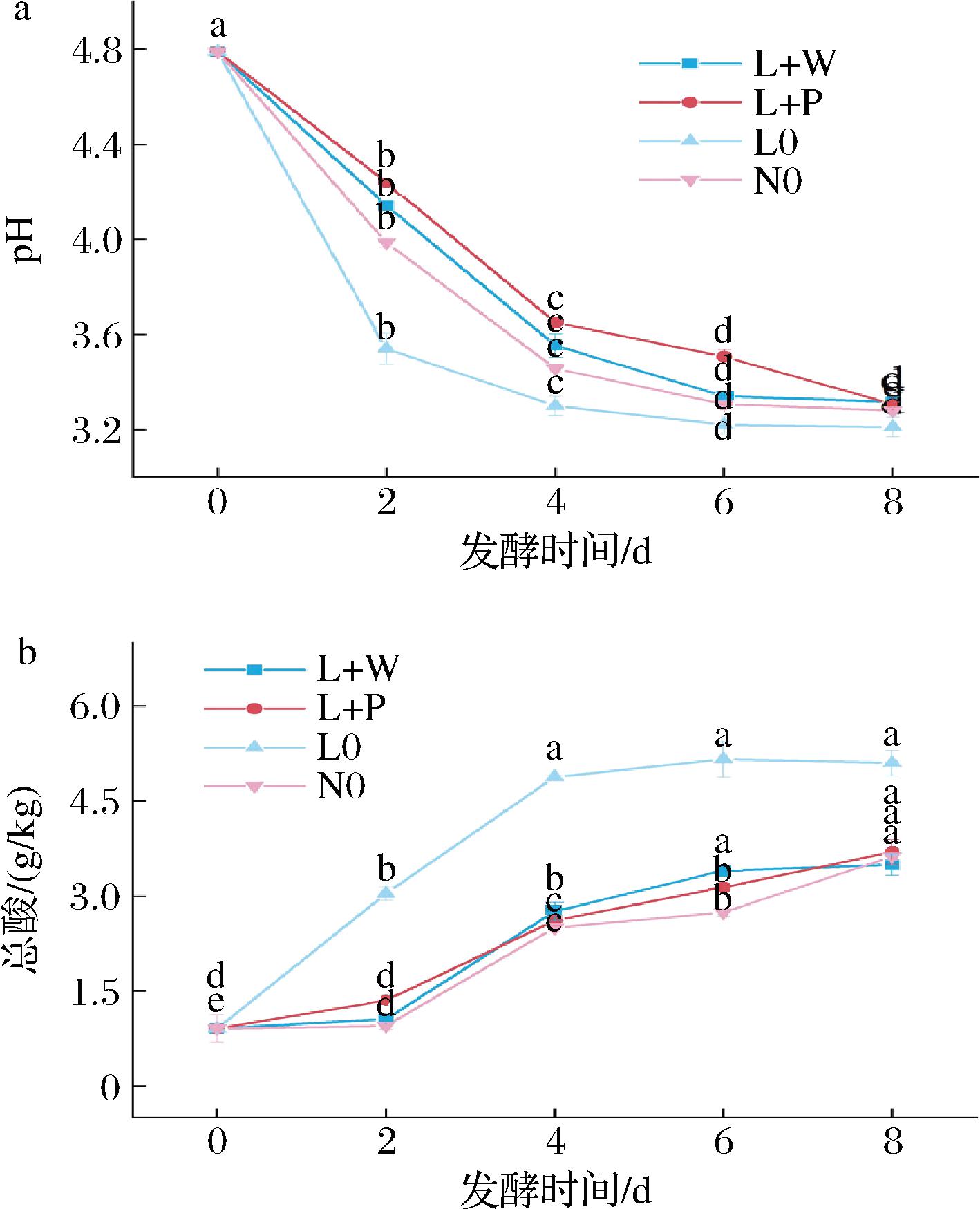
a-pH值;b-总酸含量
图1 发酵过程中酸菜pH值与总酸含量的变化
Fig.1 Changes of pH value and total acid content of pickled cabbage during fermentation
注:不同小写字母表示显著差异(P<0.05)(下同)。
2.2 不同酵母菌与乳酸菌协同发酵对酸菜质构特性的影响
如图2-a所示,除L0组外,其余3组的硬度在发酵全程均表现显著降低的趋势(P<0.05)。L0组在发酵中表现出最低的硬度,这表明乳酸菌的接种能够加速降低酸菜的硬度。原果胶在果胶酶和酸的作用下水解为可溶的果胶酸,使细胞壁中胶层溶解,细胞间黏合力下降,导致硬度下降[18]。发酵第0~6天,L+W组与L+P组硬度高于L0组,说明酵母菌对酸菜发酵过程中质地软化有一定的抑制作用。发酵第8天,4组硬度范围为497~678 g,其中L0组硬度最高,L+P组最低,由图2-b可知,所有处理组的咀嚼性均呈下降趋势,L+W组发酵初期降速最快,发酵第8天达最低值(1.40±0.29)mJ。L0组发酵初期降速最慢,最终维持最高的咀嚼性(2.80±0.21)mJ。
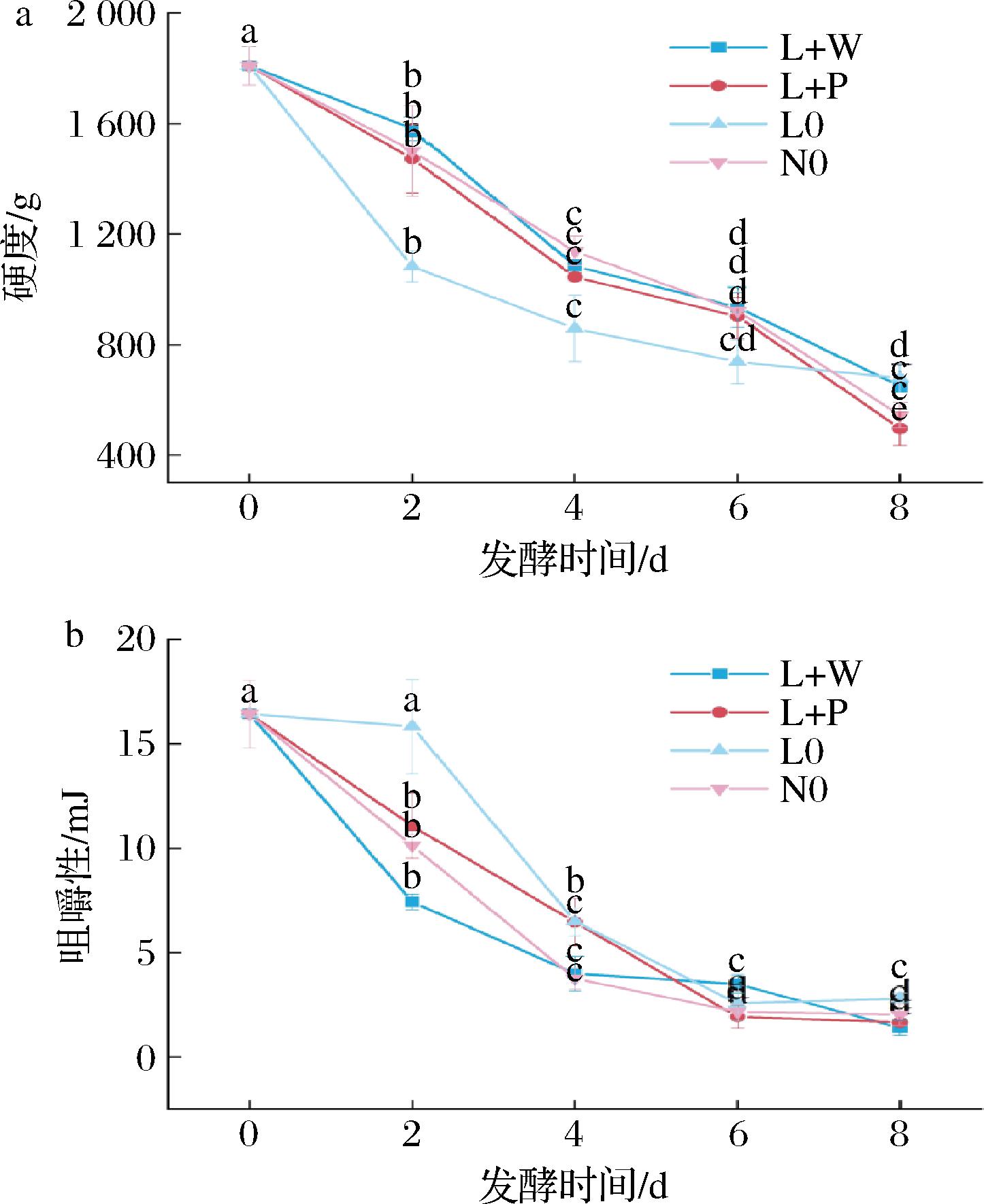
a-硬度;b-咀嚼性
图2 发酵过程中酸菜质构特性的变化
Fig.2 Changes of texture characteristics of pickled cabbage during fermentation
2.3 不同酵母菌与乳酸菌协同发酵对酸菜亚硝酸盐含量与总酯含量的影响
2.3.1 不同酵母菌与乳酸菌协同发酵对酸菜亚硝酸盐含量的影响
亚硝酸盐是评价酸菜食用安全的重要指标[19]。由图3-a可知,发酵第0~2天,除N0组外,其余3组亚硝酸盐含量显著增加(P<0.05),L+P组与L+W组在发酵第2天分别出现亚硝峰(2.87 mg/kg和1.37 mg/kg),而N0组亚硝酸含量略微下降。发酵第2~4天,L0组在第2天出现亚硝峰(3.82 mg/kg),N0组亚硝酸盐含量显著增加(P<0.05)。发酵第4~6天,L+P组与L0组亚硝酸盐含量显著降低(P<0.05),N0组在发酵第6天达到峰值(3.55 mg/kg),而L+W组变化始终保持平稳。发酵过程中,蔬菜原料中的硝酸盐被微生物还原为亚硝酸盐,亚硝酸盐含量随时间逐渐增加,而乳酸菌在发酵中逐渐成为优势菌群,通过产酸、产酶和乳酸菌素降解等方式有效降低亚硝酸盐[19]。相较于L0组与N0组,L+P组与L+W组亚硝峰值相对较低,表明乳酸菌与酵母菌的混合接种可以有效降低亚硝酸盐的生成。这与WU等[20]的研究结果相似。发酵过程中所有试验组亚硝酸盐含量均低于国家标准限量20 mg/kg。
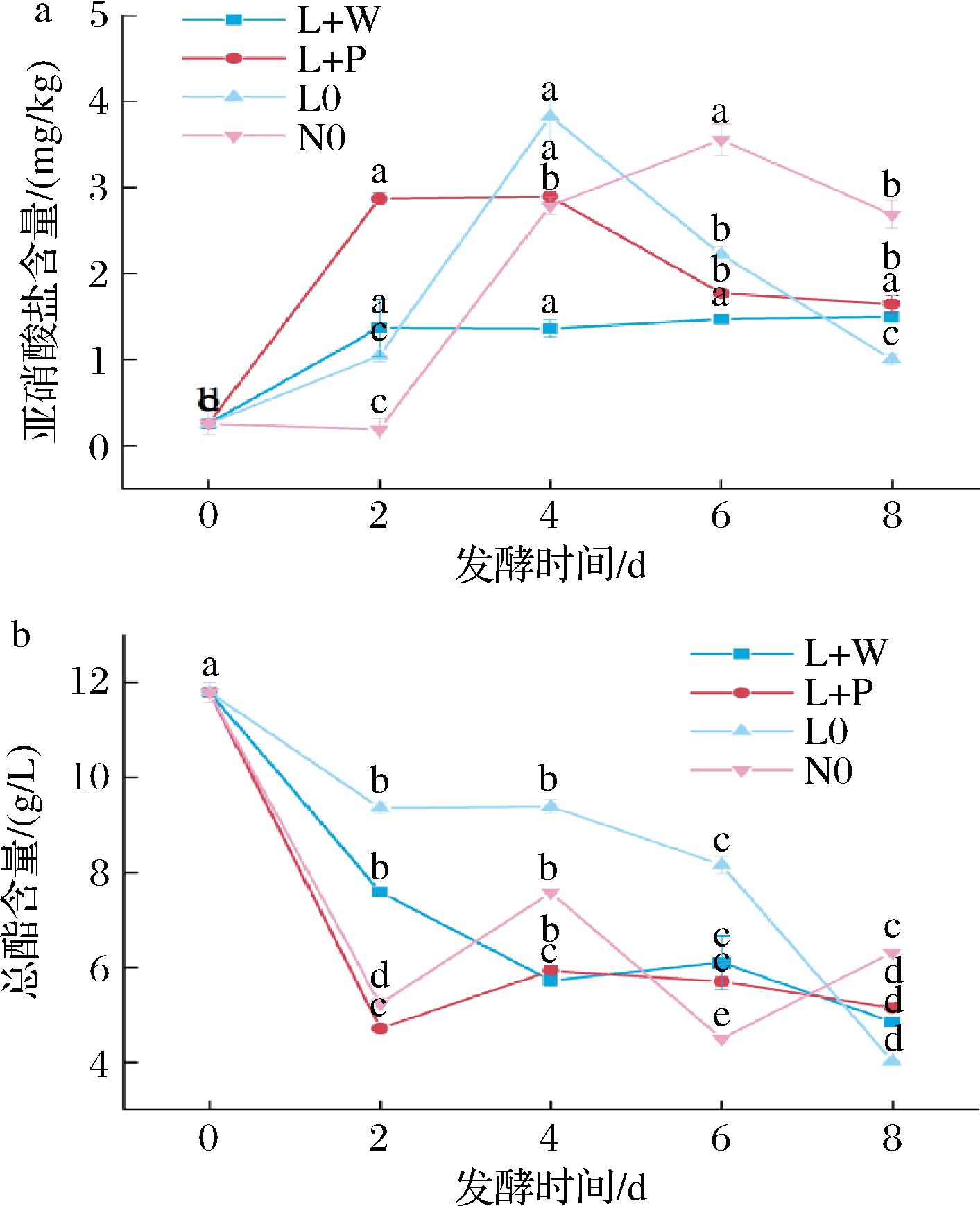
a-亚硝酸盐含量;b-总酯含量
图3 发酵过程中酸菜亚硝酸盐含量和总酯含量的变化
Fig.3 Changes of nitrite content and total ester content in pickled cabbage during fermentation
2.3.2 不同酵母菌与乳酸菌协同发酵对酸菜总酯含量的影响
总酯含量是产香酵母产酯总量的直接衡量标准,是酸菜风味的关键指标[21]。如图3-b所示,发酵第0~2天,所有试验组总酯含量均显著减少(P<0.05),这意味着挥发性酯类物质的快速生成。发酵过程中L+P组与L+W组的总酯含量始终低于L0组,这表明酵母菌与乳酸菌联合发酵可以加快风味化合物的富集。发酵第2~4天L0组总酯含量变化较平稳,第4~8天显著减少(P<0.05),而其余3组在整个发酵过程中均出现总酯含量回升的现象,这是由于总酯合成的速率超过了挥发性损失。随着总酸含量的积累,酵母菌在发酵过程中产生醇类物质与之结合增加了酯类物质的合成,而乳酸菌的代谢物质为酵母菌提供碳源,促进了酵母菌的生长和代谢,从而进一步增加了酯类物质的合成[16]。N0组总酯含量在发酵过程中呈波动变化,这归因于自然发酵体系中微生物群落组成的复杂性和多变性。
2.4 不同酵母菌与乳酸菌协同发酵对酸菜微生物菌落数的影响
如图4-a所示,发酵初期所有试验组的乳酸菌菌落数均增加,其中N0组的乳酸菌菌落数增长最显著(P<0.05)。发酵第8天,N0组乳酸菌菌落数最高,L0组次之。酸菜发酵时乳酸不断积累,此时乳酸菌自身的生长出现抑制作用,导致发酵后期乳酸菌增长速率缓慢甚至抑制生长。此外,酵母菌通过竞争碳源、代谢乙醇影响乳酸菌的细胞结构产物,抑制乳酸菌的生长[16]。自然发酵过程中其他微生物之间可能形成了复杂的代谢网络和相互作用,促进乳酸菌的生长维持较高水平[22]。如图4-b所示,发酵前后L0组与N0组的酵母菌菌落数显著增加(P<0.05),L+P组酵母菌菌落数显著减少(P<0.05),而L+W组变化不显著(P>0.05)。发酵第8天,L0组与N0组的酵母菌菌落数高于L+W组与L+P组。这在乳酸菌当中也有相同的现象,这说明酵母菌的存在可以促进乳酸菌的生长。这是因为乳酸菌与酵母菌存在着代谢互补机制,酵母产生的代谢物质能诱导乳酸菌中氨基肽酶的合成,使氨基酸含量增加,乳酸菌利用其促进自身的生长[16]。此外,酵母自溶产生的吡喃甘露糖可以吸收中链脂肪酸,解除其对乳酸菌的毒害作用,还可能增加乳酸菌的α-葡萄糖苷酶、β-葡萄糖苷酶、N-乙酰-β-葡萄糖脱水酶及肽酶的活性,提供稳定碳源,促进乳酸菌的生长[23]。而乳酸菌可以代谢乳酸形成乳酸盐为酵母菌提供碳源、还可以分解乳糖,所产生的葡萄糖也可被酵母菌利用[16]。L+W组与L+P组的乳酸菌与酵母菌菌落数水平在发酵后期均明显低于N0组。这是因为直投式接菌使得2组微生物群落优劣差异明显,乳酸菌和酵母菌之间的竞争更加直接突出。
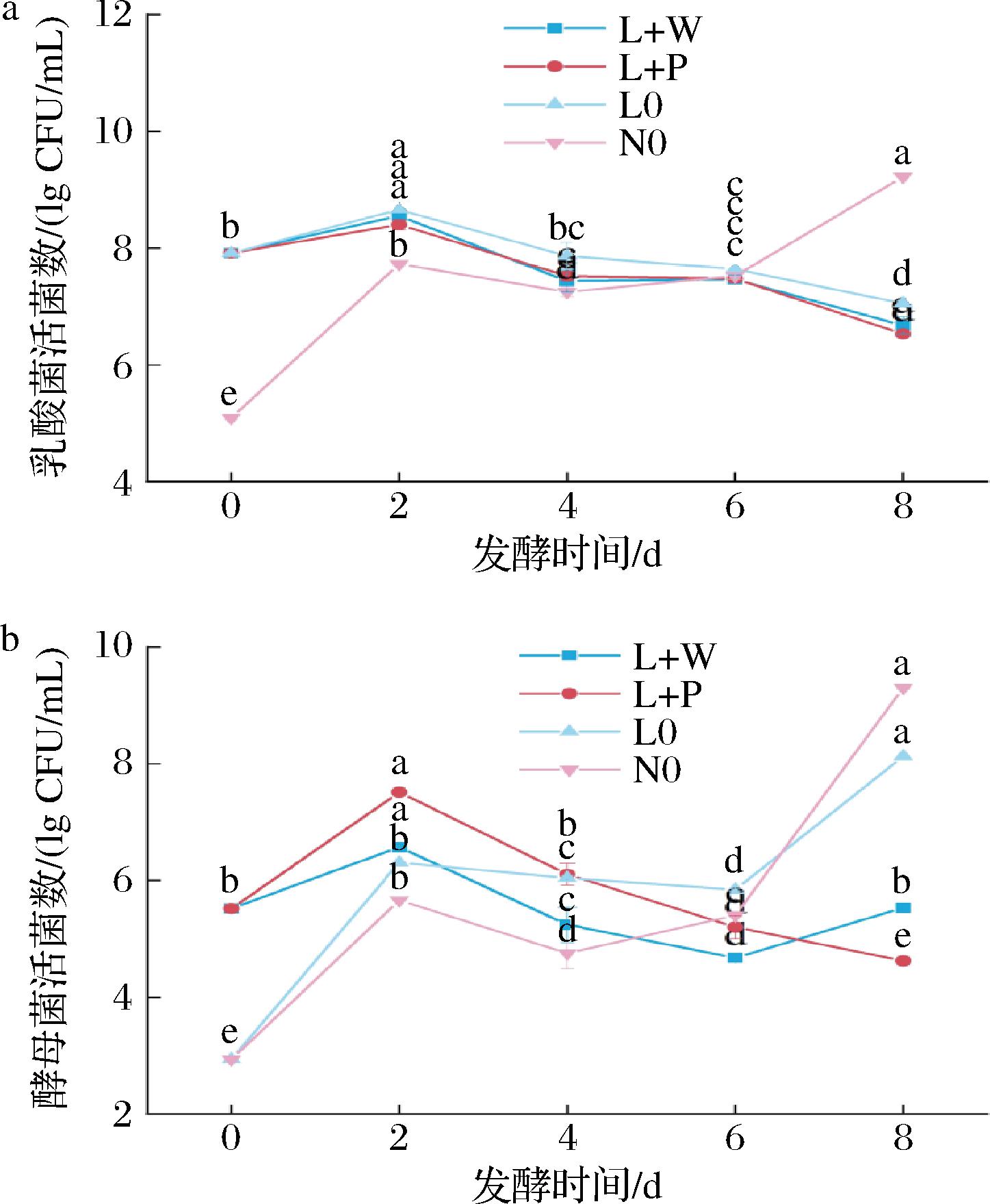
a-乳酸菌活菌数;b-酵母菌活菌数
图4 发酵过程中酸菜微生物菌落数的变化
Fig.4 Variation of microbial colony number of pickled cabbage during fermentation
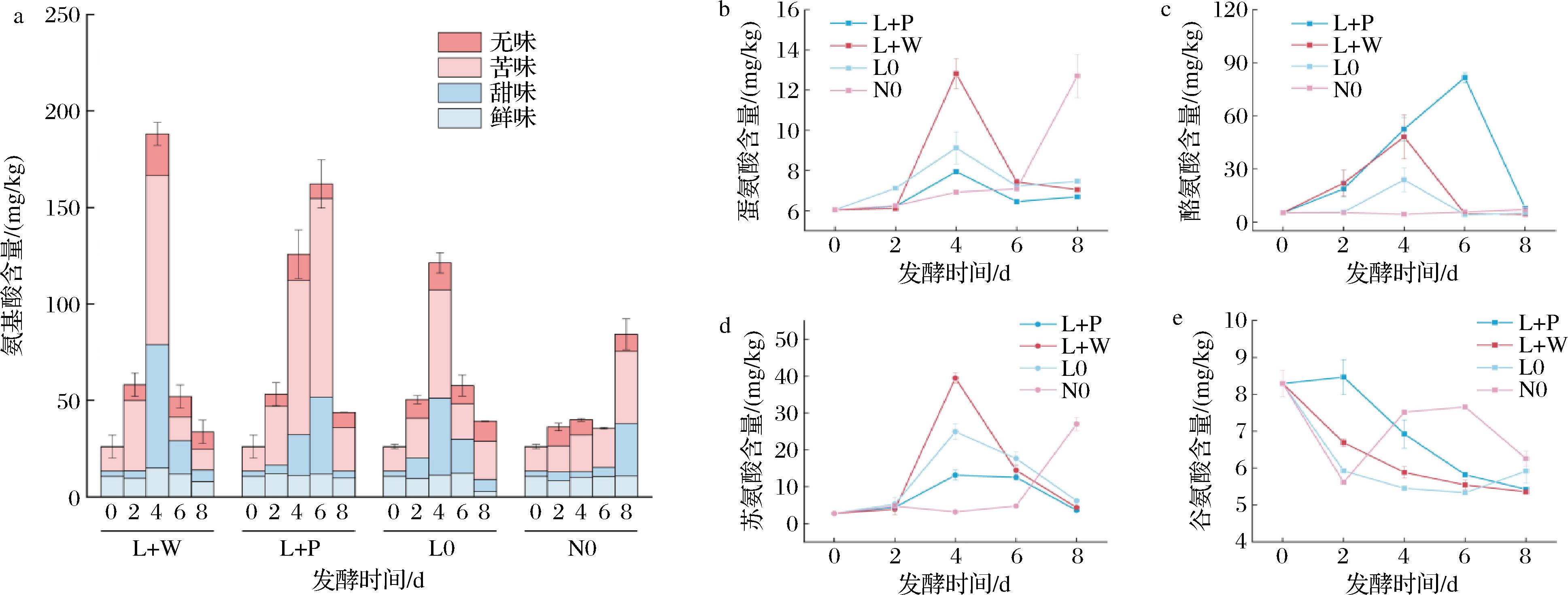
a-氨基酸的总含量;b-蛋氨酸含量;c-酪氨酸含量;d-苏氨酸含量;e-谷氨酸含量
图5 发酵过程中酸菜游离氨基酸的变化
Fig.5 Changes of free amino acids in pickled cabbage during fermentation
2.5 不同酵母菌与乳酸菌协同发酵对酸菜游离氨基酸的影响
在所有样本中共检测到3种甜味氨基酸(Ala、Ser、Thr)、2种鲜味氨基酸(Glu、Asp)、7种苦味氨基酸(Leu、Ile、Met、Lys、Tyr、Phe、Val)、2种无味氨基酸(Cys、Pro)。如图5-a所示,L+W组、L+P组与L0组的氨基酸总量呈先上升后下降的趋势,其中L+W组的氨基酸总量峰值最高。发酵前后N0组氨基酸总量呈上升的趋势,但氨基酸总量峰值最小。然而,发酵第8天,L+W组、L+P组与L0组的氨基酸总量低于N0组。氨基酸是乳酸菌生长代谢的重要营养物质,接菌发酵过程中,乳酸菌消耗更多基质中的氨基酸,而酵母菌的引入可通过分泌蛋白酶促进蛋白质的降解,进一步累积游离氨基酸。酸菜发酵过程中,苦味氨基酸占比最高,其中苦味氨基酸中以酪氨酸与蛋氨酸为主。如图5-b、图5-c所示,L+W组蛋氨酸与L+P组酪氨酸在发酵过程中迅速增加后又被大量消耗,N0组蛋氨酸含量持续累积。酪氨酸与蛋氨酸是细菌繁殖生长重要的营养来源,发酵初期蛋白质被分解为氨基酸,氨基酸含量增加,而后酪氨酸经催化脱氨生成对羟基苯丙酮酸,进一步转化为α-酮酸,再氧化脱羧生成醛类和羧酸,含量减少,而蛋氨酸作为含硫化合物的前体,均可以赋予酸菜独特香气[24]。甜味氨基酸以苏氨酸为主,如图5-d所示,L+W组苏氨酸含量最高达到39.46 mg/kg,N0组含量整体呈上升趋势。苏氨酸可通过酶促反应转化为异亮氨酸,进而在支链氨基酸转氨酶催化下转化为对应的α-酮酸,最终转化为挥发性醇类物质[25]。由此发现,酵母菌可以提高酸菜在发酵过程中苦味与甜味氨基酸的含量。如图5-e所示,除N0组外,其余处理组谷氨酸含量呈下降趋势,其中L+W组下降水平最低,N0组谷氨酸含量呈波动变化。发酵过程中无味氨基酸占比较小,变化不大。
2.6 不同酵母菌与乳酸菌协同发酵对酸菜有机酸的影响
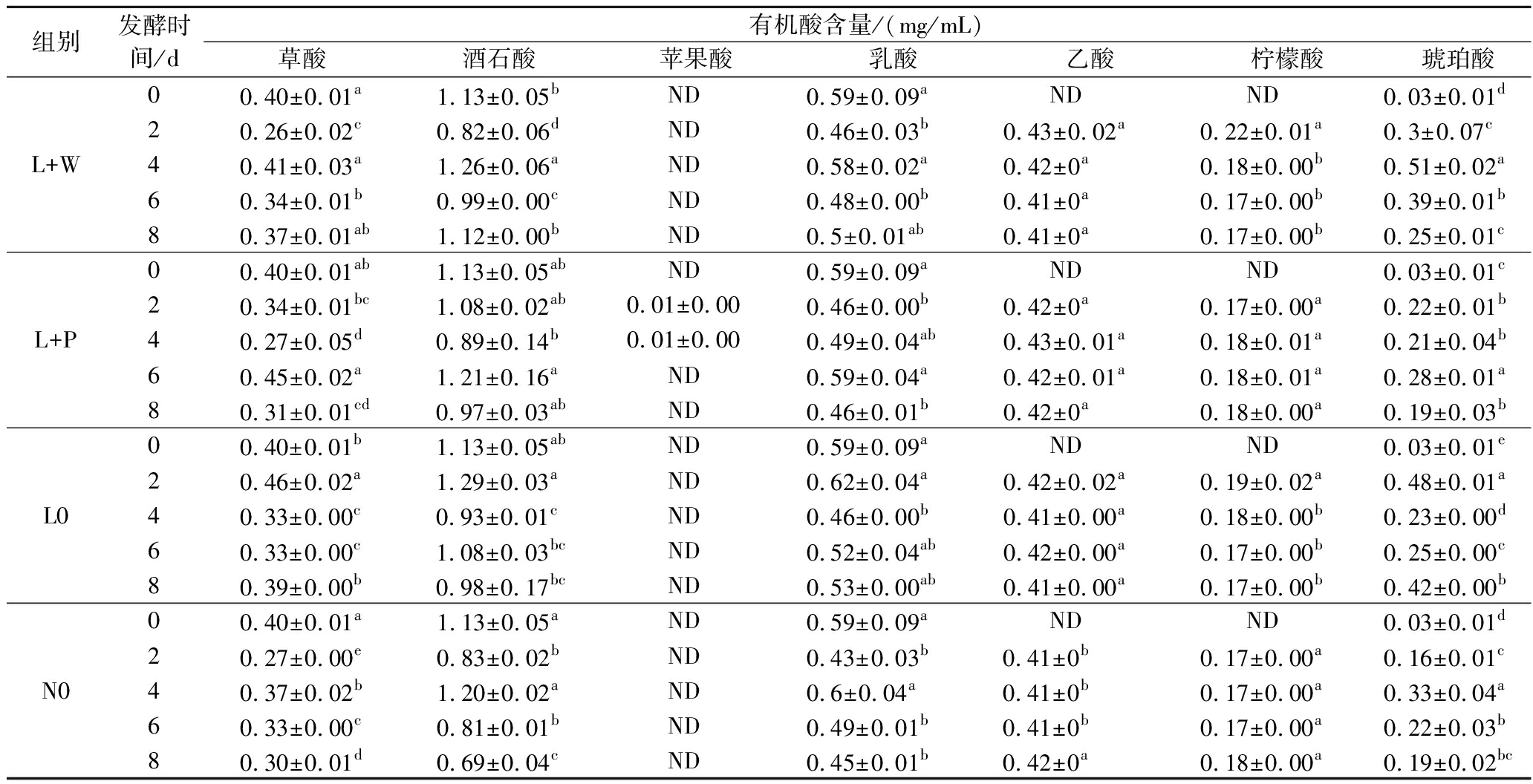
有机酸的成分与含量是酸菜酸味的重要因素。共7种有机酸,包括草酸、酒石酸、乳酸、乙酸、琥珀酸、柠檬酸、苹果酸。如表1所示,酸菜中主要有机酸是酒石酸(1.13 mg/mL)、乳酸(0.59 mg/mL)和乙酸(0.42 mg/mL),这与ZHANG等[26]的研究结果相似。L+W组、L+P组与L0组的酒石酸含量发酵第8天含量差异不显著(P>0.05),N0组的酒石酸含量显著下降至(0.69±0.04)mg/mL(P<0.05)。酒石酸味道醇和,接菌组酒石酸含量的增加促进酸菜风味的提升。乳酸赋予温和的酸味,乙酸赋予刺激性的酸味,均促进酸菜风味的形成[24]。L+P组与N0组乳酸含量发酵第8天显著下降(P<0.05)。发酵第0天,酸菜中乙酸与柠檬酸含量低于检测限值。随着发酵进行,所有试验组乙酸和柠檬酸含量分别显著增加至0.41~0.43 mg/mL与0.17~0.22 mg/mL(P<0.05),而后均保持稳定。乳酸和乙酸通常由大多数乳酸菌产生,而柠檬酸的积累可能与一些真菌群落相关[27]。除L0组外,其余3组琥珀酸含量呈现先增后减的趋势,发酵末期L0组远高于其余试验组。乳酸菌将酒石酸转化为草酰乙酸,草酰乙酸进一步用于三羧酸循环,从而产生琥珀酸代谢产物[28]。仅在L+P组发酵中期检测到苹果酸的存在,苹果酸是生物体代谢三羧酸循环的中间体,随着发酵进行,苹果酸被分解为乳酸等物质。这说明L+P组乳酸菌与酵母菌发生拮抗作用较强,乳酸菌代谢活动较弱,苹果酸分解较慢。
表1 发酵过程中酸菜有机酸的变化
Table 1 Changes of organic acids in pickled cabbage during fermentation
组别发酵时间/d有机酸含量/(mg/mL)草酸酒石酸苹果酸乳酸乙酸柠檬酸琥珀酸L+W00.40±0.01a1.13±0.05bND0.59±0.09aNDND0.03±0.01d20.26±0.02c0.82±0.06dND0.46±0.03b0.43±0.02a0.22±0.01a0.3±0.07c40.41±0.03a1.26±0.06aND0.58±0.02a0.42±0a0.18±0.00b0.51±0.02a60.34±0.01b0.99±0.00cND0.48±0.00b0.41±0a0.17±0.00b0.39±0.01b80.37±0.01ab1.12±0.00bND0.5±0.01ab0.41±0a0.17±0.00b0.25±0.01cL+P00.40±0.01ab1.13±0.05abND0.59±0.09aNDND0.03±0.01c20.34±0.01bc1.08±0.02ab0.01±0.000.46±0.00b0.42±0a 0.17±0.00a0.22±0.01b40.27±0.05d0.89±0.14b0.01±0.000.49±0.04ab0.43±0.01a0.18±0.01a0.21±0.04b60.45±0.02a1.21±0.16aND0.59±0.04a0.42±0.01a0.18±0.01a0.28±0.01a80.31±0.01cd0.97±0.03abND0.46±0.01b0.42±0a0.18±0.00a0.19±0.03bL000.40±0.01b1.13±0.05abND0.59±0.09aNDND0.03±0.01e20.46±0.02a1.29±0.03aND0.62±0.04a0.42±0.02a0.19±0.02a0.48±0.01a40.33±0.00c0.93±0.01cND0.46±0.00b0.41±0.00a0.18±0.00b0.23±0.00d60.33±0.00c1.08±0.03bcND0.52±0.04ab0.42±0.00a0.17±0.00b0.25±0.00c80.39±0.00b0.98±0.17bcND0.53±0.00ab0.41±0.00a0.17±0.00b0.42±0.00bN000.40±0.01a1.13±0.05aND0.59±0.09aNDND0.03±0.01d20.27±0.00e0.83±0.02bND0.43±0.03b0.41±0b 0.17±0.00a0.16±0.01c40.37±0.02b1.20±0.02aND0.6±0.04a0.41±0b0.17±0.00a0.33±0.04a60.33±0.00c0.81±0.01bND0.49±0.01b0.41±0b0.17±0.00a0.22±0.03b80.30±0.01d0.69±0.04cND0.45±0.01b0.42±0a0.18±0.00a0.19±0.02bc
注:“ND”表示未检测到。不同小写字母表示显著差异(P<0.05)。
2.7 不同酵母菌与乳酸菌协同发酵对酸菜挥发性物质的影响
挥发性物质是酸菜风味的重要来源。本研究共测得挥发性物质101种,其中酯类30种、酸类5种、醇类20种、醛类20种、酮类10种、烃类5种、酚类5种、醚类1种、其他类5种。如图6-a所示,发酵后所有处理组挥发性物质总量增加,发酵第8天,N0组的挥发性物质含量最高,其次是L+W组,L+P组挥发性物质含量最低。酯类物质是酸菜中重要的风味成分。酯类在酸菜发酵过程中表现出最高的相对含量(32.75%~60.33%),其中异硫氰酸酯类占酯类较大占比,主要包括异硫氰酸烯丙酯、异硫氰酸丁酯、异硫氰酸苯乙酯。异硫氰酸酯类是十字花科植物及其发酵成品特有的风味物质,阈值较低,呈现辛香味[24]。其余酯类(如棕榈酸乙酯、多不饱和脂肪酸甲酯等)贡献果香与花香[4]。接菌组间对比显示,发酵第8天L+W组酯类含量高于L0组,但低于N0组,表明酵母菌与乳酸菌协同作用可增强挥发性酯类合成,而自然发酵积累更高。醇类物质通过原料中蛋白质与氨基酸的降解、酵母代谢与乳酸异型发酵持续积累[16,19],含量显著增加(P<0.05)。醇类主要包含苯乙醇、正戊醇、1-壬醇、2-癸炔-1-醇等多种醇类。其总含量排序为L+W>L0>N0>L+P,说明W.anomalus对挥发性醇类的合成具有促进作用。酸类以乙酸、辛酸为主,兼具降低酸菜pH值和增加酸菜酸味的作用。发酵过程中以脂肪酸为前体的醛类物质[(Z)-2-庚烯醛、苯甲醛等],贡献蔬菜清香的香气[16,25]。酮类物质以二氢-β-紫罗兰酮、β-紫罗兰酮为主,性质稳定,赋予酸菜花果香[24]。L+W组的醛酮类含量最高,L+P组的酮类含量高于L0组与N0组。酚类物质(4-乙基苯酚等)阈值较低,常产生刺激性气味,具有抗氧化、抗真菌的作用[29]。而烃类、醚类等阈值普遍较高,总量较少,对酸菜的风味贡献不大。PCA进一步说明不同试验组酸菜风味差异。如图6-a所示,共得到2个主成分,累积方差贡献率达到55.1%。不同试验组的酸菜差异明显,表明不同的接菌种类发酵酸菜的挥发性物质风味差异明显。L+W组在x轴下方,L+P组、L0组与N0组在x轴上方,L+W组离3组均最远,表明其风味差异最大。L+P组与L0组同在x轴上方、y轴左侧,且距离较近,意味着2组挥发性风味相近。N0组与另外3组距离均较远,这说明接菌发酵与自然发酵风味差异较大。
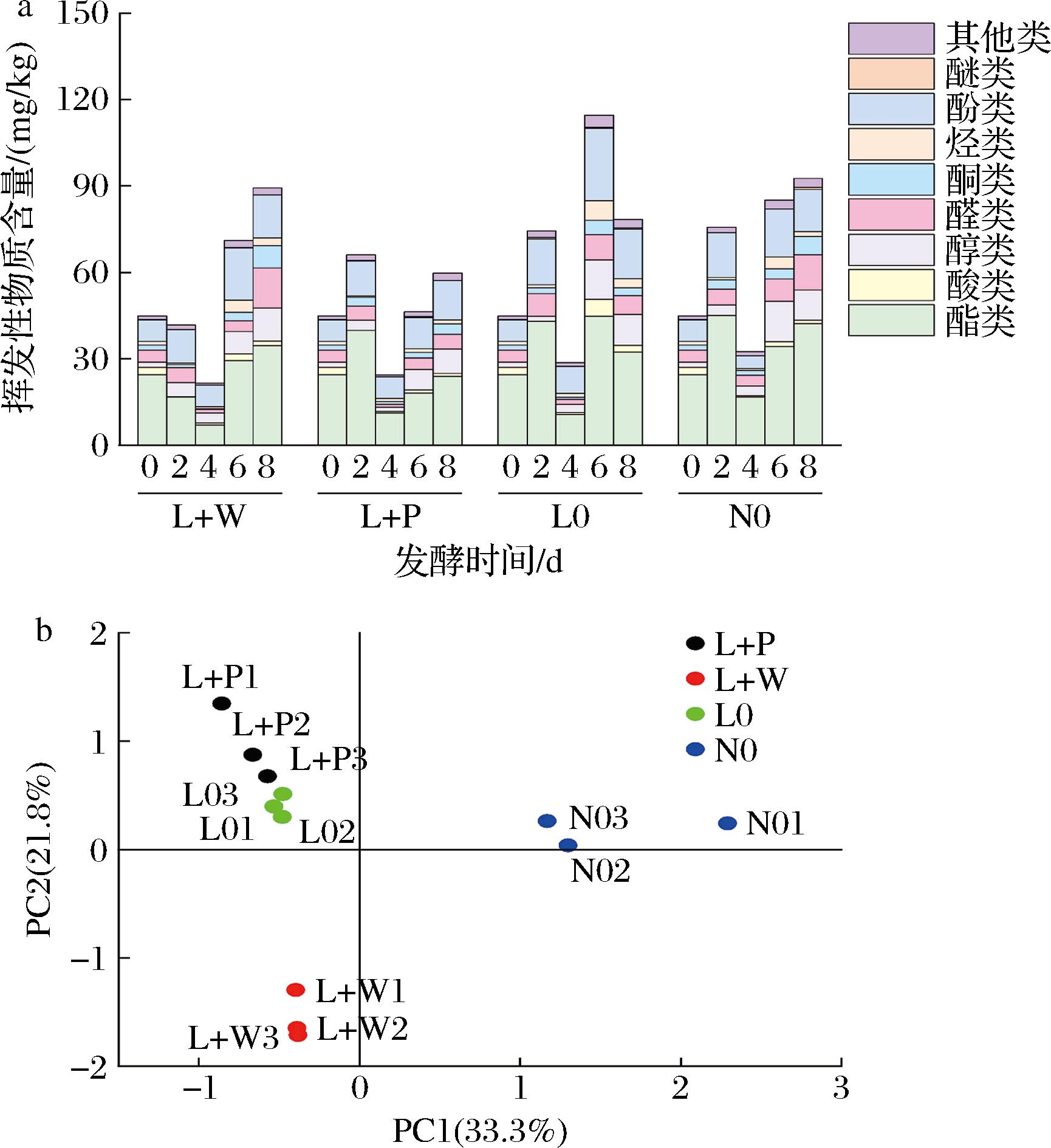
a-挥发性物质含量;b-挥发性物质PCA分析
图6 发酵过程中酸菜挥发性物质含量的变化及第8天各组酸菜挥发性物质的PCA结果
Fig.6 Changes of volatile substances in sauerkraut during fermentation and PCA results of volatile substances in pickled cabbage on day 8
3 结论与讨论
本研究对W.anomalus与P.kudriavzevii分别联合乳酸菌发酵酸菜的理化性质与挥发性风味物质进行分析,结果表明L+W组与L+P组通过代谢互补机制,有效缓解乳酸菌过度产酸,抑制亚硝酸盐积累,降低峰值,W.anomalus的代谢活动促进了挥发性物质中酯类(如异硫氰酸烯丙酯、棕榈酸乙酯)、醇类(如苯乙醇、正戊醇)和醛酮类(如二氢-β-紫罗兰酮、4-乙基苯酚)的生成。此外,酵母菌提升了苦味(酪氨酸、蛋氨酸)与甜味(苏氨酸)氨基酸含量,进一步强化了酸菜的味觉层次。值得注意的是,不同酵母菌株与乳酸菌联合发酵对酸菜的挥发性风味的影响上存在差异:L+W组更显著提升酯类、醇类与醛酮类物质含量,其风味相较于其他3组相比差异显著,而L+P组的接入整体上降低了酸菜挥发性风味物质的含量,其风味与L0发酵的风味更为相近。综上所述,W.anomalus可作为优选菌株,用于开发低亚硝酸盐、高酯香的酸菜。研究结果为酸菜发酵微生物调控提供一定的理论依据。
[1] 王佳仪. 酸菜鱼预制菜市场步入增长期[N].中国食品报, 2023-10-10(6).
[2] 周润嫦, 刘锶彤, 曾洁妹, 等.乳酸菌发酵蔬菜的研究进展[J].2024(22):109-113.ZHOU R C, LIU S T, ZENG J M, et al.Research progress on lactic acid bacteria fermented vegetables[J].Farm Products Processing, 2024(22):109-113.
[3] LEE J J, CHOI Y J, LEE M J, et al.Effects of combining two lactic acid bacteria as a starter culture on model kimchi fermentation[J].Food Research International, 2020, 136:109591.
[4] 张楠笛, 祝林, 许琴, 等.食窦魏斯氏菌协同植物乳杆菌改善四川泡菜风味[J].食品科学, 2020, 41(14):102-108.ZHANG N D, ZHU L, XU Q, et al. Weissella cibaria synergizes with Lactobacillus plantarum to improve the flavor of Sichuan paocai[J].Food Science, 2020, 41(14):102-108.
[5] 刘玉凌, 任亭, 彭玉梅, 等.老盐水中乳酸菌的筛选鉴定及其在青菜头泡菜中的应用[J].食品与发酵工业, 2020, 46(2):208-213.LIU Y L, REN T, PENG Y M, et al.Screening and identification of lactic acid bacteria from old brine and its application in tumor stem mustard pickles[J].Food and Fermentation Industries, 2020, 46(2):208-213.
[6] GAO Y Y, LAN Y F, YANG J X, et al.Improving the quality and flavor of radish paocai by inoculating with Lactobacillus plantarum-1 and Leuconostoc mesenteroides-7[J].Journal of Food Science, 2025, 90(3):e70127.
[7] 张文娟, 陈安特, 韩宇琴, 等.酿酒酵母对萝卜泡菜发酵的影响[J].食品与发酵工业, 2017, 43(8):134-137.ZHANG W J, CHEN A T, HAN Y Q, et al.Effect of Saccharomyces cerevisiae on the fermentation of radish and pickle[J].Food and Fermentation Industries, 2017, 43(8):134-137.
[8] 陈偲, 张明, 付竹贤, 等.乳酸菌与酵母菌的复配筛选及在传统泡菜中应用[J].食品工业科技, 2023, 44(16):155-163.CHEN C, ZHANG M, FU Z X, et al.Screening a combination of lactic acid bacteria and yeast and application in traditional pickle[J].Science and Technology of Food Industry, 2023, 44(16):155-163.
[9] CAI W Q, WAN Y, CHEN Y R, et al.Transcriptomics to evaluate the influence mechanisms of ethanol on the ester production of Wickerhamomyces anomalus with the induction of lactic acid[J].Food Microbiology, 2024, 122:104556.
[10] LIU S X, LOU Y, ZHAO Y, et al.Multi-omics analyses of the mechanism for formation of key aroma-active compounds in blood orange wine fermented by Pichia kudriavzevii[J].Food Research International, 2024, 198:115321.
[11] YANG Y L, FAN Y, LI T, et al.Microbial composition and correlation between microbiota and quality-related physiochemical characteristics in Chongqing radish Paocai[J].Food Chemistry, 2022, 369:130897.
[12] 经骐源, 李婷, 曾凡坤, 等.发酵剂对泡萝卜品质的影响[J].2021(22):171-177.JING Q Y, LI T, ZENG F K, et al.Effect of starter on the quality of pickled radish[J].Food Science, 2021(22):171-177.
[13] 钱杨, 吴李川, 许童桐, 等.不同空气暴露条件下四川泡菜的品质变化及产植物细胞壁降解酶微生物分析[J].食品工业科技, 2020, 41(13):128-133;147.QIAN Y, WU L C, XU T T, et al.Analysis of quality changes and plant cell wall degrading enzymes producing microorganism in Sichuan pickle under different air exposure conditions[J].Science and Technology of Food Industry, 2020, 41(13):128-133;147.
[14] 唐蓉, 陈骏飞, 杨海泉, 等.乳酸菌与酵母菌联合发酵对芥菜理化性质及保藏期品质的影响[J].食品工业科技, 2024, 45(10):141-148.TANG R, CHEN J F, YANG H Q, et al.Effects of lactic acid bacteria and yeast co-fermentation on the physicochemical properties and storage period quality of mustard[J].Science and Technology of Food Industry, 2024, 45(10):141-148.
[15] 汪冬冬, 唐垚, 陈功, 等.不同发酵方式盐渍萝卜挥发性成分动态分析[J].食品科学, 2020, 41(6):146-154.WANG D D, TANG Y, CHEN G, et al.Dynamic analysis of volatile components of salted radish during different fermentation processes[J].Food Science, 2020, 41(6):146-154.
[16] 刘超, 毕玉平, 马德源, 等.乳酸菌与酵母菌共发酵芦笋汁工艺优化及其风味成分分析[J].食品与发酵工业, 2023, 49(9):128-134.LIU C, BI Y P, MA D Y, et al.Optimization of Asparagus juice co-fermented with lactic acid bacteria and yeast, and the flavor components analysis of the products[J].Food and Fermentation Industries, 2023, 49(9):128-134.
[17] LI W W, FAN G S, FU Z L, et al.Effects of fortification of Daqu with various yeasts on microbial community structure and flavor metabolism[J].Food Research International, 2020, 129:108837.
[18] FULLERTON C G, PRAKASH R, NINAN A S, et al.Fruit from two kiwifruit genotypes with contrasting softening rates show differences in the xyloglucan and pectin domains of the cell wall[J].Frontiers in Plant Science, 2020, 11:964.
[19] 郑超, 侯信哲, 陈天花, 等.乳酸菌在蔬菜发酵中的作用机制研究进展[J].中国调味品, 2024, 49(8):205-210.ZHENG C, HOU X Z, CHEN T H, et al.Research progress of action mechanism of lactic acid bacteria in fermentation of vegetables[J].China Condiment, 2024, 49(8):205-210.
[20] WU C D, ZHENG J, HUANG J, et al.Reduced nitrite and biogenic amine concentrations and improved flavor components of Chinese sauerkraut via co-culture of Lactobacillus plantarum and Zygosaccharomyces rouxii[J].Annals of Microbiology, 2014, 64(2):847-857.
[21] XIONG Y L, GUAN J, WU B Z, et al.Exploring the profile contributions in Meyerozyma guilliermondii YB4 under different NaCl concentrations using GC-MS combined with GC-IMS and an electronic nose[J].Molecules, 2023, 28(19):6979.
[22] PARK E J, CHUN J, CHA C J, et al.Bacterial community analysis during fermentation of ten representative kinds of kimchi with barcoded pyrosequencing[J].Food Microbiology, 2012, 30(1):197-204.
[23] 王龄焓, 陈辰, 万洋灵, 等.乳酸菌在豆乳中的生长特性及其与酵母菌联合发酵作用[J].食品工业科技, 2019, 40(19):129-135.WANG L H, CHEN C, WAN Y L, et al.Growth characteristics of lactic acid bacteria in soymilk and its combined fermentation with yeast[J].Science and Technology of Food Industry, 2019, 40(19):129-135.
[24] 汪冬冬, 唐垚, 伍亚龙, 等.泡菜细菌多样性和风味成分研究进展[J].食品与发酵工业, 2021, 47(21):296-302.WANG D D, TANG Y, WU Y L, et al.Advances on bacterial diversity and flavor of Paocai[J].Food and Fermentation Industries, 2021, 47(21):296-302.
[25] 郭精桐, 赵圆, 孙玉敬.番茄果实风味及其影响因素的研究进展[J].食品科学, 2023, 44(17):169-177.GUO J T, ZHAO Y, SUN Y J.Recent advances in research on flavor substances in tomato fruit and their influential factors[J].Food Science, 2023, 44(17):169-177.
[26] ZHANG C C, ZHANG J M, LIU D Q.Biochemical changes and microbial community dynamics during spontaneous fermentation of Zhacai, a traditional pickled mustard tuber from China[J].International Journal of Food Microbiology, 2021, 347:109199.
[27] XU X X, WU B B, ZHAO W T, et al.Shifts in autochthonous microbial diversity and volatile metabolites during the fermentation of chili pepper (Capsicum frutescens L.)[J].Food Chemistry, 2021, 335:127512.
[28] DUAN W H, GUAN Q J, ZHANG H L, et al.Improving flavor, bioactivity, and changing metabolic profiles of goji juice by selected lactic acid bacteria fermentation[J].Food Chemistry, 2023, 408:135155.
[29] RATHNA J, BAKKIYARAJ D, PANDIAN S K.Anti-biofilm mechanisms of 3, 5-di-tert-butylphenol against clinically relevant fungal pathogens[J].Biofouling, 2016, 32(9):979-993.