益生菌因其在调节肠道微生态、增强免疫功能等方面的显著作用,广泛应用于功能性食品及特殊医学用途配方食品中[1-3]。传统益生菌制剂多以冻干粉[4]、胶囊[5]、片剂[6]、发酵乳制品[7]或发酵果汁[8]等形式存在,虽具有一定的应用基础,但整体结构单一、功能设计有限,难以实现个性化呈现,也较难激发消费者的摄入兴趣。因此,急需引入具备结构可设计与视觉吸引力的新型加工技术,以提升消费者对益生菌制剂的接受度。然而,益生菌自身物理性质较为敏感,在食品应用中对载体结构与成型条件具有较高要求,限制了其多样化开发与个性化制备[9]。
3D打印技术作为一种融合数字化控制与精密成型的智能制造手段,近年来在生物材料、航空航天、医疗器械及建筑工程等多个领域展现出日益显著的应用潜力[10-15]。在食品加工领域,3D打印技术凭借其结构可设计性、成分可控性及个性化营养定制等优势,为益生菌包埋结构的构建与个性化定制提供了创新性的解决方案[16]。同轴挤出式3D打印技术通过双通道材料同步挤出与协同成型,可构建具备核壳结构的功能载体,特别适用于活性物质的包埋与保护。如WANG等[17]研究开发了嵌套螺杆同轴3D打印技术,突破传统同轴打印中黏度匹配限制,实现高黏度材料的稳定共挤与成型。构建的模型提升了打印精度与重复性,验证了仿生芯-壳结构在增强力学性能方面的优势,损伤吸收能力提升达30.1%。AHMADZADEH等[18]利用同轴3D打印技术,将叶黄素封装于以乙基纤维素为内核、淀粉糊为外层的双层凝胶结构中,系统优化了打印参数(层高、材料浓度、温度)。结果显示,该方法显著提升了叶黄素的形状保真度与储存稳定性,保留率在优化条件下可达70%,为功能性食品中活性物质的稳定封装提供了有效方案。
此外,已有研究证实,海藻酸钠与钙源之间的离子交联反应可在温和条件下快速形成结构稳定、可控性强的凝胶结构,具有良好的生物相容性,成为益生菌包埋材料体系的优选方案。如JAMES等[19]基于海藻酸钠与Ca2+的离子交联机制,开发了海藻酸钙、明胶、κ-卡拉胶复合水凝胶体系,并研究出质量分数为2.2%海藻酸钠、1%明胶、4% κ-卡拉胶的最佳配比,在62 ℃、0.864 mm喷嘴和48.2 kPa压力条件下实现了良好的打印稳定性与成型性能。FERREIRA等[20]结合3D打印与电沉积技术,利用海藻酸钠与碳酸钙纳米颗粒混合液,在电场作用下释放Ca2+实现原位交联,构建可控成型的三维海藻酸钙水凝胶结构。实验实现多种形貌打印,细胞存活率高达99%,展示出良好生物相容性与应用潜力。ZHOU等[21]提出一种无需添加增稠剂或支撑材料的海藻酸钠水凝胶直接3D打印方法,利用乙醇诱导溶胶-凝胶转变提升墨水可打印性,后续通过Ca2+交联实现结构稳定成型。结果显著提高了打印精度(提升超10%),为复杂海藻酸钙水凝胶结构的高效构建提供了新方案,具有良好应用前景。尽管上述研究为海藻酸钙基水凝胶的3D打印奠定了基础,但针对益生菌嵌入型凝胶结构的研究仍相对较少,相关成型机制与影响因素尚不明确,需开展深入系统的研究。
本研究旨在基于同轴挤出食品3D打印平台,开发一种具备形态可定制化、结构可控化的益生菌嵌入型凝胶构建方法。选取海藻酸钠-乳酸钙作为外内层材料体系,通过系统调控原料浓度、挤出速度及益生菌添加量等关键参数,评估其对打印结构成型效果的影响。研究目标在于探索益生菌包埋结构形成的关键影响因素,建立稳定、高效、可个性化定制的3D打印包埋策略,为特医食品中益生菌的智能化、定制化载体设计提供技术支持与理论依据。
1 材料与方法
1.1 材料与仪器
海藻酸钠(食品级),青岛明月海藻集团有限公司;乳酸钙(食品级),山东润泽生物科技有限公司;益生菌粉末,北京同仁堂健康药业股份有限公司。
TD-4HKT光学显微镜,深圳市三锵泰达光学仪器有限公司;TA.XT PlusC质构仪,英国Stable Micro Systems公司。
本研究采用的食品3D打印机为课题组自主研发设备,具备传统食品3D打印机的基本功能,实物图可见电子版增强出版附图1(https://doi.org/10.13995/j.cnki.11-1802/ts.043871,下同),所使用的挤出机构为柱塞式结构。该结构通过电机驱动丝杆推动活塞,实现线性精确挤出,执行机构由课题组自主设计与加工,主要材质为不锈钢。为提升系统适应性,挤出端设计为标准鲁尔接头接口,便于快速更换同轴喷嘴以满足不同实验条件的需求[22-25]。喷头部分基于同轴结构原理设计了一款定制化同轴喷嘴,其工作原理图及实际成型效果见附图2。运动控制系统选用Zmotion公司(中国深圳)生产的ZMC408SCAN型运动控制器。
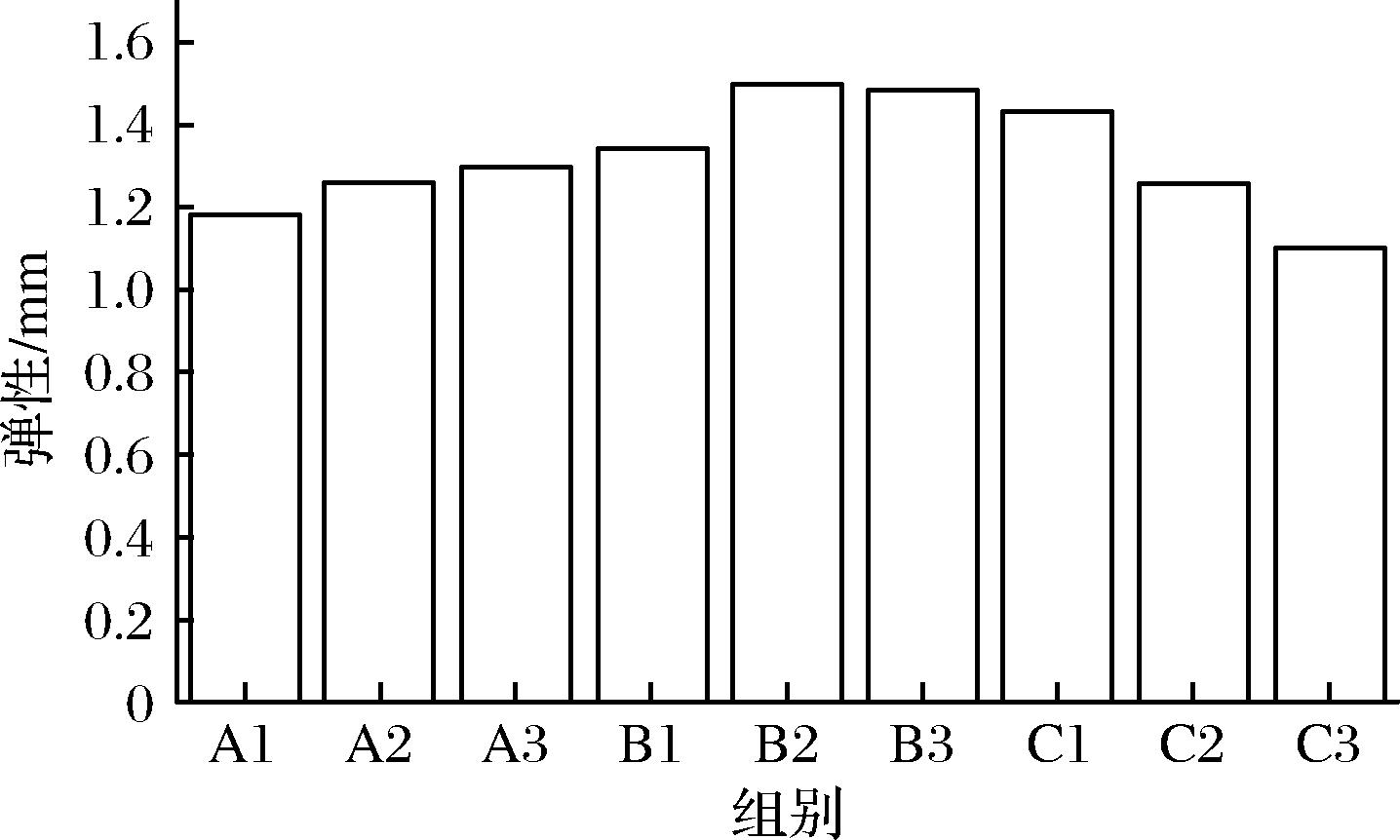
图1 弹性变化统计图
Fig.1 Elasticity change statistics chart
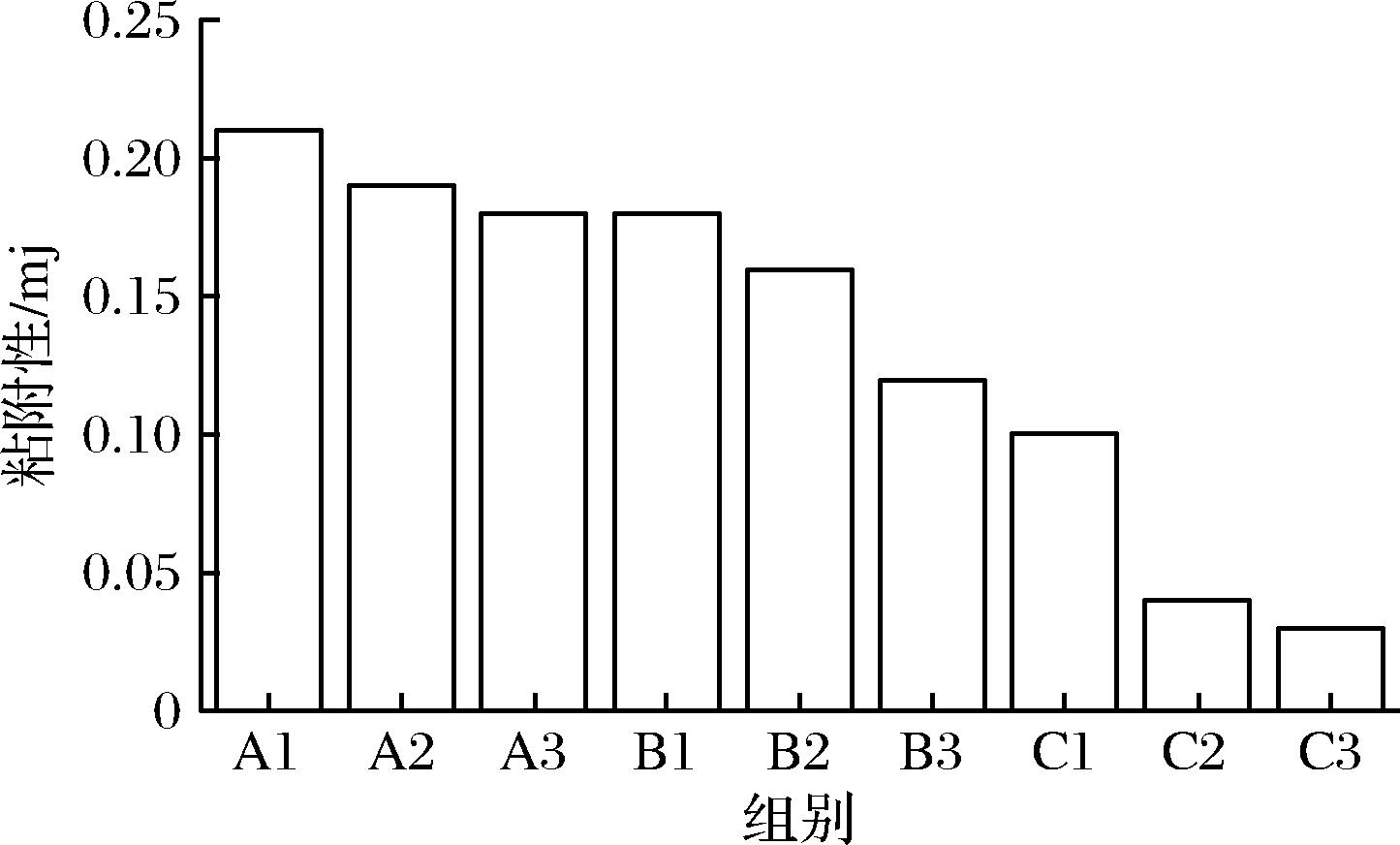
图2 黏附性变化统计图
Fig.2 Adhesion change statistics
1.2 实验方法
1.2.1 打印原料制备
本文采用食品级海藻酸钠和乳酸钙溶液作为同轴3D打印的外相与内相材料。乳酸钙释放Ca2+较为缓慢,能减缓交联反应,避免在接触初期形成致密壳层,减少未固化海藻酸钠流失的风险。海藻酸钠在外层与内层乳酸钙溶液发生离子交联,形成稳定凝胶结构,益生菌预先分散于乳酸钙中,实现同步包埋。所有溶液均经磁力搅拌30 min,静置脱泡2 h,确保打印流动性和成型一致性[26]。
1.2.2 模型设计与切片
本研究采用SolidWorks 2020(Dassault Systèmes,美国)对益生菌包埋结构进行三维建模,并导出标准.STL文件用于切片处理。由于现有切片软件多面向热熔型材料,缺乏针对食品类同轴3D打印的专用平台,软件的兼容性与参数设定对打印效果影响显著。经多款软件测试后,最终选用Repetier-Host 2018(Repetier,德国)作为切片与打印控制平台。该软件支持.STL模型导入,并可在切片设置中调整层厚、填充密度、图案及速度,在材料和设备设置中配置料筒直径、喷嘴直径、回抽长度等参数[27-28]。完成设置后,软件生成G-code控制打印设备运行。本研究结合同轴打印特点,在G-code基础上进一步调试内外通道的同步挤出速度与启停延时,确保包埋结构的完整性与成型质量。
1.2.3 控制系统介绍
食品3D打印控制系统采用C语言开发,整体系统架构主要由两部分构成,分别对应同轴打印系统中的外轴与内轴控制。
第一部分为外轴运动控制模块,由团队自主研发,其核心是通过解析G-code指令中的位置信息,由运动控制器协调电机实现精准移动。打印平台的X轴与Y轴运动分别由对应的X轴与Y轴电机模组驱动完成,平台的升降则由两台联动的U轴电机模组控制。此外,外层材料的挤出通过一台Z轴微型电机模组来实现。每行G-code指令中的字母X、Y、Z、U分别对应上述4个电机轴向,其后的数值表示各自的绝对位移量,控制系统据此进行协调运动。
第二部分为内轴控制模块,即微量注射泵驱动系统。该部分作为内层材料(含益生菌)的精密挤出装置,通过独立控制回路实现稳定、连续的推送过程。内轴的工作与外轴的移动过程相配合,以确保同轴结构的同步成型与包埋质量。
1.2.4 原料浓度对结构成型影响实验设计
为系统评估凝胶原料配比对益生菌嵌入型同轴结构成型效果的影响,参考相关研究[29-31],本研究设计了3种海藻酸钠浓度(质量分数为3%、4%、5%)与3种乳酸钙浓度(质量分数为2%、3%、4%)的组合,构建共计9组基础实验,开展配比优化研究。通过质构仪测量,系统对比不同组合下的成型完整性、界面清晰度与凝胶弹性与黏附性,筛选出最优浓度组合,作为后续实验的基础参数。
1.2.5 挤出速度对结构成型影响实验设计
在完成原料浓度优化的基础上,进一步探讨了内外轴挤出速度对同轴凝胶结构成型性能的影响。首先,采用COMSOL Multiphysics软件构建流体动力学模型,对内轴(乳酸钙溶液)与外轴(海藻酸钠溶液)在共挤出过程中的流速分布与界面变化进行数值模拟。考虑到设备系统中内轴与外轴挤出机构存在最大运行速度限制(内轴最大为1.5 mm/s,外轴最大为1.0 mm/s),本研究在该范围内设定多组速度组合进行仿真,具体参数见附表1。通过对不同速度条件下的速度梯度分布与流场特征进行分析,初步筛选出内外轴速度的适宜范围。随后,通过控制内外轴速度进行模拟,评估其对成型效果的影响,为后续物理实验提供了可靠的参数参考。
在此基础上,设计了2组速度组合实验以系统分析速度匹配对成型质量的影响:第一组中,外轴挤出速度固定,内轴速度设定为多个梯度进行对照测试;第二组中,内轴速度保持不变,分别设定不同外轴速度进行对比分析。通过对各组打印样品的成型完整性、结构连续性及界面清晰度等指标进行综合评价,最终确定了性能最优的内外轴配速组合。
1.2.6 益生菌浓度对结构成型影响实验设计
在确定原料配比和挤出速度的最优参数基础上,为进一步实现益生菌的有效嵌入与负载,分别在内轴乳酸钙溶液中添加质量分数为0%、5%、10%、15%、20%的益生菌,形成混合溶液开展打印实验。通过综合评价结构成型效果与益生菌负载能力,筛选出兼具良好打印性能的最佳添加浓度。
1.2.7 成型效果评价
为全面评估所构建的同轴益生菌包埋结构的成型质量与结构稳定性,本文从成型精度入手,对打印样品进行了系统测试与分析。成型精度作为衡量3D打印结构与其设计模型一致性的重要指标,是评价打印质量的关键参数之一。具体考察内容包括打印结构的完整性,以及是否存在断层、塌陷、偏移等缺陷。同时,借助光学显微镜对样品内外层的径向尺寸进行测量与比对,以验证同轴打印过程中内外层材料的协同匹配程度与成型稳定性。此外,为进一步探究不同材料浓度组合对所得凝胶结构力学性能与流变行为的影响,本文采用质构仪对样品进行了弹性和黏附性指标的测试与分析。
1.3 数据处理
每组实验均进行不少于3次的重复测量,所得结果以“平均值±标准差”的形式表示,以确保数据的代表性与可靠性。实验数据的图表绘制与可视化分析由Origin 2018软件完成。
2 结果与分析
2.1 凝胶原料配比对成型效果的影响
本研究选取海藻酸钠溶液(3%、4%、5%,质量分数)作为外层包埋材料,乳酸钙溶液(2%、3%、4%,质量分数)作为内层交联反应介质。为便于观察交联反应过程,实验在黑色背景下进行打印,并采用波浪形线条的打印方式,挤出速度固定为轴系统初始默认速度(内轴0.8 mm/s,外轴0.2 mm/s),以验证不同配比条件下的成型性能。最终共构建9组不同浓度组合情况,具体编号方式及各组的成型见附表2。
从打印结果可见,当海藻酸钠质量分数为3%时,A组的3组实验均表现出不理想的成型效果。由于离子浓度较低,交联反应较弱,导致液体严重流淌,成型不稳定。尽管A3组能够形成一定的凝胶线条形态,但在触碰后出现明显凹陷,表面仍残留较多液体,表明其凝胶强度较低。当海藻酸钠质量分数升至4%时,B组的3组实验整体成型效果较为理想。其中,B1组凝胶在接触后仍表现出一定的柔软性,说明其成型强度尚不足。而B2、B3成型效果较好,仅凭观察无法得出最优浓度配比,因此采用光学显微镜对其内外轴进行观测,观测情况见附图3,B3组内轴乳酸钙溶液发生较多处断裂,成型效果较差,B2组相对B3组内轴成型效果较好。当海藻酸钠浓度进一步提高至5%时,C组3组实验均出现过度凝胶化现象,表明2种溶液间的交联反应过强,所形成的凝胶具有较高强度但流变性能较差,显著影响挤出过程的顺利进行。在打印过程中,由于所需挤出压力较大,凝胶易发生来回摆动,致使线条出现偏移。此外,C3组在打印过程中发生断裂,推测系凝胶强度过大且流动性不足,导致挤出受阻所致。为进一步量化各配比下凝胶结构的力学性能,采用质构仪对所得样品进行弹性与黏附性测试,结果分别如图1和图2所示。由图1可见,凝胶弹性呈现先上升后下降的趋势,其中B2组达到最大弹性值。A组弹性偏低,主要由于交联反应不充分;而C组弹性下降,则可能由于过度交联引发结构刚化与打印不连续所致。图2显示,A1至B2组的黏附性均处于适宜的范围内(0.15~0.25 mm),满足凝胶打印对结构稳定性与流变性能的双重要求[32]。综上所述,选择B2(4%海藻酸钠与3%乳酸钙,均为质量分数)作为最佳原料配比来进行接下来的实验。

图3 光学显微镜下凝胶内外轴示意图
Fig.3 Schematic diagram of the inner and outer axes of the gel under an optical microscope
2.2 挤出速度对成型效果的影响
通过对附表1中不同速度组合的仿真分析发现,当外轴速度达到0.3 mm/s时,即使将内轴速度提高至最大值1.5 mm/s,仍出现内轴流体断裂的现象(图3)。其主要原因在于外轴流速相对较高,而内轴流速不足,导致海藻酸钠溶液在界面处包裹过多,从而抑制了有效交联,最终造成打印物体呈现黏液状外观。考虑到系统的运行极限及成型稳定性,确定仿真速度范围为:外轴0~0.25 mm/s,内轴0~1.5 mm/s。
在利用COMSOL进行仿真实验过程中,首先将外轴速度固定为0.25 mm/s,依次设置内轴速度为0.2、0.4、0.6、0.8、1.0、1.2 mm/s,仿真结果如图4所示。随着内轴速度的增加,同轴打印结构的内径逐渐增大。然而,从图4-a可见,在内轴速度为0.2 mm/s的条件下,内轴流体的表现(蓝色区域)较不明显,形成效果不理想,考虑其实际成型性能较差,在后续研究中删去该组合,实验时将内轴速度调整范围确定为0.4~1.2 mm/s。图4-e内轴挤出效果较均匀,因此在固定内轴速度为1.0 mm/s的基础上,设置外轴速度为0.05、0.1、0.15、0.2、0.25 mm/s进行仿真,结果如图5所示。考虑到仿真条件设置外壁无法突破,不易直接通过外径变化进行判断。而外轴溶液的增大将对内轴形成更强的包裹挤压效应,因此,本研究通过观察内径变化趋势,间接推断外轴速度对整体结构成型的影响。仿真结果显示,在内轴速度恒定的条件下,可推测外轴速度的增加显著推动外径的增大。
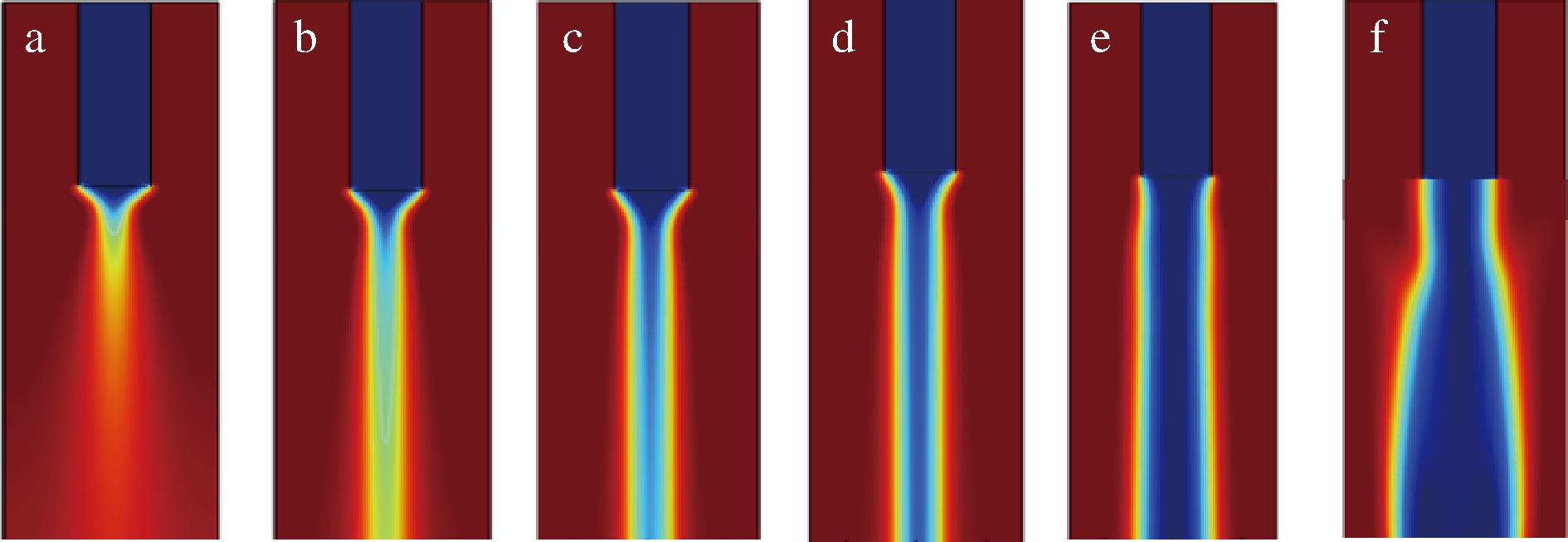
a-0.2 mm/s;b-0.4 mm/s;c-0.6 mm/s;d-0.8 mm/s;e-1.0 mm/s;f-1.2 mm/s
图4 不同外轴速度下同轴打印结构的仿真对比图
Fig.4 Simulation comparison of coaxial printing structure at different external axis speeds
注:外轴速度固定为0.25 mm/s。
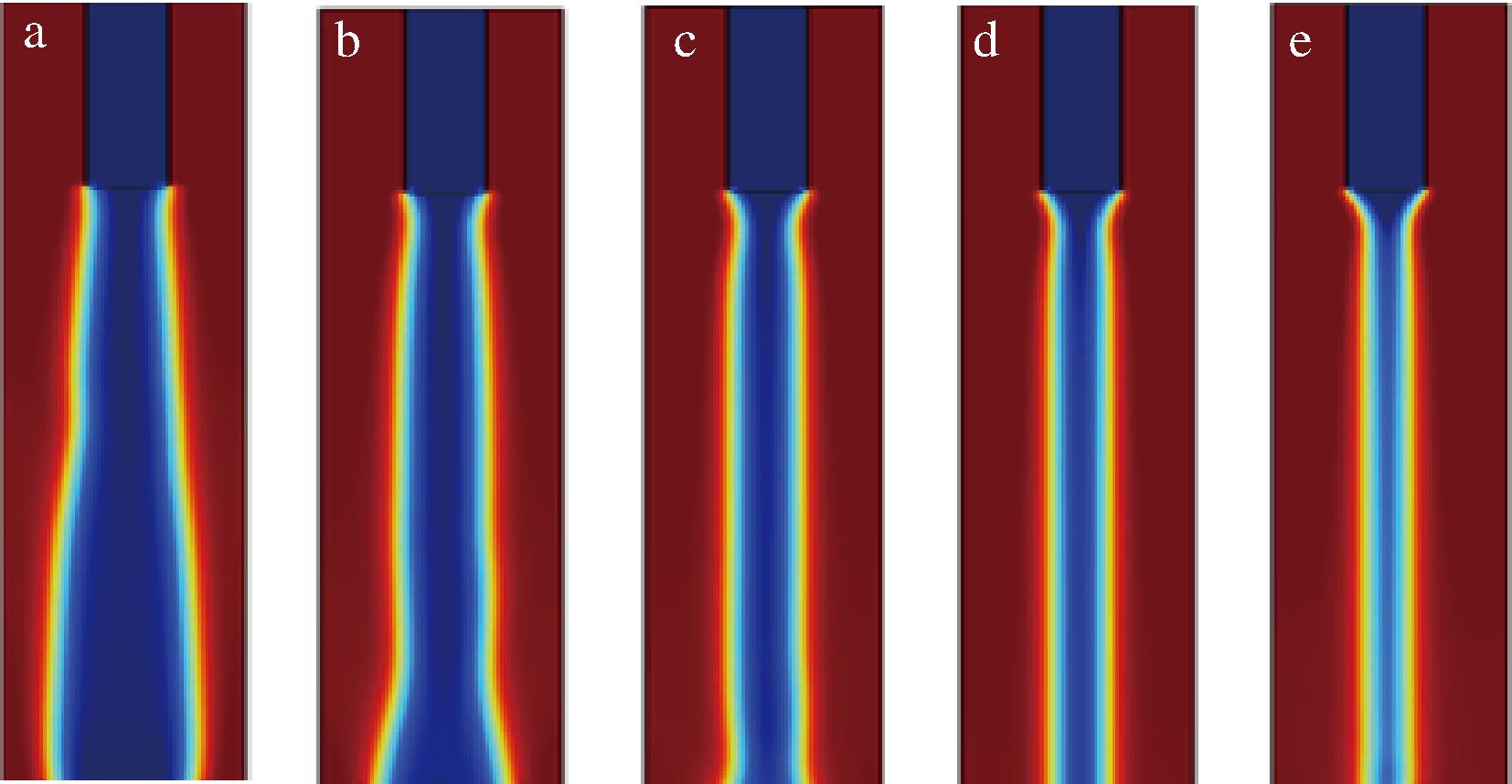
a-0.05 mm/s;b-0.1 mm/s;c-0.15 mm/s;d-0.2 mm/s;e-0.25 mm/s
图5 不同外轴速度下同轴打印结构的仿真对比图
Fig.5 Simulation comparison of coaxial printing structure at different external axis speeds
注:内轴速度固定为0.1 mm/s。
打印实验在最佳溶度配比的条件下(B2浓度),采用分组对照设计方法,分别调整内外轴的挤出速度组合,并用光学显微镜观察打印情况,考察其对成型完整性、界面清晰度及凝胶连续性的影响。根据仿真参数范围设计两组速度组合实验:第一组中外轴速度固定为0.25 mm/s,内轴速度设为0.4、0.8、1.0、1.2、1.4 mm/s;第二组中内轴速度固定为1 mm/s,外轴速度分别设为0.05、0.1、0.15、0.2、0.25 mm/s。这些速度组合均处于较低范围,可延长外层材料在交联区域的停留时间,确保海藻酸钠与Ca2+充分反应,提高交联效率,有效减小材料接触初期形成的海藻酸钙壳层阻碍Ca2+扩散的影响。打印情况可见附表3。此外,内径的大小直接影响到包埋益生菌含量的效率,因此为探究挤出速度与内外径大小的关系,将凝胶产品打印到图6中带有刻度的玻璃板上,放在显微镜下进行观察测量。测量数据如图7所示。

图6 内外径测量
Fig.6 Inner and outer diameter measurement
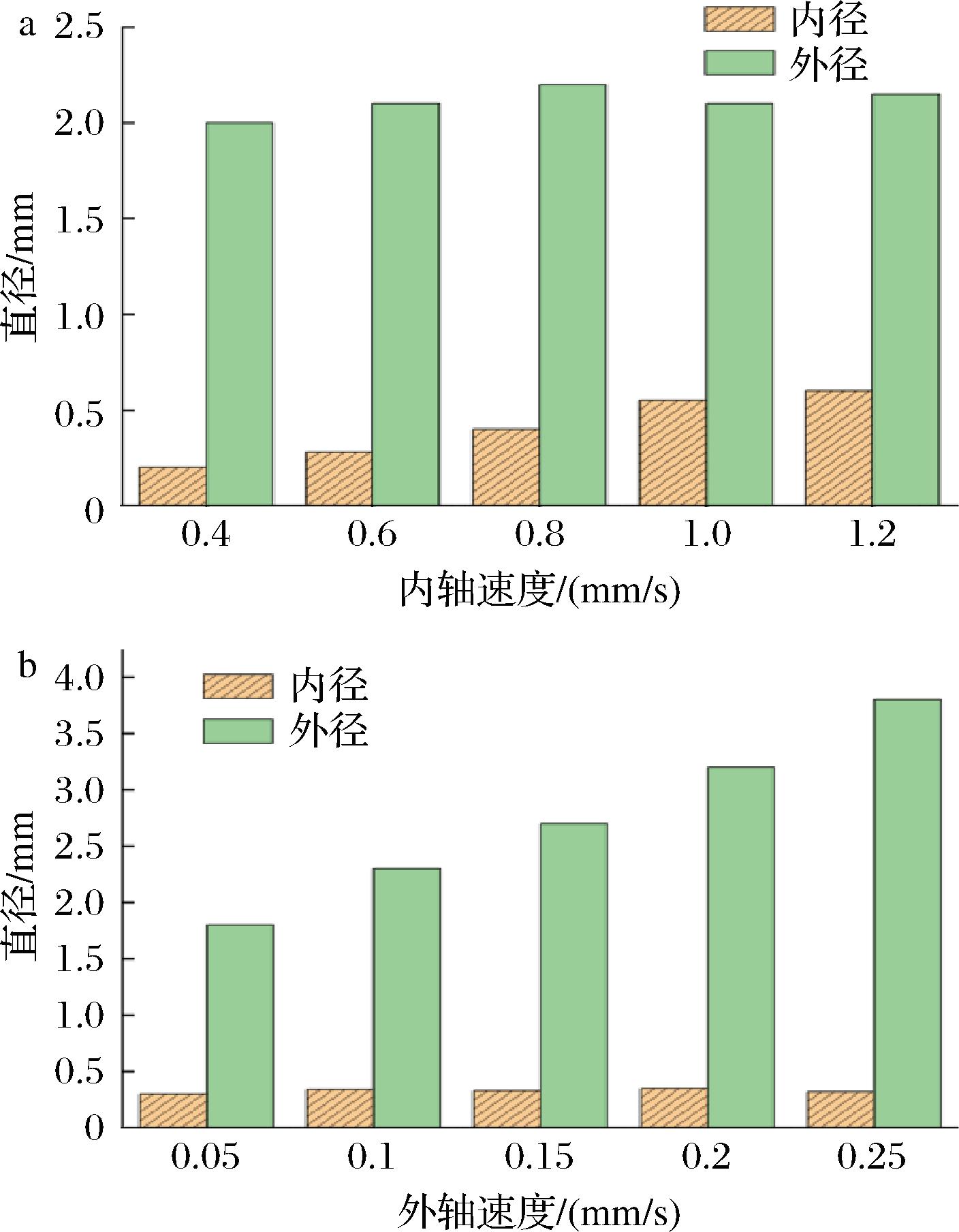
a-外轴速度固定为0.15 mm/s;b-内轴速度固定为0.8 mm/s
图7 内外径尺寸柱状图
Fig.7 Inner and outer diameter bar graph
从包埋效率的角度分析,内轴直径越大,嵌入结构中所包埋的益生菌含量相对越高。如图7所示,内外径随内外轴挤出速度的增大呈递增趋势,因此在保证结构稳定性的前提下,优先选择挤出速度较大的参数组合具有一定优势。然而,由附表3数据可知,与外轴相比,当内轴挤出速度过大时,易导致离子交联反应不完全,成型结构表面出现明显液体残留现象,如0.15/1.2和0.05/0.8组合。进一步观察发现,当内外轴挤出速度同时增大至较高水平时,成型结构的内外径显著增大,导致整体结构发生坍塌,凝胶形貌趋于扁平,严重影响了打印成型质量及结构完整性。综上权衡包埋效率与成型质量2个因素,最终选取内轴速度为1 mm/s、外轴速度为0.15 mm/s的参数组合,此时打印结构饱满,形貌良好,综合性能较优。
2.3 益生菌含量对成型效果的影响
为系统评估益生菌添加浓度对凝胶结构成型效果的影响,本节设置5组不同质量分数(0%、5%、10%、15%、20%)的益生菌混合溶液作为实验变量。在实验中,固定其他条件不变,均采用前期优化获得的最佳组分配比(4%海藻酸钠溶液与3%乳酸钙溶液)以及最优打印参数(内轴挤出速度为0.1 mm/s,外轴挤出速度为0.15 mm/s)进行打印成型实验,探究益生菌浓度对成型质量的影响规律。为突出益生菌包埋效果,加入奶粉使内轴颜色更加明显,打印效果可见附表4。样品的力学性能通过质构仪测试弹性与黏附性,结果见图8和图9。
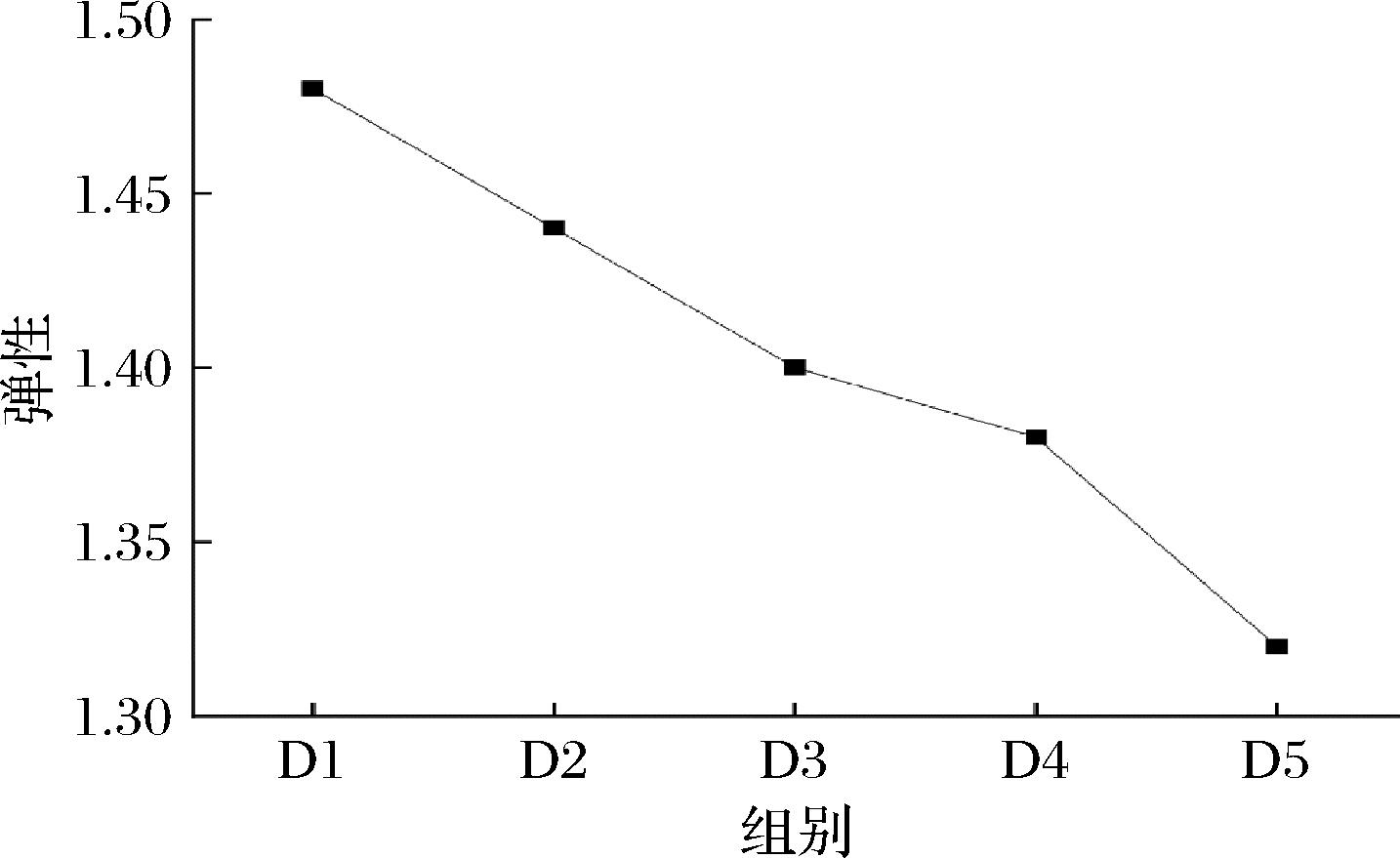
图8 不同益生菌浓度弹性统计图
Fig.8 Elasticity statistics of different probiotic concentrations
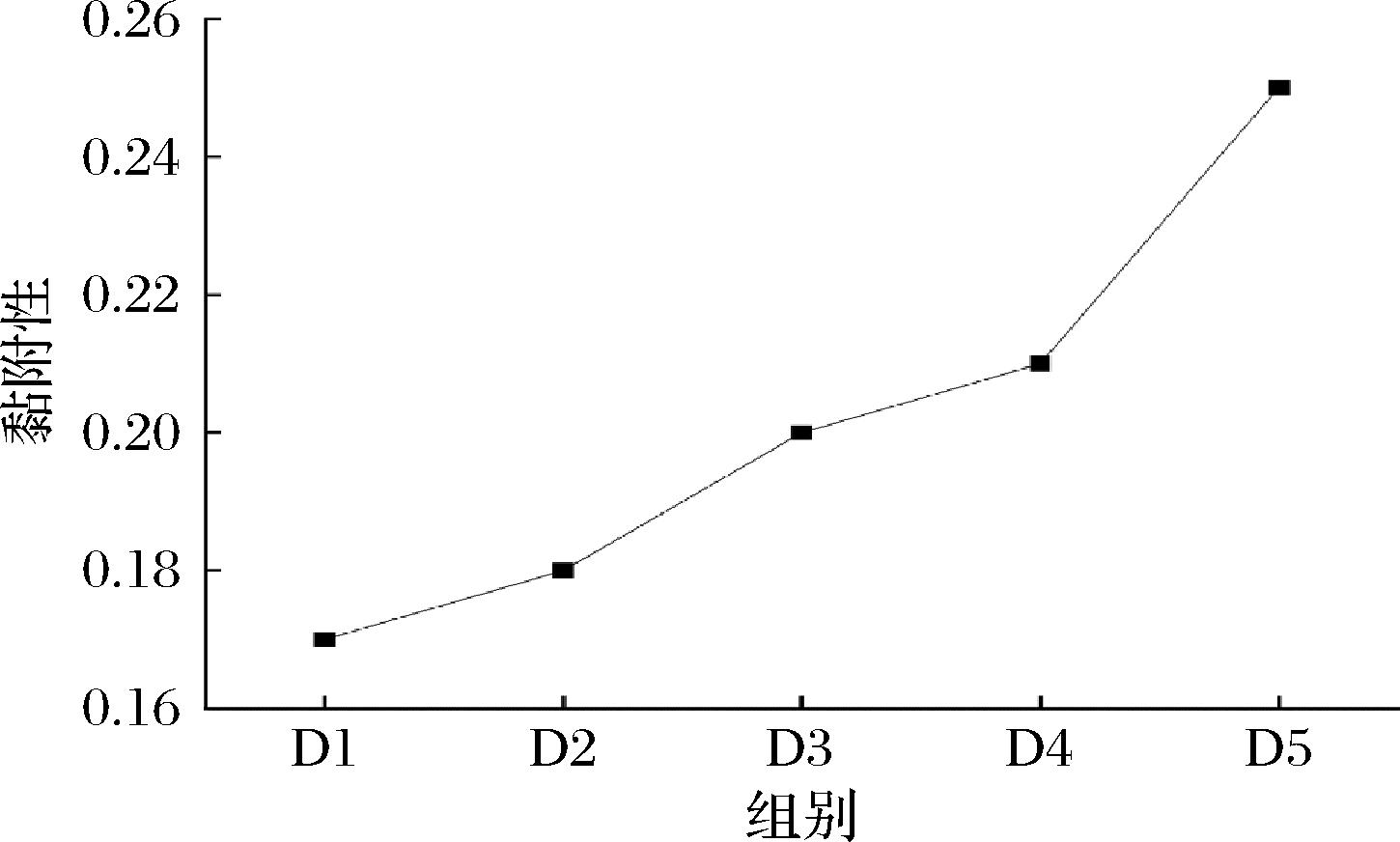
图9 不同益生菌浓度黏附性统计图
Fig.9 Adhesion statistics of different probiotic concentrations
在打印过程中,我们观察到一个有趣的现象:由于喷嘴未完全固定,挤出过程中产生了左右摆动,从而在打印路径中形成了具有波浪状结构的内轴通道。这一现象不仅使内轴结构的视觉可辨性显著增强,也使整体打印效果更加美观。因此,我们在该条件下继续开展了后续的结果分析与结构评估。实验结果表明,随着益生菌浓度的增加,外层海藻酸钠的交联反应逐渐减弱。可引入Fick第一定律来解释这一现象,如公式(1)所示:
(1)
式中:J,Ca2+扩散通量; D,扩散系数;![]() 在乳酸钙-海藻酸钠界面的浓度梯度。
在乳酸钙-海藻酸钠界面的浓度梯度。
其主要原因在于,高浓度益生菌以颗粒形式分散于乳酸钙溶液中,在交联过程中对Ca2+向海藻酸钠分子的扩散形成物理阻碍,有效减小,限制了Ca2+与海藻酸钠链的充分接触,进而降低了交联效率与凝胶结构的致密性。相比之下,D2组(5%益生菌质量分数)外层凝胶结构较为完整,成型效果良好,说明在该浓度下交联反应相对充分。结合图8和图9所示的弹性与黏附性测试结果,D2组表现出较高的弹性,且黏附性处于该类凝胶结构的最佳范围内。综合成型效果与力学性能指标,最终确定5%的益生菌质量分数为本实验的最优参数,并应用于后续研究中。
2.4 打印效果图
为验证同轴3D打印系统的成型能力与包埋效果,本研究在最优参数条件下打印多个结构模型,如图10所示。打印样品整体结构完整,内外轴材料包覆均匀,表面平整,边缘无明显塌陷或破裂现象,表现出良好的成型稳定性。此外,为了使内轴结构更加明显,通过控制喷嘴产生微小抖动,形成波浪状效果,从而增强内轴的可视化特征。

a-单层立方体;b-单层田字格;c-7层口字形(内轴加牛奶);d、e、f-7层口字形(内轴加可食用色素)
图10 益生菌包埋打印效果图
Fig.10 Probiotic encapsulation printing result
3 结论
本研究基于同轴挤出3D打印技术,提出了一种用于构建益生菌嵌入型凝胶结构的可控成型方法。通过系统调控海藻酸钠与乳酸钙的配比、内外轴挤出速度及益生菌浓度等关键参数,深入探究了各因素对打印成型效果的影响,并获得以下结论。在所选材料体系中,质量分数为4%海藻酸钠与3%乳酸钙的浓度组合可实现较强的离子交联反应,打印成型结构完整、界面清晰,具有良好的成型稳定性;挤出速度对同轴结构的内外径及成型质量影响显著。内轴速度为1.0 mm/s、外轴速度为0.15 mm/s时,包埋结构饱满均匀,兼顾了益生菌负载效率与结构完整性;益生菌浓度的增加会干扰Ca2+的扩散交联过程,过高浓度将导致外层凝胶成型不良。综合考量包埋效果与结构稳定性,质量分数为5%的益生菌添加量为较优选择。此外,在打印过程中,可控制喷嘴轻微摆动,使内轴结构呈现规律性波浪形貌,提升了内轴的视觉辨识度与成型美观性。综上所述,本研究验证了基于同轴3D打印构建益生菌包埋结构的可行性,并明确了各关键工艺参数对成型质量的影响规律,为营养食品中益生菌的包埋结构与个性化制造提供了理论依据与技术支持。
[1] 童强, 杨俊豪, 肖帅磊, 等.3D打印技术在特医食品中的应用研究进展[J/OL].食品工业科技, 2025.DOI:10.13386/j.issn1002-0306.2025030360.TONG Q, YANG J H, XIAO S L, et al.Research progress on the application of 3D printing technology in special medical foods[J/OL].Science and Technology of Food Industry, 2025.DOI:10.13386/j.issn1002-0306.2025030360.
[2] NIGAM D.Functional Food and Human Health[M].Singapore:Springer, 2018:59-82.
[3] LIN D C.Probiotics as functional foods[J].Nutrition in Clinical Practice, 2003, 18(6):497-506.
[4] GE S T, HAN J R, SUN Q Y, et al.Research progress on improving the freeze-drying resistance of probiotics:A review[J].Trends in Food Science &Technology, 2024, 147:104425.
[5] OLIVARES A, SILVA P, ALTAMIRANO C.Microencapsulation of probiotics by efficient vibration technology[J].Journal of Microencapsulation, 2017, 34(7):667-674.
[6] ULLAH F S, SAEED M, SHABBIR M A, et al.Microencapsulation of Lactobacillus acidophilus LA-832 and Bifidobacterium longum BL-101 by using sodium alginate and chitosan to improve the survival in simulated gastrointestinal conditions[J].Journal of Food Science and Technology, 2025, 62(12):2360-2371.
[7] SALEEM G N, GU R X, QU H X, et al.Therapeutic potential of popular fermented dairy products and its benefits on human health[J].Frontiers in Nutrition, 2024, 11:1328620.
[8] YERLIKAYA O.Starter cultures used in probiotic dairy product preparation and popular probiotic dairy drinks[J].Food Science and Technology (Campinas), 2014, 34(2):221-229.
[9] KOWALCZYK D, SZYMANOWSKA U, SKRZYPEK T, et al.Edible films based on gelatin, carboxymethyl cellulose, and their blends as carriers of potassium salts of iso-α-acids:Structural, physicochemical and antioxidant properties[J].Food Hydrocolloids, 2021, 115:106574.
[10] WANG J R.Techniques and applications of 3D bioprinting[C].Proceedings of the 3rd International Conference on Biological Engineering and Medical Science.Washington:SPIE, 2023.
[11] FU Z Q, OUYANG L L, XU R Z, et al.Responsive biomaterials for 3D bioprinting:A review[J].Materials Today, 2022, 52:112-132.
[12] 童强, 肖帅磊, 李易, 等.3D打印技术在太空食品加工领域的研究进展[J].食品科学, 2024, 45(18):299-306.TONG Q, XIAO S L, LI Y, et al.Research progress on 3D printing technology in the field of space food processing[J].Food Science, 2024, 45(18):299-306.
[13] QIU K Y, HAGHIASHTIANI G, MCALPINE M C.3D printed organ models for surgical applications[J].Annual Review of Analytical Chemistry, 2018, 11:287-306.
[14] AL-TAMIMI A K, ALQAMISH H H, KHALDOUNE A, et al.Framework of 3D concrete printing potential and challenges[J].Buildings, 2023, 13(3):827.
[15] SALEH ABD ELFATAH A.3D printing in architecture, engineering and construction (concrete 3D printing)[J].Engineering Research Journal, 2019, 162:119-137.
[16] 丁可盈, 金晶, 任玉, 等.3D打印技术在食品中的研究进展[J].南京农业大学学报, 2025, 48(1):70-84.DING K Y, JIN J, REN Y, et al.Recent research progress of 3D printing technology in food products[J].Journal of Nanjing Agricultural University, 2025, 48(1):70-84.
[17] WANG B, DENG X, MING Y K, et al.Hybrid coaxial 3D printing with nested-screw mechanism:Optimizing material integration and structural performance for coaxial designs[J].Journal of Manufacturing Processes, 2024, 120:517-528.
[18] AHMADZADEH S, UBEYITOGULLARI A.Enhancing the stability of lutein by loading into dual-layered starch-ethyl cellulose gels using 3D food printing[J].Additive Manufacturing, 2023, 69:103549.
[19] JAMES S, MOAWAD M.Study on composite hydrogel mixture of calcium alginate/gelatin/kappa carrageenan for 3D bioprinting[J].Bioprinting, 2023, 31:e00273.
[20] FERREIRA K N, GIR N J B, GOMES G H M, et al.Innovative thermosensitive alginate bioink combining cations for enhanced 3D extrusion bioprinting for tissue engineering[J].Bioprinting, 2024, 39:e00340.
N J B, GOMES G H M, et al.Innovative thermosensitive alginate bioink combining cations for enhanced 3D extrusion bioprinting for tissue engineering[J].Bioprinting, 2024, 39:e00340.
[21] ZHOU Q, CHNG C P, ZHAO Y K, et al.Ethanol-induced gelation enables direct three-dimensional printing of sodium alginate hydrogel[J].Materials &Design, 2024, 239:112746.
[22] QIAO J, JIN G Z, LI G H, et al.Study on improving the sealing reliability of fluid connector[J].Journal of Physics:Conference Series, 2021, 2125(1):012070.
[23] OUTREQUIN T C R, GAMONPILAS C, SIRIWATWECHAKUL W, et al.Extrusion-based 3D printing of food biopolymers:A highlight on the important rheological parameters to reach printability[J].Journal of Food Engineering, 2023, 342:111371.
[24] SONG S X, SHI J W, REN Q B, et al.Comparative study on extrusion 3D printing of solid propellant based on plunger and screw[J].Materials, 2025, 18(4):777.
[25] 童强, 杨俊豪, 肖帅磊, 等.多喷头3D打印技术在食品加工中的应用研究进展[J].食品工业科技, 2025, 46(19):492-500.TONG Q, YANG J H, XIAO S L, et al.Research progress on the application of multi-nozzle 3D printing technology in food processing[J].Science and Technology of Food Industry, 2025, 46(19):492-500.
[26] CHEREPANOVA V A, GORDEEV E G, ANANIKOV V P.Magnetic stirring may cause irreproducible results in chemical reactions[J].JACS Au, 2025, 5(8):3789-3798.
[27] TRISAKTI U, CAHYATI S, AZIZ H R.The influence of different slicer software on 3D printing products accuracy and surface roughness[J].Jurnal Rekayasa Mesin, 2021, 12(2):371-380.
[28] LISYAK V V.Overview of 3D printing slicers[J].IZVESTIYA SFedU ENGINEERING SCIENCES, 2022(3):60-74.
[29] 李瑜, 刘媛媛, 李帅, 等.交联直写海藻酸盐水凝胶中空纤维的凝胶率与溶胀度[J].化工学报, 2014, 65(12):5090-5096.LI Y, LIU Y Y, LI S, et al.Gel fraction and swelling degree of hollow alginate fiber fabricated by direct writing and crosslinking[J].CIESC Journal, 2014, 65(12):5090-5096.
[30] LI Y, LIU Y, JIANG C, et al.A reactor-like spinneret used in 3D printing alginate hollow fiber:A numerical study of morphological evolution[J].Soft Matter, 2016, 12(8):2392-2399.
[31] 胡颖. 凝胶流道网络3D打印制造研究[D].杭州:浙江大学, 2015.HU Y.Research on 3D printing manufacturing of gel channel network[D].Hangzhou:Zhejiang University, 2015.
[32] MOUSAVI S M R, RAFE A, YEGANEHZAD S.Optimization of textural characteristics of restructured pimiento strips by response surface methodology[J].Food Science &Nutrition, 2019, 7(5):1595-1605.