玉米须又称玉麦须、蜀黍须,是禾本科植物玉米雌花的花柱和柱头[1]。玉米须作为一种“药食同源”的食材,除作为中药外,玉米须还用于各种食品和保健品,这表明玉米须在多样化的医药和食用产品中可能具有潜在价值。由于玉米须资源丰富,其在中国和其他国家广泛用于加工。我国是全球最大的鲜食玉米生产和消费国,鲜食玉米成为继玉米饲料和玉米深加工之后又一新兴的玉米产业,促使我国鲜食玉米面积快速攀升,而多数玉米副产物在采收后未能进行有效利用。同时,玉米须植物化学和药理特性的研究已成为热门话题,其具有广泛的生物活性,包括大分子多糖和各种小分子成分,如皂苷、类黄酮、甾醇、氨基酸、萜烯和有机酸[2]。此外,含有许多药理活性,如抗高血压活性[3]、降血脂活性[4]、抗炎活性[5]、抗尿路结石活性、抗氧化活性、保护肝脏和其他作用已在以往的研究中得到验证。
前期研究发现,发酵对玉米须的化学成分和功能特性有很大影响,玉米须发酵会产生较高含量的多酚和黄酮[6],以及较强的抗氧化能力和降血糖能力[7]。体外模拟消化技术已成为现代科学研究中评估物质组成及其生物活性的重要手段,因其具有可重复性强、耗财少、实验周期短和能够系统地考察目标成分在模拟消化中的转化过程和功能特性表现,并成为食品及药品在生理过程中化学成分和生物活性变化常用的研究途径[8]。陈希苗等[9]研究发现山楂的多酚类物质和抗氧化活性会因体外模拟胃肠道消化而发生改变。人体胃肠道的复杂环境可能会影响植物中活性物质的形态和功能活性。因此,探究玉米须发酵液在模拟体外消化过程中的生物活性物质和功能活性变化具有重要的现实意义。
本研究通过建立体外模拟消化模型,初步探讨连续体外消化环境对玉米须发酵液中生物活性成分及其抗氧化活性、降血糖功能特性的影响,并评价在体外连续消化不同阶段生物活性物质与功能活性之间的相关性。本研究旨在对开发玉米须发酵液体外消化过程中活性物质的变化及作用机制提供有价值的参考,对功能性食品的开发具有一定意义。
1 材料与方法
1.1 材料与试剂
玉米须:收集于青冈县鲜食玉米基地;类干酪乳杆菌(Lactobacillus paracasei)、酿酒酵母(Saccharomy ces cerevisiae)和巴氏醋杆菌,上海沪峥生物科技有限公司;α-葡萄糖苷酶(酶活力50 U/mg)、对硝基苯基-β-D-吡喃葡萄糖苷,美国Sigma公司;胃蛋白酶、胰蛋白酶、胆汁盐、没食子酸、芦丁、α-淀粉酶,上海源叶生物科技有限公司。
1.2 仪器与设备
SHP-250F生化培养箱、TNZ5-WS低速多管架自动平衡离心机,湖南湘仪实验室仪器开发有限公司;YXQ-100G立式压力蒸汽灭菌器,上海博迅医疗生物仪器股份有限公司;ZQZY-CF8ES直流无刷恒速恒温振荡器,常州荣华仪器制造有限公司;T6新世纪紫外可见分光光度计,北京普析通用仪器有限责任公司。
1.3 实验方法
1.3.1 玉米须发酵液的制备
玉米须经清洗、粉碎,过60目筛,以料液比1∶8(g∶mL)加去离子水,90 ℃回流提取2 h后,121 ℃灭菌30 min冷却至室温。将L. paracasei和S.cescerevisiae以2∶1比例混合制备复合菌悬液,按10%的接种量接入玉米须水提液,于恒温振荡器120 r/min、34 ℃发酵72 h。发酵结束,将发酵液121 ℃灭菌30 min后冷却至室温。按2%的接种量接入巴氏醋杆菌菌液,于恒温振荡器120 r/min,32 ℃发酵24 h。发酵结束,过滤并离心,取上清液121 ℃灭菌30 min后冷却至室温。
1.3.2 体外连续模拟消化
体外连续模拟消化试验参考DONG等[10]的方法并略有改动。对玉米须发酵液进行口腔、胃肠道体外模拟消化。
模拟口腔消化:将50 mL发酵液装至250 mL锥形瓶中,然后加入50 mL模拟唾液(1 mmol/L CaCl2,每10 mL中加入0.65 mg α-淀粉酶100 U/L)混合。将pH值调至6.5并置于37 ℃水浴锅中振荡,于0、5、10、15、20 min分别均匀取样10 mL,离心取上清液即为口腔消化阶段样品。
模拟胃部消化:将剩余消化液pH值调到2.0,加入50 mL模拟胃液(NaCl 3.1 g、KCl 1.1 g、NaHCO3 0.6 g和CaCl2 0.15 g,完全溶解后加水定容至1 L,pH 2.0,每10 mL胃液加入25 mg胃蛋白酶)混合,将样品置于37 ℃、120 r/min的恒温摇床中避光振荡,于0、30、60、60、90、120 min分别均匀取样10 mL,离心后取上清液,得到胃消化阶段样品。
模拟肠部消化:将剩余的消化液pH值调至7.0,加入50 mL模拟肠液(0.1 mol/L NaHCO3,pH值调至7.0,每10 mL肠液加入4 mg胰酶、30 mg猪胆盐)混合,将样品置于37 ℃、120 r/min下的恒温摇床中避光振荡,于0、30、60、90、120 min分别均匀取样10 mL,离心取上清液即为肠消化阶段样品。玉米须水提液为未发酵组。
1.3.3 总多酚含量测定
参照汪娣等[11]的方法测定总多酚含量。取1 mL体外连续模拟消化过程中各时间点的样品溶液,依次加入0.4 mL福林酚、4 mL质量分数为7.5%的Na2CO3溶液,涡旋混匀后静置反应5 min。用蒸馏水定容至10 mL,置于50 ℃恒温水浴锅中避光反应5 min,于765 nm处测定吸光度。
1.3.4 总黄酮含量测定
参照MENA等[12]的方法测定总黄酮含量。取1 mL体外连续模拟消化过程中各时间点的样品溶液,分别加入300 μL 50 g/L NaNO2溶液、4 mL蒸馏水混匀,随后加入1 mL 100 g/L AlCl3溶液,充分混匀后静置5 min,加入2 mL 1 mol/L NaOH溶液、2.4 mL的蒸馏水,25 ℃振荡20 min,静置10 min以去离子水作为空白对照,于510 nm处测定吸光度。
1.3.5 DPPH自由基清除能力的测定
参考KWAW等[13]的方法并稍作改动。配制浓度为0.1 mmol/L的DPPH-乙醇工作液。移取1 mL体外连续模拟消化过程中各时间点的样品溶液,加入2 mL DPPH工作液并充分混匀,涡旋振荡30 s使其充分反应。于室温避光条件下反应30 min后,于517 nm处测定吸光度。样品对DPPH自由基清除能力按公式(1)计算:
DPPH自由基清除率![]()
(1)
式中:A1,样品的吸光度;A2,乙醇代替DPPH溶液的吸光度;A3,乙醇代替样品的吸光度。
1.3.6 羟自由基清除能力的测定
参考石雪萍等[14]的方法并稍作改动。移取1 mL体外连续模拟消化过程中各时间点的样品溶液,将其与2 mL 6 mmol/L的H2O2溶液、2 mL 6 mmol/L的FeSO4溶液混合,室温下静置10 min。加入2 mL 6 mmol/L的水杨酸溶液,充分混匀后于避光条件下静置30 min,于510 nm处测定吸光值。样品对羟自由基清除能力按公式(2)计算:
羟自由基清除率![]()
(2)
式中:A1,蒸馏水代替样品的吸光度;A2,样品的吸光度;A3,蒸馏水和水杨酸溶液的吸光度;A4,样品和水杨酸溶液的吸光度。
1.3.7 铁离子还原能力的测定
参考杨月杭等[15]的方法并稍作改动。移取1 mL体外连续模拟消化过程中各时间点的样品溶液,依次加入2.5 mL 0.2 mol/L磷酸盐缓冲液(pH 6.6)和2.5 mL 10 g/L的铁氰化钾溶液,混匀后50 ℃水浴锅中培育30 min,再加入2.5 mL 100 g/L的FeCl3溶液,离心取2.5 mL上清液,加入2.5 mL蒸馏水和0.5 mL 1 g/L的 FeCl3溶液,充分混匀静置10 min,以去离子水为空白对照,于700 nm处测定吸光度。
1.3.8 α-葡萄糖苷酶抑制率的测定
参考JIN等[16]的方法并作适当的修改。向3 mL pH 6.8磷酸盐缓冲溶液中加入100 μL体外连续模拟消化过程中各时间点的样品溶液,分别再加入0.5 mL 0.01 mol/mL对硝基苯基-β-D-吡喃葡萄糖苷溶液,混匀后放入37 ℃水浴锅中10 min后,加入0.5 mL 0.4 mg/mL α-葡萄糖苷酶溶液,再次放入37 ℃水浴锅中1 h,最后加入5 mL质量分数为4% Na2CO3溶液,于400 nm处测定吸光度。α-葡萄糖苷酶抑制率按公式(3)计算:
α-葡萄糖苷酶抑制率![]()
(3)
式中:A1,样品的吸光度;A2,缓冲液代替酶溶液的吸光度;A3,缓冲液代替样品的吸光度;A4,缓冲液代替样品和酶溶液的吸光度。
1.3.9 α-淀粉酶抑制率的测定
参考黎素玲等[17]的方法并作适当的修改。取100 μL体外连续模拟消化过程中各时间点的样品溶液分别和100 μL 0.5 U/mL α-淀粉酶溶液在37 ℃恒温水浴锅中5 min后,加入100 μL 5 g/L的淀粉溶液,继续于37 ℃水浴中20 min。随后加入1 mL 3,5-二硝基水杨酸溶液并充分混匀,沸水浴10 min后冷却至室温,5 500 r/min离心10 min,于410 nm处测定吸光度。α-淀粉酶抑制率按公式(4)计算:
α-淀粉酶抑制率![]()
(4)
式中:A1,样品的吸光度;A2,缓冲液代替酶溶液的吸光度;A3,缓冲液代替样品的吸光度;A4,缓冲液代替样品和酶溶液的吸光度。
1.4 数据处理
采用软件SPSS 22.0和Origin 2024软件进行数据分析。所有试验均重复3次,结果以“平均值±标准偏差”表示。
2 结果与讨论
2.1 体外消化过程中总多酚含量变化
如电子版增强出版附表1所示(https://doi.org/10.13995/j.cnki.11-1802/ts.043625,下同),与未消化的初始样品相比,玉米须发酵液在经过体外连续消化后总多酚含量升高。在口腔消化过程中,发酵组总多酚含量无显著变化。在胃消化过程中,发酵组总多酚含量变化显著增加(P<0.05),在胃消化120 min时达到最大值,为92.78 μg/mL。未发酵组在胃消化120 min后总多酚含量增加至76.84 μg/mL。总多酚含量在消化过程中的动态变化与消化体系的理化特性密切相关。一方面,胃蛋白酶的蛋白水解作用促使总多酚的释放,另一方面胃液酸性环境能够断裂多酚分子间的酯键和糖苷键,从而释放出更多的可溶性多酚。当样品进入到肠消化时,发酵组总多酚含量呈先上升后下降趋势,消化30~60 min显著升高,消化60~120 min显著降低。未发酵组的总黄酮含量变化趋势与发酵组一致。
肠消化阶段总多酚含量的增加可能与消化环境呈中性有关,部分酚类物质结构比较稳定,不易被分解,所以体外模拟肠消化总多酚含量增加,这也证明了胆汁和胰蛋白酶对总多酚含量的促进作用。随着消化时间的延长和pH值的变化,大分子进一步降解,碳水化合物与酚类物质的相互作用减弱,这些都有利于酚类物质的释放,从而在肠消化阶段显著增加[18]。生物活性成分有助于增强玉米须发酵液的抗氧化能力,而发酵基质和消化环境也受到影响。模拟体外消化过程中生物活性物质的变化分析进一步表明,胃肠道环境可能同样具备生物活性成分的提取功能。
2.2 体外消化过程中总黄酮含量变化
如附表2所示,在口腔消化过程中,发酵组总黄酮含量呈现逐渐上升的趋势,并在消化反应20 min时总黄酮含量达到最高17.92 μg/mL。在胃消化阶段结束后,玉米须发酵液中的总黄酮含量呈现出显著的上升趋势(P<0.05),发酵组在胃消化阶段总体呈上升趋势,在胃消化120 min时达到最大值45.38 μg/mL。进入肠消化阶段后,其总黄酮含量降低至44.13 μg/mL,随着消化进行,总黄酮含量升高。这可能是加入的肠消化液会导致原本的黄酮浓度降低,故在肠液消化初期阶段其黄酮含量要低于胃消化阶段[19]。但随着肠消化阶段时间的不断延长,在肠液的微碱性及其中胰蛋白酶的作用下,促使蛋白质水解,导致一些与蛋白质结合的黄酮类物质释放出来,故肠消化阶段后期黄酮含量升高[20]。
未发酵组在口腔消化过程中较发酵组总黄酮含量高,并在消化反应20 min时总黄酮含量达到最高23.08 μg/mL。未发酵组在胃消化30 min时达到最大值31.41 μg/mL。进入肠消化阶段,总黄酮含量总体呈上升趋势,发酵组较未发酵组总黄酮含量高,这可能是因为对玉米须进行发酵导致部分黄酮类物质转化为更易吸收的游离态,使其在肠消化阶段表现出更高的生物利用度。
2.3 体外消化过程中DPPH自由基清除能力变化
由图1所示,在口腔模拟消化过程中,DPPH自由基的清除能力呈现先升后降的变化趋势,消化到5 min时,发酵组清除率为36.44%,消化到20 min时,发酵组清除率降低至30.60%。在胃消化过程中,发酵组中的DPPH自由基清除能力显著增加(P<0.05),在消化120 min时达到最高58.95%。肠消化阶段,DPPH自由基清除率整体呈现递减趋势,发酵组和未发酵组在120 min内显著降低,分别达到最低值为49.73%和55.57%。DPPH自由基清除率的降低可能是由于胰蛋白酶降低了抗氧化活性物质的释放,更多疏水性氨基酸残基的侧链基团得以暴露,产生更多的亲水性氨基酸,难与脂溶性DPPH自由基反应,导致抗氧化性的降低[21]。
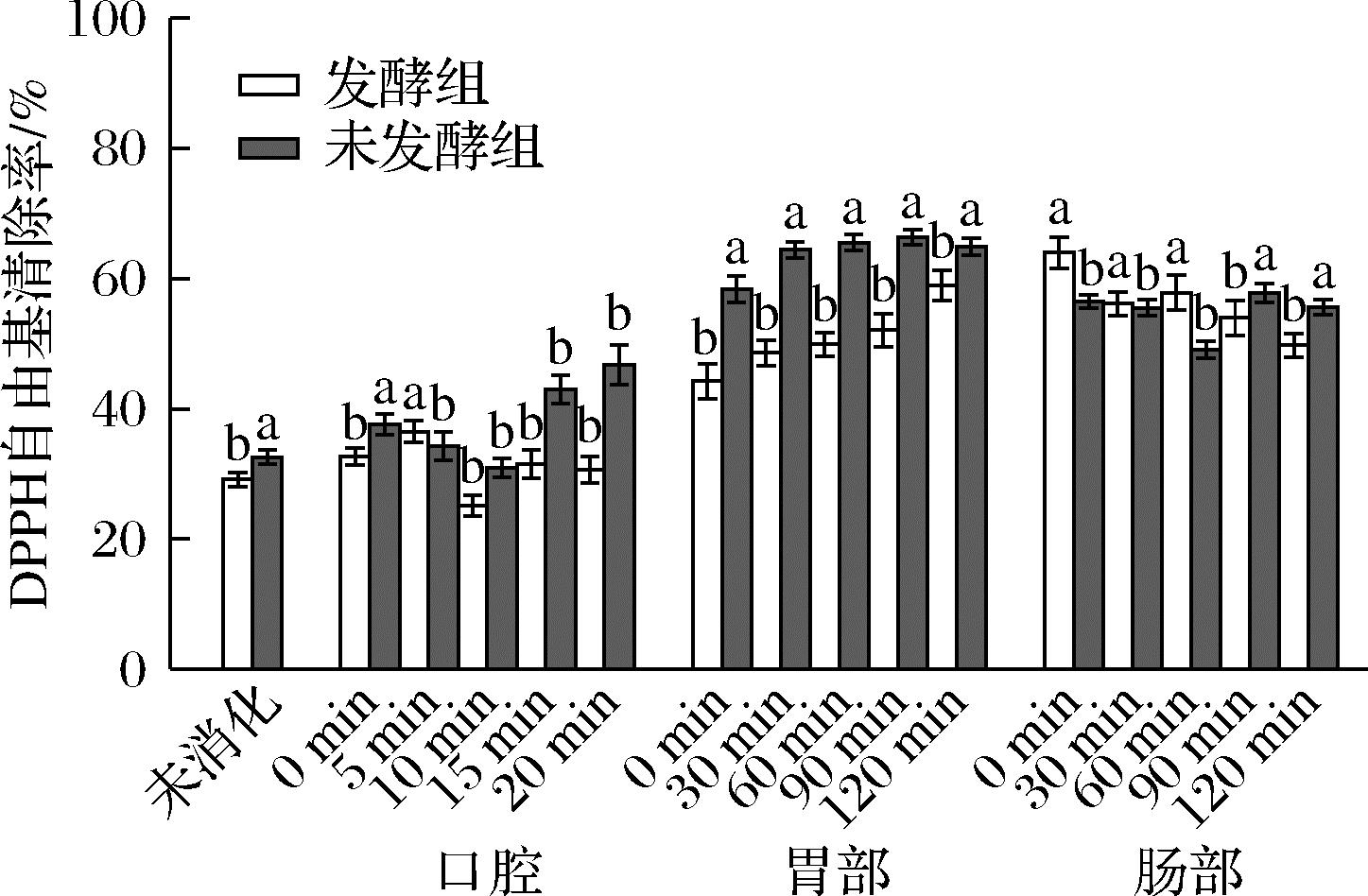
图1 DPPH自由基清除能力在体外消化中的变化
Fig.1 Changes in DPPH radical scavenging capacity in vitro digestion
注:不同小写字母表示差异显著(P<0.05)(下同)。
2.4 体外消化过程中羟自由基清除能力变化
由图2所示,在口腔消化阶段,羟自由基清除能力总体呈下降趋势。在胃部消化初期,发酵组的羟自由基清除能力显著提升至82.29%;随着消化时间的延长,清除率无显著变化。未发酵组羟自由基清除能力在胃消化过程中呈上升趋势,消化120 min结束后清除率达到71.92%。进入肠消化阶段,发酵组羟自由基清除能力在消化过程中呈先上升后下降趋势,最终羟自由基清除能力为86.61%,与肠消化0 min时相比,经过肠部消化结束后羟自由基清除能力明显上升。未发酵组羟自由基清除能力在肠消化阶段无显著变化。模拟胃部消化所呈现的强酸环境,会导致羟自由基与生物活性物质之间的电子转移过程减弱,因此胃消化液的羟自由基清除能力整体低于肠消化液[22]。此外,体外模拟消化过程中,肠消化阶段对羟自由基清除能力高于胃消化阶段,这与纪正业等[23]的研究结果相一致。
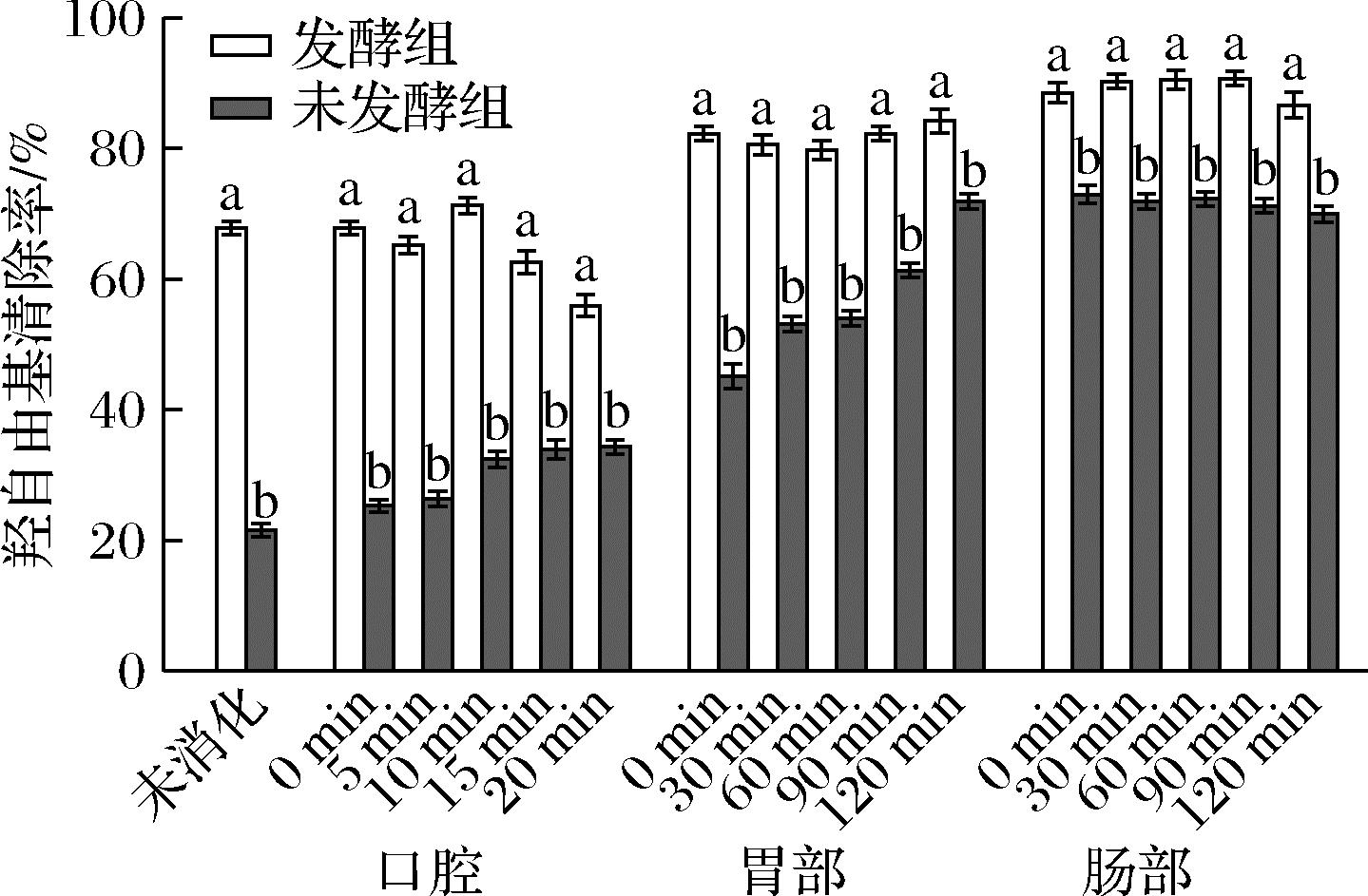
图2 羟自由基清除能力在体外消化中的变化
Fig.2 Changes in hydroxyl radical scavenging capacity in vitro digestion
2.5 体外消化过程中铁离子还原力变化
由图3所示,在口腔消化过程中,消化5 min时,发酵组吸光度降低至0.44,口腔消化结束发酵组吸光度提升至0.51。模拟胃消化过程中发酵组的铁离子还原力显著降低,到胃消化120 min结束时,发酵组的吸光度降至0.32,可能是酸性环境阻碍玉米须发酵液中皂苷、黄酮等活性物质的释放或迫使其发生结合或转化导致其含量降低,抗氧化活性与总黄酮等含量呈正相关,进而导致其抗氧化活性降低[24]。肠消化阶段,发酵组铁离子还原力呈先下降后上升的趋势,肠消化120 min后发酵组吸光度上升至0.32。未发酵组的铁离子还原力变化趋势与发酵组一致。这可能与肠道消化过程中活性物质浓度的变化有关,也可能与pH值的变化有关[25]。
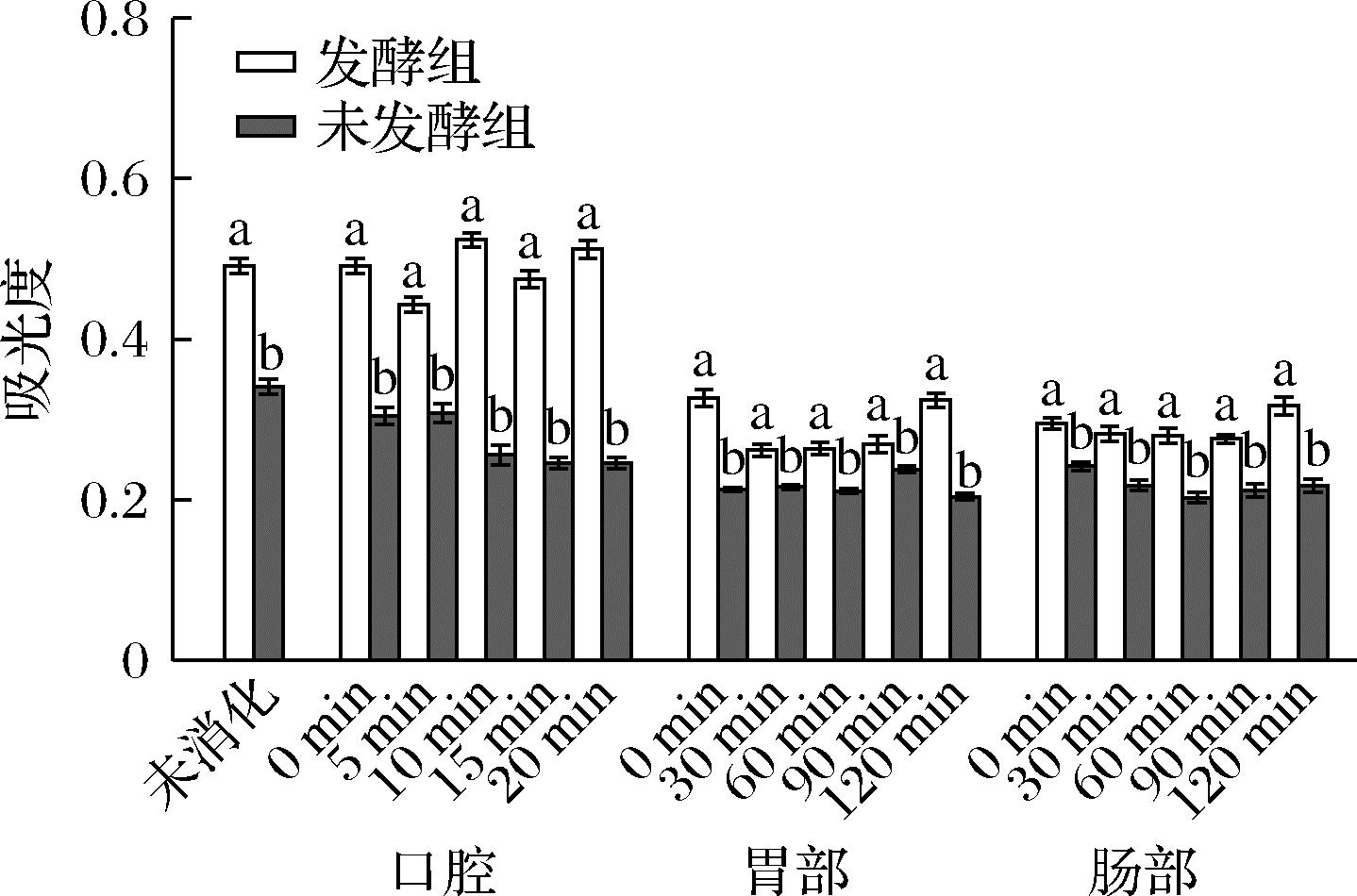
图3 铁离子还原力在体外消化中的变化
Fig.3 Changes in ferric reducing antioxidant power in in vitro digestion
2.6 体外消化过程中α-葡萄糖苷酶抑制率变化
由图4所示,在口腔消化阶段初期,玉米须发酵液对α-葡萄糖苷酶的抑制率呈现显著下降趋势。随着消化时间的延长,在胃部消化后,发酵组抑制率升高至62.67%,未发酵组的α-葡萄糖苷酶抑制率变化趋势与发酵组一致。肠消化阶段,消化90 min时发酵组α-葡萄糖苷酶抑制率显著提升至83.80%(P<0.05),随着肠消化的进行,抑制率无显著变化。未发酵组α-葡萄糖苷酶抑制率在肠消化过程中呈先下降再上升的趋势,肠消化120 min时,抑制率达60.77%。这可能是因为肠消化前期弱碱性的肠液破坏了活性物质与蛋白的结合,活性物质大量释放,抑制活性显著增强。在肠消化后期,α-葡萄糖苷酶抑制活性的稳定可能是由于小肠的近中性环境对α-葡萄糖苷酶的抑制率影响较小[26]。
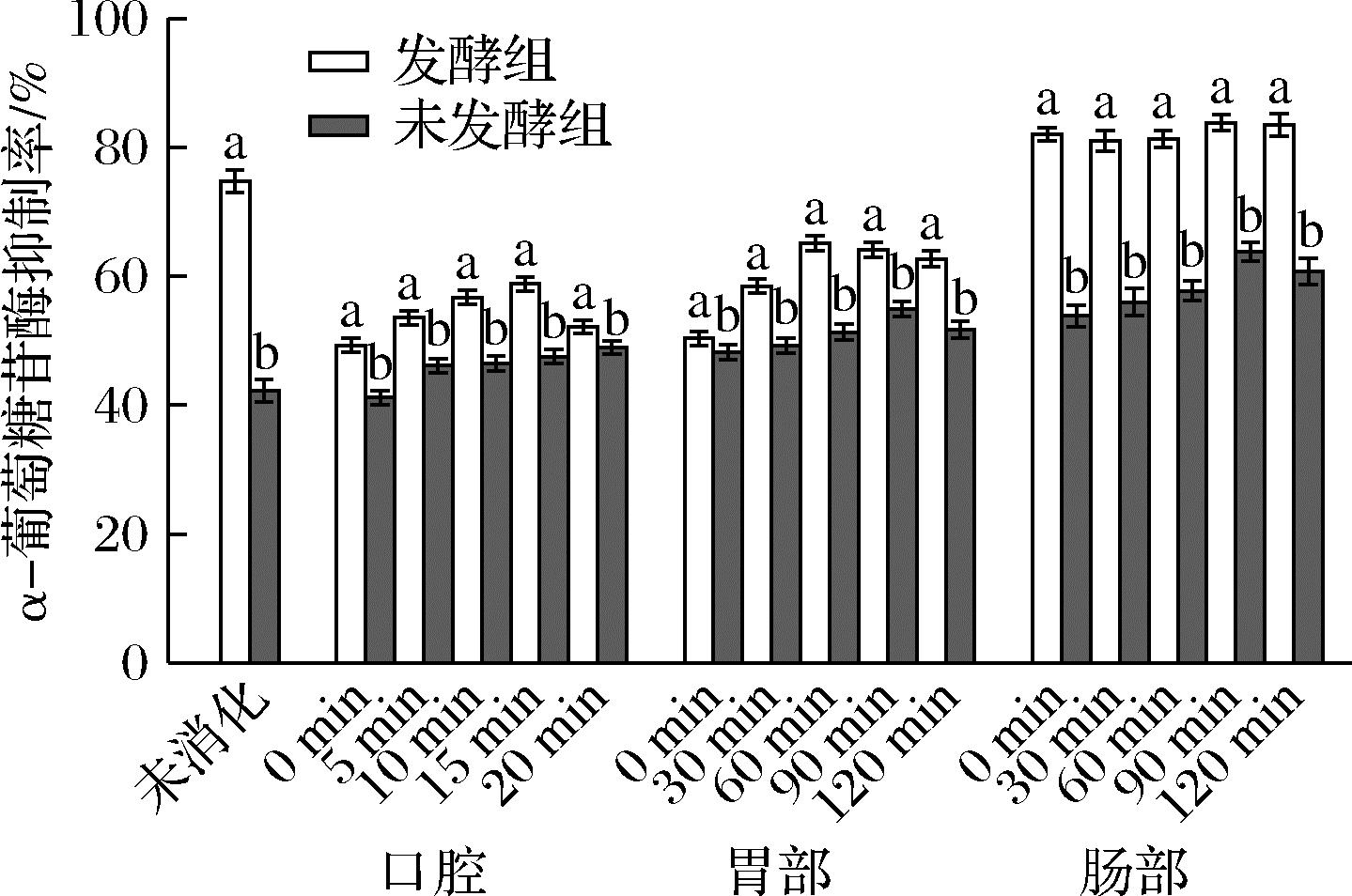
图4 α-葡萄糖苷酶抑制率在体外消化中的变化
Fig.4 Change in α-glucosidase inhibition rate in in vitro digestion
2.7 体外消化过程中α-淀粉酶抑制率变化
由图5所示,玉米须发酵液α-淀粉酶抑制率总体呈上升趋势。在口腔消化20 min时,发酵组α-淀粉酶抑制率提升至55.23%。在胃消化阶段,发酵组在胃消化30 min达到最大值75.39%,进入肠消化阶段,抑制率总体呈上升趋势,在肠消化到120 min时实验组抑制率提升至74.04%,对照组的α-淀粉酶抑制率变化趋势与实验组一致。发酵组与未发酵组后期经过胃肠道消化后α-淀粉酶抑制率增强,可能是含有的蛋白质发生了部分降解,形成多肽、氨基酸和还原糖。疏水氨基酸的存在通过改变α-淀粉酶内的疏水环境,导致酶的空间结构破坏[27]。同时,与未发酵组相比,发酵组经消化后α-淀粉酶抑制率更高,其可能原因在于玉米须经发酵处理后产生了成分差异,发酵组中的成分可直接与α-淀粉酶的活性位点结合,通过竞争性抑制作用阻碍底物分解[28]。多种抑制成分的协同效应可能在肠道阶段重新形成,进而导致抑制率升高。
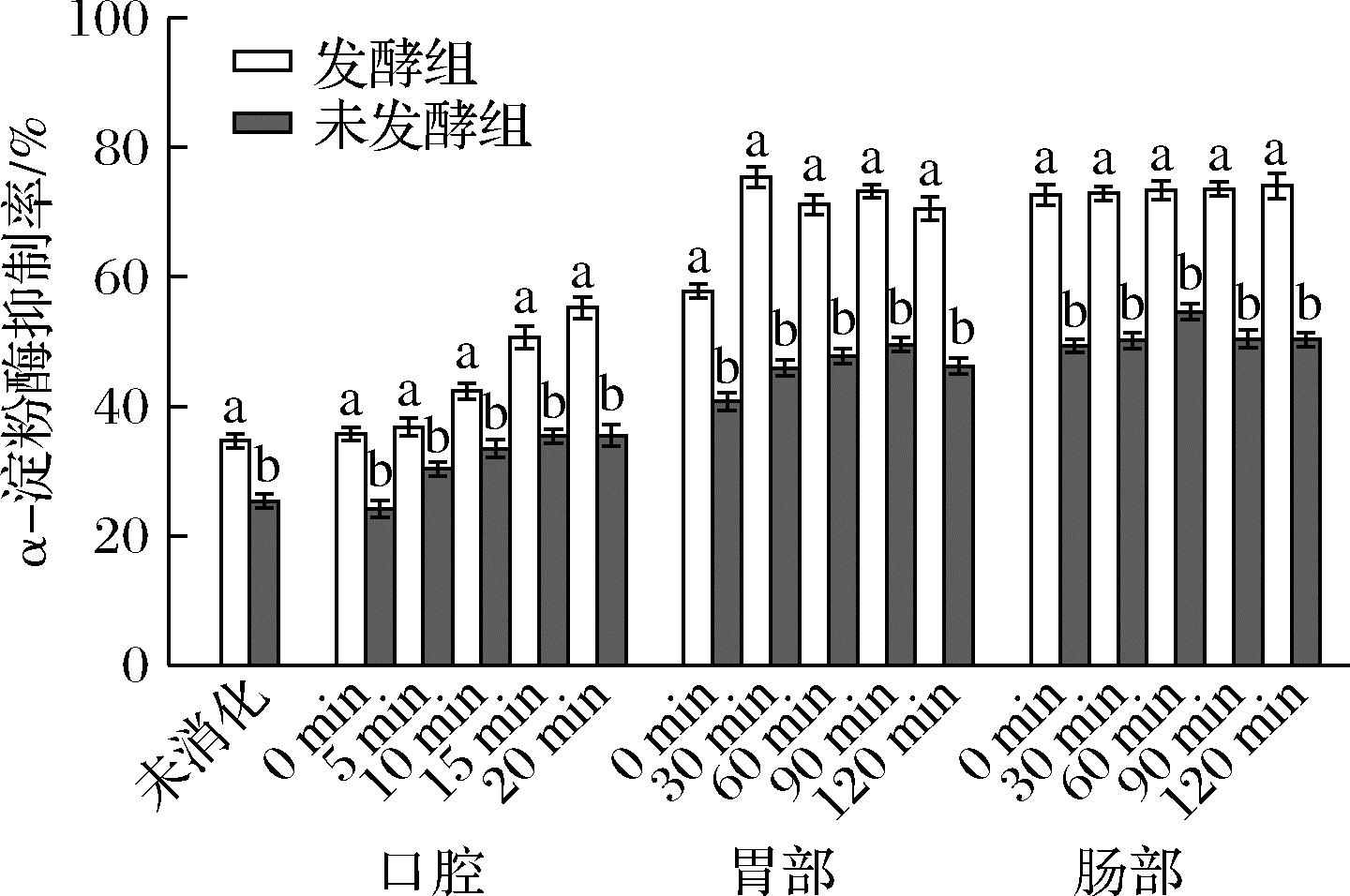
图5 α-淀粉酶抑制率在体外消化中的变化
Fig.5 Change in α-amylase inhibition rate in in vitro digestion
2.8 相关性分析
大量研究表明,植物的抗氧化能力、降血糖能力与其活性成分有关[29]。本研究测定了体外模拟消化过程中7项指标的变化,包括总多酚含量、总黄酮含量、DPPH自由基清除能力、羟自由基清除能力、铁离子还原力、α-葡萄糖苷酶抑制率、α-淀粉酶抑制率,以探究它们在消化过程中的相互作用及变化规律。如附图1所示,发酵组总多酚含量与羟自由基清除能力、α-葡萄糖苷酶抑制率呈极显著正相关(P<0.001),相关系数分别为0.804、0.902;与铁离子还原能力呈显著负相关(P<0.01),相关系数为-0.601;与其他指标显著相关(P<0.01)。发酵组总黄酮含量与α-淀粉酶抑制率、DPPH自由基清除能力和羟自由基清除能力之间存在极显著正相关(P<0.001)。铁离子还原能力与DPPH自由基清除能力、羟自由基清除能力呈极显著负相关(P<0.001),相关系数分别为-0.893、-0.890。由上述相关性分析说明发酵液的化学成分与功能活性之间存在显著的关联性。因此,玉米须发酵液中产生的酚类化合物与其生物活性存在强相关性,这一相关性凸显了酚类化合物对其生物活性的显著影响,且此类结论在其他食品副产品的相关研究中亦得到验证[30-31]。
3 结论
目前关于人类营养摄入的研究主要集中在食品中生物活性成分的提取和功能,少量研究考虑生物活性成分在体外消化过程中的释放和可能的变化。研究结果表明,经体外模拟消化后的活性物质增加,且总多酚和总黄酮含量显著高于未发酵组,其中发酵组的总多酚和总黄酮含量较未消化前分别增加了57.63%和77.45%。DPPH自由基清除能力、α-葡萄糖苷酶抑制率、α-淀粉酶抑制率在模拟体外消化过程中呈上升趋势,而铁离子还原能力呈下降趋势。本研究通过体外模拟消化对玉米须发酵液的总多酚和总黄酮含量、抗氧化能力和降血糖能力进行动态研究,为评价玉米须发酵液生物可及性提供理论依据。同时,各个生物活性成分在体外消化过程中的稳定性差异是否与其内在特性、降解途径、代谢物之间的相互作用有关,后续可以采用动物及细胞模型进一步验证。
[1] WANG Y M, MAO J L, ZHANG M, et al.An umbrella insight into the phytochemistry features and biological activities of corn silk:A narrative review[J].Molecules, 2024, 29(4):891.
[2] FOUG RE L, ZUBRZYCKI S, ELFAKIR C, et al.Characterization of corn silk extract using HPLC/HRMS/MS analyses and bioinformatic data processing[J].Plants, 2023, 12(4):721.
RE L, ZUBRZYCKI S, ELFAKIR C, et al.Characterization of corn silk extract using HPLC/HRMS/MS analyses and bioinformatic data processing[J].Plants, 2023, 12(4):721.
[3] SINGH J, RASANE P, NANDA V, et al.Bioactive compounds of corn silk and their role in management of glycaemic response[J].Journal of Food Science and Technology, 2023, 60(6):1695-1710.
[4] WANG X Z, DONG L, DONG Y F, et al.Corn silk flavonoids ameliorate hyperuricemia via PI3K/AKT/NF-κB pathway[J].Journal of Agricultural and Food Chemistry, 2023, 71(24):9429-9440.
[5] FAIZA N, IMRAN A, ARSHAD M U, et al.Valorization and characterization of corn by-product polyphenols through green extraction technologies[J].Frontiers in Nutrition, 2023, 10:1107067.
[6] 邰佳, 马海英.玉米须固体发酵的工艺优化研究[J].当代化工研究, 2022(15):165-167.TAI J, MA H Y.Optimization of solid fermentation process of corn silk[J].Modern Chemical Research, 2022(15):165-167.
[7] 王佳瑶, 李源, 李一鸣, 等.玉米副产物发酵饮料对链脲佐菌素诱导的糖尿病小鼠糖脂代谢的改善作用[J].食品工业科技, 2023, 44(4):395-402.WANG J Y, LI Y, LI Y M, et al.Effect of corn by-product fermented beverage on glucolipid metabolism in streptozotocin induced diabetes mice[J].Science and Technology of Food Industry, 2023, 44(4):395-402.
[8] GUO Y X, CHEN X F, GONG P, et al.Advances in the in vitro digestion and fermentation of polysaccharides[J].International Journal of Food Science and Technology, 2021, 56(10):4970-4982.
[9] 陈希苗, 李美英, 许秋莉, 等.体外模拟胃肠消化中山楂多酚及抗氧化活性的变化[J].食品科学, 2019, 40(5):31-37.CHEN X M, LI M Y, XU Q L, et al.Changes in polyphenol contents and antioxidant activity in hawthorn (Crataegus pinnatifida Bunge)during simulated gastrointestinal digestion[J].Food Science, 2019, 40(5):31-37.
[10] DONG X B, QI J, XU K, et al.Effect of lactic acid fermentation and in vitro digestion on the bioactive compounds in Chinese wolfberry (Lycium barbarum) pulp[J].Food Bioscience, 2023, 53:102558.
[11] 汪娣, 曾雪莹, 胡玉清, 等.野樱莓果酒酿造工艺优化及抗氧化活性分析[J].食品工业, 2023, 44(6):26-30.WANG D, ZENG X Y, HU Y Q, et al.Optimization of brewing technology and antioxidant activity of wild cherry berry wine[J].The Food Industry, 2023, 44(6):26-30.
[12] MENA P, S NCHEZ-SALCEDO E M, TASSOTTI M, et al.Phytochemical evaluation of eight white (Morus alba L.) and black (Morus nigra L.) mulberry clones grown in Spain based on UHPLC-ESI-MSn metabolomic profiles[J].Food Research International, 2016, 89:1116-1122.
NCHEZ-SALCEDO E M, TASSOTTI M, et al.Phytochemical evaluation of eight white (Morus alba L.) and black (Morus nigra L.) mulberry clones grown in Spain based on UHPLC-ESI-MSn metabolomic profiles[J].Food Research International, 2016, 89:1116-1122.
[13] KWAW E, MA Y K, TCHABO W, et al.Effect of Lactobacillus strains on phenolic profile, color attributes and antioxidant activities of lactic-acid-fermented mulberry juice[J].Food Chemistry, 2018, 250:148-154.
[14] 石雪萍, 郑萍.紫包菜花色苷提取工艺及其对DPPH·清除活性研究[J].食品研究与开发, 2018, 39(1):37-40.SHI X P, ZHENG P.Study on the extraction and DPPH·scavenging activities of anthocyanin from purple cabbage[J].Food Research and Development, 2018, 39(1):37-40.
[15] 杨月杭, 邱爱东, 夏陈, 等.不同酸性溶剂提取黑青稞麸皮多酚及其体外抗氧化和降血糖活性[J].粮食与油脂, 2025, 38(3):34-40.YANG Y H, QIU A D, XIA C, et al.Extraction of polyphenols from black highland barley bran with different acidic solvents and their in vitro antioxidant and hypoglycemic activities[J].Cereals &Oils, 2025, 38(3):34-40.
[16] JIN H M, DANG B, ZHANG W G, et al.Polyphenol and anthocyanin composition and activity of highland barley with different colors[J].Molecules, 2022, 27(11):3411.
[17] 黎素玲, 滕聪, 刘金阁, 等.条斑紫菜可溶性膳食纤维的理化性质及体外生物活性研究[J].食品安全质量检测学报, 2023, 14(22):9-18.LI S L, TENG C, LIU J G, et al.Study on the physicochemical properties and in vitro biological activities of soluble dietary fiber from Porphyra yezoensis[J].Journal of Food Safety &Quality, 2023, 14(22):9-18.
[18] ZHOU H L, HU Y Y, TAN Y B, et al.Digestibility and gastrointestinal fate of meat versus plant-based meat analogs:An in vitro comparison[J].Food Chemistry, 2021, 364:130439.
[19] 韩明冲, 李云嵌, 王怡惠, 等.体外模拟消化对三七叶化学成分、功能活性及皂苷变化的影响[J].食品科学, 2025, 46(12):57-66.HAN M C, LI Y Q, WANG Y H, et al.Effect of in vitro simulated digestion on changes in chemical composition, functional activity and saponins of Panax notoginseng leaves[J].Food Science, 2025, 46(12):57-66.
[20] 石志娇, 韦桂芳, 何旭华, 等.体外模拟消化对黑果腺肋花楸叶片抗氧化及抑制糖消化酶活性影响[J].食品与发酵工业, 2023, 49(14):147-153.SHI Z J, WEI G F, HE X H, et al.Effects of simulated digestion in vitro on activities of antioxidant and sugar digestion enzyme inhibition in Aronia melanocarpa leaves[J].Food and Fermentation Industries, 2023, 49(14):147-153.
[21] 万红霞, 孙海燕, 赵旭, 等.糙米、米糠和精米在体外模拟消化过程中抗氧化活性的变化规律[J].食品与生物技术学报, 2018, 37(1):93-99.WAN H X, SUN H Y, ZHAO X, et al.Changes in antioxidant activity regularity in brown rice, rice bran and polished rice during in vitro simulated digestion process[J].Journal of Food Science and Biotechnology, 2018, 37(1):93-99.
[22] WU C Y, WANG J, LIU N, et al.Phytochemical properties and antioxidant capacities of apple juice fermented by probiotics during refrigerated storage and simulated gastrointestinal digestion[J].Applied Biochemistry and Biotechnology, 2023, 195(10):6032-6049.
[23] 纪正业, 金红举, 周治强, 等.体外消化对金针菇粉抗氧化活性及α-葡萄糖苷酶和α-淀粉酶抑制活性的影响[J].食品安全质量检测学报, 2025, 16(3):176-183.JI Z Y, JIN H J, ZHOU Z Q, et al.Effects of in vitro digestion on antioxidant activity and α-glucosidase and α-amylase inhibitory activity of Flammulina velutipes powder[J].Journal of Food Safety &Quality, 2025, 16(3):176-183.
[24] SP NOLA V, PINTO J, LLORENT-MART
NOLA V, PINTO J, LLORENT-MART NEZ E J, et al.Changes in the phenolic compositions of Elaeagnus umbellata and Sambucus lanceolata after in vitro gastrointestinal digestion and evaluation of their potential anti-diabetic properties[J].Food Research International, 2019, 122:283-294.
NEZ E J, et al.Changes in the phenolic compositions of Elaeagnus umbellata and Sambucus lanceolata after in vitro gastrointestinal digestion and evaluation of their potential anti-diabetic properties[J].Food Research International, 2019, 122:283-294.
[25] MADUWANTHI S D T, MARAPANA R A U J.Total phenolics, flavonoids and antioxidant activity following simulated gastro-intestinal digestion and dialysis of banana (Musa acuminata, AAB) as affected by induced ripening agents[J].Food Chemistry, 2021, 339:127909.
[26] ZHAO Y Y, GONG Y H, WANG D, et al.Changes in phenols, antioxidant ability, in vitro hypoglycemic activity of Flos Sophorae immaturus during different drying methods[J].Journal of Food Measurement and Characterization, 2024, 18(10):8540-8554.
[27] OU Y J, XIE W, WANG H Y, et al.In vitro digestion of glycoproteins from Porphyra haitanensis:Effects on structure, hypoglycemic activity, and fermentation characteristics[J].International Journal of Biological Macromolecules, 2025, 289:138699.
[28] BANDI C K, AGRAWAL A, CHUNDAWAT S P.Carbohydrate-Active enZyme (CAZyme) enabled glycoengineering for a sweeter future[J].Current Opinion in Biotechnology, 2020, 66:283-291.
[29] LIM Y P, PANG S F, YUSOFF M M, et al.Correlation between the extraction yield of mangiferin to the antioxidant activity, total phenolic and total flavonoid content of Phaleria macrocarpa fruits[J].Journal of Applied Research on Medicinal and Aromatic Plants, 2019, 14:100224.
[30] CA AS S, REBOLLO-HERNANZ M, BERM
AS S, REBOLLO-HERNANZ M, BERM DEZ-G
DEZ-G MEZ P, et al.Radical scavenging and cellular antioxidant activity of the cocoa shell phenolic compounds after simulated digestion[J].Antioxidants, 2023, 12(5):1007.
MEZ P, et al.Radical scavenging and cellular antioxidant activity of the cocoa shell phenolic compounds after simulated digestion[J].Antioxidants, 2023, 12(5):1007.
[31] TU F, XIE C Y, LI H N, et al.Effect of in vitro digestion on chestnut outer-skin and inner-skin bioaccessibility:The relationship between biotransformation and antioxidant activity of polyphenols by metabolomics[J].Food Chemistry, 2021, 363:130277.