油茶(Camellia oleifera Abel)原产我国,又名茶子树、油茶树,为我国特有的木本油料树种,与油橄榄、油棕、椰子并称为世界四大木本油料植物[1]。油茶饼粕是油茶籽经过提取油脂后的残渣,是油茶产业主要的加工废弃物[2]。油茶饼粕含有丰富的营养物质、生物活性物质和微量物质,可以作为天然优良食品、饲料、化工等来源。练杰等[3]研究发现,油茶饼粕含脂肪、蛋白质、多糖、茶皂素、粗纤维等物质,其中粗脂肪为5%~8%,粗蛋白为12%~18%,糖类物质为30%~60%,茶皂素为10%~14%,粗纤维为5%~8%。但由于油茶饼味苦、不适口等原因,油茶饼粕长期以来没有得到合理的利用,大量的油茶饼粕被遗弃,造成资源浪费和环境污染[4]。
微生物发酵是一种提高植物副产物资源价值的有效方法。微生物在繁殖时会分泌酶类,如纤维素酶、果胶酶、半纤维素酶等,致使植物细胞壁破裂,促进其有效成分从胞内释放[5]。黄纯莹等[6]利用巨大芽孢杆菌和黑曲霉分别发酵三七药渣,发现发酵后三七药渣中多糖的含量比发酵前分别提高了5.74%和5.03%。此外,通过微生物的生物转化和微生物代谢,植物废渣可转化为有机肥、生物能源、高附加值产物,还可以做成环保吸附材料及蛋白饲料等产品。因此,通过发酵可使植物废渣中有效成分含量达到增效作用,加大资源利用率。
代谢组学是研究生物体内小分子代谢物及其动态变化的一种整合分析化学与生物信息学技术,其技术体系分为2类:非靶向代谢组学(采用高分辨质谱等技术全景扫描未知代谢物差异)与靶向代谢组学(聚焦特定通路精确定量目标化合物)[7]。目前,代谢组学常被用于揭示生理、病理及环境响应中的代谢调控网络[8-9]。因此,本研究以课题组前期分离得到的真菌粗壮脉纹孢菌(Neurospora crassa)和细菌副干酪乳酪杆菌(Lacticaseibacillus paracasei)D16作为微生物菌种,用于发酵云南油茶饼粕,分析2种菌种对油茶饼粕的增效作用,并采用基于超高效液相色谱-质谱联用技术的非靶向策略分析2种微生物发酵7 d的油茶饼粕中代谢物的整体差异,以鉴定微生物发酵增强油茶饼粕抗氧化活性关键代谢物。本研究可为油茶饼粕的开发利用提供理论依据。
1 实验材料
1.1 实验材料与预处理
油茶饼粕,由江西省林业科学院提供。将油茶饼粕与石油醚按1∶5(g∶mL)的料液比混合,并于通风橱中使用磁力搅拌器搅拌3 h脱脂,抽滤后自然风干,粉碎过筛,于-4 ℃密封贮藏[10]。粗壮脉纹孢菌、副干酪乳酪杆菌D16,项目组前期分别从发酵豆粕和云南乳饼中分离得到。
1.2 仪器与设备
DHG-9240A电热恒温鼓风干燥箱,上海齐欣科学仪器有限公司;SB-400DTY超声波清洗机,宁波新芝生物科技股份有限公司;Infinite F50酶标仪,帝肯贸易有限公司(上海);DZKW-4电热恒温水浴锅,北京中兴伟业仪器有限公司;BSA224S电子天平,赛多利斯科学仪器(北京)有限公司;5430R高速冷冻离心机,德国Eppendorf公司;LDZF-50L-I灭菌锅,上海申安医疗器械厂;TS-111B恒温摇床,上海天呈实验仪器制造有限公司;SW-CJ-2FD洁净工作台,苏净集团苏州安泰空气技术有限公司。
1.3 实验试剂
NaNO2、NaOH、邻苯二甲酸氢钾(C8H5KO4)、K2S2O8、FeCl3、FeSO4,天津市风船化学试剂科技有限公司;福林酚、2,4,6-三吡啶基三嗪[2,4,6-Tri(2-pyridyl)-1,3,5-triazine,TPTZ]、芦丁、没食子酸、茶皂素、DPPH、ABTS、奎诺二甲基丙烯酸酯(6-Hydroxy-2,5,7,8-tetramethylchromane-2-carboxylic acid,Trolox)、维生素C、二丁基羟基甲苯(butylatedhydroxy toluene,BHT),上海源叶生物科技有限公司;Na2CO3、乙酸钠、酚酞、无水乙醇、无水甲醇,天津市大茂化学试剂厂;Al(NO3)3,广东光华科技股份有限公司;盐酸、硫酸,汕滇药业有限公司;香草醇,天津市科密欧化学试剂有限公司。
2 实验方法
2.1 菌种活化与培养
将粗壮脉纹孢菌、副干酪乳酪杆菌D16分别接种于PDA培养基和MRS培养基上,37 ℃恒温培养48 h 后分别挑取单菌落接种到PDA、MRS液体培养基中,得到浓度为1×105 个/mL的菌悬液[10]。
2.2 样品及发酵液制备
取3 g脱脂油茶粕粉末,加30 mL纯水,121 ℃高压蒸汽灭菌20 min,冷却至室温后,在未接种的脱脂油茶粕溶液中取样,作为空白对照,即为第0天发酵液。将4 mL浓度为1×105 个/mL的粗壮脉纹孢菌、副干酪乳酪杆菌D16菌悬液分别接种于脱脂油茶粕溶液中,于37 ℃恒温培养箱中培养7 d,每隔24 h等体积取样1次,取样后置于4 ℃冰箱中停止发酵[11],并将所有样品保存在-20 ℃冰箱备用。待所有发酵结束后,取出冻存样品,室温溶解,于4 ℃、8 000 r/min离心10 min,取上清液用于指标测定[11]。
2.3 pH与酸度测定
发酵液的pH值用pH计测定,其酸度参考GB 5009.239—2016《食品安全国家标准 食品酸度的测定》测定。取10 g样液(10 mL水作为空白对照)置于锥形瓶中,加入20 mL纯水,滴加2滴酚酞溶液,混匀后使用0.1 mol/L的NaOH溶液滴定至粉红色,保持5 s不褪色,记录NaOH溶液的使用量,通过公式(1)计算获得酸度值。
(1)
式中:X,样品总酸度,g/L;CNaOH,NaOH浓度,mol/L;V1,样品组NaOH消耗量,mL;V2,空白组NaOH消耗量,mL;K,酸的换算系数,g/mmoL,以柠檬酸计(0.064);V,样品体积,mL。
2.4 活性成分测定
2.4.1 总酚含量测定
参考刘晓海等[12]的方法并稍作修改。取50 μL样品液于酶标板中,接着加入125 μL 0.1 mol/L福林酚试剂混合,再加100 μL 75 g/L Na2CO3溶液,静置避光反应30 min,以纯水替代Na2CO3溶液作空白,于765 nm测定吸光度。标准曲线以没食子酸浓度梯度0、10、20、40、60、80、100 μg/mL构建,得线性方程y=0.012 9x+0.055 1(R2=0.998),据此计算样品总酚含量(μg GAE/mg)。
2.4.2 总黄酮含量测定
参考黄鑫等[13]的方法稍作修改。取40 μL样品液,依次添加20 μL质量分数3%的NaNO2溶液反应6 min、20 μL质量分数6%的Al(NO3)3溶液反应6 min 及140 μL质量分数4%的NaOH溶液反应15 min,于510 nm测定吸光度,以等体积纯水替代试剂作对照。标准曲线以芦丁浓度梯度0、100、200、400、600、800、1 000 μg/mL建立,得方程y=0.000 9x+0.044 8(R2=0.999),据此计算总黄酮含量(μg RT/mg)。
2.4.3 茶皂素含量测定
参考易笑生等[14]的方法,并稍作修改。取50 μL样品与50 μL 0.08 g/mL香草醛溶液混合,冰水浴中加入400 μL体积分数77%硫酸溶液,60 ℃水浴15 min后冰浴冷却,于550 nm测吸光度,以纯水替代香草醛和硫酸做空白。基于0、0.1、0.2、0.4、0.6、0.8、1.0 mg/mL茶皂素标准曲线(y=0.484 2x+0.021 2,R2=0.994),计算茶皂素含量(μg RT/mg)。
2.5 抗氧化活性测定
2.5.1 DPPH自由基清除率测定
参考李雅静等[15]的方法并稍作修改。将100 μL样品与等体积0.15 mol/L DPPH避光反应30 min,于517 nm测吸光度,以水为空白对照。采用0、5、10、20、30、40、50 μg/mL 维生素E梯度溶液建立标准曲线(y=-0.006 1x+0.403 7,R2=0.998),据此计算DPPH自由基清除能力,结果以μg Trolox/mg表示。
2.5.2 ABTS阳离子自由基清除率测定
参考李云嵌等[16]的方法并稍作修改。取50 μL样品与200 μL稀释ABTS工作液避光反应6 min,于734 nm测吸光度,以水为空白对照。采用0、5、10、20、30、40 μg/mL维生素E梯度溶液建立标准曲线(y=-0.011 6x+0.956 4,R2=0.996),据此计算ABTS阳离子自由基清除率,结果以μg Trolox/mg表示。
2.5.3 铁离子还原能力(ferric reducing antioxidant power,FRAP)测定
参考丁林玲等[17]的方法并稍作修改。取50 μL适当稀释样品与250 μL FRAP工作液混合,37 ℃反应10 min后于593 nm测定吸光度,以维生素C、BHT为对照。同等条件下测定10、20、40、60、80、100、120 μg/mL FeSO4梯度溶液建立标准曲线(y=0.012 5x+0.014 1,R2=0.999),计算FRAP并以μg FeSO4/mg表示。
2.5.4 代谢组学分析
代谢物提取:样本在4 ℃环境下缓慢解冻后,取适量样本加入预冷甲醇/乙腈/水溶液(2∶2∶1,体积比),涡旋混合,低温超声波处理30 min,-20 ℃静置10 min,4 ℃下以14 000×g离心20 min,取上清液,真空干燥,质谱分析时加入100 μL乙腈水溶液(乙腈∶水=1∶1,体积比)复溶,涡旋,4 ℃下以14 000×g离心15 min,取上清液进样分析。
色谱条件:样品采用Vanquish LC超高效液相色谱系统HILIC色谱柱进行分离;柱温25 ℃;流速0.5 mL/min;进样量2 μL;流动相组成A:水+25 mmol/L乙酸铵+25 mmol/L氨水,B:乙腈;梯度洗脱程序如下:0~0.5 min,95% B;0.5~7 min,B从95%线性变化至65%;7~8 min,B从65%线性变化至40%;8~9 min,B维持在40%;9~9.1 min,B从40%线性变化至95%;9.1~12 min,B维持在95%;整个分析过程中样品置于4 ℃自动进样器中。为避免仪器检测信号波动而造成影响,采用随机顺序进行样本的连续分析。样本队列中插入QC样品,用于监测和评价系统的稳定性及实验数据的可靠性。
质谱条件:样品经用Vanquish LC超高效液相色谱系统分离后,用Orbitrap ExplorisTM 480质谱仪进行质谱分析,分别采用电喷雾电离(ESI)正离子和负离子模式进行检测。ESI源及质谱设置参数如下:雾化气辅助加热气1(Gas1):50,辅助加热气2(Gas2):2,离子源温度350 ℃,喷雾电压(ISVF)正离子模式3 500 V,负离子模式2 800 V;一级质荷比检测范围70~1 200 Da,分辨率60 000,扫描累积时间100 ms,二级采用分段式采集方法,扫描范围70~1 200 Da,二级分辨率60 000,扫描累积时间100 ms,动态排除时间4 s。
2.6 数据处理
各项实验均进行至少3轮重复,结果表述为“平均值±标准差”。相关数据的统计处理采用SPSS 24.0版本软件内嵌的单变量方差分析(ANOVA)工具,以检验样本间的差异性(P<0.05)。图形绘制及呈现依靠Origin 2021软件与中科新生命云平台(https://bio-cloud.aptbiotech.com/login)、联川生物云平台(https://www.omicstudio.cn/tool)的功能。
3 结果与分析
3.1 两种益生菌发酵对油茶饼粕中pH、酸度的影响
发酵液的pH值反映了发酵的进程[18]。由图1-a可见,发酵24 h内,pH值下降速率最快,可能由于发酵初期条件适宜,粗壮脉纹孢菌、副干酪乳酪杆菌的迅速增殖、代谢产生了大量有机酸等物质,导致pH值下降。受2种微生物发酵影响,油茶饼粕pH值随时间下降,在第3天至第5天保持相对稳定。其中,粗壮脉纹孢菌与副干酪乳酪杆菌D16发酵的pH值在第2~3天降幅最大,分别从5.49降至5.02、从5.41降至5.13;对比2种益生菌发酵前后油茶粕的pH变化,副干酪乳酪杆菌D16的pH差值最大。
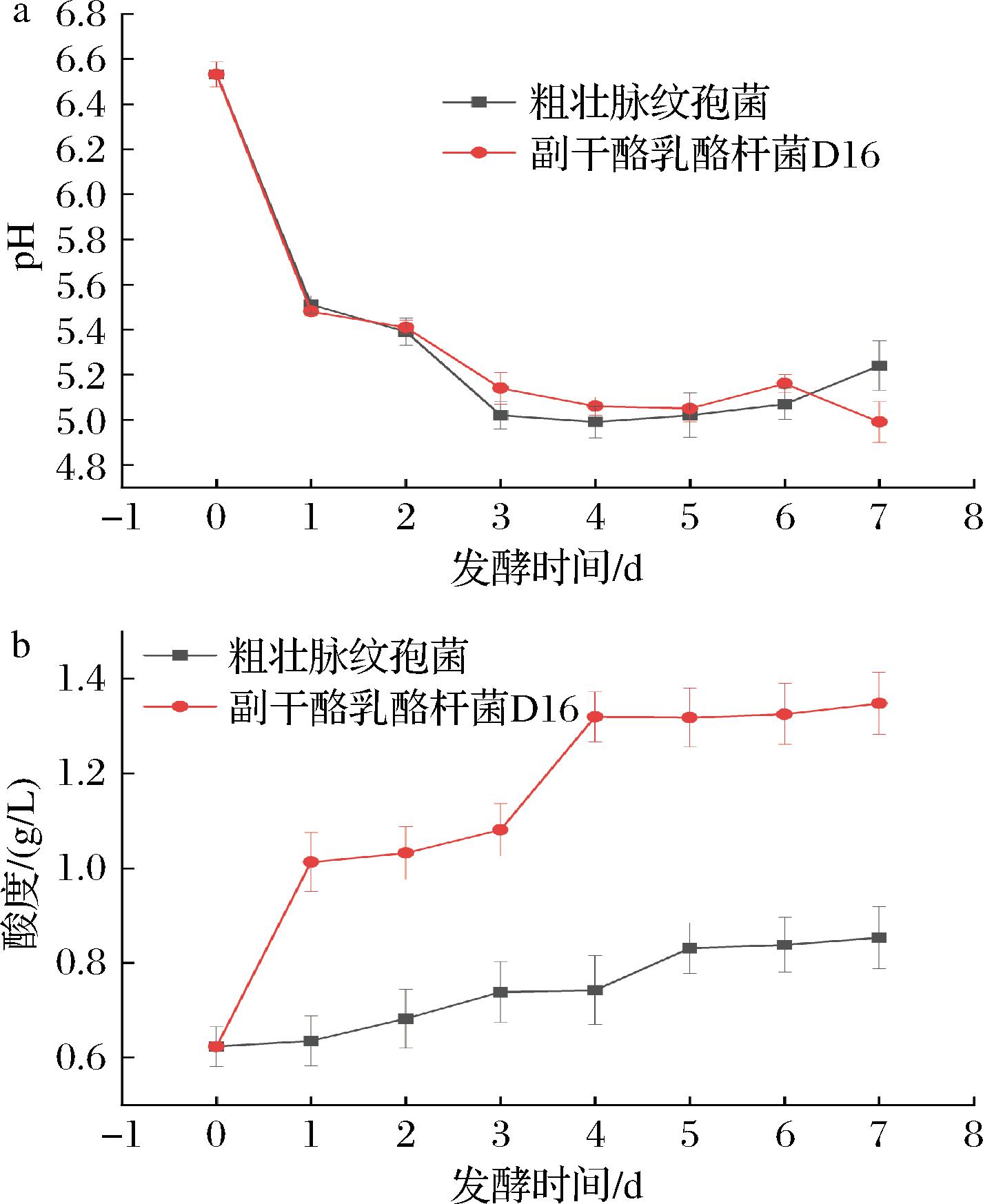
a-pH;b-酸度
图1 发酵过程中油茶饼粕的pH、酸度变化情况
Fig.1 Changes of pH and acidity of C.oleifera seed cake during the fermentation process
酸是水中能中和强碱的物质。由图1-b可知,与pH值变化趋势相反,2种微生物发酵液的酸度随时间上升,且均在第5天后趋于稳定。同一发酵时段内,粗壮脉纹孢菌发酵液酸度显著低于副干酪乳酪杆菌D16。副干酪乳酪杆菌D16发酵液酸度在第3~4天急剧上升,第7天达最高值1.35 g/L。结果表明,副干酪乳酪杆菌对油茶粕发酵效果较好。
3.2 两种益生菌发酵对油茶粕总酚、总黄酮和茶皂素含量的影响
多酚是一种天然存在于植物中的化合物,具有帮助人体清除自由基,保护细胞免受氧化损伤,延缓衰老的功效[19]。2种微生物发酵油茶饼粕总酚含量的变化如图2-a所示。发酵过程中,油茶饼粕的总酚含量均随时间下降。由粗壮脉纹孢菌发酵的油茶粕在第3天急剧下降,从4.09 μg GAE/mg降至1.73 μg GAE/mg,此后下降速率变缓;而副干酪乳酪杆菌D16发酵的油茶粕总酚含量始终维持较低水平,下降趋势也较为平缓。相关研究表明,微生物发酵可使植物中的总酚含量增加[20]。但本实验发现,总酚含量整体呈下降趋势,可能由于油茶饼粕中酚类物质被粗壮脉纹孢菌、副干酪乳酪杆菌D16降解转化,导致总酚含量降低[21]。对比发现,粗壮脉纹孢菌发酵的油茶粕总酚含量显著高于副干酪乳酪杆菌D16(P<0.05),发酵效果较好。
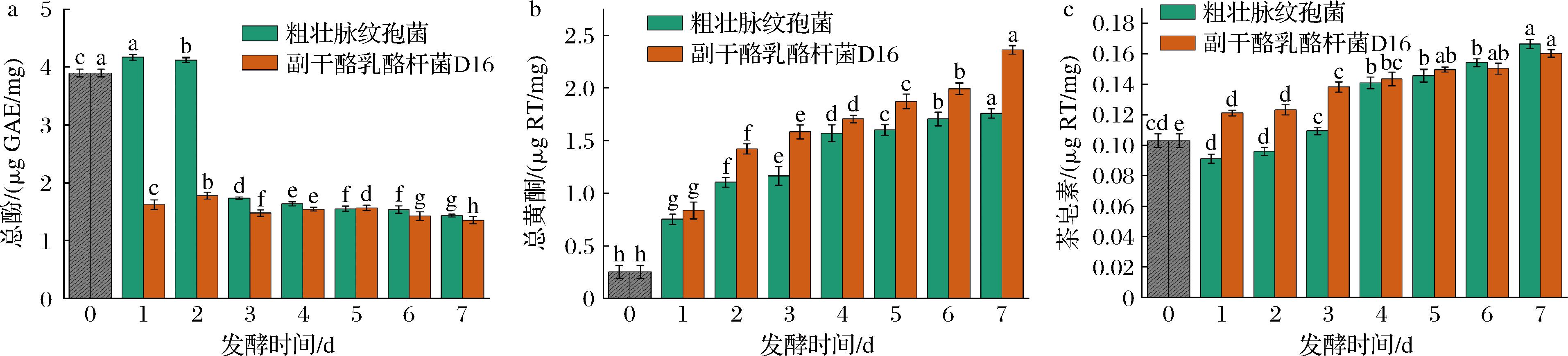
a-总酚;b-总黄酮;c-茶皂素
图2 发酵过程中油茶饼粕中总酚、总黄酮和茶皂素含量的变化
Fig.2 Changes of total phenols, total flavonoids, and tea saponins in C.oleifera seed cake during fermentation
注:不同小写字母表示差异显著(P<0.05)(下同)。
类黄酮是植物天然产生的一大类非营养化合物[22],同样具有良好的抗氧化功效。由图2-b可知,经粗壮脉纹孢菌与副干酪乳酪杆菌D16发酵的油茶粕,其总黄酮含量随发酵时间延长呈现逐步上升趋势,在发酵5 d后趋于稳定状态。同一发酵时间,副干酪乳酪杆菌D16发酵产物的总黄酮含量显著高于粗壮脉纹孢菌发酵产物(P<0.05)。这一现象可能归因于2种菌种来源的差异,进而导致其在油茶粕发酵过程中展现出不同的发酵性能。总黄酮含量在发酵早期增加可能归因于微生物代谢旺盛,消耗了油茶饼粕中的淀粉、蛋白质、果胶等成分,导致酚类和类黄酮的释放[23]。
在医药上,茶皂素能调节血脂、改善血液循环与血液状态,保护心肌细胞膜完整性[24-25]。由图2-c可知,粗壮脉纹孢菌与副干酪乳酪杆菌D16发酵油茶粕时,茶皂素含量均随发酵进行而上升,3 d后趋于稳定,发酵结束时达最高值,即粗壮脉纹孢菌和副干酪乳酪杆菌D16发酵7 d后的茶皂素含量分别为0.17、0.16 μg/mg。结果表明,发酵前期(1~3 d)副干酪乳酪杆菌D16发酵油茶粕茶皂素含量显著高于粗壮脉纹孢菌发酵油茶粕(P<0.05),发酵后期(4~7 d)无显著差异(P>0.05)。
3.3 两种益生菌发酵对油茶粕抗氧化活性的影响
多酚的酚羟基可作为氢供体,提供电子与DPPH自由基配对,进而快速清除自由基,发挥抗氧化作用[26],虽然总酚含量随着发酵时间的延长而降低,但是黄酮含量显著上升,可能是微生物通过定向生物转化将低活性的黄酮糖苷转化为高活性的游离苷合成其他强有效的抗氧化成分,最终提高了抗氧化能力[27]。由图3-a可知,2种微生物发酵的油茶粕对DPPH自由基的清除能力随发酵进程不断提升,发酵后期无显著性变化。粗壮脉纹孢菌发酵液的DPPH自由基清除能力显著强于副干酪乳酪杆菌D16发酵液(P<0.05),2种微生物发酵液的DPPH自由基清除能力分别在第5天和第7天达到峰值:粗壮脉纹孢菌0.75 μg Trolox/mg,副干酪乳酪杆菌D16 0.73 μg Trolox/mg。与未发酵样品相比,2种微生物发酵分别将油茶粕的DPPH自由基清除能力提升8.86倍和8.62倍,表明发酵能有效提升油茶粕的抗氧化性能。
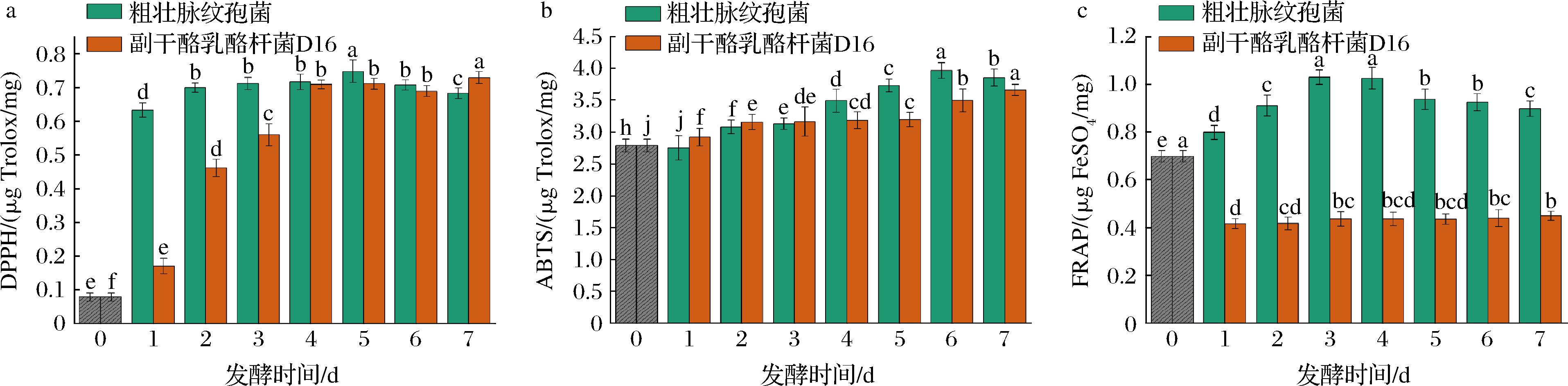
a-DPPH自由基清除能力;b-ABTS阳离子自由基清除能力;c-FRAP
图3 发酵过程中油茶饼粕DPPH、ABTS、FRAP的变化情况
Fig.3 Changes in the DPPH, ABTS, and FRAP of C.oleifera seed cake during fermentation
由图3-b可知,与DPPH自由基清除能力变化趋势一致,2种微生物发酵液的ABTS阳离子自由基清除能力随时间上升,其中,粗壮脉纹孢菌发酵液的ABTS阳离子自由基清除能力在第3~4天上升最快,第4~7天保持相对稳定,ABTS阳离子自由基清除能力由2.86 μg Trolox/mg上升到3.85 μg Trolox/mg,增加了35%。在发酵后期(6~7 d),2种微生物发酵液的ABTS阳离子自由基清除能力均达到最大值。整体上,粗壮脉纹孢菌发酵后油茶饼粕的ABTS阳离子自由基清除能力显著高于副干酪乳酪杆菌D16发酵的油茶饼粕(P<0.05)。
FRAP方法是基于氧化还原反应,在酸性条件下,Fe3+与TPTZ形成络合物(Fe3+-TPTZ)并被还原为Fe2+,该产物在593 nm处有清晰可见的最大吸收峰,且吸收变化与还原物质含量成比例,常被用于测定物质铁离子还原能力[28]。由图3-c可知,副干酪乳酪杆菌D16发酵液的铁离子还原能力在发酵过程中变化不明显,且均显著低于未发酵时的0.70 μg FeSO4/mg(P<0.05)。而粗壮脉纹孢菌发酵液的铁离子还原能力在前3 d逐渐上升且达到最高值1.03 μg FeSO4/mg,相较于未发酵样品上升了47%,此后逐渐下降并趋于稳定。3种抗氧化指标的结果综合表明,经粗壮脉纹孢菌发酵对油茶饼粕抗氧化能力的提升效果显著高于副干酪乳酪杆菌D16(P<0.05)。
4 代谢分析
采用基于液相色谱-质谱联用仪的非靶向代谢组学研究方法测定发酵7 d的粗壮脉纹孢菌发酵油茶粕(N.c)、副干酪乳酪杆菌发酵油茶饼粕(D16)、空白未发酵油茶饼粕(BC)3个样品的代谢产物数量,通过多元统计分析与单变量统计分析方法筛选不同时期的显著差异代谢物,然后对差异代谢物进行功能注释。经代谢组学分析,从所有样品中共鉴定出1 544种代谢物,其中正离子模式下检测到927种,负离子模式下617种,说明正离子模式能检测到更多的代谢物。如图4-a~图4-b所示,在类水平上,羧酸及其衍生物的占比最高(15.48%),其次是异戊二烯脂类(8.87%)和有机氧化合物(8.03%)。超类分析表明,脂质和类脂质分子占比为31.74%、有机酸及其衍生物占比为18.26%,两者是在超类中最丰富的类别,生物碱及其衍生物(0.58%)、木脂素、新木脂素及相关化合物(0.26%)是在超类中最少的类别。如图4-c~图4-d所示,主成分分析表明,2种电离模式下的不同菌种发酵的油茶饼粕样品具有明显的聚类,证实了组间代谢差异显著。
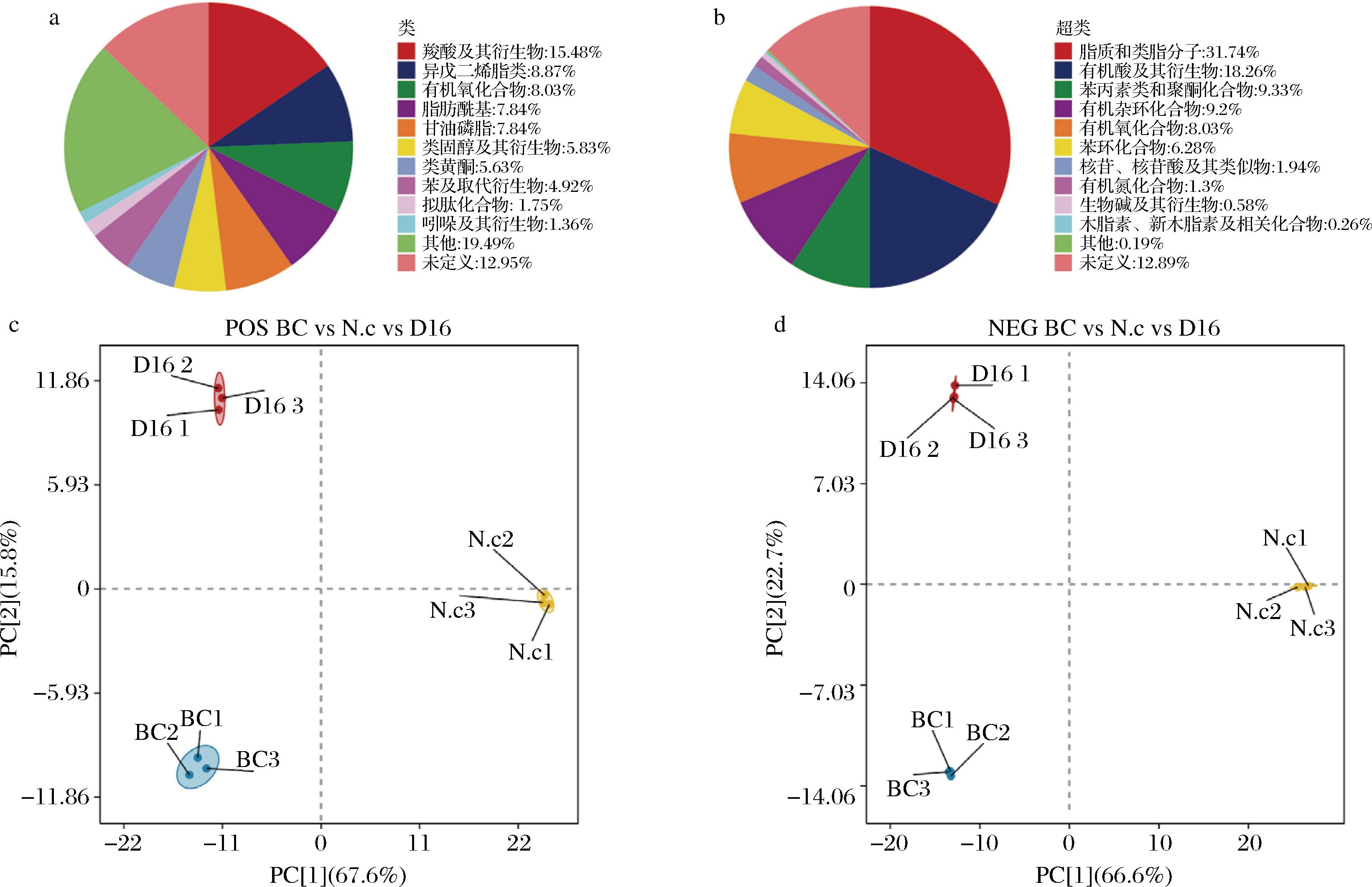
a-类条件下发酵油茶饼粕的代谢物分类;b-超类条件下发酵油茶饼粕的代谢物分类;c-发酵油茶饼粕在正离子模式下的PC评分图;d-发酵油茶饼粕在负离子模式下的PC评分图
图4 酵油茶饼粕代谢物分类及主成分分析评分
Fig.4 Metabolite classification and principal component analysis score of fermented C.oleifera seed cake
注:BC是空白对照组、N.c是粗壮脉纹孢菌发酵油茶饼粕、D16是副干酪乳酪杆菌D16发酵油茶饼粕(图5同)。
4.1 差异分析
采用偏最小二乘判别分析获取变量重要性投影值(variable importance in projection,VIP),并选择VIP值排名前20的差异代谢物绘制聚类热图。如图5所示,在正离子模式下副干酪乳酪杆菌D16发酵的油茶饼粕的5-甲基苯并三唑、吡多醇等物质的表达量显著高于粗壮脉纹孢菌发酵的油茶饼粕,粗壮脉纹孢菌发酵的油茶饼粕中的异麦芽糖、表面活性剂、甜菜碱等物质的表达量显著高于副干酪乳酪杆菌D16发酵的油茶饼粕。5-甲基苯并三唑、吡多醇、N-甲基-3,4-亚甲二氧基苄胺等物质在副干酪乳酪杆菌D16发酵的油茶饼粕中的表达量显著高于空白发酵的油茶饼粕。空白发酵的油茶饼粕中腺嘌呤、腺苷、烟酰胺等物质的表达量显著高于副干酪乳酪杆菌D16发酵的油茶饼粕。异麦芽糖、表面活性剂、甜菜碱等物质在粗壮脉纹孢菌发酵的油茶饼粕中的表达量显著高于空白发酵的油茶饼粕。空白发酵的油茶饼粕(K)中腺嘌呤、腺苷、烟酰胺、(负)麦芽四糖、西替利嗪等物质的表达量显著高于粗壮脉纹孢菌发酵的油茶饼粕。在负离子模式下,副干酪乳酪杆菌D16发酵的油茶饼粕的胆色素原、苯乳酸、4-甲氧基黄酮等物质的表达量显著高于粗壮脉纹孢菌发酵的油茶饼粕,粗壮脉纹孢菌发酵的油茶饼粕中的棕榈酸、2,3-二羟基苯甲酸等物质的表达量显著高于副干酪乳酪杆菌D16发酵的油茶饼粕。胆色原素、苯乳酸、4-甲氧基黄酮等物质在副干酪乳酪杆菌D16发酵的油茶饼粕中的表达量显著高于空白发酵的油茶饼粕。空白发酵的油茶饼粕中麦芽四糖、西替利嗪等物质的表达量显著高于副干酪乳酪杆菌D16发酵的油茶饼粕。棕榈酸、2,3-二羟基苯甲酸等物质在粗壮脉纹孢菌发酵的油茶饼粕中的表达量显著高于空白发酵的油茶饼粕。空白发酵的油茶饼粕(K)中麦芽四糖、西替利嗪等物质的表达量显著高于粗壮脉纹孢菌发酵的油茶饼粕对不同微生物发酵油茶饼粕中差异代谢物进行对比,发现不同物质在不同微生物发酵油茶饼粕中的积累情况各有不同,这进一步揭示了粗壮脉纹孢菌发酵的油茶饼粕与副干酪乳酪杆菌D16发酵的油茶饼粕代谢物组成的差异性。
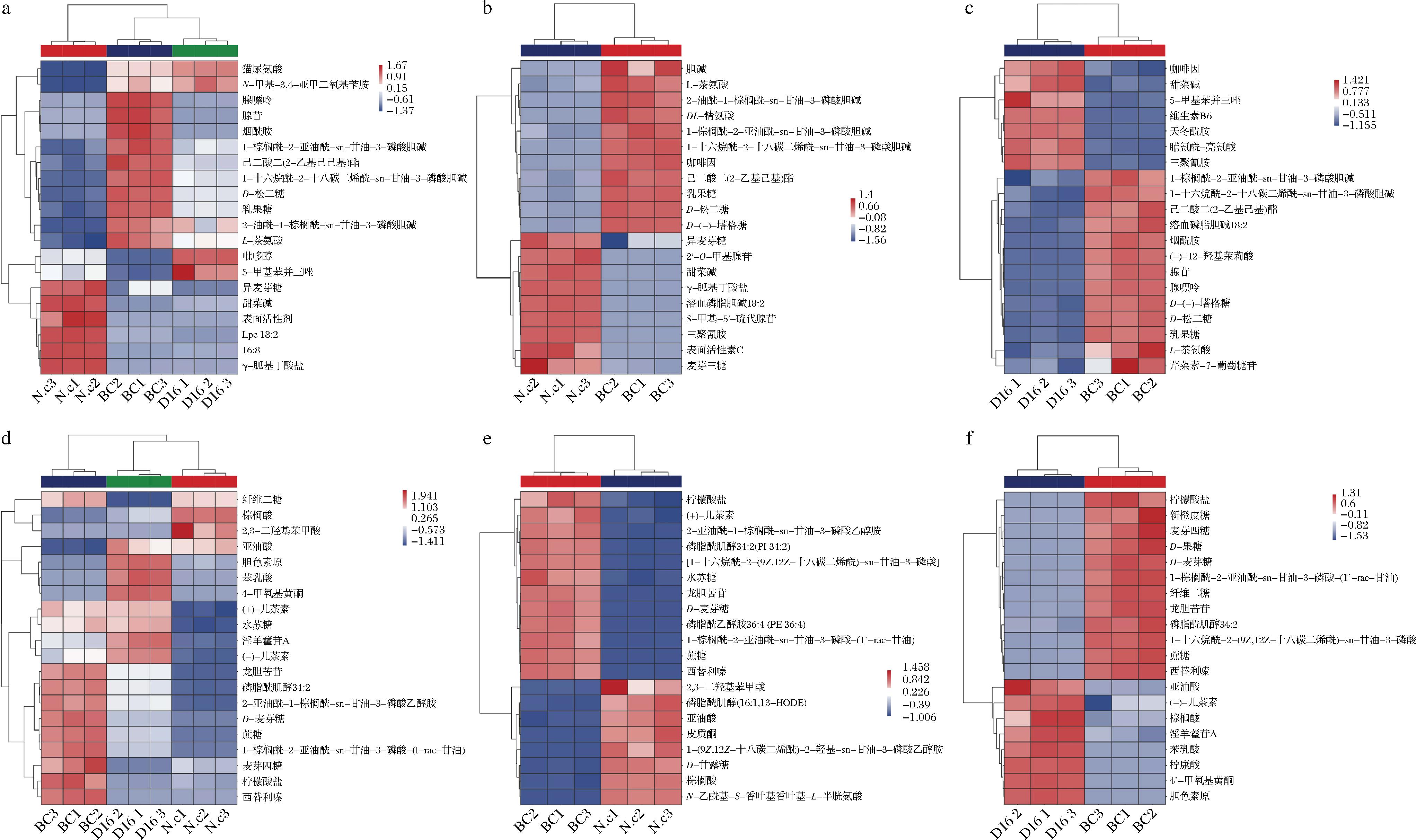
a-D16 vs N.c的正离子对比热图;b-BC vs N.c的正离子对比热图;c-D16 vs BC的正离子对比热图;d-D16 vs N.c的负离子对比热图;e-N.c vs BC的负离子对比热图;f-D16 vs BC的负离子对比热图
图5 不同微生物发酵油茶饼粕的代谢物热图
Fig.5 Heat map of metabolites produced by different microorganisms fermenting Camellia oleifera seed cake
4.2 关联性分析
采用Spearman相关性分析将代谢物与抗氧化活性及其他指标进行关联,结果以相关性热图表示,如图6所示。在正、负离子模式下,分别有许多不同类别的代谢物与抗氧化活性显著相关,这说明发酵油茶饼粕的抗氧化活性是许多代谢物协同作用的结果,而不是单一几个化合物的作用。其中,在负离子模式下,2,3-二羟基苯甲酸、纤维二糖、柠檬酸盐与抗氧化能力显著正相关(P<0.05),另外它们还与酸度值显著负相关,说明这些物质除了贡献抗氧化活性外,还参与调控发酵进程;在正离子模式下,甜菜碱、烟酰胺、异麦芽糖、溶血磷脂酰胆碱18∶2(LPC 18∶2)、腺苷与总黄酮、ABTS阳离子自由基显著正相关(P<0.05)。根据已报道的研究,2,3-二羟基苯甲酸和烟酰胺具有较强的抗氧化能力[29-30],柠檬酸盐和血磷脂酰胆碱18∶2可能通过螯合金属离子或辅助生成抗氧化物质间接发挥抗氧化能力[31-33]。这些与抗氧化指标显著相关的代谢物在油茶饼粕发酵过程中的含量变化可能决定了发酵饼粕的抗氧化强度,是微生物发酵发挥作用的关键代谢物。结果表明,油茶饼粕的功能活性由多种代谢物综合作用所决定,并非取决于单一类型成分,这也体现了其多成分、多作用靶点的特点。
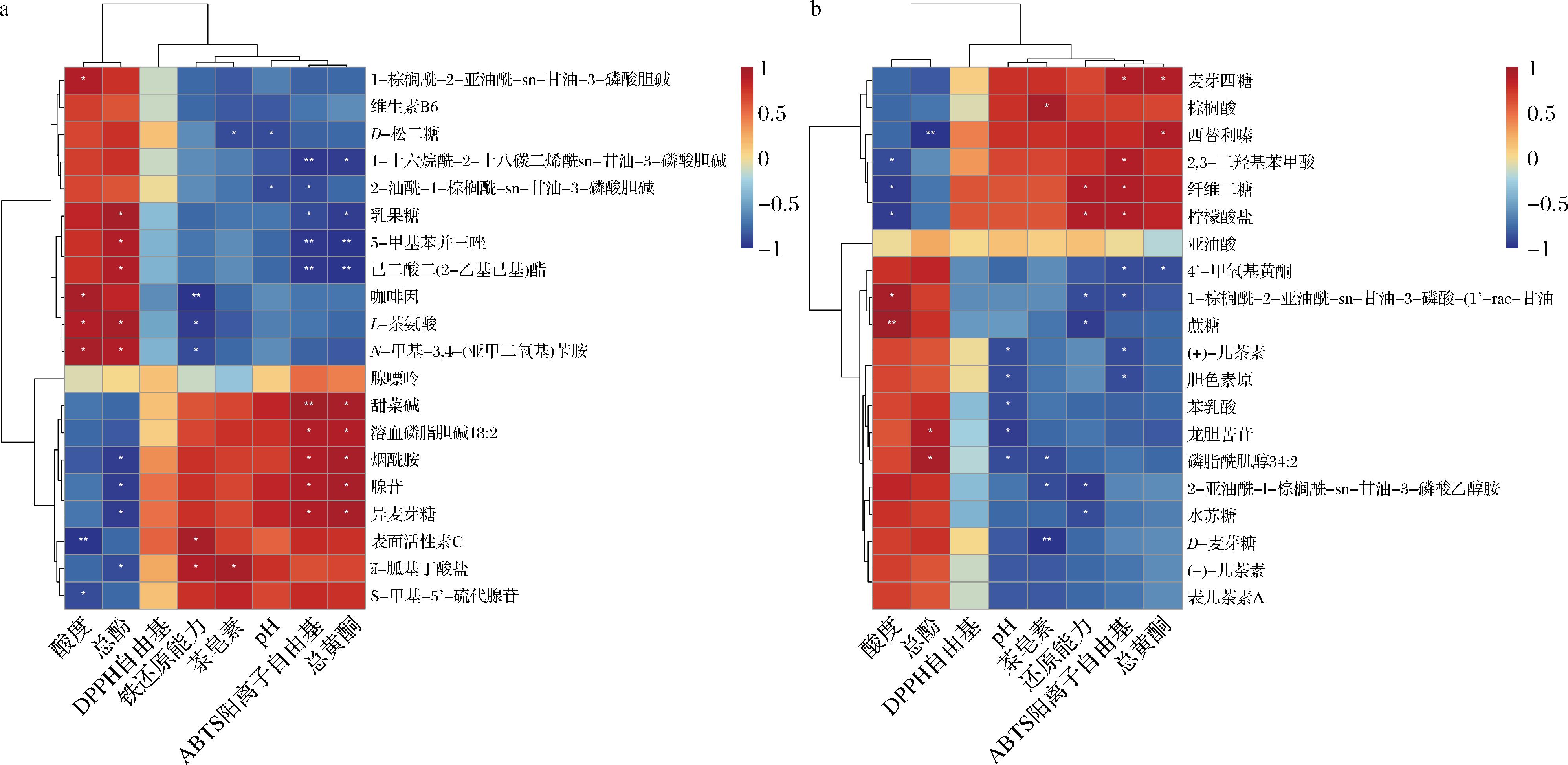
a-正离子模式;b-负离子模式
图6 不同微生物发酵油茶饼粕的差异代谢物(VIP值排名前20)与理化指标、抗氧化活性之间的相关性
Fig.6 Correlation between metabolites and physicochemical indicators of fermented C.oleifera seed cake by different microorganisms and antioxidant activity
注:*表示FDR校正(P<0.05);**表示FDR校正(P<0.01)。
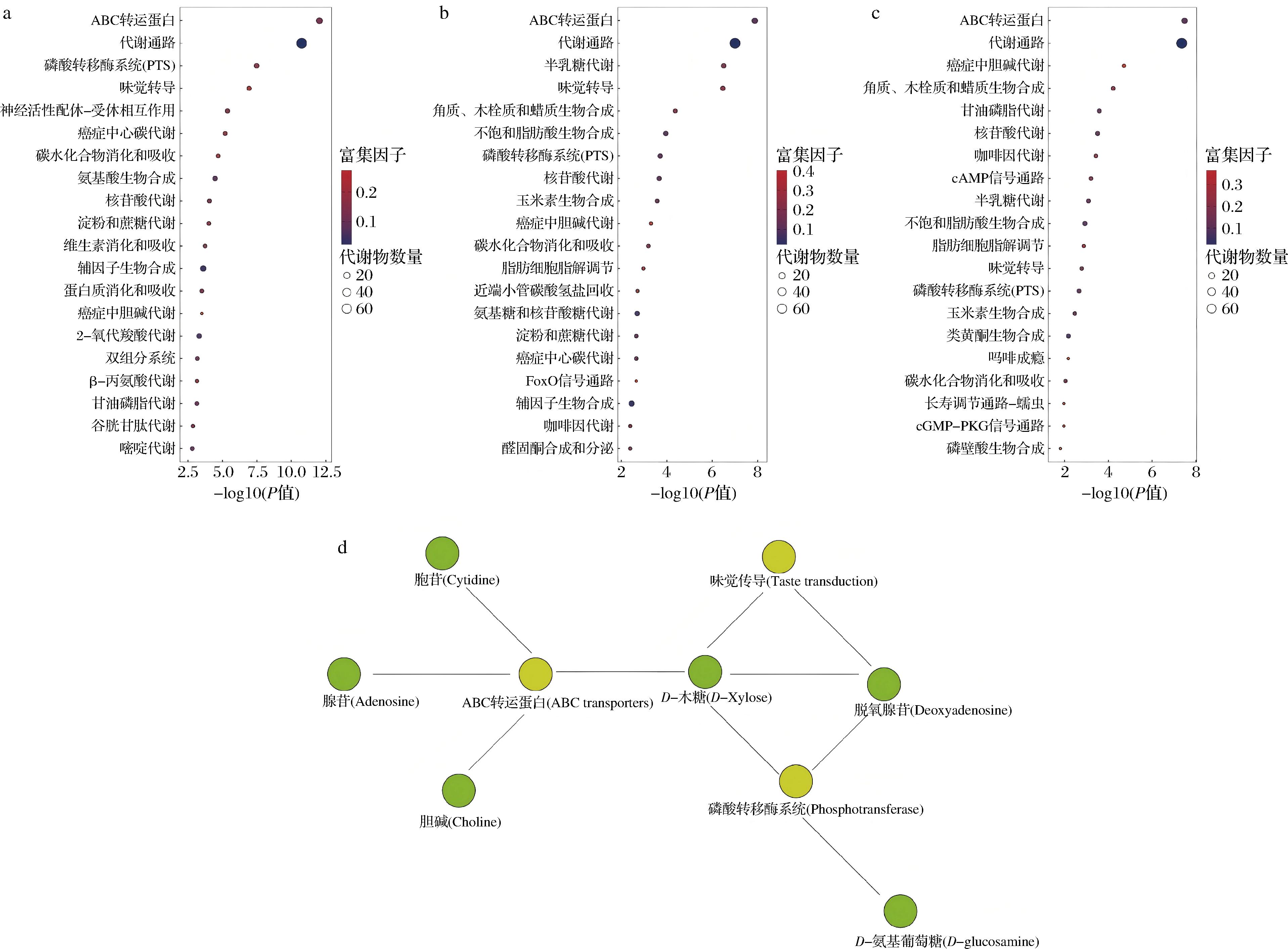
a-N.c与D16 的KEGG富集通路;b-N.c与BC的富集通路;c-D16 与BC的富集通路;d-网络图
图7 前20位KEGG富集途径图及关键代谢产物网络结构图
Fig.7 Top 20 KEGG enriched pathway diagrams and key metabolic product network structure diagram
4.3 代谢通路分析
为进一步比较不同微生物发酵油茶饼粕中差异代谢物参与的功能途径的差异,将数据导入MetaboAnalyst云平台,对差异代谢物参与的通路进行KEGG富集分析,结果如图7-a~图7-b所示。发现以ABC转运蛋白、味觉传导、磷酸转移酶系统、半乳糖代谢、癌症中的胆碱代谢5条代谢通路富集的代谢物较多。代谢途径中的关键代谢产物包括腺苷、D-木糖、脱氧腺苷等代谢产物,它们的网络结构图如图7-d所示。
5 结论
本研究系统比较了不同微生物发酵对油茶饼粕活性成分、功能活性及其代谢组学特征的影响,得出以下结论:不同微生物发酵油茶饼粕中总酚、总黄酮和茶皂素含量都呈现差异,发酵导致总酚含量下降,总黄酮和茶皂素含量上升。2种微生物发酵均提升了油茶饼粕的抗氧化能力,粗壮脉纹孢菌发酵的提升效果最佳。相关性分析显示,总黄酮含量增加的关键原因是微生物发酵增强油茶饼粕抗氧化作用。此外,代谢组学分析表明,脂质和类脂分子、有机酸及其衍生物、羧酸及其衍生物、苯丙素类化合物和聚酮类化合物、有机杂环化合物、类异戊二烯脂质类在代谢物中所占比例最大。差异代谢物主要富集在ABC转运蛋白、味觉传导、磷酸转移酶系统、半乳糖代谢、癌症中的胆碱代谢等5条代谢通路。这些发现为油茶饼粕资源的合理开发利用提供了科学依据,未来研究可进一步探讨油茶饼粕活性成分的作用机制及其在食品、饲料等领域的应用价值。
[1] QIU C Y, CHEN Z H, HU F J, et al.Simultaneous extraction of oil, protein and polysaccharide from residual seed cake of Camellia oleifera Abel.using three phase partitioning[J].Industrial Crops and Products, 2024, 209:117994.
[2] YIN S Q, LIU G Q, LIU X Q, et al.Study on solubility, water-holding capacity and stability of polypeptide from Camellia seed meal[J].Advanced Materials Research, 2014, 1033-1034:758-761.
[3] 练杰, 金青哲, 王兴国.油茶籽粕微生物发酵研究进展[J].中国油脂, 2012, 37(7):24-26.LIAN J, JIN Q Z, WANG X G.Research advance in microbial fermentation of oil-tea Camellia seed meal[J].China Oils and Fats, 2012, 37(7):24-26.
[4] 宁忻, 方伟, 董海燕, 等.云南墨红玫瑰主要营养成分分析[J].现代食品, 2021, 27(18):225-228.NING X, FANG W, DONG H Y, et al.Analysis and evaluation of the nutritional components in Rosa Crimson Glory[J].Modern Food, 2021, 27(18):225-228.
[5] 信珊珊, 丁浩, 杨阳, 等.酵母菌发酵植物粕类饲料研究进展[J].中国饲料, 2023(3):5-10.XIN S S, DING H, YANG Y, et al.Research progress on yeast-fermented plant meal feed[J].China Feed, 2023(3):5-10.
[6] 黄纯莹, 侯小涛, 杜正彩, 等.不同菌种发酵前后三七药渣中多糖的含量变化[J].食品安全质量检测学报, 2020, 11(10):3164-3168.HUANG C Y, HOU X T, DU Z C, et al.Changes of polysaccharide content in Panax notoginseng residue before and after fermentation with different strains[J].Journal of Food Safety &Quality, 2020, 11(10):3164-3168.
[7] CEVALLOS-CEVALLOS J M, REYES-DE-CORCUERA J I, ETXEBERRIA E, et al.Metabolomic analysis in food science:A review[J].Trends in Food Science &Technology, 2009, 20(11-12):557-566.
[8] 范琦琦, 赵香香, 吴鸣, 等.代谢组学在谷物食品中的应用研究进展[J].食品工业科技, 2024, 45(7):35-43.FAN Q Q, ZHAO X X, WU M, et al.Advances in the application of metabolomics in cereal foods[J].Science and Technology of Food Industry, 2024, 45(7):35-43.
[9] 马兆晴, 耿雅雯, 王桥, 等.代谢组学在食品品质研究中的应用进展[J].食品安全质量检测学报, 2023, 14(23):1-8.MA Z Q, GENG Y W, WANG Q, et al.Progress in application of metabolomics in the study of food quality[J].Journal of Food Safety and Quality, 2023, 14(23):1-8.
[10] 吴永祥, 吴丽萍, 胡晓倩, 等.不同真菌固体发酵对蕨菜主要活性成分及其体外抗氧化和抗炎症作用的影响[J].食品科学, 2018, 39(24):168-174.WU Y X, WU L P, HU X Q, et al.Effect of solid-state fermentation with various fungi on main bioactive components of Pteridium aquilinum and their antioxidant and anti-inflammatory activities in vitro[J].Food Science, 2018, 39(24):168-174.
[11] YANG M, TAO L, ZHAO C C, et al.Antifatigue effect of Panax notoginseng leaves fermented with microorganisms:In-vitro and in-vivo evaluation[J].Frontiers in Nutrition, 2022, 9:824525.
[12] 刘晓海, 茹月蓉, 张雪春, 等.103种药食两用植物化学成分分析及功能活性评价[J].中国食品学报, 2024, 24(8):385-402.LIU X H, RU Y R, ZHANG X C, et al.Analysis of the chemical constituents and evaluation of the functional activities of 103 kinds of medicinal and edible plants[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(8):385-402.
[13] 黄鑫, 刘晓海, 张雪春, 等.墨红玫瑰营养和化学成分、体外抗氧化和护肤活性研究[J].食品与发酵工业, 2025, 51(4):205-213.HUANG X, LIU X H, ZHANG X C, et al.Nutritional and chemical composition, in vitro antioxidant and skincare activities of Rosa ‘Crimson Glory’[J].Food and Fermentation Industries, 2025, 51(4):205-213.
[14] 易笑生, 刘汝宽, 肖志红, 等.正丁醇提取油茶饼粕中茶油和茶皂素的研究[J].中国粮油学报, 2016, 31(4):67-71.YI X S, LIU R K, XIAO Z H, et al.Research on tea oil and tea saponin extracted by N-butyl alcohol from pressed Camellia cake[J].Journal of the Chinese Cereals and Oils Association, 2016, 31(4):67-71.
[15] 李雅静, 宋静, 陈万谨, 等.3种云南酿酒葡萄皮渣的营养、化学成分及功能活性[J].食品科学, 2024, 45(12):194-204.LI Y J, SONG J, CHEN W J, et al.Nutrient and chemical composition and functional activity of three varieties of wine grape pomace from Yunnan[J].Food Science, 2024, 45(12):194-204.
[16] 李云嵌, 何霞红, 吴光顺, 等.干燥方式对三七叶主要活性成分、体外抗氧化、α-葡萄糖苷酶抑制活性、挥发性成分和代谢物的影响[J].食品科学, 2023, 44(21):98-113.LI Y Q, HE X H, WU G S, et al.Effect of drying method on the major active components, in vitro antioxidant activity, α-glucosidase inhibitory activity, volatile components, and metabolites of Panax notoginseng leaves[J].Food Science, 2023, 44(21):98-113.
[17] 丁林玲, 谢颖欣, 高伟, 等.三叶木通果肉提取物的体外抗氧化及抑制α-葡萄糖苷酶和乙酰胆碱酯酶能力[J].南方农业学报, 2021, 52(4):1058-1065.DING L L, XIE Y X, GAO W, et al.In vitro antioxidant activities, α-glucosidase and acetylcholinesterase inhibition ability of Akebia trifoliata pulp extracts[J].Journal of Southern Agriculture, 2021, 52(4):1058-1065.
[18] PAN T, XIANG H Y, DIAO T T, et al.Effects of probiotics and nutrients addition on the microbial community and fermentation quality of peanut hull[J].Bioresource Technology, 2019, 273:144-152.
[19] ZAMAN S, AHMAD R, ABDULAZIZ BINOBEAD M, et al.Polyphenolic contents and antioxidant potential in Nasturtium officinale[J].Journal of King Saud University-Science, 2024, 36(6):103223.
[20] 张居新. 铁皮石斛汁乳酸菌发酵特性及其乳酸菌饮料制备[D].芜湖:安徽工程大学, 2020.ZHANG J X.Fermentation characteristics of lactic acid bacteria in Dendrobium ironum juice and its lactic acid bacteria beverage preparation[D].Wuhu:Anhui University of Technology, 2020.
[21] 宫晓玥. 铁皮石斛植物乳杆菌发酵及其发酵物活性研究[D].海口:海南大学, 2020.GONG X Y.Fermentation of Lactobacillus plantarum and its fermentation activity in Dendrobium iridum[D].Haikou:Hainan University, 2020.
[22] CAMACHO M D M, ZAGO M, GARC A-MART
A-MART NEZ E, et al.Free and bound phenolic compounds present in orange juice by-product powder and their contribution to antioxidant activity[J].Antioxidants, 2022, 11(9):1748.
NEZ E, et al.Free and bound phenolic compounds present in orange juice by-product powder and their contribution to antioxidant activity[J].Antioxidants, 2022, 11(9):1748.
[23] 卢赛赛, 许凤, 王鸿飞, 等.杨梅叶中总黄酮提取及其抗氧化能力研究[J].果树学报, 2015, 32(3):460-468.LU S S, XU F, WANG H F, et al.Extraction and antioxidant activities of total flavonoids from Myrica rubra leaves[J].Journal of Fruit Science, 2015, 32(3):460-468.
[24] 杨孝辉, 郭君.超高压法提取油茶籽粕中茶皂素的工艺研究[J].粮食与油脂, 2023, 36(2):106-109.YANG X H, GUO J.Study on extraction of tea saponin from Camellia oleifera seed meal by ultrahigh pressure[J].Cereals &Oils, 2023, 36(2):106-109.
[25] 尤龙, 张营, 范传海, 等.国内茶皂素应用研究进展[J].山东化工, 2018, 47(17):64-65.YOU L, ZHANG Y, FAN C H, et al.Domestic progress in application of tea saponin[J].Shandong Chemical Industry, 2018, 47(17):64-65.
[26] 贾贵华, 任雪峰.锁阳提取物抗氧化及降糖活性研究[J].中兽医医药杂志, 2020(4):15-22.JIA G H, REN X F.Antioxidant and hypoglycemic activity of Herba Cynomorii extract[J].Journal of Traditional Chinese Veterinary Medicine, 2020(4):15-22.
[27] ZHANG H C, YU H N.Enhanced biotransformation of soybean isoflavone from glycosides to aglycones using solid-state fermentation of soybean with effective microorganisms (EM) strains[J].Journal of Food Biochemistry, 2019, 43(4):e12804.
[28] 陈玉霞, 刘建华, 林峰, 等.DPPH和FRAP法测定41种中草药抗氧化活性[J].实验室研究与探索, 2011, 30(6):11-14.CHEN Y X, LIU J H, LIN F, et al.Determination of antioxidative activity of 41 kinds of Chinese herbal medicines by using DPPH and FRAP methods[J].Research and Exploration in Laboratory, 2011, 30(6):11-14.
[29] FU X Z, BELWAL T, HE Y H, et al.UPLC-Triple-TOF/MS characterization of phenolic constituents and the influence of natural deep eutectic solvents on extraction of Carya cathayensis Sarg.peels:Composition, extraction mechanism and in vitro biological activities[J].Food Chemistry, 2022, 370:131042.
[30] BLANCO-DOVAL A, BARRON L J R, ALDAI N.Changes during lactation in the mineral element content of mare milk produced in semi-extensive rural farms[J].Journal of Food Composition and Analysis, 2023, 123:105629.
[31] ZHANG L, GUO K J, HUANG Y K, et al.Preparation and characterization of liposoluble tea polyphenol based functional emulsion films and the regulation of its releasing property[J].Food Chemistry, 2025, 476:143413.
[32] RAJAGOPAL M S.Canarium patentinervium Miq.(Burseraceae Kunth.):A phytochemical and pharmacological study[J].The University of Nottingham (United Kingdom), 2014,47(2):157.
[33] QIANG X, ZHAO M, XIA T, et al.The functional components and hepatic protective mechanism of wolfberry vinegar by mixed-culture fermentation[J].Foods, 2025, 14(7):1278.