粮谷类制品是我国居民的传统主食,其中所含的镁元素多分布于谷物的表层,对其进行精深加工会使镁元素大量流失,使得居民从中获取的镁严重不足。镁是人体必需的矿物质,在细胞中仅次于钾,参与人体80%以上的代谢和350多种酶促反应;是参与DNA、RNA和蛋白质的合成及维持核酸稳定的关键元素[1-2],同时,还具备调节神经传导、肌肉收缩,维持心血管和骨骼健康等功能[3-4]。人体摄入的镁主要来自植物性食品中的绿色蔬菜、全谷物、豆类、坚果以及动物性食品等,但植物性食物中植酸、草酸、多酚等物质会影响镁的吸收[5]。动物性食品的过量摄入会引起高血压、高血脂、高血糖等并发症。因此,消费者通常借助补镁剂来补充日常所需的镁元素。目前市面上的补镁剂主要分为无机镁和有机镁。前者必须依靠载体或者消耗机体内相关的酶,才能够被吸收。后者在胃肠道中会受到食物成分,或与之同时服用的其他药物干扰;此外,还会和其他矿物质以及运输蛋白竞争吸收位点,这些因素都可能会对其生物利用度产生直接影响[6]。目前国内市场高镁吸收利用率的产品非常匮乏,花生肽螯合镁正是着眼于此而开展的研究。
花生是世界上重要的经济与营养作物,不仅富含油脂与蛋白质,还包含糖类、膳食纤维、维生素以及微量元素等多种人体必需的营养成分[7]。但中国产花生多用于榨油,花生蛋白资源未能充分利用[8]。为避免蛋白质资源的浪费,大力推进花生蛋白深加工产品的开发已成为亟待解决的重要任务。此外,花生蛋白不仅产量丰富,来源广泛,而且价格相对较低,易于获取,非常适合进行工业化大规模生产。花生蛋白水解物(peanut protein hydrolysate,PPH)作为花生蛋白的深加工产物,不仅稳定性显著提升,且可直接被小肠吸收,在增强人体免疫力方面发挥积极作用。其功能特性多元,已证实具备抗菌、抗氧化及降血压等生物活性[9-11],同时还拥有优异的金属离子螯合能力,能够通过特定作用机制与金属离子结合,形成稳定性常数高于单一氨基酸的螯合物。该螯合形式中,配体的保护作用可有效避免金属离子转化为难以溶解的无机盐,且此吸收途径无需与其他物质协同作用,即可实现高效吸收,进而显著提升金属离子的生物利用度[12-13]。因此,本研究以PPH为原料制备肽-镁螯合物,旨在开辟花生蛋白深加工的新方向,进一步提升其附加值。
本研究采用6种蛋白酶对花生蛋白进行酶解,将酶解产物与MgCl2·6H2O螯合,以螯合率为指标筛选出最佳的蛋白酶,然后通过单因素试验和响应面试验探究制备花生肽-镁螯合物(peanut peptide-magnesium complex,PPH-Mg)的最佳工艺条件,以期研制出一种镁结合能力强的PPH-Mg,再利用扫描电镜、红外光谱以及荧光光谱等一系列现代分析技术对PPH和PPH-Mg的结构进行解析,探究螯合前后物质的结构变化。本研究可为多肽-镁螯合物的工业化生产提供理论支撑,同时为新型高效补镁剂的研发与应用奠定基础。
1 材料与方法
1.1 材料与试剂
花生蛋白[蛋白质质量分数为(88.28±0.29)%],实验室自提;碱性蛋白酶(Alcalase 2.4 L FG)、木瓜蛋白酶、风味蛋白酶、中性蛋白酶(Neutrase 0.8 L),诺维信(中国)生物技术有限公司;Savinase酶、胰蛋白酶,上海源叶生物科技有限公司;MgCl2·6H2O,天津市科密欧化学试剂有限公司;盐酸,四川西陇科学有限公司;NaOH,洛阳昊华化学试剂有限公司;EDTA二钠盐标准滴定溶液,山东普惠分化学科技有限公司;无水乙醇,天津市富宇精细化工有限公司。
1.2 仪器与设备
FJS-6恒温数显磁力搅拌水浴锅,上海维诚仪器有限公司;PHSJ-3F实验室pH计,上海仪电科学仪器股份有限公司;离心机,上海安亭科学仪器厂;LGJ-25E冷冻干燥机,四环福瑞科仪科技发展(北京)有限公司;氨基酸分析仪,塞卡姆特仪器有限公司;傅里叶红外光谱仪,德国布鲁克公司;FS5荧光光谱仪,天美仪拓实验室设备(上海)有限公司;纳米粒度及zeta电位分析仪,丹东百特仪器有限公司;扫描电子显微镜,荷兰FEI公司。
1.3 实验方法
1.3.1 花生肽的制备
称取一定质量的花生蛋白粉,将其配成质量分数3%的花生蛋白溶液,将pH和温度调节至表1中蛋白酶的最适条件,加入蛋白酶进行水浴酶解,通过pH计持续测量pH值,并用1 mol/L NaOH溶液维持作用条件,酶解至特定时间(30、60、90、120、150、180、210 min)。反应完成后,将酶解液在100 ℃下煮沸10 min使酶失活,然后在室温条件下,以5 000 r/min离心20 min,收集上清液冻干得到不同水解度(degree of hydrolysis,DH)的PPH。
表1 六种蛋白酶的最适pH值和温度
Table 1 Optimum pH and temperature of six proteases
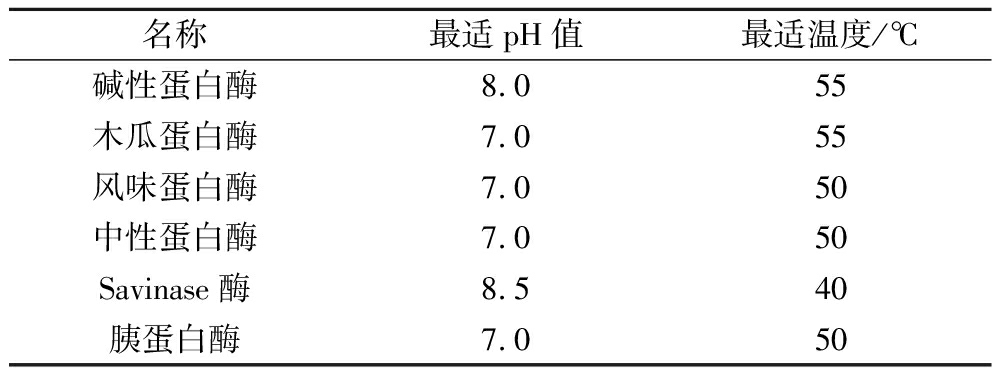
名称最适pH值最适温度/℃碱性蛋白酶8.055木瓜蛋白酶7.055风味蛋白酶7.050中性蛋白酶7.050Savinase酶8.540胰蛋白酶7.050
1.3.2 酶解液DH测定
利用pH-Stat法[14]测定花生蛋白的DH,由公式(1)~公式(3)进行计算。
(1)
(2)
pK=7.8+[(298-T)×2 400]/(298×T)
(3)
式中:V,酶解反应中消耗的碱液体积,mL;c,NaOH溶液的浓度,mol/L;m,底物中蛋白质的质量,g;htot,单位质量原料蛋白中肽键的总数,mmol/g,相对花生蛋白而言,htot=7.13 mmol/g;α,氨基的平均解离度;pK,氨基的解离常数;T,热力学温度。
1.3.3 螯合物的制备
称取一定质量的PPH加入去离子水配成质量分数3%的多肽溶液,调节溶液温度为40 ℃、pH值为7.5,按照PPH∶MgCl2·6H2O=6∶1(质量比)的比例,搅拌反应40 min,期间控制反应温度和pH值保持不变,反应结束后加入5倍的无水乙醇混匀,室温下,5 000 r/min离心20 min,取沉淀冷冻干燥后得到PPH-Mg。
1.3.4 镁含量及螯合率的测定
采用EDTA滴定法[15],测定镁含量,对PPH-Mg螯合反应进行评价。按照公式(4)进行计算。
镁螯合率![]()
(4)
式中:m,螯合物中镁的质量,mg;m0,加入反应体系中镁的总质量,mg。
1.3.5 螯合物得率的测定
采用公式(5)计算螯合物的得率。
螯合物得率![]()
(5)
式中:m1,螯合物总质量,mg;m2,加入反应体系中花生肽和镁的总质量,mg。
1.3.6 单因素试验
在50 ℃、50 min、pH值为7.5的条件下探究肽镁质量比(2∶1、4∶1、6∶1、8∶1、10∶1)对螯合率的影响;在肽镁质量比6∶1、50 ℃、50 min的条件下探究pH值(6.5、7.0、7.5、8.0、8.5)对螯合率的影响;在肽镁质量比6∶1、50 min、50 ℃、pH值为7.5的条件下探究时间(30、40、50、60、70 min)对螯合率的影响;在肽镁质量比6∶1、50 min、pH值为7.5的条件下探究温度(30、40、50、60、70 ℃)对螯合率的影响。
1.3.7 响应面试验
基于单因素试验,将螯合率作为响应值,运用Box-Behnken中心组合设计对反应条件做进一步优化,响应面试验的因素与水平如表2所示。
表2 响应面因素与水平
Table 2 Response surface factors and levels

编码因素水平-101ApH值7.07.58.0B肽镁质量比4∶16∶18∶1C温度/℃304050
1.3.8 氨基酸组成分析
称取一定质量PPH与PPH-Mg于样品试管中,加入10 mL浓度为6 mol/L的盐酸,充入N2后在(110±1) ℃烘箱内水解22 h,取出冷却后过滤至容量瓶并用一级水定容,吸取1 mL滤液于50 mL离心管中,在45 ℃的条件下干燥处理25 min,随后用1 mL一级水将其溶解,再次干燥,直至完全蒸干后,用1 mL pH值为2.2的样品稀释液溶解残留物,超声波处理1~2 min,之后通过0.22 μm过滤头过滤至液相小瓶中,使用氨基酸分析仪测定。
1.3.9 傅里叶变换红外光谱
将烘干12 h的KBr按照100∶1(质量比)与PPH和PPH-Mg粉末分别进行混合,在玛瑙研钵中研磨成均匀的粉末,在压片机中压成透明的薄片,扫描波长4 000~500 cm-1、扫描次数32。
1.3.10 荧光光谱
用去离子水将PPH和PPH-Mg配成1.0 mg/mL的溶液,荧光光谱法对样品扫描分析,激发波长280 nm,发射波长290~500 nm,裂缝宽度5 nm。
1.3.11 Zeta电位
将PPH和PPH-Mg配成1 mg/mL的溶液,利用纳米粒度及zeta电位分析仪对其进行电位分析。
1.3.12 扫描电镜
取PPH和PPH-Mg粉末均匀涂抹至导电胶上,喷金后在扫描电镜下观察其微观形貌,采集5 000×及10 000×的图片。
1.4 数据处理
所有实验均重复3次,结果用“平均值±标准差”表示。运用SPSS 26软件对数据加以处理,采用Duncan’s多重比较法进行显著性差异分析。响应面分析借助Design Expert 13软件完成,制图则使用Origin 2024软件。
2 结果分析
2.1 蛋白酶种类及其DH对螯合率的影响
由图1可知,各类蛋白酶对花生蛋白的水解程度有所差异,不过总体趋势相近,皆伴随酶解时间的延长,酶解液的DH起初升高,随后逐渐趋向稳定。这可能是因为不同蛋白酶的酶切位点及活性不一样,导致所获酶解产物不同,暴露的螯合位点在种类与数量上也有较大区别。螯合率呈现出先上升后下降的变化态势,而且即便酶解液的DH相同,螯合率依然存在差异,这表明螯合率和DH之间并未呈现出显著的线性关系。当DH过小时,多肽所暴露的螯合位点不多,与Mg2+的结合不够充分;相反,如果DH过大,螯合位点又会被破坏,同样不利于螯合反应的进行[16]。
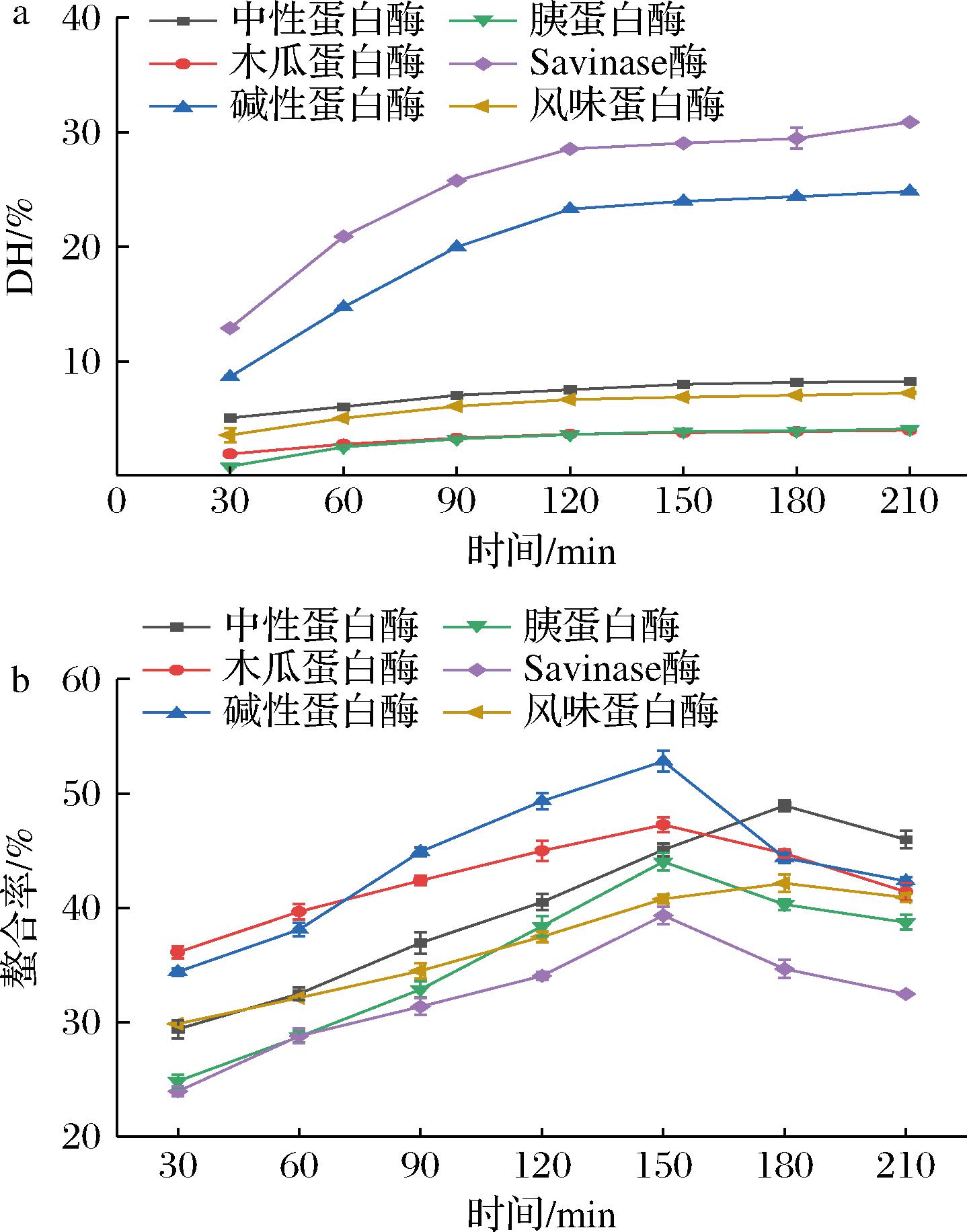
a-DH;b-螯合率
图1 不同蛋白酶及酶解时间对酶解液DH及螯合率的影响
Fig.1 Effect of different proteases and enzyme digestion time on the enzyme solution on degree of hydrolysis and chelating rate
综合来看,在酶解时间为150 min时,碱性蛋白酶作用下的花生蛋白酶解液具有更高的螯合率,达到了(52.81±0.21)%,所以本研究选择碱性蛋白酶作为实验用酶。
2.2 单因素试验结果
2.2.1 温度对螯合率及螯合物得率的影响
由图2-a可知,伴随温度逐步升高,螯合率以及螯合物得率均呈现出先上升而后下降的走向。当反应温度达到40 ℃的时候,螯合率和得率达到最大值分别为(69.55±0.12)%和(63.61±0.23)%。这是因为分子间运动速率与温度紧密相关,在特定温度区间内,温度上升,反应体系中分子间运动速率会逐渐加快,使得Mg2+与多肽上氨基酸残基碰撞并结合的概率提高。然而,当温度进一步升高,螯合效果显著降低,这是由于温度过高可能破坏PPH分子结构,还可能致使分子间发生团聚,减少了能够与Mg2+螯合的基团数量,进而导致镁螯合率下降[17]。因此,在响应面设计过程中,将40 ℃设定为温度的中心试验点。
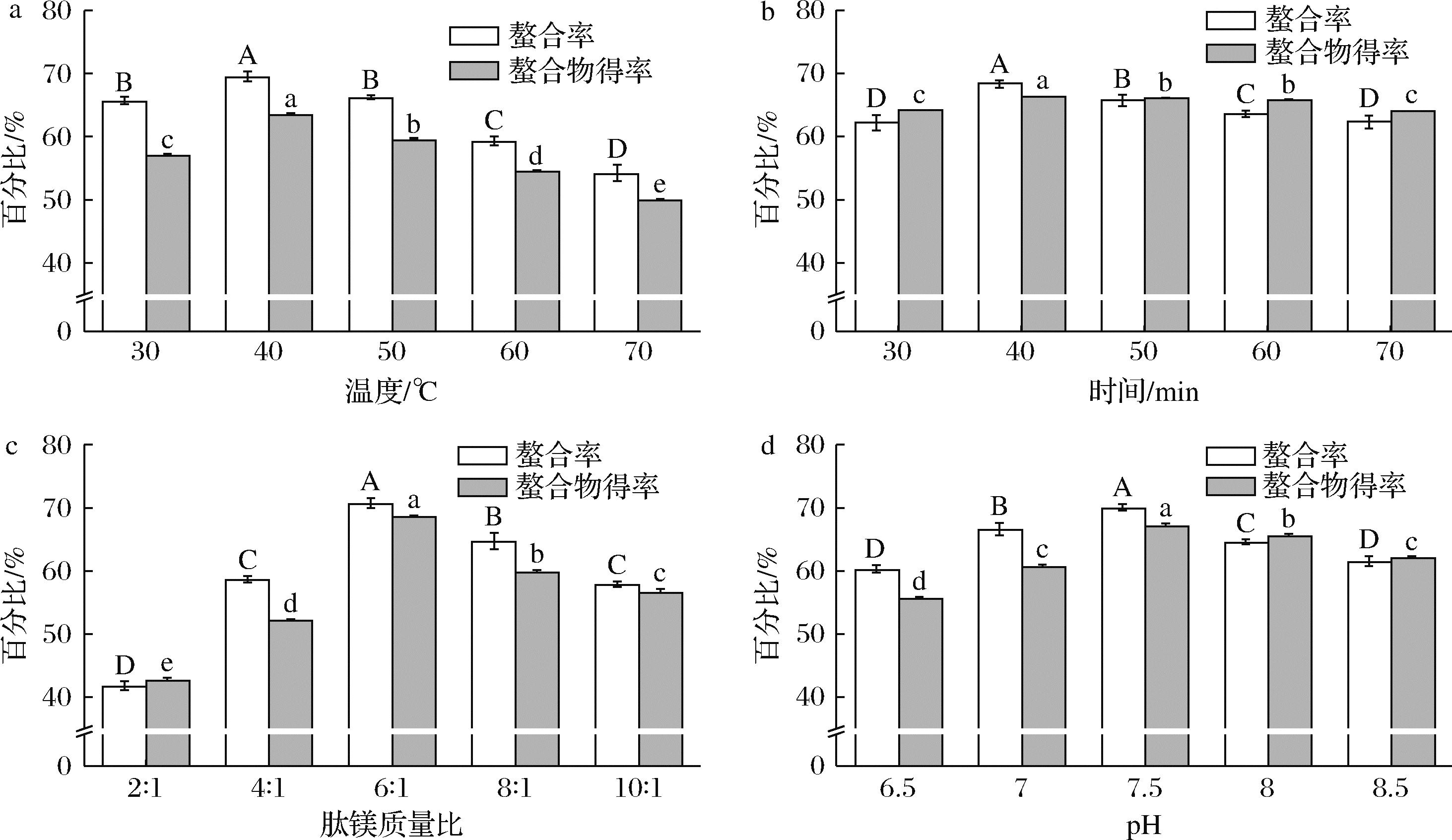
a-温度;b-时间;c-肽镁质量比;d-pH
图2 单因素对螯合率及螯合物得率的影响
Fig.2 Effect of single factor on chelation rate and chelate yield
注:不同大小写字母表示差异显著(P<0.05)(下同)。
2.2.2 时间对螯合率及螯合物得率的影响
由图2-b可知,螯合率与螯合物得率随着时间的延长,变化并不明显,在40 min时二者均达到最大值。随着时间进一步延长,二者均出现了小幅度的下降。这种现象可能是由于反应时间过久,使得螯合物的稳定性减弱,从而发生了解离。相较于其他因素,反应时间对于螯合率和螯合物得率的影响程度相对较小。因此不参与响应面试验设计。基于此,选择40 min作为反应时间开展后续研究。
2.2.3 肽镁质量比对螯合率及螯合物得率的影响
由图2-c可知,螯合率和螯合物得率随肽镁质量比由2∶1增加至6∶1时呈上升趋势,增至最大值分别为(70.76±0.20)%和(68.68±0.15)%。随着质量比继续增加至10∶1时螯合率呈下降趋势。出现这种现象的原因可能是,当肽镁质量比不足6∶1时,反应体系中PPH的量过低,提供不了足够的活性位点与Mg2+结合;当肽镁质量比超过6∶1时,PPH含量又过高,Mg2+与肽的螯合达到饱和状态,多肽之间会发生竞争性抑制,从而使螯合率和螯合物得率降低。因此,在响应面设计过程中,将6∶1设置为肽镁质量比的中心试验点。
2.2.4 pH对螯合率及螯合物得率的影响
如图2-d所示,当pH值为7.5时螯合率和螯合物得率达到最大值,分别为(70.06±0.21)%和(67.23±0.17)%;过酸或过碱的环境均不利于反应的进行,当pH较低时,反应体系中的H+过多,会抑制羧基上H+的电离,且会与Mg2+产生竞争关系而阻碍螯合反应的进行。pH较大时,过多的OH-又会于Mg2+形成Mg(OH)2沉淀,也不利于螯合物的形成[7]。因此,在响应面设计过程中,将7.5设置为pH值的中心试验点。
2.3 响应面试验
2.3.1 响应面试验设计及结果
为得到更优的制备条件,在单因素试验的基础上,根据表1因素水平编码选择pH(7~8)、肽镁质量比(4∶1~8∶1)、温度(30~50 ℃)为影响因子,以螯合率为响应指标,进行三因素三水平的响应面优化试验。具体试验设计及结果见表3,试验重复3次。试验结果通过Design Expert 13软件处理,得到回归方程模型为:Y=70.86-1.42A+0.916 2B+1.1C-2.11AB-0.547 5AC-0.862 5BC-4.08A2-3.68B2-2.24C2。
表3 响应面设计及结果
Table 3 Response surface design and results
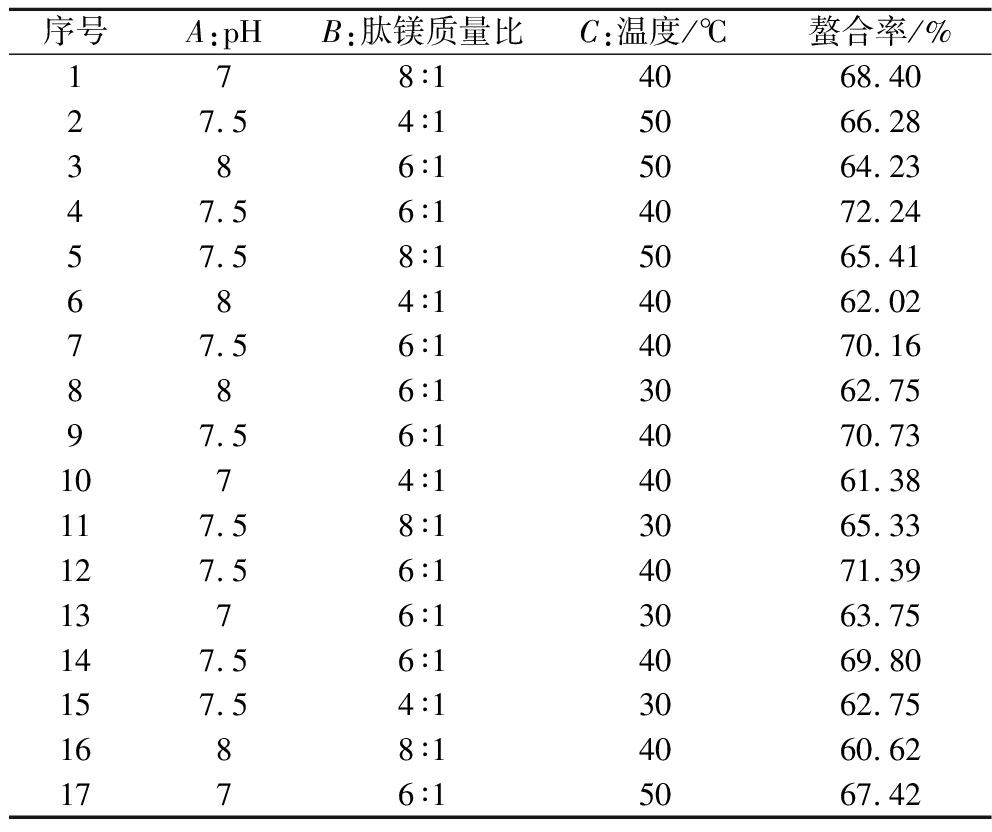
序号A:pHB:肽镁质量比C:温度/℃螯合率/%178∶14068.4027.54∶15066.28386∶15064.2347.56∶14072.2457.58∶15065.41684∶14062.0277.56∶14070.16886∶13062.7597.56∶14070.731074∶14061.38117.58∶13065.33127.56∶14071.391376∶13063.75147.56∶14069.80157.54∶13062.751688∶14060.621776∶15067.42
由表4可知,回归模型P=0.000 2<0.01,失拟项不显著P=0.393 5>0.05,且回归模型系数R2和矫正决定系数![]() 分别为0.968 5和0.928 0,这意味着此模型的试验误差较小,拟合程度颇佳,能够切实反映出因变量的变动情形。因此,该方程模型可用于分析和预测PPH-Mg的制备工艺参数。
分别为0.968 5和0.928 0,这意味着此模型的试验误差较小,拟合程度颇佳,能够切实反映出因变量的变动情形。因此,该方程模型可用于分析和预测PPH-Mg的制备工艺参数。
表4 回归模型的方差分析结果
Table 4 ANOVA of the regression model
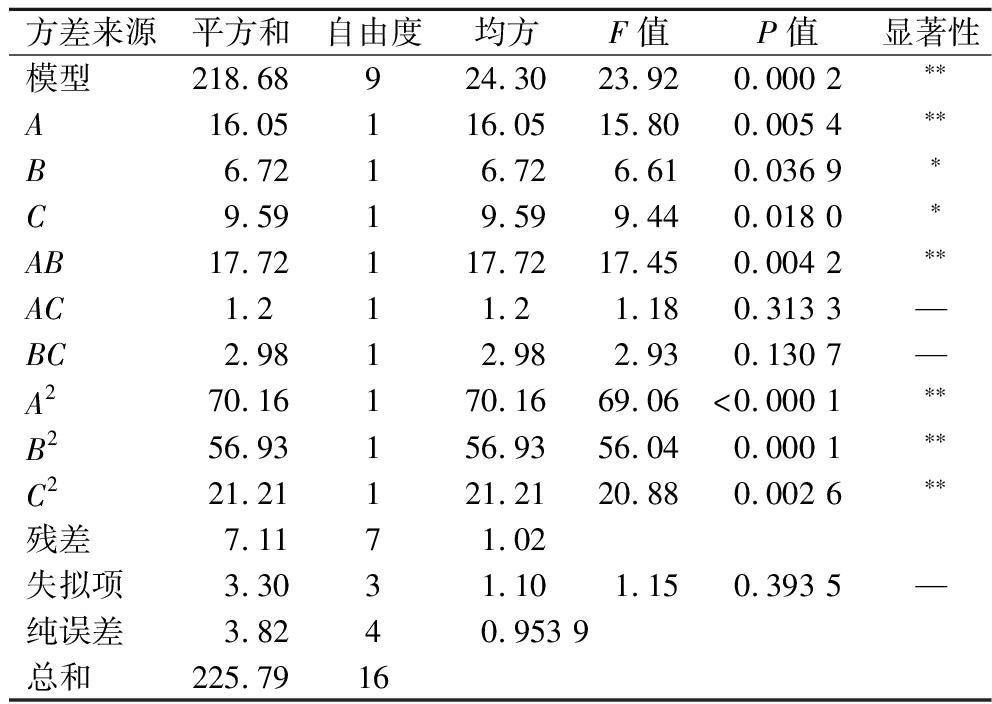
方差来源平方和自由度均方F值P值显著性模型218.68924.3023.920.000 2∗∗A16.05116.0515.800.005 4∗∗B6.7216.726.610.036 9∗C9.5919.599.440.018 0∗AB17.72117.7217.450.004 2∗∗AC1.211.21.180.313 3—BC2.9812.982.930.130 7—A270.16170.1669.06<0.000 1∗∗B256.93156.9356.040.000 1∗∗C221.21121.2120.880.002 6∗∗残差7.1171.02失拟项3.3031.101.150.393 5—纯误差3.8240.953 9总和225.7916
注:*表示差异显著(P<0.05),**表示差异极显著(P<0.01)。
回归模型的显著性检验表明,A、B、C的线性系数、AB的交互项系数,以及A2、B2和C2的二次项系数对镁螯合率均有显著影响,其中A、AB、A2、B2、C2项影响极显著(P<0.01)。根据F值不同比较自变量对螯合率的影响[18],各因素对镁螯合率的影响顺序为:pH>温度>肽镁质量比。
2.3.2 交互作用对螯合率的影响分析
图3是pH、肽镁质量比以及温度对镁螯合率影响的响应面图与等高线图。极值处于圆形中心位置,表明选取的参数水平具备合理性。响应面曲线的倾斜程度,体现的是螯合率对于各工艺参数的敏感状况。曲线斜率越大,表明螯合率对该工艺参数的敏感程度越高;相反,响应曲面曲线的斜率越小,说明该工艺参数的变动对螯合率产生的影响越小。3D图像能直观展现各个因素对响应值的作用,从中可以观察到每2个因素相结合均呈现为凸面,这表明随着因变量之间交互作用的增强,螯合率会先上升而后下降,中间存在一个极值,此结果与回归方程模型相契合。除此之外,图3中a1、a2的椭圆形等高线显示,pH与肽镁质量比之间的交互作用对镁螯合率存在显著影响,这与表4中的结果一致。
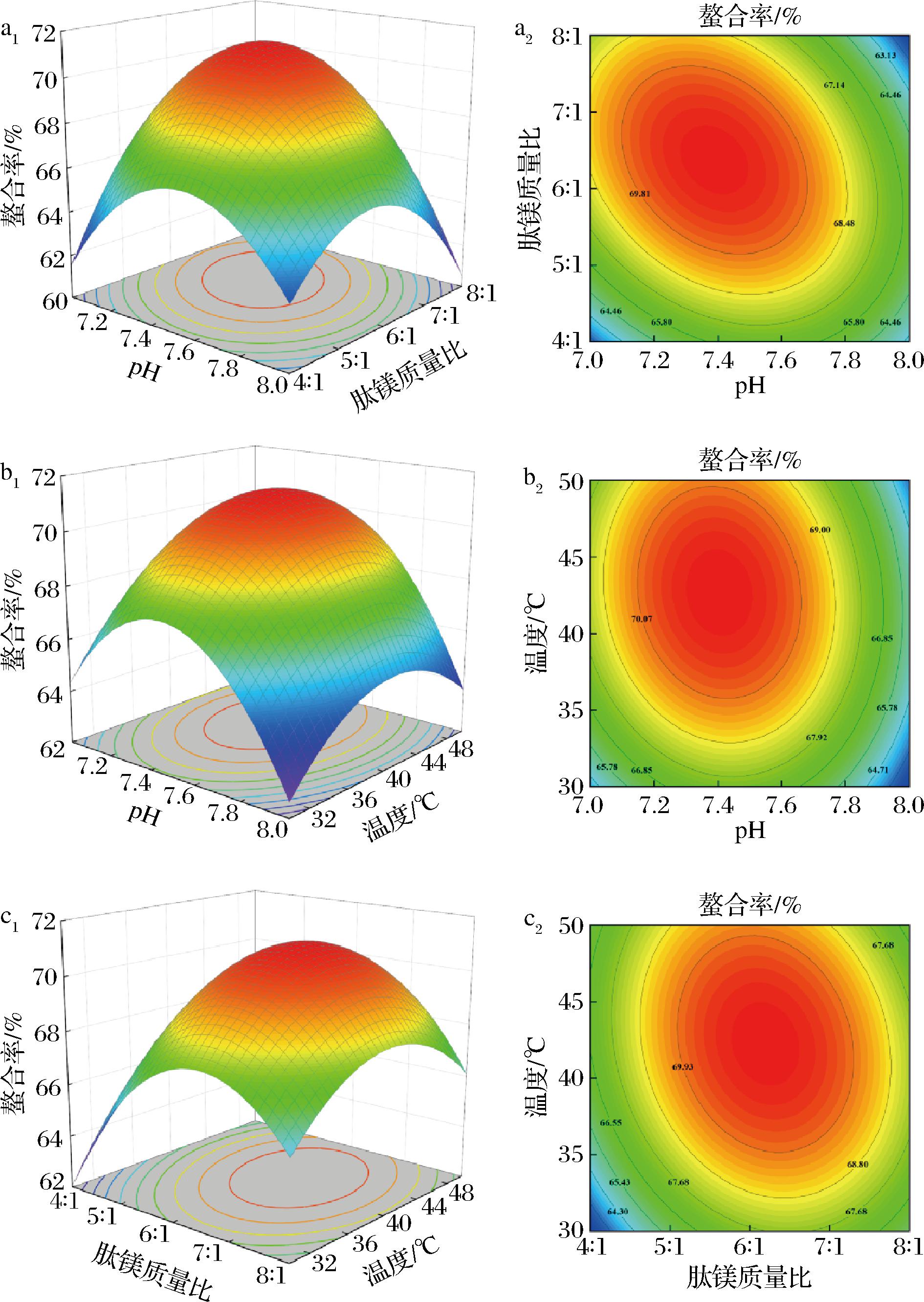
a1、a2-AB;b1、b2-AC;c1、c2-BC
图3 自变量之间交互作用对螯合率的影响
Fig.3 Influence of interaction between independent variables on chelation rate
2.3.3 最佳制备工艺的验证
由回归模型分析得到最佳螯合条件是pH值为7.384 36、肽镁质量比为6.324 32∶1、温度为42.410 5 ℃,在此条件下螯合率预测值为71.234 4%。实际应用中调整pH值为7.4、肽镁质量比6.3∶1、温度42.5 ℃,得到的螯合率为(71.06±0.53)%,实际测量得出的值与预测值较为相近,所构建的回归模型具有较高的拟合程度,能够很好地阐述各因素和响应值之间的实际关联,由此获取的参数具备较高可靠性。此外,本方法制得的螯合物,其镁螯合率显著高于同类型的带鱼蛋白水解肽-镁螯合物[19]的65.7%和鳕鱼皮胶原蛋白肽-镁螯合物的37.9%[20],具有作为新型补镁剂的优越性。
2.4 花生肽及其螯合物的结构特性
2.4.1 氨基酸组成分析
多肽的功能性质取决于其氨基酸组成,氨基酸在与金属离子结合过程中起着重要作用。如表5所示,与金属离子螯合相关的酸性和碱性氨基酸(谷氨酸、天冬氨酸、精氨酸、赖氨酸和组氨酸)占PPH氨基酸总量的40.072%。这些氨基酸能够通过配位或静电相互作用,为金属离子提供更多的反应性侧基[21]。PPH中谷氨酸(17.747%)、天冬氨酸(8.404%)、赖氨酸(4.967%)和脯氨酸(4.018%)的含量相对较高,在PPH-Mg中这4种氨基酸含量分别增加至30.978%、8.843%、5.060%和4.339%,说明Mg2+易于这4种氨基酸发生螯合反应。有研究发现谷氨酸、天冬氨酸和赖氨酸等氨基酸中的羧酸基团,通过改变局部电荷密度来促进多肽与金属离子的螯合[22]。
表5 PPH与PPH-Mg的氨基酸组成
Table 5 Amino acid composition of PPH and PPH-Mg
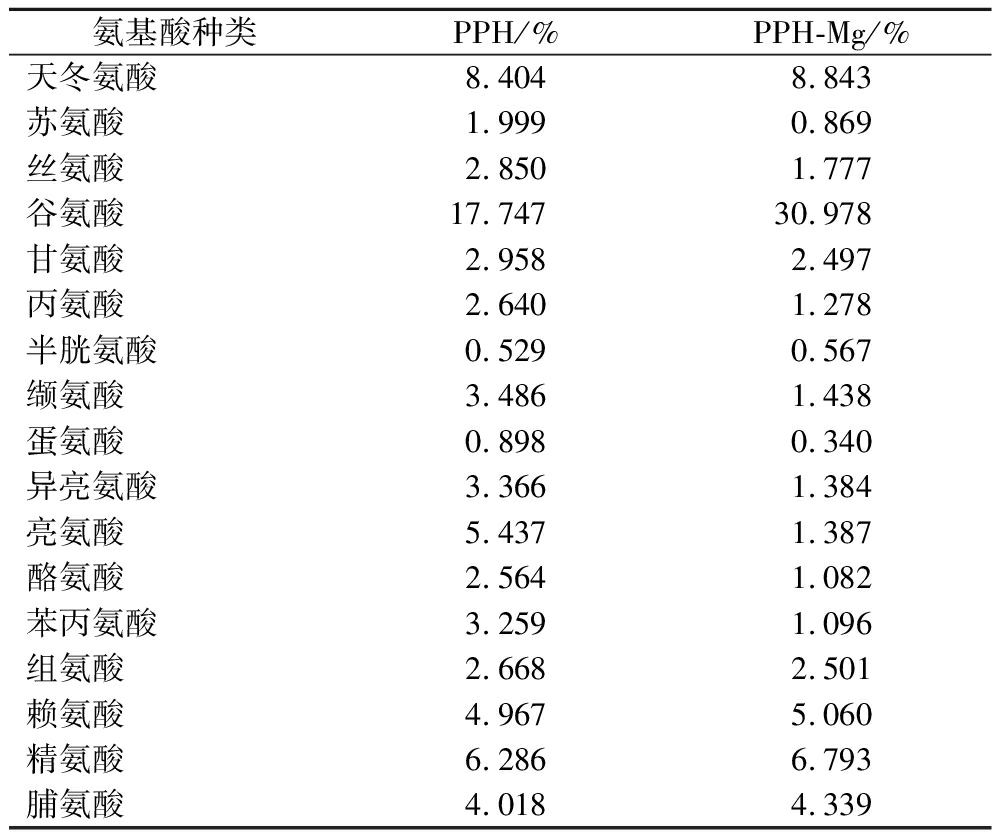
氨基酸种类PPH/%PPH-Mg/%天冬氨酸8.4048.843苏氨酸1.9990.869丝氨酸2.8501.777谷氨酸17.74730.978甘氨酸2.9582.497丙氨酸2.6401.278半胱氨酸0.5290.567缬氨酸 3.4861.438蛋氨酸 0.8980.340异亮氨酸 3.3661.384亮氨酸 5.4371.387酪氨酸 2.5641.082苯丙氨酸 3.2591.096组氨酸 2.6682.501赖氨酸 4.9675.060精氨酸 6.2866.793脯氨酸 4.0184.339
此外,PPH螯合后,氨基酸的种类未发生改变,表明PPH-Mg保留了PPH原有的营养和功能特性。
2.4.2 官能团分析
由图4可知,PPH-Mg的红外光谱图较PPH的红外光谱图出现较大变化。与Mg2+螯合后,PPH在3 301.47 cm-1处的吸收峰红移至3 345.59 cm-1,该区域对应的是—NH2的伸缩振动,表明—NH2参与了螯合物的形成,形成的N-Mg键代替了氢键。在PPH-Mg的光谱中,—COO-基团的谱带(1 399.51 cm-1)红移至较高频率(1 406.86 cm-1),表明—COO-在与Mg2+的过程中也起着关键作用,—COO- 与Mg2+结合并形成—COO-Mg的结构。此外,源自O![]() C—N键面内振动的588.24 cm-1特征峰红移至600.49 cm-1,这可能是由于螯合作用增加了O
C—N键面内振动的588.24 cm-1特征峰红移至600.49 cm-1,这可能是由于螯合作用增加了O![]() C—N中—C
C—N中—C![]() O周围的电子云密度[23]。傅里叶变换红外光谱的结果表明,Mg2+主要通过与羧基氧原子和氨基氮原子相互作用来结合肽,因为其中含有未成对的电子,能够与Mg2+形成环状螯合物[22]。由此可以得出,当金属离子与肽中的活性基团发生螯合时,其傅里叶变换红外光谱也会出现相应的变化[17]。
O周围的电子云密度[23]。傅里叶变换红外光谱的结果表明,Mg2+主要通过与羧基氧原子和氨基氮原子相互作用来结合肽,因为其中含有未成对的电子,能够与Mg2+形成环状螯合物[22]。由此可以得出,当金属离子与肽中的活性基团发生螯合时,其傅里叶变换红外光谱也会出现相应的变化[17]。
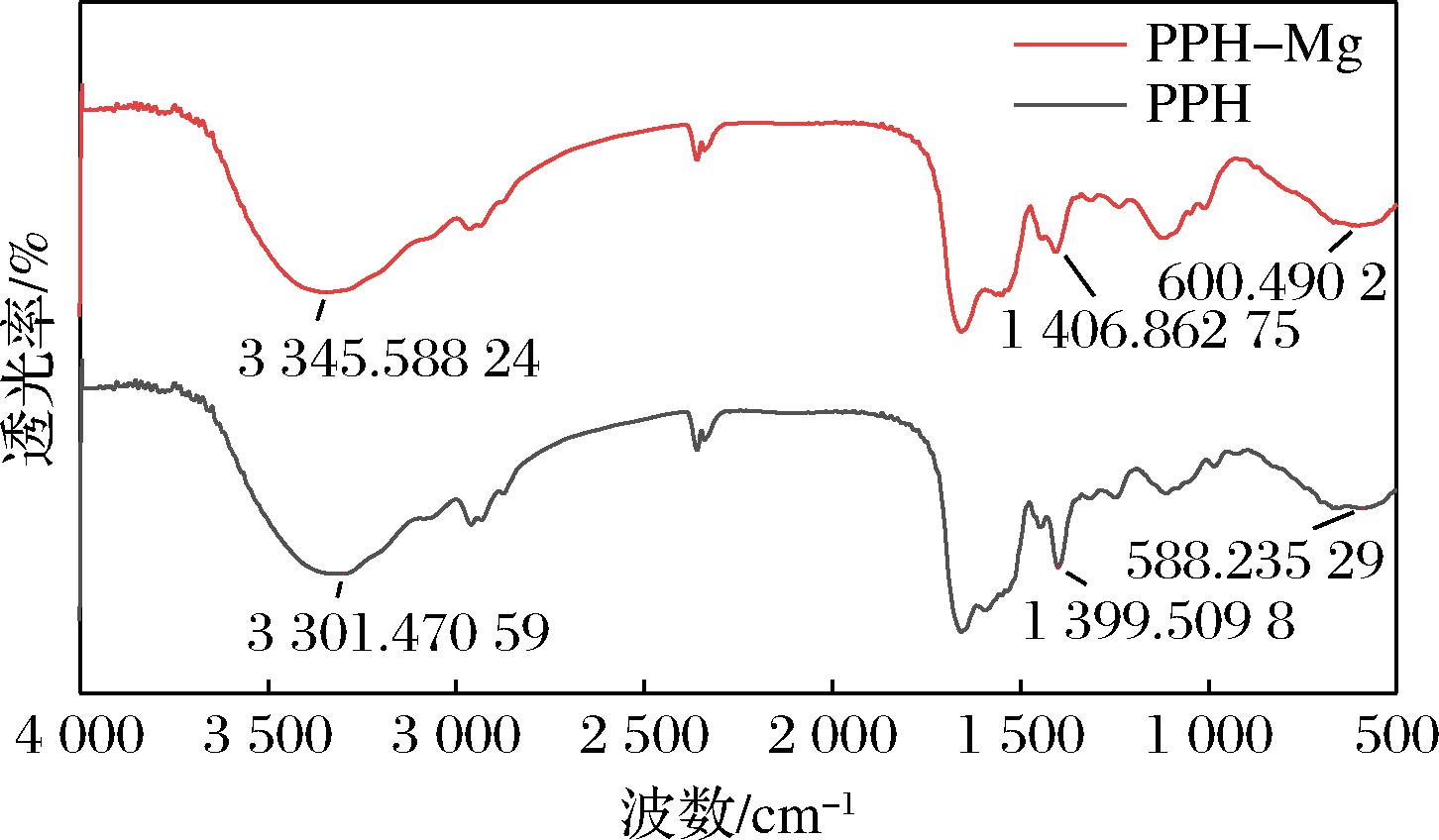
图4 PPH与PPH-Mg的傅里叶变换红外光谱图
Fig.4 Fourier infrared spectra of PPH and PPH-Mg
2.4.3 空间结构分析
PPH中含有酪氨酸和苯丙氨酸等在特定波长条件下能够产生内源荧光的氨基酸,当PPH中这类氨基酸与Mg2+结合后,结构发生变化,其荧光强度也会跟着改变。在特定激发波长下这类氨基酸发出内源荧光的强度变化能有效反映多肽与金属离子的相互作用[24-25]。如图5所示,PPH与Mg2+螯合后在325 nm处的荧光强度显著降低,一方面可能是因为Mg2+与肽之间的螯合反应诱导其结构发生折叠和聚集,导致荧光猝灭;另一方面可能是由于螯合反应产生了新的发色团会导致激发态能量发生变化,从而使荧光强度发生变化[26]。此外,Mg2+的引入会促使氨基酸向分子表面转移,也会导致荧光强度降低[27]。
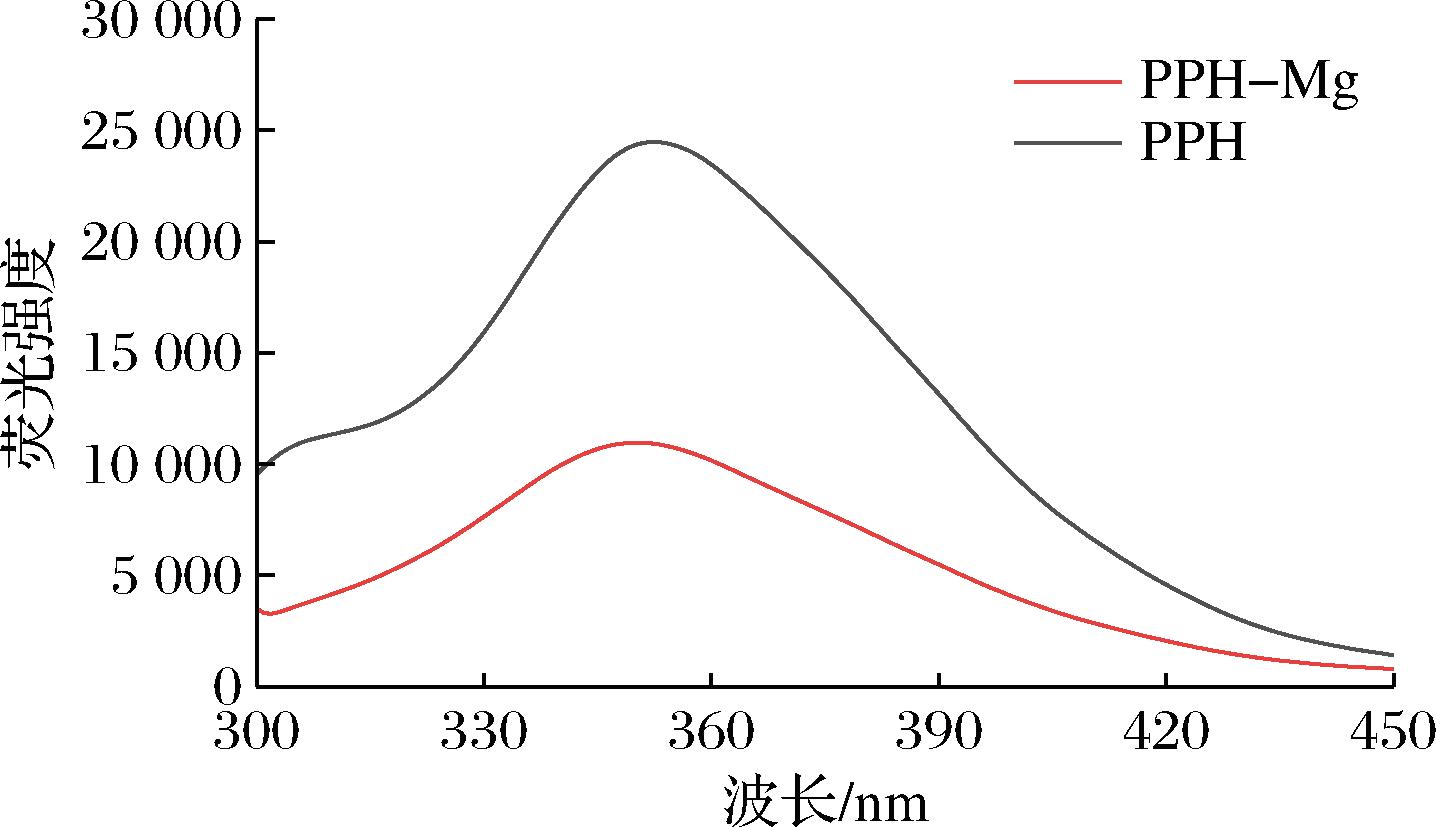
图5 PPH与PPH-Mg的荧光光谱图
Fig.5 Fluorescence spectra of PPH and PPH-Mg
2.4.4 表面电荷分析
如图6所示,显示了PPH和PPH-Mg的zeta电位存在差异,这主要是由于Mg2+的介入导致其表面电荷状态发生变化。PPH的zeta电位为-29.96 mV,这种负电荷源自PPH上大量存在的谷氨酸和天冬氨酸残基。与Mg2+螯合后,其zeta电位从-29.96 mV显著降低至-18.78 mV,表明螯合反应过程中发生了电子转移;PPH与Mg2+之间存在相互作用,肽表面的部分负电荷被中和,降低了整体电荷密度,说明肽和Mg2+形成了一种新的化合物[28]。
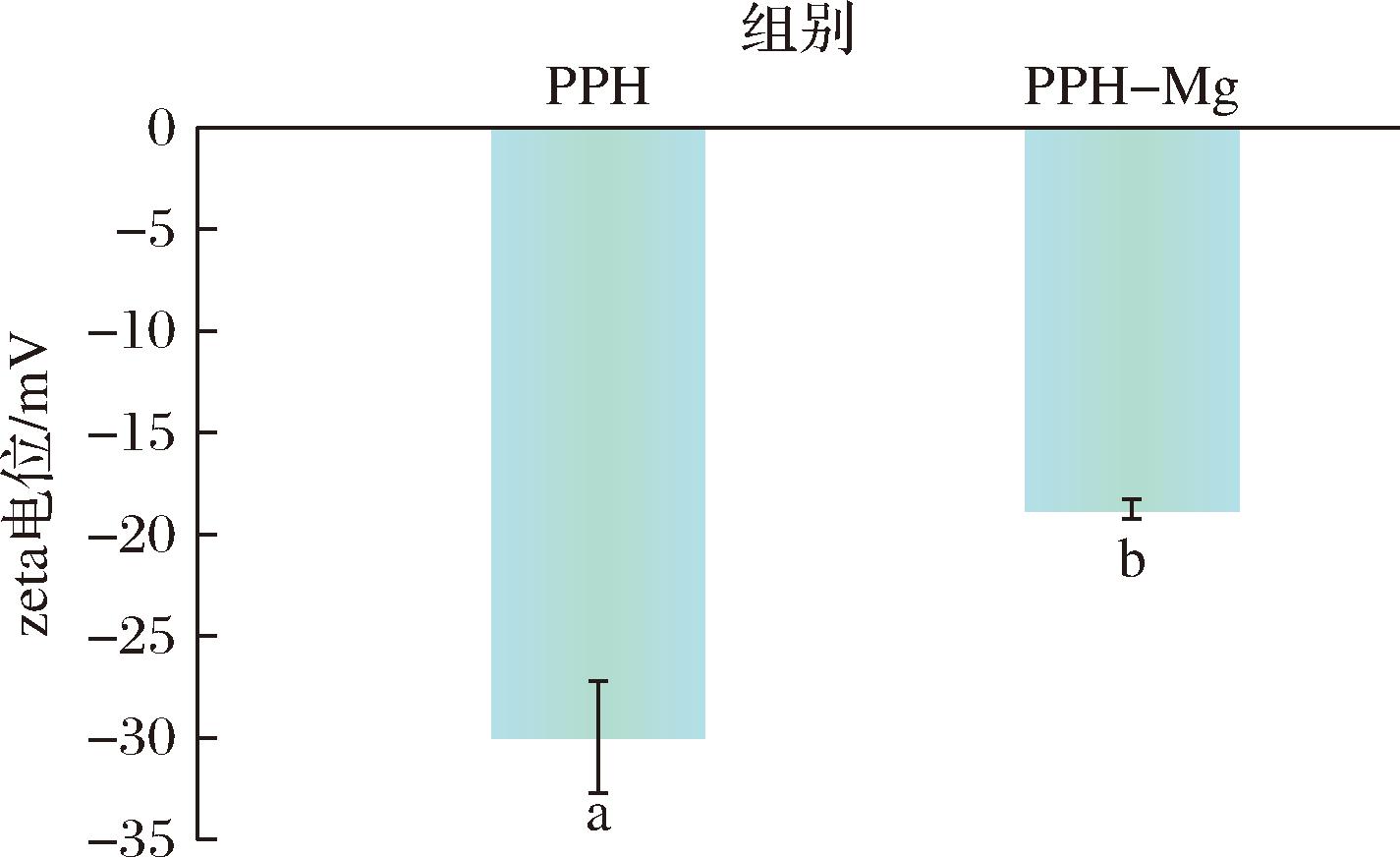
图6 PPH与PPH-Mg的zeta电位图
Fig.6 Zeta potential maps of PPH and PPH-Mg
2.4.5 表面微观形貌观察
扫描电镜是观察样品表面微观形貌的一种有效分析方法。PPH与Mg2+之间的相互作用,会使螯合过程中PPH原本的结构被破坏,使得PPH与PPH-Mg的微观结构存在差异。图7是放大5 000×及10 000× 下的PPH和PPH-Mg的扫描电镜图。PPH表面呈现不规则的片状或块状结构,质地疏松且比较光滑,而PPH-Mg表面粗糙,颗粒变小,表面呈现出更为致密的球形聚集体形态,可能是因为螯合反应中PPH的氨基酸残基与Mg2+配位,改变了其原有的结构,肽链之间发生重组聚集,形成了新的环状结构[29]。

a1-PPH 5 000×;a2-PPH 10 000×;b1-PPH-Mg 5 000×;b2-PPH-Mg 10 000×
图7 PPH与PPH-Mg的扫描电镜图
Fig.7 Scanning electron microscopy of PPH and PPH-Mg
3 结论
本项研究旨在通过酶解花生蛋白制备PPH-Mg。发现用碱性蛋白酶酶解150 min所得PPH与Mg2+的螯合率最高。经单因素分析和响应面优化,确定最佳工艺参数为:pH值为7.4、肽镁质量比6.3∶1、反应温度42.5 ℃。在此条件下,PPH-Mg的螯合率能够达到最大(71.06±0.53)%。结构分析显示,谷氨酸、天冬氨酸、赖氨酸及脯氨酸等氨基酸残基为主要螯合位点,确认PPH-Mg为新型镁配合物。其高螯合率、低成本、简便工艺,使其具有潜在的补镁应用价值,为镁补充剂的开发提供理论基础。未来可通过体内实验进一步评估其生物利用度。
[1] DENT A, SELVARATNAM R.Measuring magnesium-Physiological, clinical and analytical perspectives[J].Clinical Biochemistry, 2022, 105-106:1-15.
[2] SCHWALFENBERG G K, GENUIS S J.The importance of magnesium in clinical healthcare[J].Scientifica, 2017, 2017(1):4179326.
[3] PANTA R, REGMI S.Role of magnesium, effects of hypomagnesemia, and benefits of magnesium supplements in cardiovascular and chronic kidney diseases[J].Cureus, 2024, 16(7):e64404.
[4] KIRKLAND A E, SARLO G L, HOLTON K F.The role of magnesium in neurological disorders[J].Nutrients, 2018, 10(6):730.
[5] PARDO M R, GARICANO VILAR E, SAN MAURO MART N I, et al.Bioavailability of magnesium food supplements:A systematic review[J].Nutrition, 2021, 89:111294.
N I, et al.Bioavailability of magnesium food supplements:A systematic review[J].Nutrition, 2021, 89:111294.
[6] TIAN Q J, FAN Y, HAO L, et al.A comprehensive review of calcium and ferrous ions chelating peptides:Preparation, structure and transport pathways[J].Critical Reviews in Food Science and Nutrition, 2023, 63(20):4418-4430.
[7] CAI C N, LIU Y T, XU Y L, et al.Mineral-element-chelating activity of food-derived peptides:Influencing factors and enhancement strategies[J].Critical Reviews in Food Science and Nutrition, 2025, 65(16):3241-3255.
[8] 王孟丽, 布冠好, 陈复生, 等.花生肽-钙螯合物的制备及其结构表征[J].河南工业大学学报(自然科学版), 2021, 42(5):47-54;76.WANG M L, BU G H, CHEN F S, et al.The preparation and structural characterization of peanut peptide-calcium chelate[J].Journal of Henan University of Technology (Natural Science Edition), 2021, 42(5):47-54;76.
[9] HARIHARAN S, PATTI A, ARORA A.Functional proteins from biovalorization of peanut meal:Advances in process technology and applications[J].Plant Foods for Human Nutrition, 2023, 78(1):13-24.
[10] LIU J L, SONG W T, GAO X, et al.A combined in vitro and in silico study of the inhibitory mechanism of angiotensin-converting enzyme with peanut peptides[J].International Journal of Biological Macromolecules, 2024, 268:131901.
[11] NIU J L, TIAN Q, HUI M, et al.Purification, identification, and synthesis of novel antioxidant peptides from peanut meal and their protective effects against H2O2-induced oxidative damage in HepG2 cells[J].Food Chemistry, 2025, 486:144568.
[12] SANTOS S, VINDEROLA G, SANTOS L, et al.Biodisponibilidad de minerales Que lados y no Que lados:Una revisión sistemática[J].Revista Chilena de Nutrición, 2018, 45(4):381-392.
[13] WALTERS M E, ESFANDI R, TSOPMO A.Potential of food hydrolyzed proteins and peptides to chelate iron or calcium and enhance their absorption[J].Foods, 2018, 7(10):172.
[14] LIU F R, WANG L, WANG R, et al.Calcium-binding capacity of wheat germ protein hydrolysate and characterization of peptide-calcium complex[J].Journal of Agricultural and Food Chemistry, 2013, 61(31):7537-7544.
[15] 崔潇, 江虹锐, 刘小玲, 等.响应面法优化罗非鱼鱼皮胶原多肽螯合镁的工艺条件的研究[J].食品工业科技, 2013, 34(15):238-241;245.CUI X, JIANG H R, LIU X L, et al.Optimization of process conditions for tilapia skin collagen peptides chelating with magnesium by response surface methodology[J].Science and Technology of Food Industry, 2013, 34(15):238-241;245.
[16] LIU Y, WANG Z, KELIMU A, et al.Novel iron-chelating peptide from egg yolk:Preparation, characterization, and iron transportation[J].Food Chemistry, 2023, 18:100692.
[17] SUN R N, LIU X F, YU Y, et al.Preparation process optimization, structural characterization and in vitro digestion stability analysis of Antarctic krill (Euphausia superba) peptides-zinc chelate[J].Food Chemistry, 2021, 340:128056.
[18] QI Y Q, LIU G Y, ZHANG Z, et al.Optimization of green extraction process of Cinnamomum camphora fruit dye and its performance by response surface methodology[J].BioResources, 2023, 18(3):4916-4934.
[19] 王晓玲, 张玉清, 贺延茏, 等.带鱼蛋白水解肽-金属配合物制备工艺[J].食品工业, 2019, 40(7):77-80.WANG X L, ZHANG Y Q, HE Y L, et al.The preparation technology of hairtail hydrolyzed peptides-metal complexes[J].The Food Industry, 2019, 40(7):77-80.
[20] 王春燕, 陈忻, 孙恢礼, 等.鳕鱼皮胶原蛋白肽螯合镁工艺条件探究[J].广东化工, 2014, 41(20):28-30.WANG C Y, CHEN X, SUN H L, et al.Studies on the reaction conditions of producing and chelate of collagen peptide with Mg (Ⅱ)[J].Guangdong Chemical Industry, 2014, 41(20):28-30.
[21] CAETANO-SILVA M E, NETTO F M, BERTOLDO-PACHECO M T, et al.Peptide-metal complexes:Obtention and role in increasing bioavailability and decreasing the pro-oxidant effect of minerals[J].Critical Reviews in Food Science and Nutrition, 2021, 61(9):1470-1489.
[22] WU Y M, WANG Y, MA Z Z, et al.Novel insights into whey protein peptide-iron chelating agents:Structural characterization, in vitro stability and functional properties[J].Food Bioscience, 2024, 60:104317.
[23] YANG X, YU X J, YAGOUB A G, et al.Structure and stability of low molecular weight collagen peptide (prepared from white carp skin)-calcium complex[J].LWT, 2021, 136:110335.
[24] MIRON S, DURAND D, CHILOM C, et al.Binding of calcium, magnesium, and target peptides to Cdc31, the centrin of yeast Saccharomyces cerevisiae[J].Biochemistry, 2011, 50(29):6409-6422.
[25] ZHANG Z R, ZHOU F B, LIU X L, et al.Particulate nanocomposite from oyster (Crassostrea rivularis) hydrolysates via zinc chelation improves zinc solubility and peptide activity[J].Food Chemistry, 2018, 258:269-277.
[26] YUAN F H, FU Y, MA L, et al.Calcium-chelating peptides from rabbit bone collagen:Characterization, identification and mechanism elucidation[J].Food Science and Human Wellness, 2024, 13(3):1485-1493.
[27] LUO J Q, YAO X T, SOLADOYE O P, et al.Phosphorylation modification of collagen peptides from fish bone enhances their calcium-chelating and antioxidant activity[J].LWT, 2022, 155:112978.
[28] ATHIRA S, MANN B, SHARMA R, et al.Preparation and characterization of iron-chelating peptides from whey protein:An alternative approach for chemical iron fortification[J].Food Research International, 2021, 141:110133.
[29] CASE D R, ZUBIETA J, P DOYLE R.The coordination chemistry of bio-relevant ligands and their magnesium complexes[J].Molecules, 2020, 25(14):3172.