肌原纤维蛋白(myofibrillar protein,MP)约占动物肌肉总蛋白的55%~60%,其热诱导凝胶性能是赋予肉糜制品良好质构和保水性的基础[1]。然而,在加工过程中,肌肉组织不可避免地暴露于促氧化环境中,导致活性氧(reactive oxygen species,ROS)大量累积。ROS通过氧化修饰MP的侧链氨基酸、破坏疏水核心以及诱导蛋白交联,使MP发生去折叠、聚集甚至沉淀,最终造成凝胶网络疏松、保水性下降、质构劣化及色泽发暗[2]。因此,如何有效抑制MP氧化损伤、维持或提升其凝胶功能,已成为肉品科学领域亟待解决的核心问题之一。
近年来,植物提取物因其富含多酚、黄酮等活性成分而被广泛关注。但有研究发现,其在使用过程中存在剂量效应,适量多酚能通过清除ROS、稳定蛋白构象,促进均匀致密凝胶网络的形成,过量多酚可能通过疏水聚集或醌-蛋白共价交联,反而削弱凝胶性能。CAO等[3]以绿原酸为例,发现0.05~0.2 mmol/L绿原酸即可恢复氧化MP的储能模量(G′)与持水性(water holding capacity,WHC),而0.5 mmol/L以上却因过度交联显著削弱凝胶强度。JIA等[4]亦证实,0.1 mmol/L儿茶素可提升MP凝胶弹性,0.5 mmol/L以上则因疏水聚集导致孔径增大、WHC降低。
杜仲(Eucommia ulmoides Oliv.)是中国传统的药食同源植物,其叶提取物(Eucommia ulmoides leaf extract,EULE)富含绿原酸、槲皮素、山奈酚等多酚及黄酮类化合物,总多酚含量可达15%~20%[5]。已有研究表明,EULE具有显著的DPPH自由基、羟自由基(·OH)和超氧阴离子(·O2-)清除能力,可有效抑制脂质氧化和蛋白羰基化[6]。HAN等[7]发现,在淀粉体系中,适量添加EULE能改善凝胶流变与WHC。然而,EULE对氧化应激下MP凝胶的宏观性能、水分分布及微观结构尚缺乏系统研究。
因此,本文以鸡胸肉MP为研究对象,在Fenton氧化体系中添加0、0.2、0.6、1 mg/mL EULE,系统评估其对凝胶强度、WHC、白度、质构、流变、水分分布及微观结构的影响,旨在阐明EULE-蛋白作用机制,确定最适剂量,为杜仲叶资源在肉制品加工中的高值化利用提供一定理论依据。
1 材料与方法
1.1 材料与试剂
新鲜鸡大胸(屠宰后48 h内),洛阳本地大张超市。
质量分数2%的EULE,西安沐萌生物制品有限公司;Na2HPO4、NaH2PO4、MgCl2,天津市德恩化学试剂有限公司;NaCl,天津巴斯夫化工有限公司;FeCl3、抗坏血酸,天津市风船化学试剂科技有限公司;30%(质量分数)H2O2,烟台市双双化工有限公司;3,5-二氧杂-1,8-辛二胺四酸[ethylene glycol-bis(2-aminoethylether)- N,N,N′,N′-tetraacetic acid,EGTA]、牛血清白蛋白,上海阿拉丁生化科技股份有限公司。以上所有试剂均为分析纯。
1.2 仪器与设备
RS-JR20绞肉机,合肥荣事达电子电器有限公司;FA30高速均质机,上海昂尼仪器仪表有限公司;LG-25M冷冻离心机,四川蜀科仪器有限公司;TM 3030 Plus台式扫描电镜,日本日立公司;JF-10N-50A 真空冷冻干燥机,杭州旌婓仪器科技有限公司;NMI20-015V-I低场核磁共振成像分析仪,上海纽迈电子科技有限公司;DHR-2食品流变仪,美国沃特斯公司;A.XT Express型物性分析仪,英国SMS公司。
1.3 方法
1.3.1 EULE化学成分含量测定
根据刘仙俊等[8]的方法,以没食子酸为标准器,采用福林酚法对EULE中的总多酚含量进行测定;EULE中的总黄酮含量依据王萍等[9]的方法,采用NaNO2-Al(NO3)3法进行测定。
1.3.2 鸡肉MP的提取
根据尉立刚等[10]的方法并结合实际情况进行适当调整。将鸡胸肉切成小块后,使用绞肉机将其绞打成肉泥。按照料液比1∶4(g∶mL),向肉泥中加入预冷的提取缓冲液(该缓冲液含有10 mmol/L Na3PO4、0.1 mol/L NaCl、2 mmol/L MgCl2、1 mol/L EGTA,pH值为7.0)。接着用均质机以8 000 r/min的转速对混合物进行匀浆处理,匀浆时每均质30 s后暂停30 s,总均质时间为3 min。匀浆完成后,使用双层纱布对混合液进行过滤,以去除肉浆中的结缔组织。随后,将滤液在4 ℃的条件下,10 000 r/min离心15 min,弃去上清液。重复上述离心步骤2次后,得到粗MP沉淀。将粗MP沉淀按料液比1∶4(g∶mL)的比例重新悬浮于含0.1 mol/L NaCl的洗涤缓冲液中,按照上述条件再次进行匀浆和过滤处理。对所得滤液进行相同的离心操作,弃去上清液并重复2次,最终得到纯化的MP。整个MP提取过程均在4 ℃下进行,所得MP样品于4 ℃保存且贮存时间不超过48 h。以牛血清蛋白作为标准品,MP溶液的浓度用双缩脲法进行测定。
1.3.3 EULE的添加及氧化体系的构建
参考常海军等[11]的方法并进行适当调整。采用15 mmol/L 磷酸缓冲液(含0.6 mol/L NaCl,pH 6.25)及Fenton氧化体系溶液(含30 μmol/L FeCl3、100 μmol/L抗坏血酸、3 mmol/L H2O2,溶解于15 mmol/L磷酸缓冲液)分别将MP稀释至目标浓度,以用于后续指标检测。实验共设置5个处理组,其中4个为氧化处理组,采用 Fenton 氧化体系溶液稀释MP,并分别添加EULE,使其终质量浓度依次为 0、0.2、0.6、1.0 mg/mL;另设1个空白对照组,以等体积磷酸缓冲液替代Fenton氧化体系溶液,且不添加EULE。将所有样品置于4 ℃冰箱中避光氧化12 h。
1.3.4 MP凝胶的制备
参照杨兰心等[12]的方法并稍作修改。用1.3.3节中所述的预冷磷酸缓冲液及氧化缓冲液(pH 7.0)(下文同)将各组MP样品稀释至60 mg/mL。取50 mL烧杯分装MP溶胶,置于恒温水浴锅中以1 ℃/min的速率从室温加热到80 ℃,并在80 ℃保温20 min。加热完成后,迅速将样品取出并置于冰水中进行冷却处理,之后4 ℃冷藏过夜。进行凝胶性能测定前在室温下平衡1 h。
1.3.5 凝胶WHC测定
参考陈昌等[13]的方法并进行适当调整。精确称量10 g凝胶样品,转移至50 mL离心管中。4 ℃,10 000 r/min离心15 min。离心结束后,弃去上清液,使用滤纸轻轻吸去凝胶表面残留的水分,精确称量离心后凝胶的质量。凝胶WHC的计算如公式(1)所示:
(1)
式中:m0,空离心管质量,g;m1,离心前离心管与凝胶的总质量,g;m2,离心后离心管与凝胶的总质量,g。
1.3.6 凝胶白度测定
将MP凝胶样品切成质量相同的小块,用保鲜膜包住,采用色差仪对MP凝胶样品表面的L*、a*、b*值进行测定。仪器经自检及零点、白板校正后,每个样品选取3个不同部位进行测定。凝胶白度值的计算如公式(2)所示:
凝胶白度![]()
(2)
1.3.7 凝胶强度测定
参照李保玲等[14]的测定方法并略作修改。利用凝胶模具将凝胶样品切割成直径10 mm、高度约15 mm的圆柱体试样。采用TA.XT Express型物性分析仪进行凝胶强度测试,选用P/0.5型号探头,测试前2 mm/s、测试中1 mm/s、测试后2 mm/s,压缩比例调整至40%,触发力阈值设定为5 g。
1.3.8 凝胶质构特性测定
将制备好的凝胶样品从冰箱中取出,室温下平衡1 h。样品析出的水分用滤纸吸干,然后使用圆柱体凝胶模具将其切割成直径20 mm、高10 mm的圆柱体。采用质构分析仪对MP凝胶样品的质构性能进行测定。测定程序采用质构剖面分析(texture profile analysis,TPA)模式,测前速率2 mm/s,测中速率1 mm/s,测后速率2 mm/s,压缩比50%,触发力5 g,探头型号为P 36R。记录各组凝胶样品的硬度、弹性、黏附性和回弹性等质构参数的变化[15]。
1.3.9 凝胶动态流变学测定
参考LIN等[16]的方法并结合实际略作调整。用预冷的磷酸缓冲液与氧化缓冲液(pH 7.0)将MP样品质量浓度稀释至60 mg/mL,以此制备MP溶胶。随后对溶胶样品进行离心(4 ℃,2 000 r/min,2 min)以脱气,去除气泡后备用。采用振荡温度扫描测试模式,选用40 mm平板并安装适配转子,将脱气后的溶胶样品均匀涂抹于测试平台上,确保无小气泡产生。振荡频率0.1 Hz,最大应力2%,上下板狭缝1 mm。将样品以2 ℃/min从20 ℃加热至80 ℃,同时记录升温过程曲线。对样品进行刮边处理后,使用硅油密封平板外蛋白质与空气接触的部位,防止蛋白溶液在加热时蒸发,同时记录储存模量(G′)和损耗模量(G″)。
1.3.10 凝胶水分布特性测定
1.3.10.1 凝胶低场核磁共振
按照郭家刚等[17]的方法测定MPs凝胶的水分布特性。取适量制备好的MPs凝胶样品,分装于核磁小瓶中,随后将核磁瓶放入核磁共振管内。采用低场核磁共振分析仪并选用CPMG(Carr-Purcell-Meiboom-Gill)序列测定MPs凝胶样品的自旋弛豫时间T2,并对T2数据进行反演获取反演谱图。温度32 ℃,采样频率(SW)250 kHz,采样间隔时间(TW)4 000 ms,回波个数(NECH)5 000。脉冲参数:RG1 20 db,P1 6 μs,P2 10 μs,TE 0.200 ms,NS 16。
1.3.10.2 凝胶核磁共振成像(magnetic resonance imaging,MRI)
MRI通过磁共振成像技术实现。使用多自旋回波(MSE)成像序列对MP凝胶的质子密度图像进行分析,使用低场核磁共振仪扫描MP凝胶内的氢质子密度。具体MRI成像参数设置如下:脉冲持续时间1 200 μs,扫描宽度20 kHz,相位编码时间1 ms。所获取的MRI图像为灰度图,经映射处理后,运用Osiris软件对图像进行伪彩处理。伪彩色图像依据质子密度图像以及水分布情况生成,最终将图像以BMP格式导出。
1.3.11 凝胶微观结构测定
参照李学鹏等[18]的方法。将MP凝胶切割成边长为50 mm的正方体,置于10 mL质量分数为 2.5%的戊二醛溶液(含有10 mmol/L、pH 6.8的PBS)中固定24 h。随后,用0.1 mol/L的磷酸缓冲液(pH 6.8)漂洗3次,每次持续10 min。接着进行梯度脱水处理,依次使用体积分数为50%、70%、80%、90%和100%的乙醇溶液各处理3次,每次10 min,确保样品完全浸没。脱水完成后,将样品在100%乙醇与叔丁醇(体积比1∶1)的混合液中浸泡15 min。之后,将样品放在冷冻干燥机的样品台上,-50 ℃、10 Pa冷冻干燥36 h。最后,用离子溅射仪对样品表面进行喷金处理,并通过扫描电子显微镜在5.0 kV加速电压和500倍放大下观察MP凝胶的微观结构变化。
1.4 数据处理
所有实验均重复3次,结果以“平均值±标准差”表示。使用SPSS 21.0软件对数据进行单因素方差分析及显著性检验(P<0.05为差异显著),图表绘制使用Origin 2024 Pro软件完成。
2 结果与分析
2.1 EULE成分含量
经测定,EULE中总多酚含量为(173.6±2.19)mg/g,总黄酮含量为(157.3±1.3)mg/g。
2.2 EULE的添加对MP凝胶强度和WHC的影响
凝胶的强度与WHC能在一定程度上能体现其性能的优劣。凝胶强度是指刺破凝胶时所需的初始压力,其数值可反映蛋白形成凝胶的能力。如图1-a所示,与对照组相比,MP氧化处理后其凝胶强度显著下降(P<0.05)。这说明氧化会改变蛋白质结构,破坏MP的三维凝胶网络结构,从而导致凝胶成型能力下降。与氧化对照组相比,添加EULE后,MP凝胶强度呈现不规则变化。当EULE添加量较低时,MP凝胶强度略有提升,但无显著差异。随着EULE添加量的增加,当添加量达到0.6 mg/mL时,MP凝胶的强度显著增强,这一现象可能与EULE中含有的槲皮素成分有关。贾娜等[19]的研究表明,槲皮素浓度越高,MP凝胶强度越强,更利于蛋白质凝胶的形成。但当EULE添加量进一步增加时,MP凝胶强度出现降低的现象。这可能是由于高浓度EULE中的多酚类物质与蛋白质发生交联反应,进而形成了复杂的网络结构所致。这种交联反应可能会破坏蛋白质原有的凝胶网络,使凝胶的稳定性和强度下降。已有研究表明,高浓度的EGCG[20]、儿茶素[21]、绿原酸[3]等均会大幅降低MP凝胶强度。
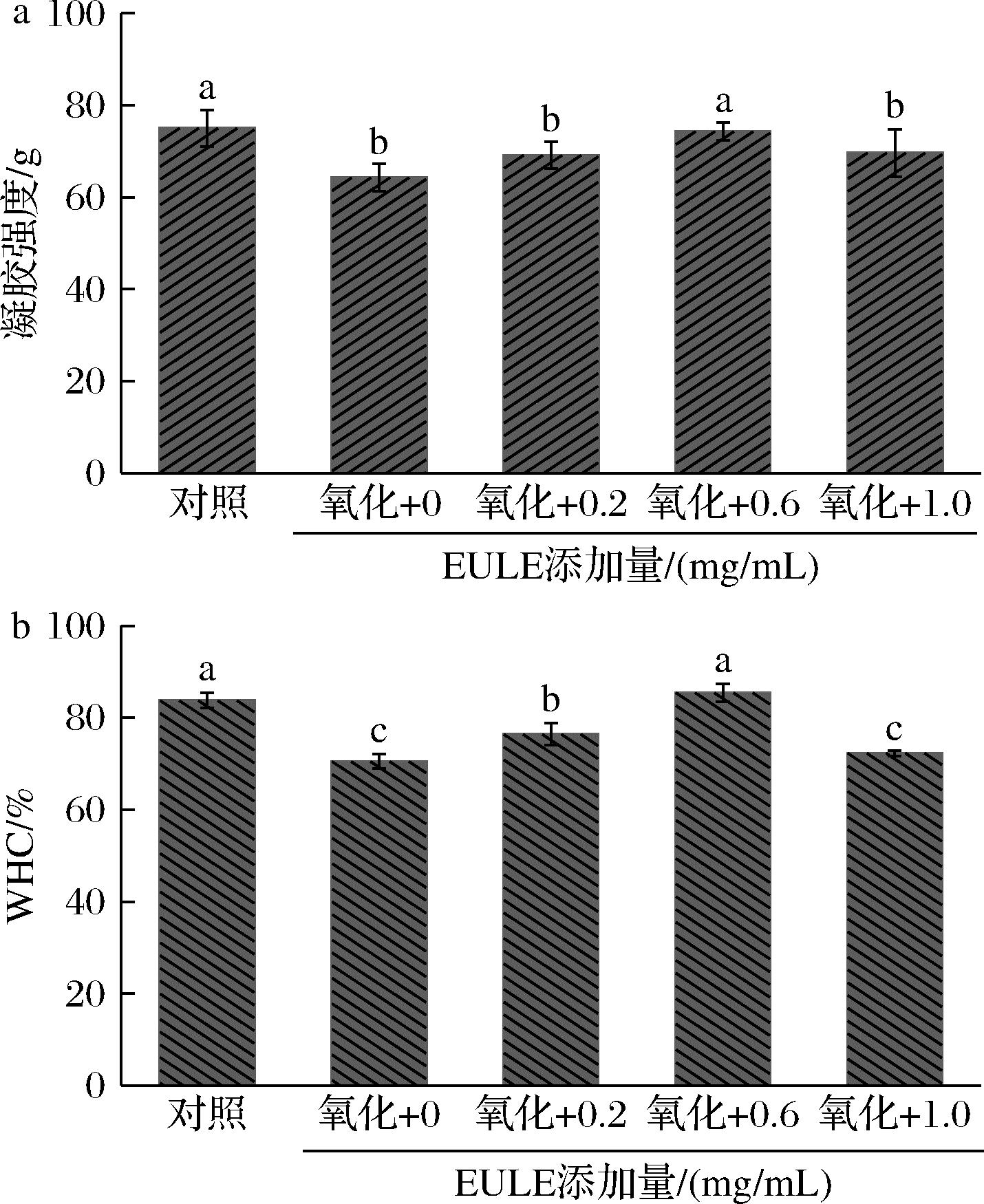
a-凝胶强度;b-凝胶WHC
图1 EULE对氧化MP凝胶强度和WHC的影响
Fig.1 Effects of EULE on the gel strength and water holding capacity of oxidized MP
注:不同小写字母表示差异显著(P<0.05)(下同)。
WHC是评价蛋白质凝胶网络保水能力的重要指标。如图1-b所示,氧化处理后MP凝胶的WHC较对照组显著下降,从83.78%降至70.5%(P<0.05)。与氧化对照组相比,添加EULE后,MP凝胶的持水性显著提升(P<0.05)。当EULE添加量为0.6 mg/mL时,凝胶持水性提高了21.23%,这可能归因于EULE中酚类物质具有较强的自由基清除能力,有助于保护蛋白质结构,形成更致密的凝胶网络,从而提高凝胶的WHC[22]。然而,当EULE添加量达到1.0 mg/mL时,凝胶WHC急剧下降至72.3%,与氧化处理组无显著差异。这表明过量的多酚类物质可能破坏凝胶网络结构的致密性,导致部分结合水转变为自由水,从而降低WHC。这与高剂量EULE导致MP凝胶强度下降的结论一致,也与后续实验凝胶质构特性的变化趋势相符。EULE与蛋白质的相互作用在高剂量下可能破坏蛋白质结构,导致MP凝胶的三维网络结构破裂,进而降低凝胶的WHC和硬度[4]。
2.3 EULE的添加对MPs凝胶白度的影响
MP凝胶的白度值对其物理特性存在显著影响。如图2所示,对照组MP凝胶的白度值为81.8,经氧化处理后显著降低至80.51(P<0.05),这可能是由于氧化作用导致过氧自由基增加,进而降低了凝胶的白度值[23]。添加EULE后,随着EULE剂量的增加,MP凝胶的白度值呈现出逐渐下降的趋势。当EULE添加量为0.2 mg/mL时,凝胶白度与氧化对照组相比无显著差异(P>0.05),这表明低剂量的EULE无法较好地发挥抗氧化作用;而当EULE添加量继续增加至0.6 mg/mL时,凝胶白度显著降低至78.15(P<0.05);当EULE添加量达到1.0 mg/mL时,凝胶白度进一步显著降低至68.78(P<0.05),明显低于空白对照组。这可能是因为EULE本身呈土棕色,且其在水中的溶解度随浓度增加而提高,导致溶液颜色加深,从而增加了凝胶的b*值,降低了凝胶的白度值。这一现象与常海军等[24]的研究结果相一致,其发现添加姜黄素后,凝胶的白度值也会随着添加量的增加而显著下降。
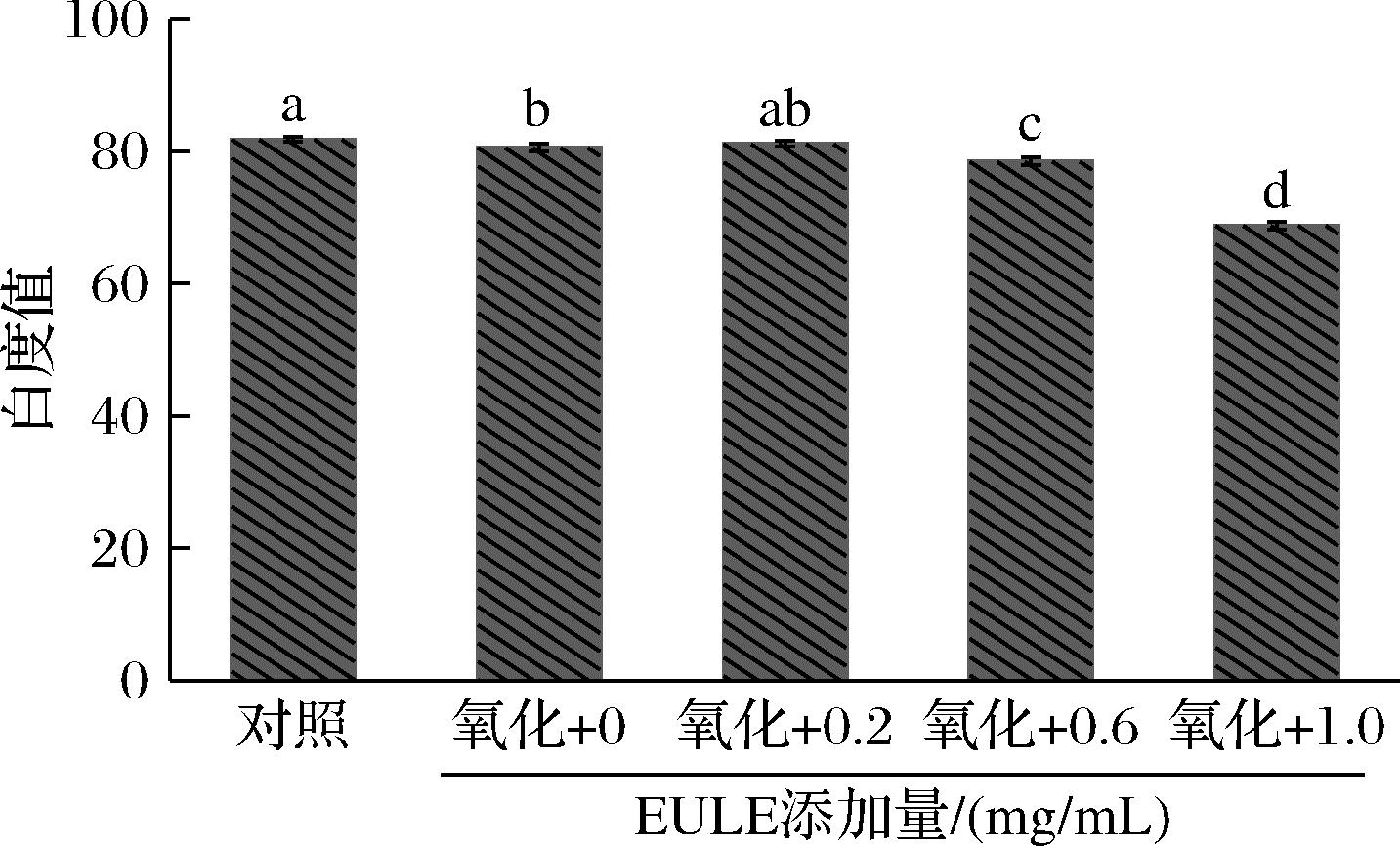
图2 EULE对氧化MP凝胶白度值的影响
Fig.2 Effect of EULE on the whiteness value of oxidized MP gel
2.4 EULE的添加对MP凝胶质构特性的影响
凝胶的硬度、弹性、胶黏性和回弹性是评价其质构特性的关键指标。由表1可知,氧化处理显著降低了MP凝胶的质构性能,与空白对照组相比,其硬度、弹性、胶黏性和回弹性分别下降了22.63%、6.32%、41.62%和32.43%(P<0.05),表明氧化修饰破坏了蛋白质凝胶网络结构的完整性,导致整体质构性能变差。
表1 EULE对氧化MP凝胶质构特性的影响
Table 1 Effects of EULE on the textural properties of oxidized MP gel
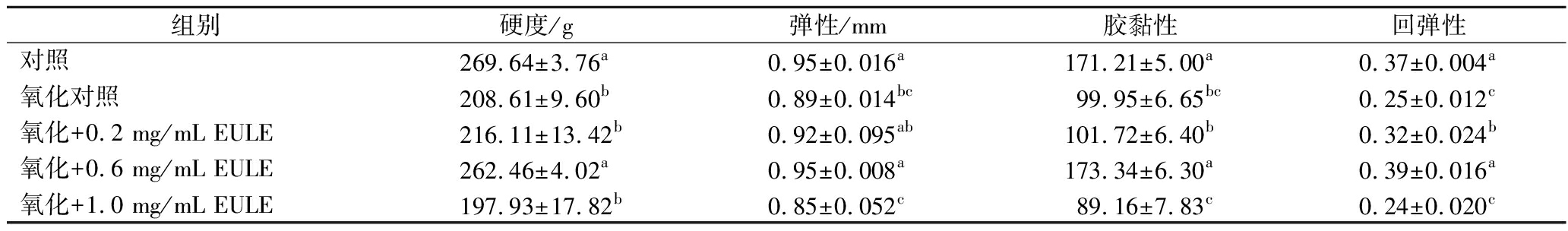
组别硬度/g弹性/mm胶黏性回弹性对照269.64±3.76a0.95±0.016a171.21±5.00a0.37±0.004a氧化对照208.61±9.60b0.89±0.014bc99.95±6.65bc0.25±0.012c氧化+0.2 mg/mL EULE216.11±13.42b0.92±0.095ab101.72±6.40b0.32±0.024b氧化+0.6 mg/mL EULE262.46±4.02a0.95±0.008a173.34±6.30a0.39±0.016a氧化+1.0 mg/mL EULE197.93±17.82b0.85±0.052c89.16±7.83c0.24±0.020c
注:同列不同小写字母表示差异显著(P<0.05)。
添加EULE后,MP凝胶的硬度和弹性随EULE添加量的增加呈现先升高后降低的趋势。当EULE添加量为0.6 mg/mL时,凝胶硬度和弹性均显著高于氧化对照组(P<0.05),说明适宜添加量的EULE可有效缓解氧化应激对蛋白质交联网络的破坏作用,改善凝胶质构特性。然而,当EULE添加量达到1.0 mg/mL时,凝胶硬度和弹性显著下降,可能是由于高添加量EULE改变了蛋白质与水分子的相互作用,导致结合水减少、自由水增加,破坏了凝胶的持水能力和结构致密性,从而降低了硬度和弹性。这一结果与后续观察到的“高添加量EULE使MP凝胶体系自由水增多、结合水减少”的现象相一致。凝胶的胶黏性是指凝胶表面与探头或其他表面接触时产生的“黏附”力,而回弹性则反映凝胶在受到压缩后迅速恢复原状的能力。凝胶的胶黏性和回弹性的变化趋势与硬度和弹性的变化趋势相一致,氧化处理和高添加量EULE添加均显著降低了MP凝胶的胶黏性和回弹性(P<0.05),适量添加EULE(0.6 mg/mL)能够有效改善凝胶的胶黏性和回弹性,说明过量添加EULE(1.0 mg/mL)反而会破坏凝胶结构,导致质构性能下降。这种剂量依赖性现象与CHENG等[25]的研究结果相符,即低浓度下通过抗氧化作用提升凝胶性能,高浓度下则可能因促氧化效应导致性能劣化。
2.5 EULE的添加对MP凝胶流变特性的影响
G′和G″分别用于表征凝胶形成过程中的弹性和黏性特征,其变化与蛋白质三维网络结构的形成密切相关。如图3-a和图3-b所示,在加热过程中,不同处理组MP溶液的G′和G″随温度变化呈现一定规律。由图3-a可以看出,所有处理组样品的G′值在45~53 ℃总体呈上升趋势,说明在此阶段MP溶液开始形成凝胶网络结构。当温度进一步升高至53~60 ℃时,G′值出现下降,这可能是由于高温诱导肌球蛋白部分变性,分子链流动性增强,从而破坏了初始形成的蛋白质凝胶网络结构[26]。此外,氧化对照组MP样品的G′值整体显著低于空白对照组,说明蛋白质氧化削弱了凝胶网络的稳定性,降低了凝胶的弹性。这一现象可能与氧化导致MP凝胶WHC显著下降有关。WHC降低使得水分从凝胶网络中析出,出现“脱水”现象,凝胶网络失去水分支撑后结构进一步塌陷,使得G′值和整体稳定性明显下降。添加EULE后,G′值较对照组和单独氧化组均有所提高,其中0.6 mg/mL处理组在加热终点时的G′值升高尤为明显,甚至超过对照组,表明适量EULE可促进形成弹性更强的蛋白凝胶网络。这可能是由于其有效抑制蛋白质氧化,维持蛋白质结构完整性,从而优化凝胶网络的稳定性。然而,当EULE添加量达到1.0 mg/mL时,MP的G′值整体急剧下降,说明高添加量EULE会严重损害蛋白凝胶性能,导致凝胶弹性大幅降低。
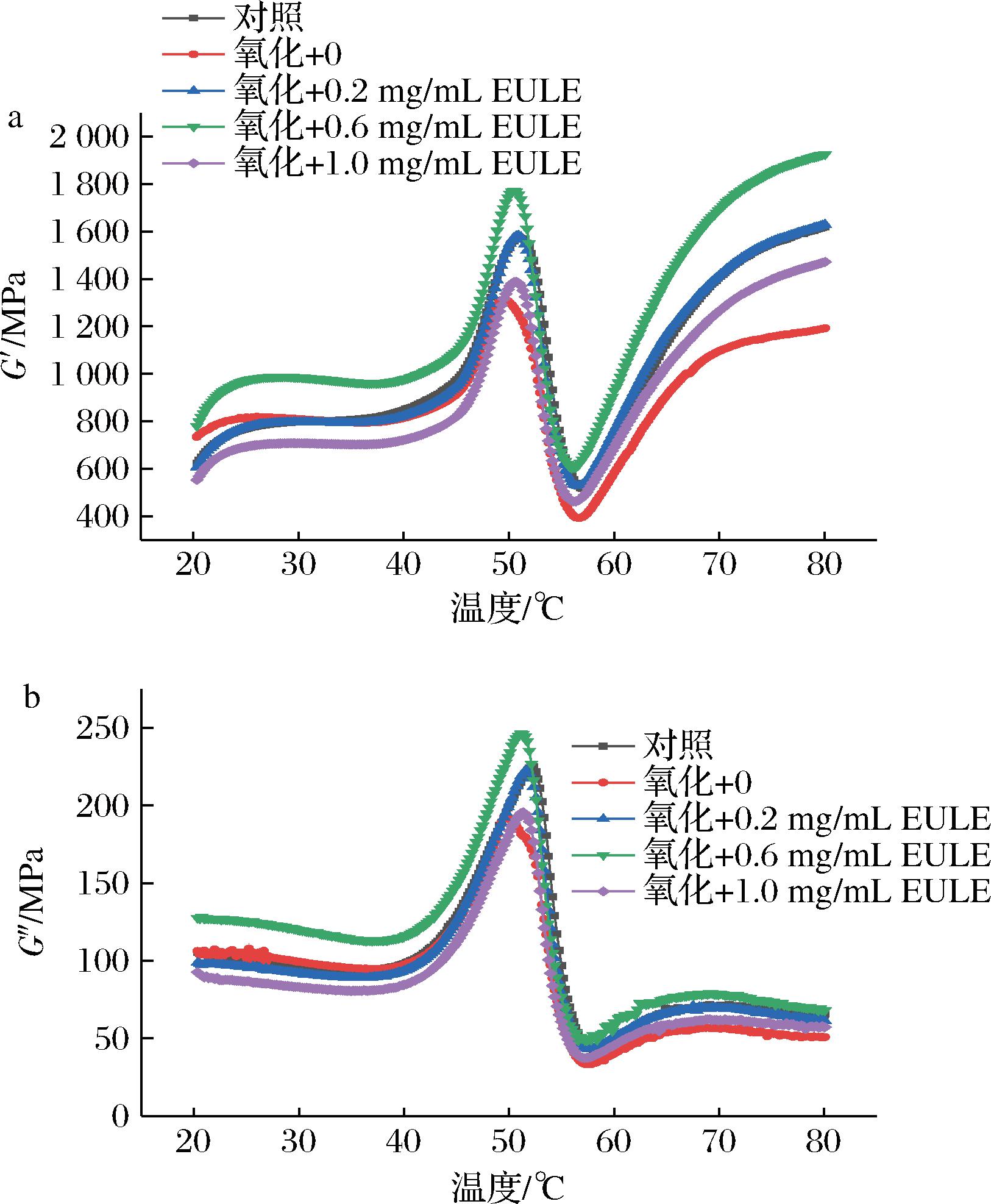
a-G′;b-G″
图3 EULE对氧化MP凝胶G′和G″的影响
Fig.3 Effect of EULE on the G′and G″ of oxidized MP gel
如图3-b所示,G″变化趋势与G′一致,均表现为先上升后下降。氧化对照组的G″峰值明显低于对照组,且在20~45 ℃ G″值整体偏低。这一现象表明,氧化作用会破坏蛋白质分子结构,削弱分子间交联的初始驱动力,阻碍凝胶形成期的黏性增长;同时可能减少蛋白分子有效相互作用位点,增强低温条件下体系的流动性[27]。其深层原因可能与氧化处理后MP凝胶的微观结构劣化相关,氧化使凝胶网络结构松散、孔径增大且分布不均,减少了有效连接点和蛋白间相互作用,降低了体系能量耗散能力,导致G″显著下降。在添加EULE后,0.2~0.6 mg/mL条件下G″值均高于单独氧化处理组,其中0.6 mg/mL处理组的G″峰值提升尤为显著。这可能是因为适量添加EULE后多酚类物质能够抑制蛋白质氧化,减少蛋白质过度聚集,改善凝胶网络结构的均匀性和致密性,进而使G″值升高。然而,当EULE添加量进一步增加至1.0 mg/mL时,G″峰值低于所有处理组且曲线最低。这可能是高添加量多酚与蛋白质形成不溶性复合物,导致凝胶基质中出现相分离或局部结构塌陷,破坏凝胶的整体均一性,最终导致G″值显著下降。G′与G″的变化与质构特性中黏弹性的变化趋势相一致,表明适量EULE能够改善MP凝胶的黏弹性,而高添加量EULE则会对凝胶性能产生不利影响。这与姜黄素在适宜浓度范围内通过抗氧化和分子交联双重机制有效修复氧化MP流变特性的研究结果相一致[24]。
2.6 EULE的添加对MP凝胶水分布特性的影响
低场核磁共振技术通过T2弛豫时间能够表征凝胶体系的水分分布及迁移特性。如图4-A1所示,在MP凝胶体系中检测到4种具有不同弛豫时间的水组分,即T2b(0.1~10 ms)、T21(10~100 ms)、T22(100~1 000 ms)和T23(1 000 ~ 10 000 ms)[28]。这4种组分分别对应凝胶体系中的3种水相状态:结合水、固定水和自由水。具体而言,T2b与T21的弛豫峰对应结合水,T22和T23分别对应固定水与自由水,相应的峰面积分别记为 P2b、P21、P22和 P23。与对照组相比,氧化处理使MP凝胶的T23弛豫时间增加,P22占比减小,P23值增加。这说明MP凝胶体系中的结合水和不易流动水更多地转化为了自由水。这是因为氧化作用削弱了破坏的水束缚能力,导致自由水含量增加。这一结果与MP凝胶强度及WHC实验结果一致。添加中低量EULE 后,MP凝胶的 T23弛豫时间缩短,P23值也降低,表明MP凝胶中的水分分布得到改善。这可能是EULE 中酚类物质促进了MP分子间及蛋白-多酚间的共价/非共价交联,形成了更致密的凝胶网络所致。然而,1.0 mg/mL EULE组P23值明显增加,促使结合水和固定水更多转化为自由水。这可能是高添加量EULE阻碍了凝胶网络形成,导致自由水增加。
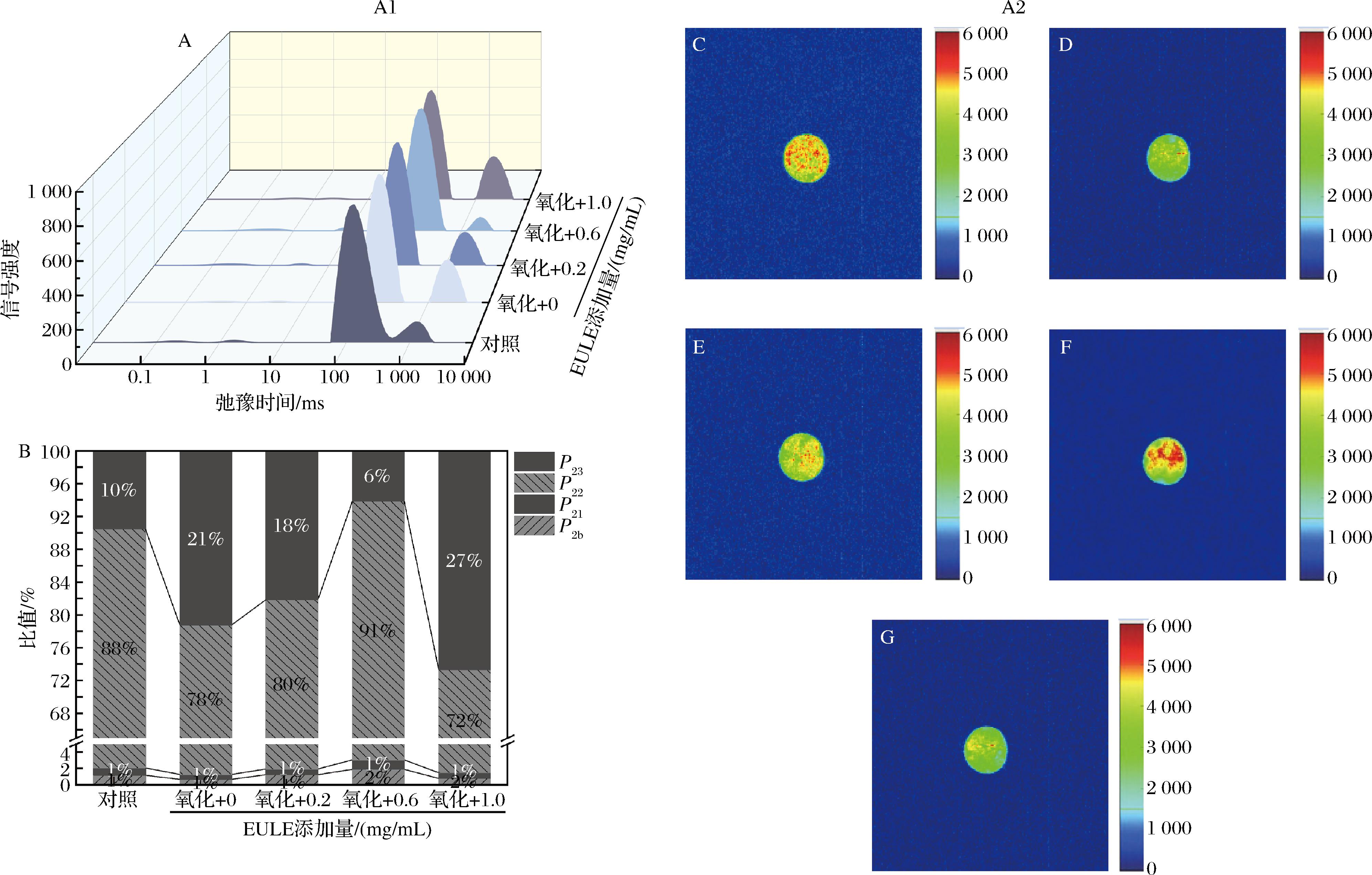
C为空白对照组;D~G均为氧化处理组,其中D为氧化对照组,E~G依次为添加0.2、0.6、1.0 mg/mL EULE处理组;
图A2右侧标尺代表信号强度,数值越高,代表该区域的信号越强A1-A和B分别为MP凝胶核磁3D瀑布图和核磁柱状堆积图;A2-凝胶MRI图像
图4 EULE对氧化MP凝胶水分布特性的影响
Fig.4 Effect of EULE on water distribution characteristics of oxidized MP gel
MRI技术能直观展示出MP凝胶中的水分迁移情况。图4-A2呈现了MP凝胶中水分状态的差异性。其中,绿色区域代表自由水的存在,红色区域代表结合水或固定水的存在[29]。对照组的凝胶水分分布均匀,且结合水含量较高。MP凝胶经过氧化处理后,其图像呈现大面积绿色,说明自由水含量较多。添加中低添加量的EULE显著提升了MP凝胶WHC,其中0.6 mg/mL处理组凝胶呈现强烈鲜红色信号,表明凝胶中结合水与固定水含量有所增加。此现象可能归因于EULE中多酚类物质的作用机制:其能够抑制蛋白质聚集,推动凝胶网络实现有序交联,促使规则亲水孔隙形成,进而提升持水能力。然而,1.0 mg/mL组凝胶的图像颜色与氧化对照组相似,同样呈现出大面积的绿色,表明凝胶中的固定水和结合水减少,而自由水含量增多。
2.7 EULE的添加对MP凝胶微观结构的影响
如图5所示,扫描电子显微镜观察发现,未经氧化处理的MP凝胶呈现出均匀、致密的三维网络结构。然而,氧化处理后,这种有序结构遭到明显破坏,凝胶网络变得松散,孔径增大且分布不均,甚至出现明显的聚集块。这一现象与氧化处理导致MP凝胶的G′显著下降、WHC和凝胶强度明显降低的结果相一致。氧化引起的蛋白质分子间交联聚集以及凝胶孔隙结构劣化,可能是导致凝胶微观结构恶化的主要原因。添加中低量的EULE后,MP凝胶的网络结构得到一定程度的优化。与氧化对照组相比,适量EULE处理的MP凝胶表面更加光滑细致,孔径减小,网络结构趋于规则有序。推测可能是EULE中的酚类化合物通过抗氧化作用改善了凝胶结构,使其网络更均匀,孔径缩小。然而,当EULE添加量较高(1.0 mg/mL)时,凝胶网络结构再次变得粗糙,孔径显著增大,三维网状结构被破坏。已有研究表明,EULE在高浓度下会降低淀粉类凝胶的G′和G″,使凝胶表现出更强的“液态”特征,结构稳定性下降[7]。类似机制可能也适用于MP蛋白凝胶,即高添加量EULE削弱了凝胶的弹性与机械强度,导致微观结构松散、孔洞粗大。凝胶微观结构的改变直接影响其功能特性。网络致密、孔径均匀的凝胶通常具有较高的WHC和凝胶强度,而结构松散、孔洞粗大的凝胶则表现出较差的持水性和较弱的机械性能。这一结论与WHC和凝胶强度的实验结果相一致。
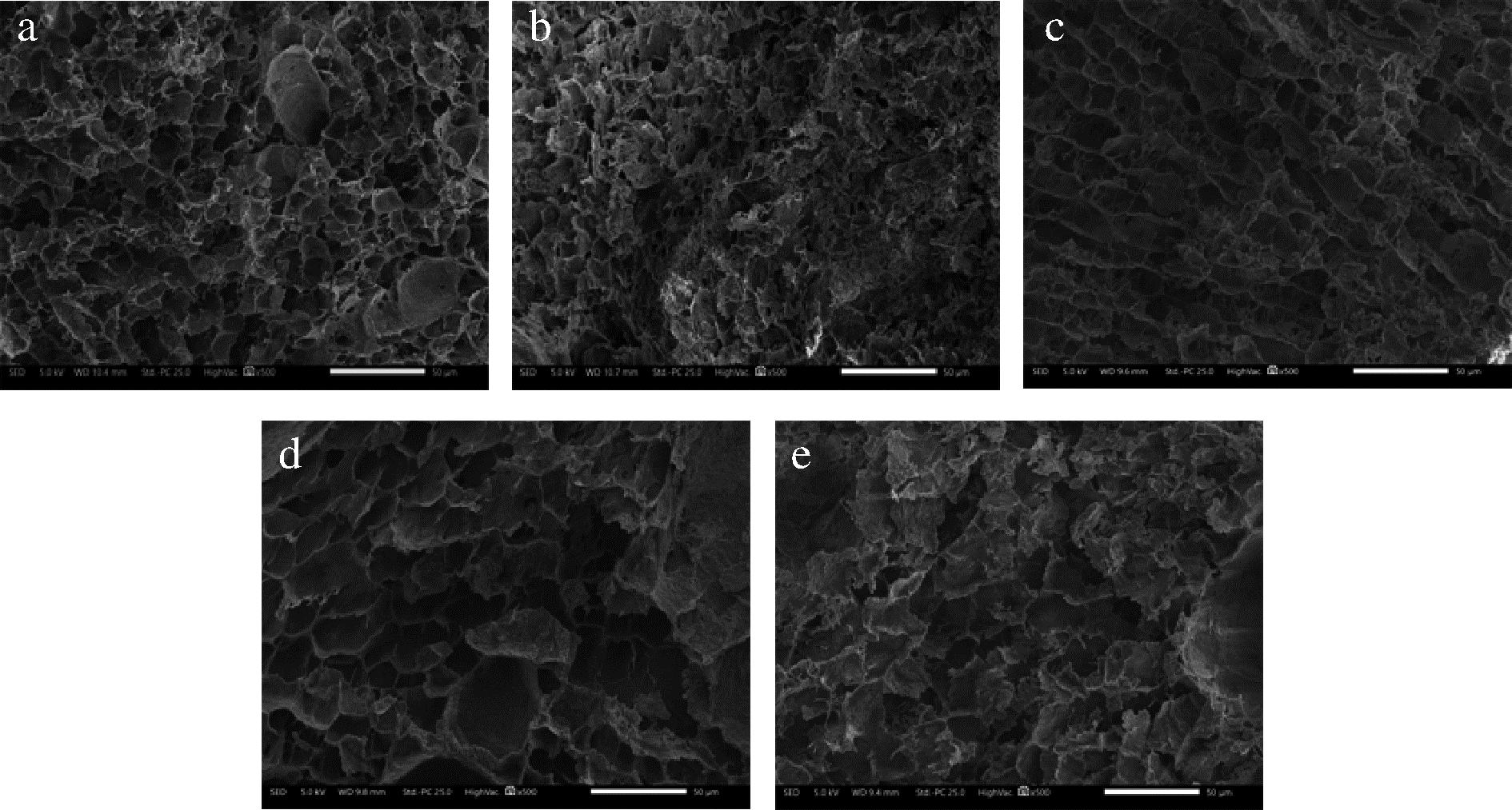
a-空白对照组;b-氧化对照组;c-0.2 mg/mL EULE处理组;d-0.6 mg/mL EULE处理组;e-1.0 mg/mL EULE处理组
图5 EULE对氧化MP凝胶微观结构的影响
Fig.5 Effects of EULE on the microstructure of oxidized MP gel
3 结论与讨论
EULE对氧化应激条件下MP凝胶特性的调控作用呈现明显的剂量依赖性效应。结果表明,氧化处理会显著削弱MP凝胶的各项性能。EULE的添加效果因浓度不同而表现出显著差异:在低添加量(0.2 mg/mL)时,对凝胶性能的提升作用较小;在中添加量(0.6 mg/mL)时,凝胶的强度、WHC显著增强,质构特性得到优化,结合水比例增加,G′和G″显著提升,且形成了致密均匀的三维网络结构;而在高添加量(1.0 mg/mL)时,过量多酚引发蛋白质过度交联,破坏网络连续性,导致凝胶微观结构再度粗糙、孔径增大,WHC、凝胶强度等功能指标回落至氧化对照组水平,自由水比例回升。综上,质量浓度为0.6 mg/mL 的EULE能有效调控氧化MP的交联平衡与微观结构完整性,显著改善其凝胶功能特性。这一发现为EULE作为天然抗氧化剂在肉制品加工中的应用提供了理论依据,同时也为杜仲叶资源在食品工业中的高值化利用提供了新的思路。
[1] 卢海立, 屈莎, 唐善虎, 等.姜黄提取物对牦牛肌原纤维蛋白抗氧化性及凝胶特性的影响[J].现代食品科技, 2024, 40(9):288-295.LU H L, QU S, TANG S H, et al.Effects of turmeric extract on the antioxidant activity and gel properties of yak myofibrillar protein[J].Modern Food Science &Technology, 2024, 40(9):288-295.
[2] LUND M N, HEINONEN M, BARON C P, et al.Protein oxidation in muscle foods:A review[J].Molecular Nutrition &Food Research, 2011, 55(1):83-95.
[3] CAO Y G, XIONG Y L.Chlorogenic acid-mediated gel formation of oxidatively stressed myofibrillar protein[J].Food Chemistry, 2015, 180:235-243.
[4] JIA N, WANG L T, SHAO J H, et al.Changes in the structural and gel properties of pork myofibrillar protein induced by catechin modification[J].Meat Science, 2017, 127:45-50.
[5] WANG W R, LIU F S, DAI G L, et al.Preparative separation of chlorogenic acid from Eucommia ulmoides extract via fractional extraction[J].Journal of Chemical Technology &Biotechnology, 2020, 95(8):2139-2148.
[6] ZHAO Y N, WANG W H, WU Y Q, et al.Effects of Eucommia ulmoides leaf extract on the technological quality, protein oxidation, and lipid oxidation of cooked pork sausage during refrigerated storage[J].Foods, 2025, 14(3):441.
[7] HAN S H, WU Y Y, CHEN S M, et al.Effects of Eucommia ulmoides leaf powder on the gelatinization, rheology, and gel properties of sweet potato starch[J].LWT, 2024, 203:116428.
[8] 刘仙俊, 范向前, 史起鹏, 等.燕麦总多酚的微波辅助提取工艺研究[J].食品研究与开发, 2016, 37(17):55-58;59.LIU X J, FAN X Q, SHI Q P, et al.Study on microwave-assisted extraction of total polyphenols from oat[J].Food Research and Development, 2016, 37(17):55-58;59.
[9] 王萍, 王宇鹤, 李辉, 等.枇杷核不同极性萃取物总黄酮、总多酚含量与其抗氧化活性的相关性[J].化学试剂, 2020, 42(9):1067-1072.WANG P, WANG Y H, LI H, et al.Correlation between the content total flavonoids and total polyphenols in loquat nuclear with different extracts and their antioxidant activities[J].Chemical Reagents, 2020, 42(9):1067-1072.
[10] 尉立刚, 孙文艳, 范三红, 等.冷冻期间猪肌内脂肪氧化及肌纤维蛋白凝胶性能的差异分析[J].现代食品科技, 2022, 38(2):104-109.YU L G, SUN W Y, FAN S H, et al.Analysis of differences in lipid oxidation and gel properties of porcine myofibrillar protein during frozen storage period[J].Modern Food Science &Technology, 2022, 38(2):104-109.
[11] 常海军, 胡渝, 石源伟, 等.鼠曲草提取物-焦磷酸钠对热诱导的猪肌原纤维蛋白凝胶特性的影响[J/OL].重庆工商大学学报(自然科学版), 2025.https://link.cnki.net/urlid/50.1155.N.20240521.1242.002.CHANG H J, HU Y, SHI Y W, et al.Effects of Gnaphalium affine extract(GAE) and sodiumpyrophosphate(PP) on the gel properties of heat-induced pork myofibrillar proteins[J/OL].Journal of Chongqing Technology and Business University (Natural Science Edition), 2025.https://link.cnki.net/urlid/50.1155.N.20240521.1242.002.
[12] 杨兰心, 漆越, 黄江, 等.竹叶粉对肌原纤维蛋白凝胶特性和蛋白结构的影响[J].食品与发酵工业, 2025, 51(17):249-255.YANG L X, QI Y, HUANG J, et al.Effect of bamboo leaf powder on myofibrillar protein gel properties and protein structure[J].Food and Fermentation Industries, 2025, 51(17):249-255.
[13] 陈昌, 王鹏, 徐幸莲.不同质量比鸡胸肉、鸡腿肉混合肌原纤维蛋白的热诱导凝胶特性[J].食品科学, 2012, 33(9):58-63.CHEN C, WANG P, XU X L.Heat-induced gel prosperities of mixed chicken breast and leg myofibrillar proteins at various ratios[J].Food Science, 2012, 33(9):58-63.
[14] 李保玲, 李颖, 范鑫, 等.焦磷酸钠与谷氨酰胺转氨酶对氧化损伤肌原纤维蛋白凝胶性能的协同改善效应[J].中国农业科学, 2021, 54(16):3527-3536.LI B L, LI Y, FAN X, et al.Synergistic enhancement of gelling properties of oxidatively damaged myofibrillar protein by sodium pyrophosphate and transglutaminase[J].Scientia Agricultura Sinica, 2021, 54(16):3527-3536.
[15] 李苓, 杨明柳, 周迎芹, 等.加热温度对鳜鱼肌原纤维蛋白凝胶特性的影响[J].食品与发酵工业, 2023, 49(19):242-248.LI L, YANG M L, ZHOU Y Q, et al.Effects of heating temperature on gel properties of mandarin fish (Siniperca chuatsi) myofibrillar protein[J].Food and Fermentation Industries, 2023, 49(19):242-248.
[16] LIN D Q, ZHANG L T, LI R J, et al.Effect of plant protein mixtures on the microstructure and rheological properties of myofibrillar protein gel derived from red sea bream (Pagrosomus major)[J].Food Hydrocolloids, 2019, 96:537-545.
[17] 郭家刚, 杨松, 童光祥, 等.低压静电场辅助冷冻对竹笋品质的影响[J].食品科学, 2022, 43(23):82-88.GUO J G, YANG S, TONG G X, et al.Effect of low voltage electrostatic field-assisted freezing on the quality of bamboo shoots[J].Food Science, 2022, 43(23):82-88.
[18] 李学鹏, 刘慈坤, 周明言, 等.羟自由基氧化对草鱼肌原纤维蛋白结构和凝胶性质的影响[J].食品科学, 2017, 38(21):30-37.LI X P, LIU C K, ZHOU M Y, et al.Effect of hydroxyl radical oxidation on structural and gel properties of myofibrillar protein from grass carp[J].Food Science, 2017, 38(21):30-37.
[19] 贾娜, 孙嘉, 刘丹, 等.槲皮素对氧化条件下猪肉肌原纤维蛋白结构及凝胶特性的影响[J].食品科学, 2021, 42(10):45-51.JIA N, SUN J, LIU D, et al.Effect of quercetin on the structure and gel properties of pork myofibrillar protein under oxidative conditions[J].Food Science, 2021, 42(10):45-51.
[20] FENG X C, CHEN L, LEI N, et al.Emulsifying properties of oxidatively stressed myofibrillar protein emulsion gels prepared with (-)-epigallocatechin-3-gallate and NaCl[J].Journal of Agricultural and Food Chemistry, 2017, 65(13):2816-2826.
[21] 贾娜, 金伯阳, 刘丹, 等.儿茶素对肌原纤维蛋白氧化、结构及凝胶特性的影响[J].肉类研究, 2020, 34(4):13-19.JIA N, JIN B Y, LIU D, et al.Effect of catechin on the oxidation, structure and gel properties of myofibrillar protein[J].Meat Research, 2020, 34(4):13-19.
[22] 李玲, 季慧, 康大成, 等.氧化条件下茶多酚对猪肉肌原纤维蛋白理化和凝胶特性的影响[J].食品科学, 2019, 40(2):12-17.LI L, JI H, KANG D C, et al.Effect of tea polyphenols on physicochemical and gel properties of pork myofibrillar protein under oxidative conditions[J].Food Science, 2019, 40(2):12-17.
[23] 周非白. 氧化修饰对猪肉肌原纤维蛋白结构与功能特性的调控研究[D].广州:华南理工大学, 2016.ZHOU F B.Study on the regulation of oxidative modification on the structural and functional characteristics of pork myofibrillar protein[D].Guangzhou:South China University of Technology, 2016.
[24] 常海军, 石源伟, 伯朝英, 等.氧化条件下姜黄素对猪肉肌原纤维蛋白理化和凝胶特性的影响[J].食品科学, 2024, 45(8):63-71.CHANG H J, SHI Y W, BO Z Y, et al.Effect of curcumin on physicochemical and gel properties of pork myofibrillar proteins under oxidative condition[J].Food Science, 2024, 45(8):63-71.
[25] CHENG J R, LIN Y S, TANG D B, et al.Structural and gelation properties of five polyphenols-modified pork myofibrillar protein exposed to hydroxyl radicals[J].LWT, 2022, 156:113073.
[26] 李可, 李燕, 康超娣, 等.常压等离子体射流对鸡肉肌原纤维蛋白结构和流变特性的影响[J].食品科学, 2020, 41(19):124-131.LI K, LI Y, KANG C D, et al.Effect of atmospheric pressure plasma jet on structural and rheological properties of chicken myofibrillar protein[J].Food Science, 2020, 41(19):124-131.
[27] ZHU X S, SHI X D, LIU S H, et al.Physicochemical properties and gel-forming ability changes of duck myofibrillar protein induced by hydroxyl radical oxidizing systems[J].Frontiers in Nutrition, 2022, 9:1029116.
[28] CAO Y G, LI B L, FAN X, et al.Synergistic recovery and enhancement of gelling properties of oxidatively damaged myofibrillar protein by L-lysine and transglutaminase[J].Food Chemistry, 2021, 358:129860.
[29] WANG H L, KAY M, ZHANG D J, et al.Improvement of oxidized myofibrillar protein gel properties by black rice extract[J].Food Chemistry:X, 2024, 21:101117.