高效酶的理性设计一直是蛋白质工程领域的难点之一。虽然定向进化等实验方法在酶改造领域已取得了重大突破,但上述方法通常存在周期长、准确率低、资源浪费等问题[1-2]。随着计算机和人工智能技术的发展,许多酶分子理性设计工具(如PROSS[3]、FuncLib[4]、FireProt[5]等)已被开发出来并用于酶分子的理性设计。近年来,尤其是基于蛋白质的序列和三维结构进行蛋白质理性设计的深度学习工具推动了酶工程领域的快速发展。例如,KAO等[6]使用基于深度学习和图神经网络开发的AlphFold2预测出泛素突变体与泛素连接酶所形成的稳定复合物的三维结构,随后通过实验证实了结构的准确性。基于图神经网络和消息传递机制开发的ProteinMPNN是一个先进的酶分子设计工具,能够执行多种设计任务并表现出卓越的设计潜力[7-9]。例如,BAKER团队利用该工具成功提升了血红蛋白和TEV蛋白酶的热稳定性和表达水平[10]。基于物理和统计能量函数开发的Rosetta经过多年的发展已成为蛋白质设计领域的最全软件包之一。它可以执行蛋白结构预测、从头设计蛋白质等定制化的酶分子改造任务。例如ABBASS等[11]和RICHTER等[12]利用Rosetta3从头设计出高性能的三碳糖磷酸异构酶。此外,分子动力学模拟赋予静态蛋白质以动态行为,为酶的理性改造及其催化机制的深入解析提供了重要的理论支撑,已在酶分子设计领域得到了广泛的应用。例如,ZHU等[13]利用分子动力学模拟的方法解析了脂肪酶热稳定性提升的原因,氢键相互作用维持了突变体loop区的构象,从而增加了酶的刚性使得热稳定性得到提升。
γ-氨基丁酸(γ-aminobutyric acid,GABA)是一种广泛存在于自然界中的非蛋白质氨基酸,在微生物以及动植物的生命活动过程中发挥着重要功能,如预防神经性疾病、增强免疫力等[14-15]。谷氨酸脱羧酶(glutamate decarboxylase,GAD)能催化L-谷氨酸(L-glutamic acid,L-Glu)脱羧生成GABA,目前已有多个研究对GAD催化L-Glu生成GABA进行了报道,然而天然的GAD通常存在热稳定性差的缺点[16-18]。因此提高其热稳定性成为近年来的热点,目前对GAD的改造方法主要集中在实验方法。例如,YAO等[19]通过构建共表达GAD体系提高了GABA的产量,方卉等[20]通过脯氨酸效应提高了GAD的热稳定性,CHA等[21]通过激活xyl操纵子的方法显著提高了短乳杆菌GABA的产量。SHI等[22]、YANG等[23]通过定点突变的方法拓宽了GAD催化pH值的范围。为了提高GAD的热稳定性,本研究使用深度学习工具ProteinMPNN、AlphaFold2以及分子动力学模拟对GAD进行了理性设计,得到稳定性提高的突变体,并利用分子模拟和生物信息学方法探究了突变体热稳定性和底物结合能力提高的机制。
1 材料与方法
1.1 ProteinMPNN设计更稳定的GAD
野生型GAD(wild-type,WT)的三维结构通过AlphaFold v2.3.1生成,相关的结构信息参考了蛋白质结构数据库中登录号为5GP4的GAD结构[24]。为评估GAD序列的进化保守性,使用Bioinformatics Toolkit从UniRef30数据库(版本2023_02)中检索同源性高的GAD序列1 000条,随后利用hhfilter进一步过滤收集到的序列来获得高质量的同源序列集合98条,最后利用这些序列计算每个位置氨基酸的保守性[25-26]。深度学习工具ProteinMPNN用于设计突变体,设计的过程中使用3个不同采样温度(0.1、0.2、0.3),每种温度下生成5个突变体,所有突变体的三维结构通过AlphaFold v2.3.1获得。
1.2 分子对接
GAD在催化L-Glu生成GABA时磷酸吡哆醛(pyridoxal phosphate, PLP)和L-Glu会形成重要的醛亚胺结构,是催化过程中的关键步骤,因此将PLP与L-Glu形成的醛亚胺结构(PLP-Glu)作为底物分子,PLP与Glu形成的醛亚胺结构通过PyMOL构建[27]。Rosetta用于执行柔性分子对接以初步模拟GAD与PLP-Glu的结合模式,过程如下:AddOrRemoveMatchCsts用于约束对接过程中PLP与催化残基K280之间的距离<3.5 Å,Transform用于设置对接过程中每次采样移动的距离为0.2 Å,角度20°,HighResDocker用于执行高分辨率的对接,每一次对接可以循环6次取其中最佳对接结果进行输出。
1.3 GAD的分子动力学模拟
分子动力学模拟通过GROMACS 2022.6软件包进行[28],初步筛选的模拟过程使用计算效率更高的Gromos 54A7力场进行参数化,依次完成能量最小化、恒温恒体积(constant number of particles, volume and temperature ensemble, NVT)和恒温恒压(constant number of particles, pressure and temperature ensemble, NPT)预平衡后进行50 ns的模拟,初步筛选以均方根偏差的变化(change of root mean square deviation,ΔRMSD,ΔRMSD=RMSD_Mut-RMSD_WT)<-0.1 nm作为标准[29]。随后将模拟温度升高至320 K进一步筛选,使用精度更高的力场Amber14 sb对初步筛选到的突变体进行参数化,依次完成能量最小化、NVT和 NPT预平衡后进行50 ns模拟,选择RMSD值最低的突变体进一步研究。在探究热稳定性时,模拟温度升高至350 K,使用Amber14 sb力场进行参数化,依次完成能量最小化、NVT和NPT预平衡后进行300 ns模拟。在探究底物与酶分子相互作用的模拟中,模拟温度使用反应温度310 K,力场使用Amber14 sb力场并使用最陡下降法和共轭梯度法进行能量最小化,经过NVT、NPT预平衡后执行300 ns的模拟,小分子拓扑文件通过使用Sobtop和Multiwfn生成[30-31]。gmx_mpi rms、gmx_mpi rmsf、gmx_mpi mindist以及gmx_mpi sasa分别用于计算均方根偏差(root mean square deviation,RMSD)、均方根波动(root mean square fluctuation,RMSF)、接触数(number of contact)、溶剂可及表面积(solvent accessible surface area,SASA)。gromos聚类算法用于找到模拟过程中的典型构象,设置RMSD的截断值为0.15 nm。GAD与底物之间的相互作用指纹通过Prolif进行分析,结合口袋通过CASTpFold进行分析。
2 结果与分析
2.1 ProteinMPNN结合分子动力学模拟设计更稳定的GAD
ProteinMPNN可以读取输入蛋白质的结构信息但无法直接获取有关功能的信息,因此需要将参与反应的残基作为关键残基,并作为额外补充的功能信息(图1-a红色区域)。关键残基通过参考GAD的晶体结构确定。此外,还需要考虑GAD的进化信息,每个位置氨基酸的保守性如图1-b所示。基于GAD的结构信息和进化信息,本研究使用ProteinMPNN开展突变体设计,共设置了2种设计方案,方案一为固定关键残基及其6 Å范围内的残基和保守性排名前50%的残基(图1-a),方案二是固定关键残基及其6 Å范围内的残基和保守性排名前70%的残基,每一个方案设计15个突变体,最终得到30个不同的突变(Mut1-Mut30)。所有突变体的三维结构均由AlphaFold v2.3.1预测生成,图1-c和图1-d分别展示了2种设计策略所对应突变体的三维结构,所有突变体的结构都有较高的结构置信度(pLDDT>90,如电子版增强出版附表1,https://doi.org/10.13995/j.cnki.11-1802/ts.043702, 下同)且与WT的结构高度一致(RMSD<1 Å,附表1),为保持其催化活性提供了坚实的结构基础。
表1 模拟过程中最后10 ns GAD与PLP-Glu之间的结合能
Table 1 Binding energy between GAD and PLP-Glu during the last 10 ns of the simulation
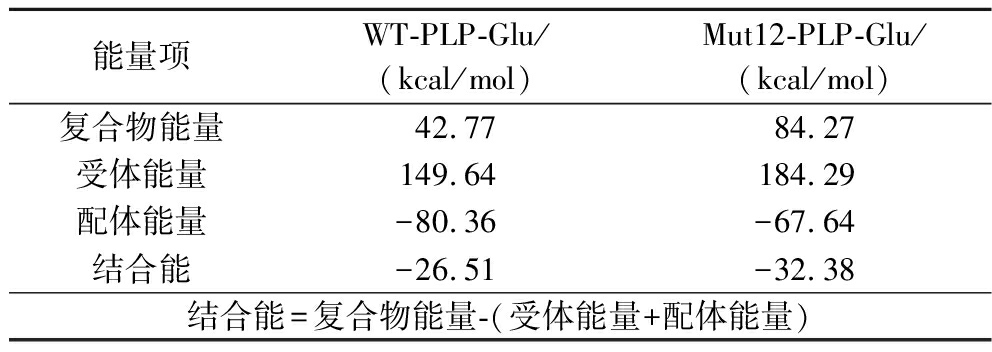
能量项WT-PLP-Glu/(kcal/mol)Mut12-PLP-Glu/(kcal/mol)复合物能量42.7784.27受体能量149.64184.29配体能量-80.36-67.64结合能-26.51-32.38结合能=复合物能量-(受体能量+配体能量)
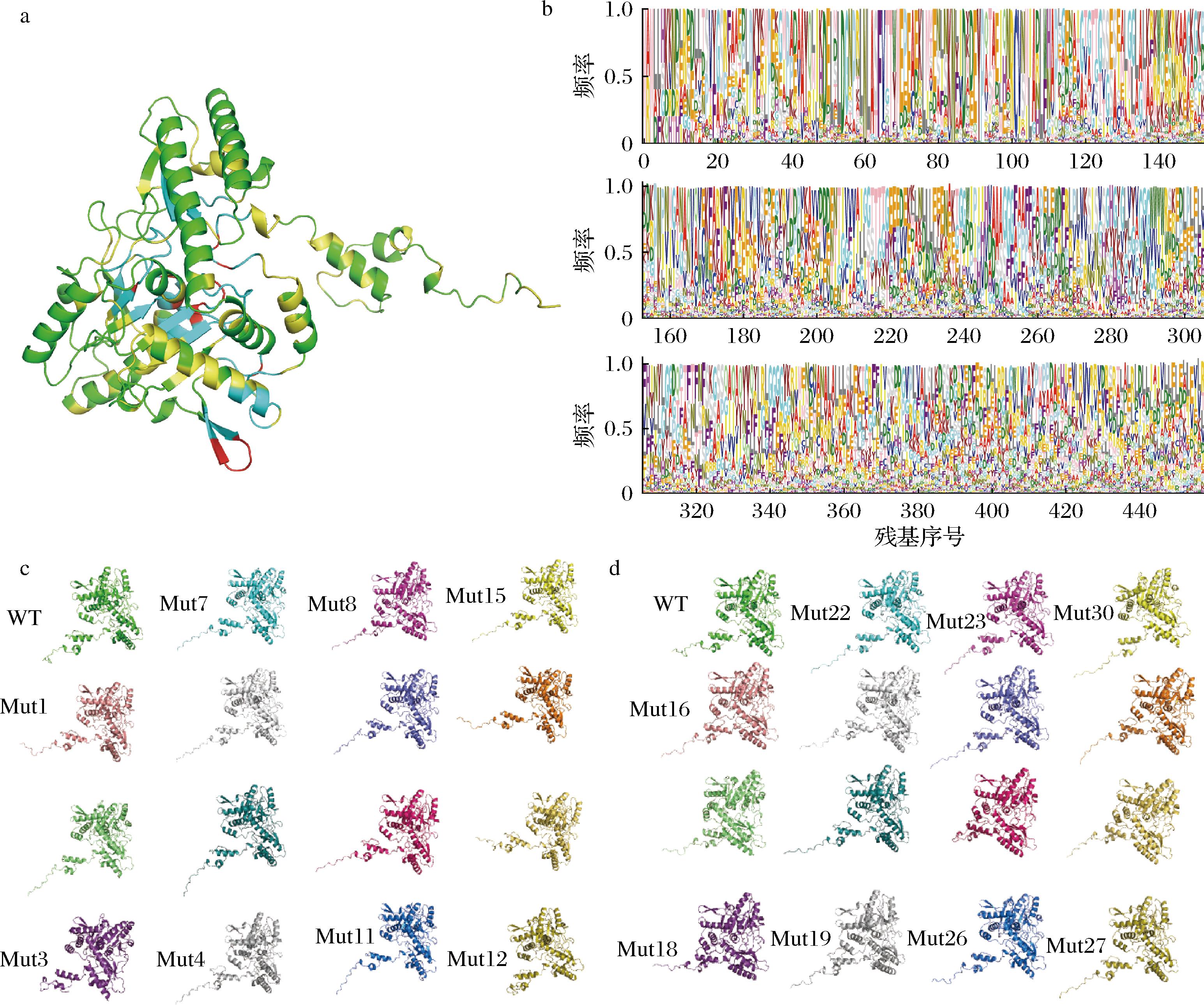
a-设计过程中固定的氨基酸残基;b-每个位置氨基酸保守性分析;c-WT与Mut1-Mut15的结构;d-WT与Mut16-Mut30的结构
图1 利用ProteinMPNN设计GAD
Fig.1 GAD designed using ProteinMPNN
注:a图中红色为催化关键残基,蓝色为其6 Å范围内残基,黄色为保守性排名前50%的残基。
随后采用分子动力学模拟方法筛选突变体,在初步的筛选工作中,首先使用更高效率的Gromos 54A7力场在310 K的温度下对WT及所有的突变进行了50 ns的分子动力学模拟,来初步评估突变体的稳定性。模拟过程中的RMSD是衡量蛋白质稳定性重要参数,以ΔRMSD<-0.1 nm为筛选标准,初步筛选出8个稳定性更高的突变体Mut10、Mut12、Mut14、Mut17、Mut19、Mut27、Mut28、Mut29(图2-a、图2-b)。随后将温度升高至320 K进一步筛选,使用精度更高的Amber14 sb力场对WT与8个潜在突变体进行50 ns的分子动力学模拟,模拟发现,当温度升高之后,Mut12表现出最佳的热稳定性,Mut12的RMSD在0.6~0.7 nm波动,而WT却在1~1.2 nm波动(图2-c)。进一步对两者在320 K下的主链波动情况进行分析,发现相比WT,Mut12的N端区域结构也更加稳定(图2-d)。
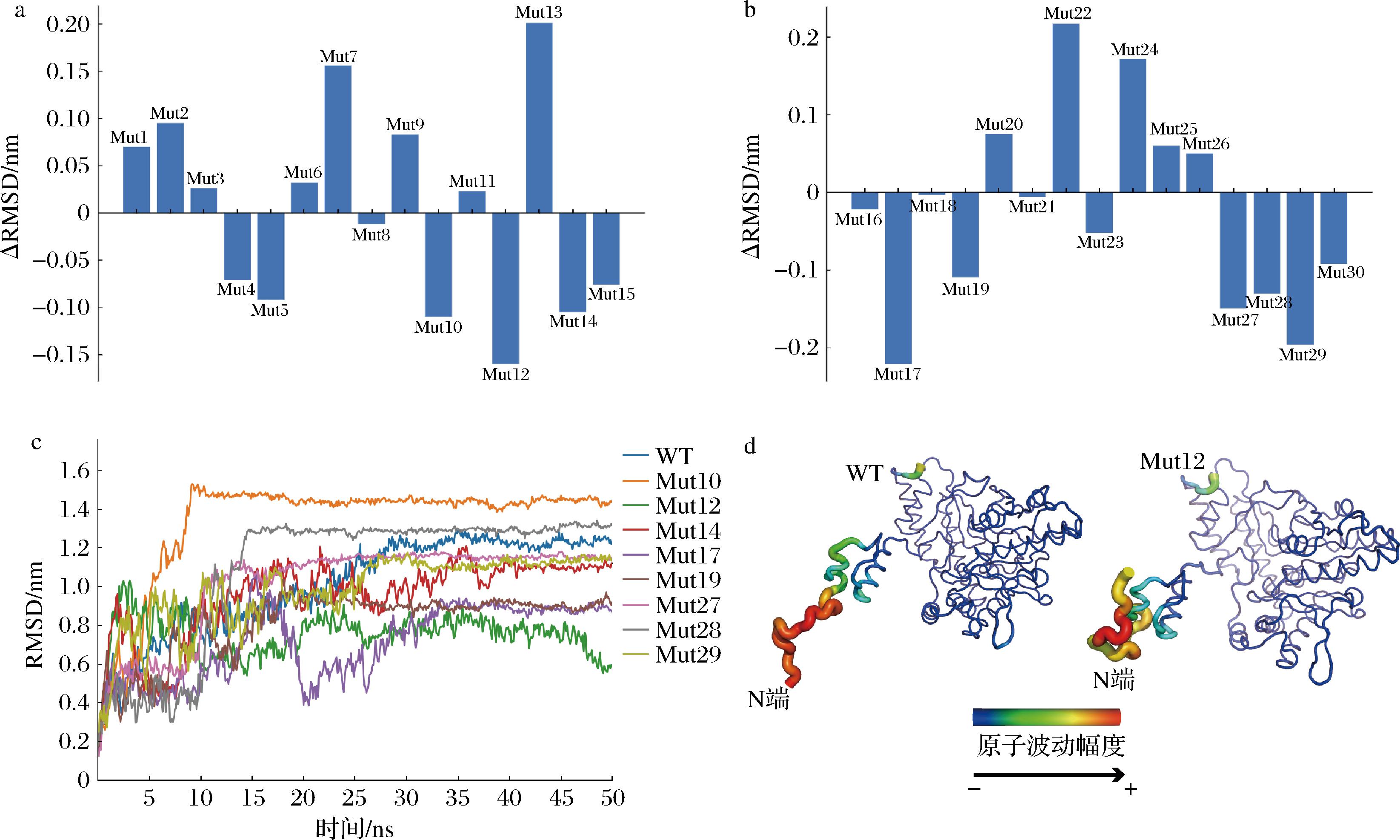
a-Mut1-Mut15的ΔRMSD;b-Mut16-Mut30的ΔRMSD;c-WT及8个潜在突变体在320 K环境下模拟中RMSD的变化;d-WT与Mut12模拟过程中骨架的波动情况
图2 分子动力学模拟筛选突变体
Fig.2 Screening of mutants by molecular dynamics simulation
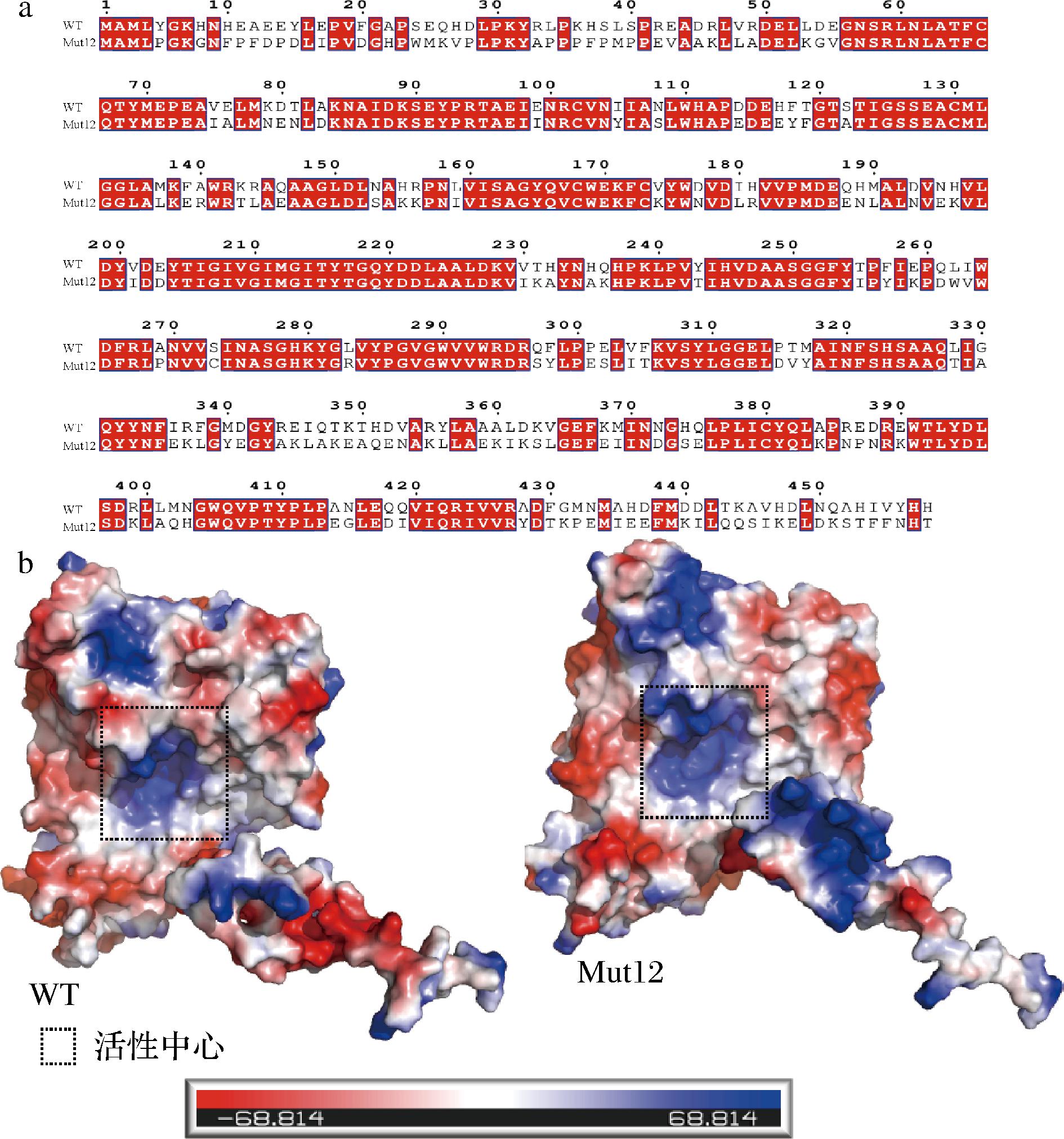
a-序列比对;b-电荷密度的分布
图3 WT与Mut12的序列比对及电荷分布分析
Fig.3 Sequence alignment and electrostatic surface analysis of WT and Mut12
将WT的序列与Mut12进行序列比对(图3-a),发现ProteinMPNN重新设计了159个位点,其中在GAD的N端区域以及269、386等多个位点引入了脯氨酸,脯氨酸是一种具有较大刚性的氨基酸,能够通过限制主链构象的自由度,增加蛋白质的刚性,从而提升蛋白质的结构稳定性[32]。此外,还发现在80、83、156等位点引入了酸性或者碱性氨基酸,这种改变通常会使得酶分子的电荷密度分布发生改变,因此分析了WT与Mut12的电荷分布情况,结果如图3-b所示。结果表明Mut12口袋区域的正电荷密度更高,在发生反应时有助于带负电荷的底物谷氨酸(L-Glu)结合,从而增强其催化效率。综上所述,Mut12被推测为具有较高热稳定性和良好底物结合能力的潜在突变体,因此本研究进一步对其热稳定性及对底物的亲和力进行了深入分析。
2.2 分子动力学模拟探究GAD的热稳定性
高温可以增加分子间接触的概率从而加速反应的进行,但通常也会降低酶的稳定性,GAD的最适催化温度通常为37 ℃(310 K),当温度再升高时会使GAD的结构发生改变从而失去催化活性[33]。为了进一步探究Mut12的热稳定性,将WT和Mut12分别在350 K(87 ℃)的高温下进行了300 ns的分子动力学模拟。图4-a为WT和Mut12模拟过程中蛋白骨架的RMSD变化情况,当体系达到平衡后,WT的RMSD在1.4 nm附近波动,而Mut12的RMSD稳定在1.15 nm附近,这表明Mut12在高温环境下结构变化更小、更稳定。同时还分析了模拟过程中SASA的变化,Mut12在模拟的过程表现出更低的疏水性(图4-b),这表明Mut12在高温环境下结构更加紧密和稳定。
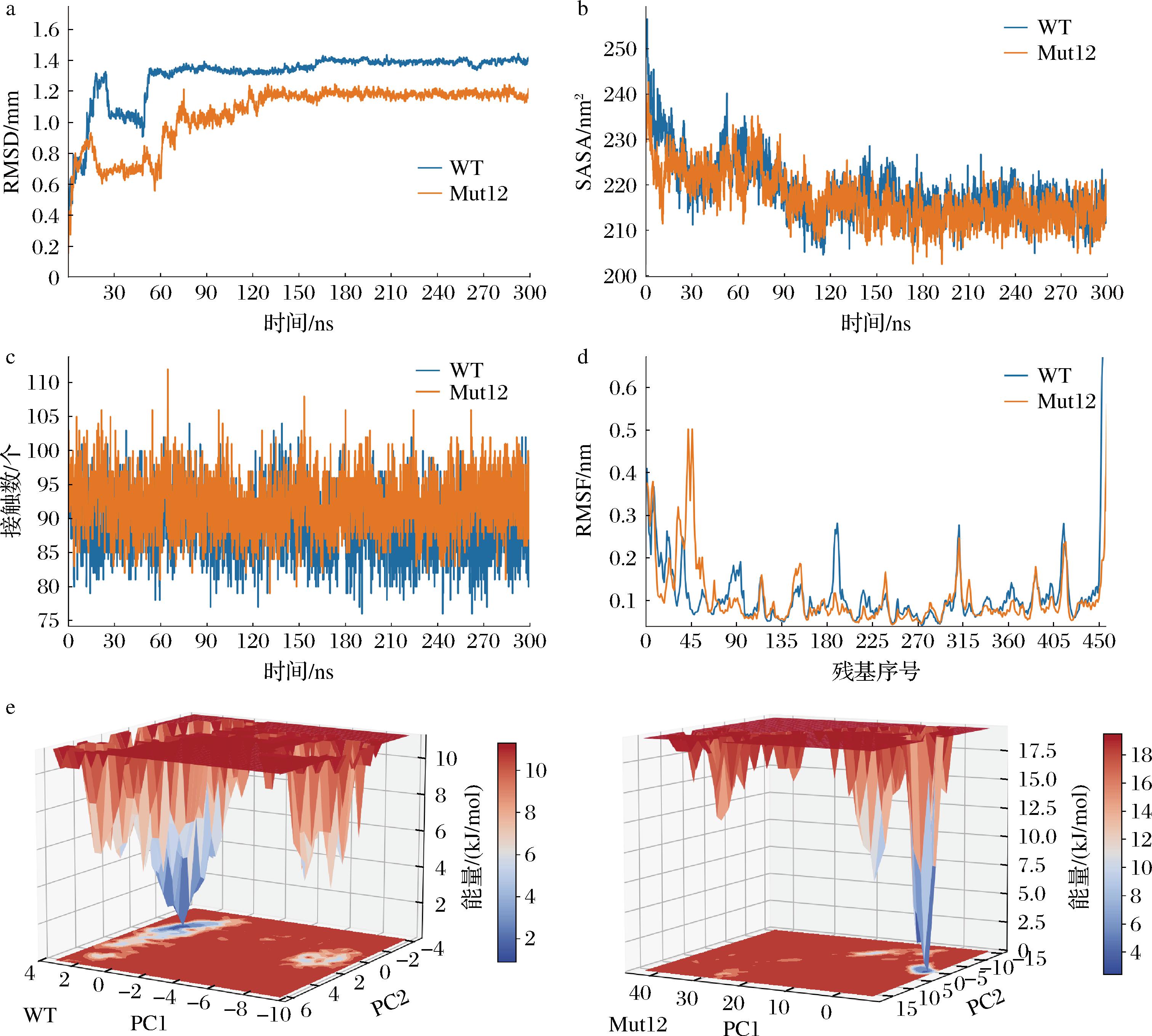
a-WT与Mut12模拟过程中RMSD的变化;b-WT与Mut12模拟过程中SASA的变化;c-WT与Mut12模拟过程中活性中心氢键数量的变化;d-WT与Mut12模拟过程中的RMSF的变化;e-WT与Mut12模拟过程中的自由能形貌图
图4 WT与Mut12在350 K下的分子动力学模拟
Fig.4 Molecular dynamics simulations of WT and Mut12 at 350 K
氢键是热稳定性提高的关键因素,本研究对活性中心形成的氢键数量进行了分析,在模拟的过程中WT的活性中心形成的氢键数量稳定在87个左右,而Mut12形成的氢键数量维持在94个左右,这表明Mut12的活性中心在氢键的加持下比WT要更加稳定,具有在高温下催化反应的潜力(图4-c)[13]。除此之外还分析了模拟过程中每个残基的波动情况(图4-d),从整体上看Mut12具有更强的刚性,80~100残基区域、180~200残基区域、350~380残基区域刚性增强的程度尤为明显,这是Mut12在高温环境下更稳定的关键因素。为进一步探究蛋白质体系的稳定性和构象特性,绘制了自由能形貌图(图4-e),WT体系呈现多个能量集中的低谷,表明其存在多种亚稳态,在多种亚稳态结构之间进行转换,结构稳定性较差,而突变体Mut12只形成了1个明显的能量低谷,表明体系趋向于相对集中的稳定构象。
综上所述,Mut12突变体在350 K高温条件下活性中心和整体结构更加稳定,展现出良好的耐热性,显示出其在高温环境中的应用潜力。
2.3 GAD与底物分子的对接与结合能力评估
本研究通过分子对接初步探索GAD与底物的相互作用模式,在对接过程中,GAD活性位点附近的残基侧链可发生一定程度的构象变化来模拟自然条件下酶与底物的结合。每个体系对接产生200个构象(附图1-a、附图1-b),WT最佳构象的总能量为-1 324.08 REU,Mut12产生的最佳构象有着更低的总能量-1 423.77 REU,Mut12体系更低的总能量意味着更加稳定的体系。图5展示了各体系的最佳结合构象,图5为WT与PLP-Glu的结合模式,底物分子通过与F65、C66、S127、A249、H279、K280、R423之间形成氢键、盐键、疏水相互作用以及π-阳离子相互作用结合在一起,Mut12突变体与底物分子的相互作用通过与G164、T215、A249、S250、K280、R423形成氢键、盐键、疏水相互作用与底物分子稳定地结合在一起。
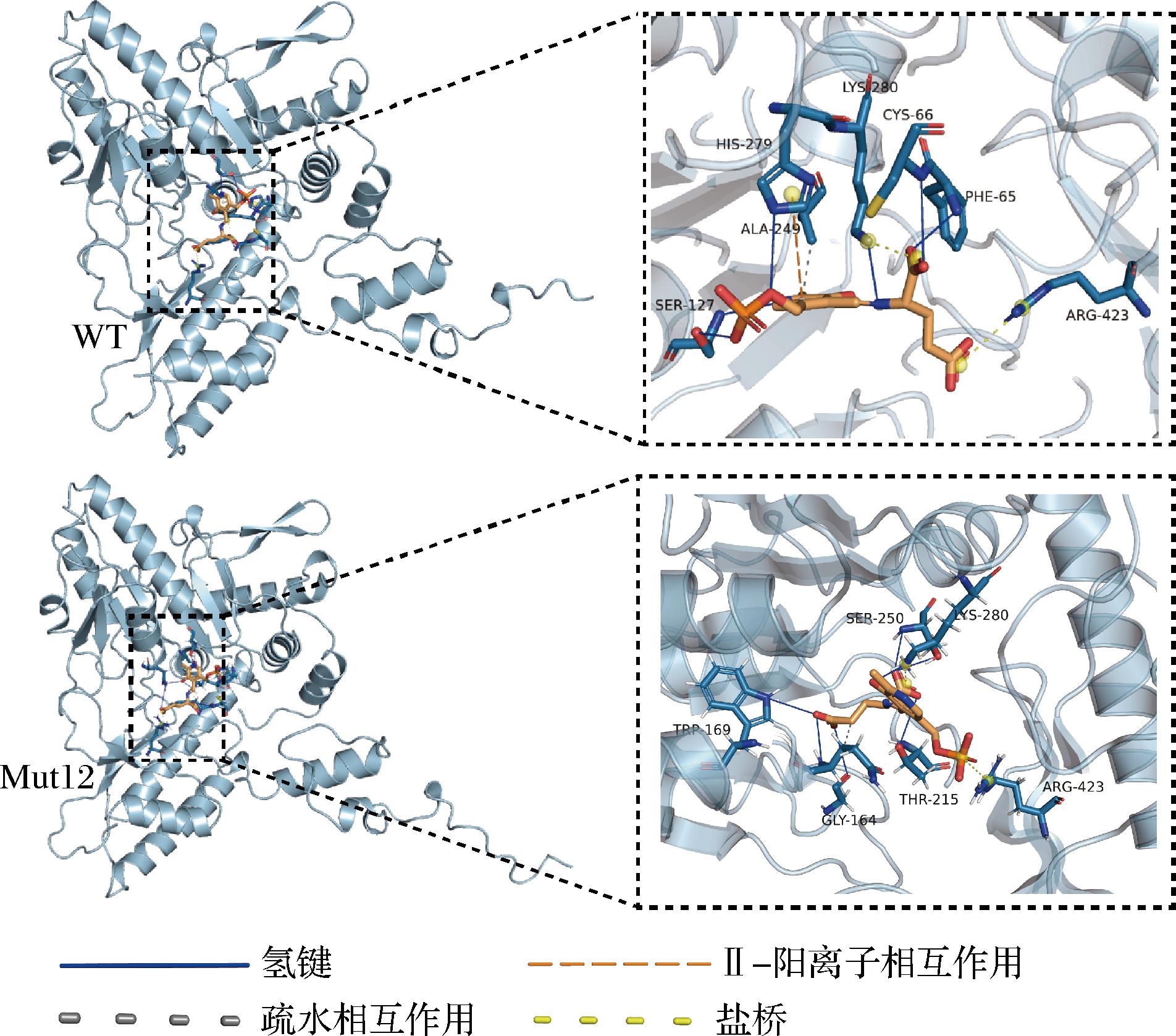
图5 WT、Mut12分别与PLP-Glu之间的相互作用
Fig.5 Interactions between WT or Mut12 and PLP-Glu
基于分子对接获得的复合物构象,进一步通过分子动力学模拟的方法探究WT与Mut12突变体的相互作用模式。在反应温度310 K下,分别对WT-PLP-Glu复合物和Mut12-PLP-Glu复合物进行了300 ns的分子动力学模拟(图6-a)。为了评估GAD与PLP-Glu的结合能力,本研究计算了2个体系模拟过程中最后10 ns的结合能(表1),WT与底物分子间的结合能为-26.51 kJ/mol,Mut12与底物分子间的结合能-32.38 kJ/mol,相较于WT组提升了约22%,这表明Mut12是一个更有利于PLP-Glu结合的GAD突变体[34]。
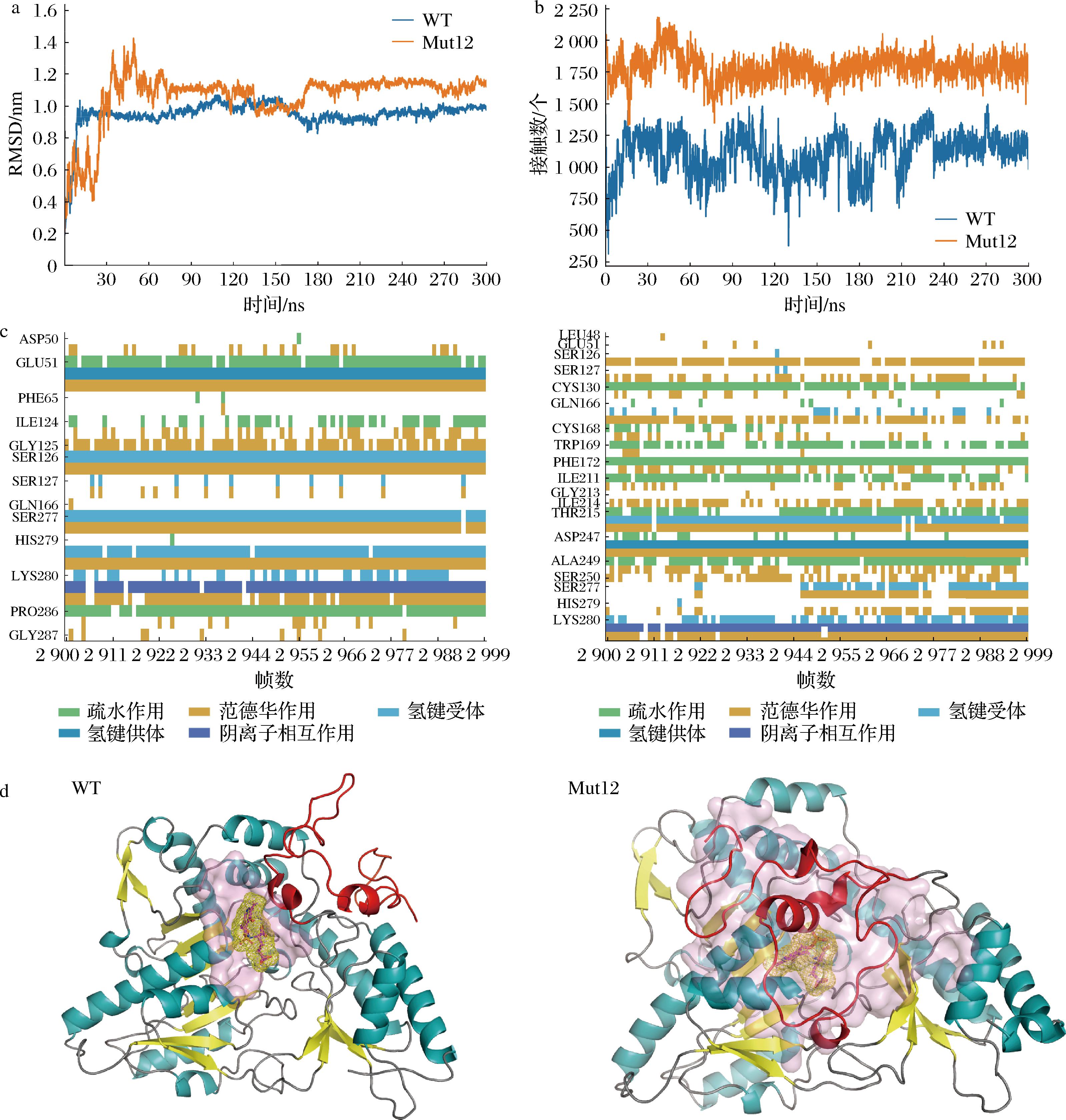
a-模拟过程中的RMSD变化;b-模拟过程中底物与酶分子间接触数的变化;c-WT、Mut12模拟过程中与底物的相互作用指纹分析;d-WT、Mut12模拟过程中典型构象的口袋分析
图6 WT、Mut12在配体结合状态下的分子动力学模拟
Fig.6 Molecular dynamics simulations of WT and Mut12 in the ligand-bound state
注:d图中粉红色区域是形成的口袋,红色区域是N端区域。
接触数可以初步反应酶与底物分子间发生相互作用的强弱以及结合稳定性。在模拟的过程中WT与底物分子间的接触数维持在1 000附近,Mut12与底物分子间的接触数稳定维持在1 750附近(图6-b),这表明Mut12与底物分子发生了更加强烈的相互作用且与底物的结合更稳定,是结合能提高的重要原因之一,这有极大可能促进酶促反应的进行。附图1-c、附图1-d分别为WT与Mut12贡献结合能的关键残基,Mut12相较于WT有更多的残基参与底物的结合,这些残基围绕在底物的周围(附图1-e),这使得Mut12更有利于底物结合。使用Prolif分析了模拟过程中最后10 ns酶与底物之间的相互作用指纹,Mut12相较于WT,有更多的残基能与底物发生范德华相互作用、氢键相互作用以及疏水相互作用(图6-c),这是Mut12体系结合能更大的重要原因[35]。
随后使用CASTpFold分析2个体系模拟过程中的典型构象[36]。发现WT形成了1个窄而浅的口袋,这限制了底物分子的结合,而Mut12形成了1个更加契合底物宽而深的口袋(图6-d),两者的结构差异导致WT体系的结合能小于Mut12体系。导致口袋差异的主要原因是WT的N端有较大的灵活性(附图1-f),使其N端游离在活性位点区域之外从而无法形成更加契合底物的口袋(图6-d)。而D28P、K34P的突变增加了Mut12 N端的刚性(附图1-f),使其能够更好地与活性中心共同形成更加契合底物宽而深的口袋(图6-e)。
3 结论与讨论
GAD是生产GABA的关键限速酶,具有良好的热稳定性和较高的底物亲和力是其工业化应用的重要前提,但实验改造的方法通常存在周期长、准确率低等缺点。因此能否通过更高效的蛋白质工程方法来提高GAD热稳定性、底物结合能力具有重要的研究价值。基于此,本研究通过深度学习工具ProteinMPNN与分子动力学模拟相结合的方法,成功设计并筛选出在高温环境下具有更高结构稳定性、更高底物亲和力的Mut12突变体。设计过程中综合考虑了GAD的进化信息与结构信息,合理保留关键功能位点,有效避免对蛋白整体构象的破坏。结果表明,Mut12与WT相比在高温环境下表现出显著的热稳定性增强。进一步通过柔性对接构建酶-底物复合物并进行分子动力学模拟,发现Mut12参与底物结合的残基数量增加,亲和力增强,结合口袋更加契合底物结构,最终其结合能相较于野生型提高了约22%。
本研究不仅为GAD催化L-Glu高效生产GABA奠定了坚实的理论基础,也为其他酶的热稳定性改造提供了新思路、新方法。综上,本研究充分展示了深度学习与分子模拟技术在现代酶工程中的强大优势与协同潜力,拓宽了蛋白质理性设计的研究视角,为构建具备更优工业性能的酶分子提供了重要参考和理论基础。
[1] COBB R E, CHAO R, ZHAO H M.Directed evolution:Past, present, and future[J].AIChE Journal, 2013, 59(5):1432-1440.
[2] ARNOLD F H.Directed evolution:Bringing new chemistry to life[J].Angewandte Chemie International Edition, 2018, 57(16):4143-4148.
[3] BEDNAR D, BEERENS K, SEBESTOVA E, et al.FireProt:Energy- and evolution-based computational design of thermostable multiple-point mutants[J].PLoS Computational Biology, 2015, 11(11):e1004556.
[4] GOLDENZWEIG A, GOLDSMITH M, HILL S E, et al.Automated structure- and sequence-based design of proteins for high bacterial expression and stability[J].Molecular Cell, 2016, 63(2):337-346.
[5] KHERSONSKY O, LIPSH R, AVIZEMER Z, et al.Automated design of efficient and functionally diverse enzyme repertoires[J].Molecular Cell, 2018, 72(1):178-186.e5.
[6] KAO H W, LU W L, HO M R, et al.Robust design of effective allosteric activators for Rsp5 E3 ligase using the machine learning tool ProteinMPNN[J].ACS Synthetic Biology, 2023, 12(8):2310-2319.
[7] HUANG Z L, NI D W, CHEN Z W, et al.Application of molecular dynamics simulation in the field of food enzymes:Improving the thermal-stability and catalytic ability[J].Critical Reviews in Food Science and Nutrition, 2024, 64(31):11396-11408.
[8] CHEN X H, CHEN Y J, TANG D D, et al.Recent advances in bioinspired multienzyme engineering for food applications[J].Trends in Food Science &Technology, 2025, 156:104840.
[9] LI J L, WANG S J, LIU C, et al.Going beyond the local catalytic activity space of chitinase using a simulation-based iterative saturation mutagenesis strategy[J].ACS Catalysis, 2022, 12(16):10235-10244.
[10] SUMIDA K H, N
 EZ-FRANCO R, KALVET I, et al.Improving protein expression, stability, and function with ProteinMPNN[J].Journal of the American Chemical Society, 2024, 146(3):2054-2061.
EZ-FRANCO R, KALVET I, et al.Improving protein expression, stability, and function with ProteinMPNN[J].Journal of the American Chemical Society, 2024, 146(3):2054-2061.
[11] ABBASS J, NEBEL J C.Rosetta and the journey to predict proteins’ structures, 20 years on[J].Current Bioinformatics, 2020, 15(6):611-628.
[12] RICHTER F, LEAVER-FAY A, KHARE S D, et al.De novo enzyme design using Rosetta3[J].PLoS One, 2011, 6(5):e19230.
[13] ZHU E H, XIANG X, WAN S D, et al.Discovery of the key mutation site influencing the thermostability of Thermomyces lanuginosus lipase by Rosetta design programs[J].International Journal of Molecular Sciences, 2022, 23(16):8963.
[14] LIU Z Y, GUO X L, DAI K Q, et al.Biosynthesis of gamma-aminobutyric acid by engineered Clostridium tyrobutyricum co-overexpressing glutamate decarboxylase and class I heat shock protein[J].Fermentation, 2023, 9(5):445.
[15] ZHU F, HU S, ZHAO W R, et al.A novel method for γ-aminobutyric acid biosynthesis using glutamate decarboxylase entrapped in polyvinyl alcohol-sodium alginate capsules[J].Molecules, 2023, 28(19):6844.
[16] UENO H.Enzymatic and structural aspects on glutamate decarboxylase[J].Journal of Molecular Catalysis B:Enzymatic, 2000, 10(1-3):67-79.
[17] FENALTI G, LAW R H P, BUCKLE A M, et al.GABA production by glutamic acid decarboxylase is regulated by a dynamic catalytic loop[J].Nature Structural &Molecular Biology, 2007, 14(4):280-286.
[18] LIU S J, WEN B T, DU G M, et al.Coordinated regulation of Bacteroides thetaiotaomicron glutamate decarboxylase activity by multiple elements under different pH[J].Food Chemistry, 2023, 403:134436.
[19] YAO L L, LYU C J, WANG Y T, et al.High-level production of γ-aminobutyric acid via efficient co-expression of the key genes of glutamate decarboxylase system in Escherichia coli[J].Engineering Microbiology, 2023, 3(2):100077.
[20] 方卉, 吕常江, 花雨娇, 等.利用脯氨酸效应提高短乳杆菌谷氨酸脱羧酶的热稳定性[J].生物工程学报, 2019,35(4):636-646.FANG H, LYU C J, HUA Y J, et al.Increasing the thermostability of glutamate decarboxylase from Lactobacillus brevis by introducing proline[].Chinese Journal of Biotechnology, 2019,35(4):636-646.
[21] CHA X C, DING J J, BA W Y, et al.High production of γ-aminobutyric acid by activating the xyl operon of Lactobacillus brevis[J].ACS Omega, 2023, 8(8):8101-8109.
[22] SHI F, XIE Y L, JIANG J J, et al.Directed evolution and mutagenesis of glutamate decarboxylase from Lactobacillus brevis Lb85 to broaden the range of its activity toward a near-neutral pH[J].Enzyme and Microbial Technology, 2014, 61-62:35-43.
[23] YANG L J, ZHANG X, CHEN J, et al.Expanding the pH range of glutamate decarboxylase from L.pltarum LC84 by site-directed mutagenesis[J].Frontiers in Bioengineering and Biotechnology, 2023, 11:1160818.
[24] HUANG J, FANG H, GAI Z C, et al.Lactobacillus brevis CGMCC 1306 glutamate decarboxylase:Crystal structure and functional analysis[J].Biochemical and Biophysical Research Communications, 2018, 503(3):1703-1709.
[25] STEINEGGER M, MEIER M, MIRDITA M, et al.HH-suite3 for fast remote homology detection and deep protein annotation[J].BMC Bioinformatics, 2019, 20(1):473.
[26] GABLER F, NAM S Z, TILL S, et al.Protein sequence analysis using the MPI Bioinformatics Toolkit[J].Current Protocols in Bioinformatics, 2020, 72(1):e108.
[27] JOHN R A.Pyridoxal phosphate-dependent enzymes[J].Biochimica et Biophysica Acta (BBA) - Protein Structure and Molecular Enzymology, 1995, 1248(2):81-96.
[28] ABRAHAM M J, MURTOLA T, SCHULZ R, et al.GROMACS:High performance molecular simulations through multi-level parallelism from laptops to supercomputers[J].SoftwareX, 2015, 1-2:19-25.
[29] SCHMID N, EICHENBERGER A P, CHOUTKO A, et al.Definition and testing of the GROMOS force-field versions 54A7 and 54B7[J].European Biophysics Journal, 2011, 40(7):843-856.
[30] LU T.A comprehensive electron wavefunction analysis toolbox for chemists, Multiwfn[J].The Journal of Chemical Physics, 2024, 161(8).DOI:10.1063/5.0216272.
[31] MAIER J A, MARTINEZ C, KASAVAJHALA K, et al.Ff14SB:Improving the accuracy of protein side chain and backbone parameters from ff99SB[J].Journal of Chemical Theory and Computation, 2015, 11(8):3696-3713.
[32] OSV TH S, GRUEBELE M.Proline can have opposite effects on fast and slow protein folding phases[J].Biophysical Journal, 2003, 85(2):1215-1222.
TH S, GRUEBELE M.Proline can have opposite effects on fast and slow protein folding phases[J].Biophysical Journal, 2003, 85(2):1215-1222.
[33] YANG X W, HUO X J, TANG Y Q, et al.Integrating enzyme evolution and metabolic engineering to improve the productivity of γ-aminobutyric acid by whole-cell biosynthesis in Escherichia coli[J].Journal of Agricultural and Food Chemistry, 2023, 71(11):4656-4664.
[34] VALDÉS-TRESANCO M S, VALDÉS-TRESANCO M E, VALIENTE P A, et al.Gmx_MMPBSA:A new tool to perform end-state free energy calculations with GROMACS[J].Journal of Chemical Theory and Computation, 2021, 17(10):6281-6291.
[35] BOUYSSET C, FIORUCCI S.ProLIF:A library to encode molecular interactions as fingerprints[J].Journal of Cheminformatics, 2021, 13(1):72.
[36] YE B W, TIAN W, WANG B S, et al.CASTpFold:Computed atlas of surface topography of the universe of protein folds[J].Nucleic Acids Research, 2024, 52(W1):W194-W199.