糟鱼是我国传统发酵水产制品的典型代表,是江西、福建等地区的传统特色产品,其制作以米酒酿造产生的酒糟为关键辅料,与新鲜鱼肉共形成独特的“糟香浓郁、肉质细嫩”品质特征。该工艺融合了微生物的糖化、蛋白酶解及酯化作用,通过微生物代谢生成还原糖、游离氨基酸及挥发性风味物质,赋予了糟鱼诱人的色泽与风味[1]。然而,传统自然发酵依赖环境中的微生物群落,其生产条件简陋,存在发酵周期长、品质波动大、安全性难以保证等问题,严重制约了标准化生产与市场推广[2]。研究表明,发酵方式通过调控微生物群落结构、酶活性及代谢产物,直接影响糟鱼的品质形成。目前米酒酿造采用的方式主要有3种:糖化发酵[3]、单边发酵[4]和双边发酵[5]。3种发酵方式产生的酒糟在时序分布、微生物代谢路径及酶活性上存在显著差异,导致产品风味强度、质构特性及营养组成的显著变化。如段姿睿等[6]研究表明,酒醪发酵的酒糟草鱼在气味、色泽、滋味和质地上表现最佳。YOSHIKAWA等[7]发现将耐盐酵母接种到麦曲发酵的鱼酱醪液中,可抑制野生酵母的生长,避免对发酵鱼露风味产生不良影响。
近年来,发酵技术在食品工业中得到了广泛地应用,尤其是在传统发酵食品的现代化研究中。红米糟作为一种传统的发酵原料,具有良好的风味和价值。然而关于红米糟在不同发酵方式下对淡水鱼品质的影响的研究尚不多见。因此,本文采用高通量测序、理化分析和感官评价等方法,比较不同发酵方式(糖化发酵、单边发酵和双边发酵)制备的红米酒糟对红米糟香草鱼品质的影响。重点考察色差、质构特性、微生物群落结构、挥发性风味物质等变化规律,以期阐明不同发酵方式对红米糟香草鱼微生物生长情况的影响和对致腐微生物的抑制强度。本研究结果将为传统发酵工艺的科学化改良、品质精准调控及工业化生产提供理论依据,对推动我国传统水产发酵食品的标准化、产业化发展具有重要意义。
1 材料与方法
1.1 材料与试剂
新鲜草鱼(每条质量约1.25 kg),南昌市当地农贸市场;红米(糙米),井冈山市忆味食品有限公司;甜酒曲(仅含根霉菌),安琪酵母股份有限公司;酵母曲(含酵母菌),深圳市宝安区醇香酿贸易商行。
1.2 仪器与设备
GA2100气相色谱-离子迁移谱联用仪(gas chromatography-ion mobility spectrometry,GC-IMS),美国安捷伦科技有限公司;PEN3电子鼻,德国埃尔森斯科技公司;CM-23 d色差仪,中国柯尼卡美能达公司;TA.XT质构仪,英国Stable Micro System公司。
1.3 实验方法
1.3.1 红米醪糟的制备
清洗:准确称取100 g红米,淘米,洗净;
泡米:向红米中加入300 mL沸水,在常温下浸泡约24 h,直至米粒可以轻易碾碎,沥干水分备用;
蒸米:蒸屉蒸制1 h后,迅速摊开并不断淋洒无菌水,直至渗出的水不再烫手,沥干水分备用;
糖化发酵:称取0.200 g甜酒曲,与红米拌匀后搭窝,30 ℃发酵72 h,每隔12 h开盖换气2 min,自36 h起每隔12 h取样1次;
单边发酵:称取0.200 g甜酒曲,与红米拌匀搭窝,30 ℃发酵24 h,期间每12 h开盖换气2 min。之后再加入0.500 g酵母曲,搭窝后密封,30 ℃ 继续发酵,总发酵时长72 h,自36 h起每12 h取样1次;
双边发酵:称取0.200 g甜酒曲、0.500 g酵母曲,与红米拌匀后搭窝,在30 ℃下密封发酵72 h,自36 h起每隔12 h取样1次。
1.3.2 红米醪糟感官评价
根据段泽瑞等[8]方法稍作修改。邀请10位食品专业品鉴师对红米醪糟进行感官评价,红米醪糟整体混匀后,置于品尝盘中,对样品随机编号,室温下对样品的气味、外形、口味、口感进行打分(总分100分),评分标准如表1所示。选定糖化发酵、单边发酵、双边发酵最佳时间的红米醪糟作为辅料制备红米糟香草鱼。
表1 感官评价评分标准
Table 1 Sensory evaluation scoring criteria
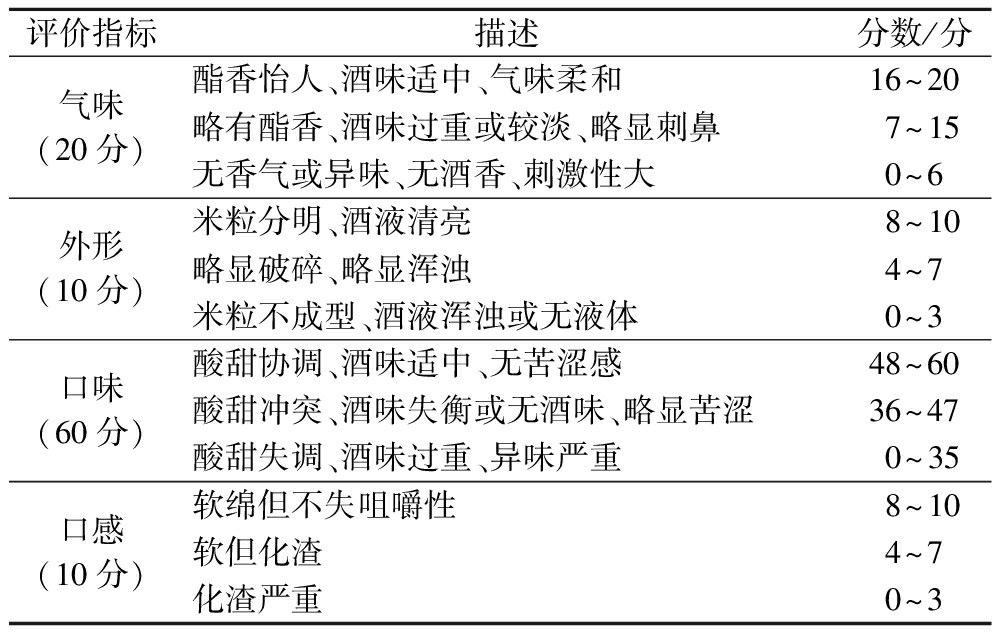
评价指标描述分数/分气味(20分)酯香怡人、酒味适中、气味柔和16~20略有酯香、酒味过重或较淡、略显刺鼻7~15无香气或异味、无酒香、刺激性大0~6外形(10分)米粒分明、酒液清亮8~10略显破碎、略显浑浊4~7米粒不成型、酒液浑浊或无液体0~3口味(60分)酸甜协调、酒味适中、无苦涩感48~60酸甜冲突、酒味失衡或无酒味、略显苦涩36~47酸甜失调、酒味过重、异味严重0~35口感(10分)软绵但不失咀嚼性8~10软但化渣4~7化渣严重0~3
1.3.3 红米糟香草鱼制备
新鲜草鱼屠宰后,将鱼肉洗净并沥干水分,取中段鱼肉,整形分割为4 cm×2 cm×1 cm鱼块。每100 g鱼肉加入300 mL质量分数5%NaCl溶液浸没,4 ℃腌制4 h后沥干,50 ℃烘干30 min后室温放凉30 min,重复3次后烘干备用。
将上述3种最佳发酵时间制备的红米醪糟分别控干水分至无液体滴落,将红米醪糟和鱼肉按质量比2∶1混匀,使用真空袋密封,其中糖化发酵组每12 h换气1次,单边发酵组及双边发酵组抽真空处理,4 ℃进行糟制3 d,每隔1 d取样1次。未经糟制为对照组,3种发酵方式糟制为实验组。
1.3.4 水分含量
根据GB 5009.3—2016《食品安全国家标准 食品中水分的测定》,测定糖化发酵、单边发酵、双边发酵对红米糟香草鱼水分的影响。
1.3.5 色差测定
使用色差计测定鱼肉的色泽变化,测定时确保色差计的镜头垂直置于样品上方,且将镜口紧贴肉样的表面,以防漏光影响实验结果,每组样品重复测试5次,记录L*、a*、b*值,其中,L*表示样品的亮度,a*表示样品的红绿度,b*表示样品的黄蓝度[9]。
1.3.6 质构特性
使用质构仪测定鱼肉的质构变化,探头型号为P/36 R,设置测试前速度2.00 mm/s,测试中速度1.00 mm/s,测试后速度1.00 mm/s,压缩深度60%,时间间隔5 s,压缩2次,每组样品测试5次。数据由计算机软件收集完成。记录以下参数结果:硬度、弹性、内聚性、胶着性、咀嚼性和回复性[10]。
1.3.7 电子鼻的测定
采用电子鼻对红米糟香草鱼的挥发性成分进行区分[11]。该设备由10条金属氧化物半导体型化学传感元件组成,每个传感元件对应的主要敏感物质如表2所示。称取5.0 g样品于15 mL离心管中,3层保鲜膜封口,恒温水浴锅40 ℃孵育20 min,冷却至室温后进行测定,测试时间150 s,气体流量400 mL/min,冲洗时间100 s。
表2 电子鼻化学传感器及其对应的敏感物质类型
Table 2 Electronic nose chemical sensors and their corresponding sensitive substance types
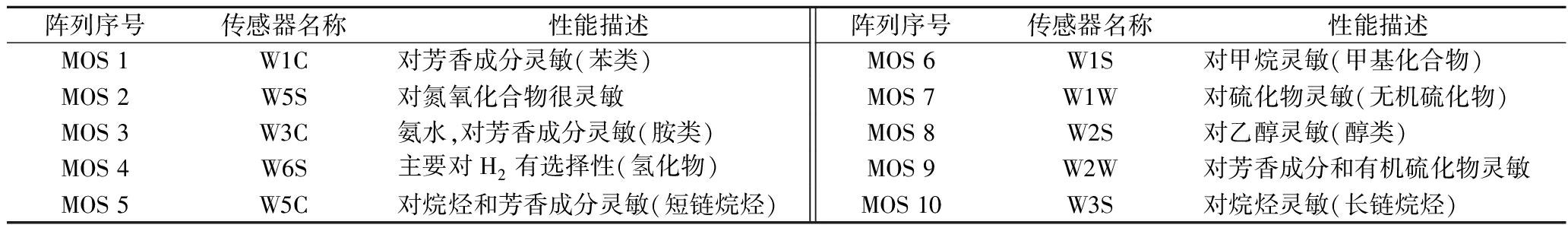
阵列序号传感器名称性能描述阵列序号传感器名称性能描述MOS 1W1C对芳香成分灵敏(苯类)MOS 6W1S对甲烷灵敏(甲基化合物)MOS 2W5S对氮氧化合物很灵敏MOS 7W1W对硫化物灵敏(无机硫化物)MOS 3W3C氨水,对芳香成分灵敏(胺类)MOS 8W2S对乙醇灵敏(醇类)MOS 4W6S主要对H2有选择性(氢化物)MOS 9W2W对芳香成分和有机硫化物灵敏MOS 5W5C对烷烃和芳香成分灵敏(短链烷烃)MOS 10W3S对烷烃灵敏(长链烷烃)
1.3.8 GC-IMS分析
采用GC-IMS进一步分析红米糟香草鱼中的挥发性化合物的特征指纹图谱。将红米糟香草鱼样品使用破壁机打碎后,精确称取2.0 g置于20 mL顶空瓶内,60 ℃孵育15 min后进样500 μL。GC-IMS采用MTX-5型极性柱(15 m×0.53 mm,1 μm),测定时柱温40 ℃,采用N2作为载气和漂移气。样品进样方式为自动进样,孵育时间15 min,孵育转速500 r/min,孵育温度60 ℃,进样针温度为65 ℃,漂移气流量150 mL/min,初始载气流量2 mL/min,并保持2 min,随后在10 min时线性提高至10 mL/min,并在25 min时提高至100 mL/min,30 min时提高至150 mL/min[12]。
1.3.9 DNA提取和PCR扩增
取样后立即使用无菌手术剪,将鱼肉剪碎为黄豆大小后装入2 mL冻存管于-80 ℃冻存,待所有样品取样完成后,按照MagBeads FastDNA Kit试剂盒的使用说明进行微生物总基因组DNA的抽提,使用质量浓度8 g/L的琼脂糖凝胶电泳检测分子大小,使用酶标仪测定DNA浓度和定量。
选用细菌16S rRNA基因中高度可变的V3~V4区用来测序,长度约为468 bp。PCR扩增选用细菌16S rRNA V3~V4区特异性引物:338F(5′-ACTCCTACGGGAGGCAGCA-3′),806R(5′-GGACTACHVGGGTWTCTAAT-3′)。PCR扩增程序如下:先在98 ℃预变性30 s使碱基暴露,随后进行25~27个循环(98 ℃变性15 s,50 ℃退火30 s结合引物,72 ℃延伸30 s复制遗传物质),然后72 ℃稳定延伸5 min,最后于4 ℃环境中保存。每个样品3个平行。扩增结果经质量浓度为20 g/L的琼脂糖凝胶电泳分离为不同分子质量的片段,根据需求切取目的片段后,用Axygen凝胶回收试剂盒回收纯化目的片段进行分析。
1.3.10 高通量测序和数据分析
回收纯化目的片段送至上海派森诺生物科技股份有限公司进行高通量测序。通过QIIME2 2019.4版本软件,按照手册标注流程对红米糟香草鱼样品的微生物组生物学信息进行分析。使用demux插件解码处理原始序列数据,cutadapt插件切除引物,随后通过DADA2插件对所得序列进行质量过滤、去噪、拼接和嵌合体去除等操作,整合为可识别序列。按100%聚类的序列相似度对获得的序列归类,生成特征性序列ASVs以及丰度数据表格。所有数据分析均在派森诺基因云平台(https://www.genescloud.cn/)上进行,分析α-多样性、β-多样性分析之间差异性。
1.4 数据处理
所有实验均重复3次以上,结果以“平均值±标准差”表示。统计分析采用SPSS 27统计软件,进行单变量方差分析,并通过Waller-Duncan检验进行事后检验分析,当P<0.05时认为有显著差异。GC-IMS分析应用软件内置NIST数据库和IMS数据库进行定性,并通过插件(Reporter和Gallery Plot)分析样品和指纹之间的差异。使用SIMCA 14.1和Origin 2022绘制相关数据图。
2 结果与讨论
2.1 红米醪糟感官评价
糖化发酵、单边发酵、双边发酵对红米醪糟品质的影响如表3所示,糖化发酵组发酵72 h时,红米醪糟整体得分最高,且气味最佳;在48、60 h口味得分反而下降,主要源于酒味与甜味的冲突,在72 h时酒味与甜味已经能较好地结合,导致口味得分反而超过了36 h时只有甜味所致的单调感;单边发酵组发酵48 h时,红米醪糟整体得分最高且气味和口感最佳,从60 h左右开始,单边发酵组的红米醪糟已逐渐难以入口;双边发酵组发酵60 h,红米醪糟整体得分最高,且气味、外形和口味最佳,但在72 h时由于酒味过重导致评分有所下降。综上所述,选定糖化发酵72 h、单边发酵48 h、双边发酵60 h的红米醪糟作为辅料来制备红米糟香草鱼。
表3 红米醪糟感官评价得分情况
Table 3 Sensory evaluation score of red rice mash
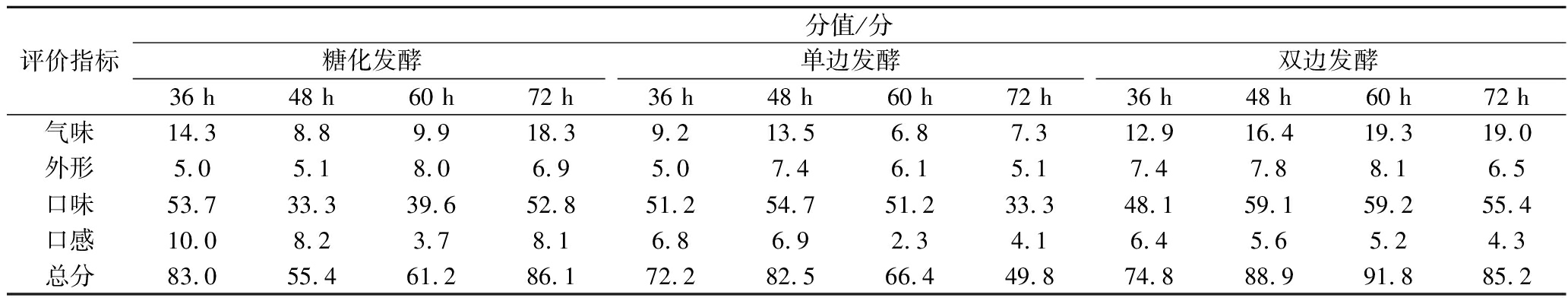
评价指标分值/分糖化发酵单边发酵双边发酵36 h48 h60 h72 h36 h48 h60 h72 h36 h48 h60 h72 h气味14.38.89.918.39.213.56.87.312.916.419.319.0外形5.05.18.06.95.07.46.15.17.47.88.16.5口味53.733.339.652.851.254.751.233.348.159.159.255.4口感10.08.23.78.16.86.92.34.16.45.65.24.3总分83.055.461.286.172.282.566.449.874.888.991.885.2
2.2 红米糟香草鱼水分含量
根据王少伟[13]的研究,糟鱼的水分含量越高,表明糟醉液进入鱼肉的量越大,同时糟鱼的硬度也越低,因而糟鱼鱼肉水分含量的变化可以间接反映糟鱼风味、质构特性的变化。如图1所示,在糟制过程中,3种发酵方式的糟鱼水分含量均有显著提高(P<0.05),整体呈现阶梯式上升。但单边发酵组水分增幅最小,且伴随硬度显著增加(图2-a),这一现象与王少伟[13]研究的普遍规律相悖,表明单边发酵可能通过微生物代谢产物(如胞外多糖)增加凝胶网络结构,从而在低水分渗透下维持鱼肉紧实度,这与段姿睿等[6]在酒糟鱼中发现片球菌属(Pediococcus)等乳酸菌产生的胞外多糖可提升持水性并优化质构的结果相一致。
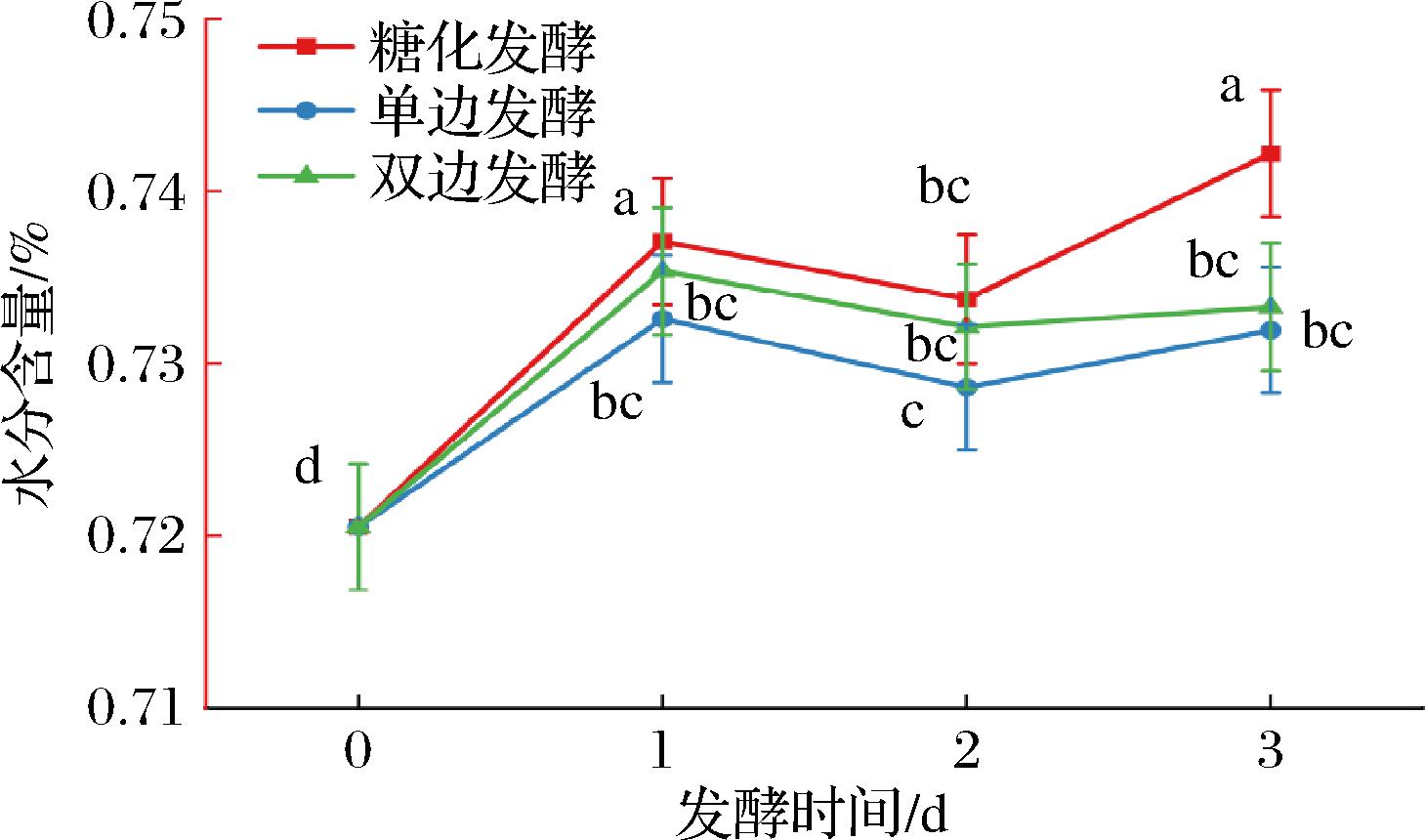
图1 不同发酵方式对红米糟香草鱼水分含量的影响
Fig.1 Influence of different fermentation methods on the moisture content of red rice lees-scented fish
注:不同小写字母表示差异显著(P<0.05)(下同)。
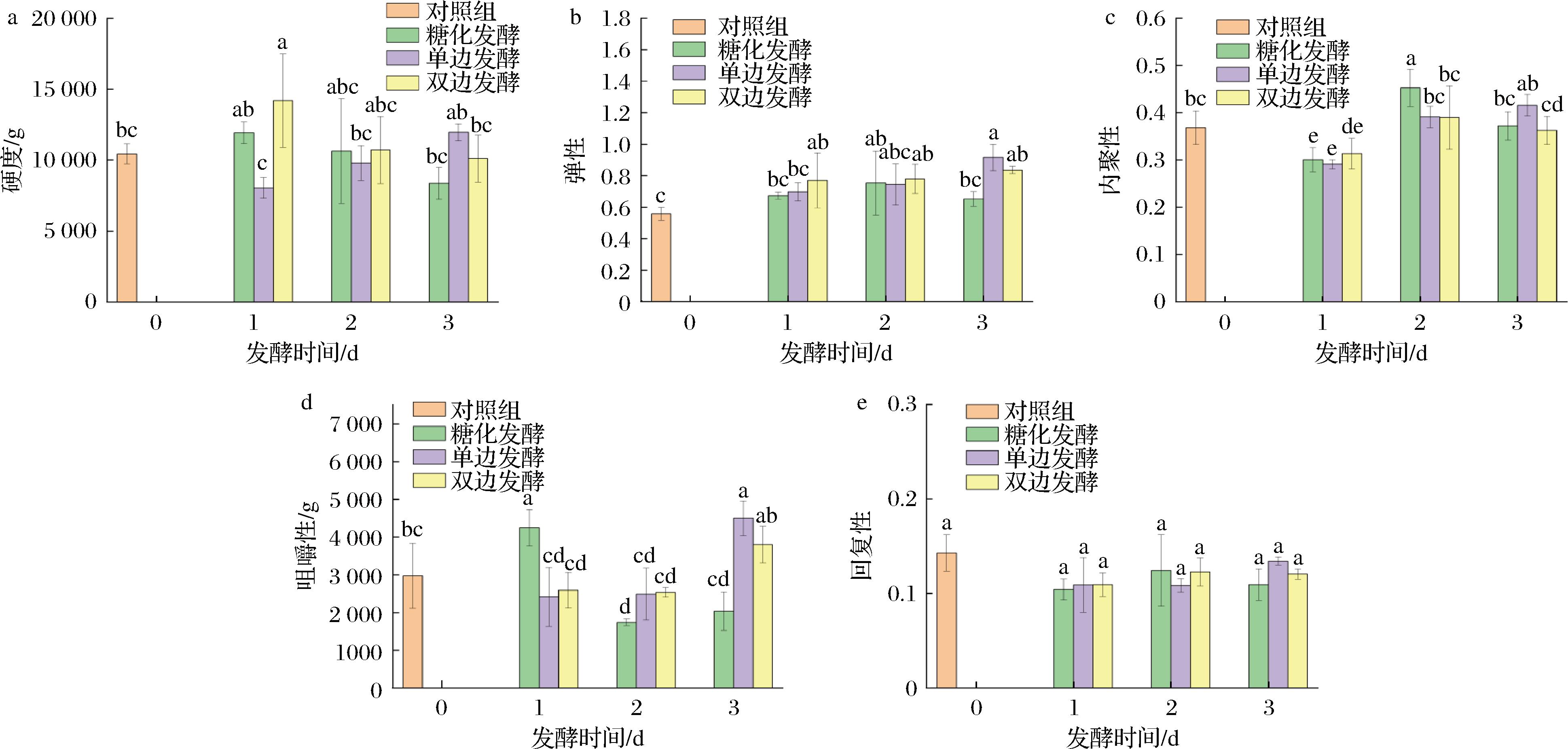
a-硬度;b-弹性;c-内聚性;d-咀嚼性;e-回复性
图2 发酵时间对红米糟香草鱼质构特性的影响
Fig.2 Influence of fermentation time on the texture characteristics of red rice lees-scented fish
2.3 红米糟香草鱼色泽
色泽是糟鱼给人的第一感官印象,糟鱼色泽的好坏会直接影响人的食欲。由表4可知,与未经糟制(对照组)相比,糟制3 d对糟鱼的亮度(L*)并没有显著影响(P>0.05),表明糟鱼中微生物产生抗氧化酶可抑制脂质氧化,避免鱼肉表面失光暗沉;单边发酵组糟制3 d后a*为-1.25±0.348,可能与单边发酵组中乳球菌属(Lactococcus,图8)含量高有关,可抑制杂菌并维持天然肌红蛋白状态,而糖化发酵组整体相对偏红(0.443±2.536)、双边发酵组整体相对偏黄绿(-0.94±0.475),单边发酵组糟制3 d后b*为7.786±1.691,同样高于糖化发酵组(6.160±1.550)和双边发酵组(5.406±1.545),可有效延缓脂肪氧化的黄变[6]。
表4 发酵时间对糟鱼色泽的影响
Table 4 Effect of fermentation time on color of rice mash carp
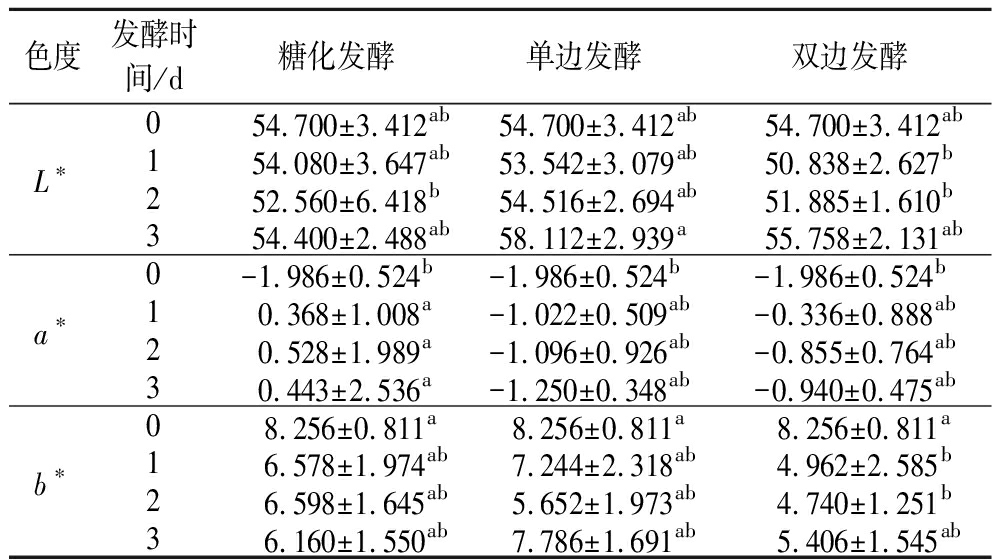
色度发酵时间/d糖化发酵单边发酵双边发酵L∗0 54.700±3.412ab 54.700±3.412ab 54.700±3.412ab154.080±3.647ab53.542±3.079ab50.838±2.627b252.560±6.418b54.516±2.694ab51.885±1.610b354.400±2.488ab58.112±2.939a55.758±2.131aba∗0-1.986±0.524b-1.986±0.524b-1.986±0.524b10.368±1.008a-1.022±0.509ab-0.336±0.888ab20.528±1.989a-1.096±0.926ab-0.855±0.764ab30.443±2.536a-1.250±0.348ab-0.940±0.475abb∗0 8.256±0.811a 8.256±0.811a 8.256±0.811a16.578±1.974ab7.244±2.318ab4.962±2.585b26.598±1.645ab5.652±1.973ab4.740±1.251b36.160±1.550ab7.786±1.691ab5.406±1.545ab
注:不同小写字母表示差异显著(P<0.05)(下同)。
2.4 红米糟香草鱼质构
由图2可知,糖化发酵组和双边发酵组红米糟香草鱼的硬度均随糟制时间延长呈现下降的趋势,但单边发酵组硬度反而上升,与此对应的是单边发酵组在糟制过程中水分含量上升幅度最小,硬度上升可能与此有关;与对照组相比,各发酵组的弹性略有升高的趋势,其中糟制至3 d时弹性升高较为显著,可能与各发酵组在糟制过程中鱼肉水分含量增加有关;糟制1 d时,各发酵组的内聚性低于对照组,这是因为当蛋白质大量水解时,肌肉纤维断裂导致鱼肉组织凝聚力下降[14]。之后各发酵组的凝聚力呈现上升的趋势,推测与鱼肉蛋白质水解导致的鱼肉持水力变化有关,当肽链少量断裂时,由于氢键增加,肌肉组织的凝胶网状结构反而得到增强;糖化发酵组的咀嚼性在糟制进程呈现下降的趋势,单边发酵组和双边发酵组的咀嚼性呈现上升的趋势,且单边发酵组糟制3 d红米糟香草鱼有最好的咀嚼性;各发酵组鱼肉的回复性要略微差于对照组,但并不具有显著性差异(P>0.05)。综上所述,3种发酵方式的红米糟香草鱼在大部分指标上未与对照组产生显著性差异,且单边发酵组在糟制3 d后,其鱼肉硬度、弹性、内聚性、咀嚼性和回复性都高于糖化发酵组和双边发酵组。
2.5 电子鼻分析
由图3-a可知,各组的PC1和PC2均解释了95%以上的变量,证明了模型的可靠性。各处理组与对照组的置信椭圆均不相交,说明各组相比对照组的风味特征均有较好的区分度,3种发酵方式都有改善红米糟香草鱼气味的能力;糖化发酵组中,糟制1~3 d的实验组虽然与对照组区分度较好,但各实验组之间并没有明显分离,说明糖化发酵的糟香草鱼各发糟制阶段气味差异不大;单边发酵组中,糟制2~3 d的实验组仅在PC2上有所分离,气味差异较小,但均与糟制1 d完全分离,而整体气味差异随时间延长并未表现出明显分离趋势,且在发酵至2 d后,整体气味开始趋于稳定;双边发酵组中,各实验组呈现随发酵时间延长气味与对照组差异变大的趋势,但各组之间置信椭圆存在小范围的相交,表明双边发酵组的气味变化过程并不剧烈。
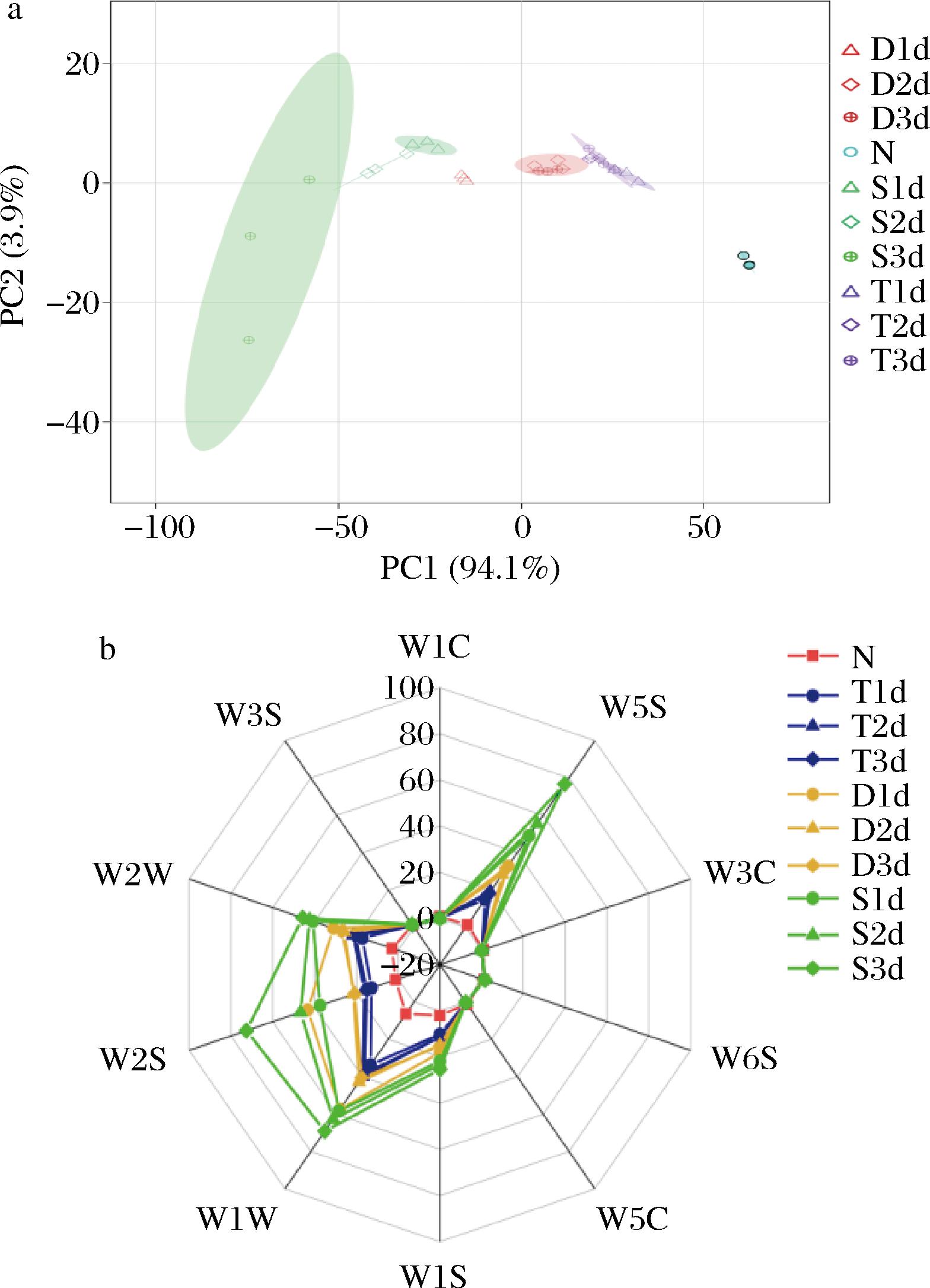
a-主成分分析图;b-电子鼻气味雷达图
图3 红米醪糟的挥发性风味特征的雷达指纹分析和主成分分析
Fig.3 Radar fingerprinting and principal component analysis of volatile flavor profiles of red rice mash
注:N表示对照组,T表示糖化发酵,D表示单边发酵,S表示双边发酵;1、2、3 d表示糟制时间(下同)。
由图3-b可知,各实验组均表现出对W1W(无机硫化物)、W2S(醇类)、W5S(氮氧化合物)、W2W(芳香族化合物和有机硫化物)、W1S(甲基化合物)的强烈反应,表明它们可以代表各组红米醪糟的气味特征。其中双边发酵组在各传感器的响应值均最高,说明双边发酵组的挥发性气味物质可能最为丰富,糖化发酵组的响应值相对最低,但也表现出与对照组的明显差异。值得注意的是双边发酵组各糟制时间在W2S传感器(醇类)的响应值明显高于其他实验组,且随时间延长响应值大幅增加,可能来源于酵母菌旺盛的无氧发酵,导致鱼肉酒味增加明显。单边发酵组在糟制1 d时也出现了对W2S传感器(醇类)的高响应值,但随后消失;糖化发酵组中,各实验组别差异不大。
2.6 基于GC-IMS的红米糟香草鱼香气特征分析
为准确判别3种红米醪糟所制备的红米糟香草鱼气味特征,使用GC-IMS测定其挥发性气味化合物并做定性分析,如电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.043759,下同)所示,从各糟香草鱼样品中共检测到52种香气化合物(包括单体和二聚体)其中包括12种醇、3种醛、6种酮、15种酸、8种酯和8种其他化合物,其中共有4种芳香族化合物。
由图4-a可知,GC-IMS有效分离了挥发性风味化合物。由图4-b可知,其3种发酵方式的实验组的红色区域明显较蓝色区域(对照组)多且颜色更深[15],表明糟制后的草鱼香气化合物浓度增加,与对照组差异较大,这说明糟制可以有效改善糟香草鱼的香气。3种发酵方式的实验组共有的化合物主要为短、中链醛酮及酯类化合物,大多具有令人愉悦的气味,其含量随时间延长变化幅度不大。按照风味化合物浓度变化趋势将指纹图谱划分为4个区域:对于1-辛烯-3-醇、二甲基三硫等产生腥味的主要物质[16]仅在对照组检出(A区),表明3种发酵方式糟制可以起到消减鱼肉腥味的作用;糖化发酵组的特征香气化 合物主要集中于B区,正丁酸、3-甲基-2-戊酮、环戊酮、2-庚醇4种化合物是糖化发酵组的特征化合物,其中高浓度正丁酸呈现腐臭酸味[17];C区为双边发酵组的特征香气化合物,为2-己醇、乙基二硫醚、对甲苯酚、一缩二乙二醇单丁醚4种化合物,其含量随时间变化延长幅度不大,且乙基二硫醚呈现硫磺、腐蛋臭,一缩二乙二醇单丁醚有微弱的溶剂味[18];D区有2-甲基-2-戊烯醛、2-己醇、乙酸正戊酯等化合物,呈现为青草味、果香味[19],且在单边发酵组中有明显的随发酵时间延长含量增加的趋势,表明单边发酵能够有效促进风味物质的生产。
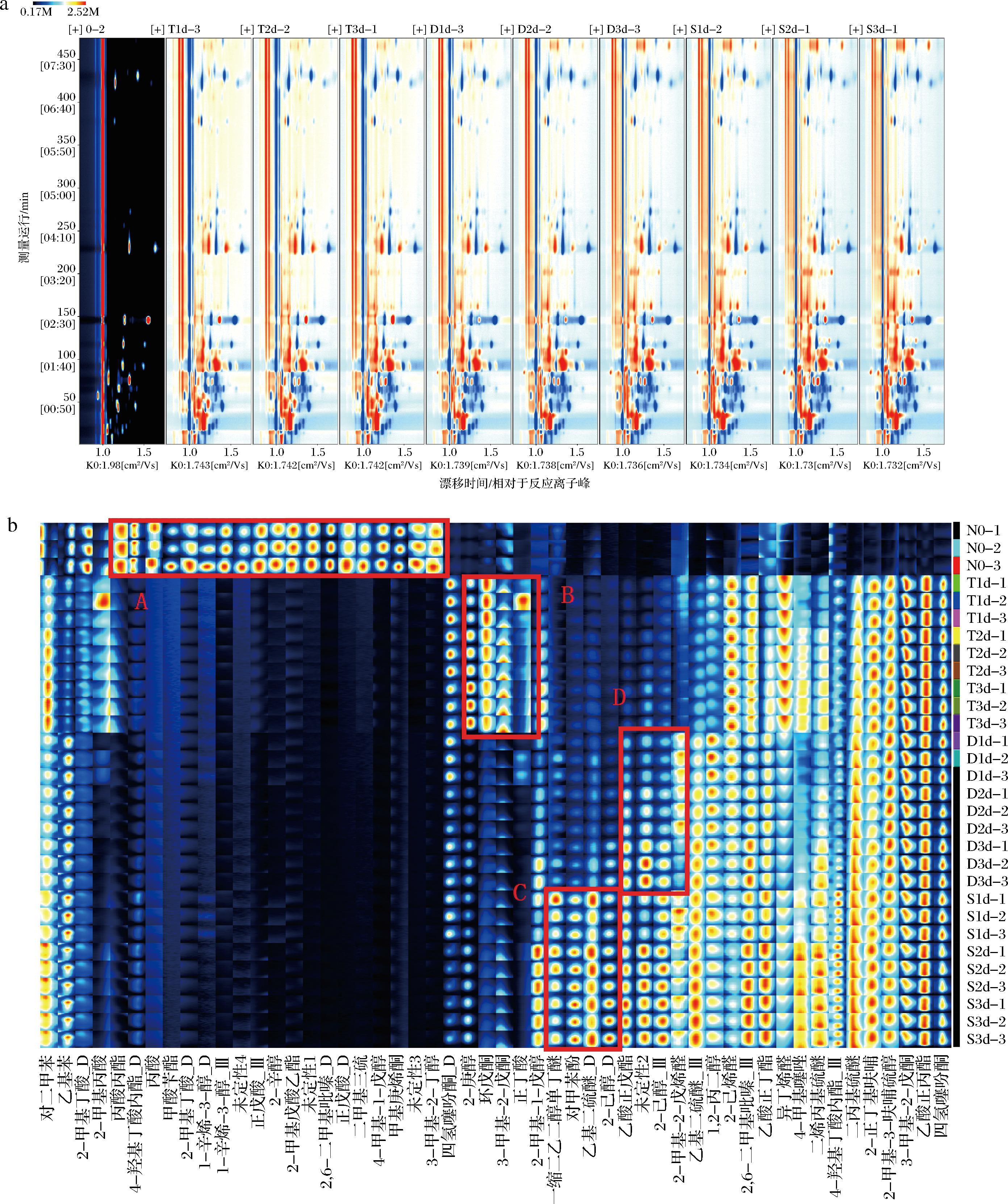
a-二维图谱;b-指纹图谱
图4 不同发酵组的GC-IMS的挥发性化合物分析
Fig.4 Volatile compound analysis of GC-IMS in different fermentation groups
2.7 红米糟香草鱼物种组成分析
操作分类单元(operational taxonomic unit,OTU)分析通过人为设置统一标志区分指定分类单元,来了解样本在种、属水平的微生物丰度信息[20]。OTU是指将测序得到的序列结果按照相似性分组,比对相应的物种数据库后,从而得到样本中微生物的分类学信息和丰度信息。Rank-abundance曲线可以协助分析样品中物种的丰富度和分布均匀性,若曲线平滑下降,表明样本的物种群落组成均匀度较高,快速陡然下降则表明物种群落组成均匀度较低。由图5可知,各实验组的Rank-abundance曲线均呈现快速下降的趋势,表明在糟制过程中各实验组的优势菌均能够抑制其他菌落的生长,其中糖化发酵组的物种丰度最高,说明其优势菌群对其他菌属的抑制效果最弱;双边发酵组的下降趋势最为快速,物种丰度最低;而单边发酵组物种丰度次之,可以确认单边发酵组和双边发酵组主要菌群建立优势地位的用时更短,发酵过程更为稳定。
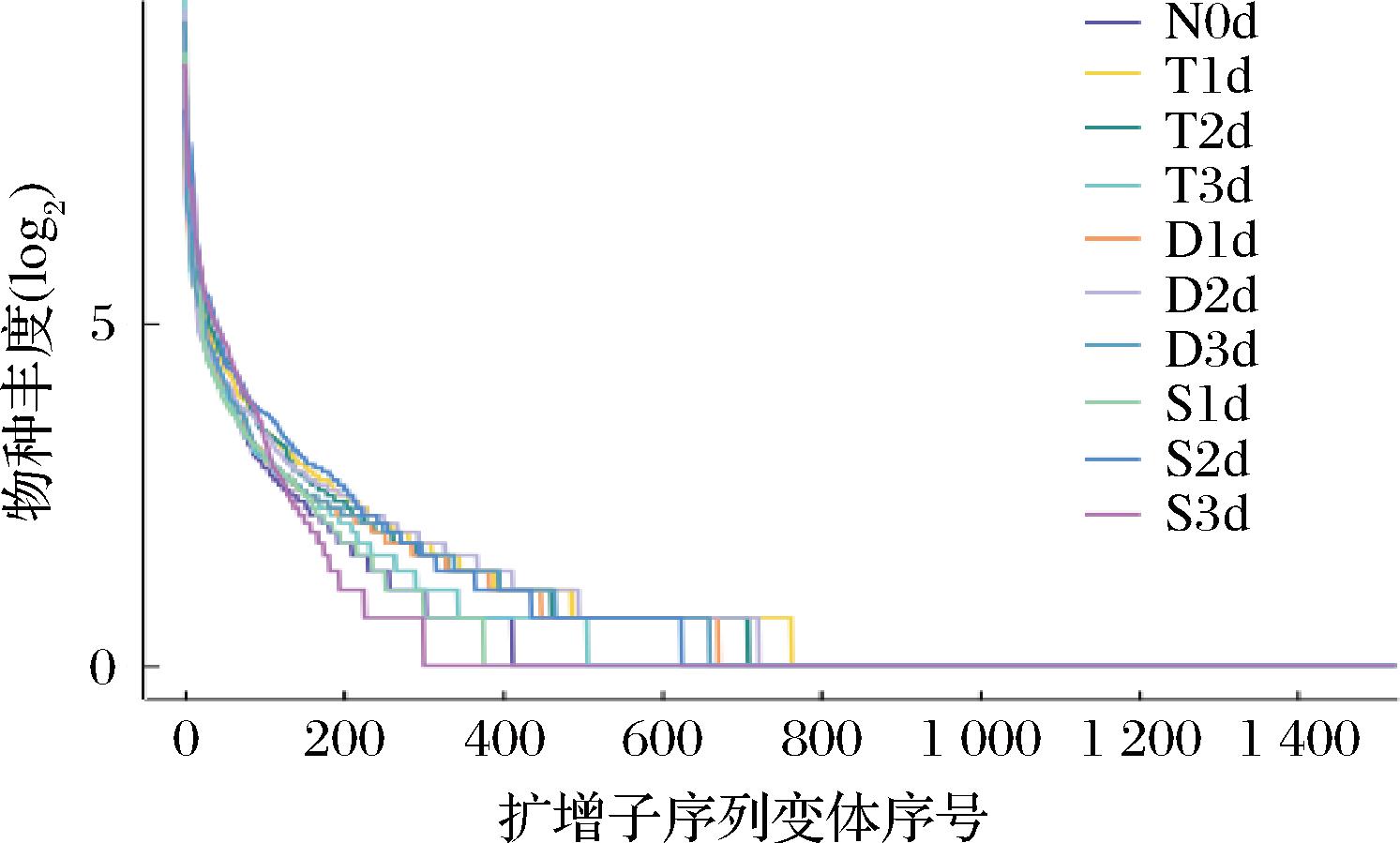
图5 不同红米糟香草鱼样品的丰度曲线
Fig.5 Abundance curves of different red rice residue fragrant grass carp samples
通过Pan/Core物种曲线可以分析物种总量和核心物种量随样本数量增加的变化情况,并以此进一步评估取样环境中的物种丰富程度。其中Pan曲线是所有样本包含的物种总和,物种丰富程度越高时Pan曲线上扬幅度越为明显;Core曲线反映的是所有样本中共有物种的数目,也即核心物种。由电子版增强出版附图1可知,随着样本数目增加,Pan/Core物种曲线略显陡峭,但最终逐渐趋于平缓,表明测序的样本量能够满足分析要求,上述结论成立。
2.8 α-多样性分析
α-多样性指标主要从丰富度、多样性等方面对一个生态环境内的物种多样性情况进行分析,利用Chao1和Observed species指数表征物种丰富度,Shannon指数表征物种多样性,Good’s coverage指数表征采样深度对完整生境全部物种的覆盖率指标。表5为各实验组在糟制期间的α-多样性指数,可以看出所有样品的覆盖率都达到了99%,表明测序结果具有一定的可信度,在物种丰富度上,3种发酵方式实验组的Chao1、Observed_species指数均高于对照组,但都随着糟制时间延长呈现下降的趋势,单边发酵组下降较为缓慢,物种丰富度依然保持较高位置;在物种多样性上,与对照组相比,3种发酵方式实验组的Shannon指数无显著差异(P>0.05),但单边发酵组在糟制进程中,Shannon指数缓慢增加,表明单边发酵组红米糟香草鱼的优势菌群在不断扩大自身优势,挤压其他微生物的生存空间,对其他微生物的繁殖起到了抑制作用。
表5 红米糟香草鱼样品的α-多样性指数
Table 5 α-Diversity index of red rice lees-scented grass carp samples
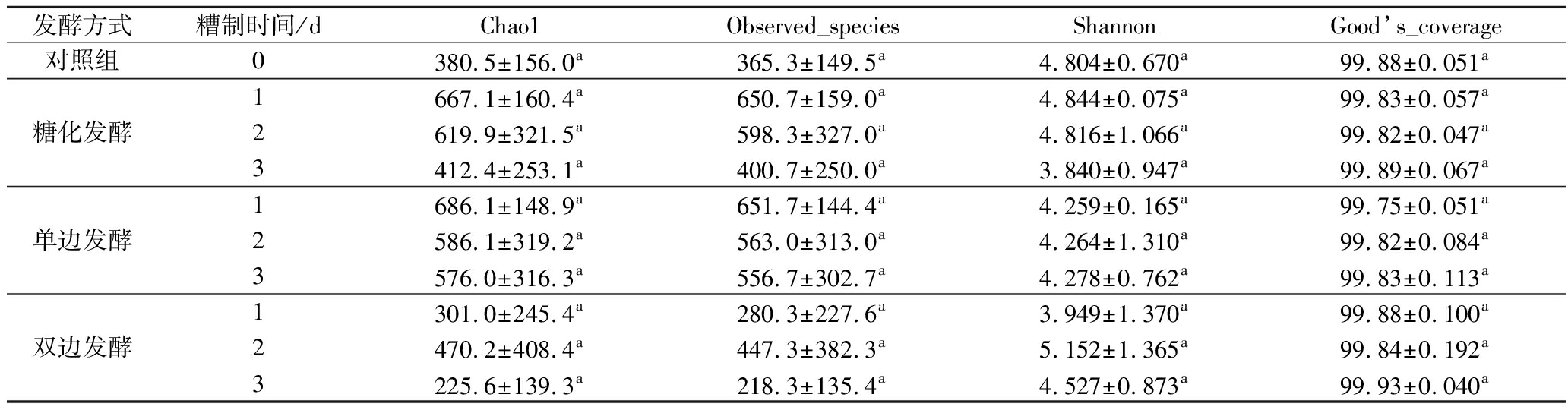
发酵方式糟制时间/dChao1Observed_speciesShannonGood’s_coverage对照组0380.5±156.0a365.3±149.5a4.804±0.670a99.88±0.051a糖化发酵1667.1±160.4a650.7±159.0a4.844±0.075a99.83±0.057a2619.9±321.5a598.3±327.0a4.816±1.066a99.82±0.047a3412.4±253.1a400.7±250.0a3.840±0.947a99.89±0.067a单边发酵1686.1±148.9a651.7±144.4a4.259±0.165a99.75±0.051a2586.1±319.2a563.0±313.0a4.264±1.310a99.82±0.084a3576.0±316.3a556.7±302.7a4.278±0.762a99.83±0.113a双边发酵1301.0±245.4a280.3±227.6a3.949±1.370a99.88±0.100a2470.2±408.4a447.3±382.3a5.152±1.365a99.84±0.192a3225.6±139.3a218.3±135.4a4.527±0.873a99.93±0.040a
2.9 群落组成分析
图6反映的是3种发酵方式红米糟香草鱼在门水平上不同样品的微生物组成情况,糟鱼肉中厚壁菌门(Firmicutes)、变形菌门(Proteobacteria)和放线菌门(Actinobacteriota)是最主要的门水平微生物种类,其中厚壁菌门在各阶段所占的比例均为最高,最低也达到了47%,但随着糟制时间延长,厚壁菌门的丰富度有所下降,而变形菌门、放线菌门及拟杆菌门(Bacteroidota)则开始逐渐占据更多的优势。值得注意的是,单边发酵组糟制的红米糟香草鱼门水平微生物变化规律与其他2组并不相同,其厚壁菌门细菌始终占有较大的比例,且变形菌门所占比例表现为先上升后下降而非持续上升,放线菌门则始终受到抑制。
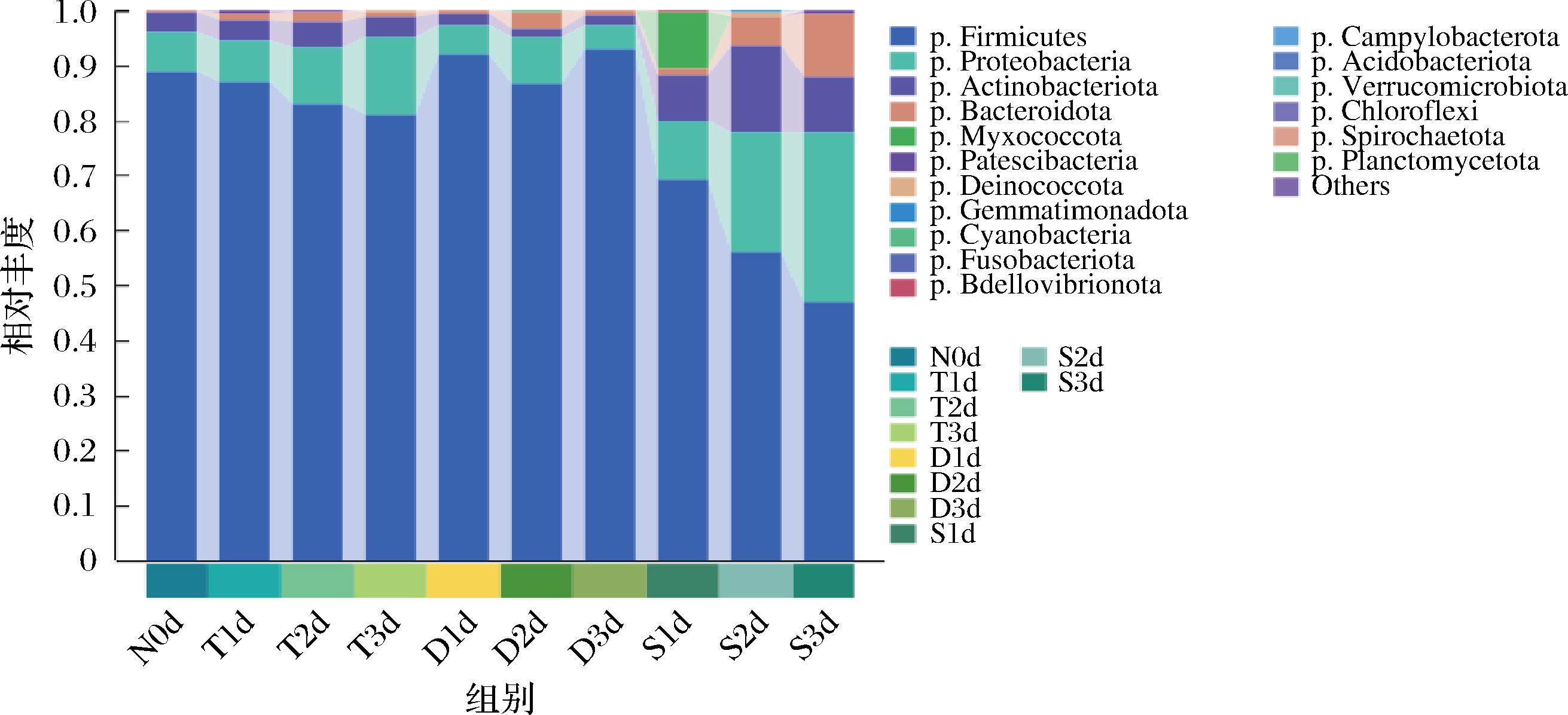
图6 红米糟香草鱼样品基于门水平的物种组成
Fig.6 Species composition of red rice lees-scented grass carp samples based on phylum level
图7反映的是3种发酵方式红米糟香草鱼在属水平上不同样品的微生物组成情况。糖化发酵组在糟制初期的明串珠菌属(Leuconostoc)、乳球菌属(Lactococcus)、葡萄球菌属(Staphylococcus)占比较高,但在糟制至3 d时葡萄球菌属占比大幅下降,相应的明串珠菌属占比大幅提高,可能是因为明串珠菌属和乳球菌属都能进行乳酸发酵产酸,较为适应发酵后期的酸性环境,同时乳球菌属还能产生乳酸菌素抑制其他原核生物生长。单边发酵组的微生物群落较为稳定,分别是片球菌属(Pediococcus)、乳球菌属(Lactococcus)、葡萄球菌属(Staphylococcus)占据前三,且所占比例最大,这3种菌属都具有较好的制造风味物质或风味前体物质的能力,这一结果与单边发酵组的红米糟香草鱼在GC-IMS结果中挥发性香气化合物含量相对最高、比例最稳定(图4)相符。双边发酵组的微生物菌落组成较为复杂,相对丰度较高的有葡萄球菌属、片球菌属、嗜冷杆菌属(Psychrobacter)、链球菌属(Streptococcus)等,在糟制初期为葡萄球菌属、片球菌属丰度较高,随后被嗜冷杆菌属、链球菌属和金黄杆菌属(Chryseobacterium)取代,值得注意的是在糟制3 d后,嗜冷杆菌属和金黄杆菌属丰度大幅上升,而这2种菌属均是腐败菌[21],这可能意味着双边发酵组糟制1 d后鱼肉品质正在急剧下降。
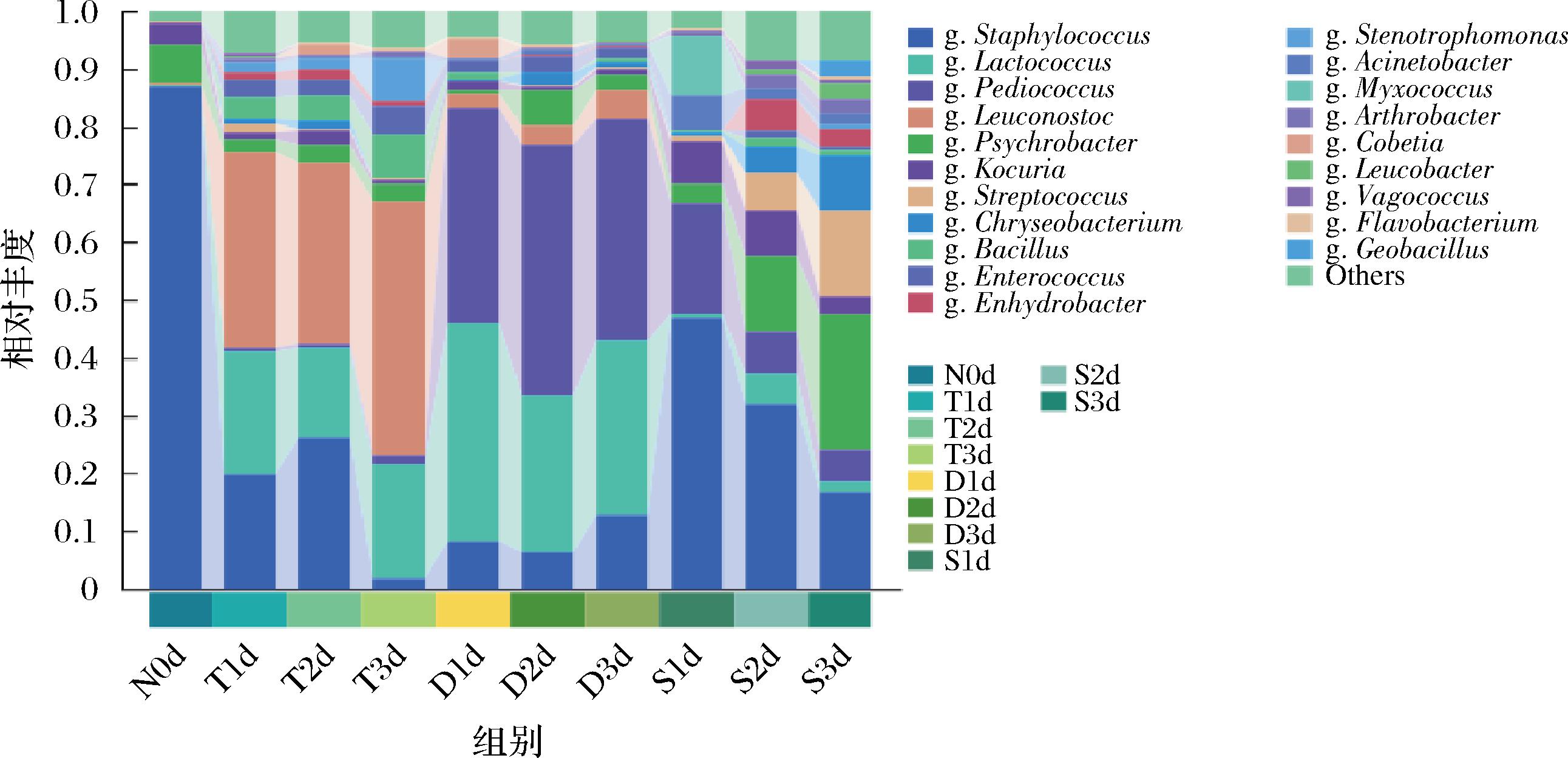
图7 红米糟香草鱼样品基于属水平的物种组成
Fig.7 Species composition of red rice lees-scented grass carp samples based on genus level
2.10 β-多样性分析
β-多样性是指分析不同组别间微生物群落组成差异性的方法,目前研究者们多采用层次聚类的方法进行β-多样性聚类分析,样本间的相似度以等级树的形式展示,并通过聚类树的分枝长短直观地展示出各样本之间物种组成的差异程度,从而衡量聚类效果的好坏。3种发酵方式的红米糟香草鱼样品在属水平上的层级聚类树如图8所示,可以发现双边发酵组与对照组在微生物组成上最为接近,其次为糖化发酵组,而在同一组中,糖化发酵和双边发酵都是随着糟制时间延长,微生物组成差异逐渐变大。但单边发酵组的微生物组成差异相对较小,说明单边发酵组能够更早达成微生物菌群的稳定,与图8结果相吻合。层级聚类结果表明,单边发酵组能够更早达成微生物菌群的稳定,且与对照组差异最大。
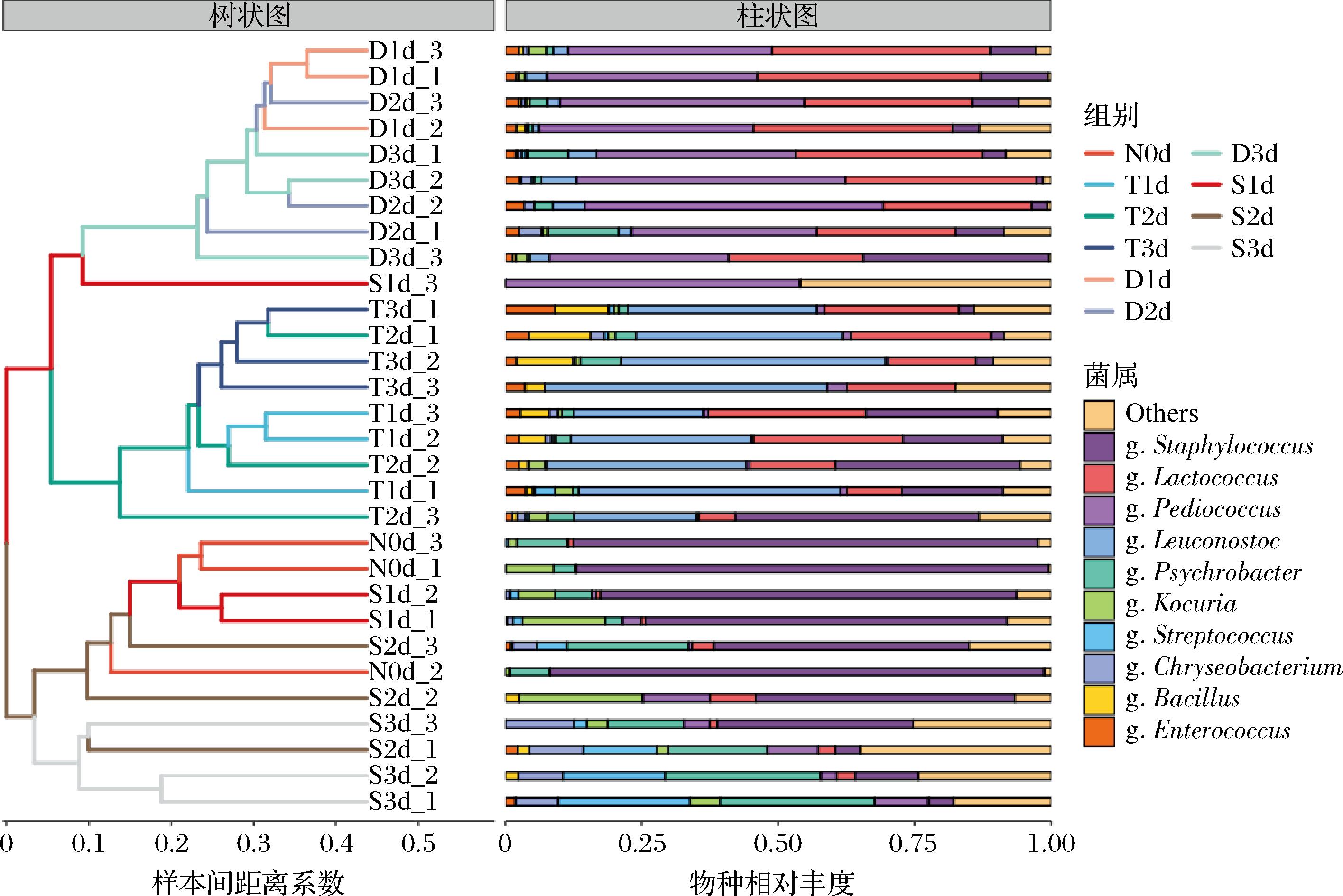
图8 红米糟草鱼样品间基于属水平的层级聚类树
Fig.8 Hierarchical clustering tree based on genus level among red rice lees-scented grass carp samples
3 结论
本文以草鱼肉为研究对象,筛选出糖化发酵72 h、单边发酵48 h、双边发酵60 h的最佳的红米醪糟,并在4 ℃下对草鱼肉糟制3 d制备红米糟香草鱼,探究不同发酵工艺糟制的红米糟香草鱼品质风味上的差异,并分析微生物与风味的关联。结果显示:糟制进程中红米糟香草鱼的水分含量增加,但色泽和质构无显著性差异。在气味化合物方面,3种发酵方式都有改善红米糟香草鱼气味的能力,单边发酵组的鱼肉含有2-甲基-2-戊烯醛、2-己醇、乙酸正戊酯等化合物,呈现青草味、果香味;而糖化发酵组和双边发酵组则含有正丁酸、乙基二硫醚、一缩二乙二醇单丁醚等物质,呈现腐臭酸味、硫磺等令人不悦的气味。在微生物多样性分析中,α-多样性分析结果显示,单边发酵组所含微生物群落中,厚壁菌门在发酵全期的占比很高,其中优势细菌为片球菌属、乳球菌属、葡萄球菌属等具有风味改善能力的菌属。而糖化发酵组随着糟制时间的延长,明串珠菌属大幅度上升,抑制了葡萄球菌属;双边发酵组却会产生嗜冷杆菌属和金黄杆菌属等致腐微生物,导致鱼肉品质下降。β-多样性分析结果显示,双边发酵组与对照组在微生物组成上最为接近,其次为糖化发酵组;另外在同一组中,糖化发酵和双边发酵均随着糟制时间的延长,微生物组成差异逐渐变大。但单边发酵组的微生物组成与其他实验组差异较大,而组内差异则较小,说明单边发酵组能够更早达成微生物菌群的稳定。综上所述,单边发酵是更适合红米糟香草鱼的制备方式,具有较高的应用潜力。未来的研究可以进一步优化单边发酵的工艺参数,以提高其工业化应用的可行性。
[1] 夏文水. 肉制品加工原理与技术[M].北京:化学工业出版社, 2003.XIA W S.Principles and Techniques of Meat Product Processing [M].Beijing:Chemical Industry Press, 2003.
[2] 杨锡洪, 吴海燕, 解万翠, 等.传统咸鱼风味快速形成技术[J].现代食品科技, 2009, 25(11):1295-1298.YANG X H, WU H Y, XIE W C, et al.Quickly formation of flavor in traditional cured fish[J].Modern Food Science and Technology, 2009, 25(11):1295-1298.
[3] 郑伟, 薛江林, 张炼, 等.不同糖化发酵剂酿造复合香型白酒工艺研究[J].食品与发酵工业, 2022, 48(21):61-66.ZHENG W, XUE J L, ZHANG L, et al.Fermentation process for composite aromatic Baijiu with different saccharification agents[J].Food and Fermentation Industries, 2022, 48(21):61-66.
[4] 张旭. 不同谷物曲发酵燕麦黄米醪糟工艺优化及品质评价[D].呼和浩特:内蒙古农业大学, 2023.ZHANG X.Process optimization and quality evaluation of oat millet laozao fermented with different grain koji[D].Hohhot:Inner Mongolia Agricultural University, 2023.
[5] 高银涛, 何璇, 余博文, 等.白酒固态双边发酵糖化机理及其对发酵过程的影响[J].食品与发酵工业, 2021, 47(13):92-97.GAO Y T, HE X, YU B W, et al.Saccharification mechanism of solid-state fermentation of Chinese Baijiu and its influence on fermentation process[J].Food and Fermentation Industries, 2021, 47(13):92-97.
[6] 段姿睿, 杨絮, 陈小娥, 等.酒糟草鱼发酵过程中微生物菌群组成与挥发性风味物质及其相关性分析[J].食品科学, 2025, 46(14):111-123.DUAN Z R, YANG X, CHEN X E, et al.Microbial community composition and volatile flavor substances in fermented grass carp with rice wine lees during fermentation and correlation between them[J].Food Science, 2025, 46(14):111-123.
[7] YOSHIKAWA S, YASOKAWA D, NAGASHIMA K, et al.Microbiota during fermentation of chum salmon (Oncorhynchus keta) sauce mash inoculated with halotolerant microbial starters:Analyses using the plate count method and PCR-denaturing gradient gel electrophoresis (DGGE)[J].Food Microbiology, 2010, 27(4):509-514.
[8] 段泽瑞, 田梅兰, 刘杨柳, 等.食盐添加量对虾酱理化性质和细菌多样性的影响[J].食品科学, 2024, 45(15):85-93.DUAN Z R, TIAN M L, LIU Y L, et al.Effect of salt concentration on physicochemical properties and bacterial diversity of shrimp paste[J].Food Science, 2024, 45(15):85-93.
[9] CHAIJAN M, PANPIPAT W, BENJAKUL S.Physicochemical properties and gel-forming ability of surimi from three species of mackerel caught in Southern Thailand[J].Food Chemistry, 2010, 121(1):85-92.
[10] 尹红梅, 陈浩然, 尹紫冉, 等.传统发酵和接种发酵霉鱼的品质比较分析[J].食品工业科技, 2024, 45(15):56-65.YIN H M, CHEN H R, YIN Z R, et al.Comparison of volatile flavor compounds and qualities between traditional fermented and inoculated fermented of Mei Yu[J].Science and Technology of Food Industry, 2024, 45(15):56-65.
[11] HUANG M Z, LI T T, HARDIE W J, et al.Comparative characterization and sensory significance of volatile compounds in Rosa roxburghii Tratt fruit from five geographic locations in Guizhou, China[J].Flavour and Fragrance Journal, 2022, 37(3):163-180.
[12] 沙小梅, 蒋文丽, 李鑫, 等.不同烹饪方式小龙虾的风味特征分析[J].食品与发酵工业, 2023, 49(13):288-296.SHA X M, JIANG W L, LI X, et al.Analysis of flavor characteristics of Procambarus clarkia in different cooking methods[J].Food and Fermentation Industries, 2023, 49(13):288-296.
[13] 王少伟. 酒糟鱼加工技术研究[D].无锡:江南大学, 2012.WANG S W.The processing technology of wine-lees fish[D].Wuxi:Jiangnan University, 2012.
[14] 李本相, 卫育良, 梁萌青, 等.水解鱼蛋白对大菱鲆生长、体组成及肌纤维组织形态结构的影响[J].渔业科学进展, 2019, 40(5):155-165.LI B X, WEI Y L, LIANG M Q, et al.The effects of fish protein hydrolysate on the growth, body composition and morphological structure of muscle fiber of turbot(Scophthalmus maximus L.)[J].Progress in Fishery Sciences, 2019, 40(5):155-165.
[15] 王依文, 田瑶瑶, 张克粉, 等.不同季节及层级浓香型白酒窖泥微生物群落多样性与风味物质的比较及相关性分析[J].食品科学, 2025, 46(4):100-109.WANG Y W, TIAN Y Y, ZHANG K F, et al.Comparison and correlation analysis of microbial community diversity and flavor compounds in different layers of pit mud for Luzhou-flavor Baijiu in different seasons[J].Food Science, 2025, 46(4):100-109.
[16] ZHANG Z C, WANG J, DONG M, et al.Integration of untargeted lipidomics and targeted metabolomics revealed the mechanism of flavor formation in lightly cured sea bass driven via salt[J].Food Chemistry, 2025, 470:142675.
[17] ZHAO X, CHEN J, LI H, et al.Integration of volatilomics and microbiome diversity reveals key flavor-related metabolic pathways in semi-dried large yellow croaker (Pseudosciaena crocea)[J].Food Chemistry, 2025, 470:142518.
[18] 桂倩, 苟帮超, 樊敏.鱼腥味的化学成分、形成机理与去腥方法[J].化学教育(中英文), 2024, 45(20):10-15.GUI Q, GOU B C, FAN M.Chemical composition, formation mechanism and removal methods of fishy odor[J].Chinese Journal of Chemical Education, 2024, 45(20):10-15.
[19] TANG M, LIU X P, YU Y, et al.Deodorization mechanism of the main aroma compounds on the fishy odor in boiled fish during heating[J].Food Chemistry, 2025, 465:142179.
[20] ANUKAM K.Effects of ampicillin on the gut microbiome of an adult male as determined by 16S rRNA V4 metagenomics sequencing and greengenes bioinformatics suite[J].Journal of Advances in Microbiology, 2018, 7(4):1-18.
[21] 毛俊龙, 祁雪儿, 张宾, 等.基于高通量测序的大黄鱼表面微生物群落组成及变化分析[J].现代食品科技, 2020, 36(12):27-35;167.MAO J L, QI X E, ZHANG B, et al.Analysis microbial community on the surface of large yellow croaker(Larimichthys crocea) based on high-throughput sequencing[J].Modern Food Science and Technology, 2020, 36(12):27-35;167.