沙丁鱼油是多不饱和脂肪酸的重要来源,富含维生素A、维生素D等,研究显示鱼肝油中的ω-3系列脂肪酸具有提高免疫力、预防和治疗心脑血管疾病的功效。其中二十二碳六烯酸除有以上功效外,还具有促进婴幼儿智力发育、抗衰老等作用[1]。但有研究表明富含不饱和脂肪酸的油脂极易在加工、贮藏和食用过程中发生自动氧化、光敏氧化或酶促氧化作用,产生脂质氧化产物,其中以自由基引发的自动氧化为主要途径[2]。所产生的氧化产物不仅对色泽、风味和质地等食品感官品质造成不良影响,且会产生对人体有害的氧化产物,因此食品脂质氧化的安全问题备受关注。
此外,脂质氧化产物也会引起消化系统紊乱[3]。食品中的氧化脂肪酸可被肠道吸收并与脂蛋白结合,并加剧氧化应激和动脉粥样硬化[3-4]。SONG等[5]研究发现氧化鱼油显著增加了鱼肝脏中的丙二醛(malondialdehyde,MDA)含量,氧化应激水平升高影响脂肪代谢。GAO等[6]研究表明,喂养氧化鱼油降低了鱼的生长性能,增加了MDA含量并激活了免疫缺陷和TOLL信号通路传导。
果蝇作为遗传学、衰老和氧化应激研究的理想模型,具有遗传背景清晰、肠道微生物组成简单且实验便于操作等优势[7-8]。本研究通过建立沙丁鱼油氧化程度与果蝇生理损伤的对应模型,分析沙丁鱼油在80 ℃时发生氧化后的品质变化,并建立新鲜和氧化前、中、后期不同氧化程度,以黑腹果蝇为研究对象,在培养基中添加不同氧化程度的沙丁鱼油,研究产生的相关多不饱和脂肪酸和其他有害物质对果蝇寿命、攀爬和繁殖等影响。以期为评估氧化油脂安全问题提供相关依据,为氧化脂质对衰老及生理过程的影响及其安全摄入提供理论依据。
1 材料与方法
1.1 材料与试剂
新鲜沙丁鱼油,浙江兴业集团有限公司;FWA00022 nubbin黑腹果蝇,北大华东院启东芳景生物科技有限公司。
三氯甲烷、KI、硫代硫酸钠标准滴定溶液、可溶性淀粉、NaOH、三氯乙酸、乙二胺四乙酸二钠、KBr、三氟化硼、甲醇等(分析纯),国药集团化学试剂有限公司;冰乙酸、硫代巴比妥酸(分析级),上海阿拉丁生化科技股份有限公司。
1.2 仪器与设备
TU-1810型紫外可见分光光度计,北京普析通用仪器有限责任公司;THZ-100型恒温培养摇床、HWS-12型电热恒温水浴锅,上海一恒科学仪器有限公司;Nicolet Is50型傅里叶红外光谱(Fourier transform infrared spectroscopy,FTIR)仪,美国Thermo Fisher Scientific公司;7890A型气相色谱仪,美国Agilent公司。
1.3 实验方法
1.3.1 样品处理
将沙丁鱼油用50 mL离心管进行分装,并在-80 ℃冷冻备用,将鱼油(30±1) g分别放入玻璃培养皿中,烘箱80 ℃氧化10 d。
1.3.2 指标测定
取新鲜鱼油和氧化鱼油测定过氧化值(peroxide value,POV)、酸价(acid value,AV)、MDA、FTIR、脂肪酸。每天取样测定,每个样品进行6次平行。
POV测定参照GB 5009.227—2023《食品安全国家标准 食品中过氧化值的测定》。AV测定参照GB 5009.229—2025《食品安全国家标准 食品中酸价的测定》。MDA测定参照GB 5009.181—2016《食品安全国家标准 食品中丙二醛的测定》。脂肪酸含量测定参照GB 5009.168—2016《食品安全国家标准 食品中脂肪酸的测定》。
FTIR的测定参照宁海花等[9]的方法,采用FTIR采集油样的红外谱图,其扫描波数范围为500~4 000 cm-1,扫描次数3次,分辨率4 cm-1。以空气参比作为空白背景,用滴管滴加油样,使其充满整个KBr晶体表面。每次样品测试结束后,用无水乙醇清洗干净。
1.3.3 果蝇培养基配制
对照组培养基(g/L):将蔗糖31.62、葡萄糖63.24、CaCl2 0.726、琼脂粉10.6、酵母粉32.19、玉米粉77.7,加热至沸腾10 min,并且不断搅拌,防止培养基结块;加入2 g山梨酸钾和15 mL尼可净溶液,搅拌混匀;在冷却凝固前,分装到包装盒中。4 ℃保存1周。
实验组培养基(添加不同氧化程度的沙丁鱼油):将固体培养基加热,称取一定质量的培养基加热,将加热后的培养基冷却至50~55 ℃左右后,分别添加含量为质量分数0.5%不同氧化程度[新鲜、前期(氧化第5天)、中期(氧化第7天)、后期(氧化第10天]的AV含量分别为(0.58±0.04)、(10.08±0.08)、(15.62±0.86)、(31.25±0.97) mg/g的沙丁鱼油,混匀,用3 mL胶头滴管加入到培养管中。现配现用,每3 d更换1次培养基。
1.3.4 果蝇实验分组
选取羽化24 h内的果蝇,通过使用CO2进行麻醉并区分雌雄,分别置于不同培养基中饲养,保持环境温度在(21±2) ℃,湿度在(60±5)%,每天8:00~20:00正常光照,每3 d更换1次培养基。
根据SC/T 3502—2016《鱼油》规定,沙丁鱼油氧化10 d中,AV分别超过鱼油一级(≤8 mg/g)、二级(≤15 mg/g)和三级鲜度(≤30 mg/g),对鱼油限定标准更加明确,因此选择AV作为区分不同沙丁鱼油氧化程度模型的依据,并进行后续添加不同氧化程度沙丁鱼油对果蝇理化指标影响实验。
将收集到的雌果蝇随机分为5组。C:空白对照组;F:新鲜鱼油;P:氧化前期鱼油(氧化第5天);M:氧化中期鱼油(氧化第7天);L:氧化后期鱼油(氧化第10天)。
1.3.5 果蝇寿命测定
参照李秀娟等[7]的方法,稍作修改。选用雌性处女蝇每组各500只,随机分为对照组和添加鱼油组,添加鱼油组使用添加不同氧化程度沙丁鱼油的培养基进行饲养,对照组使用基础培养基饲养。每天观察计数死亡的果蝇数量。按公式(1)计算果蝇死亡率,结果不计算实验中意外飞走的果蝇。
果蝇死亡率/%=A/果蝇总数×100
(1)
式中:A,添加不同氧化程度鱼油后果蝇每天死亡数量,只。
1.3.6 果蝇攀爬能力测定
根据寿命实验(果蝇死亡率),收集对照组和添加鱼油组10、20 d的果蝇进行攀爬能力实验,每组20只处女蝇。将待测果蝇转移至测定管中,轻拍测定管使果蝇落在测定管底部,装入试管后计数15 s内从试管底部爬到管口海绵塞处的果蝇只数,每组重复5次。每隔30 min测量1次,按公式(2)计算果蝇攀爬指数[7-8]。
攀爬指数/%=A/果蝇总数×100
(2)
式中:A,15 s内爬到海绵塞处果蝇数量,只。
1.3.7 果蝇抗冷应激能力测定
参照王倩倩[10]的方法,稍作修改。根据寿命实验(果蝇死亡率),收集对照组和给药组10、20 d的果蝇进行攀爬能力的实验,每组20只处女蝇,按照1.3.3节的方法将待测果蝇管置于碎冰上,计数20 s内到海绵塞处的果蝇只数,计算每组果蝇冷冻刺激环境下较常温环境中攀附指数的变化率,以此评估果蝇抗冷应激能力的变化情况,并按公式(3)计算。每组果蝇分别测定3次,每隔30 min测量1次。
抗冷应激攀爬/%=A/果蝇总数×100
(3)
式中:A,在冷冻刺激环境下20 s内爬到海绵塞处果蝇数量,只。
1.3.8 果蝇繁殖产卵能力测定
参照GOMEZ等[11]的方法稍作修改。收集24 h内羽化的果蝇,将收集到的雌雄果蝇按照性别分组,分别置于不同培养基中饲养,即空白对照组和添加鱼油组。雌、雄果蝇培养至第10天后,每组各放入10只雌性和雄性进行喂养,记录48 h内的产卵数量。
1.4 数据处理
数据采用SPSS 27和Origin 2022进行处理,结果用“平均值±标准差”表示。采用LSD法进行统计学比较,在P<0.05水平上具有统计学意义。
2 结果与分析
2.1 沙丁鱼油POV变化
由图1可知,0~3 d的POV从1.58 meq/kg上升至49.54 meq/kg,这是由于高温加速了油脂的自动氧化反应,使得鱼油氧化初期产生大量氢过氧化物,POV随氧化程度加深而增高。从4 d开始,POV不断下降至24.66 meq/kg,随着氧化时间延长油脂深度氧化,氢过氧化物分解成醛、酮、酸等小分子等物质,导致油脂酸败[12]。氢过氧化物的分解速度超过了生成速度导致POV下降,并且次级产物积累可能抑制自由基链式反应,使POV下降[13]。
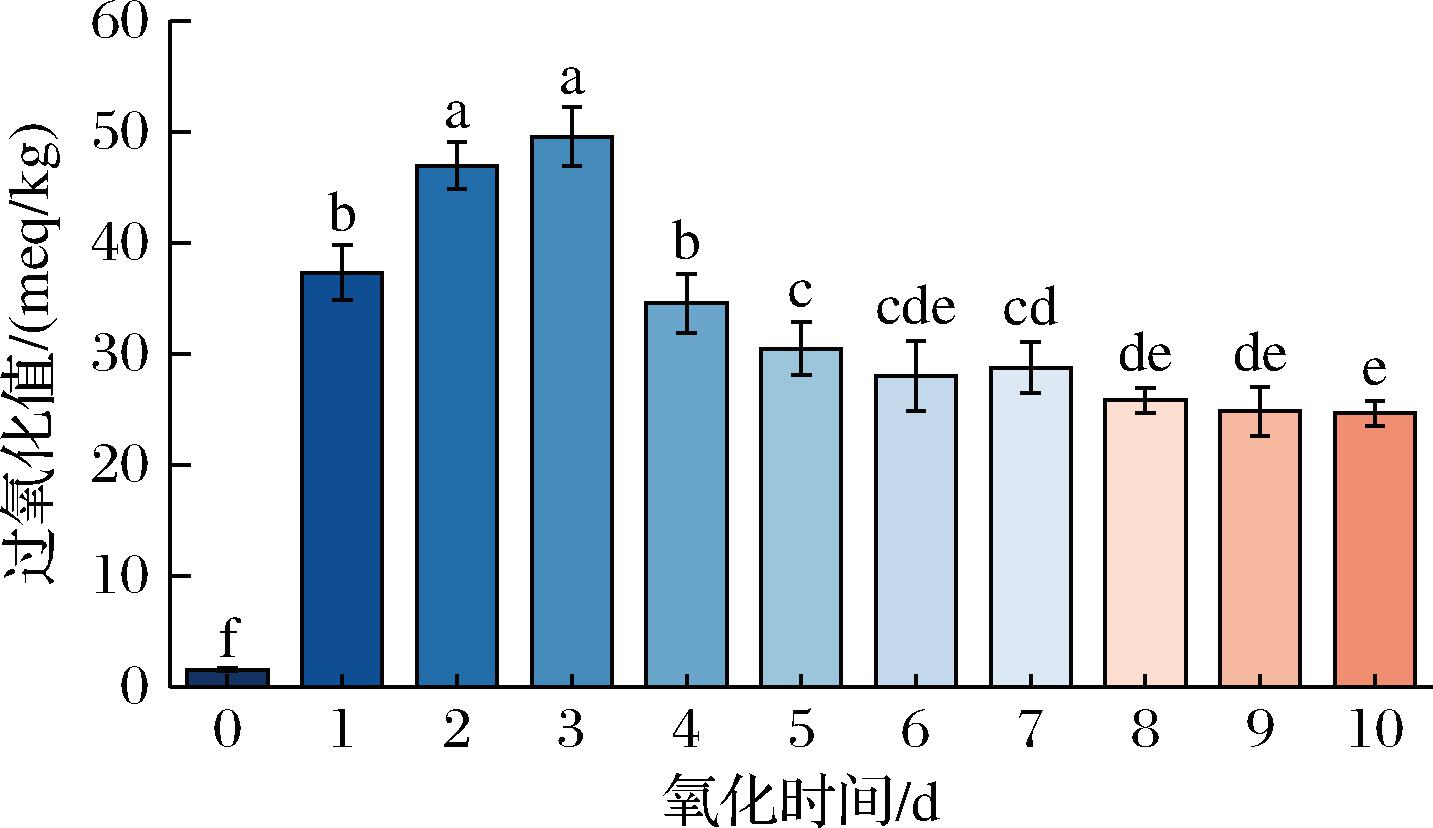
图1 80 ℃氧化鱼油POV的变化
Fig.1 Changes in POV of oxidized fish oil at 80 ℃
注:不同小写字母表示不同组间的显著性差异(P<0.05)(图2、图3、图8同)。
2.2 沙丁鱼油AV变化
由图2可知,80 ℃氧化沙丁鱼油,AV从0.58 mg/g上升至31.25 mg/g。油脂氧化初级产物的氢过氧化物进一步分解会产生小分子的醛、酸等化合物。这些小分子的酸类化合物会增加油脂中的游离脂肪酸含量,从而导致AV升高[14]。随着油脂氧化时间的延长,氧化程度不断加深,产生的氢过氧化物及其分解产物也增多,AV也会持续上升。油脂在高温、微生物和酶的作用下,可以发生热分解、热聚合、缩合、氧化反应和水解反应,使脂肪酸游离出来[15],使得油脂品质降低,黏度增大、AV逐渐升高。
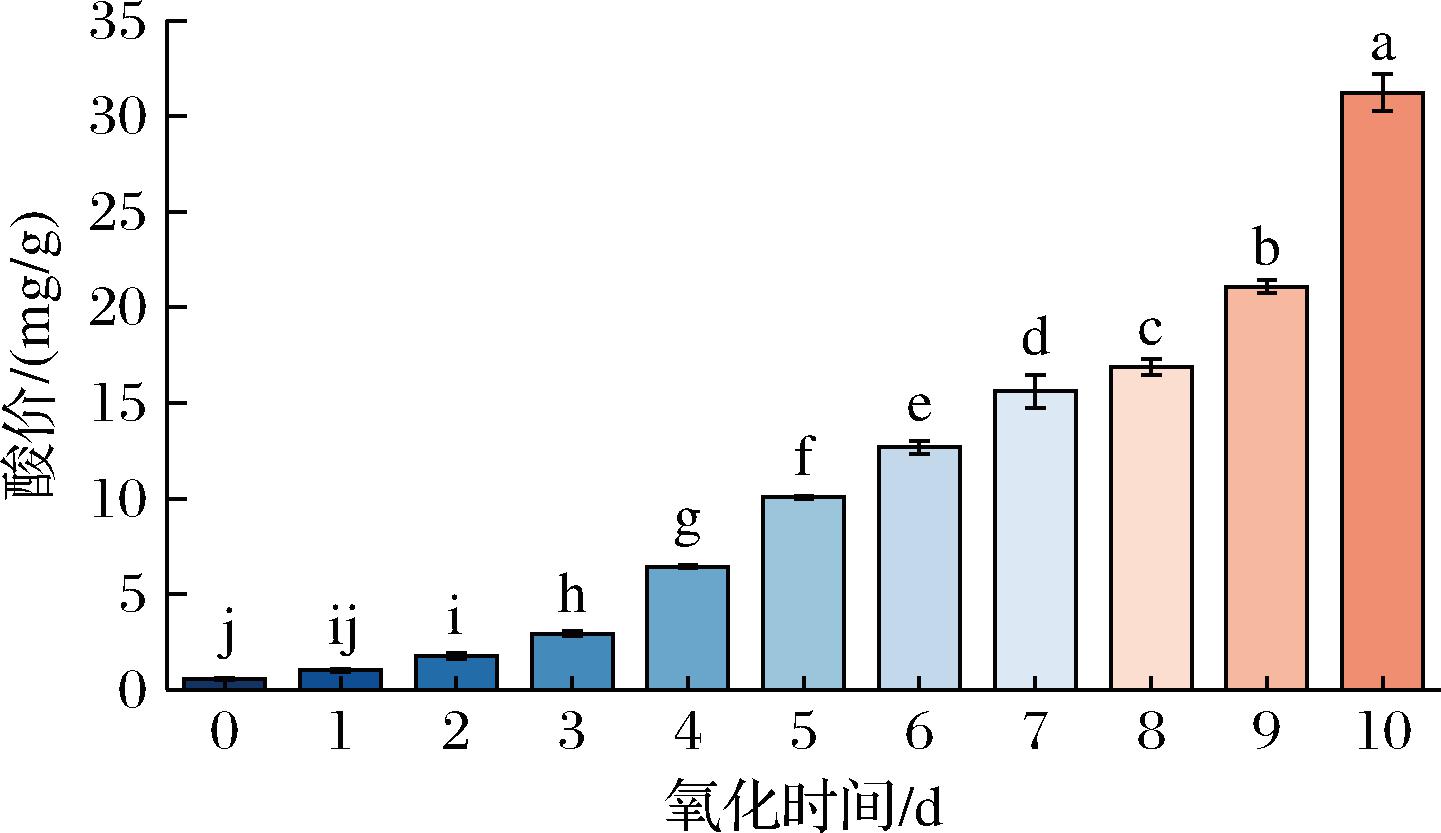
图2 80 ℃氧化鱼油AV的变化
Fig.2 Changes in AV of oxidized fish oil at 80 ℃
2.3 沙丁鱼油MDA变化
由图3可知,MDA含量随着氧化时间的延长,呈现先上升后下降的趋势。氧化初期,鱼油在高温、氧气和金属离子的催化下,发生自由基链式反应,生成大量脂质氢过氧化物,并且随着氧化的进行大量分解,生成MDA以及短链羰基化合物[16]。使MDA在前5 d大量积累,MDA含量不断上升,第5天达到最高值。氧化后期,在持续高温通氧条件下,部分游离MDA会从油相中挥发,并且与其他产生的醛类发生聚合反应[17],使得MDA含量呈下降趋势。
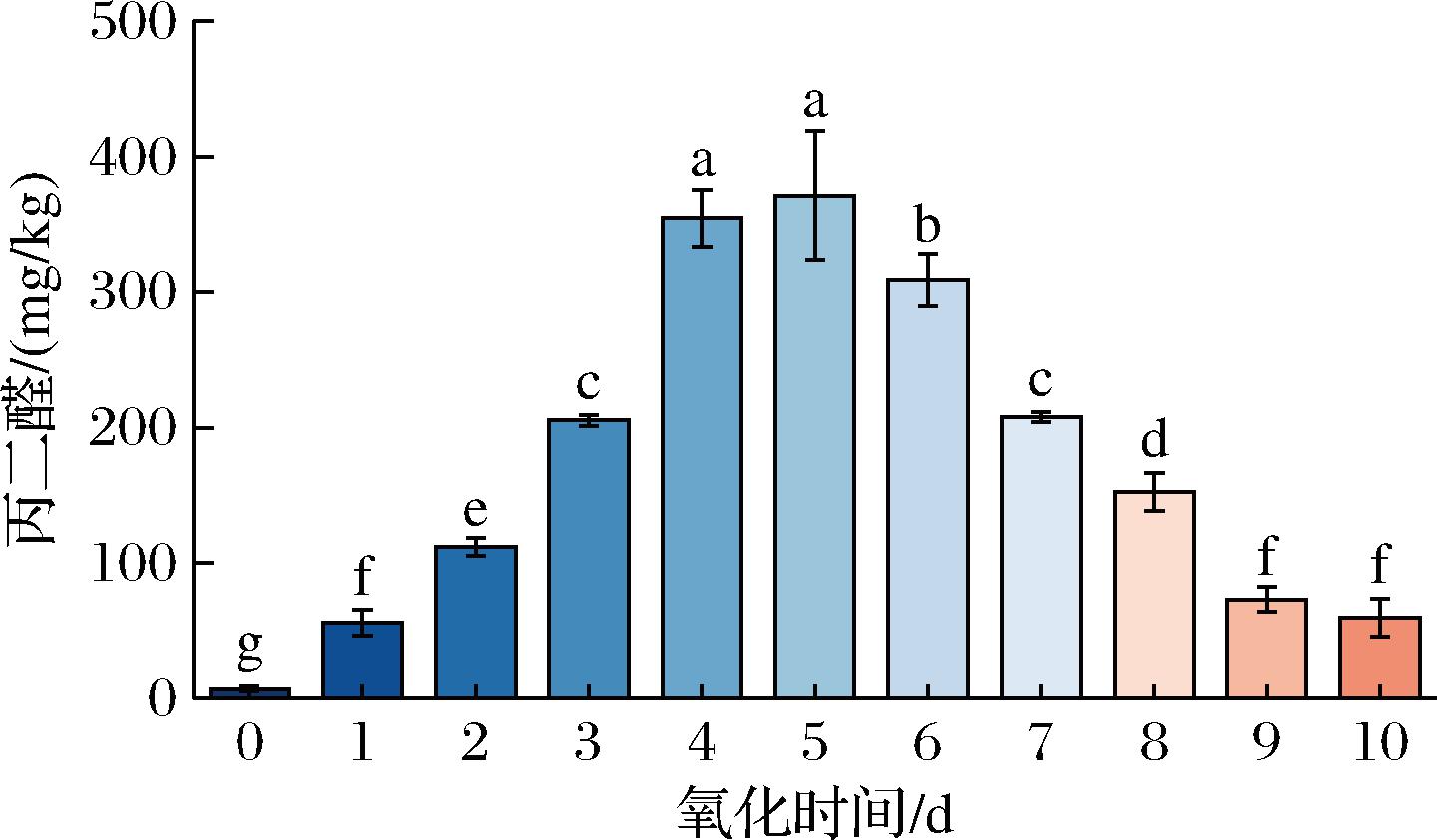
图3 80 ℃氧化鱼油MDA的变化
Fig.3 Changes in MDA of oxidized fish oil at 80 ℃
2.4 沙丁鱼油FTIR变化
在4 000~500 cm-1的光谱范围内获得了氧化沙丁鱼油的光谱信息。由图4可知,经80 ℃高温氧化后沙丁鱼油的大多数光谱信息集中在3 600~2 800 cm-1 和1 800~700 cm-1这2个区域。随着氧化的进行,脂质过氧化物中O—O—H基团导致羟基(O—H)峰吸收显著增强并变宽。在1 650~1 600 cm-1 由于不饱和脂肪酸氧化后其中双键在自由基攻击下发生重排形成共轭二烯[18],促使吸收峰出现并逐渐增强。1 737~1 740 cm-1为不饱和脂肪酸中C![]() C的伸缩振动。氧化后期次级氧化产物不断积累与氢过氧化物分解,导致在1 740~1 710 cm-1 区域的C
C的伸缩振动。氧化后期次级氧化产物不断积累与氢过氧化物分解,导致在1 740~1 710 cm-1 区域的C![]() O显著增强。油脂分子中C
O显著增强。油脂分子中C![]() C上的C—H伸缩振动吸收峰位于3 010 cm-1附近,3 000~2 900 cm-1为饱和C—H吸收峰的肩峰[19]。这反映脂质过氧化物在此阶段大量分解产生醛、酮等小分子物质。
C上的C—H伸缩振动吸收峰位于3 010 cm-1附近,3 000~2 900 cm-1为饱和C—H吸收峰的肩峰[19]。这反映脂质过氧化物在此阶段大量分解产生醛、酮等小分子物质。
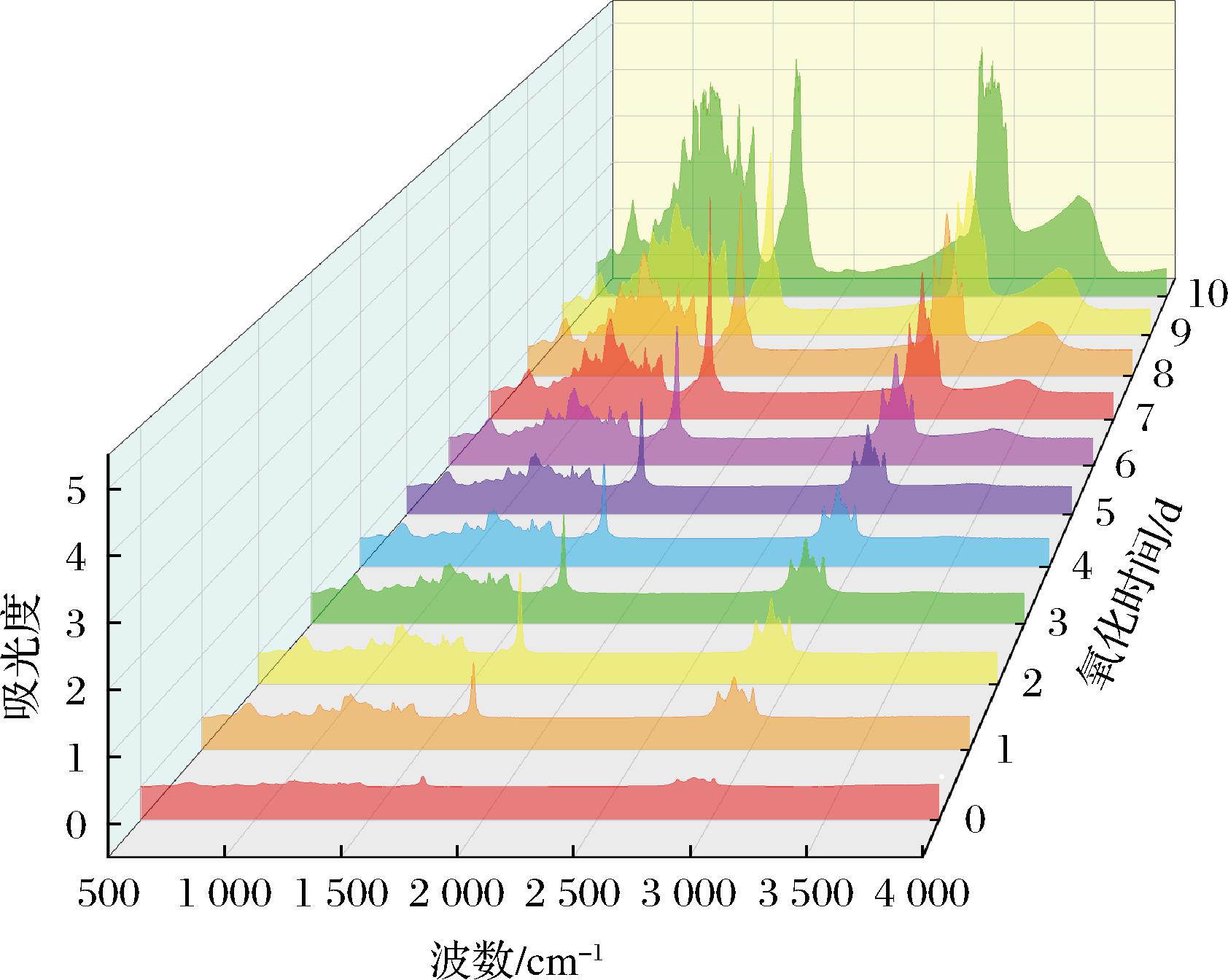
图4 80 ℃氧化鱼油FTIR的变化
Fig.4 Changes in FTIR of oxidized fish oil at 80 ℃
2.5 沙丁鱼油脂肪酸组成及含量
如表1所示,在沙丁鱼油氧化实验中,随着氧化程度增加,部分脂肪酸含量呈现显著变化。C17∶0和C21∶0在氧化后期含量显著降低,表明沙丁鱼油在长期高温氧化过程中,中短链饱和脂肪酸更易发生降解。沙丁鱼油中长链单不饱和脂肪酸(如C16∶1、C18∶1n9c、C24∶1)更易受长期高温氧化影响,而部分单不饱和脂肪酸(如C20∶1、C22∶1n9)表现出较强的抗降解能力。
表1 80 ℃氧化鱼油脂肪酸组成及含量 单位:g/100 g
Table 1 Changes in fatty acid composition and content of fish oil oxidized at 80 ℃
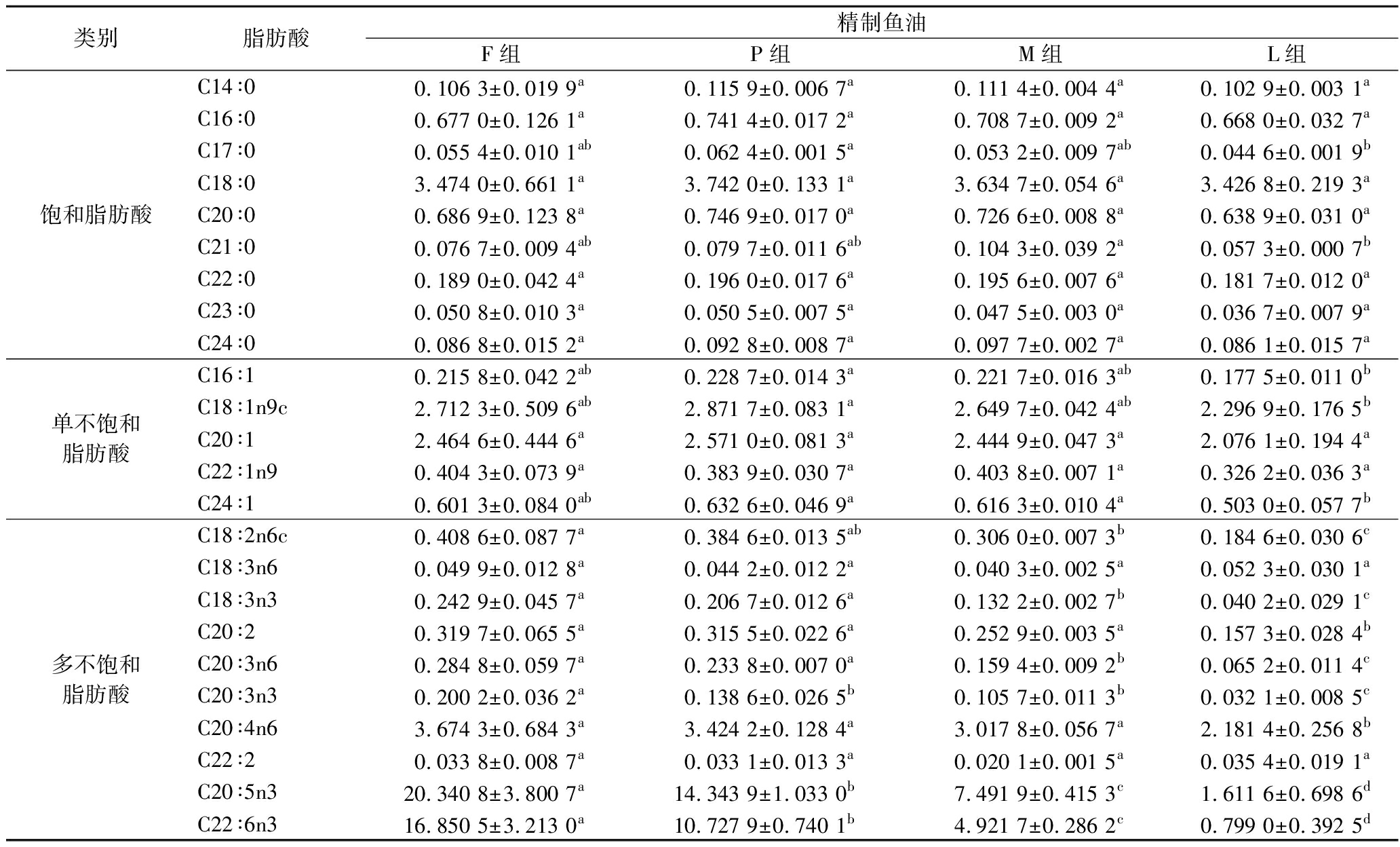
类别脂肪酸精制鱼油F组P组M组L组饱和脂肪酸C14∶00.106 3±0.019 9a0.115 9±0.006 7a0.111 4±0.004 4a0.102 9±0.003 1aC16∶00.677 0±0.126 1a0.741 4±0.017 2a0.708 7±0.009 2a0.668 0±0.032 7aC17∶00.055 4±0.010 1ab0.062 4±0.001 5a0.053 2±0.009 7ab0.044 6±0.001 9bC18∶03.474 0±0.661 1a3.742 0±0.133 1a3.634 7±0.054 6a3.426 8±0.219 3aC20∶00.686 9±0.123 8a0.746 9±0.017 0a0.726 6±0.008 8a0.638 9±0.031 0aC21∶00.076 7±0.009 4ab0.079 7±0.011 6ab0.104 3±0.039 2a0.057 3±0.000 7bC22∶00.189 0±0.042 4a0.196 0±0.017 6a0.195 6±0.007 6a0.181 7±0.012 0aC23∶00.050 8±0.010 3a0.050 5±0.007 5a0.047 5±0.003 0a0.036 7±0.007 9aC24∶00.086 8±0.015 2a0.092 8±0.008 7a0.097 7±0.002 7a0.086 1±0.015 7a单不饱和脂肪酸C16∶10.215 8±0.042 2ab0.228 7±0.014 3a0.221 7±0.016 3ab0.177 5±0.011 0bC18∶1n9c2.712 3±0.509 6ab2.871 7±0.083 1a2.649 7±0.042 4ab2.296 9±0.176 5bC20∶12.464 6±0.444 6a2.571 0±0.081 3a2.444 9±0.047 3a2.076 1±0.194 4aC22∶1n90.404 3±0.073 9a0.383 9±0.030 7a0.403 8±0.007 1a0.326 2±0.036 3aC24∶10.601 3±0.084 0ab0.632 6±0.046 9a0.616 3±0.010 4a0.503 0±0.057 7b多不饱和脂肪酸C18∶2n6c0.408 6±0.087 7a0.384 6±0.013 5ab0.306 0±0.007 3b0.184 6±0.030 6cC18∶3n60.049 9±0.012 8a0.044 2±0.012 2a0.040 3±0.002 5a0.052 3±0.030 1aC18∶3n30.242 9±0.045 7a0.206 7±0.012 6a0.132 2±0.002 7b0.040 2±0.029 1cC20∶20.319 7±0.065 5a0.315 5±0.022 6a0.252 9±0.003 5a0.157 3±0.028 4bC20∶3n60.284 8±0.059 7a0.233 8±0.007 0a0.159 4±0.009 2b0.065 2±0.011 4cC20∶3n30.200 2±0.036 2a0.138 6±0.026 5b0.105 7±0.011 3b0.032 1±0.008 5cC20∶4n63.674 3±0.684 3a3.424 2±0.128 4a3.017 8±0.056 7a2.181 4±0.256 8bC22∶20.033 8±0.008 7a0.033 1±0.013 3a0.020 1±0.001 5a0.035 4±0.019 1aC20∶5n320.340 8±3.800 7a14.343 9±1.033 0b7.491 9±0.415 3c1.611 6±0.698 6dC22∶6n316.850 5±3.213 0a10.727 9±0.740 1b4.921 7±0.286 2c0.799 0±0.392 5d
注:F:新鲜鱼油;P:氧化前期鱼油;M:氧化中期鱼油;L:氧化后期鱼油。不同小写字母表示不同组间的显著性差异(P<0.05)(下同)。
多不饱和脂肪酸含量随氧化程度加深呈现显著下降趋势。其中,二十碳五烯酸、二十二碳六烯酸下降趋势较显著,表明这2种高不饱和脂肪酸在长期氧化中几乎完全分解,说明其在高温氧化中高度不稳定,且双键数量与其氧化呈正相关[20]。
2.6 对果蝇寿命影响
将不同氧化程度的沙丁鱼油喂养果蝇后发现,氧化程度越深对果蝇的寿命影响越大,果蝇死亡率越高(图5)。F组与C组差异较小,说明未氧化的鱼油可能存在轻微的氧化或毒性有限,使影响结果不明显。喂养后期各氧化产物协同加剧氧化应激和代谢紊乱[21],导致果蝇死亡率显著上升。
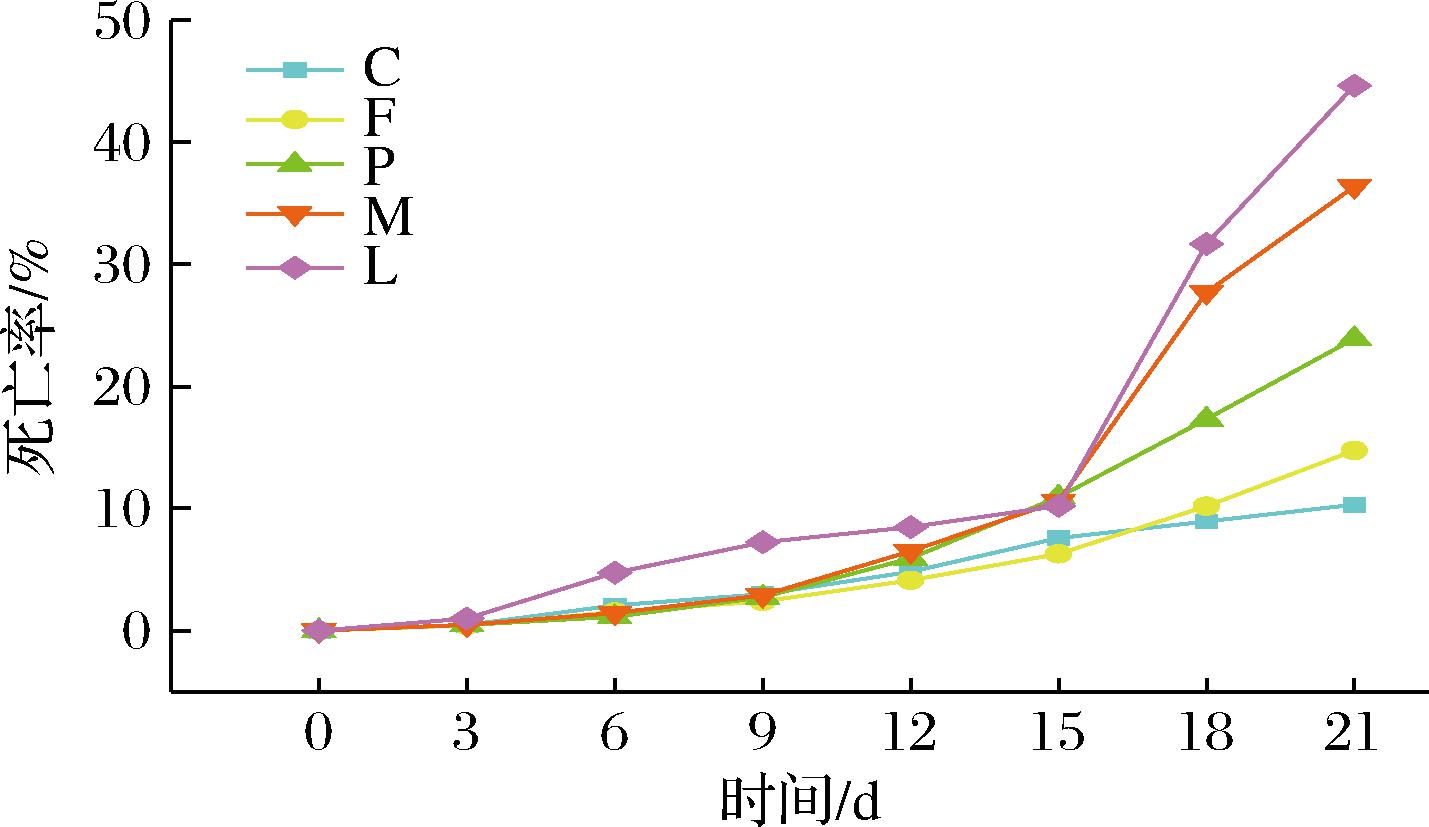
图5 不同氧化程度沙丁鱼油对果蝇寿命的影响
Fig.5 Effect of different levels of oxidation of sardine oil on the lifespan of D. melanogaster
2.7 对果蝇攀爬能力影响
如图6所示,氧化程度越高、喂养时间越长对果蝇的攀爬能力影响越大,果蝇攀爬指数越低,同组下降率越高。喂养10 d时,各组攀爬指数未呈现显著差异,可能由于氧化鱼油对运动能力影响不显著。折线表示不同氧化程度沙丁鱼油喂养果蝇后,果蝇攀爬能力在第10天和20天时同组下降率,结果表明喂养20 d攀爬指数相较于10 d显著下降,同组下降率从C组的3.29%显著上升至L组79.24%,同组下降率随氧化程度加深和喂养时间延长而不断上升,表明氧化后期的氧化产物不断积累,MDA等活性醛类可能通过破坏线粒体功能,降低ATP合成,持续加剧运动神经元退化,使运动功能下降[21-22]。
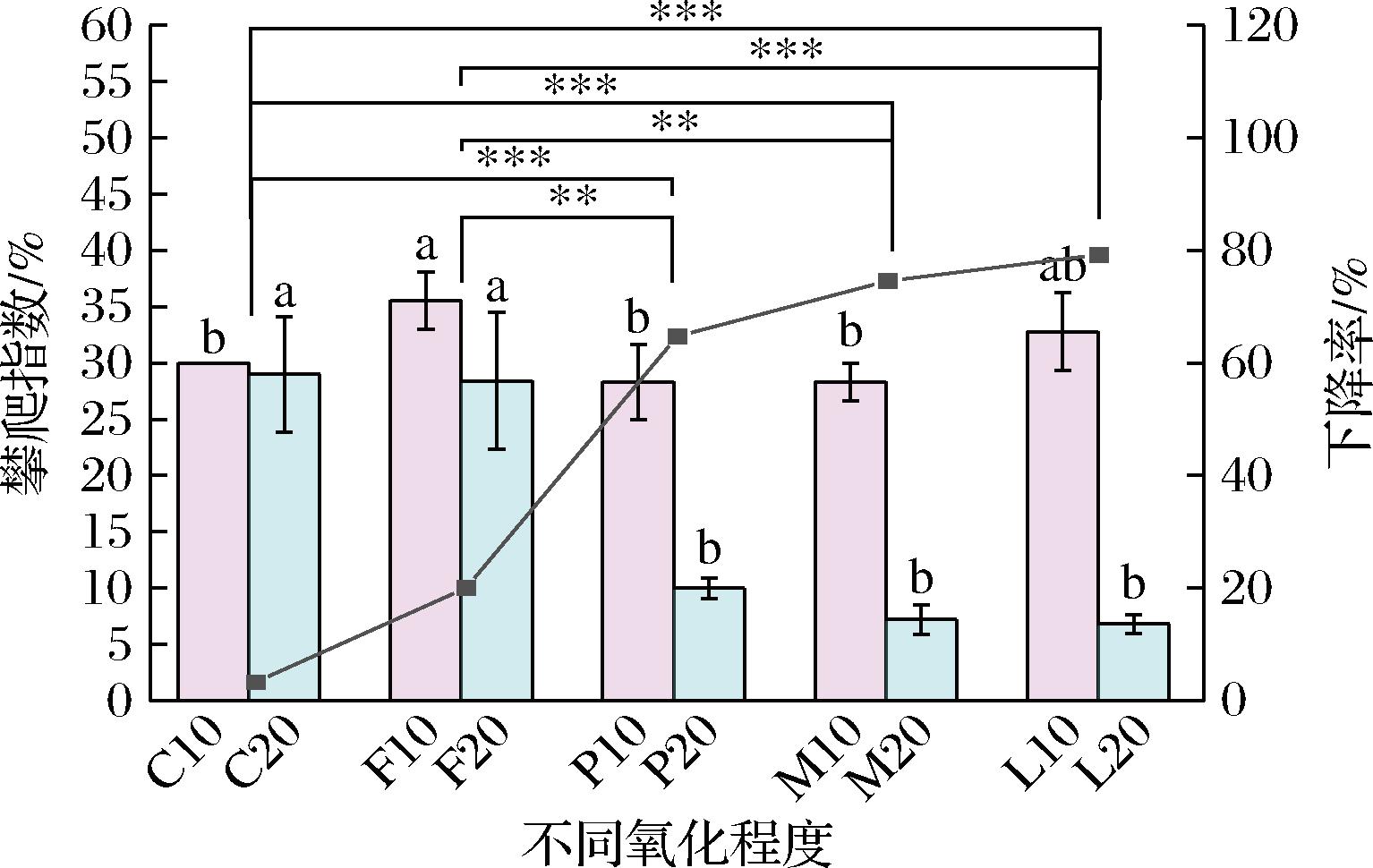
图6 不同氧化程度沙丁鱼油对果蝇攀爬能力影响
Fig.6 Effect of different levels of oxidation of sardine oil on the climbing ability of D. melanogaster
注:不同小写字母表示不同组别间的显著性差异(P<0.05);*表示P<0.05,**表示P<0.01,***表示P<0.001,图7同。
2.8 对果蝇抗冷应激能力影响
如图7所示,氧化程度越深对果蝇的抗冷应激能力损伤越严重,且随时间加剧,果蝇攀爬指数越低,同组下降率越高。折线表示不同氧化程度沙丁鱼油喂养果蝇后,果蝇抗冷应激能力在第10天和20天时同组下降率,喂养20 d攀爬指数相较于10 d显著下降,同组下降率从C组的33.46%显著上升至L组的76.72%,这可能是由于氧化鱼油会不断生成氧化产物并随喂养时间延长不断积累,抑制线粒体活性,导致果蝇在冷应激时无法产生足够能量维持运动与氧化失衡,使得攀爬指数不断下降[21-22]。
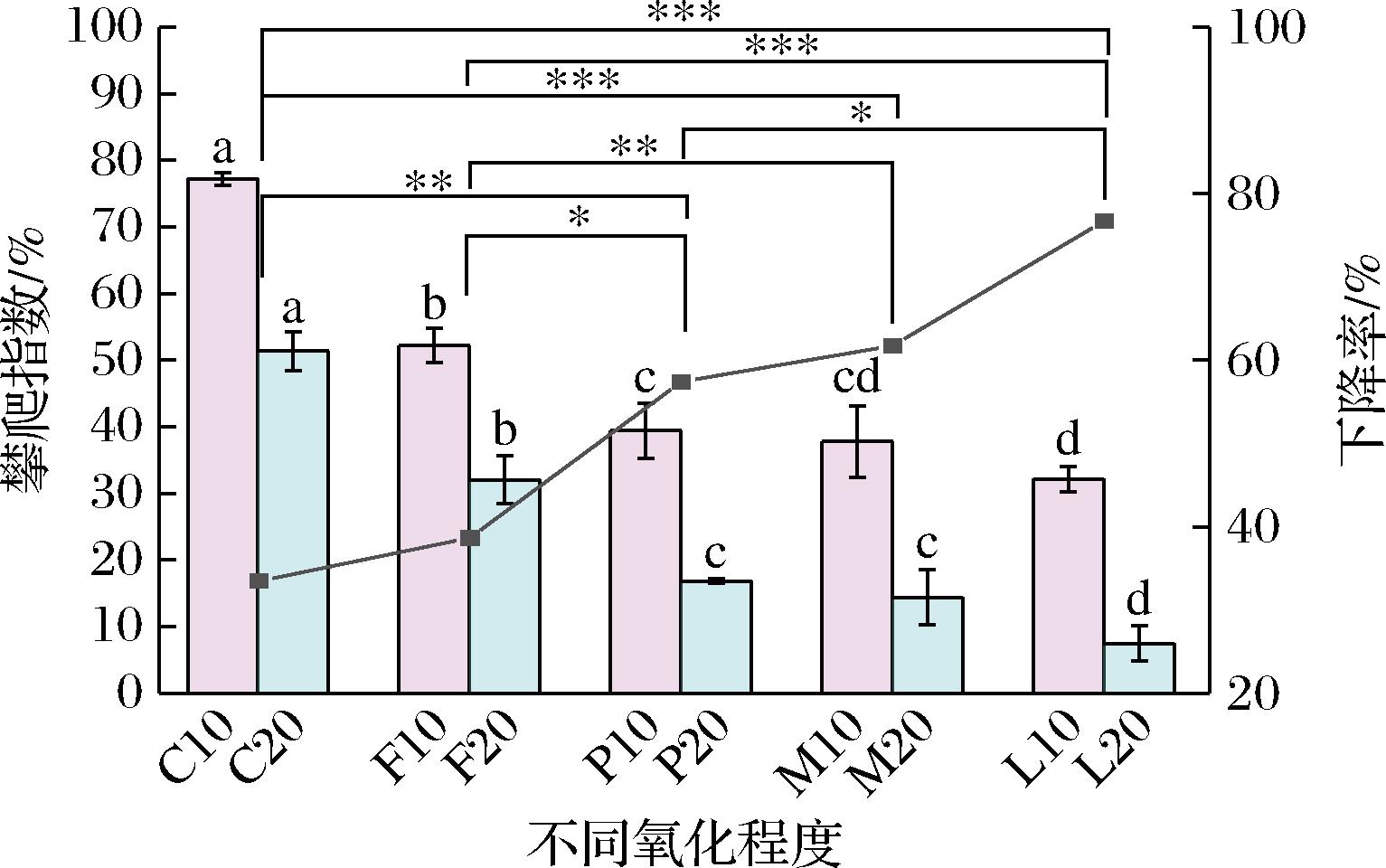
图7 不同氧化程度沙丁鱼油对果蝇抗冷应激能力影响
Fig.7 Effect of different levels of oxidation of sardine oil on cold stress resistance in D. melanogaster
冷应激下破坏了细胞膜稳定性[23]。氧化后期产物中的大分子聚合物嵌入细胞膜破坏磷脂双分子层结构,同时,氧化产物导致脂质过氧化链式反应持续消耗多不饱和脂肪酸,降低了膜流动性,使果蝇在低温下神经信号传导与肌肉收缩能力丧失,攀爬指数下降。
2.9 对果蝇繁殖能力影响
将不同氧化程度的沙丁鱼油喂养果蝇后发现(图8),产卵量C组>F组>L组>P组>M组,相较于对照组,添加新鲜、氧化前期、中期鱼油对果蝇繁殖能力出现抑制作用,可能由于氧化鱼油产生MDA等小分子醛穿透细胞膜,生殖细胞分裂期对活性醛类高度敏感,破坏卵巢线粒体功能,抑制卵母细胞能量供应,导致产卵量下降[24-25]。而L组高于P组和M组,可能由于氧化后期MDA因聚合或与氨基化合物结合,生成大分子化合物,导致其细胞穿透性降低,对生殖细胞的直接损伤减弱。
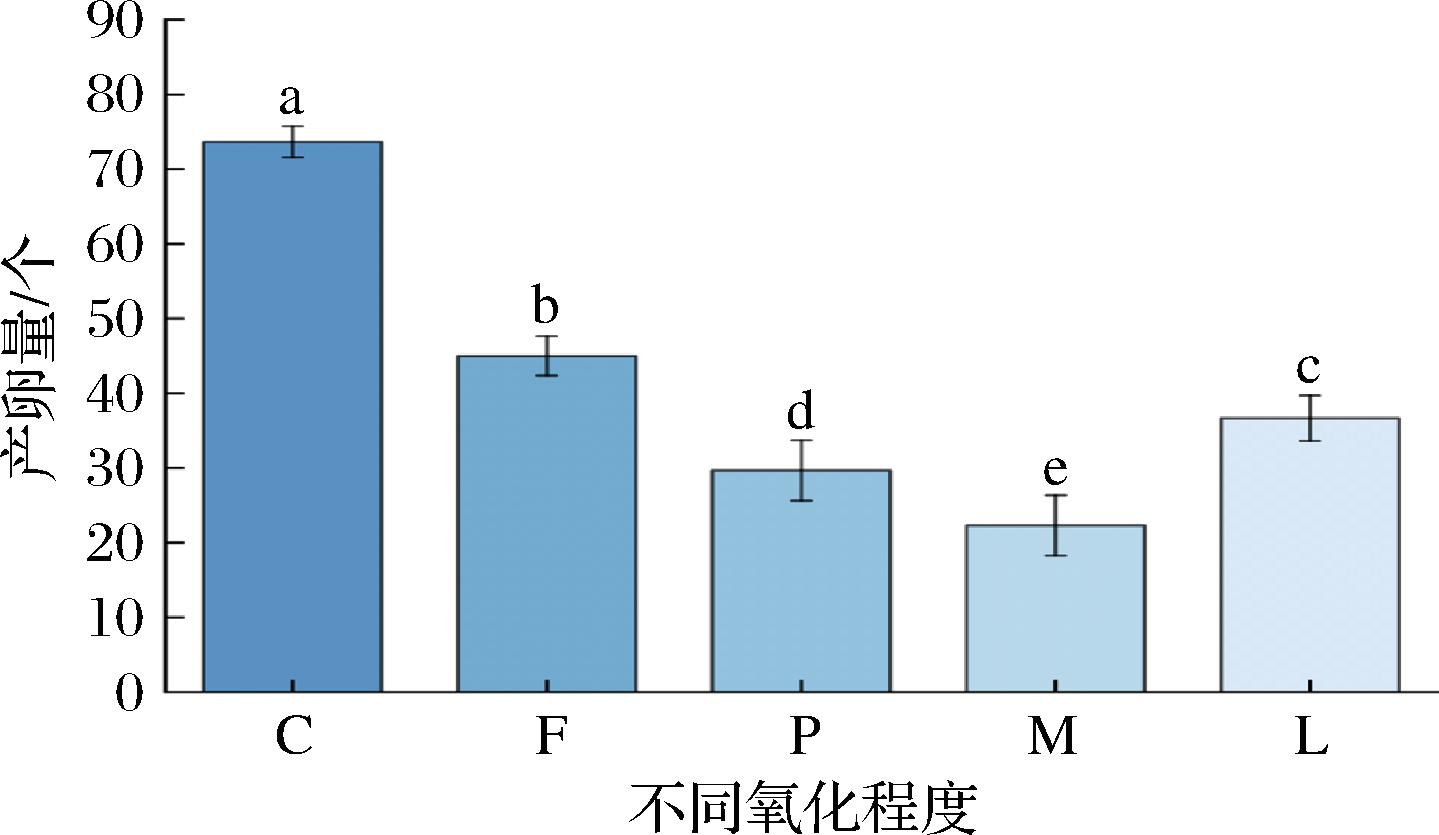
图8 不同氧化程度沙丁鱼油对果蝇繁殖产卵能力影响
Fig.8 Effect of different levels of oxidation of sardine oil on the reproductive capacity of D. melanogaster
3 结论与讨论
80 ℃氧化沙丁鱼油后,鱼油的AV含量呈现显著上升,POV、MDA和FTIR由于氧化分解产生大量氢过氧化物不断聚合导致呈现先上升后下降趋势,多不饱和脂肪酸含量随氧化时间延长呈现显著下降趋势,说明多不饱和脂肪酸在高温下几乎完全分解。氧化程度越深、喂养时间越长对果蝇的寿命、攀爬能力和抗冷应激能力影响越大,说明氧化后的鱼油产生的有害物质对果蝇线粒体和细胞膜影响较大。随着氧化时间的延长,氧化产物不断积累,产生MDA等小分子醛穿透细胞膜,破坏卵巢线粒体功能,从而对果蝇繁殖产卵能力造成显著影响。
[1] 魏文聪, 张雪冰, 陶宁萍.物理法和化学法精制对酶解法沙丁鱼油品质的影响[J].中国油脂, 2025, 50(1):9-16.WEI W C, ZHANG X B, TAO N P.Effect of physical and chemical refining on the quality of sardine oil prepared by enzymatic hydrolysis[J].China Oils and Fats, 2025, 50(1):9-16.
[2] 王正云, 李婷, 刘子潇, 等.不同贮藏温度下草鱼内脏鱼油品质变化[J].食品工业科技, 2023, 44(1):362-368.WANG Z Y, LI T, LIU Z X, et al.Quality changes of grass carp visceral fish oil under different storage temperatures[J].Science and Technology of Food Industry, 2023, 44(1):362-368.
[3] 刘秀妨, 刘胜男, 马云芳, 等.胃肠道消化过程中脂质氧化的影响因素、健康危害及控制研究进展[J].食品工业科技, 2017, 38(21):330-335.LIU X F, LIU S N, MA Y F, et al.Research progress on the influencing factors, health hazards, and control of lipid oxidation during gastrointestinal digestion[J].Science and Technology of Food Industry, 2017, 38(21):330-335.
[4] HOEBINGER C, RAJCIC D, HENDRIKX T.Oxidized lipids:Common immunogenic drivers of non-alcoholic fatty liver disease and atherosclerosis[J].Frontiers in Cardiovascular Medicine, 2022, 8:824481.
[5] SONG C Y, LIU B, LI H X, et al.Protective effects of emodin on oxidized fish oil-induced metabolic disorder and oxidative stress through Notch-Nrf2 crosstalk in the liver of teleost Megalobrama amblycephala[J].Antioxidants, 2022, 11(6):1179.
[6] GAO Q, LIU B, SHAN F, et al.Effects of oxidized fish oil on digestive enzyme activity and antioxidant system in Macrobrachium rosenbergii post-larvae[J].Aquaculture Reports, 2022, 23:101062.
[7] 李秀娟, 魏晶晶, 柴学军, 等.元宝枫油对衰老果蝇生理指标及肠道菌群的影响[J].食品科学, 2024, 45(3):76-83.LI X J, WEI J J, CHAI X J, et al.Effect of Acer truncatum seed oil on physiological indicators and intestinal flora in aging Drosophila melanogaster[J].Food Science, 2024, 45(3):76-83.
[8] 徐梦婷, 朱钰晨, 苏丹, 等.江香薷籽油对果蝇睡眠、嗅觉能力和抗氧化指标的影响[J].中国实验动物学报, 2024, 32(9):1182-1190.XU M T, ZHU Y C, SU D, et al.Effects of Mosla chinensis seed oil on sleep, olfactory ability, and antioxidant indexes in D.melanogaster[J].Acta Laboratorium Animalis Scientia Sinica, 2024, 32(9):1182-1190.
[9] 宁海花, 周啟佳, 杜枘, 等.基于中红外光谱结合化学计量法快速检测油炸食品用油品质[J].食品与机械, 2022, 38(6):93-98.NING H H, ZHOU Q J, DU R, et al.Rapid determination of the quality of frying oils using mid-infrared spectroscopy coupled with chemometrics methods[J].Food &Machinery, 2022, 38(6):93-98.
[10] 王倩倩. 东海乌参肽的抗衰老作用及机制研究[D].杭州:浙江大学, 2023.WANG Q Q.Anti-aging effect and mechanism of sea cucumber (Acaudina leucoprocta) peptides[D].Hangzhou:Zhejiang University, 2023.
[11] GOMEZ A, GONZALEZ S, OKE A, et al.A high-throughput method for quantifying Drosophila fecundity[J].Toxics, 2024, 12(9):658.
[12] 马萍. 新型迷迭香复合抗氧化剂的开发及其对花生仁氧化稳定性的影响[D].南昌:南昌大学, 2024.MA P.Development of a novel rosemary complex antioxidant for peanut and its oxidative stability[D].Nanchang:Nanchang University, 2024.
[13] 姚仕彬, 叶元土, 李洁, 等.鱼油在氧化过程中氧化指标及其脂肪酸组成的变化[J].饲料研究, 2012, 35(6):74-76.YAO S B, YE Y T, LI J, et al.Changes in oxidation indezes and their fatty acid composition during oxidation of fish oils[J].Feed Research, 2012, 35(6):74-76.
[14] 李尤好, 刘潇, 沈飞, 等.高温储藏条件对花生油脂和蛋白质品质劣变的影响[J].食品科学, 2023, 44(13):105-111.LI Y H, LIU X, SHEN F, et al.Effect of high temperature storage condition on quality deterioration of peanut oil and protein[J].Food Science, 2023, 44(13):105-111.
[15] CHEN J, ZHANG L Y, GUO X F, et al.Influence of triacylglycerol structure on the formation of lipid oxidation products in different vegetable oils during frying process[J].Food Chemistry, 2025, 464:141783.
[16] LANKIN V Z, TIKHAZE A K, MELKUMYANTS A M.Malondialdehyde as an important key factor of molecular mechanisms of vascular wall damage under heart diseases development[J].International Journal of Molecular Sciences, 2023, 24(1):128.
[17] WANG D, XIAO H M, LYU X, et al.Lipid oxidation in food science and nutritional health:A comprehensive review[J].Oil Crop Science, 2023, 8(1):35-44.
[18] 张岩, 纪俊敏, 侯利霞, 等.不同热处理葵花籽方式对葵花籽油品质的影响[J].中国调味品, 2022, 47(5):5-14.ZHANG Y, JI J M, HOU L X, et al.Effects of different heat treatment methods on the quality of sunflower seed oil[J].China Condiment, 2022, 47(5):5-14.
[19] 吴雪辉, 何俊华, 王泽富.红外光谱快速测定油茶籽油脂肪酸组成的模型建立[J].中国油脂, 2022, 47(2):124-128.WU X H, HE J H, WANG Z F.Establishment of rapid detection model of fatty acid composition of oil-tea camellia seed oil by infrared spectroscopy[J].China Oils and Fats, 2022, 47(2):124-128.
[20] CHAULA D, JACOBSEN C, LASWAI H S, et al.Changes in fatty acids during storage of artisanal-processed freshwater sardines (Rastrineobola argentea)[J].Food Science &Nutrition, 2023, 11(6):3040-3047.
[21] TORAMAN E.Biochemical and molecular evaluation of oxidative stress and mitochondrial damage in fruit fly exposed to carmoisine[J].Molecular Biology Reports, 2024, 51(1):685.
[22] PICCA A, CALVANI R, COELHO-JUNIOR H J, et al.Mitochondrial dysfunction, oxidative stress, and neuroinflammation:Intertwined Roads to neurodegeneration[J].Antioxidants, 2020, 9(8):647.
[23] HUANG J J, CHEUNG P C K.Cold stress treatment enhances production of metabolites and biodiesel feedstock in Porphyridium cruentum via adjustment of cell membrane fluidity[J].Science of The Total Environment, 2021, 780:146612.
[24] ZHANG X Y, ZHANG L, XIANG W P.The impact of mitochondrial dysfunction on ovarian aging[J].Journal of Translational Medicine, 2025, 23(1):211.
[25] GANGULY A, NANDA S, MANDI M, et al.Exploring the ameliorative potential of rutin against high-Sucrose diet-induced oxidative stress and reproductive toxicity in Drosophila melanogaster[J].Reproductive Toxicology, 2024, 130:108742.