胶原蛋白作为关键结构纤维蛋白广泛存在于各类结缔组织的细胞外基质中[1],胶原蛋白的主要类型有Ⅰ型和Ⅱ型,其中Ⅰ型胶原蛋白在成年动物的皮肤组织中含量最为丰富,由于其高生物相容性和低抗原性,常用于日化用品或组织工程起到抗皱、抗衰老作用[2];而Ⅱ型胶原蛋白只在软骨组织中发现,它是关节软骨细胞外基质的主要成分,构成了60%的软骨干质量[3],可促进软骨细胞的分化,口服Ⅱ型胶原蛋白还可有效预防和治疗类风湿性关节炎和骨关节炎,且无不良反应。由于畜禽类蛋白制品的应用存在传播疾病的风险及宗教信仰的限制[4],因此,寻找安全、接受度高的胶原蛋白来源成为迫切需要解决的问题。美国食品药品监督管理局认为海洋源胶原蛋白安全有效[5],海洋资源丰富,品种繁多且富含蛋白,是胶原蛋白制备的良好来源[5]。
鲨鱼软骨作为水产加工副产物,富含胶原蛋白、蛋白聚糖等[3]。目前关于鲨鱼软骨胶原蛋白及其产品研发报道较多,制备软骨胶原蛋白常用的方法主要有酸法、酶法、热水法等。SEIXAS等[6]采用酸法和酶法从鲨鱼和鳐鱼软骨中提取胶原蛋白,发现酶法和酸法提取的胶原蛋白均为Ⅱ型,且酶法产率高于酸法。LUO等[7]以中国大鲵为原料,将大鲵软骨通过酸法和胃蛋白酶法制备胶原蛋白,并对其组成和结构进行了分析,结果表明酶法提取的胶原蛋白具有更高的结构稳定性和热稳定性。由于Ⅱ型胶原蛋白的三级结构极易受外界环境影响,破坏三螺旋结构。这种结构变化会引发其理化性质的显著改变,同时使其生物学特性发生变化,最终导致其生物活性的丧失[8]。因此,鲨鱼软骨胶原蛋白得率、纯度及稳定性低等问题仍是影响鲨鱼软骨胶原蛋白开发应用的主要问题。基于此,在采用不同方法制备鲨鱼软骨胶原蛋白的基础上,进一步分析其结构与功能特性,为鲨鱼软骨资源的深度开发与高值化利用提供一定的理论支持。
1 材料与方法
1.1 材料与试剂
长尾鲨鱼软骨购自宁波水产批发市场;三羟甲基氨基甲烷盐酸盐(Tris-HCl)、乙酸、乙二胺四乙酸二钠盐、NaCl、KCl、NaOH等均为分析纯,国药集团化学试剂有限公司;对二甲氨基苯甲醛、羟脯氨酸(均为分析纯),上海阿拉丁生化科技有限公司;5×蛋白上样缓冲液、胃蛋白酶(5×104 U/g)、SDS-PAGE凝胶配置试剂盒,北京索莱宝科技有限公司。
1.2 主要仪器设备
BIO-RAD Gel Doc XR凝胶成像仪,美国伯乐公司;5804R高速离心机,德国Eppendorf公司;VERTEX 70傅里叶红外光谱仪,德国BRUKER公司;DSC 2500差示扫描热量仪,美国TA仪器公司;UV 1780紫外可见分光光度计,日本岛津公司;Zeiss Sigma 300,德国蔡司公司;L-8900全自动氨基酸分析仪,日本日立公司;Chirascan V100圆二色光谱仪,英国应用光物理公司。
1.3 试验方法
1.3.1 鲨鱼软骨胶原蛋白提取率的测定
参照GB/T 9695.23—2008《肉与肉制品 羟脯氨酸含量测定》的方法测定样品中羟脯氨酸含量,提取率的计算如公式(1)所示:
(1)
式中:X,提取率,%;ρ0,提取液中羟脯氨酸质量浓度,μg/mL;ρ,软骨中羟脯氨酸质量浓度,μg/mL。
1.3.2 鲨鱼软骨胶原蛋白的酶法制备
参考张武等[8]的方法,按9 150 U/g的酶添加量加入胃蛋白酶,在30 ℃、pH 1.67的条件下,振荡反应39.85 h。反应结束后进行离心分离,取上清液,向上清液中加入NaCl,使其终浓度为2.6 mol/L,进行盐析并静置过夜,依次用蒸馏水和0.1 mol/L 乙酸进行24 h的透析处理,最后通过冷冻干燥,获得酶溶性胶原蛋白(collagen prepared by enzymatic,PSC)。
1.3.3 酸法提取鲨鱼软骨胶原蛋白
参考胡艺等[9]的方法,将预处理的鲨鱼软骨按200 g/L的质量浓度溶于0.5 mol/L的乙酸中,在4 ℃下搅拌提取4 d后离心取上清液,用0.05 mol/L Tris-HCl调节pH值至7.5后往清液加入NaCl直至反应体系浓度达到2.6 mol/L,使溶液出现絮状沉淀,充分搅拌,于室温下静置过夜,将盐析液在4 ℃、10 000 r/min 离心30 min,用0.5 mol/L乙酸溶解沉淀,将所得溶液转移至截留分子质量为14 kDa的透析袋进行透析,先用0.1 mol/L乙酸透析24 h,再用去离子水透析48 h,期间每12 h定时更换1次透析液,透析完成后,将透析液冻干即得酸溶性胶原蛋白(collagen prepared by acid,ASC)。
1.3.4 热水法提取鲨鱼软骨胶原蛋白
参考PROKOPOV 等[10]的方法并稍作修改,称取预处理鲨鱼软骨按料液比1∶10(g∶mL)加入去离子水,60 ℃ 提取10 h,提取完后离心取上清液并冻干即得热水法制备的胶原蛋白(collagen prepared by hot water,HWC)。
等[10]的方法并稍作修改,称取预处理鲨鱼软骨按料液比1∶10(g∶mL)加入去离子水,60 ℃ 提取10 h,提取完后离心取上清液并冻干即得热水法制备的胶原蛋白(collagen prepared by hot water,HWC)。
1.3.5 不同方法制备的鲨鱼软骨胶原蛋白结构表征
1.3.5.1 紫外(ultraviolet,UV)吸收光谱
参考ZHU等[11]的方法并稍作修改,将样品溶于0.5 mol/L乙酸中至终质量浓度为0.25 mg/mL,并将混合物4 ℃、9 000×g离心5 min,用紫外可见分光光度计在200~400 nm扫描。
1.3.5.2 傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR)
取适量经冻干处理的样品,与干燥的光谱纯KBr充分混合。将混合物均匀研磨进行压片操作。波数采集范围为4 000~400 cm-1,分辨率为4 cm-1,运用PeakFit v4.12软件分析红外光谱的酰胺I带[(1 700~1 600) cm-1],根据各子峰与二级结构之间的对应关系,计算各吸收峰峰面积占比,得到各二级结构相对含量。
1.3.5.3 圆二色光谱(circular dichroism,CD)
称取适量胶原蛋白冻干品溶于0.5 mol/L乙酸溶液,制得质量浓度为0.5 mg/mL胶原蛋白溶液,然后采用CD仪进行分析。扫描条件:N2压力0.4 MPa,在190~260 nm波长范围内进行连续扫描,光谱带宽1 nm,信号采集响应时间0.5 s。
1.3.5.4 SDS-PAGE分析
参考SONG等[12]的方法并稍作修改,用50 g/L浓缩胶和80 g/L分离胶进行电泳。用0.5 mol/L乙酸配制5 mg/mL胶原蛋白溶液,按体积比4∶1混合上样缓冲液,沸水浴10 min后离心取上清液并上样。电泳条件:浓缩胶电压80 V,分离胶电压120 V,经染色脱色后进行分析。
1.3.5.5 氨基酸组成分析
参考王乐等[13]的方法并稍作修改,称取适量样品加入10 mL 6 mol/L盐酸,经N2置换密封处理,静置,110 ℃恒温水解24 h,将反应液定容过滤,经10 000 r/min离心10 min后,移取0.2 mL上清液至氮吹装置中干燥,向干燥样品中加入2 mL 0.02 mol/L 的盐酸溶解,溶液用0.22 μm滤膜过滤后上机分析,每个样品平行进样3次。
1.3.5.6 差示扫描量热法(differential scanning calorimeter,DSC)
参考ATA等[14]的方法并稍作修改,将冻干样品以1∶3(g∶mL)的固液比溶于去离子水中,4 ℃下放置24 h使其充分溶胀,用滤纸擦拭湿样品去除多余水分,在10~70 ℃以2 ℃/min的速度扫描样品。
1.3.5.7 扫描电子显微镜(scanning electron microscope,SEM)观察微观结构
将胶原蛋白样品在SEM样品架上固定,对其进行真空喷金后,对样品表面形态进行观察分析。
1.3.6 鲨鱼软骨胶原蛋白功能特性研究
1.3.6.1 溶解性
用0.5 mol/L乙酸配制2 mg/mL胶原蛋白溶液,加入NaCl溶液,使其最终质量浓度分别为0、10、20、30、40、60、80、100 mg/mL,4 ℃下振荡放置1 h,10 000 r/min离心15 min取上清液,采用福林酚法[15]测定,胶原蛋白含量的计算如公式(2)所示:
相对溶解度![]()
(2)
式中:ρ1,添加NaCl后上清液胶原蛋白含量,mg/mL;ρ2,不添加NaCl的上清液胶原蛋白含量,mg/mL。
1.3.6.2 吸水性和吸油性
参考蔡路昀等[16]的方法稍作修改,称取0.025 g胶原蛋白冻干样品,分别溶于25 mL水和25 mL大豆油中,快速混匀,在室温放置30 min后,6 000 r/min离心30 min取上清液,其计算如公式(3)所示:
吸水性/吸油性![]()
(3)
式中:V1,上清液体积,mL。
1.3.6.3 持水性
参考ZHANG等[17]的方法并稍作修改,取胶原蛋白冻干样品0.01 g于10 mL纯水中,快速混匀后置入培养皿中,将培养皿放入37 ℃恒温干燥箱,每20 min测量皿中剩余水分质量,持续2 h,持水性的计算如公式(4)所示:
持水性![]()
(4)
式中:m1,皿中剩余水分质量,mg;m0,最初水分质量,mg。
1.3.6.4 乳化性
参考韩霜等[18]的方法并稍作修改,称取0.1 g样品于50 mL离心管中,分别加入15 mL纯水和15 mL大豆油,经高速匀浆机均质2 min后,1 500 r/min离心10 min,计算乳化层体积与溶液总体积之比,即为乳化性。
1.3.7 数据处理与分析
数据以“平均值±标准偏差”表示,运用SPSS软件对数据进行处理分析,运用Duncan进行多重范围检验法评估组间差异,以P<0.05表示数据具有统计学意义上的显著性差异,使用GraphPad Prism 10作图。
2 结果与分析
2.1 鲨鱼软骨胶原蛋白的提取率及含量分析
采用酶法、酸法及热水法制备鲨鱼软骨胶原蛋白,发现PSC的提取率及含量最高,分别为85.09%及91.32%,其次为HWC,提取率为29.97%,含量为73.32%,而ASC提取率最低(13.78%)。这是由于酶法提取是在胃蛋白酶处理的基础上进一步采用一定浓度的乙酸溶液进行提取的,而胃蛋白酶处理可特异性地作用于胶原蛋白端的交联分子,暴露亲水基团,从而提高胶原蛋白溶解度。同时,在酸性条件下提取还可破坏胶原蛋白的非共价键,使得蛋白质内部结构更加松散,从而提高其提取率[6]。
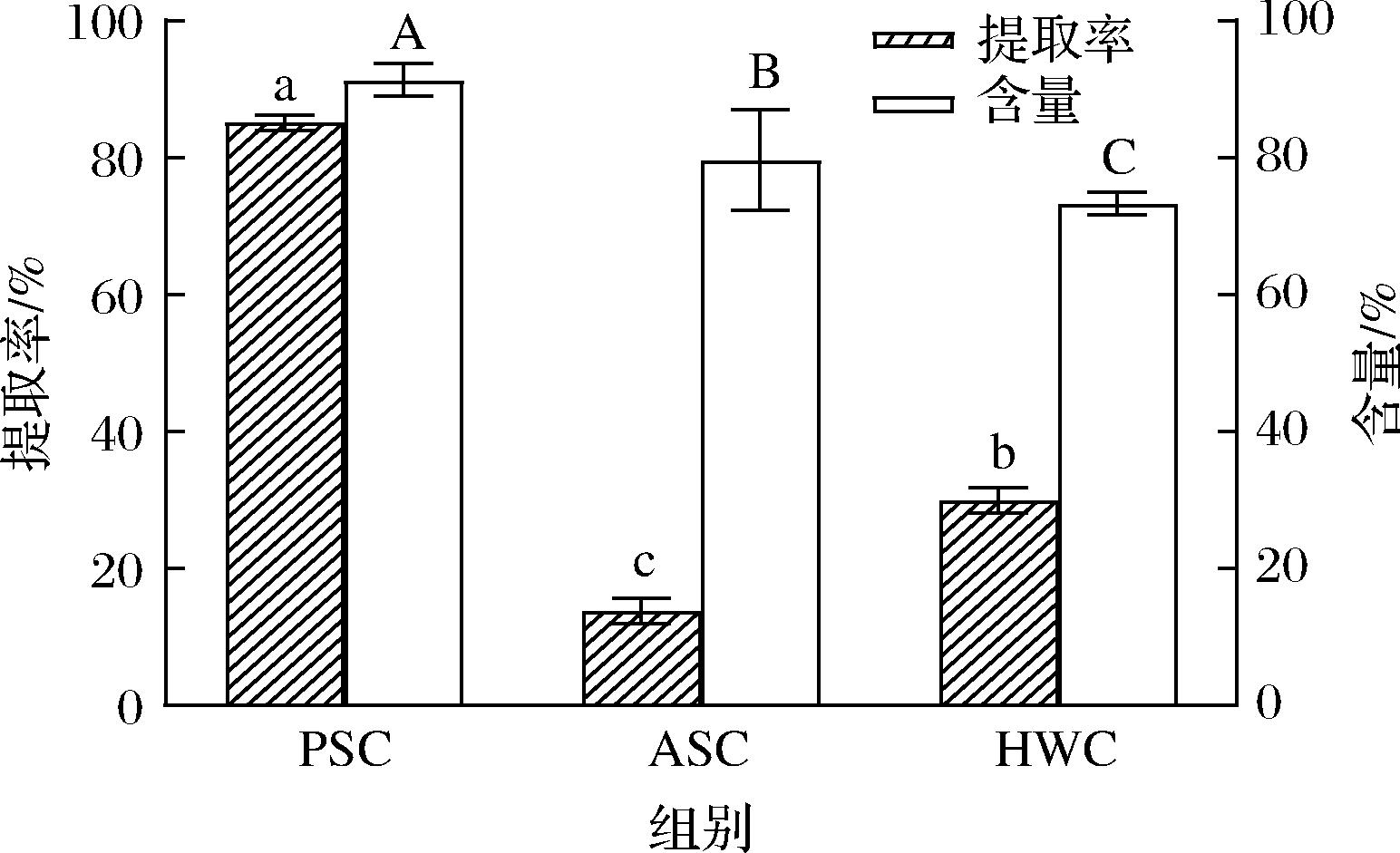
图1 不同方法制备的鲨鱼软骨胶原蛋白提取率及含量
Fig.1 Extraction rate and content of shark cartilage collagen prepared by different methods
注:不同字母表示功能特性差异显著(P<0.05)(下同)。
2.2 不同方法制备的胶原蛋白的结构表征
2.2.1 UV分析
由图2所示,通过3种不同提取工艺获得的胶原蛋白样品,其紫外光谱均显示出胶原特征性三螺旋构象对应的吸收峰(234 nm左右),符合Ⅱ型胶原蛋白特征。且在250~280 nm处均没有明显吸收峰,即芳香族氨基酸含量相对较少,表明所制备的样品杂蛋白较少。
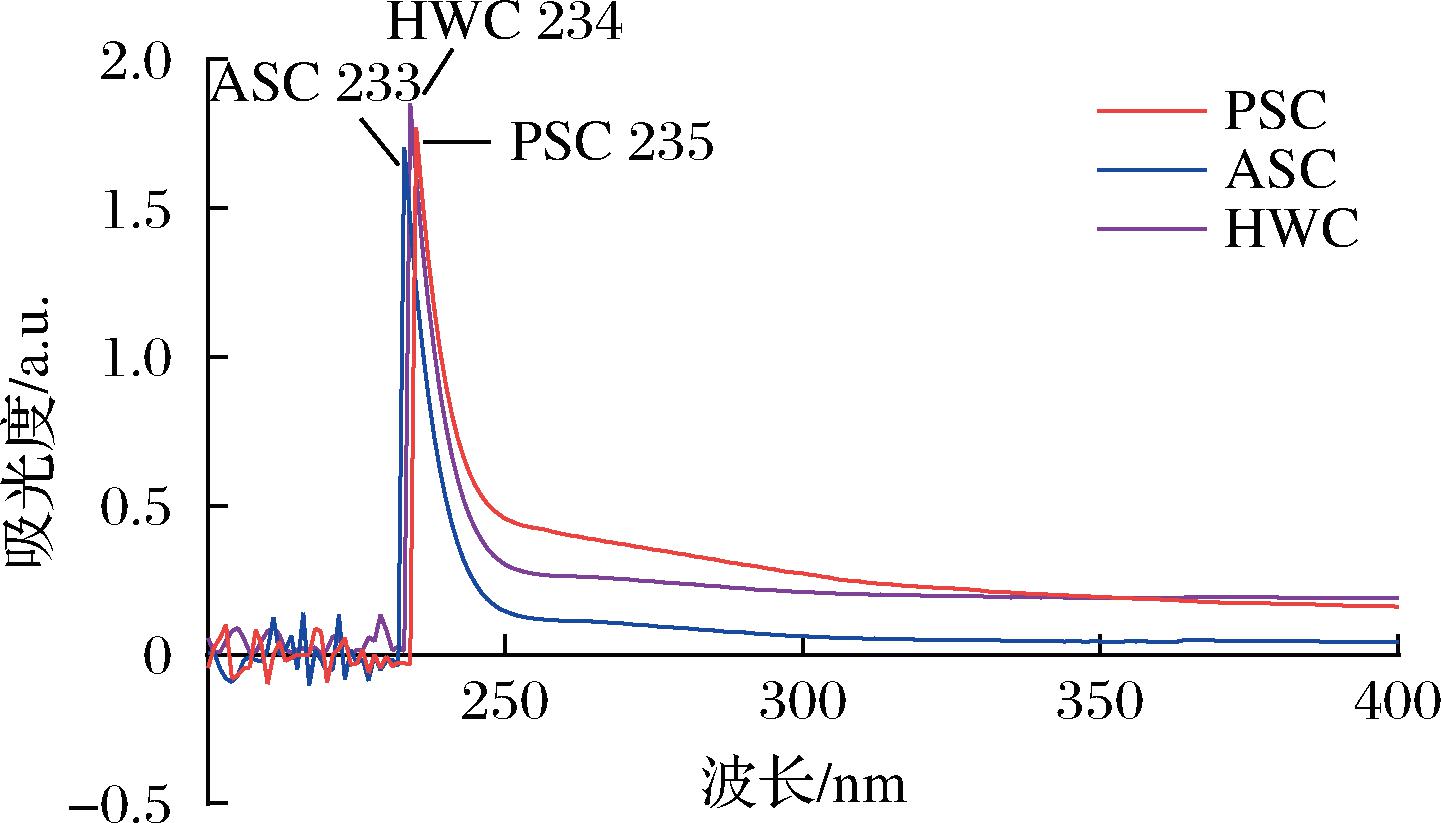
图2 不同方法制备的鲨鱼软骨胶原蛋白的UV图
Fig.2 Ultraviolet spectra of shark cartilage collagen prepared by different method
2.2.2 FT-IR分析
由图3-a可看出,所制备的PSC、ASC和HWC均有酰胺A、B、Ⅰ、Ⅱ和Ⅲ这 5个胶原蛋白特征吸收峰。其中酰胺A带的吸收峰常出现在3 450~3 400 cm-1处[19],PSC、ASC、HWC的酰胺A带分别位于3 346、3 356、3 426 cm-1,表明3种方法制备的胶原蛋白均具有氢键;PSC、ASC、HWC分别在酰胺B带2 927、2 937、2 925 cm-1有吸收峰,是由—CH2、—CH3 和C—H的不对称拉伸振动所引起的,表明三螺旋结构均未受到破坏[20]。酰胺Ⅰ和Ⅱ主要在1 700~1 600 cm-1及1 600~1 500 cm-1处出现吸收峰,酰胺Ⅰ吸收峰与C![]() O伸缩振动及N—H键与胶原分子链β折叠的叠加作用相关[21],酰胺Ⅱ吸收峰与N—H弯曲耦合、C—N伸缩振动有关,吸收峰较强,是蛋白质二级结构变化的敏感区域,而酰胺Ⅲ带可以表征胶原蛋白三螺旋结构的完整性,1 400~1 200 cm-1为N—H的伸缩振动峰和COO-的对称收缩振动峰,由于Ⅱ型胶原蛋白的甘氨酸、羟脯氨酸及脯氨酸含量较高,因此具有其他蛋白质没有的红外光谱特征。PSC、ASC、HWC的酰胺Ⅲ带位于1 240、1 241 、1 258 cm-1,酰胺Ⅲ带和1 450 cm-1附近吸收峰的强度比值越接近1,说明所提取的鲨鱼软骨胶原蛋白的三螺旋结构就越完整[22],PSC、ASC、HWC的比值分别为0.95、0.94、0.88,表明酸法和酶法提取可较好保留胶原蛋白三螺旋结构的完整性。
O伸缩振动及N—H键与胶原分子链β折叠的叠加作用相关[21],酰胺Ⅱ吸收峰与N—H弯曲耦合、C—N伸缩振动有关,吸收峰较强,是蛋白质二级结构变化的敏感区域,而酰胺Ⅲ带可以表征胶原蛋白三螺旋结构的完整性,1 400~1 200 cm-1为N—H的伸缩振动峰和COO-的对称收缩振动峰,由于Ⅱ型胶原蛋白的甘氨酸、羟脯氨酸及脯氨酸含量较高,因此具有其他蛋白质没有的红外光谱特征。PSC、ASC、HWC的酰胺Ⅲ带位于1 240、1 241 、1 258 cm-1,酰胺Ⅲ带和1 450 cm-1附近吸收峰的强度比值越接近1,说明所提取的鲨鱼软骨胶原蛋白的三螺旋结构就越完整[22],PSC、ASC、HWC的比值分别为0.95、0.94、0.88,表明酸法和酶法提取可较好保留胶原蛋白三螺旋结构的完整性。
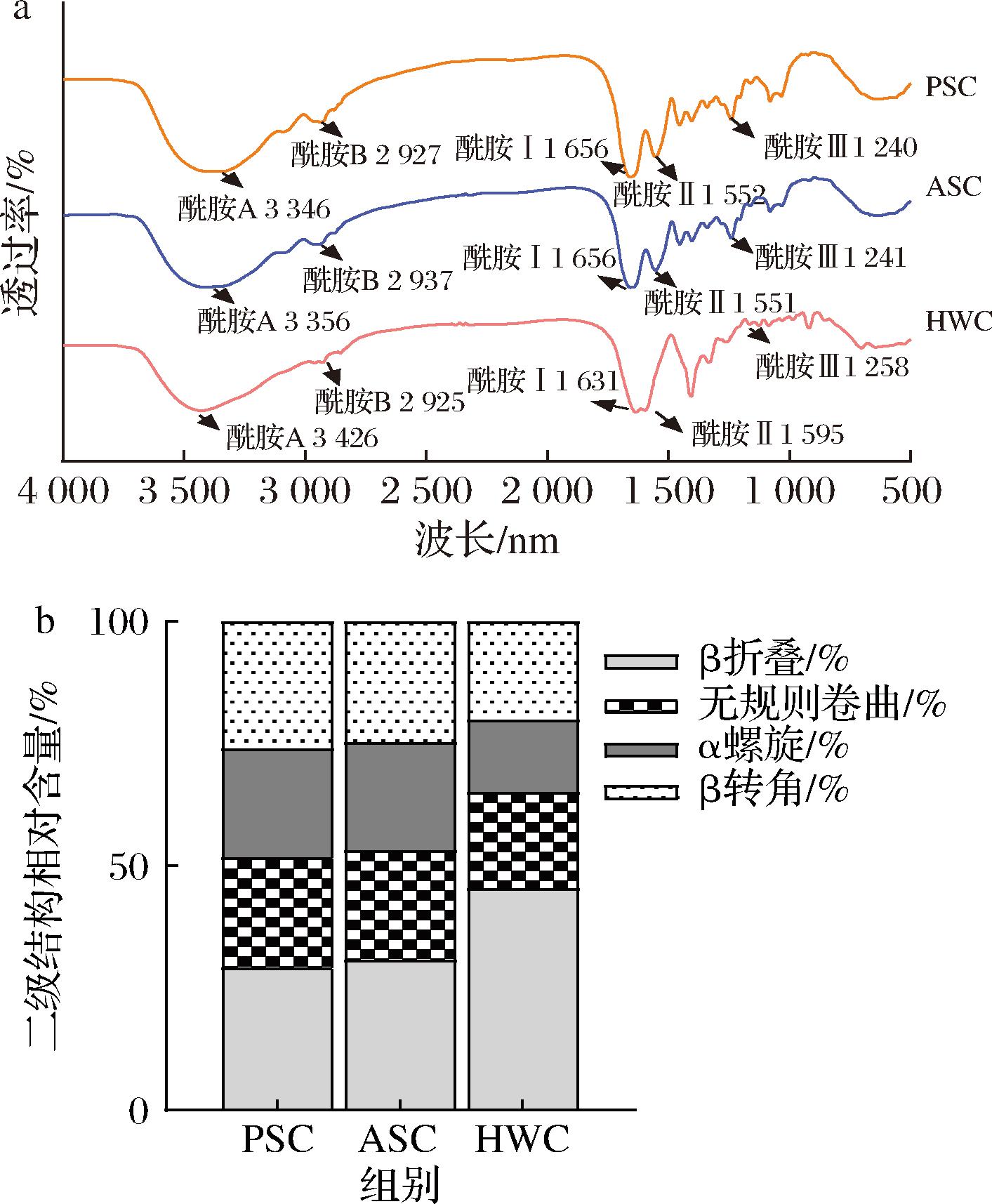
a-FT-IR;b-二级结构相对含量
图3 不同方法制备的鲨鱼软骨胶原蛋白的FT-IR及二级结构相对含量
Fig.3 Infrared absorption spectra and relative contents of secondary structures of shark cartilage collagen prepared by different methods
由图3-b可知,PSC和ASC二级结构组成较为相似。而ASC由于乙酸的加入,与胶原蛋白竞争氢键,破坏了原有的氢键网络,使二级结构中的α螺旋和β折叠结构展开,转变为无规则卷曲结构。PSC中胃蛋白酶能与胶原蛋白产生特异性作用,在酶解过程中,识别并切断胶原蛋白分子中的特定肽键,导致二级结构发生变化。HWC可能是由于提取温度过高,使得部分α螺旋结构的稳定性被破坏,从而发生裂解现象。
2.2.3 CD分析
由图4可知,PSC、ASC、HWC在221 nm存在较弱的正吸收峰,胶原蛋白特殊的重复序列结构导致其具有光学活性,β折叠及无规则卷曲的叠加吸收会形成聚脯氨酸构型肽链,即典型的胶原蛋白CD特征[9]。CD中的正吸收峰与负吸收峰强度之比,能够有效判别胶原蛋白的三螺旋结构。其中,正吸收峰的强度可直观体现Ⅱ型胶原蛋白三螺旋结构的完整程度[23]。当Ⅱ型胶原蛋白的三螺旋结构被完全破坏时,正吸收峰可能会消失,负吸收峰会出现显著的红移现象。对于发生部分变性的蛋白质而言,其正吸收峰不仅会发生红移,且强度也会急剧降低,PSC、ASC、HWC的负吸收峰分别在199、198、198 nm处,其中PSC的比值最大,HWC最小,表明PSC能够更好保持其三螺旋结构。
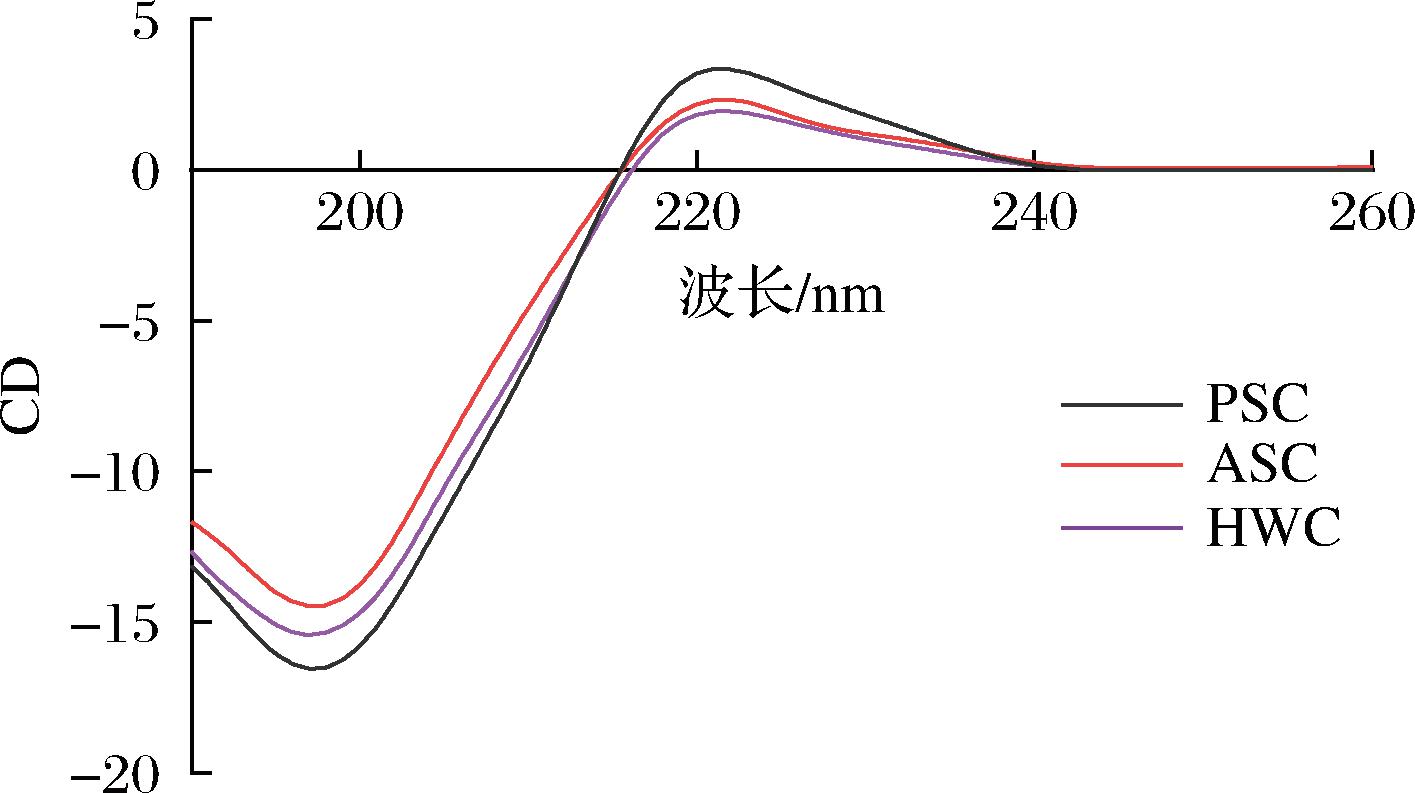
图4 不同方法制备的鲨鱼软骨胶原蛋白的CD图
Fig.4 Circular dichroic spectrum of shark cartilage collagens prepared by different methods
2.2.4 SDS-PAGE分析
如图5所示,PSC和ASC的亚基组成及分布趋势基本一致,都含有β(250 kDa)和α(130 kDa)2条链,符合Ⅱ型胶原蛋白的结构特征。此外,图5显示PSC在较低分子质量区间内有一些条带,表明存在一些不同的氨基酸序列。这与车帅等[24]提取中华鲟软骨胶原蛋白结果一致,PSC在<100 kDa的分子质量也有一些条带,可能是由于酶法提取过程中胃蛋白酶的非定向酶切导致部分胶原蛋白肽水解,分子内或分子间形成交联作用,出现不同的氨基酸序列。
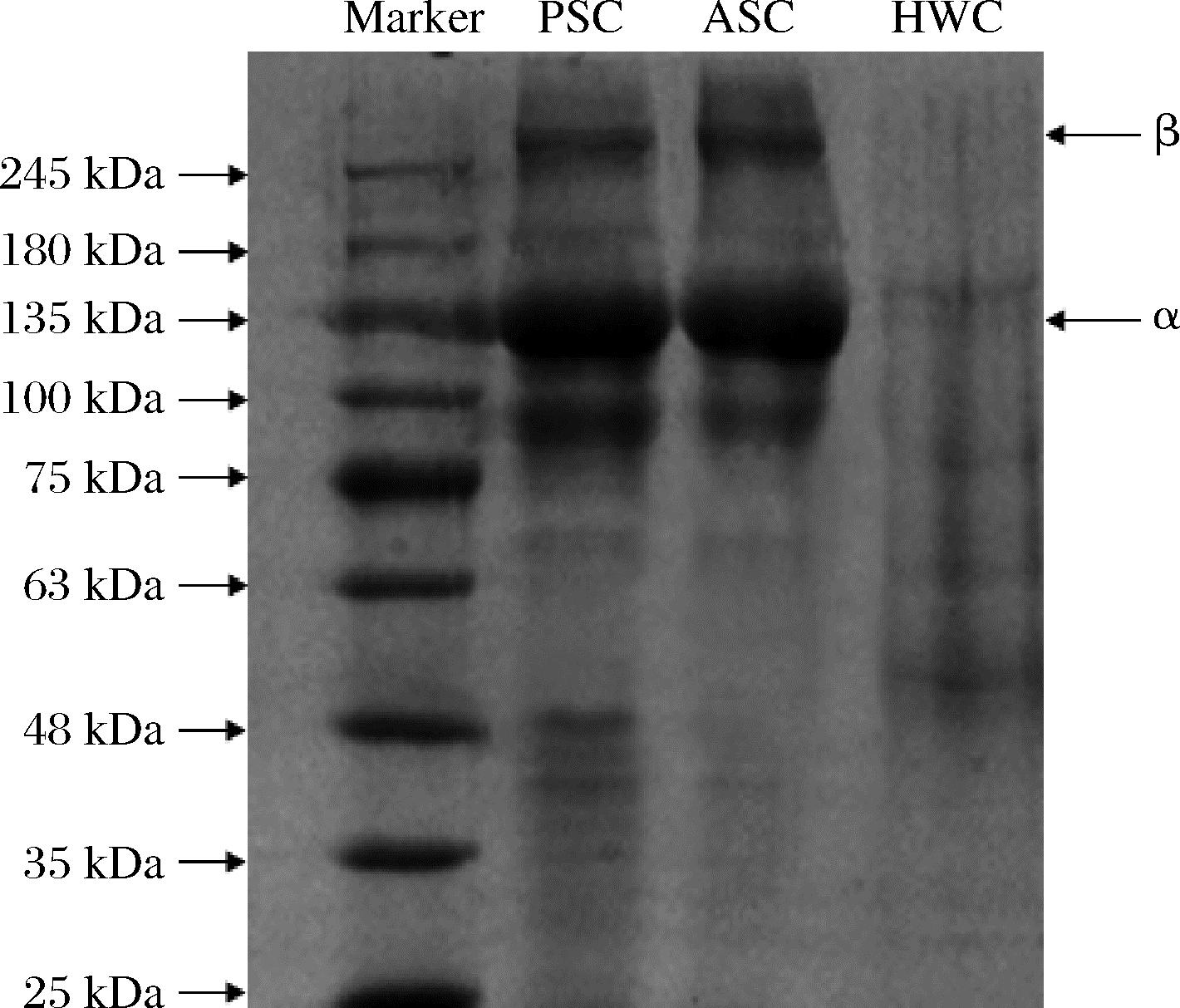
图5 不同方法制备的鲨鱼软骨胶原蛋白的SDS-PAGE图谱
Fig.5 SDS-PAGE map of shark cartilage collagens prepared by different methods
2.2.5 氨基酸分析
由表1可知,鲨鱼软骨PSC、ASC和HWC的氨基酸组成较为相似,但含量略有差异。氨基酸含量最高的是Gly、Pro和Hyp,鲨鱼软骨PSC、ASC和HWC的Gly含量分别为(34.75±2.85)%、(33.76±3.34)%和(32.30±2.74)%,约占氨基酸总量的1/3,Gly对胶原蛋白结构至关重要,其侧链为最小的氢原子,能让3条多肽链紧密排列,形成稳定的三螺旋结构。Pro和Hyp凭借环状结构,限制肽链旋转自由度,使胶原蛋白分子更稳定。该结果与文献报道的金枪鱼骨胶原肽及黑鳍鲨软骨氨基酸组成较为相似[21]。
表1 不同方法制备的鲨鱼软骨胶原蛋白的氨基酸组成及含量 单位:%
Table 1 Amino acid composition and content of shark cartilage collagens prepared by different methods
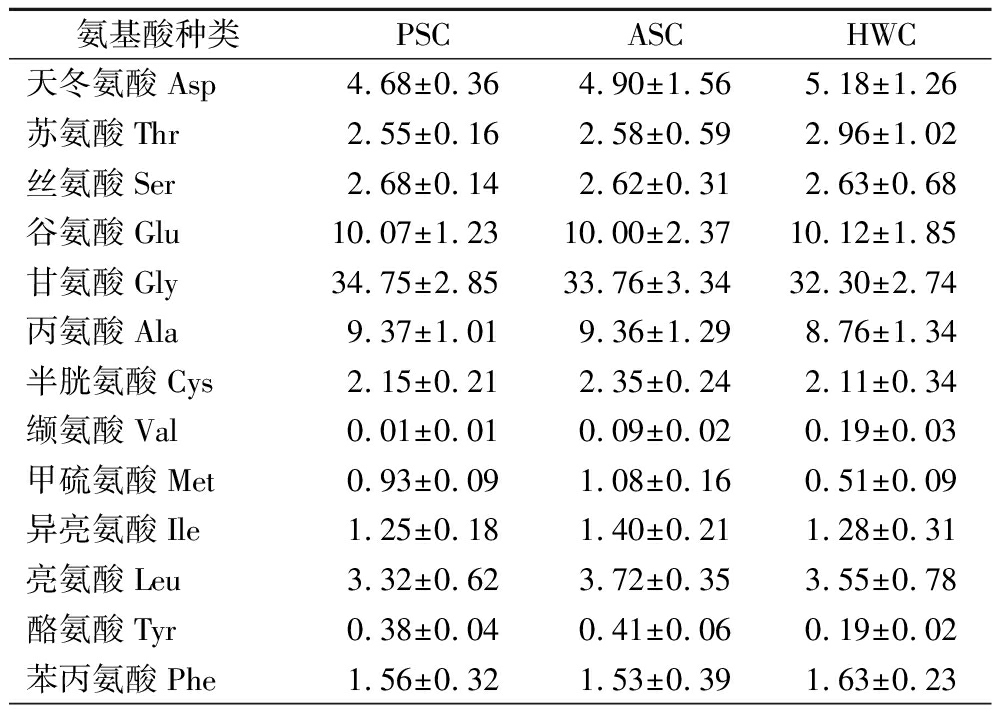
氨基酸种类PSCASCHWC天冬氨酸Asp4.68±0.364.90±1.565.18±1.26苏氨酸Thr2.55±0.162.58±0.592.96±1.02丝氨酸Ser2.68±0.142.62±0.312.63±0.68谷氨酸Glu10.07±1.2310.00±2.3710.12±1.85甘氨酸Gly34.75±2.8533.76±3.3432.30±2.74丙氨酸Ala9.37±1.019.36±1.298.76±1.34半胱氨酸Cys2.15±0.212.35±0.242.11±0.34缬氨酸Val0.01±0.010.09±0.020.19±0.03甲硫氨酸Met0.93±0.091.08±0.160.51±0.09异亮氨酸Ile1.25±0.181.40±0.211.28±0.31亮氨酸Leu3.32±0.623.72±0.353.55±0.78酪氨酸Tyr0.38±0.040.41±0.060.19±0.02苯丙氨酸Phe1.56±0.321.53±0.391.63±0.23
续表1
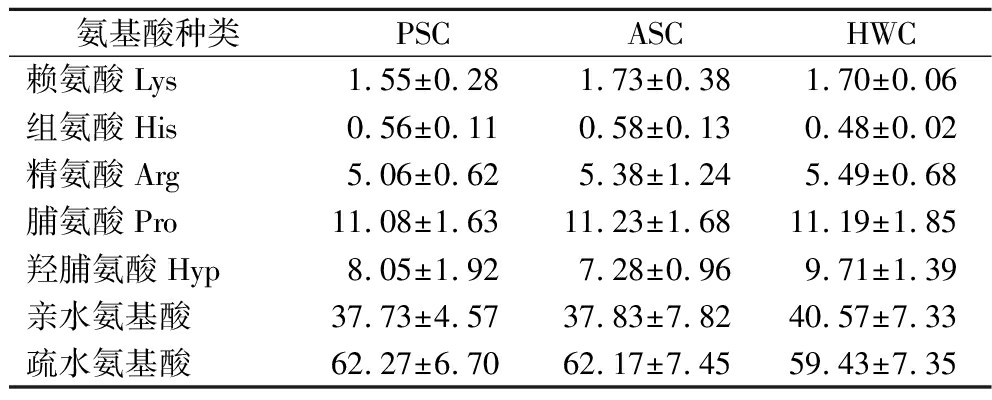
氨基酸种类PSCASCHWC赖氨酸Lys1.55±0.281.73±0.381.70±0.06组氨酸His0.56±0.110.58±0.130.48±0.02精氨酸Arg5.06±0.625.38±1.245.49±0.68脯氨酸Pro11.08±1.6311.23±1.6811.19±1.85羟脯氨酸Hyp8.05±1.927.28±0.969.71±1.39亲水氨基酸37.73±4.5737.83±7.8240.57±7.33疏水氨基酸62.27±6.7062.17±7.4559.43±7.35
2.2.6 DSC分析
如图6所示,Td是加热后胶原蛋白的热变性温度,PSC、ASC、HWC的Td分别为39.9、38.7、45.1 ℃。胶原蛋白Td与亚氨基酸(Pro和Hyp)含量有关,含量越高,胶原蛋白的热稳定性越高[14],由表1氨基酸组成分析得出,PSC、ASC和HWC的亚氨基酸含量分别占19.13%、18.51%和20.9%,这与图6中结果一致,热稳定性从高到低依次为HWC、PSC、ASC。此外,胶原蛋白热稳定性也与原材料的物种、生长环境等因素有关。鲨鱼主要生活在0~1 300 m的海水域中,其Td略高于深海鱼和冷水鱼,陆生动物的胶原蛋白比水生动物的胶原蛋白具有更好的热稳定性,如陆生生物鸡胸骨软骨Td(45.51 ℃)比大眼金枪鱼骨(32.3 ℃)高[19]。
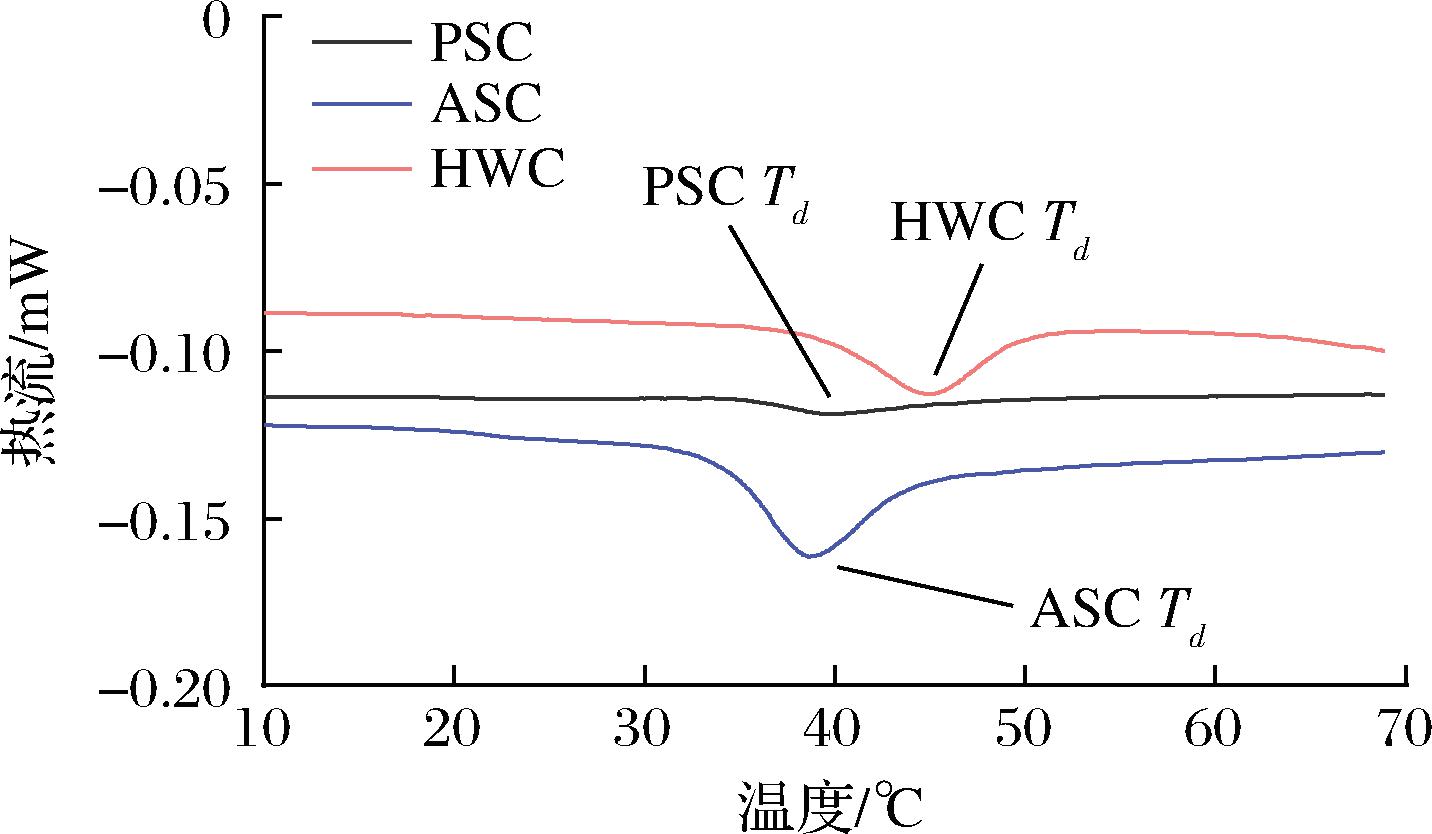
图6 不同方法制备的鲨鱼软骨胶原蛋白的 DSC曲线
Fig.6 DSC curve of shark cartilage collagens prepared by different methods
2.2.7 SEM分析
由图7可知,PSC和ASC都具有较明显的多层片状以及孔状结构,其中PSC提取的胶原蛋白结构分布相对均匀,HWC交联程度低、结构较为破碎松散,胶原破碎成小分子结构,与HWC相比,PSC和ASC都较好保留了胶原蛋白三螺旋结构。

a-PSC;b-ASC;c-HWC
图7 鲨鱼软骨胶原蛋白SEM图(200×)
Fig.7 SEM images of shark cartilage collagens(200×)
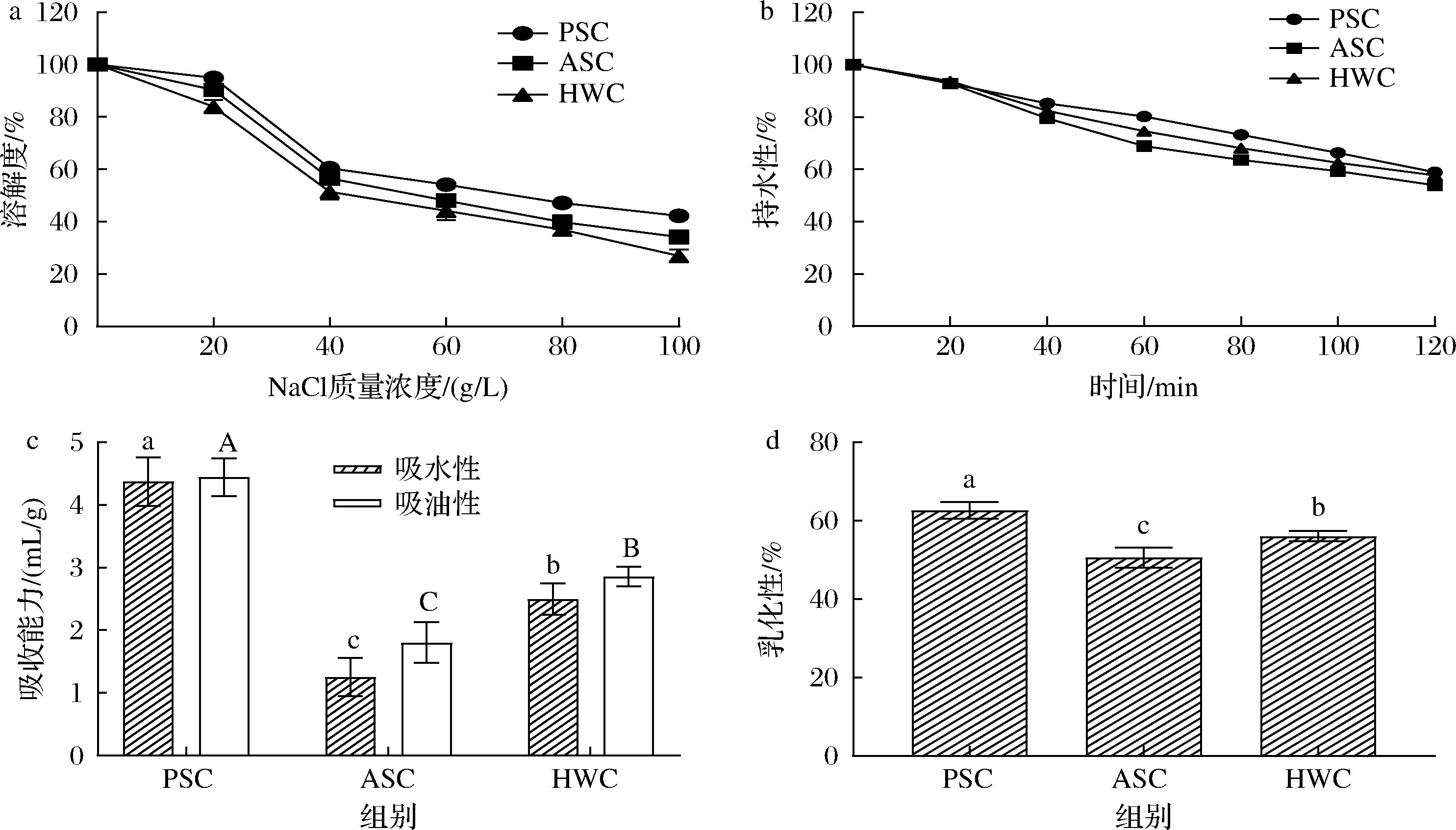
a-溶解度;b-持水性;c-吸水吸油性;d-乳化性
图8 不同制备方法的鲨鱼软骨胶原蛋白的功能特性
Fig.8 Fuctional properties of shark cartilage collagen prepared by different methods
2.3 鲨鱼软骨胶原蛋白的功能特性研究
如图8-a和图8-b所示,随着盐溶液浓度和时间的增加,3种胶原蛋白溶解性和持水性都呈逐渐降低趋势。溶液中离子浓度的增加致使胶原蛋白的表面疏水位点逐渐被暴露,链间疏水作用增大,胶原蛋白的溶解性降低[18]。此外,PSC的持水率最高,可达到(58.93±0.61)%,可能由于酶法提取时,胃蛋白酶特异性地作用于胶原蛋白N端和C端,使得提取的胶原蛋白亲水基团暴露,从而易与水形成氢键[25]。由图8-c和图8-d可知,3种不同提取方法的吸水和吸油能力及乳化性从大到小依次为PSC、HWC和ASC,表明在胃蛋白酶作用下,胶原蛋白链表面疏水基团暴露,打开PSC胶原蛋白分子链间交联,水解成小肽,从而加大与溶剂的相互作用[18]。而HWC可能是由于提取温度使胶原蛋白链更加伸展所致。
3 结论
本研究采用不同的3种方法对鲨鱼软骨胶原蛋白进行制备,其中经酶法制备胶原蛋白其得率达到85.09%,远高于酸法和热水法提取。通过UV、FT-IR、CD、SDS-PAGE、DSC、SEM和氨基酸分析等方法探讨了3种方法制备的鲨鱼软骨胶原蛋白的结构特性,发现所制备鲨鱼软骨胶原蛋白含有大量的甘氨酸、脯氨酸和羟脯氨酸,符合胶原蛋白Gly-X-Y结构,均具有胶原蛋白三螺旋结构的特征吸收峰,为典型的Ⅱ型胶原蛋白结构。其中PSC和ASC所制备的胶原蛋白三螺旋结构更加完整,具有较明显的多层片状结构,而HWC交联程度低、结构较为松散。此外,由于HWC中的脯氨酸和羟脯氨酸的含量较高,其热变性温度最大,其次为PSC和ASC。相较于ASC与HWC,PSC在溶解性、吸水吸油性、持水性以及乳化性等方面表现更好。该研究结果为鲨鱼软骨胶原蛋白资源深度开发与利用提供了一定理论依据。
[1] JAFARI H, LISTA A, SIEKAPEN M M, et al.Fish collagen:Extraction, characterization, and applications for biomaterials engineering[J].Polymers, 2020, 12(10):2230.
[2] LU W C, CHIU C S, CHAN Y J, et al.An in vivo study to evaluate the efficacy of blue shark (Prionace glauca) cartilage collagen as a cosmetic[J].Marine Drugs, 2022, 20(10):633.
[3] LI W, URA K, TAKAGI Y.Industrial application of fish cartilaginous tissues[J].Current Research in Food Science, 2022, 5:698-709.
[4] LE N-L
N-L PEZ A, MORALES-PE
PEZ A, MORALES-PE ALOZA A, MART
ALOZA A, MART NEZ-JU
NEZ-JU REZ V M, et al.Hydrolyzed collagen:Sources and applications[J].Molecules, 2019, 24(22):4031.
REZ V M, et al.Hydrolyzed collagen:Sources and applications[J].Molecules, 2019, 24(22):4031.
[5] AVILA RODR GUEZ M I, RODR
GUEZ M I, RODR GUEZ BARROSO L G, S
GUEZ BARROSO L G, S NCHEZ M L.Collagen:A review on its sources and potential cosmetic applications[J].Journal of Cosmetic Dermatology, 2018, 17(1):20-26.
NCHEZ M L.Collagen:A review on its sources and potential cosmetic applications[J].Journal of Cosmetic Dermatology, 2018, 17(1):20-26.
[6] SEIXAS M J, MARTINS E, REIS R L, et al.Extraction and characterization of collagen from elasmobranch byproducts for potential biomaterial use[J].Marine Drugs, 2020, 18(12):617.
[7] LUO J L, YANG X J, CAO Y, et al.Structural characterization and in vitro immunogenicity evaluation of amphibian-derived collagen type II from the cartilage of Chinese Giant Salamander (Andrias davidianus)[J].Journal of Biomaterials Science, Polymer Edition, 2020, 31(15):1941-1960.
[8] 张武, 应顺莉, 何璐瑶, 等.鲨鱼软骨胶原蛋白的酶法制备及其稳定性研究[J].中国食品学报, 2024, 24(9):234-243.ZHANG W, YING S L, HE L Y, et al.Study on enzymatic preparation and stability of shark cartilage collagen[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(9):234-243.
[9] 胡艺, 郑平安.鲟鱼软骨中Ⅱ型胶原蛋白的提取及其结构鉴定[J].食品安全质量检测学报, 2021, 12(6):2433-2438.HU Y, ZHENG P G.Extraction and structural identification of collagen type Ⅱ from sturgeon cartilage[J].Journal of Food Safety &Quality, 2021, 12(6):2433-2438.
[10] PROKOPOV A, G
A, G L R, MOKREJ
L R, MOKREJ P, et al.Preparation of gelatin from broiler chicken stomach collagen[J].Foods, 2023, 12(1):127.
P, et al.Preparation of gelatin from broiler chicken stomach collagen[J].Foods, 2023, 12(1):127.
[11] ZHU L L, LI J W, WANG Y C, et al.Structural feature and self-assembly properties of type II collagens from the cartilages of skate and sturgeon[J].Food Chemistry, 2020, 331:127340.
[12] SONG Z L, LIU H M, CHEN L W, et al.Characterization and comparison of collagen extracted from the skin of the Nile tilapia by fermentation and chemical pretreatment[J].Food Chemistry, 2021, 340:128139.
[13] 王乐, 李享, 刘文营, 等.清酱肉体外模拟消化后粗肽的抗氧化活性和氨基酸分析[J].中国食品学报, 2021, 21(2):319-326.WANG L, LI X, LIU W Y, et al.Antioxidant activities and amino acid composition of crude peptides extracted from pickled sauced meat after in vitro simulated gastrointestinal digestion[J].Journal of Chinese Institute of Food Science and Technology, 2021, 21(2):319-326.
[14] ATA O, BOZDOGAN N, MATARACI C E, et al.Extraction and characterization of valuable compounds from chicken sternal cartilage:Type II collagen and chondroitin sulfate[J].Food Chemistry, 2025, 462:141023.
[15] 苗会娟, 胡卫国, 徐艳梅, 等.福林酚分光光度法测定蜂毒中总蛋白质[J].化学分析计量, 2022, 31(7):5-8.MIAO H J, HU W G, XU Y M, et al.Determination of total protein in apistoxin by forint phenol spectrophotometry[J].Chemical Analysis and Meterage, 2022, 31(7):5-8.
[16] 蔡路昀, 马帅, 李秀霞, 等.不同提取方法对鲽鱼皮胶原蛋白结构特征和功能性质的影响[J].食品与发酵工业, 2017, 43(5):240-246.CAI L Y, MA S, LI X X, et al.Effects of different extraction methods on structure characteristics and functional properties of collagen from the skin of flounder(Pleuronichthys cornutus)[J].Food and Fermentation Industries, 2017, 43(5):240-246.
[17] ZHANG Y Y, HAN G X, WANG X Y, et al.Effect of tremella polysaccharides on the quality of collagen jelly:Insight into the improvement of the gel properties and the antioxidant activity of yak skin gelatin[J].Journal of the Science of Food and Agriculture, 2024, 104(11):6809-6820.
[18] 韩霜, 马良, 王雪蒙, 等.兔皮胶原蛋白的加工特性[J].食品科学, 2017, 38(5):21-25.HAN S, MA L, WANG X M, et al.Processing characteristics of rabbit skin collagen[J].Food Science, 2017, 38(5):21-25.
[19] AHMED R, HAQ M, CHUN B S.Characterization of marine derived collagen extracted from the by-products of bigeye tuna (Thunnus obesus)[J].International Journal of Biological Macromolecules, 2019, 135:668-676.
[20] ZHU B W, DONG X P, ZHOU D Y, et al.Physicochemical properties and radical scavenging capacities of pepsin-solubilized collagen from sea cucumber Stichopus japonicus[J].Food Hydrocolloids, 2012, 28(1):182-188.
[21] 魏永泽, 周娟, 陈敬华.非变性Ⅱ型胶原蛋白提取工艺优化及质量验证[J].食品科技, 2024, 49(6):194-203.WEI Y Z, ZHOU J, CHEN J H.Extraction process optimization and quality verification of undenatured type Ⅱ collagen[J].Food Science and Technology, 2024, 49(6):194-203.
[22] 舒聪涵. 金枪鱼骨胶原肽及其钙螯合物对成骨细胞的活性影响研究[D].舟山:浙江海洋大学, 2021.SHU C H.Effect of tuna bone collagen peptides and its calcium chelates on osteoblasts activity[D].Zhoushan:Zhejiang Ocean University, 2021.
[23] 许蓉, 郑淋, 赵谋明.温度和pH值对鸡胸软骨Ⅱ型胶原蛋白的结构、黏度和热稳定性的影响[J].食品科学, 2020, 41(14):66-71.XU R, ZHENG L, ZHAO M M.Effect of temperature and pH on the structure, viscosity and thermal stability of type Ⅱ collagen from chicken cartilage[J].Food Science, 2020, 41(14):66-71.
[24] 车帅, 杜芬, 刘楚怡, 等.中华鲟软骨Ⅱ型胶原蛋白的结构分析[J].食品工业科技, 2018, 39(4):60-63.CHE S, DU F, LIU C Y, et al.The structure analysis of type Ⅱ collagen from sturgeon (Acipenser sinensis) cartilage[J].Science and Technology of Food Industry, 2018, 39(4):60-63.
[25] 张晓頔. 鱼糜加工副产物水解物改善鱼糜品质及机制研究[D].杭州:浙江工商大学, 2022.ZHANG X D.Study on the of Improving the surimi quality and mechanism of surimi by-product protein hydrolysate[D].Hangzhou:Zhejiang Gongshang University, 2022.