普洱茶作为源自云南的典型后发酵茶,其独特品质与复杂风味的形成与地域环境和微生物群落的共同作用密切相关[1]。近年来,随着“景迈山普洱茶文化景观”被列入联合国教科文组织人类非物质文化遗产名录,普洱茶所承载的区域性知识体系和微生态特征日益受到重视。已有研究表明,景迈山等普洱茶核心产区的微生物群体,尤其是来源于根际或窖藏环境的功能菌株,在发酵过程中通过参与茶多酚转化、风味物质生成等代谢途径,深度介入了普洱茶品质的形成机制[2-3]。
近年来,随着分子生物学和高通量测序技术的发展,茶叶相关微生物研究不断深入。除传统分离培养法外,宏基因组、转录组及代谢组等组学手段已被广泛应用于茶叶发酵和贮藏微生物群落结构及功能研究中[4]。其中,基因组测序可系统揭示目标微生物的遗传潜力和代谢机制,为理解其生态功能提供重要基础。目前,在普洱茶发酵相关的微生物研究中,主要关注于黑曲霉、酵母菌等真菌类群,以及芽孢杆菌等细菌类群,这些被认为是主导发酵的优势微生物,而对次优势或低丰度但可能具有重要功能作用的菌株仍缺乏深入研究,限制了对微生物驱动茶叶品质演化机制的全面认识。
马赛菌属(Massilia)隶属于β-变形菌纲,氧化酶阳性、芽孢阴性、运动性强,常见于植物根际土壤、有机质丰富环境及污染修复系统中,部分菌株表现出对有机酸、芳香族化合物的降解能力及对植物生长的促进作用[5-7]。已有文献报道,Massilia属细菌能够参与碳源代谢、抗氧化应激反应、信号分子合成及微生物互作,在复杂环境中具有较强的生存和生态适应能力[8]。尽管Massilia属细菌在环境微生态系统中的作用已获得初步认识,但其在普洱茶窖藏环境中的分布情况及功能尚未被系统研究,尤其是其在有机物降解和代谢路径上的具体作用机制仍属空白。
本研究从普洱茶窖藏土样中分离获得1株具有降解潜力的马赛菌新菌株,命名为Massilia puerhi SJY3T[9]。为深入揭示该菌株的功能特征及其在普洱茶窖藏过程中的潜在生态作用,本研究采用Illumina PE150高通量测序平台对Massilia puerhi SJY3T进行全基因组测序,并GO、直系同源簇(Cluster of Orthologous Groups,COG)和KEGG等数据库进行功能注释与代谢通路分析。结合普洱茶贮藏过程中有机质降解与转化的需求,研究Massilia puerhi SJY3T的代谢功能,可为阐明其在茶叶转化中的作用机制提供理论依据。进一步分析其基因组中涉及碳代谢、芳香化合物降解、氧化还原反应等相关基因的组成与分布,有助于揭示该菌株在维持微生态稳定、促进茶叶化学成分重构中的潜在功能。
综上所述,本研究通过对Massilia puerhi SJY3T基因组结构与功能的系统解析,旨在揭示该菌株在普洱茶窖藏环境中的潜在功能。同时,本研究期望为开发利用Massilia菌株作为普洱茶窖藏微生物发酵剂或定向发酵菌剂提供理论支持,并为进一步优化普洱茶窖藏发酵工艺及推动微生物资源的应用提供数据参考与科学依据。
1 材料与方法
1.1 材料与试剂
本研究所用菌株Massilia puerhi SJY3T由云南农业大学食品科学与技术学院食药同源团队从普洱茶窖藏土壤中分离、筛选,并经过生理生化特性分析和16SrRNA基因序列鉴定,现保藏于中国普通微生物菌种保藏管理中心。R2A肉汤培养基,英国OXOID公司;甘油(纯度≥99%)、琼脂糖、十二烷基硫酸钠(SDS,纯度 99.5%),Biosharp 公司;基因组DNA提取试剂盒、PCR 纯化试剂盒,美国 OMEGA 公司;pMD18-T 载体,TaKaRa 公司;其余试剂均为国产分析纯级产品。
1.2 仪器与设备
TGL-16MJ高速冷冻离心机,上海卢湘仪离心机仪器有限公司;FA224C电子分析天平,上海辰邦西仪器科技有限公司;CR-100S超声波清洗机,深圳市春霖清洗设备有限公司;HYC-310S冷藏箱,青岛海尔生物医疗股份有限公司;Q33226 Thermo Qubit 4.0荧光定量仪、Qubit® 2.0荧光计,美国 Thermo Fisher Scientific 公司;DNA分析仪,美国 Applied Biosystems 公司。
1.3 实验方法
1.3.1 测序样品制备
将保存于-80 ℃、含15%(体积分数)甘油的Massilia puerhi SJY3T菌株悬液接种于R2A培养基中,27 ℃静置培养72 h。培养后取菌液,经生理盐水处理后,迅速冷冻保存于-80 ℃超低温冰箱备用。
1.3.2 基因组测序
基因组DNA提取采用改良的SDS法进行。提取后的DNA通过琼脂糖凝胶电泳检测质量,并使用Qubit® 2.0荧光计进行定量。库构建采用Illumina的NEBNext® UltraTM DNA Library Prep Kit(NEB,美国)制备。基因组组装分别使用SOAPdenovo、SPAdes、ABySS软件进行。
基因组功能预测包括编码基因、重复序列、非编码RNA、基因组岛、转座子、原噬菌体和(clustered regularly interspaced short palindromic repeat,CRISPR)序列等成分。编码基因预测采用GeneMarkS软件,并筛选完整的编码序列(coding sequences,CDS);散布重复序列预测使用RepeatMasker;tRNA基因通过tRNAscan-SE进行预测;rRNA基因由rRNAmmer分析获得;小核RNA(snRNA)通过BLAST比对Rfam数据库进行鉴定;基因组岛预测使用IslandPath-DIMOB程序;原噬菌体序列由PHAST工具分析;CRISPR序列预测则基于CRISPRfinder程序,基因组编码蛋白质序列经提取后,分别在GO、KEGG及COG数据库中进行BLAST检索,筛选标准为E<10-5、最小比对长度比例大于40%次级代谢基因簇的挖掘使用antiSMASH工具进行分析。此外,针对潜在致病性及耐药性特征,分别通过PHI-base(Pathogen Host Interaction Database)、VFDB(Virulence Factors Database)及ARDB(Antibiotic Resistance Genes Database)进行进一步注释分析。碳水化合物活性酶基因的预测基于CAZy数据库进行。所有测序工作由北京诺禾致源科技股份有限公司采用Illumina NovaSeq PE150平台完成。
1.4 数据处理
基因组注释结果以m8格式文件生成,并上传至NCBI数据库(https://www.ncbi.nlm.nih.gov),基因组序列已提交至GenBank,登录号为WOFW00000000。测序数据通过自编脚本分析测序深度、GC含量分布、GC-skew及基因组结构特征,并使用Proksee平台(https://proksee.ca)绘制基因组环形图。其他图表绘制由微生信平台(http://www.bioinformatics.com.cn)完成。
2 结果分析
2.1 基因组组装与预测结果
采用IIIumina PE150测序平台对Massilia puerhi SJY3T菌株进行全基因组测序。测序及组装结果显示,该菌株的基因组总长度为5 965 570 bp;平均GC含量为66.77%,GC含量作为微生物核酸序列组成的重要特征之一,常被用以推测其系统发育关系。有研究表明,细菌的GC含量与其最适生长温度呈正相关关系,较高的GC含量有助于增强细菌在高温环境下维持基因组的稳定性[10]。此外,土壤微生物群落中细菌的基因组大小及GC含量也受到土壤环境因素的显著影响,这与其代谢多样性及环境适应性密切相关[11]。因此,Massilia puerhi SJY3T较高的GC含量可能表明该菌株具有较强的环境适应能力和广泛的代谢潜力,为进一步挖掘其碳代谢、抗逆机制及次生代谢相关基因提供了基础信息。基因组编码基因预测结果显示,Massilia puerhi SJY3T基因组中共注释到5 220个CDS,编码基因总长度为5 243 352 bp,平均基因长度为1 004 bp,占基因组总长度的87.89%,编码区的GC含量与全基因组一致,亦为66.77%。此外,基因组分析还识别出若干具有潜在功能意义的结构元素,包括散在分布成簇规律间隔短回文重复序列、潜在原噬菌体区域及26个基因组岛。该菌株的完整基因组序列及16SrRNA基因序列已分别提交至GenBank数据库,对应登录号分别为WOFW00000000和MN014073。
在非编码RNA的注释方面,共鉴定出66个tRNA基因,涵盖20种氨基酸,其中以亮氨酸相关tRNA基因数量最多(8个),其次为精氨酸(7个)、丝氨酸(5个)、苏氨酸(5个)和甘氨酸(5个)。在Massilia puerhi SJY3T中,tRNA基因的组成和丰度可能与其降解功能和环境耐受性密切相关,值得在后续研究中进一步探讨其潜在的生物学意义,其具体功能尚需通过进一步实验研究加以阐明。
2.2 基因组圈图分析
利用Proksee在线平台绘制了Massilia puerhi SJY3T的基因组圈图,如图1所示。基因组圈图能够全面展示基因组的结构特征和功能元件的空间分布。便于深入理解该菌株的基因组组成,圈图由外至内依次呈现多个功能层次信息,第一圈(最外圈)用于展示基因组的主要功能元件。其中,紫色区域表示编码蛋白质的基因(CDS)、橙色表示转运RNA基因(tRNA)、青色表示核糖体RNA基因(rRNA)。CDS为编码蛋白质的主要功能单元;tRNA在翻译过程中转运氨基酸至核糖体;rRNA构成核糖体的核心结构部分,是蛋白质合成的关键组成。第二圈和第三圈分别展示正链(+链)与负链(-链)上的CDS分布。第二圈为外向紫色条带,代表位于正链上的基因,其转录方向与基因组复制方向一致;第三圈为内向紫色条带,代表负链上的基因,转录方向与复制方向相反。这2层结构有助于揭示双链DNA中基因分布的偏好性,并辅助识别潜在的基因簇、转录单元或链特异性调控区域。第四圈包括2部分信息:黑色波动线表示GC含量变化,通过滑动窗口(如1 Mb)计算GC碱基比例,其高度反映局部GC含量的高低;浅绿色区域表示GC Skew+正链的 (G-C)/(G+C),用于衡量鸟嘌呤(G)相对于胞嘧啶(C)的富集程度,正值表示G在正链富集。第五圈为深紫色,表示GC Skew-负链的(C-G)/(G+C),反映C在负链上的富集情况。GC Skew分析常用于识别复制起始位点与终止位点等重要基因组特征。最内圈为基因组物理位置的刻度标尺,标注从基因组起始点(通常设定为0 Mb)起的累计碱基对长度。总体而言,基因组圈图作为一种集成化可视分析工具,能够全面展示Massilia puerhi SJY3T基因组的结构组成与功能特征,为后续的功能基因挖掘及基因组比较研究提供了重要参考。
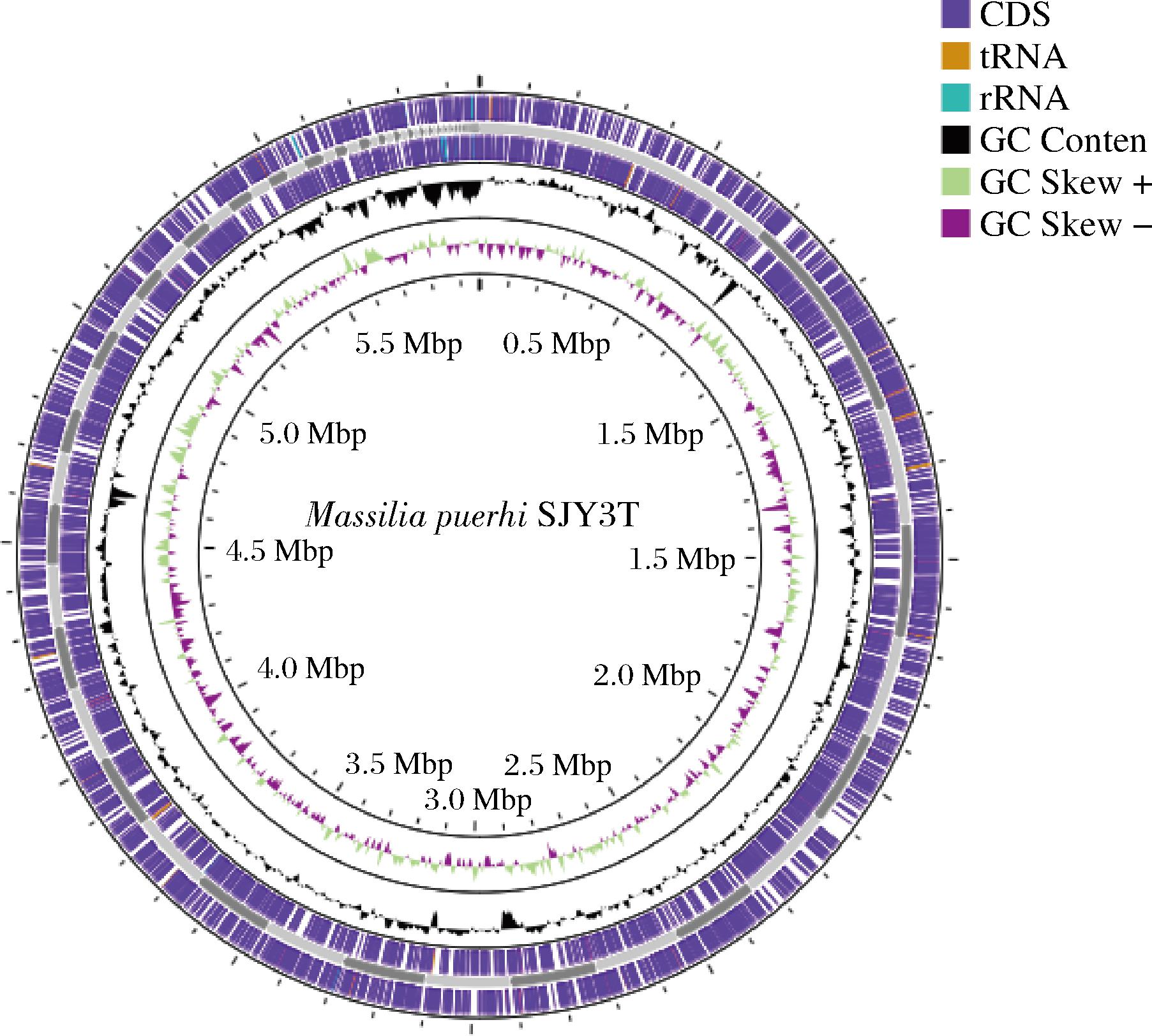
图1 Massilia puerhi SJY3T基因组圈图
Fig.1 Massilia puerhi SJY3T genome circle map
2.3 基因组功能注释
2.3.1 GO功能注释
采用IPRscan软件将Massilia puerhi SJY3T的基因组编码基因序列与GO数据库进行比对注释,结果如图2所示。注释结果表明,共有3 382个基因获得了GO注释,占总编码基因数量(5 220个)的64.79%。在GO的3个主要功能类别中,与细胞组成相关的基因数量为2 504个,与生物过程相关的基因为7 327个,与分子功能相关的基因为4 060个(由于GO分类体系中一个基因可同时注释至多个功能条目,因此总数可能超过实际基因数目)。在3个大类中,进一步可细分为44个二级功能类别。在生物过程大类的24个二级类别中,代谢过程和细胞过程占比最高,分别有1 772、1 737个基因;此外,被注释到生物调节、生物过程调控、定位、定位活性、刺激反应、信号传导、细胞组织部分或生物合成的基因数量也比较多。在细胞组分大类的11个二级分类中,细胞和细胞部分占比最高,均有997个基因,其次是细胞器、高分子复合物、细胞器部分。而在分子功能大类中有9个二级分类,占比最高的是催化活性,有1 720个基因,其次是结合活性和分子转导活性、核酸结合转录因子活性。基于GO功能注释结果推测,Massilia puerhi SJY3T可能在普洱茶窖藏发酵过程中具有一定的有机物降解能力。多个被注释为氧化还原酶(GO:0016491)、甲基转移酶(GO:0008168)和酯酶(GO:0016788)的基因,可能在茶叶成分的生化转化中发挥作用。有研究表明,氧化还原酶可参与木质纤维素的降解过程,促进复杂有机物的分解[12]。罗芳[13]研究发现,水稻中的甲基转移酶基因在应对除草剂阿特拉津胁迫时被诱导表达,参与了对该化合物的降解。此外,刘艳艳等[14]从土壤宏基因组中克隆获得一种新型酯酶基因est924,发现其产物可降解多种邻苯二甲酸酯类环境污染物,提示微生物源酯酶在环境污染治理中的潜在应用价值。综上,GO注释结果不仅揭示了Massilia puerhi SJY3T的主要功能特征,也为进一步探索其在生态系统碳循环、污染降解和食品发酵等方面的潜在功能提供了基础信息。
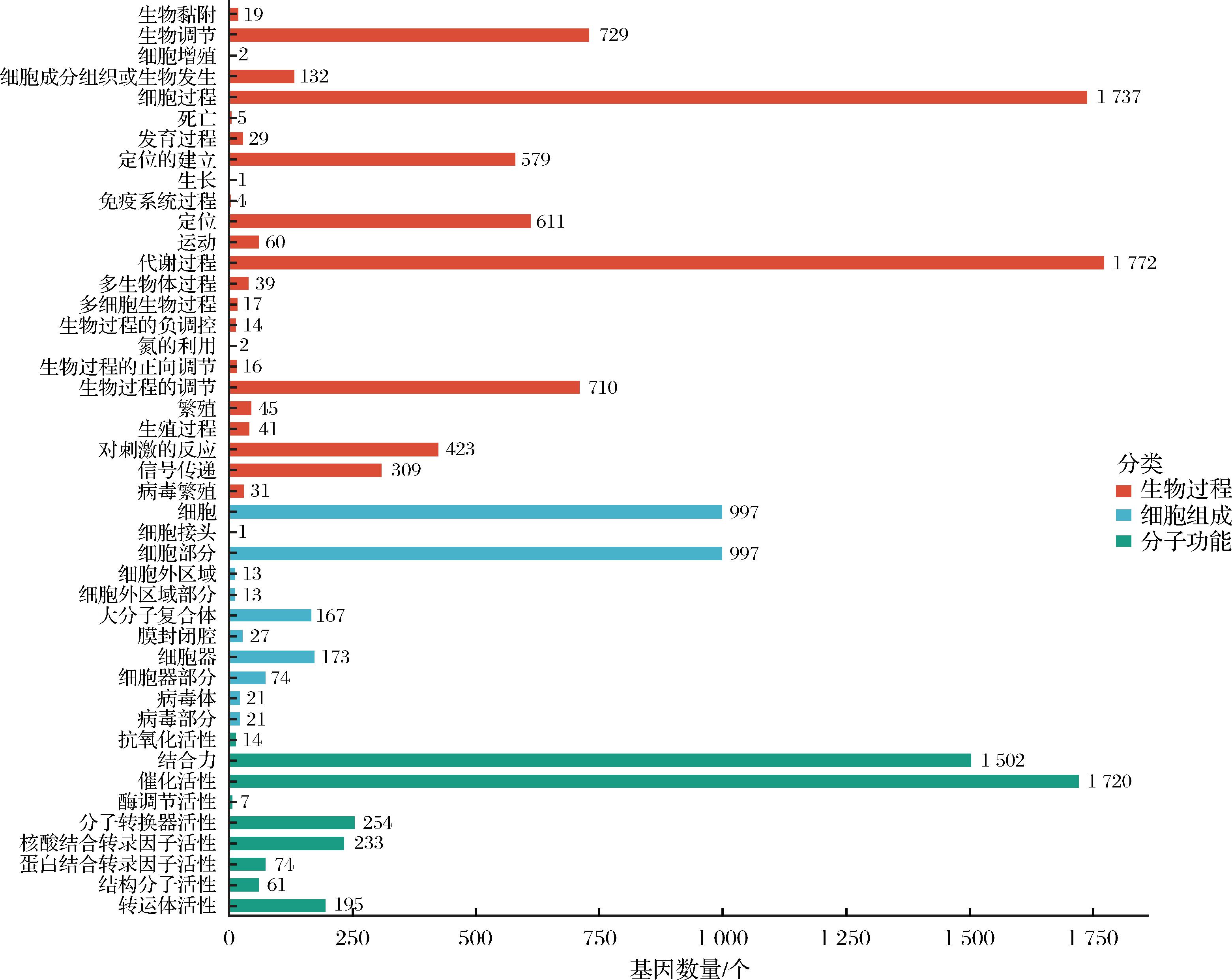
图2 Massilia puerhi SJY3T的GO功能分类
Fig.2 GO functional classification of Massilia puerhi SJY3T
2.3.2 COG功能注释
采用Diamond软件将Massilia puerhi SJY3T的氨基酸序列与COG数据库进行比对,从而获得各基因的功能注释信息,结果如图3所示,共有3 799个编码基因被成功注释至COG分类系统,占总基因数的72.78%。根据功能分类,这些基因分布于25个不同的功能类别中。在各功能类别中,注释基因数量较多的主要包括:R类:一般功能预测,415个;T类:信号转导机制,389个;K类:转录,356个;E类:氨基酸转运与代谢,279个;M类:细胞壁/膜/包膜的生物合成,278个;C类:能量生成和转化,277个。这些高丰度的功能类别反映出Massilia puerhi SJY3T在信号感应、物质代谢和细胞结构合成等方面具有较为复杂的功能体系,可能与其环境适应能力及代谢多样性密切相关。此外,与有机物降解相关的功能基因在该菌株中也得到了注释,共计54个。其中,包括与以下代谢过程相关的基因:氨基酸代谢10个;碳水化合物代谢21个;脂质代谢13个;次生代谢产物降解10个。这些基因同时在KEGG数据库中得到了相应通路的注释,进一步支持了该菌株在环境物质转化与降解方面的潜力,提示其可能在特定生态位中发挥重要的生物转化功能。
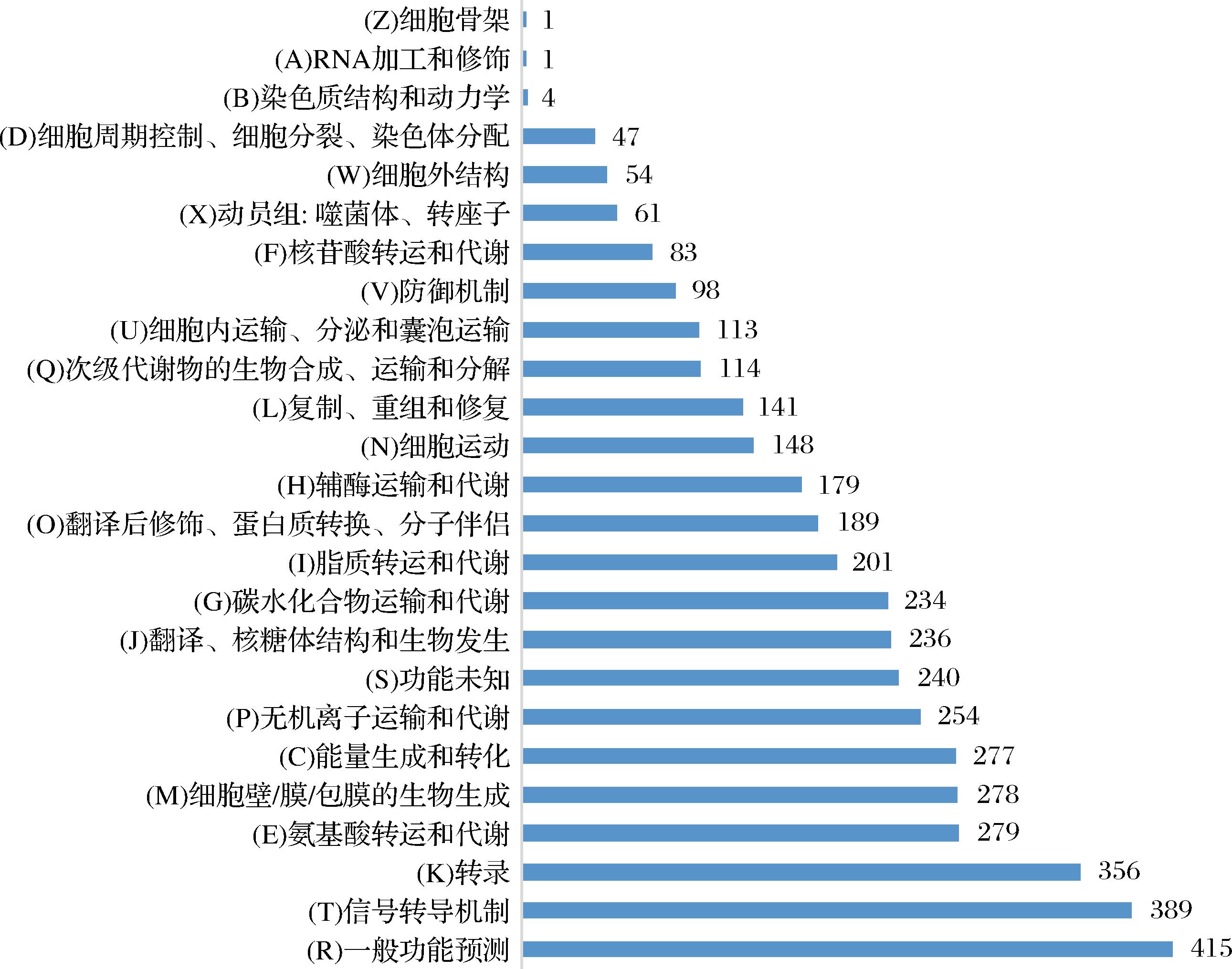
图3 Massilia puerhi SJY3T的COG注释
Fig.3 COG annotation of Massilia puerhi SJY3T
2.3.3 KEGG功能注释
在KEGG数据库中,Massilia puerhi SJY3T共有4 773个基因获得功能注释,分布于细胞过程、环境信息处理、遗传信息处理、人类疾病、新陈代谢和生物体系统6大类,共计238条代谢通路中得到功能注释,结果如图4所示。分析发现,绝大多数基因归类于“新陈代谢”类,尤其在次级代谢产物合成、多样环境中的微生物代谢、抗生素生物合成、碳代谢和氨基酸生物合成等二级分类中表现出显著的注释富集。其中,与次级代谢产物合成相关的基因共270个,占该类注释基因总数的40.06%;与环境中微生物代谢相关的基因有224个,占33.23%;与抗生素生物合成相关的注释基因为207个。碳代谢和氨基酸生物合成通路分别包含105个相关基因。
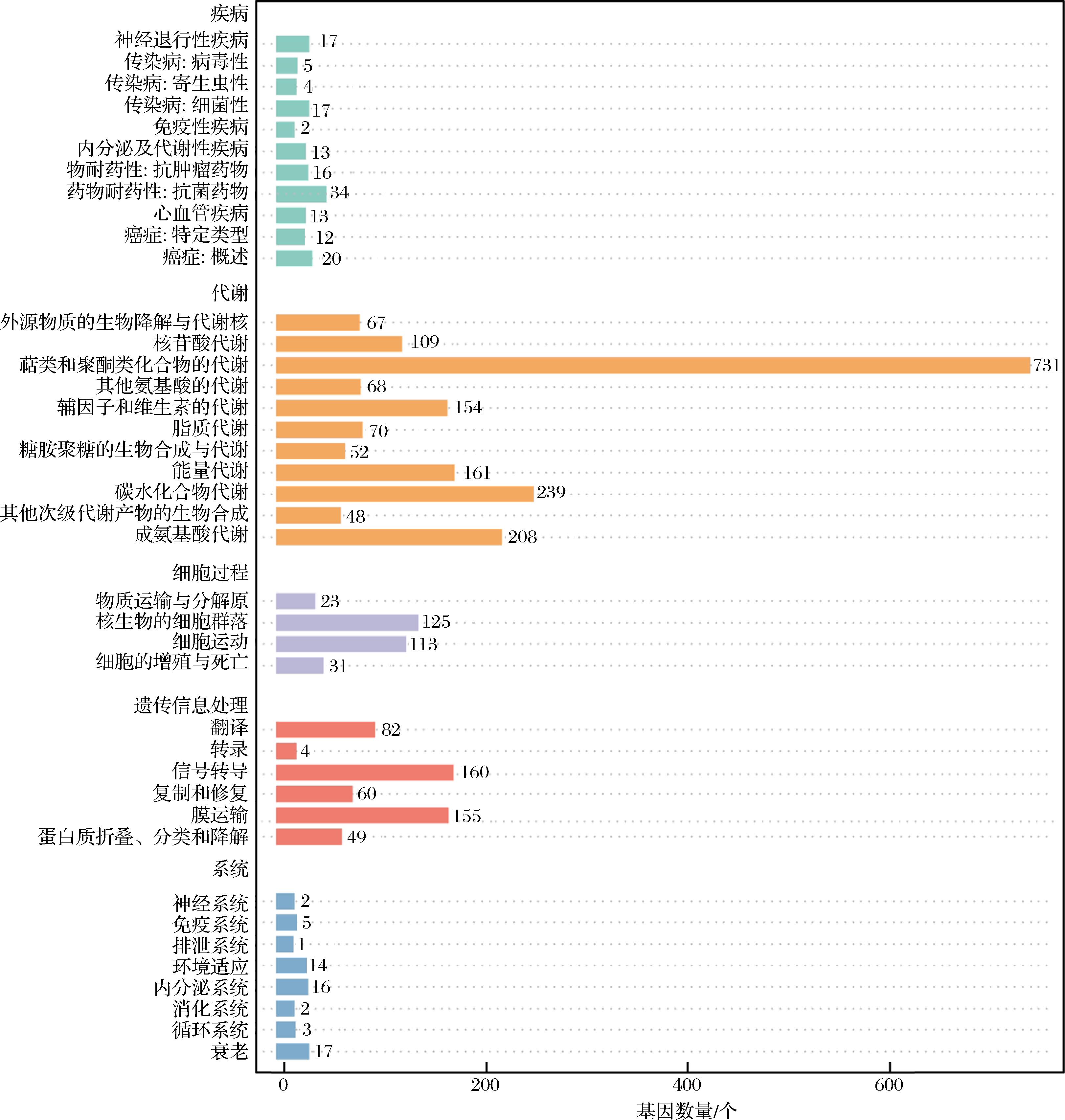
图4 Massilia puerhi SJY3T的KEGG功能分类
Fig.4 KEGG functional classification of Massilia puerhi SJY3T
整体注释结果显示,SJY3T基因组中参与新陈代谢的基因占比最高,这与GO功能注释结果一致,反映出该菌株在物质转运和能量合成机制上的强化,可能赋予其较强的环境适应性。此外,对SJY3T中与有机物降解相关的基因进行挖掘,共鉴定出128个基因,涉及30条代谢通路,结果如电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.043511,下同)所示。其中,脂肪酸降解、嘌呤降解、苯乙酸酯降解、苯甲酸降解等5条关键通路的详细注释结果见附表2。
表1 Massilia puerhi SJY3T次级代谢物合成基因簇
Table 1 Gene clusters of secondary metabolites in Massilia puerhi SJY3T
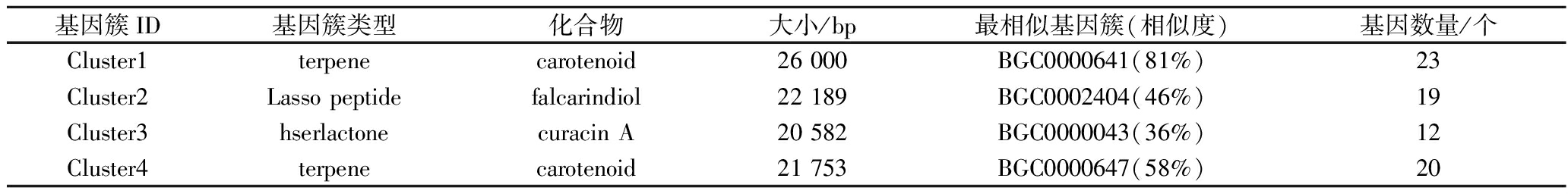
基因簇ID基因簇类型化合物大小/bp最相似基因簇(相似度)基因数量/个Cluster1terpenecarotenoid26 000BGC0000641(81%)23Cluster2Lasso peptidefalcarindiol22 189BGC0002404(46%)19Cluster3hserlactonecuracin A20 582BGC0000043(36%)12Cluster4terpenecarotenoid21 753BGC0000647(58%)20
在脂肪酸降解通路中,注释到4个基因(gene000203、gene000002、gene002894、gene000204),分别编码fadA、fadI、fadN和fadD。这些基因产物均含有辅酶A(coenzyme A,CoA)结构域,CoA作为酰基载体在脂肪酸β-氧化过程中发挥关键作用,促使脂肪酸转化为酰基辅酶A,并最终代谢为乙酰辅酶A[15]。已有研究表明,通过表达脂肪酸降解相关基因(如fadE与fadA)可显著提升黑曲霉葡糖淀粉酶的产量,提示脂肪酸代谢途径在工业微生物应用中具有潜力[16]。此外,有研究指出fad基因簇在总石油碳氢化合物污染环境的生物修复中也可能发挥重要作用[17]。基于此,推测SJY3T可能通过增强脂肪酸代谢来提升环境适应性和有机物降解能力,在普洱茶窖藏土壤微生物的生物修复中可能实现高效有机物降解的潜力。
在嘌呤降解通路中,共注释到11个基因(gene001915、gene001918、gene001917、gene000962、gene003706、gene001924、gene000134、gene003748、gene001921、gene001920、gene003747),其编码蛋白包括5′-核苷酸酶、鸟嘌呤脱氨酶、腺苷脱氨酶、多酚氧化酶、5-羟基异尿酸水解酶以及黄嘌呤脱氢酶。其中5个基因(gene000134、gene003748、gene001921、gene001920、gene003747)编码Xdh,该酶是一类含钼的氧化还原酶,广泛存在于各类微生物及真核生物中,在嘌呤代谢中催化黄嘌呤和次黄嘌呤生成尿酸,并释放可被再利用的氮源[18-19]。已有研究证实,Xdh与伴侣蛋白XdhC之间存在功能互补作用,可显著提升嘌呤降解效率,例如鲍曼不动杆菌中Xdh/XdhC系统在食品基质中表现出良好的代谢能力[20]。尽管SJY3T的Xdh基因簇同源性较低,但其保留了关键功能结构域,提示其可能具备潜在的嘌呤降解能力和环境适应机制。
在苯乙酸酯降解通路中,共注释到10个基因(gene002108、gene000002、gene002110、gene002102、gene002103、gene002104、gene002105、gene002106、gene002113、gene002107),均为paa家族成员。Paa途径广泛参与多环芳烃(polycyclic aromatic hydrocarbons,PAHs)如菲和蒽的降解过程[17]。相关研究指出,Paa基因簇通过芳香环羟基化和脂肪酸侧链的β-氧化,将PAHs分解为乙酰辅酶A等代谢中间体[21]。值得注意的是,从PAHs污染土壤中分离的Massilia sp.WF1可将菲作为唯一碳源有效降解,提示Massilia在芳香烃降解中具有显著潜力[7]。
在苯甲酸盐降解相关通路中,共注释到14个基因,其中gene001616、gene001615、gene001613、gene001614为ben基因家族成员。benABC基因编码的双加氧酶可催化苯甲酸的1,2-双加氧反应,是苯甲酸好氧降解的关键酶系[22]。HU等[23]报道的1株嗜热菌SYSU G07066T通过benABC基因实现了48 h内>90%的苯甲酸降解率,值得注意的是,系统发育分析提示该菌可能通过水平基因转移(horizontal gene transfer,HGT)从假单胞菌门获得该类降解基因。Massilia作为变形菌门一员,其基因组中已发现ben家族基因,推测其在高温或污染环境中可能通过HGT获得或优化苯甲酸降解能力,具备良好的环境适应性及生物修复潜力。
2.3.4 碳水化合物活性酶分析
利用CAZy数据库对Massilia puerhi SJY3T菌株的碳水化合物活性酶功能基因进行注释,共识别出205个相关基因,分属于6大功能类别,如图5所示。分别为糖苷水解酶(glycoside hydrolases,GHs)、糖基转移酶(glycosyltransferases,GTs)、多糖裂解酶(polysaccharide lyases,PLs)、碳水化合物结合模(carbohydrate-binding modules,CBMs)、糖酯酶(carbohydrate esterases,CEs)和氧化还原酶(auxiliary activities,AAs)。其中,GHs类酶的注释基因数量最多,共90个,其次是GTs类77个和CBMs类23个。
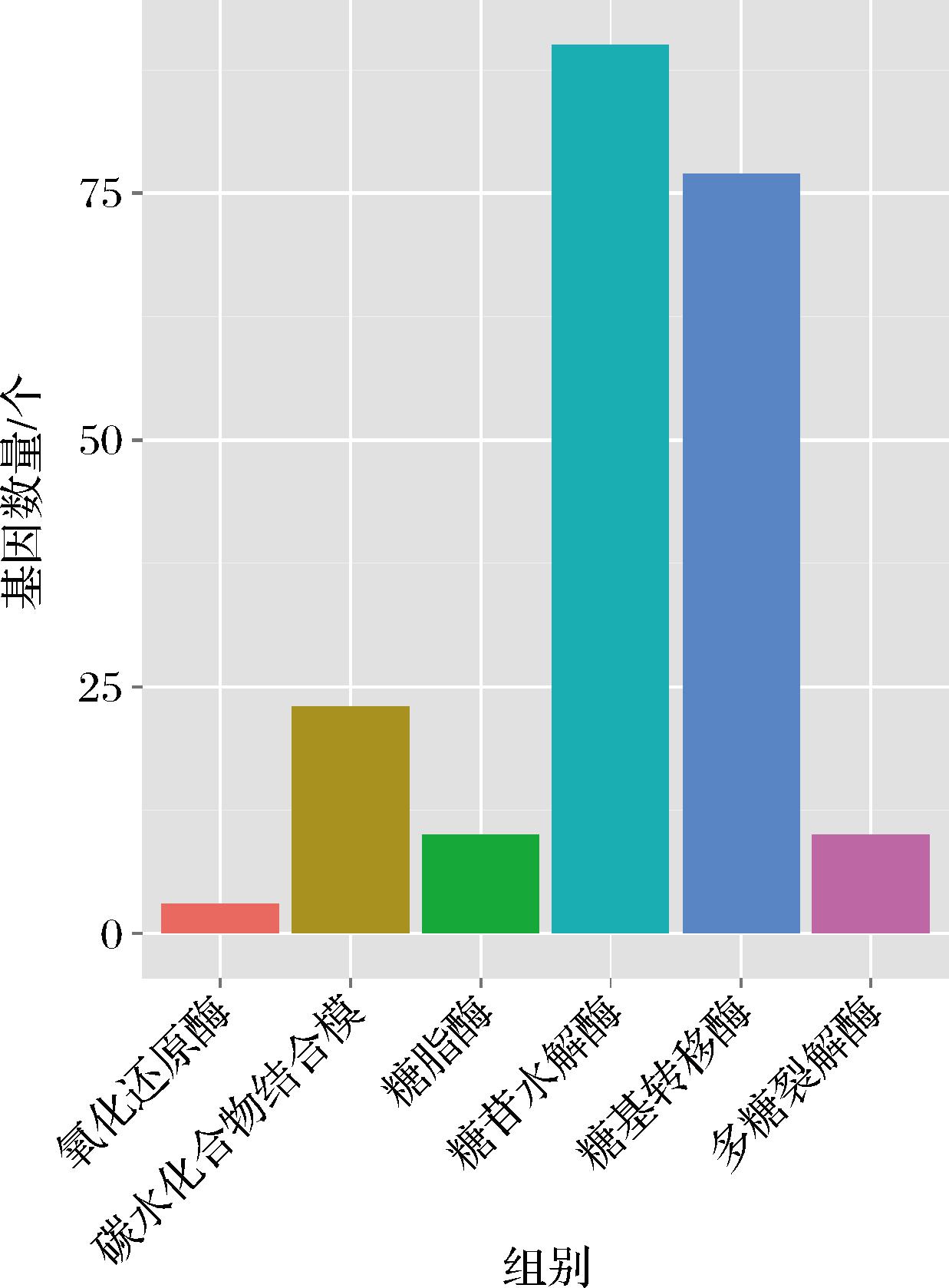
图5 Massilia puerhi SJY3T的CAZy功能分类
Fig.5 CAZy functional classification of Massilia puerhi SJY3T
在GHs家族中,占比最高的是GH23家族,包含7个基因;其次为GH2和GH3家族,分别包含5个基因。GH23家族通常与几丁质酶活性相关,而GH2和GH3家族则主要包括β-半乳糖苷酶、β-甘露糖苷酶、β-葡萄糖苷酶、木聚糖1,4-β-木糖苷酶及α-L-阿拉伯呋喃糖苷酶等。GHs类酶通过水解复杂碳水化合物(如纤维素、半纤维素)生成单糖或寡糖,为糖核苷酸的合成提供前体物质。已有研究表明,植物病原真菌可分泌GH3、GH53等家族酶类降解植物细胞壁多糖,以释放可供代谢利用的单糖[24]。在GTs类中,GT4家族占比最高,共注释到27个基因,主要包括蔗糖合酶、α-葡萄糖基转移酶、脂多糖N-乙酰氨基葡萄糖基转移酶和海藻糖磷酸化酶;其次为GT2家族,共18个基因,涉及纤维素合酶、几丁质合酶和β-1,3-葡聚糖合酶。GTs类酶催化糖基从供体分子转移至受体分子,形成胞外多糖(exopolysaccharides,EPS)重复单元,是EPS合成中的关键酶类[25]。
综上所述,CAZy分析结果表明,Massilia puerhi SJY3T含有丰富的GHs和GTs类酶基因,推测其在复杂碳源的降解与利用方面具有较强的潜力,可能通过调节胞外碳源动态变化,适应不同的发酵环境,从而在普洱茶生产中发挥重要作用。CAZy的多样性和功能潜力使该菌株可能具备降解多种多糖底物的能力,能够分泌多种糖苷水解酶、糖基转移酶及多糖裂解酶[26]。结合已有研究,在六堡茶发酵过程中,Sphingopyxis属和Massilia属可通过分泌胞外酶与黄酮苷类及萜类化合物相互作用,有助于降低苦涩味,改善茶叶风味[27]。此外,Massilia菌属中木聚糖降解酶基因可能作为激发子诱发植物抗病防御[28]。因此,SJY3T菌株可能具备较强的多糖降解能力,在普洱茶窖藏环境中有助于茶叶相关有机物的转化与利用,具有潜在的工业应用价值。
2.3.5 耐药基因与毒理基因预测结果
为识别Massilia puerhi SJY3T菌株中的抗性基因与毒力因子,分别采用CARD数据库与VFDB数据库进行功能基因注释分析。利用CARD数据库提供的Resistance Gene Identifier(RGI)软件,对SJY3T菌株的蛋白质序列进行比对分析。RGI程序基于内置的BLASTP算法进行比对,默认e-value阈值为10-30。根据比对结果,筛选并统计注释到的抗生素抗性基因信息。采用DIAMOND软件对SJY3T菌株的氨基酸序列与VFDB数据库进行高效比对,以获得与毒力因子相关的蛋白质序列注释信息。通过整合比对结果与数据库中对应的功能注释,实现对潜在毒力基因的全面识别,结果如附表3所示。本节分析为后续探讨SJY3T菌株在特定生态环境中的生存策略、与宿主或微生物群落的相互作用及其为潜在的工业应用提供基础数据支持。
2.3.6 PHI注释结果
PHI数据库是病原体与宿主之间相互作用的基因数据库,主要来源于多种病原体(如真菌、卵菌和细菌)及其感染的多类宿主,包括动物、植物、真菌和昆虫等。为探究Massilia puerhi SJY3T菌株的致病潜力与宿主相互作用特征,本研究采用DIAMOND软件将其全蛋白质序列与PHI数据库进行比对分析,并结合数据库中的功能注释信息进行归类与统计。
比对结果显示,SJY3T菌株共注释到391个与病原-宿主互作相关的基因,这些基因被归入以下8类功能类型:丧失致病性、毒力减弱、致病性不受影响、毒力增强、效应子、致死性、增强拮抗以及野生型共生关系。其中,功能注释为“毒力减弱”的基因数量最多,占注释基因总数的65.98%;其次为“致病性不受影响”类基因,占比18.67%。此外,“增强拮抗”与“野生型共生关系”相关基因占比较低,分别为0.77%和0.26%。这表明Massilia puerhi SJY3T在遗传水平上可能具有一定的环境安全性。已有研究表明,Massilia属细菌可通过调控糖酵解通路促进种子油的积累,从而改善宿主的品质性状,并影响植物根际微生物群落的组成。其中,Massilia的富集与大豆种子中油脂和脂肪酸含量的增加密切相关[29]。因此,Massilia属微生物在农业科学与生物技术领域可能具有潜在应用价值,尤其是在利用微生物干预提升作物品质与产量方面,表现出广阔的前景。
2.3.7 次级代谢基因簇分析
通过antiSMASH对Massilia puerhi SJY3T全基因组数据分析,检测到4个次级代谢产物合成基因簇,包括2个萜烯类、1个套索肽和1个高丝氨酸内酯基因簇,结果如表1所示。其中,萜类合成基因簇,具有43个编码基因,这说明萜类化合物可能是SJY3T最主要的次级代谢产物,且与其在窖藏环境中潜在的生态适应性与功能调节密切相关。此外,套索肽和高丝氨酸内酯基因簇也具有潜在功能。已有研究表明,套索肽具有抗菌活性[30],而高丝氨酸内酯作为群体感应信号分子,在微生物间的信息交流、抗性调节和代谢调控中发挥重要作用。基于此SJY3T基因组中编码的次级代谢基因簇显示出其在风味形成、微生物互作和生态位占据方面的潜力,特别是萜类和套索肽的存在,可能赋予该菌株在窖藏微生态系统中重要的生态功能。这些结果不仅揭示了Massilia puerhi SJY3T的代谢能力,也为后续针对特定产物的功能验证实验提供了方向。
3 结论
本研究对从景迈山普洱茶窖藏土壤中分离获得的Massilia puerhi SJY3T菌株进行功能注释,系统揭示了其在有机物降解和环境适应方面的基因组特征。结果显示,该菌株基因组中富含参与脂肪酸、芳香族化合物等代谢通路的关键功能基因,具备一定的碳源转化能力和微生态调节潜力,可能在茶叶贮藏发酵过程中参与有机物降解与风味物质转化。此外,分析还预测到一定数量的毒力因子和耐药相关基因,表明该菌株可能在复杂微生态系统中具有较强的环境适应能力。目前该研究主要基于基因组信息的功能注释,实际生态功能尚需进一步实验证实。未来将重点开展Massilia puerhi SJY3T在模拟普洱茶窖藏环境下的代谢验证实验,同时,将结合高通量测序,系统评估该菌株在不同普洱茶贮藏土壤环境中的分布特征及其生态意义,进一步阐明其在茶叶贮藏发酵过程中的潜在作用机制。
综上所述,本研究通过对Massilia puerhi SJY3T基因组的系统注释,初步揭示了其在代谢调控、环境适应及潜在应用等方面的分子基础,为该菌株在食品发酵、农业微生态调控等领域的研究与开发提供了理论依据。
[1] ZHAO M, SU X Q, NIAN B, et al.Integrated meta-omics approaches to understand the microbiome of spontaneous fermentation of traditional Chinese Pu-erh tea[J].mSystems, 2019, 4(6):e00680-19.
[2] 路伟尧. 普洱茶发酵微生物的溯源分析[D].北京:北京化工大学, 2013.LU W Y.Analysis of microbial tracking in Pu’er tea fermentation[D].Beijing:Beijing University of Chemical Technology, 2013.
[3] FU J Y, SHEN Y, DUAN S J, et al.Sinomonas puerhi sp.nov.isolated from the rhizosphere soil of Pu-erh tea based on whole-genomic profiling[J].International Journal of Systematic and Evolutionary Microbiology, 2025, 75(4).DOI:10.1099/ijsem.0.006752.
[4] 黄友谊, 方欣, 隋梦圆, 等.茶叶微生物研究现状与展望[J].华中农业大学学报, 2022, 41(5):24-32.HUANG Y Y, FANG X, SUI M Y, et al.Situation and prospect of studying tea microorganisms[J].Journal of Huazhong Agricultural University, 2022, 41(5):24-32.
[5] HUQ M A, MA J C, SRINIVASAN S, et al.Massilia agrisoli sp.nov., isolated from rhizospheric soil of banana[J].International Journal of Systematic and Evolutionary Microbiology, 2023, 73(5):005879.
[6] YUE J J, YANG F, WANG S Y, et al.Massilia phyllostachyos sp.nov., isolated from the roots of moso bamboo in China[J].Current Microbiology, 2022, 80(2):54.
[7] WANG H Z, LOU J, GU H P, et al.Efficient biodegradation of phenanthrene by a novel strain Massilia sp.WF1 isolated from a PAH-contaminated soil[J].Environmental Science and Pollution Research, 2016, 23(13):13378-13388.
[8] DU C J, LI C X, CAO P, et al.Massilia cellulosiltytica sp.nov., a novel cellulose-degrading bacterium isolated from rhizosphere soil of rice (Oryza sativa L.) and its whole genome analysis[J].Antonie Van Leeuwenhoek, 2021, 114(10):1529-1540.
[9] YANG R J, ZHOU D, WANG Q M, et al.Massilia puerhi sp.nov., isolated from soil of Pu-erh tea cellar[J].International Journal of Systematic and Evolutionary Microbiology, 2021, 71(9).DOI:10.1099/ijsem.0.004992.
[10] HU E Z, LAN X R, LIU Z L, et al.A positive correlation between GC content and growth temperature in prokaryotes[J].BMC Genomics, 2022, 23(1):110.
[11] CHUCKRAN P F, FLAGG C, PROPSTER J, et al.Edaphic controls on genome size and GC content of bacteria in soil microbial communities[J].Soil Biology and Biochemistry, 2023, 178:108935.
[12] SÜTZL L, FOLEY G, GILLAM E M J, et al.The GMC superfamily of oxidoreductases revisited:Analysis and evolution of fungal GMC oxidoreductases[J].Biotechnology for Biofuels, 2019, 12:118.
[13] 罗芳. 甲基转移酶参与水稻体内残留阿特拉津脱毒及降解机制的研究[D].南京:南京农业大学, 2016.LUO F.Methyltransferases involved in detoxification and degradation of atrazine residues in rice[D].Nanjing:Nanjing Agricultural University, 2016.
[14] 刘艳艳, 刘孝龙, 赵萌, 等.宏基因组来源的酯酶酶学性质及对邻苯二甲酸酯的降解[J].中山大学学报(自然科学版), 2020, 59(6):41-50.LIU Y Y, LIU X L, ZHAO M, et al.The enzymatic properties of esterase from metagenomic sources and the degradation of phthalates[J].Acta Scientiarum Naturalium Universitatis Sunyatseni, 2020, 59(6):41-50.
[15] XIE J M, YU Z, ZHU Y, et al.Functions of coenzyme a and acyl-CoA in post-translational modification and human disease[J].Frontiers in Bioscience, 2024, 29(9):331.
[16] QI J, XIAO X Z, OUYANG L M, et al.Enhancement of fatty acid degradation pathway promoted glucoamylase synthesis in Aspergillus niger[J].Microbial Cell Factories, 2022, 21(1):238.
[17] SUN S, SU Y H, CHEN S Q, et al.Bioremediation of oil-contaminated soil:Exploring the potential of endogenous hydrocarbon degrader Enterobacter sp.SAVR S-1[J].Applied Soil Ecology, 2022, 173:104387.
[18] 徐江民, 刘之陶, 蒋丹莹, 等.植物黄嘌呤脱氢酶参与代谢途径及其功能研究进展[J].生物工程学报, 2024, 40(10):3321-3336.XU J M, LIU Z T, JIANG D Y, et al.Research advances on the metabolic pathways and functions mediated by plant xanthine dehydrogenase[J].Chinese Journal of Biotechnology, 2024, 40(10):3321-3336.
[19] 陈晓楠, 高丽华, 周正富, 等.耐辐射异常球菌黄嘌呤脱氢酶在氧化胁迫反应中的作用[J].中国农业科技导报, 2021, 23(3):73-81.CHEN X N, GAO L H, ZHOU Z F, et al.Role of xanthine dehydrogenase in oxidative stress response of Deinococcus radiodurans R1[J].Journal of Agricultural Science and Technology, 2021, 23(3):73-81.
[20] WANG C H, ZHANG R, SUN Y, et al.Combinatorial co-expression of xanthine dehydrogenase and chaperone XdhC from Acinetobacter baumannii and Rhodobacter capsulatus and their applications in decreasing purine content in food[J].Food Science and Human Wellness, 2023, 12(4):1343-1350.
[21] YAM K C, VAN DER GEIZE R, ELTIS L D.Catabolism of Aromatic Compounds and Steroids by Rhodococcus[M].Biology of Rhodococcus.Berlin, Heidelberg:Springer Berlin Heidelberg, 2010:133-169.
[22] NEIDLE E L, HARTNETT C, ORNSTON L N, et al.Nucleotide sequences of the Acinetobacter calcoaceticus benABC genes for benzoate 1, 2-dioxygenase reveal evolutionary relationships among multicomponent oxygenases[J].Journal of Bacteriology, 1991, 173(17):5385-5395.
[23] HU C J, LV Y Q, XIAN W D, et al.Multi-omics insights into the function and evolution of sodium benzoate biodegradation pathway in Benzoatithermus flavus gen.nov., sp.nov.from hot spring[J].Journal of Hazardous Materials, 2024, 476:135017.
[24] 陈相永, 陈捷胤, 李蕾, 等.植物致病真菌寄生类型与胞外糖基水解酶家族分析[J].基因组学与应用生物学, 2014, 33(3):640-648.CHEN X Y, CHEN J Y, LI L, et al.The analysis of plant pathogenic fungi lifestyles and extracellular glycoside hydrolases families[J].Genomics and Applied Biology, 2014, 33(3):640-648.
[25] 李柏良, 赵莉, 王成凤, 等.嗜热链球菌KLDS3.1012胞外多糖合成途径的基因组学及表型特征分析[J].食品科学, 2019, 40(6):136-142.LI B L, ZHAO L, WANG C F, et al.Genomic and phenotypic characterization of the biosynthesis pathway of exopolysaccharides in Streptococcus thermophilus KLDS3.1012[J].Food Science, 2019, 40(6):136-142.
[26] ALEGADO R A, FERRIERA S, NUSBAUM C, et al.Complete genome sequence of Algoriphagus sp.PR1, bacterial prey of a colony-forming choanoflagellate[J].Journal of Bacteriology, 2011, 193(6):1485-1486.
[27] LIU H H, HUANG Y Y, LIU Z S, et al.Determination of the variations in the metabolic profiles and bacterial communities during traditional craftsmanship Liupao tea processing[J].Food Chemistry:X, 2024, 22:101516.
[28] 赵联正, 谢占玲, 赵朋.一种新的镰刀菌Q7-31木聚糖酶Xyn9的分离纯化鉴定及酶学特性[J].江苏农业科学, 2015, 43(5):42-45.ZHAO L Z, XIE Z L, ZHAO P.Purification identification and enzymatic characteristics of a new xylanase Xyn9 from Fusarium sp.Q7-31[J].Jiangsu Agricultural Sciences, 2015, 43(5):42-45.
[29] HAN Q, ZHU G H, QIU H M, et al.Quality traits drive the enrichment of Massilia in the rhizosphere to improve soybean oil content[J].Microbiome, 2024, 12(1):224.
[30] JANGRA M, TRAVIN D Y, ALEKSANDROVA E V, et al.A broad-spectrum lasso peptide antibiotic targeting the bacterial ribosome[J].Nature, 2025, 640(8060):1022-1030.