细胞色素C(cytochrome C,Cyt C)是一种多功能酶,具有调节能量代谢和细胞凋亡的作用。当Cyt C从线粒体释放到细胞外时,可以发挥信号分子的作用,参与调控多种病理生理过程[1]。Cyt C除参与电子传递外,还具有过氧化氢酶(catalase,CAT)活性,其血红素辅基可催化H2O2分解为H2O和O2[2]。这种酶活性为设计荧光传感体系提供了靶点。因此,建立快速、灵敏、简便的Cyt C分析方法具有十分重要的意义。传统的Cyt C检测方法有分光光度法、电化学检测法等,但存在灵敏度低、选择性差、操作复杂等缺点,难以满足现代生物医学研究对快速、准确、高灵敏度检测的需求。近年来,金纳米簇(Au nanoclusters,AuNCs)作为一种新兴的纳米材料,因其独特的光学性质、良好的生物相容性和易于功能化修饰等优势,在生物传感领域展现出巨大的应用潜力[3]。AuNCs具有荧光、表面增强拉曼散射等特性,可通过与目标生物分子的相互作用实现特异性检测。近年来,AuNCs荧光淬灭法已用于Hg2+[4]、NO2-等小分子检测,与GB 5009.33—2016《食品安全国家标准 食品中亚硝酸盐与硝酸盐的测定》检测NO2-方法相比,该方法不需要对肉制品样品进行脱脂、脱蛋白等处理,检测效率显著提高[5]。但用于蛋白质检测仍具挑战性。本研究首次将Cyt C的酶活性与AuNCs荧光淬灭结合,拓展了该方法在生物大分子检测中的应用。
本研究通过合成具有特定光学性质的AuNCs,并将其与Cyt C进行相互作用,构建一种基于AuNCs的Cyt C检测体系,实现对Cyt C的高灵敏度、高选择性检测,并将其用于毒素诱导细胞凋亡过程中Cyt C的实时原位动态监测。
1 材料与方法
1.1 材料与试剂
氯金酸(HAuCl4)、NaOH、H2O2、PBS、NaCl、KCl,国药集团化学试剂有限公司;牛血清白蛋白(bovine serum albumin,BSA)溶液、Cyt C、DNA酶、RNA酶、谷胱甘肽(glutathione,GSH),Sigma-Aldrich公司;Calcein AM细胞活性检测试剂盒(CCK-F,产品编号C2013S)、完全培养基(含10%胎牛血清、1%双抗的DMEM培养基),碧云天生物技术有限公司。
1.2 仪器与设备
UV-1800紫外-可见光分光光度计,日本岛津公司;F-7000荧光光谱分析仪,日本日立公司;JEOL JEM-2100透射电子显微镜,日本JEOL公司;激光共聚焦显微镜,德国卡尔蔡司公司;SpectraMax M5/M5e型荧光酶标仪,美国分子器件公司;恒温水浴锅,上海景宏实验设备公司;5424R台式高速离心机(转速10 000 r/min),德国艾本德公司。
1.3 实验方法
1.3.1 AuNCs的合成与表征
在三颈烧瓶中混合5 mL 50 mg/mL BSA溶液与5 mL HAuCl4溶液,避光搅拌后加入500 μL 1 mol/L NaOH溶液,于37 ℃恒温反应12 h合成AuNCs。通过紫外-可见光谱检测吸收峰变化,荧光光谱分析激发/发射波长,透射电子显微镜观察粒径分布与形貌,验证AuNCs的生成与均一性。
1.3.2 AuNCs荧光淬灭效率的时间优化
在反应体系中加入50 μL PBS、50 μL AuNCs溶液、100 μL Cyt C或蒸馏水(对照)及50 μL H2O2,于30 ℃水浴分别反应1、2、10、15、20、25、30 min,通过荧光光谱仪测定荧光强度,分别计算淬灭效率,确定最佳反应时间。
1.3.3 AuNCs荧光淬灭效率的温度优化
设置反应温度为10、20、30、40、50 ℃,在反应体系中加入50 μL PBS、50 μL AuNCs溶液、100 μL Cyt C或蒸馏水(对照)及50 μL H2O2,固定反应时间5 min,通过荧光检测比较不同温度下的淬灭效率,确定最佳反应温度。
1.3.4 AuNCs荧光淬灭效率的H2O2浓度优化
配制H2O2浓度为25、50、100、200、400、600 μmol/L,在反应体系中加入50 μL PBS、50 μL AuNCs溶液、100 μL Cyt C或蒸馏水(对照)后分别加入50 μL上述浓度的H2O2,30 ℃水浴反应5 min,通过荧光检测比较不同H2O2浓度下的淬灭效率,确定最佳H2O2浓度。
1.3.5 AuNCs荧光淬灭效率的AuNCs浓度优化
将制备的AuNCs溶液进行梯度稀释,得到以5、2.5、1.25、0.625、0.312 5 mmol/L金元素浓度代表的AuNCs溶液,在反应体系中加入50 μL PBS、100 μLCyt C或蒸馏水(对照)后分别加入上述浓度的金元素溶液,最后加入50 μL H2O2,在30 ℃水浴反应5 min,通过荧光检测比较不同金元素浓度下的淬灭效率,确定最佳的金元素浓度,即最佳的AuNCs浓度。
1.3.6 Cyt C标准曲线
在获得的最佳条件下,配制Cyt C浓度梯度为0.2、0.4、0.6、0.8、1、2、4、6、8、10 μmol/L,测定荧光淬灭效率,分析不同浓度淬灭效率与浓度的线性关系。
1.3.7 H2O2-Cyt C体系的选择性实验
向反应体系中加入0.1 mmol/L的Na+、K+、Cl-、DNA酶、RNA酶、GSH、CAT、髓过氧化物酶(myeloperoxidase,MPO)等干扰物质,以荧光淬灭效率为指标,对比实验组(含Cyt C)与干扰组的差异,验证体系对Cyt C的特异性响应。
1.3.8 AuNCs的细胞毒性实验
将Hela细胞接种于96孔板,加入不同浓度AuNCs(40~400 μmol/L)孵育6~24 h,利用Calcein AM试剂盒检测细胞活性,通过荧光强度计算细胞存活率,评估AuNCs的生物相容性与毒性效应。
1.3.9 AuNCs的共聚焦成像
将HepG2细胞在激光共聚焦专用小皿中过夜孵育至贴壁后,弃去旧培养基。将AuNCs加入小皿与细胞共孵育,使用60 μmol/L棒曲霉素刺激0~5 h,用PBS清洗后多聚甲醛固定,DAPI(4′,6-二脒基-2-苯基吲哚)染色,利用高分辨率共聚焦显微镜得到荧光成像图,同时做不进行毒素诱导的阴性对照组实验。
1.4 数据处理
所有实验均设置3组平行实验,实验数据以“平均值±标准差”表示,采用Origin 2021软件完成数据的统计分析与图表绘制。
荧光淬灭效率(Q)计算如公式(1)所示:
(1)
式中:F0,无Cyt C时体系的荧光强度;F,加入Cyt C后体系的荧光强度。
依据荧光淬灭效率与Cyt C浓度的线性关系,采用线性回归法拟合得到标准曲线,计算线性相关系数R2,并以信噪比S/N=3计算方法的最低检测限。共聚焦荧光成像图片采用Image J 1.8.0 软件进行荧光强度的定量分析,选取视野内至少5个独立区域计算平均荧光强度,以排除背景荧光干扰。
2 结果与分析
图1-a为AuNCs的合成及Cyt C催化淬灭AuNCs荧光的实验流程图,通过BSA和HAuCl4反应生成AuNCs,再分别在H2O2和H2O2-Cyt C体系下进行荧光检测得到荧光光谱图。图1-b为AuNCs荧光淬灭原理图,BSA具有保护AuNCs荧光的特性,Cyt C具有过氧化氢酶活性。在H2O2存在下,Cyt C催化氧化BSA分子中的还原性官能团(如巯基、双硫键),导致BSA从AuNCs表面脱落,进而引发荧光淬灭,导致体系的荧光强度逐渐降低。据此,建立了一种简单、快速的Cyt C荧光分析法。
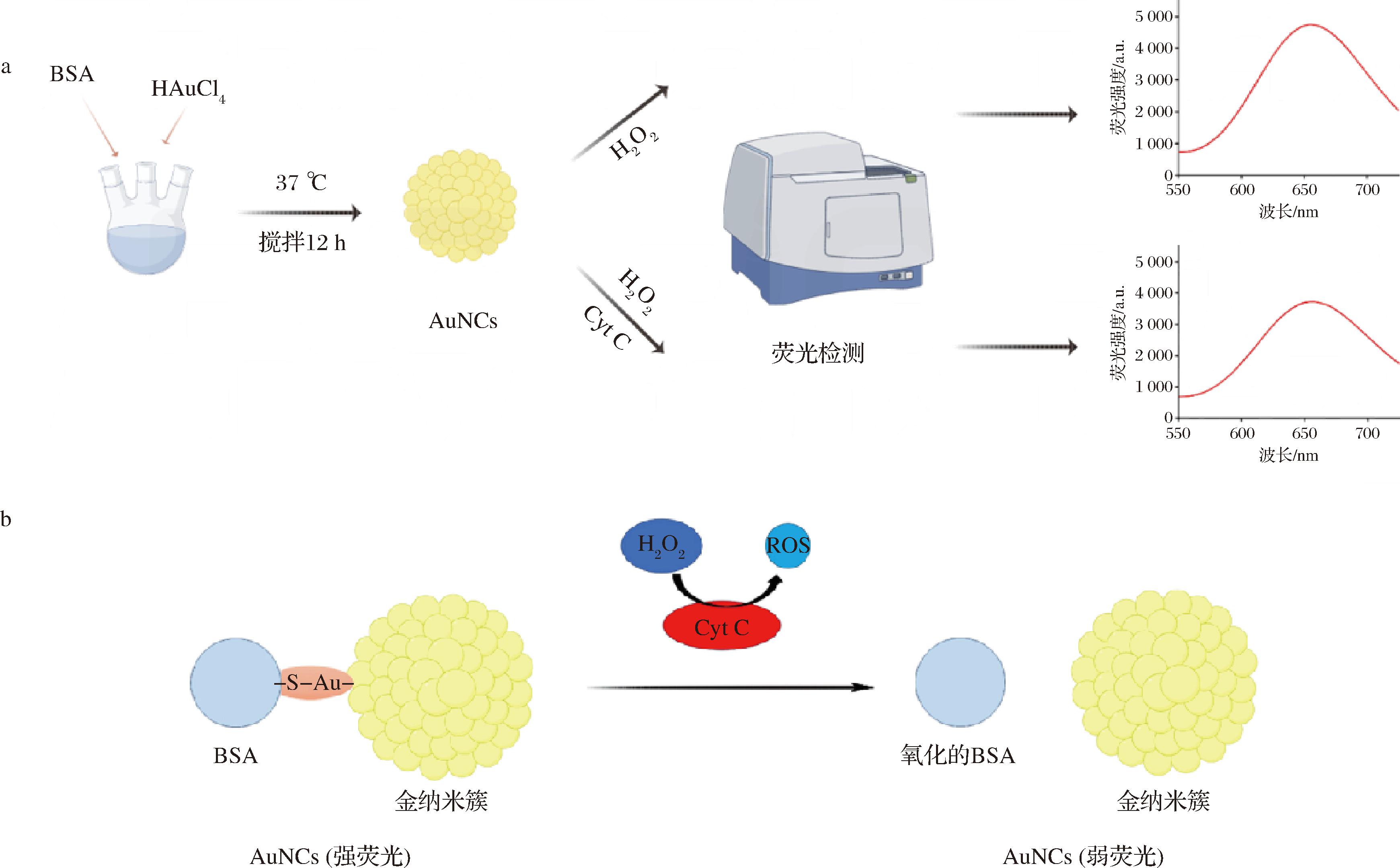
a-实验流程图;b-AuNCs荧光淬灭原理图
图1 实验流程及机理图
Fig.1 Experimental procedure and mechanism diagram
2.1 AuNCs的合成与表征
2.1.1 紫外-可见吸收光谱
本实验利用BSA作为还原剂和稳定剂,在碱性条件下合成具有一定荧光的AuNCs,采用紫外吸收光谱对AuNCs进行表征。由图2可知,HAuCl4在292 nm附近有明显紫外吸收峰,此峰为Au(Ⅲ)在水溶液中的电荷吸收峰,而AuNCs紫外吸收较弱。
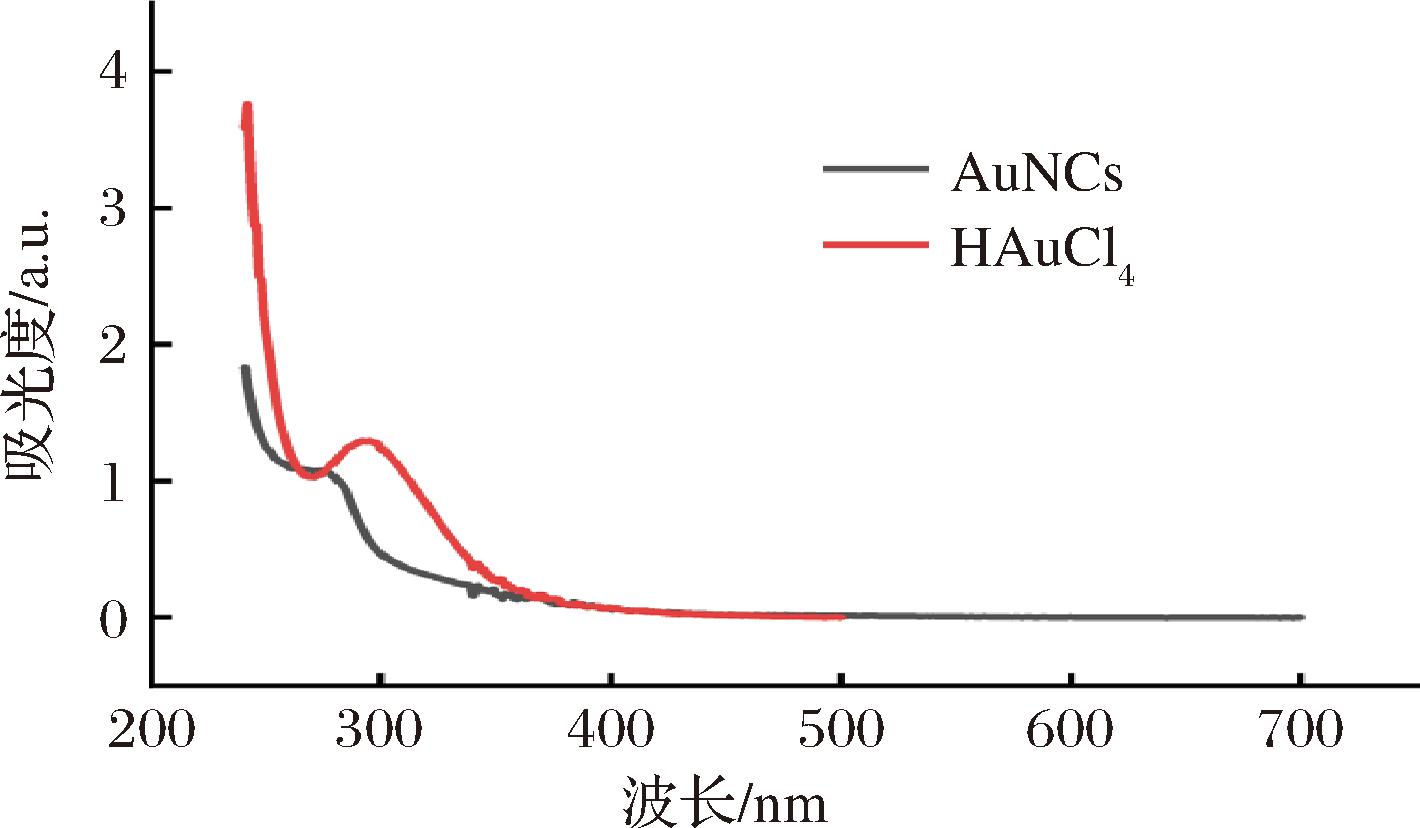
图2 AuNCs和HAuCl4的紫外-可见吸收光谱
Fig.2 Ultraviolet-visible absorption spectra of Au AuNCs and HAuCl4
2.1.2 荧光光谱
对AuNCs溶液进行荧光光谱分析,得到三维荧光光谱(图3-a)和单一荧光光谱(图3-b)。观察三维荧光光谱可以通过最高峰得到溶液的最佳激发波长为300~380 nm,最大发射波长为600~700 nm。根据单一荧光光谱得到最大发射波长为650~675 nm。两图得到的结果都与文献报道的AuNCs的荧光光谱结果一致[6]。
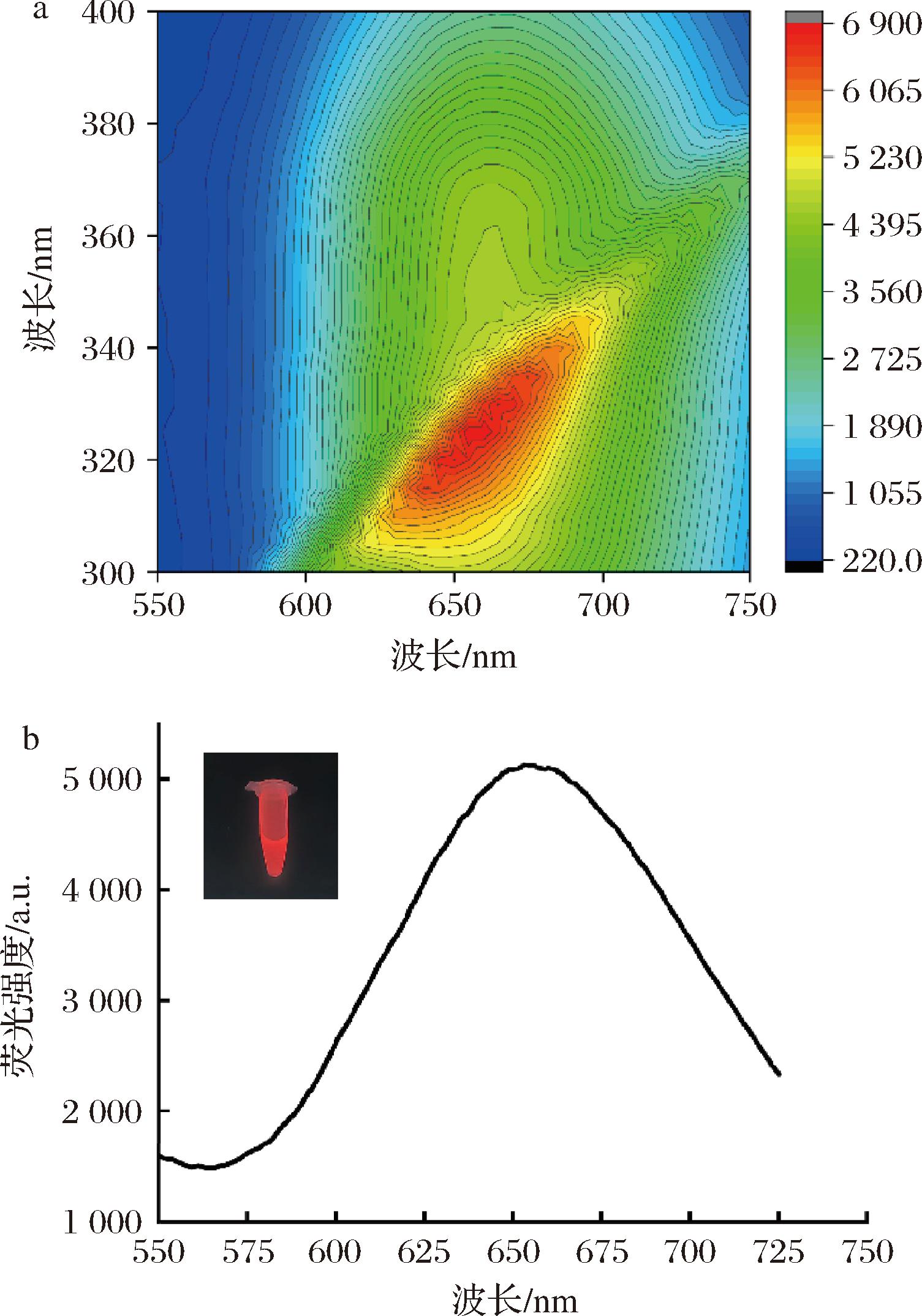
a-三维荧光光谱图;b-单一荧光光谱图
图3 AuNCs溶液荧光光谱图
Fig.3 Fluorescence spectrum of AuNCs solution
观察到三维荧光光谱中的峰型不对称,可能存在类倍频峰的信号干扰[7],为避免类倍频峰或其他信号的干扰,后续实验确定实验激发波长为375 nm,最大发射波长为660 nm。
2.1.3 粒径分布
采用透射电子显微镜对AuNCs进行表征,电镜结果如图4-a所示,可以观察到AuNCs粒子形状均一,单分散性良好。对粒径大小进行统计(图4-b),可以得到AuNCs粒径分布在2.2~3.4 nm。
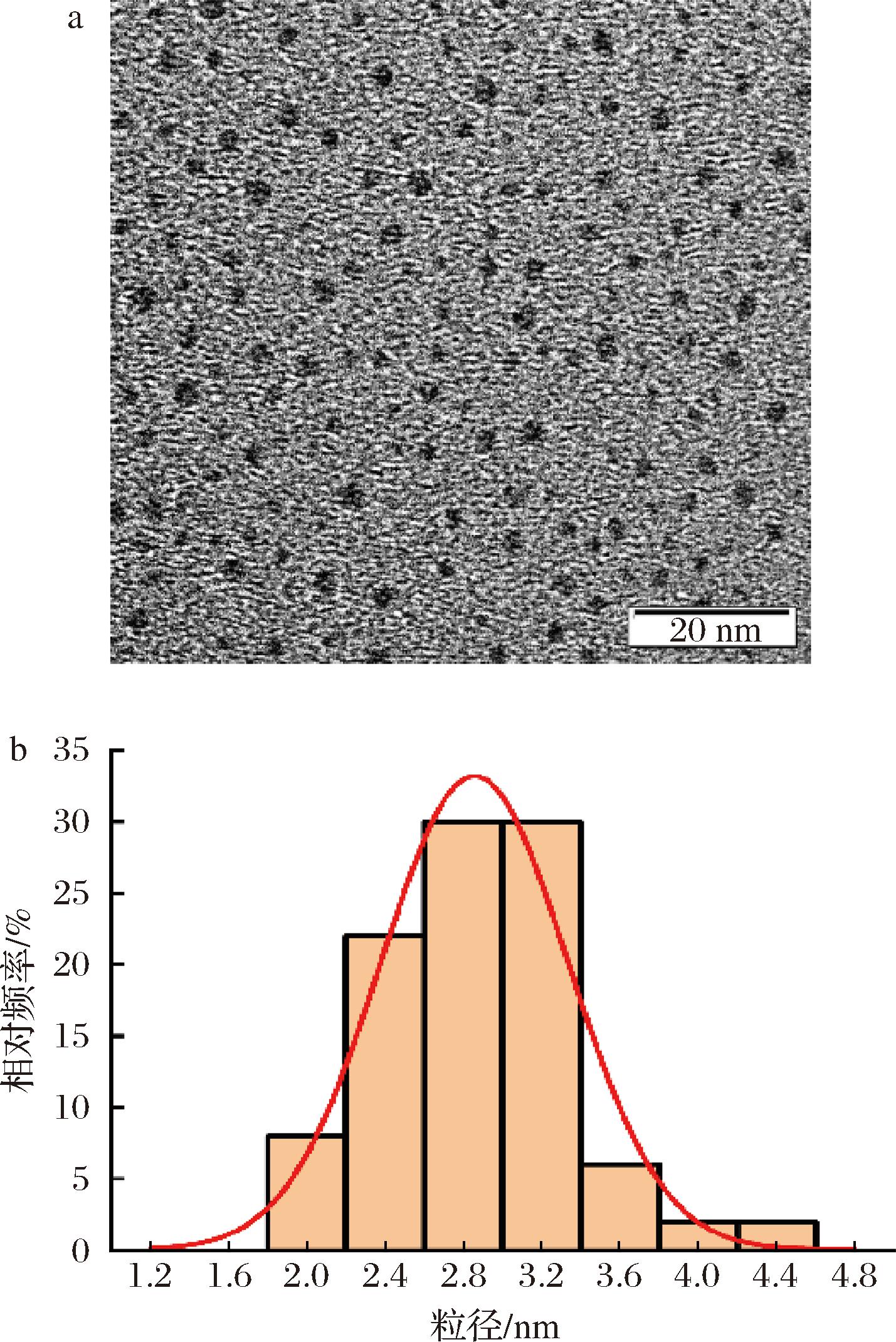
a-AuNCs的透射电子显微镜图;b-AuNCs粒径大小分布图
图4 AuNCs表征图
Fig.4 Characterization diagrams of AuNCs
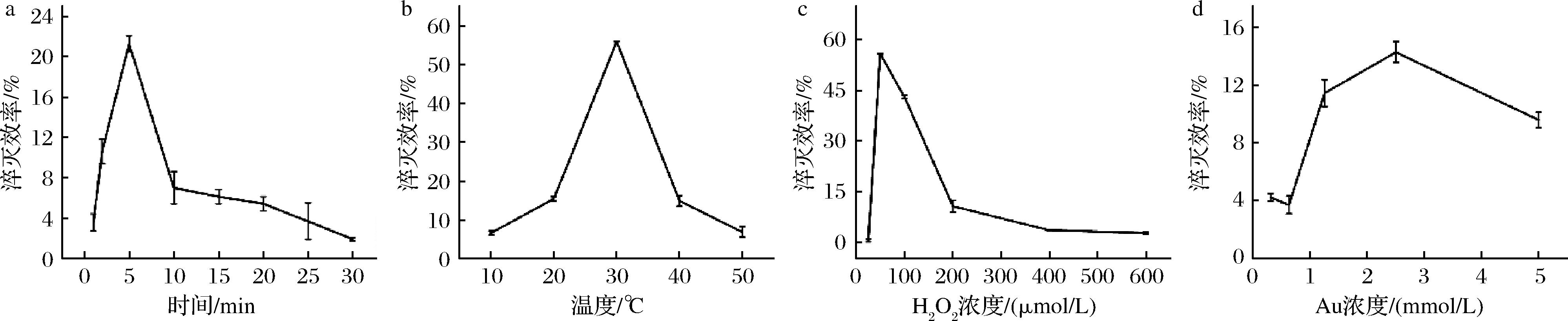
a-反应时间;b-温度;c-H2O2浓度;d-金元素浓度
图5 淬灭效率与反应条件关系曲线
Fig.5 Relationship curve between quenching efficiency and reaction conditions
2.2 AuNCs荧光淬灭优化
2.2.1 反应时间的优化
Cyt C荧光淬灭效率随时间变化关系曲线如图5-a所示,呈现先升高后降低的趋势,淬灭效率在5 min时达到峰值(21.32%)。在反应初期(0~5 min),H2O2(50 μmol/L)和Cyt C(1 μmol/L)浓度充足,催化反应快速生成大量氧化性物种,纳米簇表面未被反应产物覆盖,氧化攻击效率最高,淬灭效率迅速升至峰值[8]。5 min后,淬灭效率逐渐降低,推测原因为:1)H2O2被持续分解,浓度降低,氧化性物种生成速率下降,对纳米簇的攻击减弱[9];2)长时间反应导致Cyt C活性中心(血红素基团)因过度氧化或副产物(O2-)结合而失活,催化效率降低[10];3)氧化产物(如Au+/Au3+)或配体碎片吸附在纳米簇表面,形成钝化层,阻碍H2O2与荧光核心接触,部分纳米簇通过配体交换恢复荧光活性[11]。
2.2.2 反应温度的优化
如图5-b所示,AuNCs荧光淬灭效率随温度升高而升高,在30 ℃时达到峰值(55.93%),随后呈下降趋势。这表明在30 ℃下,Cyt C对H2O2的催化作用充分发挥,使得AuNCs荧光淬灭最为显著。随着温度继续升高,淬灭效率逐渐降低,推测原因如下:Cyt C是一类含血红素(铁卟啉基团)的蛋白质[6],其分子由蛋白质部分和血红素辅基组成,蛋白质部分为血红素提供特定的环境以实现电子传递功能[12]。温度到达30 ℃以上后,蛋白质发生变性从而使得Cyt C空间结构被破坏,催化作用降低,淬灭效率也随之降低。
2.2.3 H2O2浓度的优化
如图5-c所示,AuNCs淬灭效率在H2O2浓度为0~600 μmol/L呈现先上升后下降的趋势,当H2O2浓度为50 μmol/L时,淬灭效率最高。推测原因如下:1)从Cyt C的结构稳定性与氧化损伤分析,低浓度H2O2下保持温和氧化条件下,Cyt C维持活性构象,催化反应高效进行。高浓度H2O2下血红素铁被过度氧化为高价态(如化合物Ⅱ),降低电子传递效率;同时蛋白质侧链(如甲硫氨酸、半胱氨酸)被氧化,导致构象不可逆变性。2种情况的存在导致催化效率降低[9]。2)从反应体系的平衡来看,H2O2积累可能改变溶液pH或离子强度,酸性条件可能破坏Cyt C的稳定性,从而降低催化效率[11]。
2.2.4 AuNCs浓度优化
本研究对AuNCs浓度也进行了优化,并用金元素浓度来表示AuNCs浓度,得到荧光淬灭效率随金元素浓度变化曲线。由图5-d可知,随着金元素浓度增大,Cyt C催化H2O2与AuNCs相互作用造成荧光淬灭效率先升高再下降,淬灭效果最好在金元素浓度为2.5 μmol/L的时候。推测原因如下:1)金元素浓度较高时,AuNCs粒子数量较多,间距较小,导致其发生部分团聚,阻碍与Cyt C的充分接触。2)经适当稀释后,金元素浓度降低,AuNCs粒子分散性增强,表面配体(如硫醇或蛋白质)的暴露更充分,从而更易与Cyt C结合,促进电子转移或能量传递,提高荧光淬灭效率;同时Cyt C在H2O2存在下可催化氧化反应,生成活性氧;稀释后,H2O2与Cyt C的局部浓度可能更接近最佳反应比例,增强氧化能力,使AuNCs表面配体或金属核心的电子转移加速,从而导致荧光淬灭增强[13-14]。3)当金元素浓度过低时,AuNCs和Cyt C两者之间的碰撞频率显著下降,有效相互作用减少,电子转移或能量传递效率降低,淬灭效果减弱;另外,AuNCs的荧光特性高度依赖表面配体的保护,AuNCs溶液的过度稀释可能破坏配体的动态平衡(如配体解吸或溶剂化效应增强),导致AuNCs结构稳定性下降,荧光本底信号减弱,间接降低淬灭效率[15-16]。
2.3 Cyt C浓度标准曲线
在最优的催化实验条件下,改变Cyt C浓度,淬灭效率变化趋势如图6所示。在Cyt C低浓度(0.2~1 μmol/L)内,线性回归方程y=10.260 7x+0.408 4,线性相关系数R2=0.972 12(图6-a)。在Cyt C高浓度(2~10 μmol/L)内,线性回归方程y=0.793 3x+11.554 4,线性相关系数R2=0.999 11(图6-b)。随着Cyt C浓度升高,单位时间内生成的产物如Fe4+或Fe5+的配合物或H2O2反应产物如羟基自由基、超氧阴离子自由基等活性氧物种数量增多,与荧光物质作用更频繁,荧光强度变化更显著,淬灭效率升高[17]。
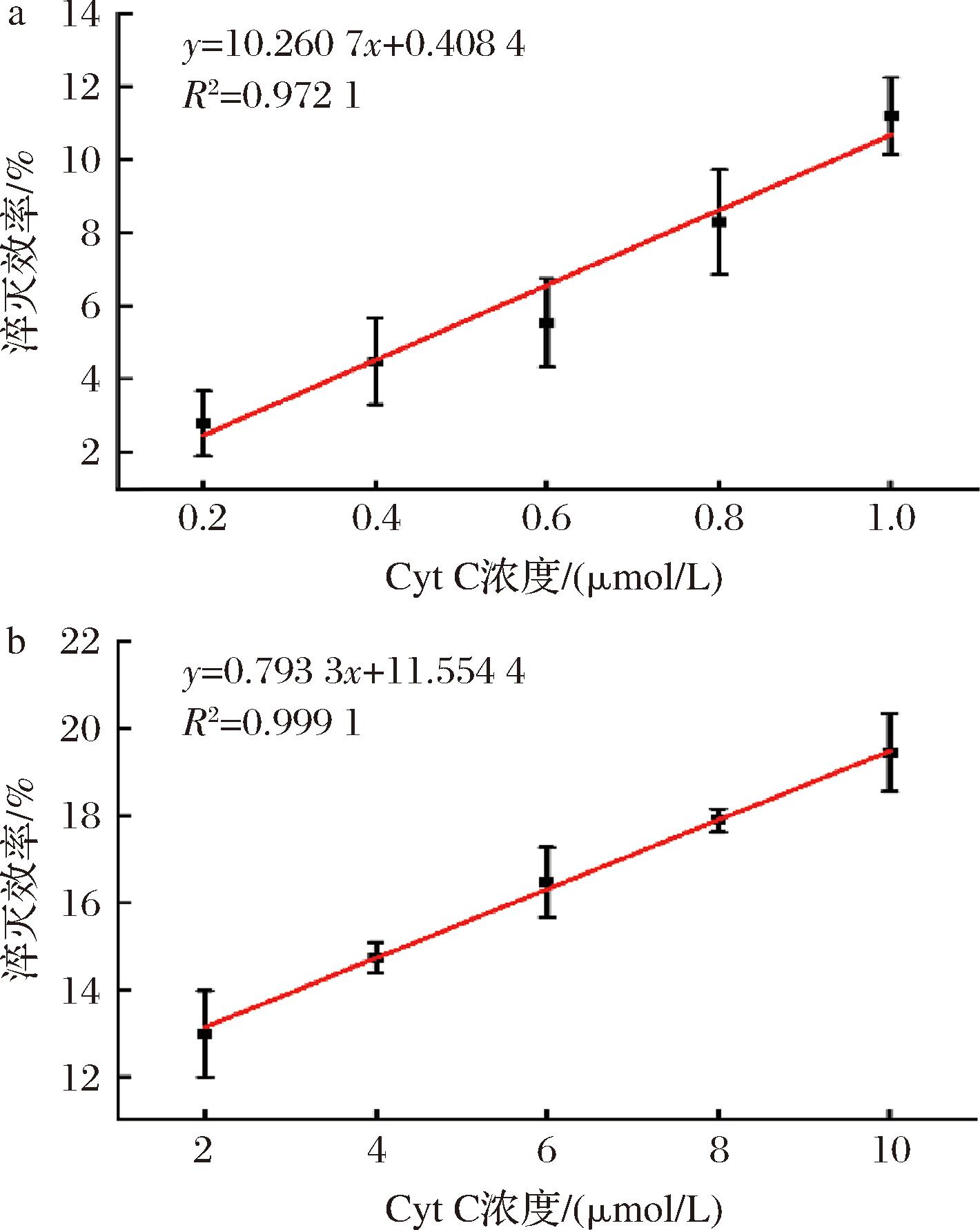
a-Cyt C低浓度;b-Cyt C高浓度
图6 淬灭效率与Cyt C浓度关系曲线
Fig.6 Relationship curve between quenching efficiency and concentration of Cyt C
在H2O2-Cyt C体系中,低浓度(0~1 μmol/L)范围标曲斜率较大,而高浓度(2~10 μmol/L)范围斜率变小,其可能原因为产物抑制效应的增强:大量Cyt C氧化产物吸附在AuNCs表面,形成电子传递屏障或荧光恢复位点(如通过配体交换修复纳米簇结构),阻碍H2O2与荧光核心的接触[18]。即使Cyt C继续催化生成中间产物,AuNCs的荧光淬灭效率也会因表面钝化而提升有限,从而导致斜率减小。
2.4 H2O2-Cyt C体系的选择性实验
为了验证Cyt C对AuNCs荧光淬灭体系的选择性,选择常见的离子(Na+、K+、Cl-)、相关生物分子(DNA酶、RNA酶、GSH)和常见过氧化物酶(CAT、MPO)进行对照实验,实验结果如图7所示,仅Cyt C组出现显著荧光淬灭,而其他干扰物质组的荧光淬灭效率均低于5%。其可能原因是Cyt C作为酶催化剂,通过催化H2O2生成羟基自由基、超氧阴离子自由基等活性氧物质,特异性攻击AuNCs表面,导致荧光淬灭[17],而其他物质无法触发该催化反应。CAT、MPO等干扰组的荧光淬灭效率均显著低于Cyt C组。这是由于Cyt C的催化活性中心(血红素基团)与H2O2的结合模式不同于其他CAT,其特异性氧化BSA的能力是荧光淬灭的关键。表明体系对Cyt C的识别依赖于其酶活性位点,而非静电作用或非特异性吸附。
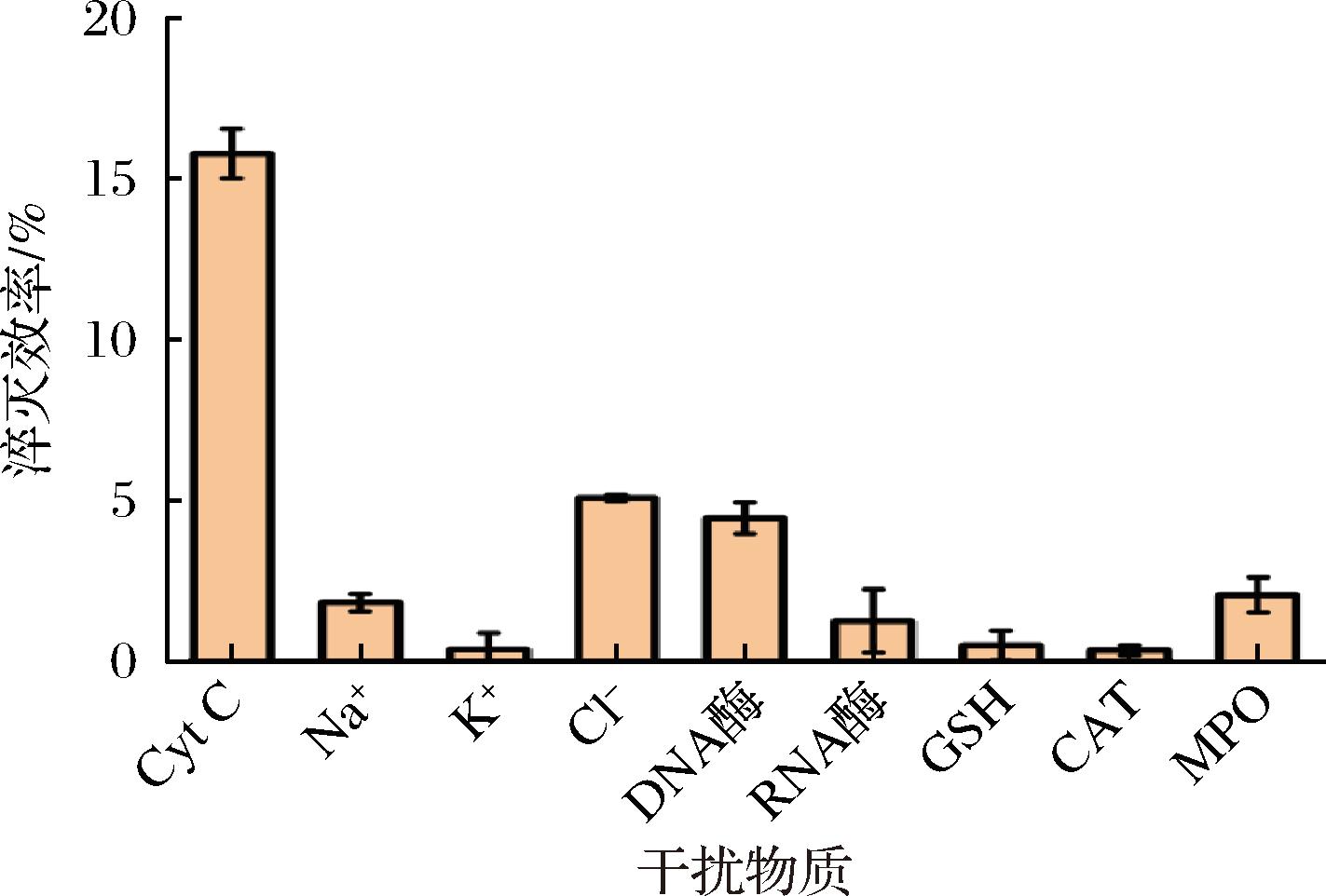
图7 各干扰物质淬灭效率图
Fig.7 Quenching efficiency diagram of each interfering substance
2.5 AuNCs体系对细胞内Cyt C的荧光成像分析
2.5.1 AuNCs的细胞毒性实验
为探究该体系在细胞生理过程检测中的适用性,首先使用CCK-F试剂盒对不同浓度AuNCs与细胞孵育不同时间的细胞毒性进行了研究,实验结果如图8所示。在相同AuNCs浓度下,随着孵育时间延长(6~24 h),细胞存活率逐渐降低,表明AuNCs对细胞的毒性作用随时间积累增强,但仍处于低毒性。在相同孵育时间下,随着AuNCs浓度升高(40~400 μmol/L),细胞存活率缓慢下降。分析原因可能是:1)高浓度AuNCs可能通过物理吸附或聚集,影响细胞膜的通透性和完整性,导致细胞损伤[19];2)AuNCs可能诱导细胞内活性氧生成,引发氧化应激,损伤细胞内生物大分子(如DNA、蛋白质、脂质),从而抑制细胞活性[20-21];3)AuNCs表面的金离子(如Au+或Au3+)释放可能干扰细胞内正常的离子平衡和酶活性,导致细胞功能紊乱[22-23]。AuNCs整体来说对细胞具有低毒性,在不同浓度孵育24 h之后,仍然保持80%以上的细胞存活率,为使实验中细胞维持一个较好的活性,本研究选择在长时间孵育24 h后仍然保持85%以上活性的浓度,也就是200 μmol/L进行后续的实验。
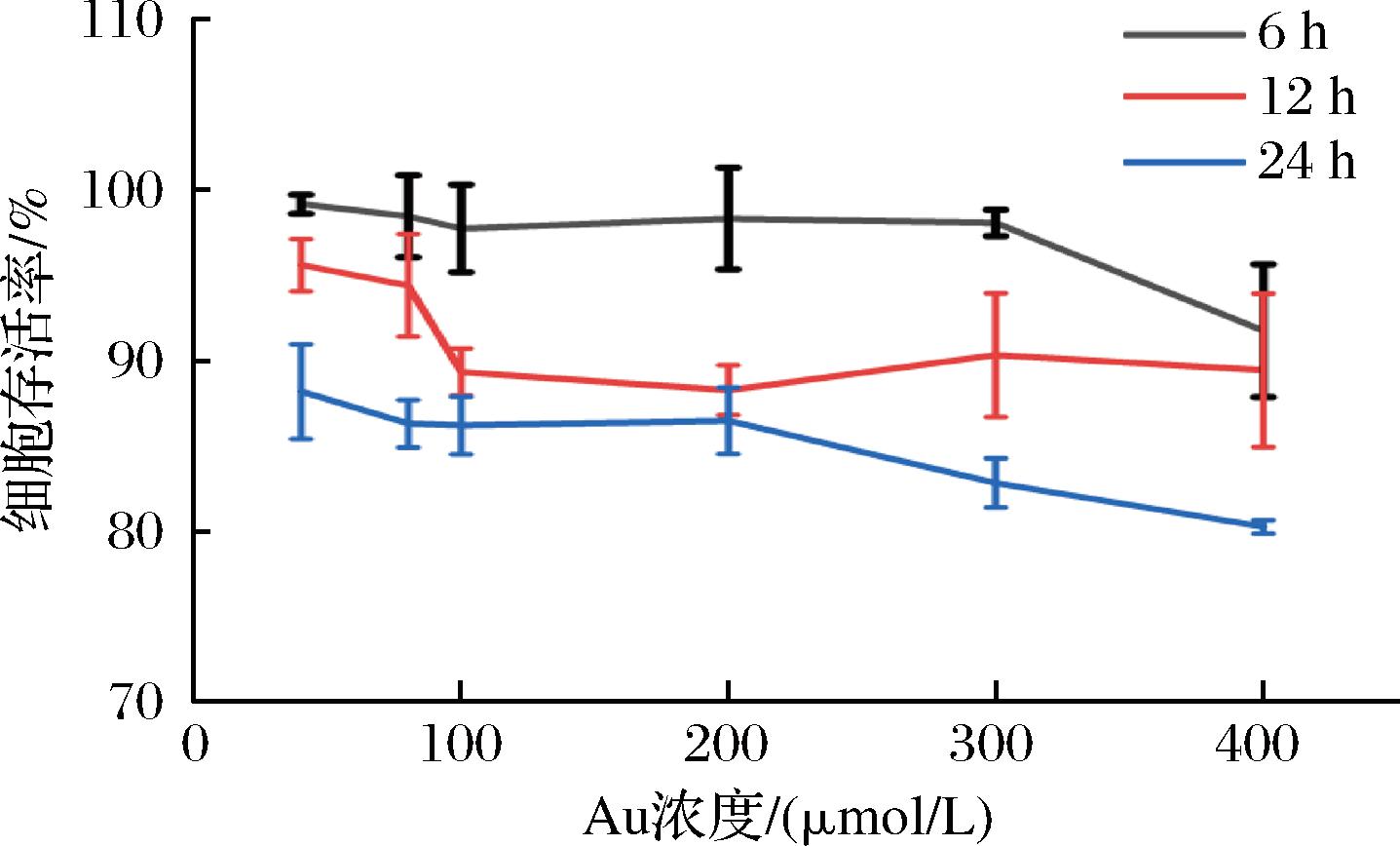
图8 各时间浓度-效应关系图
Fig.8 Concentration-effect relationship graph at each time
2.5.2 AuNCs的共聚焦成像实验
结合共聚焦显微成像技术,利用所设计的AuNCs荧光探针对毒素诱导的HepG2细胞凋亡过程中Cyt C的释放进行了成像分析,并进行了不进行毒素诱导的阴性对照组实验,如图9-a所示,蓝色是细胞核染料DAPI的荧光,对细胞进行定位。红色是AuNCs的荧光,得到荧光强度无明显变化,证明AuNCs在细胞环境中具有一定稳定性,不会随着孵育时间的延长而发生荧光淬灭。有毒素刺激的实验结果如图9-b所示。AuNCs的荧光强度逐渐减弱,是由于细胞凋亡产生Cyt C和活性氧,Cyt C发挥其酶活催化作用,促进活性氧与AuNCs的反应,导致其荧光淬灭,荧光强度逐渐下降。通过Image J对红色通道图像进行分析,得到了不同孵育时间下AuNCs的平均荧光强度(图10-a),再根据淬灭效率公式求值并作图得到图10-b,随着棒曲霉素孵育时间的延长,AuNCs荧光强度逐渐降低,而AuNCs荧光淬灭效率逐渐增大。可能原因为:棒曲霉素刺激导致了细胞凋亡,而细胞凋亡产生Cyt C,随着孵育时间延长,所产生的Cyt C含量也会增加,从而AuNCs荧光被淬灭,荧光强度下降,淬灭效率增大[23-24]。
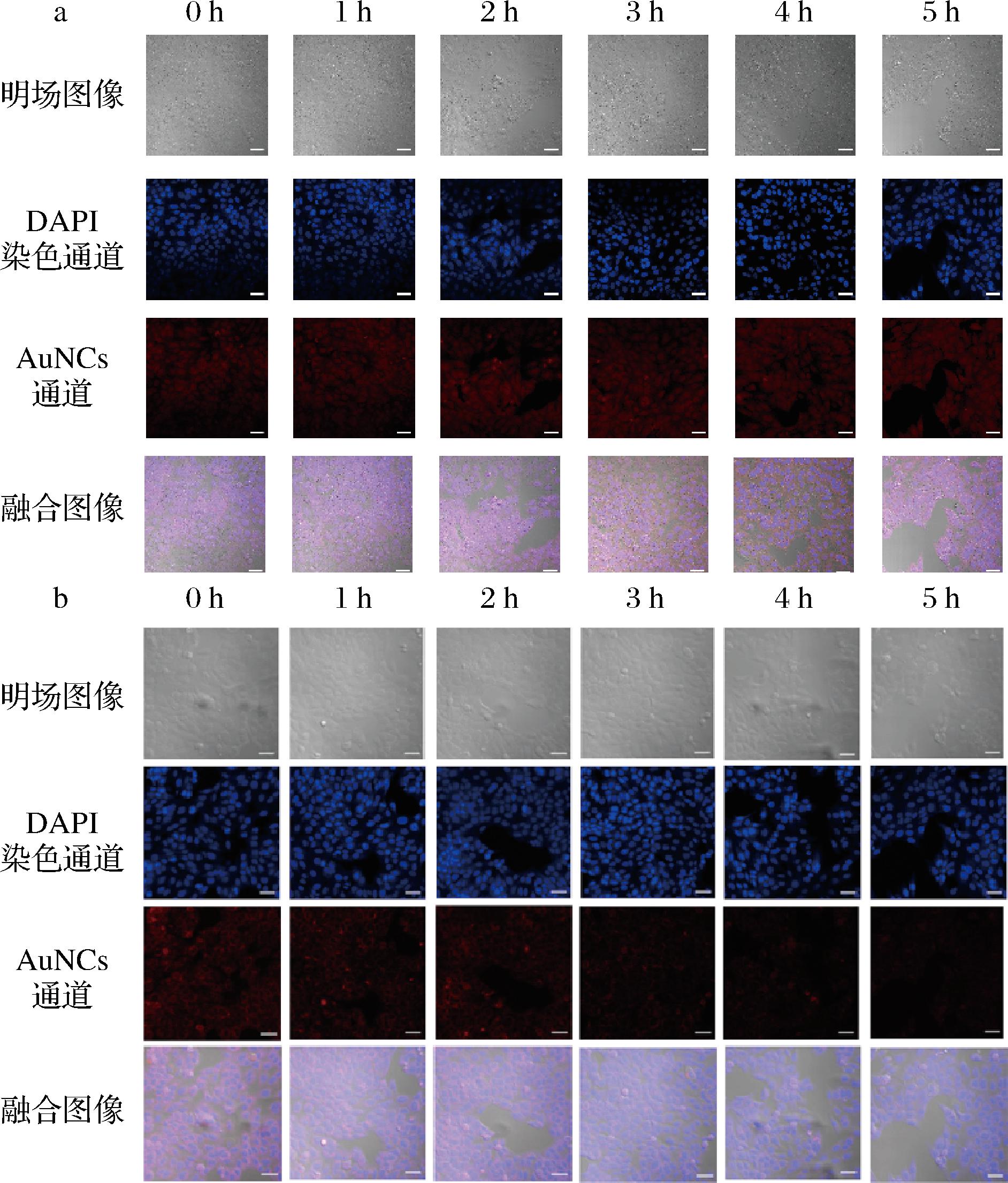
a-不进行毒素诱导的阴性对照实验的共聚焦成像;b-棒曲霉素与HepG2细胞共孵育不同时间的共聚焦荧光成像
图9 AuNCs共聚焦成像图
Fig.9 Confocal imaging of AuNCs
注:标尺为50 μm。
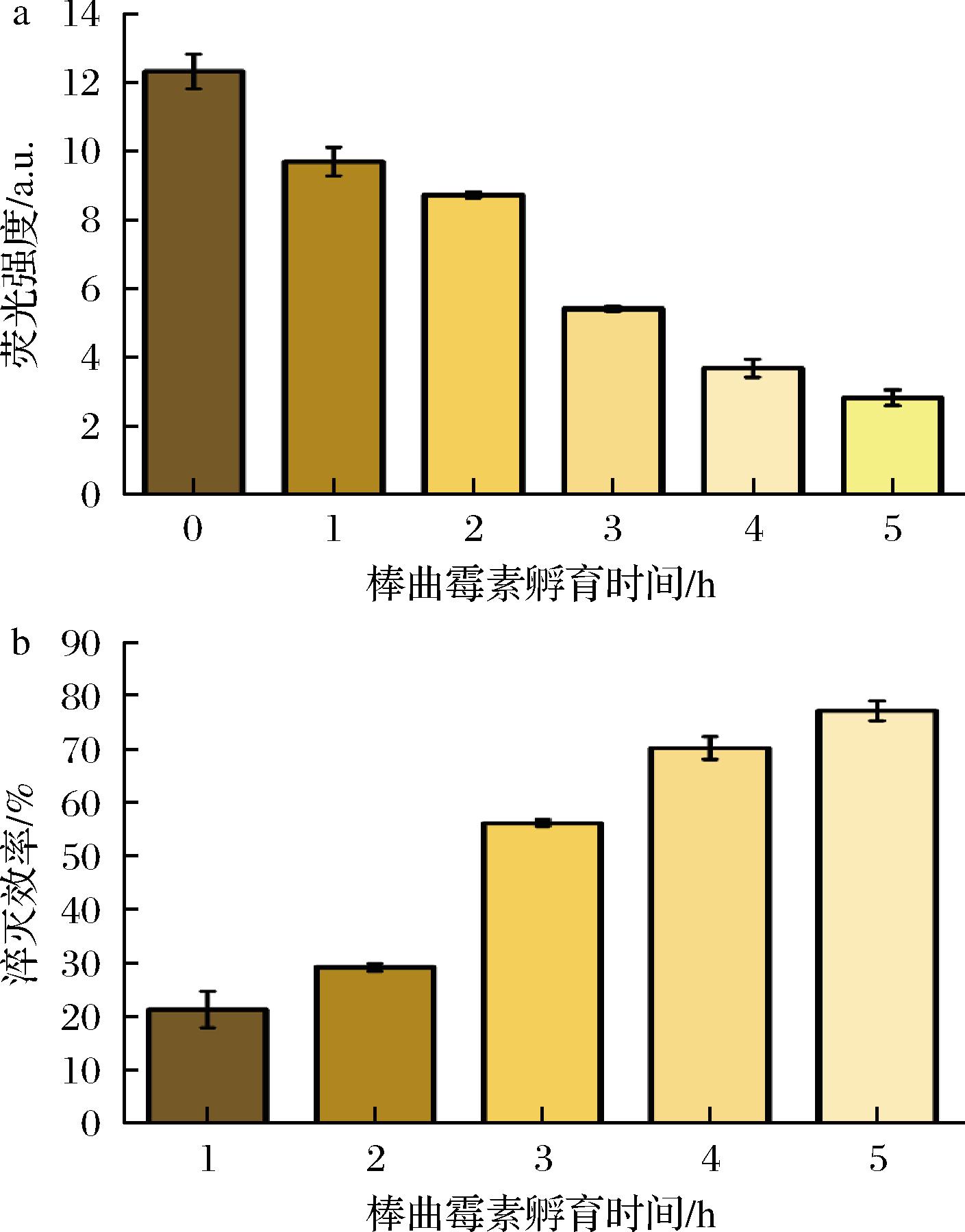
a-荧光强度;b-淬灭效率
图10 荧光强度及淬灭效率与孵育时间关系图
Fig.10 Relationship between fluorescence intensity and quenching efficiency and incubation time
3 结论
本研究通过BSA还原法合成粒径均一的AuNCs,构建“H2O2-Cyt C-AuNCs”荧光检测体系,优化确定50 μmol/L H2O2、30 ℃水浴5 min、2.5 μmol/L的AuNCs最优浓度为最佳条件,建立Cyt C两段浓度梯度标准曲线,体系对Cyt C具有高选择性,AuNCs细胞毒性低(400 μmol/L处理24 h存活率>80%),实现了毒素诱导细胞凋亡过程中Cyt C的实时成像分析,为生物样本中Cyt C的快速检测提供了新方法。
[1] 张心. 光电化学传感器的制备及在人源细胞色素c检测中的应用[D].衡阳:南华大学,2024.ZHANG X.Preparation of photoelectrochemical sensor and its application in the detection of human cytochrome C[D].Hengyang:University of South China, 2024.
[2] HILBERS F, VAN WONDEREN J, LORENZEN W, et al.The catalase activity of the aa 3 cytochrome c oxidase from Paracoccus denitrificans[J].Biochimica et Biophysica Acta (BBA) - Bioenergetics, 2012, 1817:S108.
[3] 杨敏, 张博叶, 段倩倩.镉离子修饰的金纳米簇对汞离子的快速检测[J].微纳电子技术, 2020, 57(7):556-561;567.YANG M, ZHANG B Y, DUAN Q Q.Rapid detection of Hg2+ by Cd2+-modified gold nanoclusters[J].Micronanoelectronic Technology, 2020, 57(7):556-561;567.
[4] 丛雨洁.光功能金纳米簇复合体系的设计制备及其生物应用[D].北京:北京科技大学, 2024.CONG Y J.Design and preparation of photofunctional gold nanocluster composite system and its biological application[D].Beijing:University of Science and Technology Beijing, 2024.
[5] 王松柏, 董晓芮, 李文艳, 等.金纳米团簇检测食品中NO2-的综合实验设计[J].实验技术与管理, 2024, 41(2):127-134.WANG S B, DONG X R, LI W Y, et al.Comprehensive experimental design for detecting NO2- in food using gold nanoclusters[J].Experimental Technology and Management, 2024, 41(2):127-134.
[6] 吴一帆. 金纳米簇在生物分子过氧化氢和细胞色素C检测方面的应用研究[D].西安:陕西师范大学, 2019.WU Y F.Application of gold nanoclusters in the detection of hydrogen peroxide and cytochrome C in biomolecules[D].Xi’an:Shaanxi Normal University, 2019.
[7] 杨欣, 吴支行, 叶寅, 等.店埠河农业小流域水体溶解性有机质三维荧光光谱的平行因子分析[J].光谱学与光谱分析, 2022, 42(3):978-983.YANG X, WU Z H, YE Y, et al.Parallel factor analysis of fluorescence excitation emission matrix spectroscopy of DOM in waters of agricultural watershed of dianbu river[J].Spectroscopy and Spectral Analysis, 2022, 42(3):978-983.
[8] LIU T X, WANG Y, LI X M, et al.Redox dynamics and equilibria of c-type cytochromes in the presence of Fe(Ⅱ) under anoxic conditions:Insights into enzymatic iron oxidation[J].Chemical Geology, 2017, 468:97-104.
[9] 叶青, 徐红斌, 刘洋.基于细胞色素C双通道比率型生物传感器快速测定液体乳中的过氧化氢[J].中国乳品工业, 2023, 51(7):56-59.YE Q, XU H B, LIU Y.Rapid determination of hydrogen peroxide in liquid milk based on cytochrome C dual-channel ratiometric biosensor[J].China Dairy Industry, 2023, 51(7):56-59.
[10] ZHANG Q, CHEN Z H, LI J L, et al.The deubiquitinase OTUD1 stabilizes NRF2 to alleviate hepatic ischemia/reperfusion injury[J].Redox Biology, 2024, 75:103287.
[11] 陈丽芳. “比较过氧化氢在不同条件下的分解”实验改进[J].生物学通报, 2024, 59(11):55-58.CHEN L F.Experimental improvement on comparing the decomposition of hydrogen peroxide under different conditions[J].Bulletin of Biology, 2024, 59(11):55-58.
[12] SEMENOVA M A, BOCHKOVA Z V, SMIRNOVA O M, et al.Charged amino acid substitutions affect conformation of neuroglobin and cytochrome c heme groups[J].Current Issues in Molecular Biology, 2024, 46(4):3364-3378.
[13] 蔺首睿, 王立旭, 姜秀娥, 等.纳米金三明治结构调制细胞色素c电子传递特性的分子机理研究[J].电化学, 2012, 18(3):264-269.LIN S R, WANG L X, JIANG X E, et al.Studies on the molecular mechanism of electron transfer of cytochrome c modulated by gold nanoparticles in nano-sandwich architecture[J].Journal of Electrochemistry, 2012, 18(3):264-269.
[14] LI P, ZHAN D P, SHAO Y H.Room temperature ionic liquid templated meso-macroporous material by self-assembled giant gold nanoparticles and its enhancement on room temperature ionic liquid templated meso-macroporous material by self-assembled giant gold nanoparticles and its enhance[J].Journal of Electrochemistry, 2014, 20(4):323-332.
[15] 胥彦琪. 蛋白质保护的金纳米簇为荧光探针检测甲磺酸帕珠沙星[J].现代化工, 2017, 37(9):203-205.XU Y Q.Detection of pazufloxacin mesylate by protein-protected gold nanoclusters[J].Modern Chemical Industry, 2017, 37(9):203-205.
[16] YAO Q F, ZHU M, YANG Z C, et al.Molecule-like synthesis of ligand-protected metal nanoclusters[J].Nature Reviews Materials, 2025, 10(2):89-108.
[17] SCHLAMADINGER D E, KATS D I, KIM J E.Quenching of tryptophan fluorescence in unfolded cytochrome c:A biophysics experiment for physical chemistry students[J].Journal of Chemical Education, 2010, 87(9):961-964.
[18] 欧丽娟, 李京, 张超群, 等.氧化反应调控的金纳米簇“关—开”型荧光探针检测过氧化氢和葡萄糖[J].光谱学与光谱分析, 2022, 42(12):3757-3761.OU L J, LI J, ZHANG C Q, et al.Redox-controlled turn-on fluorescence sensor for H2O2 and glucose using DNA-template gold nanoclusters[J].Spectroscopy and Spectral Analysis, 2022, 42(12):3757-3761.
[19] ZHOU J J, LI X H, HE P Y, et al.Implantable versatile oxidized bacterial cellulose membrane for postoperative HNSCC treatment via photothermal-boosted immunotherapy[J].Nano Research, 2023, 16(1):951-963.
[20] ENEA M, PEREIRA E, PEIXOTO DE ALMEIDA M, et al.Gold nanoparticles induce oxidative stress and apoptosis in human kidney cells[J].Nanomaterials, 2020, 10(5):995.
[21] ZHOU Z P, LI D, FAN X Y, et al.Gold nanoclusters conjugated berberine reduce inflammation and alleviate neuronal apoptosis by mediating M2 polarization for spinal cord injury repair[J].Regenerative Biomaterials, 2021, 9:rbab072.
[22] 张柳, 吴琪, 曲广波, 等.四膜虫摄取与外排AuNPs和Au(Ⅲ)的差异及单细胞异质性分析[J].环境化学, 2023, 42(7):2163-2170.ZHANG L, WU Q, QU G B, et al.Uptake and efflux of AuNPs and ionic Au(Ⅲ)by Tetrahymena thermophila and the single-cell heterogeneity[J].Environmental Chemistry, 2023, 42(7):2163-2170.
[23] SHI H W, RUDOLPH M, LI J, et al.Bidentate N-ligand-assisted gold redox catalysis with hydrogen peroxide[J].Nature Chemistry, 2025, 17(6):822-834.
[24] 林茜池. 构建金纳米光学探针用于监测呕吐毒素诱导的细胞凋亡标志物[D].无锡:江南大学, 2023.LIN Q C.Construction of gold nano-optical probes for monitoring markers of apoptosis induced by vomitoxin[D].Wuxi:Jiangnan University, 2023.