宁夏枸杞(Lycium barbarum L.),茄科枸杞属落叶灌木植物,其干燥果实是唯一列入《中国药典》的品种,富含多糖、黄酮、类胡萝卜素、甜菜碱、精胺/亚精胺等多种活性成分[1]。现代研究表明,枸杞具有降血糖[2]、抗衰老[3]、神经保护[4]、抗炎[5]等功效。
作为药食同源佳品,枸杞自古以来就在经典名方中发挥着重要作用[6]。炮制是中医用药的独有特色之一,历代医家在临床实践中对枸杞炮制方法不断创新,由早期以生药为主逐步发展到生熟异治,且不同年代炮制方法不尽相同,不同医家同名而异法,不同地域医家因地制宜、因材制宜、因人制宜,发展出各具特色的炮制方法[7]。《中国药典》和其他各地炮制规范记载的炮制方法大多只有净制,记载的枸杞干燥方法有热风烘干和晒干,“夏、秋二季果实呈红色时采收,热风烘干,除去果梗,或晾至皮皱后,晒干,除去果梗”,对于烘干时间、温度等均无规定[8],因此,晒干与热风烘干是过去一个时期枸杞的传统炮制工艺。但随着干燥技术与装备的不断更新升级,枸杞炮制也引入了新方法,真空脉动干燥、真空冷冻干燥已逐步应用于枸杞干果规模化生产。
作为食品,其理化、营养及活性作用等特性受到加工方法的显著影响,其中不同干燥技术的应用在食品领域受到广泛研究。热风干燥和微波干燥可获得相对含量较高的枸杞多糖,且多糖分子质量较小、抗氧化活性高,真空冷冻干燥则可获得较好的感官品质,但多糖含量较少[9]。与自然晾晒、热风干燥相比,超声辅助协同远红外干燥可增加枸杞表面的微孔数量,减少对表皮细胞的损伤,降低干燥过程的传质阻力,加快干燥过程,且一定频率的超声波处理能够显著提高干果中多糖和黄酮含量[10]。射频-热风组合分段干燥比自然干燥或热风干燥更省时,有效保留了枸杞中的多糖、抗坏血酸、甜菜碱等成分[11]。直触式超声远红外协同干燥显著保持了枸杞中维生素C、甜菜碱的含量[12]。冷冻真空干燥枸杞色泽和复水性较好,但其总酚含量、黄酮含量较低[13];与热风干燥枸杞相比,真空冷冻干燥枸杞饱满圆润,体积较大,表面较为光滑,保留了枸杞原有气味,但具有更高的甜度,易产生出糖现象[14]。
本文以4个品种(系)的宁夏枸杞为研究对象,围绕传统炮制工艺(热风干燥)及新型炮制工艺(真空脉动干燥、真空冷冻干燥),利用超高效液相色谱-三重四极杆-线性离子阱质谱联用(ultra-high performance liquid chromatography-quadrupole linear ion trap mass spectrometry,UPLC-QTRAP-MS/MS)技术探究不同炮制工艺及不同种质分别对枸杞化学成分的影响,旨在为枸杞干果品质评价及不同用途枸杞干果筛选与应用提供重要依据。
1 材料与方法
1.1 材料与试剂
4个枸杞主栽及推广品种(系):宁杞1号、宁杞7号、宁农杞15号、宁杞14-02号,宁夏中宁县中杞集团红景山基地,分别编号为LB1、LB2、LB3、LB4;葡萄糖、芦丁、没食子酸,上海源叶生物科技有限公司;三氯乙酸、铁氰化钾、无水乙醇、醋酸缓冲液、FeSO4,美国 Sigma公司;玉米黄素双棕榈酸酯,瑞士CaroteNature公司;甲醇、乙腈、甲基叔丁基醚(色谱纯),Fisher chemical公司;二氯甲烷(色谱纯),北京Mreda Technology公司;二丁基羟基甲苯(butylated hydroxytoluene,BHT)、石油醚、NaCl、无水硫酸钠、KOH、甲醇、Na2CO3等其他试剂均为国产分析纯,天津大茂化学试剂有限公司。
1.2 仪器与设备
BS224S分析天平,德国赛多利斯公司;HH-4数显恒温水浴锅,江苏国华电器有限公司;Laborota 4000真空旋转蒸发仪,德国Heidolph公司;ExionLCTM AD超高效液相色谱、QTRAP 6500串联质谱,美国AB SCIEX公司;Agilent SB-C18色谱柱(2.1 mm×100 mm,1.8 μm),美国Agilent公司;ZG-30真空冷冻干燥设备,杭州创意真空冷冻干燥设备厂。
1.3 实验方法
1.3.1 热风干燥枸杞制备
枸杞鲜果浸入质量分数5%的K2CO3溶液中浸泡1~2 min,捞出淋去多余溶液,生活饮用水淋洗后,控干倒入干燥器皿上,转入托盘均匀铺平,厚度为1~2 cm,放入烘箱中,热风80 ℃烘15 h,转60 ℃烘15 h,45 ℃保温8 h。水分含量≤13%时,取出冷却后装入自封袋,置于干燥器中密封保存备用。
1.3.2 真空脉动干燥枸杞制备
枸杞鲜果放入传送带淋洗,挑出霉烂果,沥干水分,转入托盘均匀铺平,厚度1~2 cm,真空常压脉动比12 min∶3 min,干燥温度65 ℃,干燥时间20 h,50 ℃保温8 h。水分含量≤13%时,取出冷却,装入自封袋,置于干燥器中密封保存备用。
1.3.3 真空冷冻干燥枸杞制备
真空冷冻干燥分为4个阶段:预冻→升华干燥→解析干燥→保温。将枸杞鲜果淋洗沥干水分,装盘平铺,-40 ℃,速冻4 h后进入升华干燥阶段,压力50 Pa,10 ℃干燥10 h,20 ℃干燥8 h;解析干燥阶段,40 ℃下干燥8 h,50 ℃下保温4 h后取出干燥盘,取样移入自封袋,置于干燥器中密封保存,备用。
1.3.4 主要营养及功效成分测定方法
采用蒽酮-硫酸法[15]测定总糖含量(以葡萄糖计);采用苯酚-硫酸法[15]测定多糖含量(以葡萄糖计);采用硝酸铝显色法[15]测定黄酮含量(以芦丁计);采用四氢呋喃提取样品中的类胡萝卜素[16](以玉米黄素双棕榈酸酯计)。
1.3.5 UPLC-QTRAP-MS/MS检测枸杞化学成分组成
样品研磨至粉末状,称取0.10 g粉末,加入体积分数70%甲醇溶液(内标)1.2 mL提取12 h,12 000 r/min,3 min离心后,吸取上清液,过0.22 μm微孔滤膜保存于进样瓶中,备用。
色谱柱Agilent SB-C18(2.1 mm×100 mm,1.8 μm);流动相:A相为超纯水(加入体积分数为0.1%的甲酸),B相为乙腈(加入体积分数0.1%的甲酸);洗脱梯度:0.00 min B相比例为5%,9.00 min内B相比例线性增加到95%,并维持在95% 1 min,10.00~11.10 min,B相比例降为5%,并以5%平衡至14 min;流速0.35 mL/min;柱温40 ℃;进样量2 μL。
电喷雾离子源温度500 ℃;离子喷雾电压5 500 V(正离子模式)/-4 500 V(负离子模式);离子源气体Ⅰ、气体Ⅱ和气帘气分别设置为50、60、25 psi,碰撞诱导电离参数设置为高;QQQ扫描使用MRM模式,并将碰撞气体(N2)设置为中等;通过进一步优化去簇电压(declustering potential,DP)和碰撞能(collision energy,CE),完成各个MRM离子对的DP和CE。根据每个时期内洗脱的代谢物,针对性监测一组特定的多反应监测离子对。利用Met Ware数据库,基于化合物精确质量、MS2碎片信息、MS2碎片同位素分布和保留时间对化合物定性鉴定;定量采用多反应监测模式,四极杆首先筛选目标物质的前体离子(母离子),排除掉其他分子质量物质对应的离子以初步排除干扰;前体离子经碰撞室诱导电离后断裂形成多个碎片离子,碎片离子再通过三重四极杆过滤选择特征碎片离子,排除非目标离子干扰。
1.4 数据处理
采用SPSS 21.0软件对数据进行单因素方差分析,实验结果表示为“平均值±标准差”,P<0.05表示差异显著,具有统计学意义。主成分分析(principal component analysis,PCA)与聚类分析利用R软件内置统计对数据进行归一化处理,并通过R软件heatmap包绘制热图;其他图形采用Origin 2019b软件进行绘图。采用正交偏最小二乘判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA)采用SIMCA软件建立模型,以P值和变量重要性投影(variable importance in projection,VIP)值相结合的方法筛选差异物质,筛选标准为P<0.05,VIP≥1.0,采用多重交叉验证的方法计算模型的VIP值。
2 结果与分析
2.1 不同炮制工艺对枸杞主要营养及功效成分的影响
4个枸杞品种(系)、3种炮制工艺生产的枸杞干果如图1所示。热风干燥枸杞较为干瘪,色泽呈暗红,而真空脉动干燥和真空冷冻干燥枸杞色泽较鲜艳,果型较圆润饱满。
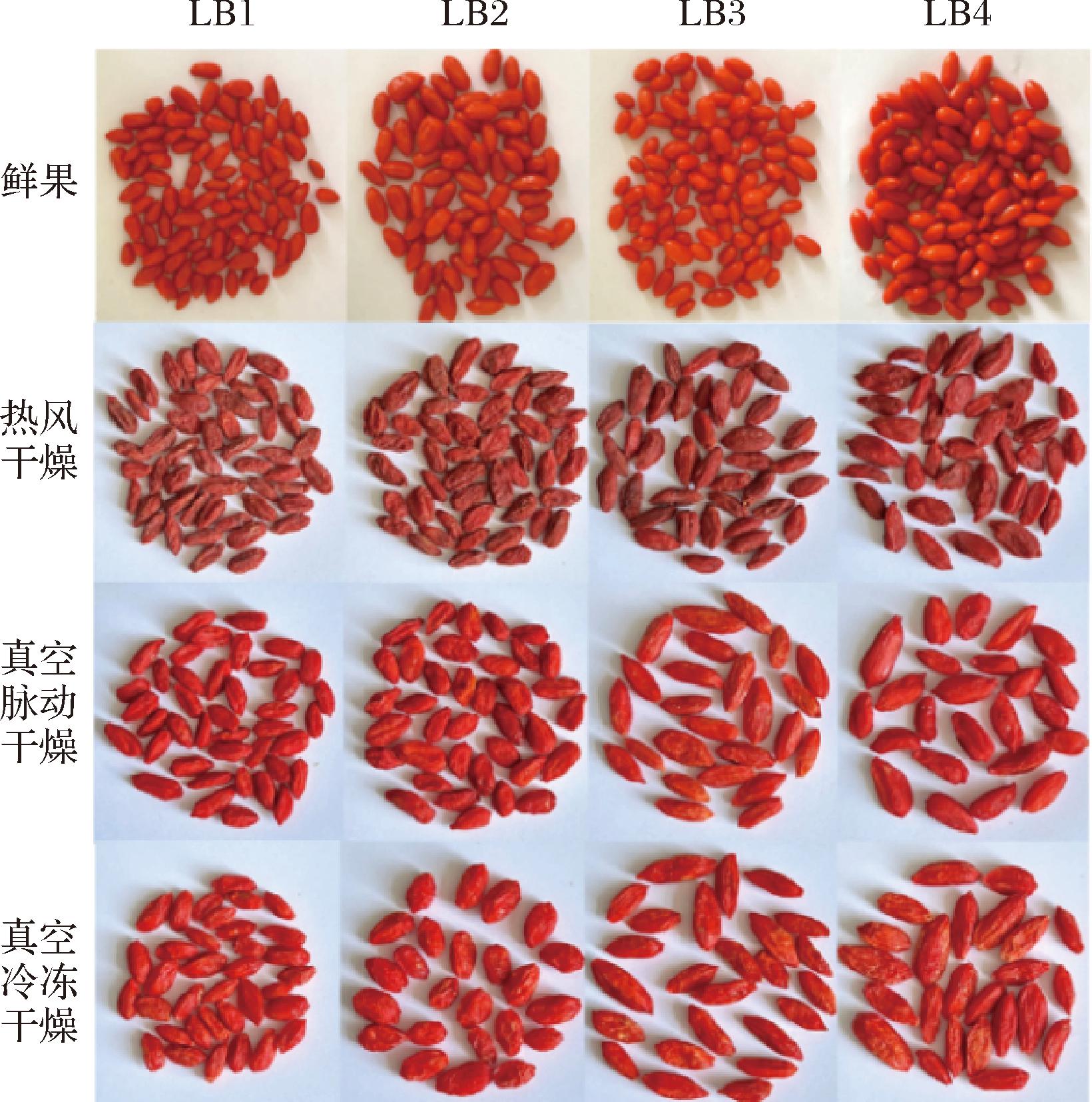
图1 不同炮制工艺生产的枸杞干果
Fig.1 Dried goji berry (Lycium barbarum L.) processed by different techniques
同一枸杞品种下,不同炮制工艺生产的枸杞干果总糖含量差异显著(P<0.05),即真空脉动干燥及热风干燥均大于真空冷冻干燥,且不同的枸杞品种表现出相同的趋势(图2-a)。对于多糖,同一品种下,不同炮制工艺对枸杞干果多糖含量的影响显著(P<0.05),但不同的枸杞品种,不同炮制工艺下对其多糖含量的影响无规律,对于LB2,热风干燥对多糖含量保持较好,而LB1、LB3、LB4在真空冷冻干燥工艺下多糖含量保持较好(图2-b)。4个枸杞品种其黄酮含量变化对炮制工艺的响应具有相同的趋势(图2-c),即热风干燥枸杞中的黄酮含量最高,其次为真空脉动干燥,最后为真空冷冻干燥。对于总类胡萝卜素,同一品种下,不同炮制工艺对枸杞总类胡萝卜素影响显著(P<0.05),但不同品种无一致性规律,热风干燥获得的枸杞干果总类胡萝卜素含量最低,而真空冷冻干燥和真空脉动干燥的枸杞总类胡萝卜素含量相对较高(图2-d)。以上研究结果表明:相较于品种,炮制工艺对枸杞总糖和黄酮的影响更大,而对于多糖和类胡萝卜素,其含量变化除了受干燥技术影响外,还与枸杞品种相关。
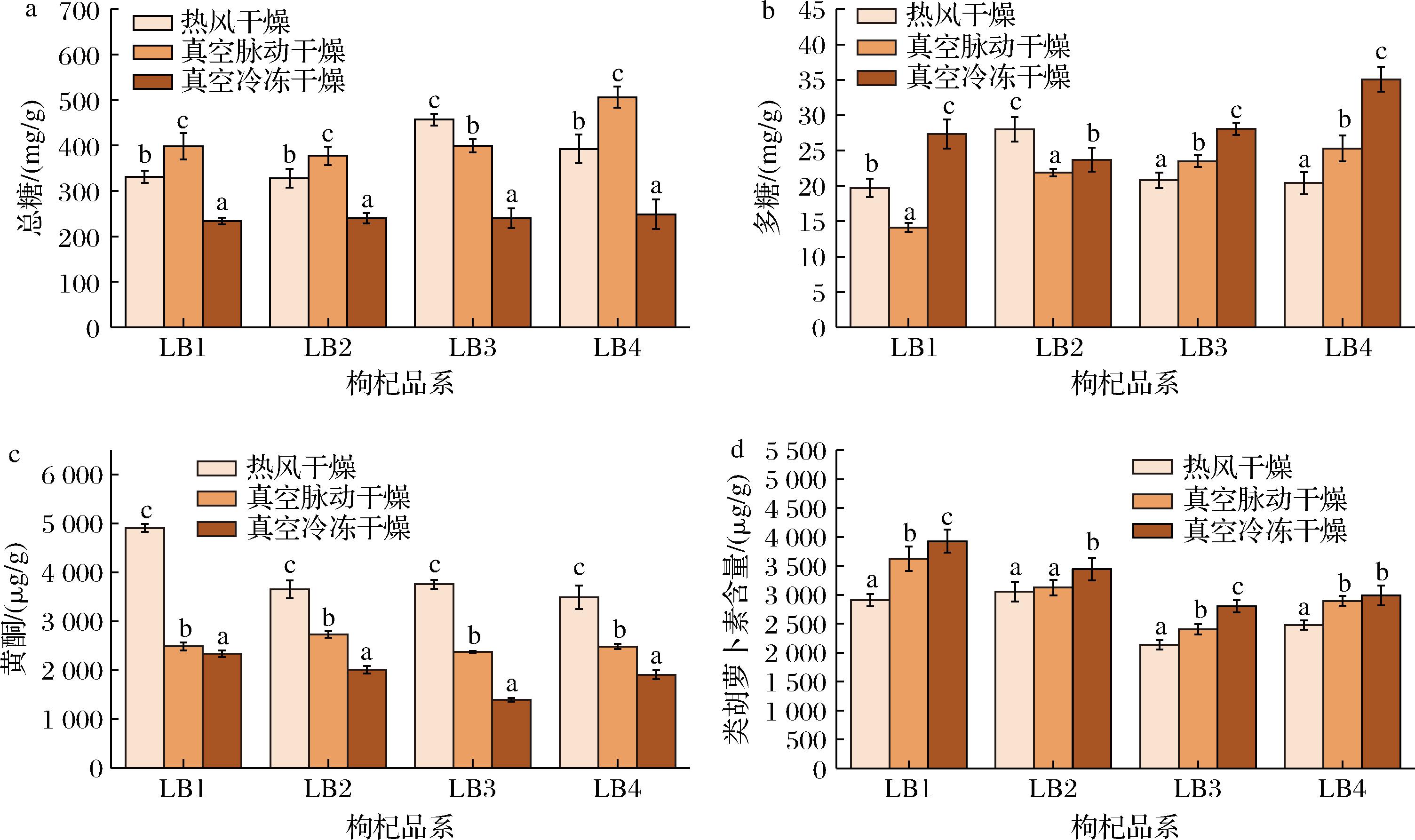
a-总糖;b-多糖;c-黄酮;d-类胡萝卜素
图2 不同炮制工艺对枸杞主要营养及功效成分的影响
Fig.2 Effects of different processing techniques on main nutrition and functional components of goji berry
注:图中组内小写字母不同表示差异显著(P<0.05)。
2.2 基于UPLC-QTRAP-MS/MS分析炮制工艺对枸杞化学成分组成的影响
2.2.1 PCA与聚类分析
基于UPLC-QTRAP-MS/MS技术鉴定出枸杞干果中的化合物825个,主要为生物碱(16.13%)、酚酸(13.99%)、黄酮类化合物(13.11%)、氨基酸及其衍生物(8.72%)。其他物质,包括糖类、醛类、酮类化合物等,约占7.52%。此外,还含有脂类、木脂素和香豆素等物质(图3)。
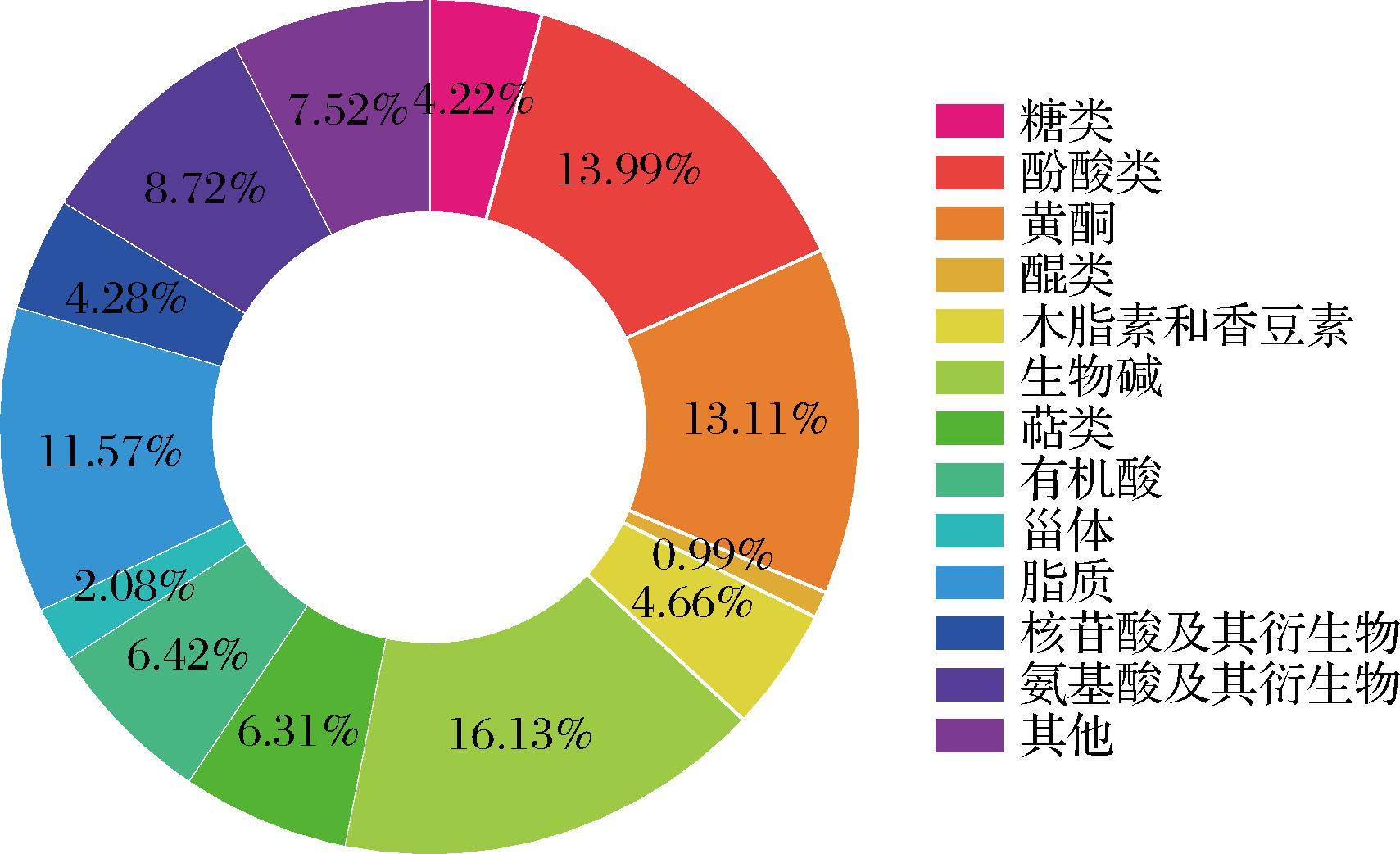
图3 炮制后枸杞化学成分类别组成环形图
Fig.3 Ring diagram of chemical component of goji berry after drying
对枸杞的化学成分进行PCA,结果如图4所示。热风干燥组、真空脉动干燥组和真空冷冻干燥组枸杞样品呈现垂直分布,分别位于PC1轴的左侧、中间和右侧,分组明显,表明不同干燥工艺对枸杞化学成分组成有较大影响,差异集中在PC1上,且真空脉动干燥组和真空冷冻干燥组距离较近,表明热风干燥组与其他2组差异较大。聚类分析可知,热风干燥组聚为一大类,真空脉动干燥组和真空冷冻干燥组聚为一大类,且聚类结果与PCA结果相互印证,表明炮制工艺对枸杞化学成分的影响较大。
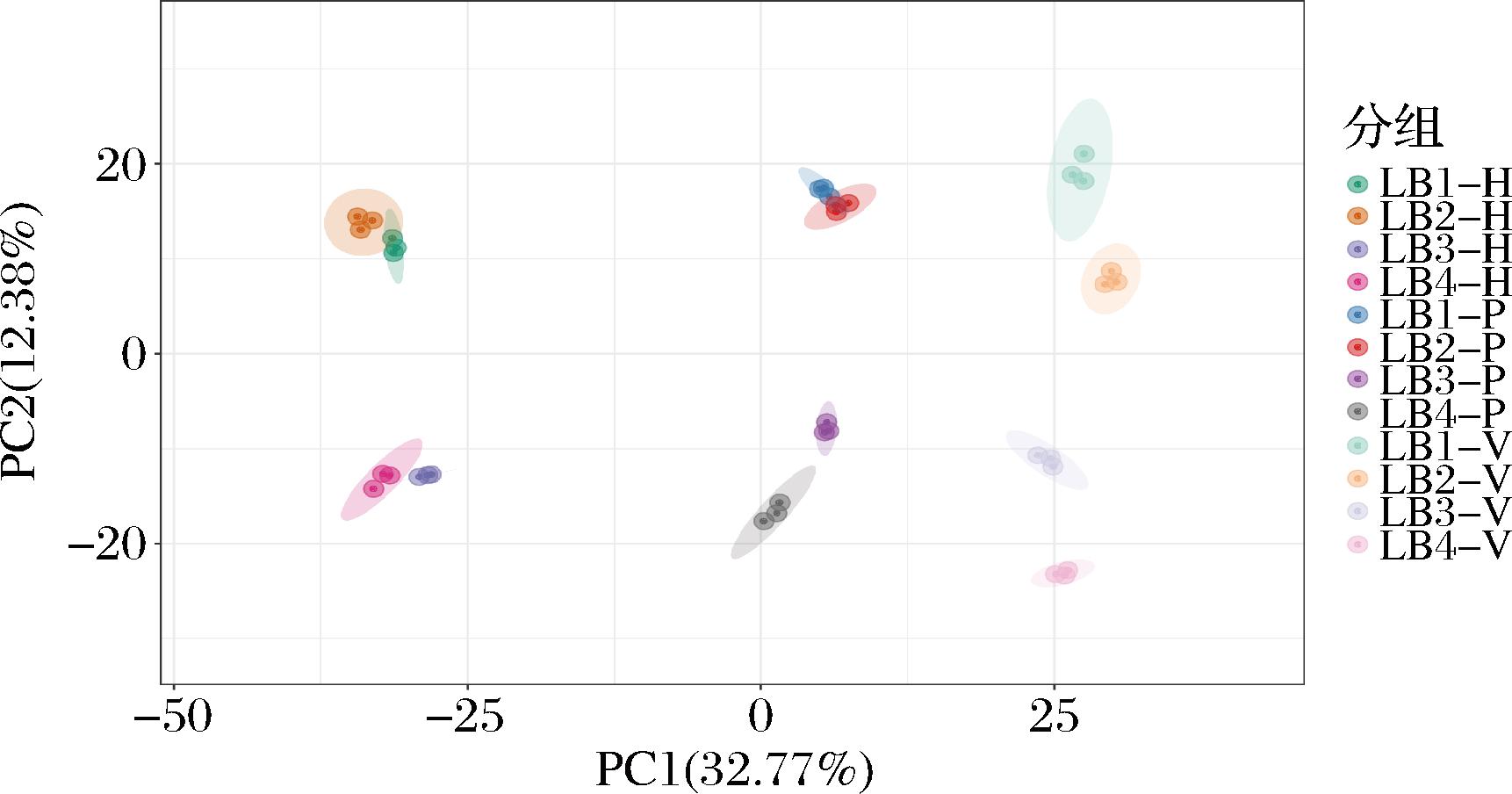
图4 不同炮制工艺下枸杞化学成分PCA得分图和聚类热图
Fig.4 PCA scoring map and cluster heat map of goji berry under different drying techniques
注:热风干燥组(H)、真空脉动干燥组(P)和真空冷冻干燥组(V)(下同)。
为进一步明确不同枸杞品种及炮制工艺对枸杞干果化学成分组成及其含量的影响,以4个枸杞品种(系)不同炮制工艺下的化学成分分别进行PCA和聚类分析(图5)。4个品种(系)基于不同炮制工艺下枸杞化学成分均分组明显,且分布一致,即热风干燥组、真空脉动干燥组和真空冷冻干燥组分别位于PC1轴的左侧、中间和右侧;真空脉动干燥组和真空冷冻干燥组距离较近,表明热风干燥组与其他2组枸杞化学成分组成差异较大,而真空脉动干燥组和真空冷冻干燥2组枸杞化学成分差异较小。在聚类分析中,4个枸杞品种(系)得到一致性结果:热风干燥组为一类,真空脉动干燥组与真空冷冻干燥组聚为一类,并在4个具有代表性的枸杞品种(系)中得以印证,表明相较于品种,炮制工艺对枸杞化学成分的影响作用更大。
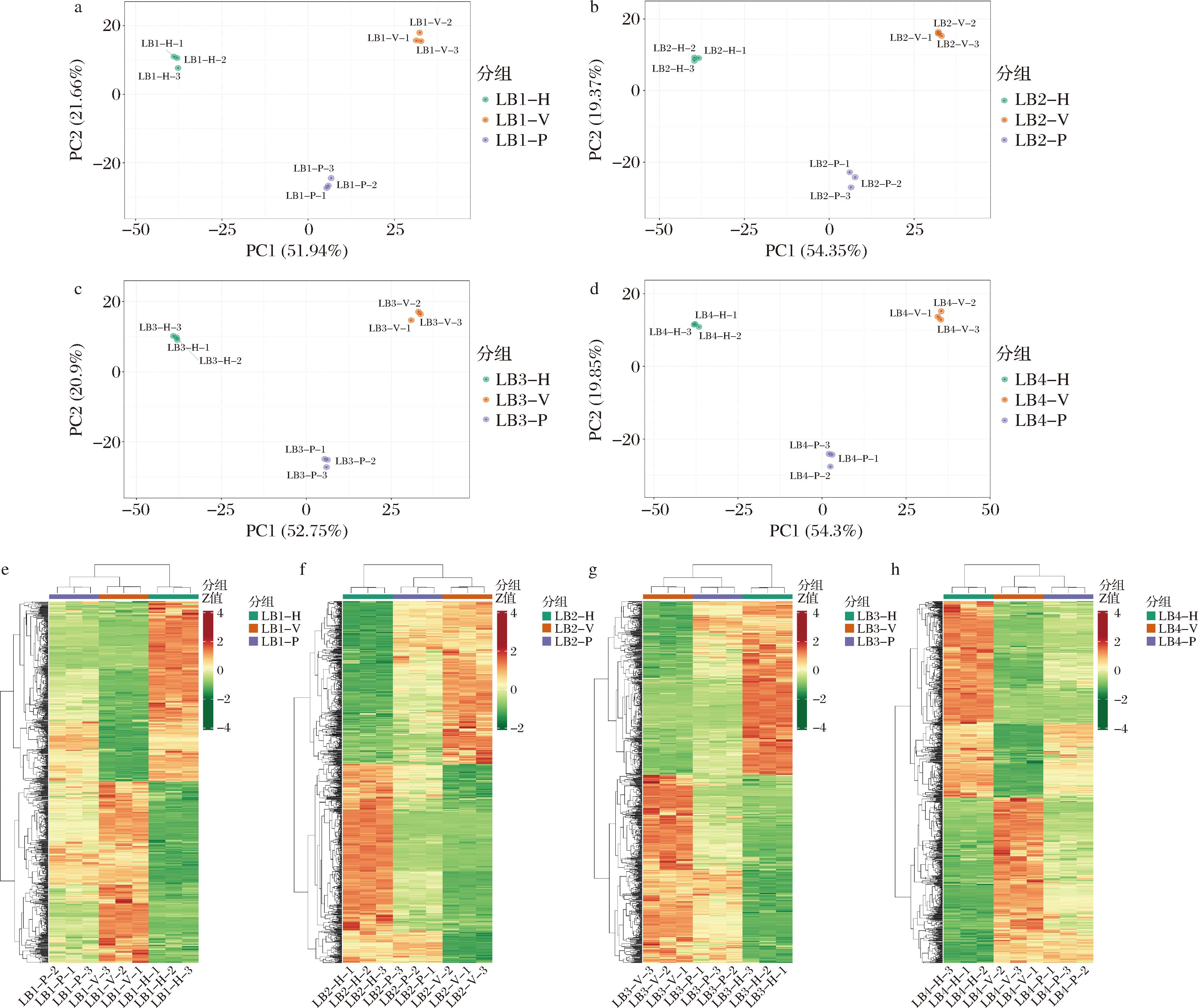
a-LB1 PCA图;b-LB2 PCA图;c-LB3 PCA图;d-LB4 PCA图;e-LB1 聚类热图;f-LB2 聚类热图;g-LB3 聚类热图;h-LB4 聚类热图
图5 不同炮制工艺下不同枸杞品系化学成分PCA得分图及聚类热图
Fig.5 PCA scoring plots and clustering heat map of chemical components of goji under different drying techniques
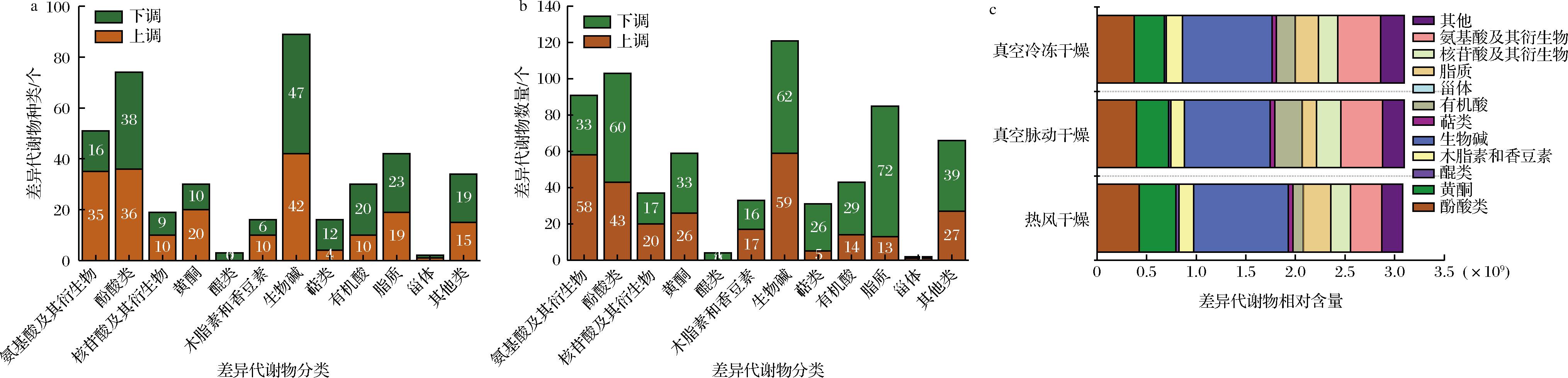
a-真空脉动干燥与热风干燥差异化合物种类;b-真空冷冻干燥与热风干燥差异化合物数量;c-差异化合物相对含量
图6 不同炮制工艺下枸杞干果中的差异化合物
Fig.6 Stacking diagram of chemical composition of goji berry under different drying techniques
2.2.2 差异化合物分析
为深入了解各组样本化合物组成差异情况,采用OPLS-DA进行多元统计分析,根据VIP值≥1.0且P<0.05的标准筛选差异化合物,进一步分析各品种中不同炮制工艺对化学成分组成的影响。如图6-a所示,从差异化合物种类上看,真空脉动干燥组与热风干燥组差异化合物为406种,上调物质为氨基酸及其衍生物、黄酮、木脂素和香豆素、核苷酸及其衍生物,下调物质为生物碱、萜类、有机酸及脂质。真空冷冻干燥组与热风干燥组差异化合物为675种,上调物质为氨基酸及其衍生物、核苷酸及其衍生物、木脂素及香豆素,下调物质主要为酚酸类、黄酮类、醌类、生物碱、有机酸及脂质(图6-b)。从相对含量上看,热风干燥枸杞富集了酚酸、黄酮、生物碱、脂质以及醌类物质,真空脉动干燥组和真空冷冻干燥组枸杞则含有丰富的氨基酸及其衍生物、核苷酸及其衍生物、有机酸和其他类物质(图6-c)。值得注意的是,有机酸种类在热风干燥枸杞中丰富,但累计相对含量远低于真空脉动干燥和真空冷冻干燥的枸杞。
依据上述VIP值≥1.0且P<0.05的标准,将筛选到的差异化合物按照VIP值从大到小排序,排名前15的差异化合物如表1所示,进一步明确这些主要差异化合物在不同炮制工艺下的变化。结果表明,在LB1枸杞中,甲硫氨酸、二氢山柰素、亚氨基二乙酸、天冬氨酸、胡桃苷D、二氢阿魏酸葡萄糖苷、3-脲基丙酸在真空脉动制干组和真空冷冻干燥组相对含量较高(P<0.05),而N-果糖基焦谷氨酸、可替宁葡萄糖苷、N-葡萄糖基对香豆酰腐胺、烟碱-N-葡萄糖醛酸苷、13-过氧化羟基-9Z,11E-十八碳二烯酸则在热风干燥枸杞中显著富集(P<0.05)。
表1 不同炮制工艺下LB1枸杞显著差异化合物
Table 1 Significantly chemical components under different drying techniques of goji berry (LB1)
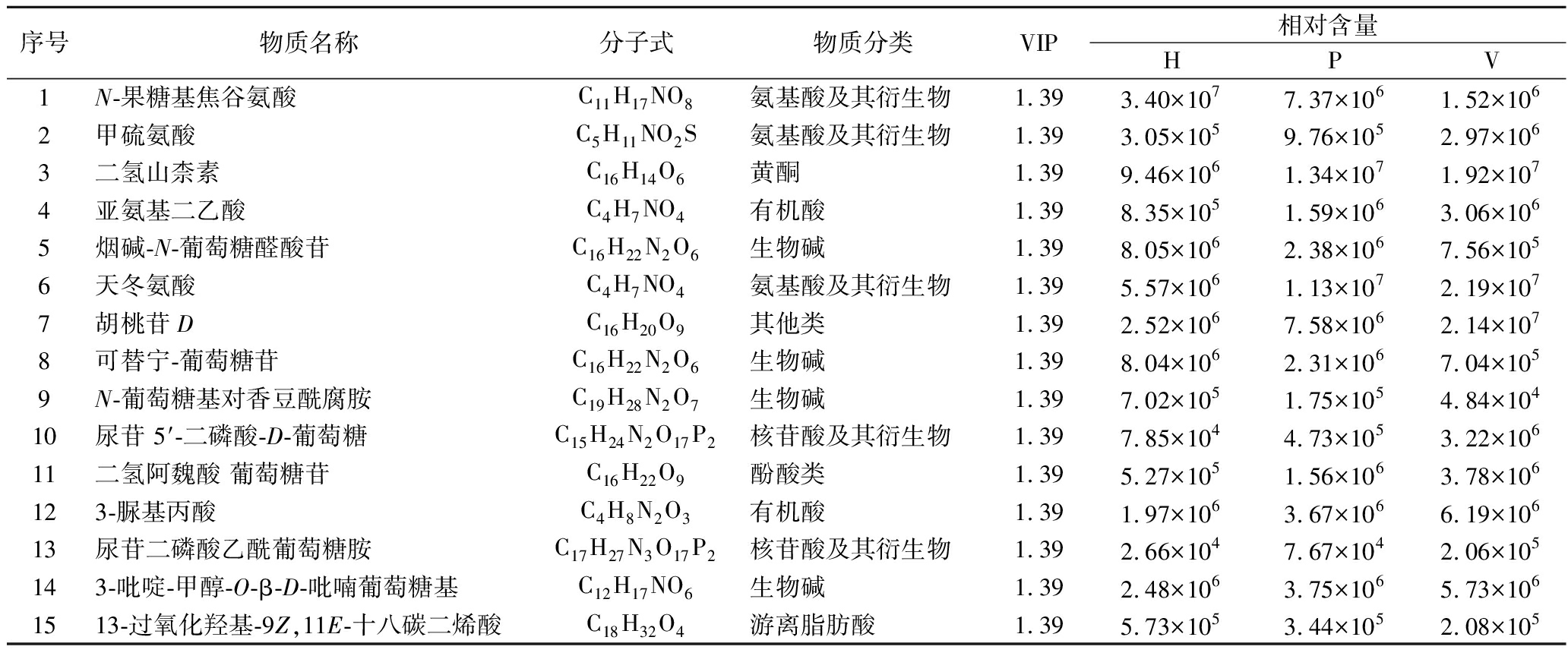
序号物质名称分子式物质分类VIP相对含量HPV1N-果糖基焦谷氨酸C11H17NO8氨基酸及其衍生物1.393.40×1077.37×1061.52×1062甲硫氨酸C5H11NO2S氨基酸及其衍生物1.393.05×1059.76×1052.97×1063二氢山柰素C16H14O6黄酮1.399.46×1061.34×1071.92×1074亚氨基二乙酸C4H7NO4有机酸1.398.35×1051.59×1063.06×1065烟碱-N-葡萄糖醛酸苷C16H22N2O6生物碱1.398.05×1062.38×1067.56×1056天冬氨酸C4H7NO4氨基酸及其衍生物1.395.57×1061.13×1072.19×1077胡桃苷DC16H20O9其他类1.392.52×1067.58×1062.14×1078可替宁-葡萄糖苷C16H22N2O6生物碱1.398.04×1062.31×1067.04×1059N-葡萄糖基对香豆酰腐胺C19H28N2O7生物碱1.397.02×1051.75×1054.84×10410尿苷 5′-二磷酸-D-葡萄糖C15H24N2O17P2核苷酸及其衍生物1.397.85×1044.73×1053.22×10611二氢阿魏酸 葡萄糖苷C16H22O9酚酸类1.395.27×1051.56×1063.78×106123-脲基丙酸C4H8N2O3有机酸1.391.97×1063.67×1066.19×10613尿苷二磷酸乙酰葡萄糖胺C17H27N3O17P2核苷酸及其衍生物1.392.66×1047.67×1042.06×105143-吡啶-甲醇-O-β-D-吡喃葡萄糖基C12H17NO6生物碱1.392.48×1063.75×1065.73×1061513-过氧化羟基-9Z,11E-十八碳二烯酸C18H32O4游离脂肪酸1.395.73×1053.44×1052.08×105
如表2所示,在LB2枸杞筛选出的15种差异化合物中,鸟氨酸在真空脉动制干组和真空冷冻干燥组相对含量较高(P<0.05),而N-果糖基焦谷氨酸、香豆酸甲酯、香草酸、苯丙酮酸、原儿茶酸、2,5-二羟基苯甲酸、2,3-二羟基苯甲酸等酚酸类物质则在热风干燥枸杞中显著富集(P<0.05)。
表2 不同炮制工艺下LB2枸杞显著差异化合物
Table 2 Significantly chemical components under different drying techniques of goji berry (LB2)
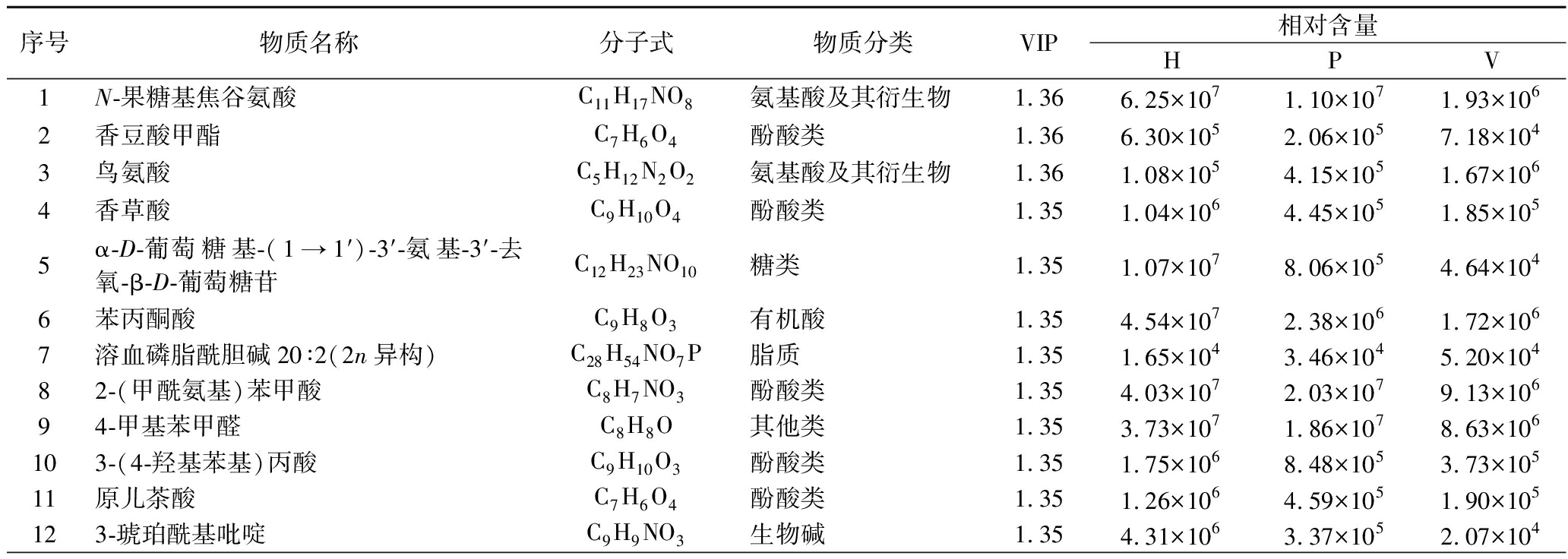
序号物质名称分子式物质分类VIP相对含量HPV1N-果糖基焦谷氨酸C11H17NO8氨基酸及其衍生物1.366.25×1071.10×1071.93×1062香豆酸甲酯C7H6O4酚酸类1.366.30×1052.06×1057.18×1043鸟氨酸C5H12N2O2氨基酸及其衍生物1.361.08×1054.15×1051.67×1064香草酸C9H10O4酚酸类1.351.04×1064.45×1051.85×1055α-D-葡萄糖基-(1→1′)-3′-氨基-3′-去氧-β-D-葡萄糖苷C12H23NO10糖类1.351.07×1078.06×1054.64×1046苯丙酮酸C9H8O3有机酸1.354.54×1072.38×1061.72×1067溶血磷脂酰胆碱20∶2(2n异构)C28H54NO7P脂质1.351.65×1043.46×1045.20×10482-(甲酰氨基)苯甲酸C8H7NO3酚酸类1.354.03×1072.03×1079.13×10694-甲基苯甲醛C8H8O其他类1.353.73×1071.86×1078.63×106103-(4-羟基苯基)丙酸C9H10O3酚酸类1.351.75×1068.48×1053.73×10511原儿茶酸C7H6O4酚酸类1.351.26×1064.59×1051.90×105123-琥珀酰基吡啶C9H9NO3生物碱1.354.31×1063.37×1052.07×104
续表2

序号物质名称分子式物质分类VIP相对含量HPV132,5-二羟基苯甲酸C7H6O4酚酸类1.356.76×1052.32×1056.53×104141-O-菊酯酰奎宁酸C17H22O10酚酸类1.351.03×1055.04×1042.36×104152,3-二羟基苯甲酸C7H6O4酚酸类1.351.21×1064.37×1051.19×105
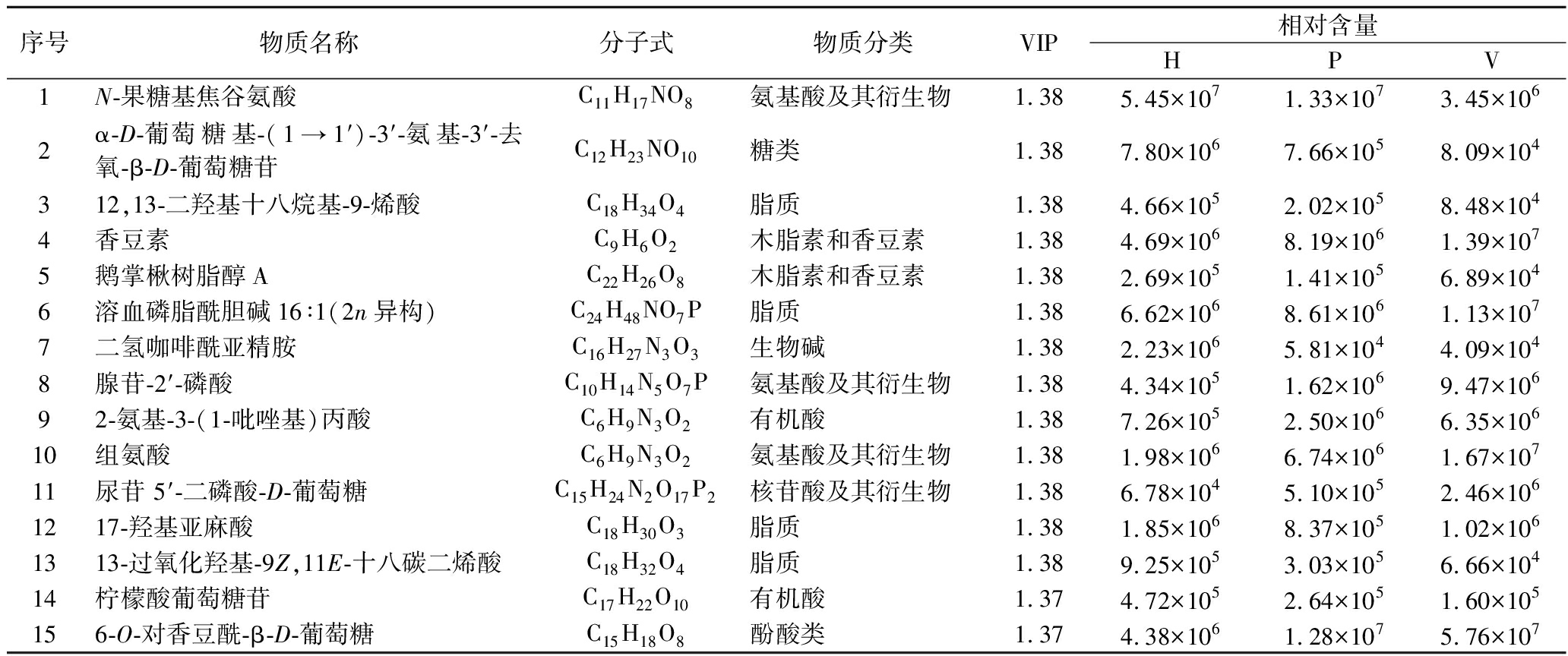
如表3所示,在LB3枸杞中,香豆素、溶血磷脂酰胆碱、腺苷2′-磷酸、2-氨基-3-(1-吡唑基)丙酸、组氨酸、尿苷5′-二磷酸-D-葡萄糖、6-O-对香豆酰-β-D-葡萄糖在真空脉动制干组和真空冷冻干燥组显著富集(P<0.05),而N-果糖基焦谷氨酸、α-D-葡萄糖基-(1→1′)-3′-氨基-3′-去氧-β-D-葡萄糖苷、12,13-二羟基十八烷基-9-烯酸、鹅掌楸树脂醇A、二氢咖啡酰亚精胺、17-羟基亚麻酸、13-过氧化羟基-9Z,11E-十八碳二烯酸、柠檬酸葡萄糖苷在热风干燥枸杞中相对含量较高(P<0.05)。
表3 不同炮制工艺下LB3枸杞显著差异化合物
Table 3 Significantly chemical components under different drying techniques of goji berry (LB3)
序号物质名称分子式物质分类VIP相对含量HPV1N-果糖基焦谷氨酸C11H17NO8氨基酸及其衍生物1.385.45×1071.33×1073.45×1062α-D-葡萄糖基-(1→1′)-3′-氨基-3′-去氧-β-D-葡萄糖苷C12H23NO10糖类1.387.80×1067.66×1058.09×104312,13-二羟基十八烷基-9-烯酸C18H34O4脂质1.384.66×1052.02×1058.48×1044香豆素C9H6O2木脂素和香豆素1.384.69×1068.19×1061.39×1075鹅掌楸树脂醇AC22H26O8木脂素和香豆素1.382.69×1051.41×1056.89×1046溶血磷脂酰胆碱16∶1(2n异构)C24H48NO7P脂质1.386.62×1068.61×1061.13×1077二氢咖啡酰亚精胺C16H27N3O3生物碱1.382.23×1065.81×1044.09×1048腺苷-2′-磷酸C10H14N5O7P氨基酸及其衍生物1.384.34×1051.62×1069.47×10692-氨基-3-(1-吡唑基)丙酸C6H9N3O2有机酸1.387.26×1052.50×1066.35×10610组氨酸C6H9N3O2氨基酸及其衍生物1.381.98×1066.74×1061.67×10711尿苷 5′-二磷酸-D-葡萄糖C15H24N2O17P2核苷酸及其衍生物1.386.78×1045.10×1052.46×1061217-羟基亚麻酸C18H30O3脂质1.381.85×1068.37×1051.02×1061313-过氧化羟基-9Z,11E-十八碳二烯酸C18H32O4脂质1.389.25×1053.03×1056.66×10414柠檬酸葡萄糖苷C17H22O10有机酸1.374.72×1052.64×1051.60×105156-O-对香豆酰-β-D-葡萄糖C15H18O8酚酸类1.374.38×1061.28×1075.76×107
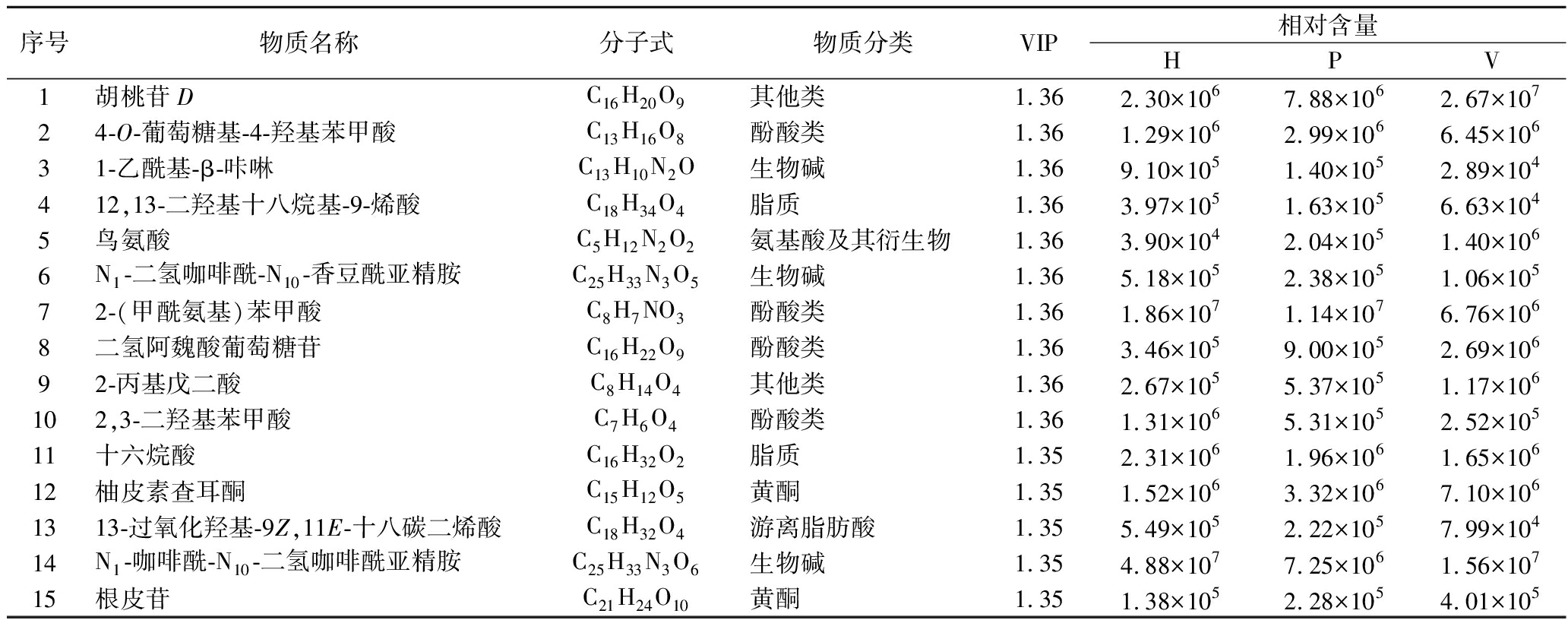
如表4所示,在LB4枸杞中胡桃苷D、4-O-葡萄糖基-4-羟基苯甲酸、鸟氨酸、二氢阿魏酸葡萄糖苷、2-丙基戊二酸、柚皮素查耳酮、根皮苷在真空脉动制干组和真空冷冻干燥组显著富集(P<0.05),而1-乙酰基-β-咔啉、12,13-二羟基十八烷基-9-烯酸、N1-二氢咖啡酰-N10-香豆酰亚精胺、2-(甲酰氨基)苯甲酸、2,3-二羟基苯甲酸、十六烷酸、13-羟基过氧-9Z,11E-十八碳二烯酸、N1-咖啡酰-N10-二氢咖啡酰亚精胺则在热风干燥组相对含量较高(P<0.05)。
表4 不同炮制工艺下LB4枸杞显著差异化合物
Table 4 Significantly chemical components under different drying techniques of goji berry (LB4)
序号物质名称分子式物质分类VIP相对含量HPV1胡桃苷DC16H20O9其他类1.362.30×1067.88×1062.67×10724-O-葡萄糖基-4-羟基苯甲酸C13H16O8酚酸类1.361.29×1062.99×1066.45×10631-乙酰基-β-咔啉C13H10N2O生物碱1.369.10×1051.40×1052.89×104412,13-二羟基十八烷基-9-烯酸C18H34O4脂质1.363.97×1051.63×1056.63×1045鸟氨酸C5H12N2O2氨基酸及其衍生物1.363.90×1042.04×1051.40×1066N1-二氢咖啡酰-N10-香豆酰亚精胺C25H33N3O5生物碱1.365.18×1052.38×1051.06×10572-(甲酰氨基)苯甲酸C8H7NO3酚酸类1.361.86×1071.14×1076.76×1068二氢阿魏酸葡萄糖苷C16H22O9酚酸类1.363.46×1059.00×1052.69×10692-丙基戊二酸C8H14O4其他类1.362.67×1055.37×1051.17×106102,3-二羟基苯甲酸C7H6O4酚酸类1.361.31×1065.31×1052.52×10511十六烷酸C16H32O2脂质1.352.31×1061.96×1061.65×10612柚皮素查耳酮C15H12O5黄酮1.351.52×1063.32×1067.10×1061313-过氧化羟基-9Z,11E-十八碳二烯酸C18H32O4游离脂肪酸1.355.49×1052.22×1057.99×10414N1-咖啡酰-N10-二氢咖啡酰亚精胺C25H33N3O6生物碱1.354.88×1077.25×1061.56×10715根皮苷C21H24O10黄酮1.351.38×1052.28×1054.01×105
综上所述,氨基酸及其衍生物、核苷酸及其衍生物、有机酸等物质在真空脉动干燥和真空冷冻干燥枸杞中得到较好的保留;而热风干燥作为传统的枸杞炮制工艺,在炮制过程中富集了更多的酚胺、酚酸及脂质等物质。
2.2.3 差异化合物富集代谢通路分析
基于KEGG数据库对不同炮制工艺产生的差异化合物进行代谢通路富集分析,通过显著性检验P值,分析不同炮制工艺下枸杞化学成分潜在的变化机制。如图7所示,LB1-H vs LB1-P vs LB1-V中,差异化合物显著富集在氨基酸生物合成、氨基酸代谢、氨酰-tRNA生物合成、丙烷哌啶和吡啶生物碱生物合成、各种植物次生代谢产物生物合成等通路;LB2-H vs LB2-P vs LB2-V中,差异化合物富集在氨基酰-tRNA生物合成、苯丙氨酸代谢、D-氨基酸代谢、色氨酸代谢、苯丙酮生物合成等途径(P<0.05);LB3-H vs LB3-P vs LB3-V中,差异化合物富集在氨酰-tRNA生物合成、色氨酸代谢、甘氨酸、丝氨酸和苏氨酸代谢、精氨酸生物合成(P<0.05);LB4-H vs LB4-P vs LB4-V中,差异化合物显著富集在辅因子生物合成、碳代谢、D-氨基酸代谢、氨酰-tRNA生物合成。以上结果表明,不同炮制工艺主要影响枸杞氨基酸代谢、氨酰-tRNA生物合成、生物碱及苯丙素的生物合成等途径。
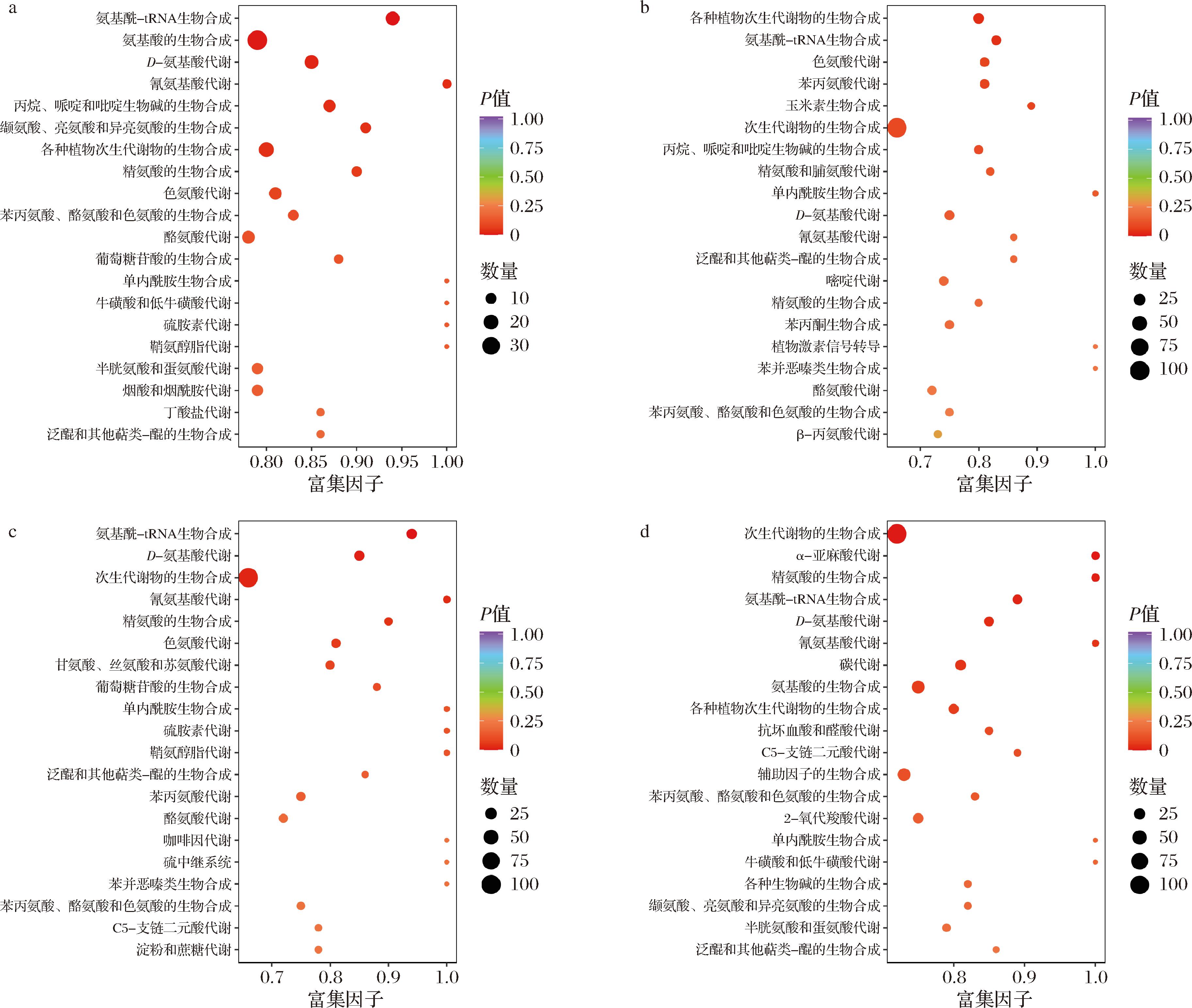
a-LB1-H vs LB1-P vs LB1-V;b-LB2-H vs LB2-P vs LB2-V;c-LB3-H vs LB3-P vs LB3-V;d-LB4-H vs LB4-P vs LB4-V
图7 不同炮制工艺下枸杞差异化合物KEGG富集代谢通路气泡图
Fig.7 Bubble diagram of KEGG-enriched metabolic pathway for different chemical components of goji berry under different drying techniques
3 讨论
枸杞多糖是枸杞中重要的功能成分之一,含量丰富(5%~8%),主要由葡萄糖、半乳糖、阿拉伯糖、半乳糖醛酸和葡萄糖醛酸等单糖通过不同形式糖苷键连接而成,并含有多种微量元素及蛋白质,分子质量在8~241 kDa[17]。本研究中,枸杞干果多糖含量变化除了受炮制工艺因素影响外,还与枸杞品种相关;在同一品种下,不同炮制工艺对枸杞干果多糖含量的影响显著(P<0.05),热风干燥枸杞多糖含量低于真空冷冻干燥(LB1、LB3、LB4),这与吴励萍等[18]研究结果一致,即热风干燥的枸杞多糖含量偏低。研究表明,在富含糖类及氨基酸的食物基质中易发生美拉德反应,尤其是在后期阶段还原酮、Strecker降解产物发生羟醛缩合和二乙醇胺缩合反应导致含氮聚合物的形成,产生大量呋喃、吡咯、吡啶、吡嗪及羰基化合物[19],影响食物营养、色泽与风味。枸杞同时富含糖类和氨基酸,在干燥过程中,随着加热的持续进行,不同炮制工艺下发生不同程度的美拉德反应,并伴随着多种氨基酸代谢,如苯丙氨酸代谢、色氨酸代谢、甘氨酸代谢、丝氨酸代谢等,以及哌啶和吡啶的生物合成,但真空脉动干燥与真空冷冻干燥由于产生了一定真空度,相较于热风干燥,干燥温度更低,因此,发生的美拉德反应历程也有所不同。本研究中,枸杞中二氢咖啡酰亚精胺、N1-咖啡酰-N10-二氢咖啡酰亚精胺、N-葡萄糖基对香豆酰腐胺等生物碱物质发生了显著变化,并在热风干燥组中富集。但美拉德反应是否是枸杞传统炮制方法促使其产生中药药理作用的关键因素有待进一步研究。
对于枸杞中的黄酮,热风干燥枸杞黄酮含量高于真空脉动干燥和真空冷冻干燥。李朋亮等[20]研究结果表明,不同干燥方式枸杞总黄酮含量从大到小依次为:热风烘干>晒干>冻干>鲜果,且差异显著,与本文结果相符;吴励萍等[18]研究发现脱蜡后40 ℃热风干燥组,黄酮含量最高;未脱蜡-40 ℃热风干燥组和红外干燥组次之;真空冷冻干燥组总黄酮量最低,也与本研究结果一致,即热风干燥枸杞黄酮含量高于真空冷冻干燥。已有研究表明,低温干燥会使黄酮含量增加的主要原因是植物细胞壁破裂,促进黄酮类化合物释放而不破坏结构,但高温(80 ℃以上)则会影响黄酮类化合物的保留[21-23]。果蔬中苯丙氨酸的变化涉及黄酮合成途径,在苯丙氨酸解氨酶、肉桂酸4-羟化酶的作用下发生羟基化反应,转化为香豆酸,在4-香豆酸辅酶A、查耳酮合成酶的催化下生成柚皮素查耳酮,并在其相关酶的催化下异构化形成黄烷酮进入其他类黄酮的合成途径[24]。枸杞干燥过程中,柚皮素查耳酮在真空脉动干燥组和真空冷冻干燥组的相对含量较高(P<0.05)。羟基酚酸类物质,如2,3-二羟基苯甲酸、2,5-二羟基苯甲酸、2-(甲酰氨基)苯甲酸及3,4-二羟基苯甲酸(原儿茶酸),在水果成熟、衰老及加工过程中存在[25-26],本研究中,这几种物质及香豆酸甲酯、香草酸等在热风干燥的枸杞中较为丰富。已有的研究表明,羟基酚酸类物质可激活抗氧化酶表达的Nrf2信号通路,从而减少氧化应激及其导致的高血压的内皮功能障碍,减少心血管疾病引发的炎症反应[27],同时这类物质还具有较好的抗氧化活性和抗菌活性,为枸杞营养及功效评价等研究提供参考。
类胡萝卜素是枸杞主要的呈色物质和活性成分,其释放依赖于干燥过程诱导的基质变化[28]。由于热效应及组织内水分的迁移耗散,类胡萝卜素常会发生复杂的降解反应并产生挥发性降异戊二烯物质。类胡萝卜素是枸杞主要的呈色物质和功效成分,其含量变化直接影响枸杞干果色泽。本研究中,热风干燥枸杞色泽较真空脉动干燥和真空冷冻干燥枸杞色泽更暗,易吸潮黏结,这与石胜强[14]、ZENG等[29]研究结果一致。此外,热风干燥的枸杞总类胡萝卜素含量较低,表明高温影响枸杞中类胡萝卜素的保留。研究证实,热处理会导致类胡萝卜素从反式向顺式转化,并伴随热降解[30],产生β-紫罗兰酮、β-环柠檬醛和二氢猕猴桃内酯等挥发性成分[18]。真空冷冻干燥可使β-胡萝卜素稳定性增强[31-32],且结合多次冻融处理可抑制类胡萝卜素降解,并保护枸杞干果色泽[32],因此,真空冷冻干燥一定程度上可减少类胡萝卜素降解和色泽损失。除营养成分外,真空冷冻干燥枸杞具有较好的感官品质,外观饱满圆润、内部孔隙小、壁薄、复水率高、表面积大[29,32],同时颜色鲜艳明亮、口感酥脆。此外,真空脉动干燥的枸杞也同样具备色泽鲜艳、明亮的特点。因此,相较于传统热风干燥,真空冷冻干燥和真空脉动干燥的枸杞具有更好的外观品质。
4 结论
本研究明确了炮制工艺对枸杞主要功效成分的响应规律:相较于品种,炮制工艺对枸杞总糖和黄酮的影响更大,而对于多糖和类胡萝卜素,其含量变化除受炮制工艺因素影响外,还与枸杞品种密切相关。炮制后,枸杞中主要的化学成分为生物碱(16.13%)、酚酸(13.99%),黄酮类化合物(13.11%),氨基酸及其衍生物(8.72%)。基于不同炮制工艺下的枸杞聚类分级明显,热风干燥组与真空脉动干燥组的差异化合物数量(406种)低于真空冷冻干燥组与热风干燥组(675种),相较于真空脉动干燥,真空冷冻干燥枸杞与传统热风干燥的枸杞在化学成分组成上存在更多差异,这些差异化合物主要富集在氨基酸代谢、氨酰-tRNA生物合成、哌啶和吡啶生物碱的生物合成、苯丙素生物合成等通路。其中,氨基酸及其衍生物、核苷酸及其衍生物、有机酸等物质在真空脉动干燥和真空冷冻干燥枸杞中富集;而热风干燥作为枸杞传统的炮制工艺,在加工过程中形成了更多的酚胺及酚酸类物质。本研究可为枸杞干果品质评价及不同用途枸杞干果筛选提供理论依据。
[1] ZHAO J H, XU Y H, LI H X, et al.Metabolite-based genome-wide association studies enable the dissection of the genetic bases of flavonoids, betaine and spermidine in wolfberry (Lycium)[J].Plant Biotechnology Journal, 2024, 22(6):1435-1452.
[2] ZHOU W T, YANG T T, XU W Q, et al.The polysaccharides from the fruits of Lycium barbarum L.confer anti-diabetic effect by regulating gut microbiota and intestinal barrier[J].Carbohydrate Polymers, 2022, 291:119626.
[3] DE FREITAS RODRIGUES C, RAMOS BOLDORI J, VALANDRO SOARES M, et al.Goji berry (Lycium barbarum L.) juice reduces lifespan and premature aging of Caenorhabditis elegans:Is it safe to consume it?[J].Food Research International, 2021, 144:110297.
[4] SUN Z Q, LIU J F, LUO W, et al.Lycium barbarum extract promotes M2 polarization and reduces oligomeric amyloid-β-induced inflammatory reactions in microglial cells[J].Neural Regeneration Research, 2022, 17(1):203-209.
[5] ZHANG N, HE Z J, HE S Y, et al.Insights into the importance of dietary Chrysanthemum flower (Chrysanthemum morifolium cv.Hangju)-wolfberry (Lycium barbarum Fruit) combination in antioxidant and anti-inflammatory properties[J].Food Research International, 2019, 116:810-818.
[6] 李静, 余意, 张小波, 等.药用枸杞本草考证[J].世界中医药, 2019, 14(10):2593-2597.LI J, YU Y, ZHANG X B, et al.Research on medicinal fructus lycii[J].World Chinese Medicine, 2019, 14(10):2593-2597.
[7] 赵佳琛, 金艳, 闫亚美, 等.经典名方中枸杞及地骨皮的本草考证[J].中国现代中药, 2020, 22(8):1269-1286.ZHAO J C, JIN Y, YAN Y M, et al.Herbal textual research on “lycii fructus” and “lycii cortex” in Chinese classical prescriptions[J].Modern Chinese Medicine, 2020, 22(8):1269-1286.
[8] 中华人民共和国卫生部药典委员会. 中华人民共和国药典[M].北京:中国医药科技出版社, 2020.Pharmacopoeia Committee of the Ministry of Health of the People’s Republic of China.Pharmacopoeia of the People’s Republic of China [M].Beijing:China Medical Science and Technology Press, 2020.
[9] FENG L, TANG N C, LIU R J, et al.Effects of different processing methods on bioactive substances and antioxidation properties of Lycium barbarum (goji berry) from China[J].Food Bioscience, 2021, 42:101048.
[10] ZHANG Q, WAN F X, ZANG Z P, et al.Effect of ultrasonic far-infrared synergistic drying on the characteristics and qualities of wolfberry (Lycium barbarum L.)[J].Ultrasonics Sonochemistry, 2022, 89:106134.
[11] XU Y R, ZANG Z P, ZHANG Q, et al.Characteristics and quality analysis of radio frequency-hot air combined segmented drying of wolfberry (Lycium barbarum)[J].Foods, 2022, 11(11):1645.
[12] 张倩. 枸杞直触式超声远红外协同干燥特性及传热传质机理研究[D].兰州:甘肃农业大学, 2023.ZHANG Q.Study on the characteristics and heat and mass transfer mechanism of direct contact ultrasonic far infrared synergistic drying of wolfberry[D].Lanzhou:Gansu Agricultural University, 2023.
[13] 宋慧慧,陈芹芹,毕金峰,等.不同干燥方式对鲜枸杞干燥品质的影响[C].中国食品科学技术学会第十四届年会暨第九届中美食品业高层论坛论文摘要集.江苏无锡, 2017:247-248.SONG H H, CHEN Q Q, BI J F, et al.The effects of different drying methods on the drying quality of fresh goji berries [C].The 14th Annual Meeting of the Chinese Institute of Food Science and Technology and the 9th China-US Food Industry Summit Forum.Wuxi, Jiangsu, 2017:247-248.
[14] 石胜强. 枸杞冷冻真空干燥下水分传输与品质研究[D].天津:天津商业大学, 2022.SHI S Q.Study on moisture transfer and quality of Lycium barbarum under freeze-vacuum drying[D].Tianjin:Tianjin University of Commerce, 2022.
[15] 曹建康, 姜微波, 赵玉梅.果蔬采后生理生化实验指导[M].北京:中国轻工业出版社, 2007.CAO J K, JIANG W B, ZHAO Y M.Experimental Instruction of Postharvest Physiology and Biochemistry of Fruit and Vegetable [M].Beijing:China Light Industry Press, 2007.
[16] 米佳, 禄璐, 戴国礼, 等.枸杞色泽与其类胡萝卜素含量和组成的相关性[J].食品科学, 2018, 39(5):81-86.MI J, LU L, DAI G L, et al.Correlations between skin color and carotenoid contents in wolfberry[J].Food Science, 2018, 39(5):81-86.
[17] XIAO Z Y, DENG Q, ZHOU W X, et al.Immune activities of polysaccharides isolated from Lycium barbarum L.What do we know so far?[J].Pharmacology &Therapeutics, 2022, 229:107921.
[18] 吴励萍, 卢有媛, 李海洋, 等.不同干燥方法对枸杞子药材多类型功效成分的影响及其分析评价[J].中草药, 2022, 53(7):2125-2136.WU L P, LU Y Y, LI H Y, et al.Analysis and evaluation of different drying methods for Lycii Fructus based on multi-type functional components[J].Chinese Traditional and Herbal Drugs, 2022, 53(7):2125-2136.
[19] NOOSHKAM M, VARIDI M, BASHASH M.The Maillard reaction products as food-born antioxidant and antibrowning agents in model and real food systems[J].Food Chemistry, 2019, 275:644-660.
[20] 李朋亮, 廖若宇, 王旭, 等.不同干燥方式和除蜡剂对枸杞总黄酮的影响[J].食品科技, 2014, 39(5):79-83.LI P L, LIAO R Y, WANG X, et al.Effect of different drying methods and wax removers on total flavonoid from Lycium barbarum L[J].Food Science and Technology, 2014, 39(5):79-83.
[21] VIDINAMO F, FAWZIA S, KARIM M A.Effect of drying methods and storage with agro-ecological conditions on phytochemicals and antioxidant activity of fruits:A review[J].Critical Reviews in Food Science and Nutrition, 2022, 62(2):353-361.
[22] LOU S N, LAI Y C, HUANG J D, et al.Drying effect on flavonoid composition and antioxidant activity of immature kumquat[J].Food Chemistry, 2015, 171:356-363.
[23] ZHANG H J, TIAN G F, ZHAO C Y, et al.Characterization of polymethoxyflavone demethylation during drying processes of citrus peels[J].Food &Function, 2019, 10(9):5707-5717.
[24] LIU W X, FENG Y, YU S H, et al.The flavonoid biosynthesis network in plants[J].International Journal of Molecular Sciences, 2021, 22(23):12824.
[25] 郭绍雷,许建兰,张斌斌,等.基于广泛靶向代谢组的桃果实衰老软化过程差异代谢物筛选与鉴定[J].江苏农业科学, 2024, 52(6):198-205.GUO S L, XU J L, ZHANG B B, et al.Screening and identification of several metabolites associated with softening and senescence in peach fruit based on widely targeted metabolomics[J].Jiangsu Agricultural Sciences, 2024, 52(6):198-205.
[26] 孙佳欣, 贾程皓, 栾爱萍, 等.‘红菠萝’熟期转色前后果肉中糖酸类代谢物变化特征分析[J/OL].分子植物育种, 2023.https://kns.cnki.net/kcms/detail/46.1068.S.20230815.1152.002.SUN J X, JIA C H, LUAN A P, et al.Analysis of carbohydrates and organic acids metabolites in pineapple flesh(Ananas comosus ‘Red sugar’)[J/OL].Molecular Plant Breeding, 2023.https://kns.cnki.net/kcms/detail/46.1068.S.20230815.1152.002.
[27] ZHANG Z Y, WANG X Y, LI Y X, et al.Evaluation of the impact of food matrix change on the in vitro bioaccessibility of carotenoids in pumpkin (Cucurbita moschata) slices during two drying processes[J].Food &Function, 2017, 8(12):4693-4702.
[28] XIAO Y D, HUANG W Y, LI D J, et al.Thermal degradation kinetics of all-trans and cis-carotenoids in a light-induced model system[J].Food Chemistry, 2018, 239:360-368.
[29] ZENG T, LIU B, BI L S, et al.Effects of different drying methods on quality and water distribution of Lycium barbarum[J].Journal of Food Process Engineering, 2023, 46(12):e14482.
[30] HARNKARNSUJARIT N, CHAROENREIN S, ROOS Y H.Porosity and water activity effects on stability of crystalline β-carotene in freeze-dried solids[J].Journal of Food Science, 2012, 77(11):E313-E320.
[31] FRATIANNI A, ALBANESE D, MIGNOGNA R, et al.Degradation of carotenoids in apricot (Prunus armeniaca L.) during drying process[J].Plant Foods for Human Nutrition, 2013, 68(3):241-246.
[32] WANG M Z, GAO Y W, HU B F, et al.Freeze-thaw pretreatment improves the vacuum freeze-drying efficiency and storage stability of goji berry (Lycium barbarum L.)[J].LWT, 2023, 189:115439.