乳酸菌作为一类革兰氏阳性菌,广泛存在于发酵食品、动物肠道及自然环境中,在食品发酵工业中扮演着核心角色,不仅赋予食品独特的风味与质地,还对人体肠道微生态平衡起到关键的调节作用。乳酸菌在生长代谢过程中会产生一系列具有特殊生理功能的活性肽,这些活性肽的氨基酸残基数目通常在2~50个,并且赋予了食品多样的功能性,如卓越的抗氧化、降血压、抗菌、免疫调节等功效,极大地拓展了食品的应用范畴[1]。然而,乳酸菌活性肽的挖掘主要依赖于传统的分离纯化与生物活性测定方法,以早期乳酸菌抗菌肽的筛选为例,往往需要经过多次层析分离、活性追踪,才可能获得一种具有潜在活性的肽段[2]。这种方法不仅效率极低,而且由于其基于单一活性指标的筛选策略,难以全面捕捉乳酸菌复杂代谢产物中丰富的活性肽信息,许多含量较低但功能独特的活性肽极易被忽视。同时,传统方法无法对活性肽的结构与功能关系进行系统研究,限制了对乳酸菌活性肽资源的深度开发。
肽组学作为一门专注于生物体内肽类物质全面分析的新兴学科,凭借其强大的技术整合能力,为乳酸菌活性肽的系统研究打开了全新的大门。在技术层面,高分辨率质谱技术的应用,能够实现对肽段质量的精确测定,其质量精度可达ppm级别,结合多维色谱分离技术,可有效分离复杂样品中的肽段,大幅提高了肽段鉴定的覆盖率[3]。生物信息学分析工具如PEAKS、MaxQuant等软件,能够快速处理质谱数据,通过与数据库比对,准确鉴定活性肽的氨基酸序列,并预测其结构特征[4]。通过这些技术的整合,肽组学能够在全局层面动态解析乳酸菌发酵体系中活性肽的组成、含量变化以及修饰情况。YU等[5]将肽组学与机器学习技术相结合,开发了一种高效的苦味肽CPM-BP预测模型,实现了超过90%的预测准确率,并通过实验验证了多个预测苦味肽的效能,揭示了乳制品苦味的产生机制,同时为改进乳制品风味品质提供了新的技术工具。
尽管肽组学技术极大地推动了乳酸菌活性肽的研究进程,但随之而来的是海量的组学数据。人工智能(artificial intelligence,AI)与机器学习(machine learning,ML)技术的迅猛发展,为破解这一难题带来了新的契机。近年来,深度学习算法如卷积神经网络(convolutional neural network,CNN)和循环神经网络(recurrent neural network,RNN)在生物信息学领域的成功应用,为活性肽筛选提供了强大的工具,研究人员通过构建基于大数据的预测模型,将活性肽的序列信息、结构特征以及生物活性数据作为训练集,使模型能够学习活性肽与生物靶点之间的相互作用模式[6]。王姝等[7]利用支持向量机(support vector machine,SVM)算法构建的抗菌肽预测模型,在训练集和测试集上均展现出较高的预测准确率,能够从海量的候选肽中快速筛选出潜在的高活性抗菌肽,相较于传统筛选方法,效率提升数十倍甚至上百倍。
从传统经验性筛选到肽组学整合,再到智能化筛选技术的应用,乳酸菌源功能活性肽的挖掘经历了从定性到定量、从单一研究到系统分析、从经验驱动到数据驱动的重大转变。这种技术革新不仅推动了乳酸菌活性肽基础研究的深入开展,更为其在功能性食品开发、疾病预防与治疗等领域的产业化应用提供了强大的技术支撑。然而,尽管相关研究已取得显著进展,但仍面临诸多挑战,如复杂体系中低丰度活性肽的检测、智能化模型的普适性优化等。深入探讨乳酸菌源功能活性肽的挖掘技术,系统剖析肽组学整合与智能化筛选过程中的关键科学问题及应用潜力,对于推动活性肽基础研究与产业发展的深度融合,满足人们日益增长的对健康食品与创新药物的迫切需求,具有不可替代的理论意义与实践价值。
1 乳酸菌源功能活性肽的分类
乳酸菌源功能活性肽作为乳酸菌代谢活动的重要产物,在食品、医药和生物技术领域展现出巨大的应用潜力。这类由2~50个氨基酸组成的小分子肽,通过核糖体或非核糖体途径合成,并经多样化的翻译后修饰形成具有特定空间构象的活性分子。目前,针对乳酸菌源功能活性肽的研究主要聚焦于抗菌、抗氧化、降血压和免疫调节等功能类别[8]。抗氧化活性肽富含组氨酸、半胱氨酸等供氢氨基酸,通过直接清除自由基和调节抗氧化酶系统发挥作用,常见于发酵乳、沙丁鱼等,可作为食品抗氧化剂及保健品成分[9];降压活性肽多为短肽,C端含脯氨酸等关键氨基酸,通过抑制血管紧张素转换酶(angiotensin converting enzyme,ACE)降低血压,在发酵乳制品中广泛存在,适用于开发功能性降压食品[10];抗菌活性肽带有正电荷且具两亲性结构,能破坏细菌细胞膜或干扰细胞代谢,如植物乳植杆菌产生的抗菌肽可作为天然防腐剂替代化学制剂[11];免疫调节活性肽含特定氨基酸模体,通过激活免疫细胞信号通路调节免疫应答[12],在免疫增强食品和疫苗佐剂研发中前景广阔;呈味功能肽分为鲜味肽、苦味肽和浓厚感肽,分别通过与不同味觉受体结合影响食品风味,可用于天然调味料的生产和发酵食品风味调控[13]。乳酸菌源功能活性肽的分类及应用如表1所示。
表1 乳酸菌源功能活性肽的分类
Table 1 Classification of functionally active peptides of lactic acid bacteria origin
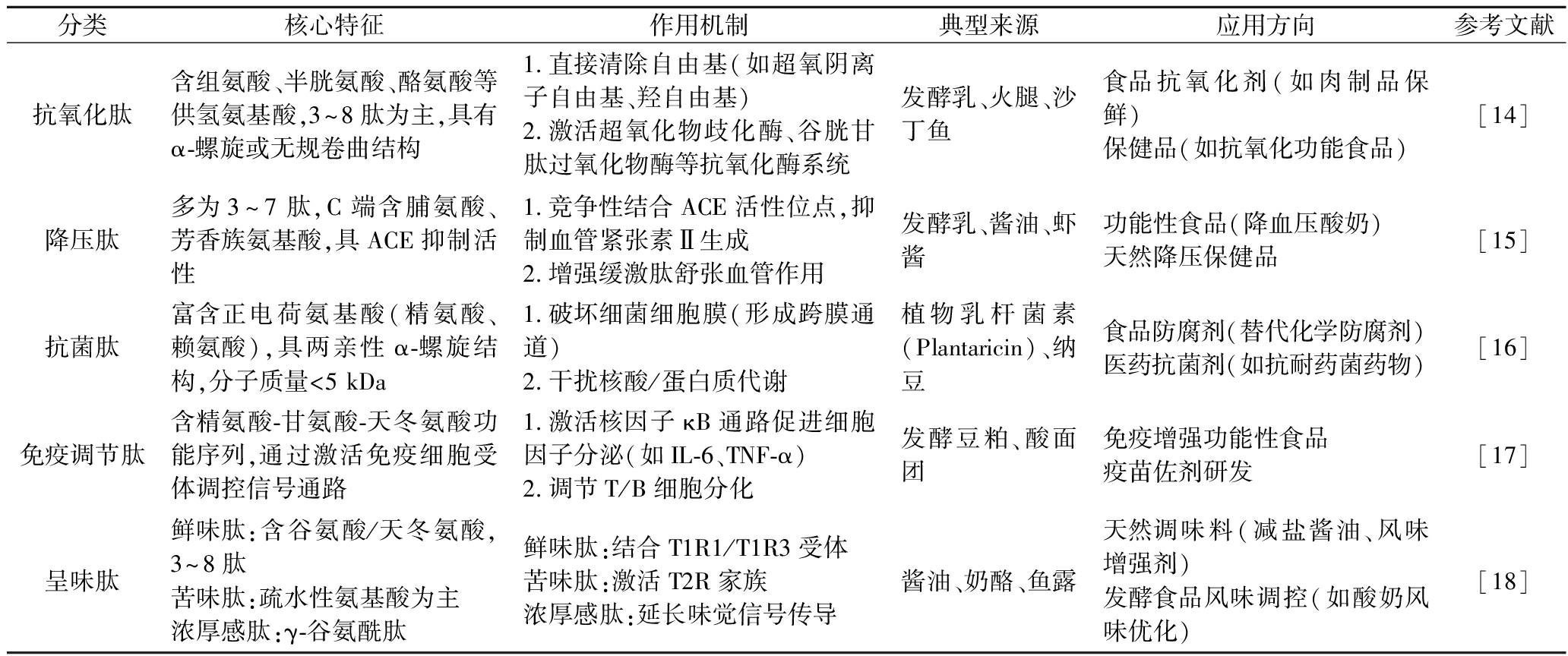
分类核心特征作用机制典型来源应用方向参考文献抗氧化肽含组氨酸、半胱氨酸、酪氨酸等供氢氨基酸,3~8肽为主,具有α-螺旋或无规卷曲结构1.直接清除自由基(如超氧阴离子自由基、羟自由基)2.激活超氧化物歧化酶、谷胱甘肽过氧化物酶等抗氧化酶系统发酵乳、火腿、沙丁鱼食品抗氧化剂(如肉制品保鲜)保健品(如抗氧化功能食品)[14]降压肽多为3~7肽,C端含脯氨酸、芳香族氨基酸,具ACE抑制活性1.竞争性结合ACE活性位点,抑制血管紧张素Ⅱ生成2.增强缓激肽舒张血管作用发酵乳、酱油、虾酱功能性食品(降血压酸奶)天然降压保健品[15]抗菌肽富含正电荷氨基酸(精氨酸、赖氨酸),具两亲性α-螺旋结构,分子质量<5 kDa1.破坏细菌细胞膜(形成跨膜通道)2.干扰核酸/蛋白质代谢植物乳杆菌素(Plantaricin)、纳豆食品防腐剂(替代化学防腐剂)医药抗菌剂(如抗耐药菌药物)[16]免疫调节肽含精氨酸-甘氨酸-天冬氨酸功能序列,通过激活免疫细胞受体调控信号通路1.激活核因子κB通路促进细胞因子分泌(如IL-6、TNF-α)2.调节T/B细胞分化发酵豆粕、酸面团免疫增强功能性食品疫苗佐剂研发[17]呈味肽鲜味肽:含谷氨酸/天冬氨酸,3~8肽苦味肽:疏水性氨基酸为主浓厚感肽:γ-谷氨酰肽鲜味肽:结合T1R1/T1R3受体苦味肽:激活T2R家族浓厚感肽:延长味觉信号传导酱油、奶酪、鱼露天然调味料(减盐酱油、风味增强剂)发酵食品风味调控(如酸奶风味优化)[18]
表1系统呈现了乳酸菌源功能活性肽的分类体系,按生物活性可分为抗氧化、降压、抗菌、免疫调节和呈味肽五大类。其中,抗氧化肽含组氨酸等供氢氨基酸,通过清除自由基及激活抗氧化酶发挥作用;降压肽多为3~7肽,通过抑制血管紧张素Ⅰ转换酶调控血压;抗菌肽具两亲性结构,可破坏细菌细胞膜或干扰代谢;免疫调节肽能激活免疫细胞信号通路;呈味肽包括鲜味、苦味和浓厚感肽,通过结合不同味觉受体调控食品风味。各类肽段均有明确的结构特征、作用机制及应用方向,为功能活性肽的开发提供了理论基础。
1.1 抗氧化活性肽
乳酸菌源抗氧化活性肽在乳酸菌源功能活性肽中占据重要地位。其作用机制精妙而复杂,主要通过提供氢原子或电子,与体内具有强氧化性的自由基如超氧阴离子自由基、羟自由基、H2O2等发生反应,将这些自由基转化为相对稳定的物质,从而中断自由基链式反应,减轻氧化应激对细胞和生物大分子的损伤[19]。在分子层面,抗氧化活性肽还可以通过调节细胞内抗氧化酶系统的活性来发挥作用。能够激活超氧化物歧化酶、过氧化氢酶和谷胱甘肽过氧化物酶等抗氧化酶的基因表达,促使细胞内这些抗氧化酶的含量增加,活性增强[20]。这些抗氧化酶协同作用,能够更有效地清除细胞内产生的自由基,维持细胞内氧化还原平衡。抗氧化活性肽的结构与活性之间存在着紧密的构效关系,富含组氨酸、半胱氨酸、酪氨酸等具有供氢能力氨基酸残基的肽段往往具有较强的抗氧化活性,这些氨基酸残基中的咪唑基、巯基和酚羟基等官能团能够稳定地提供氢原子,与自由基结合,形成稳定的产物[21]。
1.2 降压活性肽
乳酸菌源降压活性肽的降压功效主要依赖于对ACE的抑制作用。ACE在人体血压调节过程中扮演着关键角色,它能够催化血管紧张素Ⅰ转化为具有强烈收缩血管作用的血管紧张素Ⅱ,同时降解具有舒张血管作用的缓激肽[22]。当乳酸菌源降压活性肽进入人体后,能够与ACE的活性位点特异性结合,阻断血管紧张素Ⅰ向血管紧张素Ⅱ的转化过程,减少血管紧张素Ⅱ的生成,从而降低外周血管阻力,实现血压的下降[23]。同时,降压活性肽还能抑制缓激肽的降解,使缓激肽在体内的含量增加,进一步增强血管的舒张作用,协同降低血压。张文静等[24]对乳酸菌发酵羊乳的研究中发现了一种由特定氨基酸序列组成的降血压活性肽,该肽段能够精准地与ACE的活性中心结合,其结合模式类似于底物与酶的特异性结合,但结合强度更高,从而有效地竞争性抑制了ACE的活性。这种降血压活性肽的氨基酸序列中,脯氨酸残基的存在对其与ACE的结合亲和力具有重要影响。脯氨酸独特的环状结构能够使肽链在空间上形成特定的弯曲构象,恰好与ACE活性位点的空间结构互补,增强了两者之间的相互作用[25]。除了脯氨酸,其他一些氨基酸残基如精氨酸、赖氨酸等所带的正电荷也有助于与ACE活性位点上的负电荷区域通过静电相互作用结合,进一步稳定肽-酶复合物,提高抑制效果[26]。
1.3 抗菌活性肽
乳酸菌源抗菌活性肽是乳酸菌源功能活性肽中具有重要生物学功能的一类。其抗菌机制呈现出多样化的特点。一方面,部分抗菌活性肽能够与细菌细胞膜相互作用,改变细胞膜的通透性,这些肽通常具有两亲性结构,即同时含有亲水性和疏水性区域,在与细菌细胞膜接触时,亲水性区域与细胞膜表面的水分子相互作用,疏水性区域则插入细胞膜的脂质双分子层中[27]。随着更多的抗菌活性肽分子与细胞膜结合,它们在细胞膜上聚集并形成跨膜通道或孔洞,导致细胞内的离子、小分子物质和蛋白质等重要成分泄漏,最终引起细菌细胞死亡[28]。另一方面,一些抗菌活性肽可以进入细菌细胞内部,与细胞内的核酸、蛋白质等生物大分子相互作用,干扰细菌的正常代谢过程[29]。何容肖等[30]发现乳链菌肽能够与细菌的DNA结合,阻碍DNA的复制和转录过程,使细菌无法合成必要的蛋白质和酶,从而抑制细菌的生长繁殖。从乳酸菌发酵产物中分离得到的抗菌活性肽,其氨基酸组成和结构特征与抗菌活性密切相关。一般来说,抗菌活性肽富含带正电荷的氨基酸残基,如精氨酸、赖氨酸等,这些正电荷有助于抗菌活性肽与带负电荷的细菌细胞膜发生静电吸引作用,促进肽分子与细胞膜的结合[31]。
1.4 免疫调节活性肽
乳酸菌源免疫调节活性肽在维持机体免疫平衡方面发挥着关键作用。其作用机制主要是通过与免疫细胞表面的特定受体相互作用,激活或调节免疫细胞的信号转导通路,从而影响免疫细胞的增殖、分化、活化以及细胞因子的分泌等过程[32]。在巨噬细胞中,免疫调节活性肽能够与巨噬细胞表面的Toll样受体(Toll-like receptors,TLRs)等受体结合,启动细胞内的信号级联反应[33]。这一过程会激活核因子κB等转录因子,使其进入细胞核内,调控相关基因的表达,促进巨噬细胞分泌肿瘤坏死因子α、白细胞介素1β、白细胞介素6等细胞因子,这些细胞因子在免疫应答过程中发挥着重要的调节作用,能够增强巨噬细胞的吞噬能力和杀菌活性,促进炎症反应的发生,从而提高机体对病原体的抵御能力[34]。乳酸菌源免疫调节活性肽的氨基酸组成和序列特征对其免疫调节活性有着至关重要的影响,一些富含特定氨基酸模体的肽段往往具有较强的免疫调节活性[35]。含有RGD环肽序列的免疫调节活性肽,能够与免疫细胞表面的整合素受体特异性结合,通过激活整合素介导的信号通路来调节免疫细胞的功能[36]。
1.5 呈味功能肽
乳酸菌源呈味功能肽是乳酸菌源活性肽中能够直接影响食品风味的特殊类别,通过与味觉受体相互作用,赋予发酵食品独特的感官特性。其分类及呈味机制主要涵盖鲜味肽、苦味肽和浓厚感肽三大类。鲜味肽多富含谷氨酸或天冬氨酸等鲜味氨基酸残基,能够与鲜味受体T1R1/T1R3(taste receptor type1 member1/tastereceptor type1 member3,T1R1/T1R3)特异性结合,激活味觉信号传导通路,产生类似味精的鲜味感知,且部分鲜味肽的呈味强度可达味精的1.5~3倍[37]。如酱油发酵过程中,乳酸菌作用产生的天冬酰胺-脯氨酸等肽段,通过特定的氨基酸序列构象,高效地与鲜味受体结合,增强食品的鲜味层次[38]。鲜味肽的鲜味强度不仅与氨基酸组成相关,肽链长度也会产生影响,通常3~8个氨基酸组成的短肽鲜味表现更为突出。FAN等[39]研究通过定向调控乳酸菌发酵参数,使鲜味肽产量提升了40%,显著改善了发酵乳制品的风味。苦味肽通常由疏水性氨基酸组成,这些氨基酸暴露的肽段能够与苦味受体(type 2 bitter taste receptor,TAS2Rs)家族结合,触发苦味信号传递[40]。石琳等[41]探究发现在奶酪、酸奶等发酵食品中,常检测到由乳酸菌代谢产生的苦味肽。虽然单独的苦味肽会带来不良味觉体验,但在发酵食品复杂的风味体系中,苦味肽与鲜味肽、咸味肽等协同作用,能够增强风味层次感,形成独特的发酵风味特征。
各类活性肽的结构与功能紧密相关,氨基酸组成、序列及空间结构决定其活性表现。这些活性肽在食品工业和生物医药领域展现出巨大应用价值,但在生成机制解析、高效检测及工业化应用等方面仍面临挑战,未来需借助多组学技术和AI算法深入研究,推动其产业化发展。
2 基于肽组学的挖掘技术
2.1 肽组学技术体系的构建与优化
随着生命科学研究的深入,肽组学凭借其对生物体系内小分子多肽的系统性解析能力,成为乳酸菌源功能活性肽挖掘的前沿技术。该技术以高分辨质谱为核心,结合多维分离与生物信息学分析,突破传统方法的局限性,从分子水平揭示活性肽的产生规律与功能机制,为功能性食品和生物医药领域的创新发展提供关键支撑。
肽组学的技术架构围绕“分离-检测-鉴定-定量”四大环节展开。在样品前处理阶段,针对乳酸菌发酵产物的复杂性,采用分级分离策略:首先通过超滤去除大分子蛋白和菌体碎片,再利用固相萃取(solid-phase extraction,SPE)或免疫亲和富集技术特异性捕获目标肽段,显著提升低丰度活性肽的检测灵敏度。例如,AMORIM等[42]通过肽组学的方法鉴定分析开菲尔奶的生物活性肽,鉴定出35种对ACE存在抑制作用的具有潜在高血压活性的肽。而二维液相色谱与超高效液相色谱的应用,大幅提升了肽段分离的分辨率和通量。二维液相色谱通过正交分离模式,将复杂肽混合物切割为数十个组分,有效降低质谱分析的离子抑制效应;超高效液相色谱凭借亚2 μm粒径色谱柱,实现分钟级快速分离,配合在线质谱检测,可在短时间内完成大规模样品分析。HELAL等[43]在奶酪成熟过程研究中,通过高分辨率质谱对6种奶酪的肽组学谱、生物活性和生物活性肽含量进行了表征,在高达奶酪中发现最高的ACE抑制活性,也显示出最高的抗氧化活性,共鉴定出809个来源于主要乳蛋白的肽,其中82个具有生物活性。质谱检测技术的进步为多肽组学提供了高精度分析手段。高分辨质谱仪具备超过10万的分辨率和亚ppm级质量精度,结合数据非依赖采集(data independent acquisition,DIA)模式,可实现对肽段的无偏、定量分析。DIA技术通过循环扫描固定质荷比窗口,避免数据依赖型串联质谱法的随机性,显著提高低丰度肽段的检测覆盖率[44]。
2.2 多肽组学的核心应用
基于质谱的多肽鉴定技术是发现新型活性肽的核心工具。通过串联质谱的碎片离子分析,结合数据库搜索(如Mascot、PEAKS)和从头测序算法,可精确解析肽段的氨基酸序列和修饰位点。例如,HU等[45]采用高效液相色谱-串联质谱和分子对接技术,鉴定并筛选源自发酵核桃粕的抗菌肽和酚类化合物组合对抗青霉菌,通过荧光光谱、傅里叶变换红外光谱和分子对接探索协同抗真菌机制。功能验证方面,多肽组学与体外活性实验的整合形成“鉴定-验证”闭环。YANG等[46]研究发酵花椒紫菜生产抗氧化肽,粗多肽经酸水沉淀提取,经提纯得到高抗氧化活性成分。使用高效液相色谱-串联质谱技术对目标肽进行无差别分析。通过联合使用多个数据库发现了肽的潜在抗氧化活性,结合铁离子还原抗氧化能力、DPPH自由基清除能力、ABTS阳离子自由基清除能力等体外实验测定其抗氧化肽活性。这种多维度验证策略显著提升了活性肽功能注释的可靠性。
多肽组学的定量分析功能可用于筛选不同菌株、环境条件下的差异表达肽段。对比高产与低产抗菌肽的乳酸菌菌株,发现高产菌株中特定前体肽的表达量是低产菌株的8.6倍,结合基因组学分析,确认其上游调控区域存在增强子元件,使转录效率提高3.1倍[47]。在环境胁迫研究中,发现酸性条件(pH 4.5)可诱导乳酸菌产生更多含组氨酸的缓冲肽,这类肽不仅维持胞内酸碱平衡,其咪唑基还赋予其抗氧化能力[48]。
2.3 肽组学与多组学整合研究
多肽组学与基因组学、蛋白质组学、代谢组学的整合,构建了从基因到代谢产物的全链条研究体系。MARULO等[49]对假肠明串珠菌和副肠膜明串乳杆菌2种乳酸菌发酵的开心果饮料进行物理化学和微生物分析,以及肽组学和蛋白质组学分析,测定了主要由2S白蛋白、11S和7S球蛋白释放的数百条肽的氨基酸序列。研究发现,除了在酸性pH下具有活性的内源性蛋白酶外,乳酸菌的蛋白水解系统在一定程度上直接参与了肽的降解。根据BIOPEP数据库,一组31个肽具有潜在的生物活性,主要与抗氧化特性、ACE和二肽基肽酶-IV抑制有关。ZHANG等[50]采用液相二级质谱及代谢组学和肽组学研究了鼠李糖乳酪杆菌B6、发酵粘液乳杆菌B44和鼠李糖乳酪杆菌KF7这3种新型益生菌发酵新鲜奶酪的代谢物和肽谱。多变量分析显示,益生菌新鲜奶酪与对照样品的代谢物组成存在显著差异。差异代谢物主要是脂质和类脂分子以及有机氧化合物,它们与脂肪酸和碳水化合物相关途径有关。在3种益生菌中,鼠李糖乳酪杆菌KF7对蔗糖的分解效果最高。从益生菌鲜奶酪中鉴定出147个潜在的生物活性肽,主要来源于酪蛋白。
尽管多肽组学已取得显著进展,但其在乳酸菌研究中仍面临多重挑战。首先,低丰度活性肽(如免疫调节肽)的检测灵敏度不足,现有质谱技术的检测限难以满足需求,需开发新型富集材料和高灵敏度检测方法。其次,同分异构体和翻译后修饰肽段的鉴定存在困难,需结合电子转移解离、电子捕获解离等新型碎裂技术,提升结构解析能力。此外,乳酸菌特异性多肽数据库的不完善制约了数据解析效率,亟需整合全球研究成果,构建标准化、开放共享的专业数据库。
未来,多肽组学将朝着3个方向突破:一是空间多肽组学技术,结合成像质谱实现活性肽在发酵食品微生态中的可视化定位;二是单细胞多肽组学,利用微流控芯片和纳升流质谱技术,解析单个乳酸菌细胞的分泌异质性;三是AI深度融合,开发基于深度学习的质谱数据解析算法,实现活性肽序列预测、功能注释的智能化,加速新型活性肽的发现与产业化进程。
3 基于AI的挖掘技术
3.1 AI技术在活性肽挖掘中的核心架构
AI在乳酸菌源功能活性肽挖掘中的应用,依托机器学习、深度学习和自然语言处理(natural language processing,NLP)等技术,构建了“数据驱动-模型预测-实验验证-产业转化”的智能化研究体系,如图1所示。
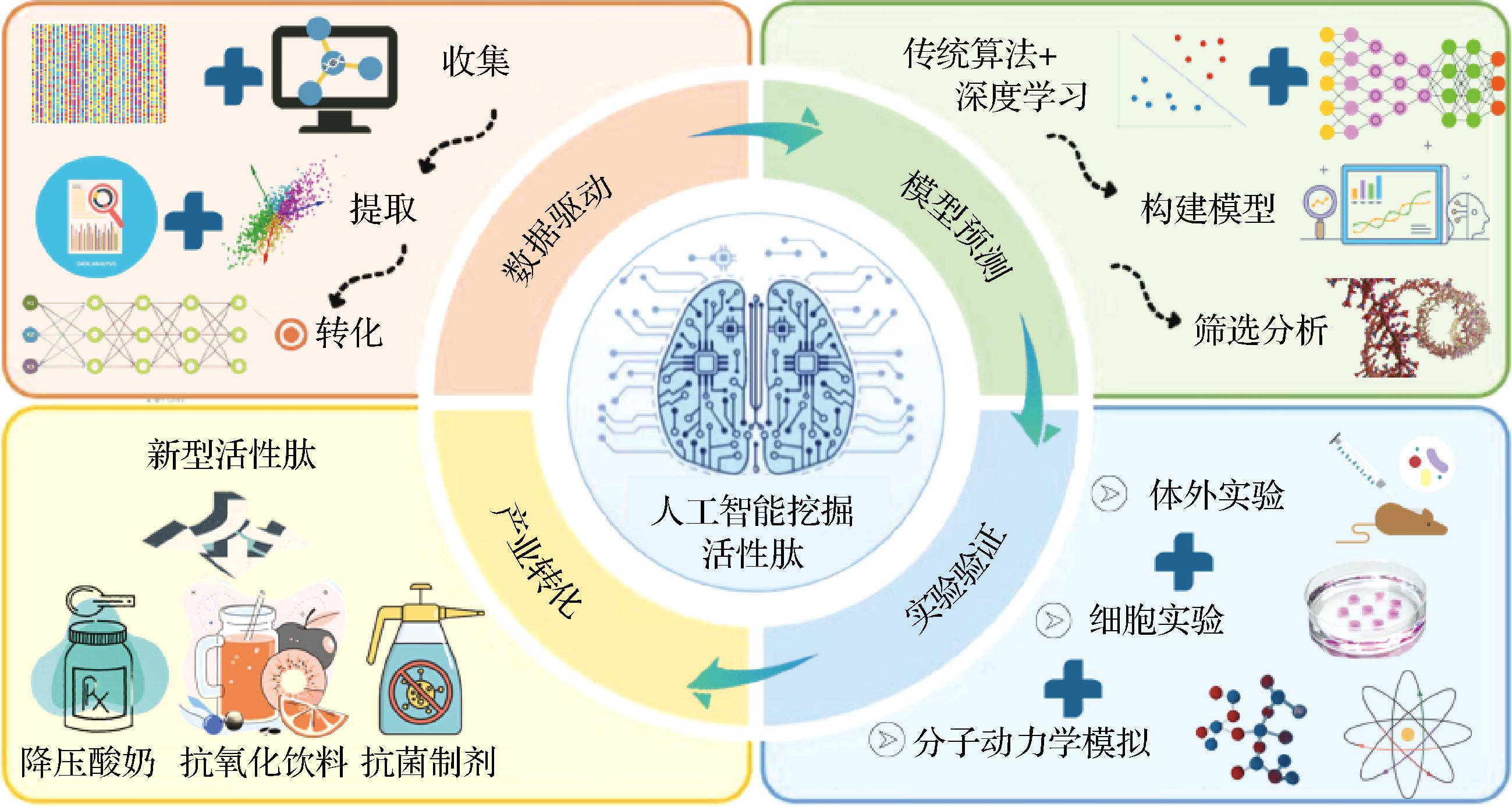
图1 AI挖掘活性肽的核心架构
Fig.1 Core architecture of AI for mining active peptides
图1展示了AI挖掘活性肽的技术架构,该体系以“数据驱动-模型预测-实验验证-产业转化”为核心:首先整合乳酸菌基因组、质谱数据及文献信息,通过特征提取构建数据集;然后利用机器学习和深度学习模型预测肽段活性,解析结构-功能关系;再通过体外活性实验、细胞水平验证及分子动力学模拟验证预测结果;最终将优化工艺和新型肽段应用于功能性食品和生物医药领域,实现从科研到产业的转化,体现了智能化筛选技术对传统方法的效率革新。
数据驱动:多渠道收集乳酸菌基因组、多肽组质谱及文献数据,通过数据清洗、标准化和特征提取,将序列数据转化为数值特征,文本数据通过NLP提取关键信息[51]。JIN等[52]通过爬取UniProt、PeptideAtlas等数据库,建立包含10万乳酸菌源肽序列的专用数据集。模型预测:将处理后的数据输入机器学习或深度学习模型进行训练,通过交叉验证优化参数;利用训练好的模型对未知肽段的抗氧化、降血压等活性进行预测,分析肽段结构-功能关系,或对发酵工艺参数进行智能优化[53]。CHANG等[54]基于CNN的抗氧化肽预测模型,通过提取肽序列的局部特征,实现对活性的精准分类。实验验证:针对模型预测结果,开展体外活性实验(DPPH自由基清除率、ACE抑制率测定等)、细胞水平实验及分子动力学模拟,从多角度验证预测的准确性与可靠性,修正模型偏差[55]。产业转化:将实验验证成功的优化工艺和新型活性肽,应用于功能性食品(如降血压酸奶、抗氧化饮料)、生物医药(抗菌制剂、免疫调节药物)等领域,推动科研成果向实际生产转化,实现经济效益与社会价值的统一。
3.2 机器学习在活性肽功能预测中的应用
支持向量机(support vector machines,SVM)在活性肽二分类任务中表现优异。以降压肽预测为例,提取肽序列的理化性质、氨基酸组成等30维特征,通过SVM-RBF核函数构建分类器,对ACE抑制肽的预测准确率可达85%[56]。随机森林(random forest,RF)则擅长处理非线性特征交互,在抗菌肽预测中,递归特征消除(recursive feature elimination,RFE)筛选关键特征,模型AUC值达0.92,显著优于单一特征模型[57]。
深度学习通过自动特征提取,解决了传统算法依赖人工特征工程的瓶颈。CNN通过多层卷积核扫描肽序列,可识别与功能相关的关键模体。例如,在免疫调节肽预测中,CNN模型识别出含RGD模体的肽段与整合素受体结合的概率提升4倍[58]。RNN及其变体长短期记忆网络(long short-term memory,LSTM)、门控循环单元则擅长处理序列顺序信息,在预测肽-蛋白相互作用时,通过捕捉氨基酸排列的长距离依赖关系,使结合能预测误差降低至±1.5 kcal/mol。
生成式对抗网络(generative adversarial networks,GAN)在活性肽设计中展现创新潜力。通过训练生成器生成新型肽序列,判别器评估其与天然活性肽的相似性,可快速设计高活性肽段。例如,基于GAN设计的乳酸菌源抗菌肽,其抑菌率较天然肽提升2~3倍,且对耐药菌表现出更强杀伤力[59]。
3.3 AI与组学数据的融合应用
AI模型与蛋白质组学和代谢组学数据的整合,可构建“基因-肽段-代谢物”关联网络。利用图神经网络(graph neural network,GNN)分析多肽组学与代谢组学联合数据,发现谷胱甘肽代谢通路与含半胱氨酸的抗氧化肽合成显著相关(Spearman系数=0.83),进而通过调控谷胱甘肽合成酶基因提升抗氧化肽产量45%[60]。基因组学数据为AI模型提供了活性肽合成的遗传基础。CARPI等[61]对植物乳植杆菌(Lactiplantibacillus plantarum)基因组进行泛基因组分析,使用ProtBERT提取肽序列特征,XGBoost模型预测潜在抗菌肽。鉴定出新型抗菌肽LP-5,对金黄色葡萄球菌的最小抑菌浓度(minimal inhibit concentration,MIC)为8 μg/mL。转录组学数据则用于解析活性肽合成的时空表达规律。GOH等[62]对发酵过程中的嗜酸乳杆菌(Lactobacillus acidophilus)进行RNA-seq分析,通过差异表达基因结合LSTM模型预测高表达肽类。发现一种新型免疫调节肽LA-1,可显著抑制TNF-α分泌。
AI算法通过分析多肽组学数据与基因组序列的关联,挖掘活性肽合成的关键基因。通过关联分析发现抗菌肽Plantaricin 423的丰度与基因组中前体肽编码基因的拷贝数呈正相关(R2=0.89)[63]。利用梯度提升树建立基因-肽段丰度预测模型,可准确识别高产菌株的基因型特征,为菌株筛选提供分子标记。AI驱动的时序数据分析,揭示活性肽合成的转录调控网络。在切达干酪成熟过程中,通过LSTM模型分析多肽组与转录组的时间序列数据,发现降压肽VPP/IPP(Val-Pro-Pro/Ile-Pro-Pro)的积累与胞内肽酶基因的表达峰值高度吻合(Spearman系数=0.93)[64]。进一步通过SHAP(shapley additive explanations)值分析,确定pepN基因表达量是影响肽段丰度的最关键因素(贡献度=38%)。AI算法通过GNN构建“多肽-代谢物”关联网络,解析活性肽合成的代谢基础。在抗氧化肽研究中,GNN模型发现含半胱氨酸的肽段丰度与谷胱甘肽代谢通路中的关键代谢物(半胱氨酸)浓度呈强正相关(边权重=0.85)[65]。通过调控GSH合成酶基因gshB,使相关代谢物浓度提升40%,带动抗氧化肽产量增加52%,验证了AI预测的准确性[66]。
尽管基于AI的挖掘技术已取得显著成果,但仍面临诸多挑战。首先,数据质量和规模是制约模型性能的关键因素。目前活性肽相关的高质量数据相对有限,且数据标注的准确性和一致性有待提高。其次,AI模型的可解释性不足,尤其是深度学习模型,其复杂的网络结构和参数使得预测结果难以解释,增加了实验验证的难度。此外,AI预测结果需要与实验验证紧密结合,建立“数据驱动-模型预测-实验验证-产业转化”的闭环研究模式。未来,随着数据积累的不断丰富、算法的持续优化以及多学科交叉融合的深入,基于AI的乳酸菌源功能活性肽挖掘技术将朝着更精准、更智能、更实用的方向发展,加速新型活性肽的发现与应用,为功能性食品、生物医药等领域带来新的突破。
4 展望
乳酸菌源功能活性肽凭借其多样的生物活性,在功能性食品与生物医药领域的应用已初具规模,但其产业化进程仍受多重技术瓶颈制约。当前主要挑战集中在3个方面:1)低丰度活性肽的检测灵敏度不足,现有质谱技术难以捕捉含量低于pmol级的肽段,导致潜在功能分子被遗漏;2)工业化生产中活性肽产量偏低,传统发酵工艺下目标肽段得率仅为毫克级/升,难以满足规模化需求;3)结构-功能关系解析不充分,制约了高活性肽的定向设计。
针对上述问题,现有技术已展现出突破潜力。在检测层面,可构建“靶向富集-多维分离-高分辨检测”联用体系:采用分子印迹聚合物或纳米材料特异性捕获低丰度肽段,结合有限蛋白酶解-质谱法增强目标肽段的特异性解析效率,搭配高场Orbitrap质谱的DIA模式,将检测限降至fmol级。在产量提升方面,合成生物学工具可改造乳酸菌基因,过表达pepN等关键肽酶基因,使降压肽VPP产量提升3倍;AI驱动的动态发酵控制系统能实时优化pH、溶氧量等参数,维持活性肽合成的最优代谢流。
未来研究应向多维度深化:1)开发空间肽组学技术,结合成像质谱实现活性肽在发酵体系中的可视化定位;2)构建智能化设计平台,基于深度学习算法整合肽序列、结构及活性数据,实现高活性肽的虚拟筛选与定向改造,缩短研发周期;3)推动多组学与AI的深度融合,解析活性肽合成的转录调控网络,实现“基因-肽段-功能”的精准关联。通过技术创新与跨学科协作,有望突破从微量检测到规模生产的全链条壁垒,加速乳酸菌源活性肽的产业化应用。
[1] 李思怡, 姜雨彤, 妥彦峰, 等.微生物发酵法制备乳源生物活性肽研究进展[J].食品科学, 2023, 44(21):312-321.LI S Y, JIANG Y T, TUO Y F, et al.Research progress in preparation of bioactive peptides from milk by microbial fermentation[J].Food Science, 2023, 44(21):312-321.
[2] 库尔旦·胡达依别尔根, 刘学莲, 卡吾萨尔·恰依马尔旦, 等.分离、鉴定和筛选具有益生特性和降胆固醇能力的发酵马乳源益生菌[J].食品与发酵工业, 2025, 51(11):171-178.KURDAN H, LIU X L, KAWUSAER Q, et al.Isolation, identification, and screening of probiotic strains with cholesterol-lowering potential from fermented mare’s milk[J].Food and Fermentation Industries, 2025, 51(11):171-178.
[3] 付英杰, 张启东, 范武, 等.组学技术在食品风味解析中的应用研究进展[J].河南工业大学学报(自然科学版), 2025, 46(3):135-147.FU Y J, ZHANG Q D, FAN W, et al.Research progress on the applications of omics technologies in food flavor analysis[J].Journal of Henan University of Technology (Natural Science Edition), 2025, 46(3):135-147.
[4] 朱华伟, 李寅.合成生物制造2025[J].生物工程学报, 2025, 41(1):1-78.ZHU H W, LI Y.Biomanufacturing driven by engineered organisms[J].Chinese Journal of Biotechnology, 2025, 41(1):1-78.
[5] YU Y, LIU S C, ZHANG X C, et al.Identification and prediction of milk-derived bitter taste peptides based on peptidomics technology and machine learning method[J].Food Chemistry, 2024, 433:137288.
[6] 钱宇辰, 聂挺, 花彦铭, 等.人工智能算法在抗菌肽预测领域的应用[J].食品科学, 2025, 46(11):384-393.QIAN Y C, NIE T, HUA Y M, et al.Application of artificial intelligence algorithms in the field of antimicrobial peptide prediction[J].Food Science, 2025, 46(11):384-393.
[7] 王姝, 徐春明.深度学习在抗菌肽设计、发现与预测中的应用:现状与展望[J].食品与发酵工业, 2024, 50(21):366-378.WANG S, XU C M.Application of deep learning in the design, discovery, and prediction of antimicrobial peptides:Current status and prospects[J].Food and Fermentation Industries, 2024, 50(21):366-378.
[8] 孙雪姣, 李蕊, 刘雨萌, 等.乳中生物活性肽对人体健康影响的研究进展[J].乳业科学与技术, 2018, 41(3):42-46.SUN X J, LI R, LIU Y M, et al.Recent progress of research on health benefits of bioactive peptides derived from milk proteins for humans[J].Journal of Dairy Science and Technology, 2018, 41(3):42-46.
[9] SRIVASTAVA U, NATARAJ B H, KUMARI M, et al.Antioxidant and immunomodulatory potency of Lacticaseibacillus rhamnosus NCDC24 fermented milk-derived peptides:A computationally guided in-vitro and ex-vivo investigation[J].Peptides, 2022, 155:170843.
[10] ABEDIN M M, CHOURASIA R, CHIRING PHUKON L, et al.Characterization of ACE inhibitory and antioxidant peptides in yak and cow milk hard chhurpi cheese of the Sikkim Himalayan region[J].Food Chemistry:X, 2022, 13:100231.
[11] CHOURASIA R, ABEDIN M M, PHUKON L C, et al.Unearthing novel and multifunctional peptides in peptidome of fermented chhurpi cheese of Indian Himalayan region[J].Food Research International, 2025, 201:115651.
[12] BROWN L, PINGITORE E V, MOZZI F, et al.Lactic acid bacteria as cell factories for the generation of bioactive peptides[J].Protein and Peptide Letters, 2017, 24(2):146-155.
[13] HARPER A R, DOBSON R C J, MORRIS V K, et al.Fermentation of plant-based dairy alternatives by lactic acid bacteria[J].Microbial Biotechnology, 2022, 15(5):1404-1421.
[14] VENEGAS-ORTEGA M G, FLORES-GALLEGOS A C, MART NEZ-HERN
NEZ-HERN NDEZ J L, et al.Production of bioactive peptides from lactic acid bacteria:A sustainable approach for healthier foods[J].Comprehensive Reviews in Food Science and Food Safety, 2019, 18(4):1039-1051.
NDEZ J L, et al.Production of bioactive peptides from lactic acid bacteria:A sustainable approach for healthier foods[J].Comprehensive Reviews in Food Science and Food Safety, 2019, 18(4):1039-1051.
[15] DALIRI E B, LEE B H, PARK B J, et al.Antihypertensive peptides from whey proteins fermented by lactic acid bacteria[J].Food Science and Biotechnology, 2018, 27(6):1781-1789.
[16] TANG H W, PHAPUGRANGKUL P, FAUZI H M, et al.Lactic acid bacteria bacteriocin, an antimicrobial peptide effective against multidrug resistance:A comprehensive review[J].International Journal of Peptide Research and Therapeutics, 2021, 28(1):14.
[17] ZHANG J, XIAO Y, WANG H C, et al.Lactic acid bacteria-derived exopolysaccharide:Formation, immunomodulatory ability, health effects, and structure-function relationship[J].Microbiological Research, 2023, 274:127432.
[18] ABDUL HAKIM B N, XUAN N J, OSLAN S N H.A comprehensive review of bioactive compounds from lactic acid bacteria:Potential functions as functional food in dietetics and the food industry[J].Foods, 2023, 12(15):2850.
[19] 姚松青. 羊肉中活性肽的抗氧化功能及应用研究[D].成都:成都大学, 2024.YAO S Q.Research on the antioxidant function and application of active peptides in mutton[D].Chengdu:Chengdu University, 2024.
[20] 赵以轩,马臻棋,王学红.Irisin在胃肠道恶性肿瘤疾病中的研究进展[J].现代消化及介入诊疗, 2024, 29(8):1015-1020.ZHAO Y X,MA Z Q,WANG X H.Research progress of Irisin in gastrointestinal malignant tumor diseases[J].Modern Interventional Diagnosis and Treatment in Gastroenterology, 2024, 29(8):1015-1020.
[21] 赵烜影. 水牛β-酪蛋白亚型结构表征及体外消化和抗氧化性能分析[D].哈尔滨:东北农业大学, 2018.ZHAO X Y.Structure characterization, digestion in vitro and antioxidation of β-casein phenotypes in buffalo[D].Harbin:Northeast Agricultural University, 2018.
[22] 张凯, 刘媛, 王健, 等.固定化酶ESM-BAP酶解制备甜杏仁ACE抑制肽及其工艺优化[J].农产品加工, 2024(10):47-52;56.ZHANG K, LIU Y, WANG J, et al.Preparation of ACE-inhibiting peptide from sweet almond by enzymatic digestion with immobilized enzyme ESM-BAP and its process optimization[J].Farm Products Processing, 2024(10):47-52;56.
[23] 冯钰瑶, 米顺利.藻类活性肽的功能活性和应用研究进展[J].食品科技, 2022, 47(3):259-264.FENG Y Y, MI S L.Active functions and application research progress of algal peptides[J].Food Science and Technology, 2022, 47(3):259-264.
[24] 张文静, 毛咏荷, 李宁, 等.酸羊乳发酵及其健康功效研究进展[J].中国乳品工业, 2024, 52(2):38-45.ZHANG W J, MAO Y H, LI N, et al.Research advance on fermentation of goat milk and its health beneficial effects[J].China Dairy Industry, 2024, 52(2):38-45.
[25] 赵斐然, 张紫怡, 魏冠棉, 等.传统发酵豆制品中血管紧张素转换酶抑制四肽的构效关系研究[J].食品与发酵工业, 2025, 51(11):216-226.ZHAO F R, ZHANG Z Y, WEI G M, et al.Structure-activity relationship of angiotensin converting enzyme inhibitor tetrapeptides in traditional fermented soybean products[J].Food and Fermentation Industries, 2025, 51(11):216-226.
[26] RUBAK Y T, NURAIDA L, ISWANTINI D, et al.Angiotensin-I-converting enzyme inhibitory peptides in milk fermented by indigenous lactic acid bacteria[J].Veterinary World, 2020, 13(2):345-353.
[27] 高楠, 李逸涵, 孙佳琦, 等.抗菌肽应用研究进展[J].农业生物技术学报, 2025, 33(6):1382-1397.GAO N, LI Y H, SUN J Q, et al.Research progress on the application of antimicrobial peptides[J].Journal of Agricultural Biotechnology, 2025, 33(6):1382-1397.
[28] JI S Q, AN F Y, ZHANG T W, et al.Antimicrobial peptides:An alternative to traditional antibiotics[J].European Journal of Medicinal Chemistry, 2024, 265:116072.
[29] 王梦婷, 卢永忠.抗弧菌多肽的设计及筛选[J].生物技术, 2025, 35(2):164-168.WANG M T, LU Y Z.Design and screening of anti-Vibrio peptides[J].Biotechnology, 2025, 35(2):164-168.
[30] 何容肖, 吴杨博, 张淑霞, 等.食品级重组乳酸乳球菌强组成型分泌猪肠道益生的pEGF-p40[J].畜牧兽医学报, 2025, 56(5):2243-2258.HE R X, WU Y B, ZHANG S X, et al.Intestinal beneficial pEGF-p40 secreted by a food-grade recombinant Lactococcus lactis strong constitutive expression system[J].Acta Veterinaria et Zootechnica Sinica, 2025, 56(5):2243-2258.
[31] 蔡育诚, 吴灌原, 杨海冬, 等.益生菌在动物健康管理中的作用机制及其应用现状[J].中国畜牧兽医, 2025, 52(5):2101-2114.CAI Y C, WU G Y, YANG H D, et al.Mechanisms and current applications of probiotics in animal health management[J].China Animal Husbandry &Veterinary Medicine, 2025, 52(5):2101-2114.
[32] JI H F, LI M, HAN X, et al.Lactobacilli-mediated regulation of the microbial-immune axis:A review of key mechanisms, influencing factors, and application prospects[J].Foods, 2025, 14(10):1763.
[33] 朱一, 武俊瑞, 纪帅奇, 等.乳源活性肽在功能性食品中的应用[J].中国乳品工业, 2024, 52(10):47-51;63.ZHU Y, WU J R, JI S Q, et al.Progress on the application of milk derived active peptides in functional foods[J].China Dairy Industry, 2024, 52(10):47-51;63.
[34] YANG B, ZHENG F L, STANTON C, et al.Lactobacillus reuteri FYNLJ109L1 attenuating metabolic syndrome in mice via gut microbiota modulation and alleviating inflammation[J].Foods, 2021, 10(9):2081.
[35] 阮昕, 汪慎燚, 徐恰, 等.乳源免疫调节肽通过泛素-蛋白酶体途径抑制卵巢癌耐药性及其机制研究[J].安徽医科大学学报, 2018, 53(7):989-993.RUAN X, WANG S Y, XU Q, et al.Immunomodulating peptide inhibits the drug resistance of ovarian cancer cell through the ubiquitin-proteasome pathway[J].Acta Universitatis Medicinalis Anhui, 2018, 53(7):989-993.
[36] IRAM D, KINDARLE U A, SANSI M S, et al.Peptidomics-based identification of an antimicrobial peptide derived from goat milk fermented by Lactobacillus rhamnosus (C25)[J].Journal of Food Biochemistry, 2022, 46(12):e14450.
[37] 杨动听, 王晔洋, 杨选, 等.食品呈味肽的呈味机制及计算机辅助分析研究进展[J].食品工业科技, 2024, 45(13):378-388.YANG D T, WANG Y Y, YANG X, et al.Progress on the tasting mechanism and computer aided analysis of food taste-modulating peptides[J].Science and Technology of Food Industry, 2024, 45(13):378-388.
[38] AN F Y, LI M, ZHAO Y, et al.Metatranscriptome-based investigation of flavor-producing core microbiota in different fermentation stages of dajiang, a traditional fermented soybean paste of Northeast China[J].Food Chemistry, 2021, 343:128509.
[39] FAN Y H, GAN R J, ZHANG Z Y, et al.Flavor effect, application status, and research trend of umami peptides based on microbial fermentation in food[J].Food Microbiology, 2025, 130:104769.
[40] XIAO M Y, HUANG T, XU Y Z, et al.Metatranscriptomics reveals the gene functions and metabolic properties of the major microbial community during Chinese Sichuan Paocai fermentation[J].Food Microbiology, 2021, 98:103573.
[41] 石琳, 贾玮, 张荣, 等.酸奶滋味特征感知、形成过程与分析评价方法研究进展[J].食品工业科技, 2025, 46(9):445-455.SHI L, JIA W, ZHANG R, et al.Progress of yoghurt taste characteristics perception, formation process and analysis and evaluation methods[J].Science and Technology of Food Industry, 2025, 46(9):445-455.
[42] AMORIM F G, COITINHO L B, DIAS A T, et al.Identification of new bioactive peptides from Kefir milk through proteopeptidomics:Bioprospection of antihypertensive molecules[J].Food Chemistry, 2019, 282:109-119.
[43] HELAL A, TAGLIAZUCCHI D.Peptidomics profile, bioactive peptides identification and biological activities of six different cheese varieties[J].Biology, 2023, 12(1):78.
[44] KAYACAN ÇAKMAKO LU S, DERE S,
LU S, DERE S, ![]() H, et al.Production of bioactive peptides during yogurt fermentation, their extraction and functional characterization[J].Food Bioscience, 2024, 61:104805.
H, et al.Production of bioactive peptides during yogurt fermentation, their extraction and functional characterization[J].Food Bioscience, 2024, 61:104805.
[45] HU Y, LING Y X, QIN Z Y, et al.Isolation, identification, and synergistic mechanism of a novel antimicrobial peptide and phenolic compound from fermented walnut meal and their application in Rosa roxbughii Tratt spoilage fungus[J].Food Chemistry, 2024, 433:137333.
[46] YANG J, ZHAO P P, WANG Q Q, et al.Peptidomics- inspired discovery and activity evaluation of antioxidant peptides in multiple strains mixed fermentation of Porphyra yezoensis[J].Food Chemistry, 2024, 455:139779.
[47] HARYANI Y, ABDUL HALID N, GOH S G, et al.Efficient metabolic pathway modification in various strains of lactic acid bacteria using CRISPR/Cas9 system for elevated synthesis of antimicrobial compounds[J].Journal of Biotechnology, 2024, 395:53-63.
[48] LIU Z Y, HU R, HUANG L J, et al.Lactic acid bacteria with weak post-acidification potential applied for low-salt Paocai fermentation:A perspective from screening to molecular mechanism[J].LWT, 2024, 206:116531.
[49] MARULO S, DE CARO S, NITRIDE C, et al.Bioactive peptides released by lactic acid bacteria fermented pistachio beverages[J].Food Bioscience, 2024, 59:103988.
[50] ZHANG X, ZHENG Y R, LIU Z M, et al.Insights into characteristic metabolites and potential bioactive peptides profiles of fresh cheese fermented with three novel probiotics based metabolomics and peptidomics[J].Food Chemistry:X, 2024, 21:101147.
[51] ZHANG X D, DE LA FUENTE-NUNEZ C, WANG J.Artificial intelligence accelerates efficient mining of functional peptides[J].Life Medicine, 2023, 2(2):lnad005.
[52] JIN H, QUAN K Y, YOU L J, et al.A genomic compendium of cultivated food-derived lactic acid bacteria unveils their contributions to human health[J].Science Bulletin, 2025, 70(11):1761-1765.
[53] 汤传根, 王璟, 张烁, 等.功能肽合成和挖掘策略研究进展[J].合成生物学, 2025, 6(2):461-478.TANG C G,WANG J, ZHANG S, et al.Advances in synthesis and mining strategies for functional peptides[J].Synthetic Biology Journal, 25, 6(2):461-478.
[54] CHANG J R, WANG H T, SU W T, et al.Artificial intelligence in food bioactive peptides screening:Recent advances and future prospects[J].Trends in Food Science &Technology, 2025, 156:104845.
[55] HABIB H M, ISMAIL R, AGAMI M, et al.Exploring the impact of bioactive peptides from fermented milk proteins:A review with emphasis on health implications and artificial intelligence integration[J].Food Chemistry, 2025, 481:144047.
[56] SHI H Y, ZHANG S L.Accurate prediction of anti-hypertensive peptides based on convolutional neural network and gated recurrent unit[J].Interdisciplinary Sciences:Computational Life Sciences, 2022, 14(4):879-894.
[57] SZYMCZAK P, SZCZUREK E.Artificial intelligence-driven antimicrobial peptide discovery[J].Current Opinion in Structural Biology, 2023, 83:102733.
[58] CHARIZANI E, DUSHKU E, KYRITSI M, et al.Predicting the immunomodulatory activity of probiotic lactic acid bacteria using supervised machine learning in a Cornu aspersum snail model[J].Fish &Shellfish Immunology, 2024, 152:109788.
[59] SUN T J, BU H L, YAN X, et al.LABAMPsGCN:A framework for identifying lactic acid bacteria antimicrobial peptides based on graph convolutional neural network[J].Frontiers in Genetics, 2022, 13:1062576.
[60] YUAN J M, MA D L, YANG Y T, et al.A review and prospects:Multi-omics and artificial intelligence-based approaches to understanding the effects of lactic acid bacteria and yeast interactions on fermented foods[J].Innovative Food Science &Emerging Technologies, 2025, 99:103874.
[61] CARPI F M, COMAN M M, SILVI S, et al.Comprehensive pan-genome analysis of Lactiplantibacillus plantarum complete genomes[J].Journal of Applied Microbiology, 2022, 132(1):592-604.
[62] GOH Y J, BARRANGOU R, KLAENHAMMER T R.In vivo transcriptome of Lactobacillus acidophilus and colonization impact on murine host intestinal gene expression[J].MBio, 2021, 12(1):e03 399-20.
[63] BALLARD J, WANG Z X, LI W R, et al.Deep learning-based approaches for multi-omics data integration and analysis[J].BioData Mining, 2024, 17(1):38.
[64] AHMED Z, WAN S B, ZHANG F, et al.Artificial intelligence for omics data analysis[J].BMC Methods, 2024, 1(1):4.
[65] HASHEMI S, VOSOUGH P, TAGHIZADEH S, et al.Therapeutic peptide development revolutionized:Harnessing the power of artificial intelligence for drug discovery[J].Heliyon, 2024, 10(22):e40265.
[66] CHICCO D, HEIDER D, FACCHIANO A.Editorial:Artificial intelligence bioinformatics:Development and application of tools for omics and inter-omics studies[J].Frontiers in Genetics, 2020, 11:309.