炎症性肠病(inflammatory bowel disease,IBD)是一类以肠道慢性复发性炎症为主要特征的疾病,主要包括溃疡性结肠炎和克罗恩病,近几十年来其发病率呈逐年上升趋势[1]。肠黏液屏障由肠上皮细胞表面的黏液层、消化液及抗菌肽等成分构成,作为机体固有防御机制的第一道防线,可将肠道细菌与黏膜组织隔离,核心功能包括:阻止致病微生物定植与入侵、维系共生肠道菌群稳态、参与免疫防御、避免细菌与肠上皮细胞直接接触(后者会导致黏液层通透性增加,进而诱导炎症等疾病发生)[2],同时还能保护肠道黏膜免受损伤[3]。IBD患者的典型特征之一是肠道细菌过度生长,这一现象可能导致肠道通透性升高,进而引发肠黏液屏障损伤及功能障碍[4]。研究表明,过量摄入特定常量营养素,可通过激活先天免疫传感器、扰动肠道微生物代谢等途径,促进肠道炎症反应[5]。膳食成分作为肠道微生物的能量与代谢底物,在调控肠道菌群组成、维持肠道屏障功能完整性方面发挥关键作用[6]。因此,优化膳食结构有望成为缓解IBD病情的有效干预手段。
1 炎症性肠病
IBD产生的机制多样且复杂,肠黏膜的慢性炎症可能是环境、微生物、遗传和免疫因素之间多向相互作用的结果,这导致胃肠道黏膜内免疫系统失衡,促进发炎过程优于抗炎过程[7]。IBD中的肠黏膜被释放细胞因子、趋化分子、活性氧(reactive oxygen species,ROS)和NO的炎性细胞浸润,这些促炎介质会触发并维持肠道中的慢性炎症反应,导致组织损伤和疾病[8]。
2 肠黏液屏障
黏液层一般由黏蛋白、水、脂质等组成,具有防止细菌和有害物质侵入细胞,吸收营养物质等作用。而黏蛋白是肠黏液的主要组成成分,黏蛋白聚糖成分在维持黏液屏障功能中起重要作用[9]。从隐窝底部到肠细胞绒毛尖端都被黏液所覆盖,外来细菌会存在于外黏液层中,但无法到达内部黏液层,而潘氏细胞分泌的抗菌肽和杯状细胞分泌的黏液和MUC2用来保护干细胞和肠细胞不受伤害[10]。当肠腔中菌群失调,导致黏液屏障异常[11]。细菌突破外部黏液层,到达内部黏液层,此时细菌细胞壁分解产生脂多糖(lipopolysaccharide,LPS),通过肠细胞进入,被巨噬细胞和T细胞识别,促使巨噬细胞和T细胞产生促炎细胞因子IL-6、IL-1β和TNF-α,从而导致肠道产生炎症,具体正常肠道黏液屏障和炎症肠道黏液屏障的示意图如图1所示。
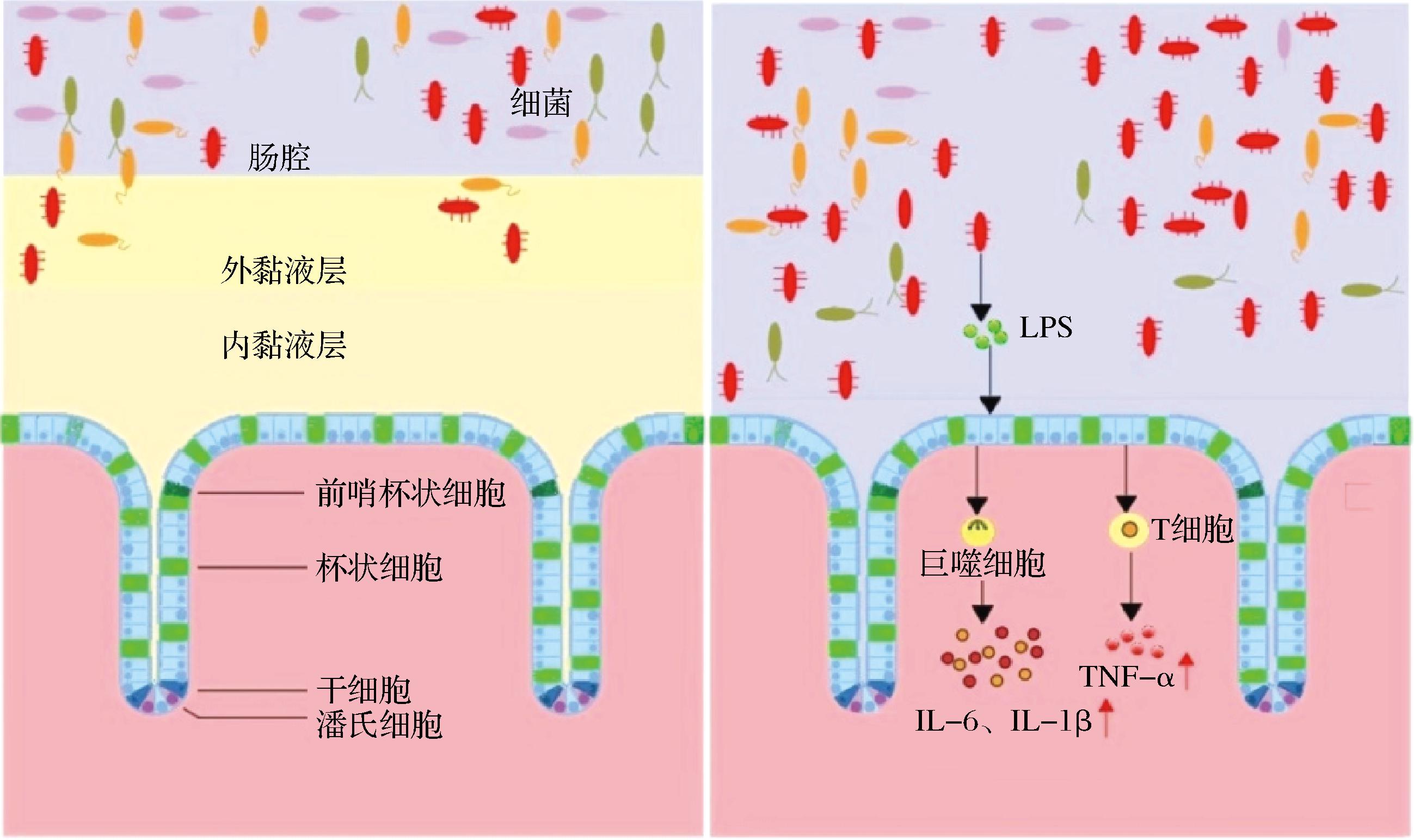
图1 正常状态和炎症状态下肠道黏液屏障模式图
Fig.1 Intestinal mucus barrier model in normal and inflammatory states
3 膳食成分对IBD患者肠黏液屏障功能的影响
膳食成分由许多营养素组成,包括脂质、蛋白质、碳水化合物、矿物质、维生素、酚类、益生菌等物质[12]。饮食模式或特定膳食营养素可通过调控与黏膜保护及炎症反应相关的肠道微生物种群数量,直接或间接影响肠黏液屏障功能,既可能增加肠道通透性,也可能增强肠道屏障的完整性与防御能力[13]。膳食成分会显著改善肠道生理机能,特异性调节肠道屏障完整性[14]。另外膳食成分通过免疫信号直接影响黏液聚糖的数量和比例,间接影响黏蛋白糖基化[15],还会影响肠道黏液的特性[16]。已有大量研究聚焦于膳食成分对肠道的调控作用,其中以膳食纤维(保护肠道黏膜)与高脂肪饮食(诱发肠道炎症)为对照的相关研究备受关注。膳食成分调控肠道功能的具体作用机制详见表1,其作用模式示意图见图2。
表1 膳食成分对肠黏液屏障的影响
Table 1 Effects of dietary components on intestinal mucus barrier
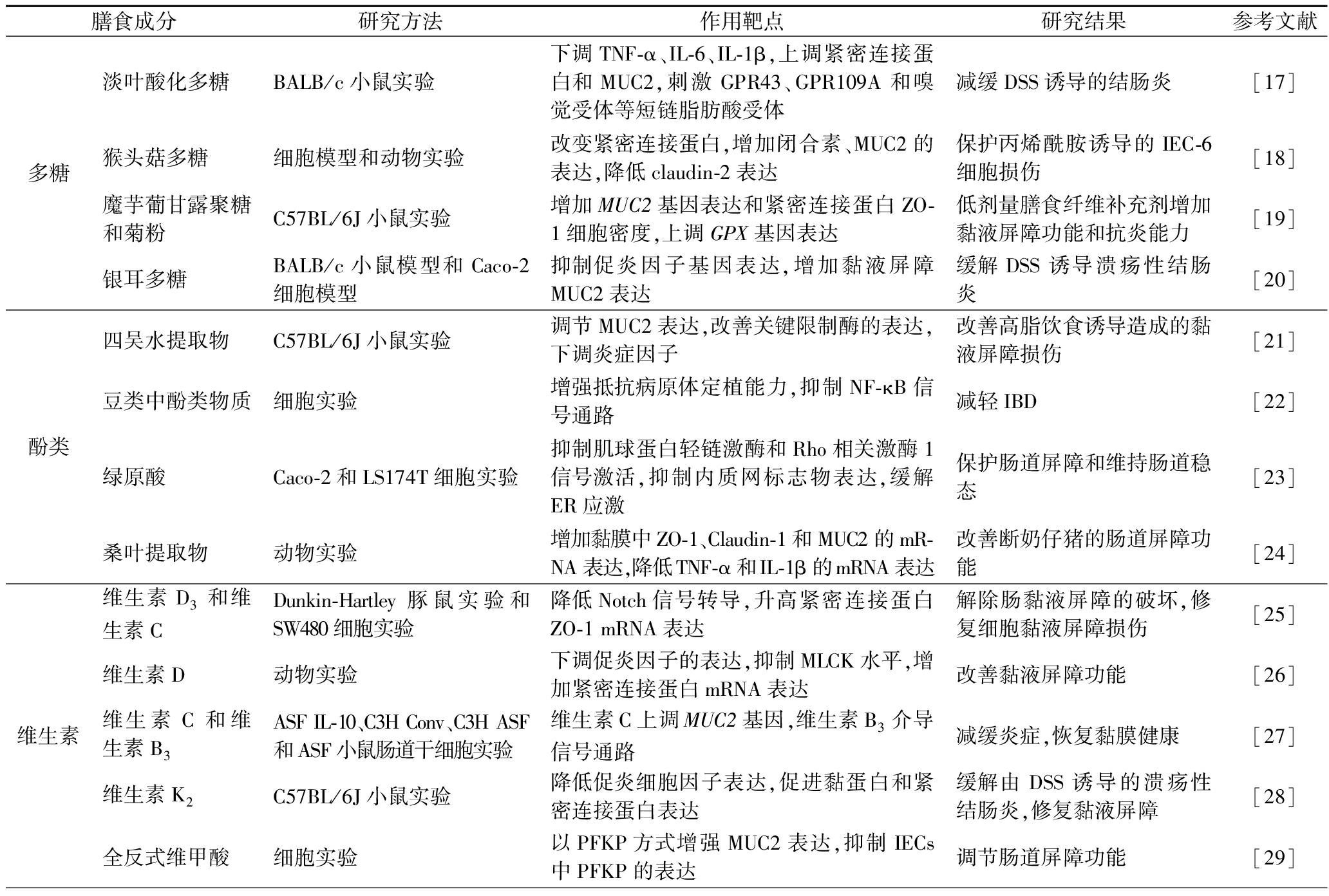
膳食成分研究方法作用靶点研究结果参考文献多糖淡叶酸化多糖BALB/c小鼠实验下调TNF-α、IL-6、IL-1β,上调紧密连接蛋白和MUC2,刺激GPR43、GPR109A和嗅觉受体等短链脂肪酸受体减缓DSS诱导的结肠炎[17]猴头菇多糖细胞模型和动物实验改变紧密连接蛋白,增加闭合素、MUC2的表达,降低claudin-2表达保护丙烯酰胺诱导的IEC-6细胞损伤[18]魔芋葡甘露聚糖和菊粉C57BL/6J小鼠实验增加MUC2基因表达和紧密连接蛋白ZO-1细胞密度,上调GPX基因表达低剂量膳食纤维补充剂增加黏液屏障功能和抗炎能力[19]银耳多糖BALB/c小鼠模型和Caco-2细胞模型抑制促炎因子基因表达,增加黏液屏障MUC2表达缓解DSS诱导溃疡性结肠炎[20]酚类四吴水提取物C57BL/6J小鼠实验调节MUC2表达,改善关键限制酶的表达,下调炎症因子改善高脂饮食诱导造成的黏液屏障损伤[21]豆类中酚类物质细胞实验增强抵抗病原体定植能力,抑制NF-κB信号通路减轻IBD[22]绿原酸Caco-2和LS174T细胞实验抑制肌球蛋白轻链激酶和Rho相关激酶1信号激活,抑制内质网标志物表达,缓解ER应激保护肠道屏障和维持肠道稳态[23]桑叶提取物动物实验增加黏膜中ZO-1、Claudin-1和MUC2的mR-NA表达,降低TNF-α和IL-1β的mRNA表达改善断奶仔猪的肠道屏障功能[24]维生素维生素D3和维生素CDunkin-Hartley豚鼠实验和SW480细胞实验降低Notch信号转导,升高紧密连接蛋白ZO-1 mRNA表达解除肠黏液屏障的破坏,修复细胞黏液屏障损伤[25]维生素D动物实验下调促炎因子的表达,抑制MLCK水平,增加紧密连接蛋白mRNA表达改善黏液屏障功能[26]维生素C和维生素B3ASF IL-10、C3H Conv、C3H ASF和ASF小鼠肠道干细胞实验维生素C上调MUC2基因,维生素B3介导信号通路减缓炎症,恢复黏膜健康[27]维生素K2C57BL/6J小鼠实验降低促炎细胞因子表达,促进黏蛋白和紧密连接蛋白表达缓解由DSS诱导的溃疡性结肠炎,修复黏液屏障[28]全反式维甲酸细胞实验以PFKP方式增强MUC2表达,抑制IECs中PFKP的表达调节肠道屏障功能[29]
续表1
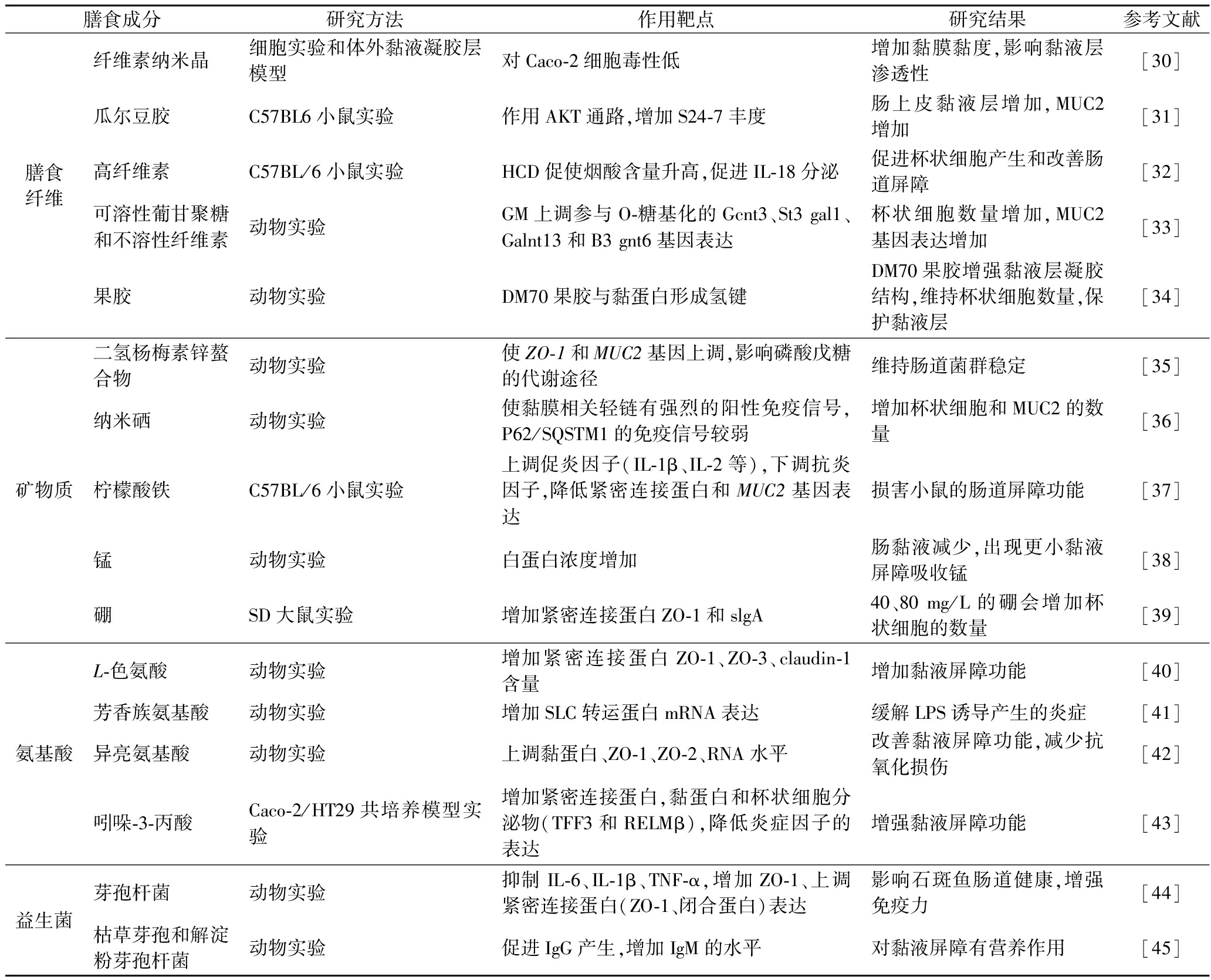
膳食成分研究方法作用靶点研究结果参考文献膳食纤维纤维素纳米晶细胞实验和体外黏液凝胶层模型对Caco-2细胞毒性低增加黏膜黏度,影响黏液层渗透性[30]瓜尔豆胶C57BL6小鼠实验作用AKT通路,增加S24-7丰度肠上皮黏液层增加,MUC2增加[31]高纤维素C57BL/6小鼠实验HCD促使烟酸含量升高,促进IL-18分泌促进杯状细胞产生和改善肠道屏障[32]可溶性葡甘聚糖和不溶性纤维素动物实验GM上调参与O-糖基化的Gcnt3、St3 gal1、Galnt13和B3 gnt6基因表达杯状细胞数量增加,MUC2基因表达增加[33]果胶动物实验DM70果胶与黏蛋白形成氢键DM70果胶增强黏液层凝胶结构,维持杯状细胞数量,保护黏液层[34]矿物质二氢杨梅素锌螯合物动物实验使ZO-1和MUC2基因上调,影响磷酸戊糖的代谢途径维持肠道菌群稳定[35]纳米硒动物实验使黏膜相关轻链有强烈的阳性免疫信号,P62/SQSTM1的免疫信号较弱增加杯状细胞和MUC2的数量[36]柠檬酸铁C57BL/6小鼠实验上调促炎因子(IL-1β、IL-2等),下调抗炎因子,降低紧密连接蛋白和MUC2基因表达损害小鼠的肠道屏障功能[37]锰动物实验白蛋白浓度增加肠黏液减少,出现更小黏液屏障吸收锰[38]硼SD大鼠实验增加紧密连接蛋白ZO-1和slgA40、80 mg/L的硼会增加杯状细胞的数量[39]氨基酸L-色氨酸动物实验增加紧密连接蛋白ZO-1、ZO-3、claudin-1含量增加黏液屏障功能[40]芳香族氨基酸动物实验增加SLC转运蛋白mRNA表达缓解LPS诱导产生的炎症[41]异亮氨基酸动物实验上调黏蛋白、ZO-1、ZO-2、RNA水平改善黏液屏障功能,减少抗氧化损伤[42]吲哚-3-丙酸Caco-2/HT29共培养模型实验增加紧密连接蛋白,黏蛋白和杯状细胞分泌物(TFF3和RELMβ),降低炎症因子的表达增强黏液屏障功能[43]益生菌芽孢杆菌动物实验抑制IL-6、IL-1β、TNF-α,增加ZO-1、上调紧密连接蛋白(ZO-1、闭合蛋白)表达影响石斑鱼肠道健康,增强免疫力[44]枯草芽孢和解淀粉芽孢杆菌动物实验促进IgG产生,增加IgM的水平对黏液屏障有营养作用[45]
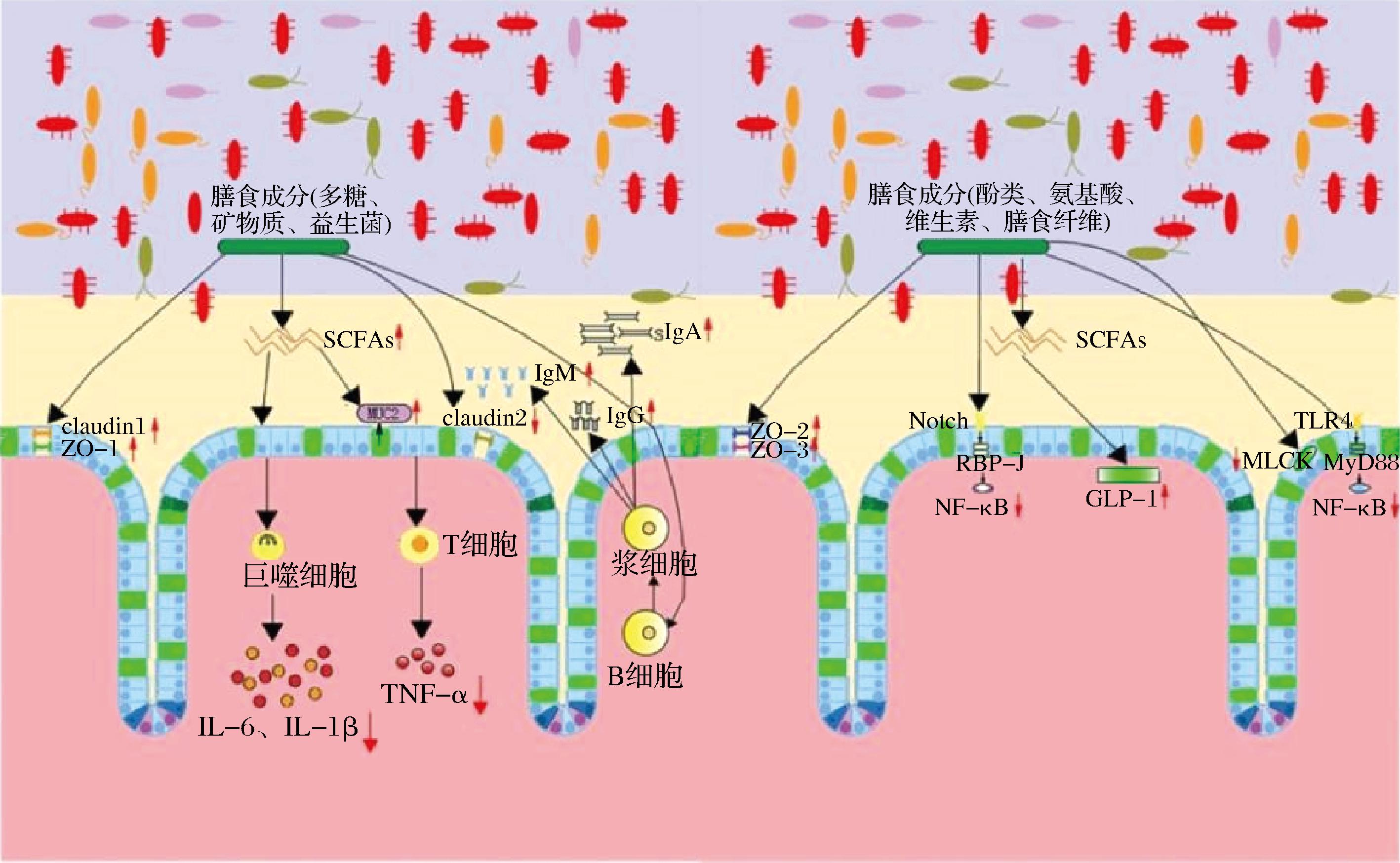
图2 膳食成分对肠黏液屏障作用机制图
Fig.2 Shows the mechanism of dietary components’ action on intestinal mucus barrier
3.1 多糖对IBD患者肠黏液屏障功能的影响
3.1.1 多糖对IBD的影响
多糖是生命体中所必需的大分子,具有增强肠道黏液屏障、改善微生物群落结构以及调控益生菌和致病菌的比例等作用。多糖可以通过多种机制治疗IBD患者,其结构特性、分子量和生物活性可以有效促进肠道损伤的恢复[46],并对IBD有显著的抑制作用。多糖可以降低与IBD相关的组织学评分和结肠损伤[47],促进微生物终产物的产生,如短链脂肪酸(short chain fatty acid,SCFA),并提高抗炎特性[48]。
3.1.2 多糖对IBD的影响机制
3.1.2.1 调控肠道内分泌物水平
肠道中产生的TNF-α和IL-1β等促炎因子,可能造成肠黏液屏障的损坏,增加肠道通透性,从而诱发IBD。实验发现多糖可以调控促炎细胞因子、白介素以及一些肠道内激素的分泌,以此影响肠黏液屏障的功能。比如HAN等[17]将淡叶酸化多糖灌胃肠道炎症小鼠,发现淡叶酸化多糖通过下调TNF-α、IL-6、IL-1β的表达和增加SCFA受体表达来减缓肠道炎症,另外上调紧密连接蛋白和MUC2的表达。SU等[18]发现猴头菇发酵前后2种多糖通过改善环磷酰胺诱导的细胞因子、TJ和MUC2表达,降低IL-1β和IL-6的水平。
3.1.2.2 提高细胞紧密连接蛋白和黏蛋白的表达
ZO家族、claudins和occludins等紧密连接蛋白负责上皮细胞和细胞间的物质扩散,炎症反应会影响紧密连接蛋白的表达[46],因此IBD中紧密连接蛋白的表达总是降低。实验发现多糖可以通过提高细胞紧密连接蛋白的表达,修复肠道损伤,抑制IBD的产生并促进IBD的恢复。比如CHANGCHIEN等[19]用魔芋葡甘露聚糖和菊粉喂养小鼠21 d后发现魔芋葡甘露聚糖和菊粉可以增加小鼠黏液层的厚度、提高黏蛋白密度、促进MUC2基因表达。XIAO等[20]用银耳多糖处理雄性小鼠UC模型和Caco-2细胞模型后发现银耳多糖可以显著提高紧密连接蛋白ZO-1和MUC2的表达,抑制促炎细胞因子表达。
3.2 酚类对IBD患者肠黏液屏障功能的影响
3.2.1 酚类对IBD的影响
酚类物质(polyphenols,PPs)通常存在于植物组织中,对人体健康具有重要作用[49]。越来越多的体外和动物模型证据表明,PPs在控制细胞因子介导的炎症、免疫信号传导和自由基活性方面具有积极作用,这些都与抑制IBD发病机制有关[50]。PPs通过调节在IBD进展中重要的细胞信号通路和转录因子发挥广泛的抗炎和抗氧化作用,此外,PPs会影响免疫细胞以及肠上皮细胞的细胞行为,从而抑制炎症和增强屏障功能[51]。
3.2.2 酚类对IBD的影响机制
PPs对IBD患者肠黏液屏障功能的影响机制主要包括抗炎、调节肠道菌群、提高紧密连接蛋白基因和黏蛋白基因表达,促使黏液的分泌量增加,从而增强黏液屏障功能。1)抗炎机制:PPs通过抑制神经酰胺激酶和长链酰基辅酶A合成酶1的表达[21]并阻断NF-κB等炎症信号通路,来下调促炎因子(IL-8、IL-6、IL-1β和TNF-α)的产生,从而减缓肠道炎症的产生。NICOL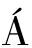 S-GARC
S-GARC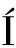 A等[22]发现豆类中酚类化合物诱导IL-8分泌,抑制NF-κB信号通路,促进黏液产生。2)调节肠道菌群:肠道内有多种微生物,肠道细菌通过提供触发免疫细胞活化的抗原或刺激信号,在启动和维持IBD患者肠道的炎症反应中起关键作用,并且PPs可能增加有益菌的丰度[51]。据报道,茶多酚可以改善肠道菌群失调,在结肠炎小鼠中,茶多酚可减少与IBD发生紧密相关的幽门螺旋杆菌数量,同时增加了双歧杆菌的群落丰度[52]。3)增强紧密连接蛋白基因和黏蛋白基因表达:黏蛋白是黏液屏障的重要组成成分,IBD患者的肠黏液屏障大部分属于受损状态,而紧密连接蛋白对肠黏液层具有重要作用,PPs可以通过促使紧密连接蛋白和黏蛋白基因表达。据报道,四吴水提取物(siwu water,SWE)中也包含酚类化合物,RUAN等[21]将四吴水提取物灌胃处理12周高脂饮食雄性小鼠后,发现SWE有效修复了高脂饮食诱导的黏液屏障损伤,增加杯状细胞的数量,促进MUC2的产生和分泌,增加黏液层的厚度。SONG等[23]发现绿原酸可以减轻肠道屏障损伤,另外还可通过抑制内质网标志物的表达激活转录因子,促进MUC2表达。桑叶提取物增加猪回肠黏膜中ZO-1、Claudin-1和MUC2的mRNA表达[24]。
A等[22]发现豆类中酚类化合物诱导IL-8分泌,抑制NF-κB信号通路,促进黏液产生。2)调节肠道菌群:肠道内有多种微生物,肠道细菌通过提供触发免疫细胞活化的抗原或刺激信号,在启动和维持IBD患者肠道的炎症反应中起关键作用,并且PPs可能增加有益菌的丰度[51]。据报道,茶多酚可以改善肠道菌群失调,在结肠炎小鼠中,茶多酚可减少与IBD发生紧密相关的幽门螺旋杆菌数量,同时增加了双歧杆菌的群落丰度[52]。3)增强紧密连接蛋白基因和黏蛋白基因表达:黏蛋白是黏液屏障的重要组成成分,IBD患者的肠黏液屏障大部分属于受损状态,而紧密连接蛋白对肠黏液层具有重要作用,PPs可以通过促使紧密连接蛋白和黏蛋白基因表达。据报道,四吴水提取物(siwu water,SWE)中也包含酚类化合物,RUAN等[21]将四吴水提取物灌胃处理12周高脂饮食雄性小鼠后,发现SWE有效修复了高脂饮食诱导的黏液屏障损伤,增加杯状细胞的数量,促进MUC2的产生和分泌,增加黏液层的厚度。SONG等[23]发现绿原酸可以减轻肠道屏障损伤,另外还可通过抑制内质网标志物的表达激活转录因子,促进MUC2表达。桑叶提取物增加猪回肠黏膜中ZO-1、Claudin-1和MUC2的mRNA表达[24]。
3.3 维生素对IBD患者肠黏液屏障功能的影响
维生素分为水溶性维生素和脂溶性维生素,维生素的缺乏会造成机体某些疾病的发生。
3.3.1 维生素D
维生素D是调节肠道稳态的免疫调节因子[53],可通过影响免疫系统功能及肠道微生物群组成,对IBD的发展中具有保护作用[54]。其主要调节机制是调节黏液中抗菌肽水平、下调促炎因子基因表达、调节紧密连接蛋白和黏蛋白基因表达,以维持黏液屏障功能。有动物实验证明,FAKHOURY等[25]发现维生素D可确保黏液中适当水平的抗菌肽,以此维持黏液屏障和调节黏液层。ZHANG等[26]给被嗜水气单胞菌攻击的草鱼饲料中添加维生素D,观察发现维生素D可以下调促炎细胞因子的表达,降低肠中IL-6、IL-8、IL-1β和TNF-α的mRNA表达。
3.3.2 维生素C
维生素C是一种抗氧化剂,可通过调控氧化还原状态,调节肠道微生物[55],上调紧密连接蛋白和黏蛋白基因表达,抑制促炎因子基因表达来维持肠道黏液屏障功能。据报道,QI等[27]探究维生素C和维生素B3对4种不同菌群小鼠肠道干细胞的影响,发现高剂量的维生素C产生大量糖蛋白,有助于上调MUC2基因来恢复黏膜健康,而维生素B3参与雷帕霉素信号通路,有助于维持肠道内稳态和减缓炎症。QIU等[56]将维生素C和维生素D混合喂养豚鼠5周后发现高剂量的维生素C和维生素D组合会使豚鼠结肠杯状细胞中的黏液减少,但5 μmol/mL维生素C+0.1 μmol/L维生素D3可以通过调控Notch-1通路来调节claudin-2表达,减轻结肠黏膜损伤。
3.3.3 其他维生素
有些维生素通过促进黏蛋白基因表达,来影响IBD患者肠黏液屏障功能。HU等[28]用维生素K2喂养老鼠2周后发现,维生素K2抑制NF-κB信号通路,增加MUC2基因表达,促进黏液蛋白和紧密连接蛋白occludin和ZO-1的表达。全反式维甲酸是维生素A的衍生物,XIE等[29]发现全反式维甲酸的加入可以增强杯状细胞标志物MUC2基因表达,另外全反式维甲酸还通过抑制PFKP的表达来促进MUC2的表达,因为PFKP的过表达会逆转全反式维甲酸对MUC2表达的促进作用。
3.4 膳食纤维对IBD患者肠黏液屏障功能的影响
膳食纤维是植物性食物中的一种营养素,高纤维膳食对肠道疾病有潜在的保护作用,在IBD动物模型中发现补充某些膳食纤维可以减缓肠黏液的病变[57]。膳食纤维通过刺激杯状细胞数量,上调紧密连接蛋白和黏蛋白基因表达,从而增加黏液层的厚度,通过调节肠道菌群、抑制炎症因子表达,影响肠黏液屏障功能。1)调节肠道菌群:膳食纤维的摄入,会增加肠道有益菌的数量、抑制有害菌的产生[58]。2)产生SCFA:SCFA是肠道菌群发酵膳食纤维的产物,丁酸盐可以为肠上皮细胞提供能量,有助于上皮完整,而乙酸盐可以激活白介素18受体来维持肠道屏障完整[58]。SCFA可以促进紧密连接蛋白基因表达,促进黏液分泌和减少肠道通透性,还可以通过抑制促炎因子基因表达来抑制炎症产生。比如:LIN等[30]在体外黏液凝胶层模型上添加纤维素纳米晶体,发现高剂量纤维素纳米晶体可能会影响黏液层的渗透性,增加消化液的黏度。KAJIWARA-KUBOTA等[31]给小鼠喂食含部分水解瓜尔豆胶的饮食后发现,小鼠结肠上皮黏液层显著增加,琥珀酸盐水平显著升高,从而诱导MUC2产生和增加结肠黏液层的厚度。KIM等[32]用高纤维素饮食或低纤维素饮食喂食雌性小鼠3个月,发现高纤维素饮食可促进小鼠肠道杯状细胞产生黏液,低纤维素饮食会导致小鼠肠道杯状细胞数量减少。3)促进黏液层修复:膳食纤维的摄入,可以增加杯状细胞数量,上调黏蛋白基因表达。ZHANG等[33]在小鼠的日粮里添加可溶性葡甘聚糖和不溶性纤维素,结果发现添加葡甘聚糖组的小鼠结肠内杯状细胞数目增多,MUC2基因表达增加,另外葡甘聚糖还参与黏蛋白O-糖基化过程,上调参与O-糖基化过程的Gcnt3、Gcnt4、Galnt13等基因表达。BEUKEMA等[34]发现不同结构的果胶对大鼠肠黏液层影响不同,DM30果胶可以刺激杯状细胞分泌黏蛋白,RG-Ⅰ果胶通过保留杯状细胞数量来保护黏液层,低酯果胶与黏蛋白形成凝胶结构来保护黏液层,而高脂果胶可以增强肠道屏障功能。
3.5 矿物质对IBD患者肠黏液屏障功能的影响
矿物质属于微量元素,虽然机体需要量少,但对机体健康很重要,当缺乏时可能会造成疾病的产生[59]。矿物质影响肠道黏液屏障机制复杂,对黏液屏障功能有利有害,目前研究主要集中在补锌、补硒、补铁上。
3.5.1 锌(Zn)
Zn缺乏在IBD患者中较为常见,有实验发现Zn的缺乏,机体会通过激活IL-23/Th 17轴加重结肠炎,以及降低机体免疫细胞表达,致使免疫力下降从而增加炎症产生的风险[60]。Zn的摄入会促使紧密连接蛋白和黏蛋白基因的表达,维持肠道稳态,提高机体免疫力,从而减缓IBD患者炎症的产生,如WANG等[35]将二氢杨梅素锌螯合物(dihydromyricetin zinc,DMY-Zn)添加到马岗鹅的日粮中,喂食4周后发现DMY-Zn上调肠道屏障基因ZO-1和MUC2的表达和Zn相关基因ZIP 5的表达,有助于维持肠道菌群平衡,提高肠道免疫力。NABI等[61]给肉鸡补充Zn和硒(Se)后发现,肉鸡小肠顶端MUC2分泌量增高。
3.5.2 Se
Se具有减轻氧化应激、调节肠道微生物和阻断结肠炎发生的作用[35],补充Se可以减轻氧化应激和促使黏蛋白基因表达,保护黏液屏障不受损伤。YIN等[36]将纳米硒饲料喂食后,蛋鸡小肠杯状细胞分泌黏液量明显增加,促进黏蛋白MUC2分泌。
3.5.3 铁(Fe)
补Fe可能会产生活性氧,增加肠道通透性,增加促炎因子基因表达,导致肠道炎症的出现[62]。据报道,LUO等[37]给雄性小鼠口服不同剂量的柠檬酸铁持续16周,结果发现不同剂量柠檬酸铁均使小鼠肠内杯状细胞数量下降,降低紧密连接蛋白ZO-1、occludin和MUC2表达,上调促炎细胞因子IL-6、IL-2、IL-1β、TNF-α,下调抗炎细胞因子。
3.5.4 其他矿物质
微量元素除了上述的Fe、Zn、Se外,还有Mn、B等。实验发现在绵羊饲料中添加Mn,进行为期4个月的实验后发现补充Mn-Gly螯合物的组中肠黏液减少[38]。低剂量B的摄入提高紧密连接蛋白的基因表达,而高剂量可能产生相反结果,动物实验发现用不同剂量B喂养大鼠60 d后发现40 mg/L或80 mg/L的B会增加杯状细胞的数量,提高紧密连接蛋白ZO-1和occludin的表达,而过高剂量的B可能会产生相反的效果[39]。
3.6 氨基酸对IBD患者肠黏液屏障功能的影响
氨基酸是人体蛋白质的组成单位,主要分为必需氨基酸和非必需氨基酸。氨基酸是肠道生长和维持黏膜完整性和屏障功能所必需的,可能会起到减少炎症产生、氧化应激和促炎因子表达的作用[63]。LIANG等[40]证实添加0.2%或0.4%的L-色氨酸可以增加仔猪十二指肠和空肠中ZO-1、ZO-3和claudin-1的含量,并且上调pBD2和pBD3的mRNA水平。另外,DUANMU等[41]发现补充芳香族氨基酸膳食补充剂可以提高仔猪体内氨基酸转运蛋白SLC7A11、SLC6A14等mRNA表达水平,刺激CCK分泌,增加色氨酸的含量,间接减少炎症发生。氨基酸补充可以提高黏蛋白和紧密连接蛋白表达。实验证明,异亮氨基酸喂养8周后,杂交疸鲶黏蛋白和ZO-1的mRNA表达上调,黏液屏障功能得以改善[42]。LI等[43]通过Caco-2/HT29细胞共培养模型研究吲哚-3-丙酸对肠道屏障的影响,研究发现上皮电阻增加,ZO-1、occludin、MUC2和MUC4表达上调,杯状细胞分泌物增加。
3.7 益生菌对IBD患者肠黏液屏障功能的影响
益生菌作为调节肠道微生物平衡的一种物质,具有稳定肠黏膜,促进黏液分泌等作用[64]。大量动物实验报道了益生菌可调节紧密连接蛋白和黏蛋白基因表达,维持黏液屏障功能,AMOAH等[44]发现velezensis GPSAK4、枯草芽孢杆菌和龙舌兰芽孢杆菌混合添加上调紧密连接蛋白基因和抗炎细胞因子表达。SU等[65]通过将益生菌喂给刚断奶的仔猪,发现益生菌可以与病原菌蛋白质竞争结合位点,以此防止病原菌的附着,并刺激黏蛋白的分泌和上调肠道TJs蛋白的表达。还有报道益生菌的摄入可以增加体内肽类物质含量和IgM的分泌水平,从而修复黏膜损伤,KONIECZKA等[45]在饲料中添加枯草芽孢杆菌和解淀粉芽孢杆菌活菌等益生菌,给仔猪喂和母猪相同剂量的益生菌,结果发现益生菌增加黏膜中IgM的分泌水平,对益生菌处理母猪的幼猪回肠黏液屏障发挥增强作用。
3.8 临床证据
取IBD患者的血清与上腔中的LPS应用在结肠上皮细胞和巨噬细胞的Transwell系统建立的共培养模型上,发现会促使巨噬细胞产生促炎因子以及生成ROS,此时加入由多糖黄蓍胶与紫草素铁构建的纳米复合材料会显著降低血清促进巨噬细胞产生的促炎因子表达水平,并在细胞水平有缓解氧化损伤的能力[66]。临床研究表明,IBD患者摄入高纤维膳食食物,有助于维持肠道健康,减缓肠道炎症。BROTHERTON等[67]研究1 130名克罗恩病和489名溃疡式结肠炎患者,发现摄入高纤维饮食后患病率大大降低。WU等[68]比较IBD患者和健康人粪便菌群,发现患者的植物乳植杆菌丰度降低,通过补充益生菌,提高紧密连接蛋白的表达水平,减缓了炎症程度,抑制肠上皮细胞凋亡。IBD患者维生素D普遍缺乏,低水平维生素D与肠道损伤相关,可以选取IBD患者若干,每日补充维生素D,观察患者的疾病活动指数(比如炎症标志物水平)是否有变化,以此通过临床实验证明维生素的作用机制。而其他膳食成分均可以按照已有的临床实验进行测试,有望进一步支持膳食成分对IBD的作用机制。
3.9 膳食成分混合使用对IBD患者肠黏液屏障功能的影响
前文已经总结单个膳食成分对IBD的影响机制,在治疗或者缓解IBD时作用效果单一,且可能存在局限性,然而混合使用存在协同效果或拮抗效果,因此研究膳食成分混合使用是否能更安全、更有效地预防和治疗IBD很有必要。目前发现益生元和益生菌混合使用形成合生元对治愈IBD的疗效更高,YUAN等[69]发现将沙棘多糖作为益生元,可以增加双歧杆菌的相对丰度并促进SCFA的产生,同时加入长双歧杆菌、嗜酸乳杆菌形成合生元,可显著改善小鼠的肠道通透性,降低促炎因子(IL-6、IL-1β、TNF-α和IL-17F)的表达水平,提高抗炎因子表达水平,另外该合生元还可通过调节关键肠道菌群结构来平衡Th17/Treg,以此减轻小鼠结肠炎。构建多糖纳米载体,负载IBD患者缺乏的矿物质,递送到肠道内也可以减缓炎症,比如HU等[66]利用多糖黄蓍胶与紫草素铁协同作用治疗IBD,构建好的纳米复合材料可以清除ROS,下调促炎因子减缓局部炎症,调节IL-17RA相关细胞信号传导并减少Th17细胞的聚集,对发炎的肠道区域有免疫效果。ZHU等[70]利用多酚、纳米酶和益生菌之间的协同作用,减轻组织损伤、调控炎症因子网络和抑制免疫细胞过度活化。发现大多数膳食成分混合使用会协同改善肠道健康和减缓肠道炎症,但是也存在拮抗作用,比如高脂高糖可增加肠道有害菌的丰度,抑制有益菌的数量,从而产生肠道炎症。
4 总结
近些年人们主要探究了不同营养素对肠道黏液屏障或黏蛋白的影响,及其对缓解炎症、调节肠道菌群平衡、改善黏液屏障功能等效果。膳食成分均通过保持肠道菌群稳态,增加有益菌的数量,间接增强IBD患者肠黏液屏障功能,还通过抑制抗炎因子基因表达,减缓肠道炎症产生,上调紧密连接蛋白和黏蛋白基因表达,从而增加肠黏液屏障功能。但膳食成分之间影响IBD患者肠黏液屏障功能机制也存在不同之处,多糖被肠道菌群发酵分解成SCFA,促进紧密连接蛋白和黏蛋白产生;酚类通过控制介导肠道炎症产生的细胞介质的表达,调节某些重要信号通路来上调紧密连接蛋白和黏蛋白基因表达;维生素促进黏液抗菌肽的产生,增强机体免疫能力,还可以促进肠上皮细胞分化,降低肠通透性;膳食纤维通过上调黏蛋白O-糖基化基因表达,作用AKT通路,促使黏蛋白增加,肠道黏液层增厚;矿物质减轻氧化应激、调节肠道微生物和阻断结肠炎发生;氨基酸减少氧化应激,增加上皮电阻,降低空肠隐窝深度,间接影响黏液屏障功能;益生菌与病原菌蛋白质竞争结合位点,以此防止病原菌的附着,直接刺激杯状细胞产生黏蛋白。膳食成分通过多种机制改善并修复IBD患者肠黏液屏障功能,具有重要作用,但当前研究仍存在某些机制不清晰或者相关临床证据不足的问题,可能会限制膳食成分在治愈疾病精准应用,另外IBD患者由于个体肠道菌群和炎症程度的不同对膳食成分治愈效果也存在差异,以及缺乏长期实验,大多数都是观察短期的治愈效果,无法确定膳食成分对患者长期的影响,比如是否还会复发或者加重肠道炎症。综上,未来可以利用基因组学和代谢组学深入研究膳食成分作用机制;根据患者个人体质及患病程度制定个性化饮食干预方案,提高膳食成分治愈的有效性;增加临床实验,进行长期追踪,完善该方面的不足;通过纳米技术或者微胶囊技术,利用膳食成分的协同作用,提高靶向递送的精准度,从而开拓预防或治愈IBD的应用道路。
[1] CAI Z B, WANG S, LI J N.Treatment of inflammatory bowel disease:A comprehensive review[J].Frontiers in Medicine, 2021, 8:765474.
[2] 黄春兰, 曾悦.杯状细胞及肠道黏液屏障的功能研究[J].国际消化病杂志, 2017, 37(6):357-360.HUANG C L, ZENG Y.Study on the function of goblet cells and intestinal mucus barrier[J].International Journal of Digestive Diseases, 2017, 37(6):357-360.
[3] 韩菲菲, 彭丽媛, 张学斐, 等.肠道黏液屏障功能的研究进展[J].动物营养学报, 2018, 30(12):4769-4775.HAN F F, PENG L Y, ZHANG X F, et al.Research progress on intestinal mucus barrier function[J].Chinese Journal of Animal Nutrition, 2018, 30(12):4769-4775.
[4] BALESTRIERI P, RIBOLSI M, GUARINO M P L, et al.Nutritional aspects in inflammatory bowel diseases[J].Nutrients, 2020, 12(2):372.
[5] ADOLPH T E, MEYER M, SCHW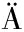 RZLER J, et al.The metabolic nature of inflammatory bowel diseases[J].Nature Reviews Gastroenterology &Hepatology, 2022, 19(12):753-767.
RZLER J, et al.The metabolic nature of inflammatory bowel diseases[J].Nature Reviews Gastroenterology &Hepatology, 2022, 19(12):753-767.
[6] 刘翼翔, 马玉, 李东慧, 等.膳食结构和成分通过调控肠道菌群影响食物过敏的研究进展[J].食品科学, 2021, 42(17):282-290.LIU Y X, MA Y, LI D H, et al.Dietary structure and components affect food allergy through regulating intestinal microflora:A review of the literature[J].Food Science, 2021, 42(17):282-290.
[7] AKUTKO K, STAWARSKI A.Probiotics, prebiotics and synbiotics in inflammatory bowel diseases[J].Journal of Clinical Medicine, 2021, 10(11):2466.
[8] RYMA T, SAMER A, SOUFLI I, et al.Role of probiotics and their metabolites in inflammatory bowel diseases (IBDs)[J].Gastroenterology Insights, 2021, 12(1):56-66.
[9] 金铭, 蒋灿灿.黏蛋白MUC2的糖基单一化对Escherichia侵袭力及代谢功能影响及其参与溃疡性结肠炎发病机制研究[J].实用临床医药杂志, 2023, 27(2):28-34.JIN M, JIANG C C.Glycosylation of MUC2 on the invasions and metabolic functions of Escherichia and its involvement in the pathogenesis of ulcerative colitis[J].Journal of Clinical Medicine in Practice, 2023, 27(2):28-34.
[10] JOHANSSON M E V.Mucus layers in inflammatory bowel disease[J].Inflammatory Bowel Diseases, 2014, 20(11):2124-2131.
[11] FANG J, WANG H, ZHOU Y P, et al.Slimy partners:The mucus barrier and gut microbiome in ulcerative colitis[J].Experimental &Molecular Medicine, 2021, 53(5):772-787.
[12] 王建霖, 李彦蓉, 李婷欣, 等.膳食成分对高血压发生的影响研究进展[J].中华健康管理学杂志, 2023, 9(6):466-470.WANG J L, LI Y R, LI T X, et al.Research progress on the effects of dietary components on the occurrence of hypertension[J].Chinese Journal of Health Management, 2023, 9(6):466-470.
[13] FERN NDEZ-TOMÉ S, ORTEGA MORENO L, CHAPARRO M, et al.Gut microbiota and dietary factors as modulators of the mucus layer in inflammatory bowel disease[J].International Journal of Molecular Sciences, 2021, 22(19):10224.
NDEZ-TOMÉ S, ORTEGA MORENO L, CHAPARRO M, et al.Gut microbiota and dietary factors as modulators of the mucus layer in inflammatory bowel disease[J].International Journal of Molecular Sciences, 2021, 22(19):10224.
[14] ROHR M W, NARASIMHULU C A, RUDESKI-ROHR T A, et al.Negative effects of a high-fat diet on intestinal permeability:A review[J].Advances in Nutrition, 2020, 11(1):77-91.
[15] QU D W, WANG G, YU L L, et al.The effects of diet and gut microbiota on the regulation of intestinal mucin glycosylation[J].Carbohydrate Polymers, 2021, 258:117651.
[16] ETIENNE-MESMIN L, CHASSAING B, DESVAUX M, et al.Experimental models to study intestinal microbes-mucus interactions in health and disease[J].FEMS Microbiology Reviews, 2019, 43(5):457-489.
[17] HAN R, MA Y X, XIAO J B, et al.The possible mechanism of the protective effect of a sulfated polysaccharide from Gracilaria lemaneiformis against colitis induced by dextran sulfate sodium in mice[J].Food and Chemical Toxicology, 2021, 149:112001.
[18] SU Y, CHENG S S, DING Y X, et al.A comparison of study on intestinal barrier protection of polysaccharides from Hericium erinaceus before and after fermentation[J].International Journal of Biological Macromolecules, 2023, 233:123558.
[19] CHANGCHIEN C H, HAN Y C, CHEN H L.Konjac glucomannan polysaccharide and inulin oligosaccharide enhance the colonic mucosal barrier function and modulate gut-associated lymphoid tissue immunity in C57BL/6J mice[J].The British Journal of Nutrition, 2020, 123(3):319-327.
[20] XIAO H Y, LI H L, WEN Y F, et al.Tremella fuciformis polysaccharides ameliorated ulcerative colitis via inhibiting inflammation and enhancing intestinal epithelial barrier function[J].International Journal of Biological Macromolecules, 2021, 180:633-642.
[21] RUAN Z, YU Y J, HAN P H, et al.Si-wu water extracts protect against colonic mucus barrier damage by regulating Muc2 mucin expression in mice fed a high-fat diet[J].Foods, 2022, 11(16):2499.
[22] NICOL S-GARC
S-GARC A M, JIMÉNEZ-MART
A M, JIMÉNEZ-MART NEZ C, PERUCINI-AVENDA
NEZ C, PERUCINI-AVENDA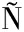 O M, et al.Phenolic compounds in legumes:Composition, processing and gut health [M].Legumes Research-Volume 2.IntechOpen, 2021.
O M, et al.Phenolic compounds in legumes:Composition, processing and gut health [M].Legumes Research-Volume 2.IntechOpen, 2021.
[23] SONG L Q, WU T, ZHANG L, et al.Chlorogenic acid improves the intestinal barrier by relieving endoplasmic reticulum stress and inhibiting ROCK/MLCK signaling pathways[J].Food &Function, 2022, 13(8):4562-4575.
[24] SONG M, WANG C P, YU M, et al.Mulberry leaf extract improves intestinal barrier function and displays beneficial effects on colonic microbiota and microbial metabolism in weaned piglets[J].Journal of the Science of Food and Agriculture, 2023, 103(3):1561-1568.
[25] FAKHOURY H M A, KVIETYS P R, ALKATTAN W, et al.Vitamin D and intestinal homeostasis:Barrier, microbiota, and immune modulation[J].The Journal of Steroid Biochemistry and Molecular Biology, 2020, 200:105663.
[26] ZHANG Y, ZHOU X Q, JIANG W D, et al.Vitamin D promotes mucosal barrier system of fish skin infected with Aeromonas Hydrophila through multiple modulation of physical and immune protective capacity[J].International Journal of Molecular Sciences, 2023, 24(14):11243.
[27] QI Y J, LOHMAN J, BRATLIE K M, et al.Vitamin C and B(3) as new biomaterials to alter intestinal stem cells[J].Journal of Biomedical Materials Research.Part A, 2019, 107(9):1886-1897.
[28] HU S N, MA Y, XIONG K, et al.Ameliorating effects of vitamin K2 on dextran sulfate sodium-induced ulcerative colitis in mice[J].International Journal of Molecular Sciences, 2023, 24(3):2986.
[29] XIE Y, HUANG S, LIU T, et al.All-Trans retinoic acid, a derivative of vitamin a, improved intestinal epithelial barrier function through PFKP [J].Research Square, 2020.DOI:10.21203/rs.3.rs-55382/v1.
[30] LIN Y J, QIN Z J, PATON C M, et al.Influence of cellulose nanocrystals (CNC) on permeation through intestinal monolayer and mucus model in vitro[J].Carbohydrate Polymers, 2021, 263:117984.
[31] KAJIWARA-KUBOTA M, UCHIYAMA K, ASAEDA K, et al.Partially hydrolyzed guar gum increased colonic mucus layer in mice via succinate-mediated MUC2 production[J].NPJ Science of Food, 2023, 7:10.
[32] KIM Y, HWANG S W, KIM S, et al.Dietary cellulose prevents gut inflammation by modulating lipid metabolism and gut microbiota[J].Gut Microbes, 2020, 11(4):944-961.
[33] ZHANG F, ZHAO Y R, LIU X, et al.Effects of soluble glucomannan and insoluble cellulose treatment on mucin secretion and mucin glycosylation-related gene expression in the colons of mice[J].Journal of the Science of Food and Agriculture, 2023, 103(15):7739-7746.
[34] BEUKEMA M, FAAS M M, DE VOS P.The effects of different dietary fiber pectin structures on the gastrointestinal immune barrier:Impact via gut microbiota and direct effects on immune cells[J].Experimental &Molecular Medicine, 2020, 52(9):1364-1376.
[35] WANG R K, REN Y L, JAVAD H U, et al.Dietary dihydromyricetin zinc chelate supplementation improves the intestinal health of Magang geese[J].Biological Trace Element Research, 2024, 202(11):5219-5234.
[36] YIN Y X, AHMED N, HASSAN M F, et al.Effect of nano-selenium on biological mechanism of goblet cells of the small intestine within laying hen[J].Biological Trace Element Research, 2024, 202(4):1699-1710.
[37] LUO Q H, LAO C J, HUANG C, et al.Iron overload resulting from the chronic oral administration of ferric citrate impairs intestinal immune and barrier in mice[J].Biological Trace Element Research, 2021, 199(3):1027-1036.
[38] MAKOV Z, FAIXOV
Z, FAIXOV Z, TARABOV
Z, TARABOV L, et al.Effects of different dietary manganese sources on thickness of mucus layer and selected biochemical and haematological indicators in sheep[J].Acta Veterinaria Brno, 2018, 87(4):351-356.
L, et al.Effects of different dietary manganese sources on thickness of mucus layer and selected biochemical and haematological indicators in sheep[J].Acta Veterinaria Brno, 2018, 87(4):351-356.
[39] LIU T, WANG C F, WU X S, et al.Effect of boron on microstructure, immune function, expression of tight junction protein, cell proliferation and apoptosis of duodenum in rats[J].Biological Trace Element Research, 2021, 199(1):205-215.
[40] LIANG H W, DAI Z L, KOU J, et al.Dietary L-tryptophan supplementation enhances the intestinal mucosal barrier function in weaned piglets:Implication of tryptophan-metabolizing microbiota[J].International Journal of Molecular Sciences, 2019, 20(1):20.
[41] DUANMU Q, TAN B, WANG J, et al.The amino acids sensing and utilization in response to dietary aromatic amino acid supplementation in LPS-induced inflammation piglet model[J].Frontiers in Nutrition, 2022, 8:819835.
[42] YIN L, ZHAO Y, ZHOU X Q, et al.Effect of dietary isoleucine on skin mucus barrier and epithelial physical barrier functions of hybrid bagrid catfish Pelteobagrus vachelli × Leiocassis longirostris[J].Fish Physiology and Biochemistry, 2020, 46(5):1759-1774.
[43] LI J J, ZHANG L, WU T, et al.Indole-3-propionic acid improved the intestinal barrier by enhancing epithelial barrier and mucus barrier[J].Journal of Agricultural and Food Chemistry, 2021, 69(5):1487-1495.
[44] AMOAH K, TAN B P, ZHANG S, et al.Host gut-derived Bacillus probiotics supplementation improves growth performance, serum and liver immunity, gut health, and resistive capacity against Vibrio harveyi infection in hybrid grouper (♀Epinephelus fuscoguttatus×♂Epinephelus lanceolatus)[J].Animal Nutrition, 2023, 14:163-184.
[45] KONIECZKA P, FERENC K, JØRGENSEN J N, et al.Feeding Bacillus-based probiotics to gestating and lactating sows is an efficient method for improving immunity, gut functional status and biofilm formation by probiotic bacteria in piglets at weaning[J].Animal Nutrition, 2023, 13:361-372.
[46] WANG Y K, ZHU H B, WANG X J, et al.Natural food polysaccharides ameliorate inflammatory bowel disease and its mechanisms[J].Foods, 2021, 10(6):1288.
[47] LI C L, WU G S, ZHAO H L, et al.Natural-derived polysaccharides from plants, mushrooms, and seaweeds for the treatment of inflammatory bowel disease[J].Frontiers in Pharmacology, 2021, 12:651813.
[48] FARID M S, SHAFIQUE B, XU R, et al.Potential interventions and interactions of bioactive polyphenols and functional polysaccharides to alleviate inflammatory bowel disease-A review[J].Food Chemistry, 2025, 462:140951.
[49] 姜忠丽, 杜昭换, 赵秀红, 等.酚类物质的研究进展[J].沈阳师范大学学报(自然科学版), 2023, 41(6):548-555.JIANG Z L, DU Z H, ZHAO X H, et al.Research progress of phenolics compounds[J].Journal of Shenyang Normal University (Natural Science Edition), 2023, 41(6):548-555.
[50] HAGAN M, HAYEE B H, RODRIGUEZ-MATEOS A.(poly)phenols in inflammatory bowel disease and irritable bowel syndrome:A review[J].Molecules, 2021, 26(7):1843.
[51] JAMIESON P E, CARBONERO F, STEVENS J F.Dietary (poly)phenols mitigate inflammatory bowel disease:Therapeutic targets, mechanisms of action, and clinical observations[J].Current Research in Food Science, 2023, 6:100521.
[52] TRUONG V L, JEONG W S.Antioxidant and anti-inflammatory roles of tea polyphenols in inflammatory bowel diseases[J].Food Science and Human Wellness, 2022, 11(3):502-511.
[53] VERNIA F, VALVANO M, LONGO S, et al.Vitamin D in inflammatory bowel diseases.mechanisms of action and therapeutic implications[J].Nutrients, 2022, 14(2):269.
[54] WU Z R, LIU D L, DENG F H.The role of vitamin D in immune system and inflammatory bowel disease[J].Journal of Inflammation Research, 2022, 15:3167-3185.
[55] RATAJCZAK A E, SZYMCZAK-TOMCZAK A, SKRZYPCZAK-ZIELI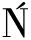 SKA M, et al.Vitamin C deficiency and the risk of osteoporosis in patients with an inflammatory bowel disease[J].Nutrients, 2020, 12(8):2263.
SKA M, et al.Vitamin C deficiency and the risk of osteoporosis in patients with an inflammatory bowel disease[J].Nutrients, 2020, 12(8):2263.
[56] QIU F B, ZHANG Z H, YANG L X, et al.Combined effect of vitamin C and vitamin D(3) on intestinal epithelial barrier by regulating Notch signaling pathway[J].Nutrition &Metabolism, 2021, 18(1):49.
[57] PITUCH-ZDANOWSKA A, BANASZKIEWICZ A, ALBRECHT P.The role of dietary fibre in inflammatory bowel disease[J].Przeglad Gastroenterologiczny, 2015, 10(3):135-141.
[58] ZHANG F, FAN D J, HUANG J L, et al.The gut microbiome:Linking dietary fiber to inflammatory diseases[J].Medicine in Microecology, 2022, 14:100070.
[59] MATTHEWMAN M C, COSTA-PINTO R.Macronutrients, minerals, vitamins and energy[J].Anaesthesia &Intensive Care Medicine, 2023, 24(2):134-138.
[60] WU Y R, LIU C, DONG W G.Adjunctive therapeutic effects of micronutrient supplementation in inflammatory bowel disease[J].Frontiers in Immunology, 2023, 14:1143123.
[61] NABI F, ARAIN M A, ALI FAZLANI S, et al.Effect of in ovo trace element supplementation on immune-related cells of the small intestine of post-hatched broiler chicken[J].Biological Trace Element Research, 2023, 201(8):4052-4061.
[62] OLDENBURG B, KONINGSBERGER J C, VAN BERGE HENEGOUWEN G P, et al.Iron and inflammatory bowel disease[J].Alimentary Pharmacology &Therapeutics, 2001, 15(4):429-438.
[63] LIU Y L, WANG X Y, HU C A.Therapeutic potential of amino acids in inflammatory bowel disease[J].Nutrients, 2017, 9(9):920.
[64] DENG Z X, LUO X M, LIU J X, et al.Quorum sensing, biofilm, and intestinal mucosal barrier:Involvement the role of probiotic[J].Frontiers in Cellular and Infection Microbiology, 2020, 10:538077.
[65] SU W F, GONG T, JIANG Z P, et al.The role of probiotics in alleviating postweaning diarrhea in piglets from the perspective of intestinal barriers[J].Frontiers in Cellular and Infection Microbiology, 2022, 12:883107.
[66] HU J L, WANG X F, SUN Q, et al.A polysaccharide metal phenolic network nanocomposite for theranostic applications in inflammatory bowel disease[J].Advanced Functional Materials, 2025, 35(11):2416918.
[67] BROTHERTON C S, MARTIN C A, LONG M D, et al.Avoidance of fiber is associated with greater risk of Crohn’s disease flare in a 6-month period[J].Clinical Gastroenterology and Hepatology, 2016, 14(8):1130-1136.
[68] WU Y Y, HUANG X Y, LI Q B, et al.Reducing severity of inflammatory bowel disease through colonization of Lactiplantibacillus plantarum and its extracellular vesicles release[J].Journal of Nanobiotechnology, 2025, 23(1):227.
[69] YUAN M Y, CHANG L L, GAO P, et al.Synbiotics containing sea buckthorn polysaccharides ameliorate DSS-induced colitis in mice via regulating Th17/Treg homeostasis through intestinal microbiota and their production of BA metabolites and SCFAs[J].International Journal of Biological Macromolecules, 2024, 276:133794.
[70] ZHU Y, FANG Z Q, BAI J, et al.Orally administered functional polyphenol-nanozyme-armored probiotics for enhanced amelioration of intestinal inflammation and microbiota dysbiosis[J].Advanced Science, 2025, 12(17):2411939.