脂肪酶作为一类具有高效催化活性和立体选择性的生物催化剂,其独特的界面催化特性使其在非均相体系中表现出显著优势。近年来,随着绿色化学与生物制造技术的快速发展,脂肪酶在生物柴油合成、食品加工、手性药物制备及生物传感器等领域的核心作用日益凸显。在生物柴油领域,脂肪酶可通过催化甘油三酯与短链醇的酯交换反应,实现可再生能源的高效转化[1];在食品工业中,其被用于油脂改性、风味物质合成及功能性脂质制备[2];在制药领域,脂肪酶的立体选择性催化为手性药物中间体的合成提供了环境友好型路径[3];此外,基于脂肪酶特异性识别的生物传感器,在环境监测和疾病诊断中展现出重要的应用潜力[4]。然而,游离脂肪酶在工业应用中面临多重技术瓶颈:首先,酶分子在极端pH、高温或有机溶剂环境中易发生构象变化而导致活性丧失;其次,游离酶难以从反应体系中分离回收,导致重复利用性差,显著提高生产成本;最后,酶促反应效率受限于底物传质阻力与酶-底物接触效率。据统计,游离酶成本占生物催化工艺总成本的60%以上,严重制约其规模化应用。因此,开发高效的脂肪酶固定化技术成为突破上述瓶颈的关键。酶固定化技术是通过将游离态酶限制于特定空间或完全固定在载体基质中,使其丧失自由迁移能力从而实现持续催化效能和循环利用的生物处理技术[5]。作为生物酶工程领域广泛应用的高效修饰方法,该技术通过空间约束效应显著提升酶分子的催化效率与反应稳定性,同时优化了工业化操作中的重复使用性能。近年来,随着纳米材料、仿生界面设计与多尺度结构调控技术的突破,固定化脂肪酶在催化活性保留率、载体-酶分子相互作用机制及工业化适配性等方面取得重要进展。本文系统综述脂肪酶固定化技术的最新研究动态,重点解析载体材料设计、固定化策略优化及其工业应用效能提升的内在关联,以期为脂肪酶的高值化应用提供理论依据与技术参考。
1 脂肪酶的来源与特性
脂肪酶是一类广泛分布于微生物、海洋生物及动植物中的水解酶,其来源多样性直接影响其催化特性与工业应用潜力。微生物属脂肪酶因种类丰富、易规模化生产而成为主要工业化来源,代表性产酶菌属包括真菌(如黑曲霉、假丝酵母)、细菌(如耐碱的假单胞菌、耐高温的枯草芽孢杆菌)及酵母(如解脂耶氏酵母),其优势在于高催化活性、宽pH/温度适应性(pH 4~10,20~60 ℃)及可基因改造特性,尤其适用于生物柴油合成与非水相催化反应[6-7]。海洋属脂肪酶近年备受关注,其来源包括深海嗜冷菌、嗜盐古菌及海洋动植物(如褐藻、深海鱼类肝脏),其特性集中于低温(10~20 ℃)或高盐(>3 mol/L NaCl)环境下的高活性,但热稳定性不足需依赖固定化技术强化;此类酶在冷加工食品与手性药物合成中展现出独特价值[8]。动植物属脂肪酶虽在工业化应用中受限,却因特异性催化功能难以替代,例如动物胰脏脂肪酶(如猪胰脂肪酶)对长链甘油三酯具有高效水解能力,以及植物种子脂肪酶(如油菜籽脂肪酶)的立体选择性酯交换能力,但其提取成本高、稳定性差(易受pH/温度波动失活)等问题亟待通过固定化技术优化[9-10]。不同来源脂肪酶的理化特性差异为固定化策略设计提供了多维切入点,同时也对载体适配性、活性保留率及规模化生产成本提出了针对性挑战。不同来源的脂肪酶及其特点比较如表1所示。
表1 不同来源脂肪酶的特性比较
Table 1 Comparison of characteristics of lipases from different sources

来源类别代表来源主要特点工业应用优势存在问题与固定化意义微生物属真菌(黑曲霉、假丝酵母)细菌(假单胞菌、枯草芽孢杆菌)酵母(解脂耶氏酵母)高催化活性,宽pH及宽温度适应性(pH 4~10,20~60 ℃),易于基因工程改造适用于生物柴油合成、非水相反应活性高,适合多种固定化方法,提高重用性海洋属深海嗜冷菌嗜盐古菌海洋动植物(褐藻、深海鱼类肝脏)低温及高盐环境中仍具高活性,活性温度10~20 ℃,耐盐性强(>3 mol/L NaCl)适用于冷链加工、手性药物合成等特殊工艺热稳定性差,依赖固定化提升耐受性与循环使用性动物属动物胰脏(如猪胰脂肪酶)对长链甘油三酯具有高效专一的水解能力适用于食品消化模拟、药物辅酶研究等稳定性差、来源有限,需固定化改善储存与重复使用植物属种子(如油菜籽脂肪酶)具有立体选择性酯交换能力,可用于手性化合物制备用于特种酯合成与光学异构体催化提取成本高、稳定性弱,固定化可提升经济性与操作性
脂肪酶的催化功能与其独特的疏水-亲水双区结构及动态“盖子”机制密切相关[11](图1)。疏水-亲水双区结构表现为:酶分子表面亲水区域通过氢键与水相环境稳定结合,而活性中心则被疏水氨基酸残基(如Leu、Val、Ile)形成的α螺旋或β折叠结构包裹,形成“疏水口袋”;“盖子”机制则指活性位点上方的一段柔性多肽链(通常为10~30个氨基酸),在非极性界面(如油-水界面)或底物诱导下发生构象变化,暴露疏水区并激活催化活性(即“界面激活”)。然而,游离脂肪酶在均相体系中因缺乏界面刺激常处于“闭合”低活性状态,且高温或极端pH易导致“盖子”结构不可逆展开而失活。固定化技术通过载体-酶界面相互作用精准调控酶活性,亲水性载体(如二氧化硅凝胶)则通过限域效应稳定酶构象,减少热运动引起的结构坍塌。由此可见,固定化不仅增强酶的稳定性,更能通过“载体-盖子”协同作用动态调控催化行为,为工业酶理性设计提供了新范式。
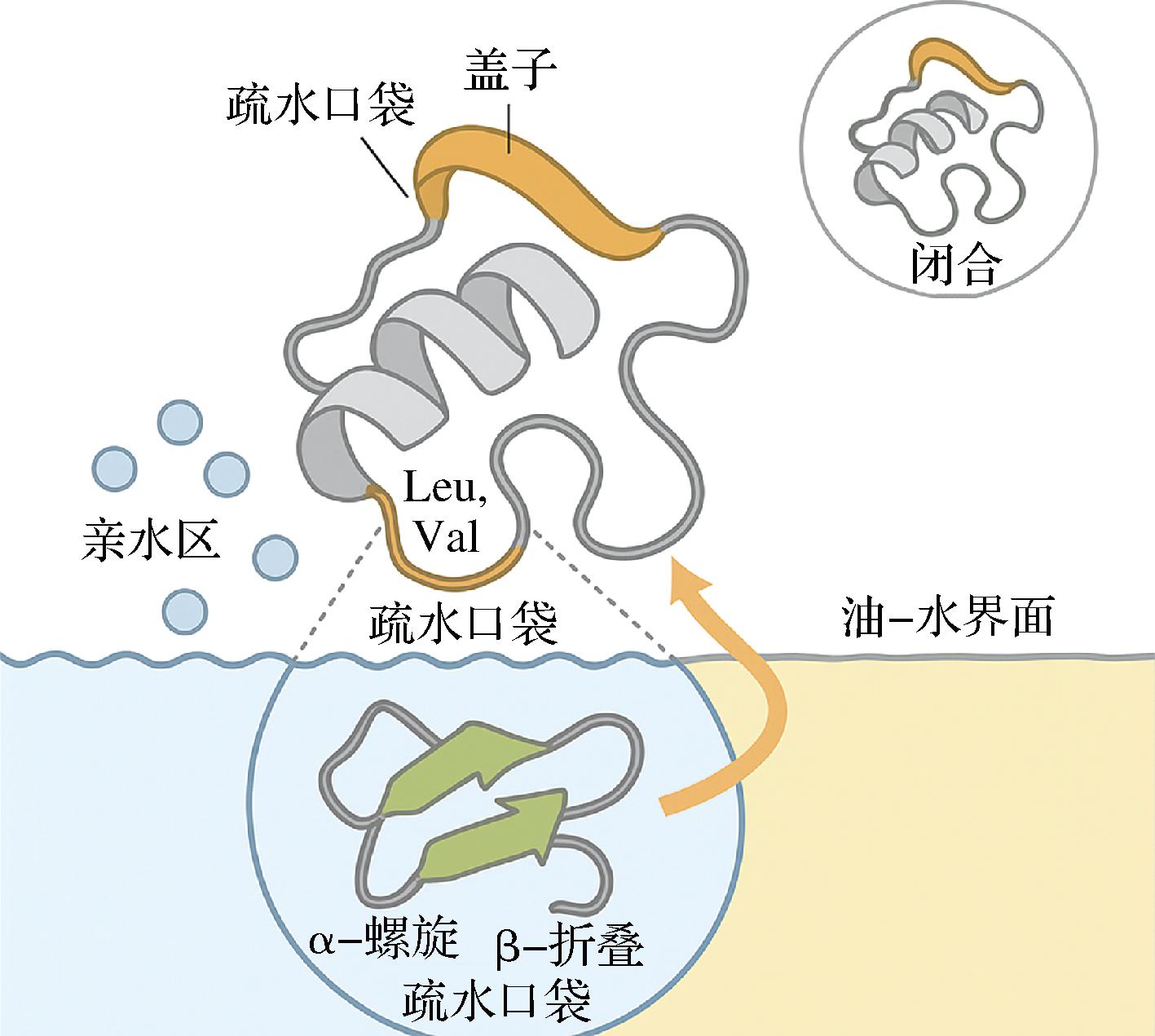
图1 脂肪酶的催化功能与其疏水-亲水双区结构及动态“盖子”示意图[11]
Fig.1 Schematic diagram of the catalytic function of lipase and its hydrophobic hydrophilic dual zone structure and dynamic “lid”[11]
2 经典脂肪酶固定化技术
2.1 物理吸附法
物理吸附法作为酶固定化的基础策略,其核心原理基于酶分子与载体间的非共价相互作用(如范德华力、疏水效应及界面吸附效应),因而存在显著的酶分子脱附风险。大孔树脂、多孔硅玻璃及分子筛等传统多孔材料因其高比表面积特性,成为早期工业化固定化酶体系的核心载体。QIN等[12]以反相乳液聚合制备的多孔聚丙烯酰胺水凝胶微球(porous polyacrylamide hydrogel microspheres, PHM)为载体,通过氢键相互作用吸附脂肪酶。与游离脂肪酶相比,所得脂肪酶多孔聚丙烯酰胺水凝胶微球(lipase porous polyacrylamide hydrogel microspheres, L-PHMs)表现出更高的温度和pH稳定性,最佳酶活性达到1 350 U/g(pH 6,40 ℃)。L-PHM在重复使用20次后仍可保持其原始活性的49%。此外,L-PHMs已成功应用于催化共轭亚油酸乙酯的合成。这种固定化方法为脂肪酶在酯合成中的应用开辟了一条新途径。物理吸附法的优势在于工艺简便、酶活性保留率较高、载体可重复利用、经济性突出且无需对酶进行化学修饰,然而其局限性亦不可忽视,主要表现为固定化酶的稳定性不足、酶分子易从载体表面解离、载体材料可能非特异性吸附反应产物等。
2.2 交联法
交联法是脂肪酶固定化中常用的一种技术,其核心在于利用交联剂在载体与酶分子之间建立稳定的共价或物理连接,从而实现酶的固定。具体操作包括:先选用具备活性官能团的载体,再通过如戊二醛、聚乙二醇二醚或聚乙烯亚胺等交联剂,引发酶分子与载体之间或酶分子间的交联反应,使酶牢固结合于载体表面。林海蛟等[13]构建了一种基于“大孔吸附树脂-先交联后吸附”的固定化策略,对海洋脂肪酶的酶学性质与稳定性进行了系统研究。该方法以大孔吸附树脂HPD700为载体,新戊二醇二缩水甘油醚为交联剂,先在温度35 ℃、pH 5.5、交联剂质量分数0.5%、反应时间2 h的条件下完成酶的交联,再通过正交优化在40 ℃、1.0 g载体量、吸附2 h的条件下完成吸附固定。实验结果表明,该方法获得的固定化酶活力可达190.80 U/g,酶活性回收率为43.04%。与游离酶相比,固定化脂肪酶最适反应温度提升了15 ℃,热稳定性显著增强,在连续使用5次后仍保留57.38%酶活力,低温贮存(4 ℃)60 d后仍可保持69.40%残余酶活力,显示出优异的操作稳定性和贮存稳定性。
2.3 共价结合法
共价结合法是当前酶固定化研究中应用广泛且机制明确的一种方法,其核心原理是通过脂肪酶分子中所含的功能基团(如氨基、羧基、巯基和羟基)与载体表面官能团之间形成稳定的共价键结合,实现酶的不可逆性固定。这种方式具有固定牢固、不易脱落的优势,能显著提高酶的结构稳定性和对高浓度底物及复杂反应环境的耐受性。TANG等[14]开发了一种基于准确选择脂肪酶固定位点的新型位点特异性和共价固定策略。脂肪酶上官能团的计算机辅助结构分析表明,具有游离氨基的赖氨酸残基远离催化袋和盖子,适合选择作为最佳固定位点,以有效减少其活性损失。同时,天然多酚修饰的磁性纳米粒子可以增加活性固定位点,脂肪酶可以通过共价反应直接固定。与随机固定(42.5%和55.9%)相比,这种特定位点固定系统在活性恢复(71.3%)方面表现较好。该技术对载体的功能化程度具有较高要求,需具备丰富的反应基团(如环氧基、羧基或氨基)或可设计性界面,以实现与酶的高效共价偶联。典型化学键合形式包括异脲键、重氮键、烷基化键等,这类强相互作用能有效维持固定化酶的结构稳定性,但需精确控制反应条件以避免酶活性位点受损。
2.4 包埋法
包埋法是通过网格状凝胶或选择性通透膜材料(如卡拉胶、聚乙烯亚胺、聚丙烯酰胺等聚电解质体系)将酶分子限域于三维空间内的固定化策略。该方法的优势在于可高效截留酶分子(固定化率>90%)并实现多酶体系协同固定,但其局限性在于载体内部传质阻力较大,当催化反应速率较高时,底物/产物的扩散受限易导致局部浓度梯度增大,进而引发载体结构溶胀甚至破裂,显著降低反应效率。传统固定化方法优缺点如表2所示。
表2 传统固定化方法的优缺点
Table 2 Advantages and disadvantages of traditional immobilization methods
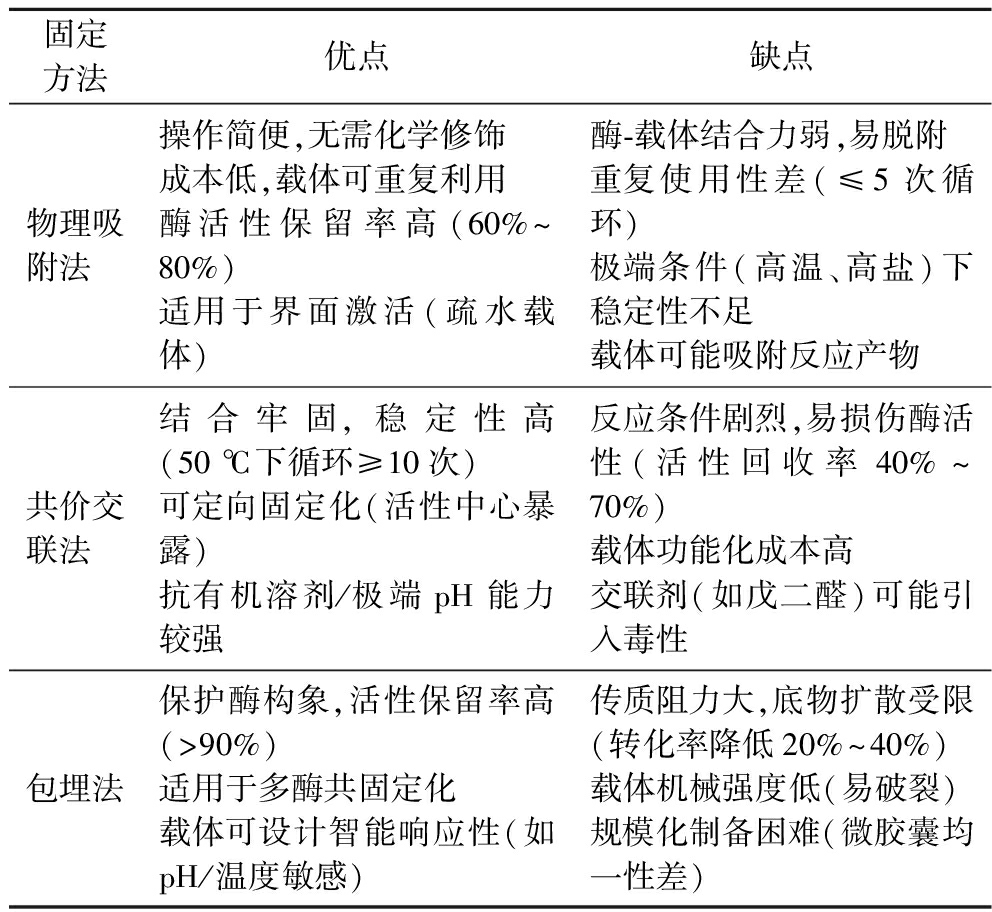
固定方法优点缺点物理吸附法操作简便,无需化学修饰成本低,载体可重复利用酶活性保留率高(60%~80%)适用于界面激活(疏水载体)酶-载体结合力弱,易脱附重复使用性差(≤5次循环)极端条件(高温、高盐)下稳定性不足载体可能吸附反应产物共价交联法结合牢固,稳定性高(50 ℃下循环≥10次)可定向固定化(活性中心暴露)抗有机溶剂/极端pH能力较强反应条件剧烈,易损伤酶活性(活性回收率40%~70%)载体功能化成本高交联剂(如戊二醛)可能引入毒性包埋法保护酶构象,活性保留率高(>90%)适用于多酶共固定化载体可设计智能响应性(如pH/温度敏感)传质阻力大,底物扩散受限(转化率降低20%~40%)载体机械强度低(易破裂)规模化制备困难(微胶囊均一性差)
3 新型固定化载体的研究进展
在脂肪酶固定化技术的创新研究中,载体材料的分类设计与功能强化成为提升酶工程性能的核心突破口。根据载体基质特性,当前主流技术聚焦三大方向:无机载体、有机载体及智能响应载体。其中,无机载体[如金属有机框架(metal-organic frameworks,MOFs)、介孔二氧化硅SBA-15]凭借其高比表面积(>1 000 m2/g)、可调孔径(2~30 nm)及优异化学稳定性,可实现脂肪酶的高密度负载(>90%固定化率)与抗溶剂变性保护;有机载体(如聚丙烯酰胺水凝胶、壳聚糖-纤维素复合物)则通过柔性网络结构维持酶分子天然构象,其生物相容性可减少活性位点损伤(活性保留率>85%);智能响应载体(如温敏型聚N-异丙基丙烯酰胺、pH敏感型聚电解质)通过环境刺激(温度/pH/光)动态调控载体孔径或表面电荷,实现酶活性的“开关式”精准操纵。这些载体的定向固定化策略的交叉创新,正推动脂肪酶工程从“被动负载”向“智能调控”跃迁。
3.1 无机载体
3.1.1 MOFs
金属有机骨架也称多孔配位聚合物,它是由金属离子和有机配体经配位作用形成的高度有序的多孔有机-无机杂化材料。鉴于MOFs的金属节点和有机配体几何结构丰富,且二者连接方式多样,所以可依据特定功能来设计合成MOFs的结构[15-16]。MOFs的多样性使其在催化、燃料储存、分离和生物医学等领域得以广泛应用[17-20]。MOFs具备比表面积大、孔隙率高、孔径易于调节、金属节点和配体易修饰以及合成条件温和等优势,因此它是酶固定化的有效载体。近年来,众多MOF-酶复合材料取得了前所未有的成果,在诸多方面远超游离酶,MOFs作为酶固定化载体材料也愈发受到人们青睐。
常见的MOFs类型有沸石咪唑骨架材料(zeolitic imidazolate frameworks,ZIF)、奥斯陆大学系列金属有机骨架(universitetet i Oslo,UiO)、拉瓦锡研究所系列材料(materials of institut Lavoisier,MIL)等。其中,ZIF是由有机咪唑酯交联连接到过渡金属上形成的四面体框架,常见的金属离子为Zn(Ⅱ)或Co(Ⅱ)。ZIF-67是最常用的沸石咪唑骨架形式之一,由钴阳离子(Co2+)和有机配体(二甲基咪唑)组成[21](图2-a)。ZHONG等[22]首先通过分子模拟研究了具有不同盖子结构的脂肪酶在不同疏水性水平的界面行为差异,发现合理的亲水/疏水表面可以促进脂肪酶进行界面活化。基于这些发现,制备了一种由疏水配体组成的新型“巢”状超疏水(nest-like ZIF, ZIFN),并用于固定米曲霉脂肪酶(Aspergillus oryzae lipase, AOL)(AOL@ZIFN)。AOL@ZIFN在对棕榈酸对硝基苯酯的水解中表现出比游离脂肪酶高2.0倍的活性。特别是,用适量的亲水性单宁酸(tannic acid, TA)对超疏水性ZIFN进行修饰,可以显著提高固定化脂肪酶的活性。AOL@ZIFN-TA的活性比游离脂肪酶高30倍,并且在连续5个循环后仍保持其初始活性的82%,表明具有良好的可重复使用性。UiO-66以锆(Zr)为核心金属元素,通常由六核锆氧簇Zr6O4(OH)4作为结构单元,这种簇通过强Zr—O键连接,赋予材料极高的化学稳定性和热稳定性(分解温度可达500 ℃)(图2-b)[23-24]。ZHONG等[25]通过在MOFs上固定化脂肪酶,成功合成了一种新的生物催化剂PCL@UiO-67(Zr)。与游离脂肪酶相比,锆基有机骨架材料UiO-67(Zr)对固定化Pseudomonas cepacia脂肪酶(Pseudomonas cepacia lipase,PCL)的修饰大大提高了它们在有机溶剂中动力学拆分外消旋4-氯-扁桃酸时的对映选择性。MIL系列材料以过渡金属为核心,主要包括三价金属离子(如Cr3+、Al3+、Fe3+、V3+)或二价金属离子(如Zn2+、Cu2+)。主要采用二羧酸(如对苯二甲酸、戊二酸)或三羧酸配体(如均苯三甲酸)作为有机配体。例如,MIL-53系列以对苯二甲酸为配体,而MIL-100则使用均苯三甲酸与金属簇结合(图2-c)。GHASEMI等[26]采用柔性纳米多孔MIL-53(Fe)用作特异腐质脂肪酶和米黑根毛霉脂肪酶的原位和共价结合固定的载体。在超声波辐射下载体被N,N-二环己基碳二亚胺官能化进行共价结合附着到酶表面。结果表明,即使在极端温度(在80 ℃时约为其初始活性的100%)和pH值(在pH=5时超过90%,在pH=9时超过100%)的条件下,所固定脂肪酶的稳定性仍有较大提高,在重复使用多达7个反应周期后仍具有90%以上的活性。
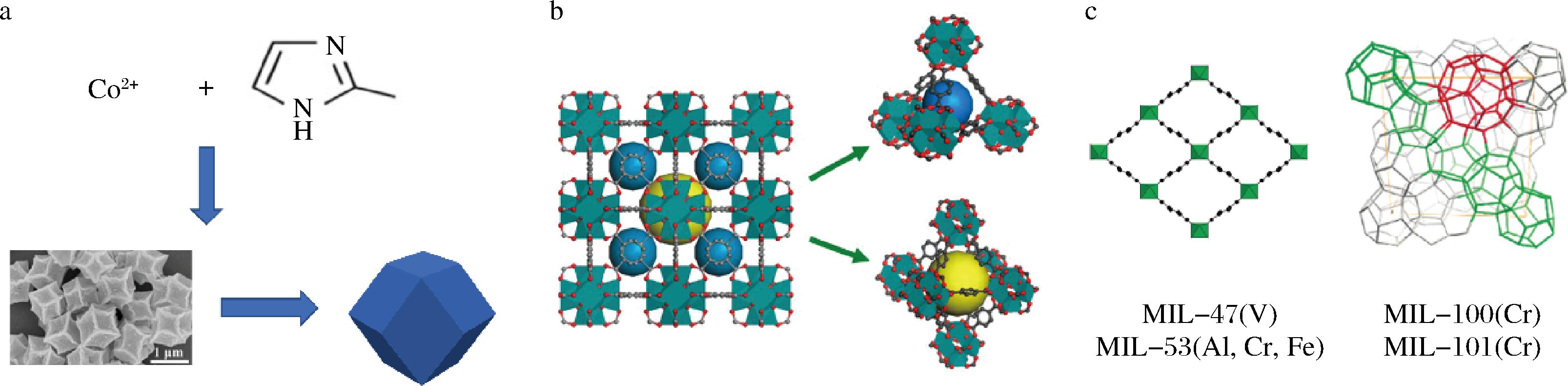
a-ZIF;b-UiO;c-MIL
图2 ZIF、UiO和MIL系列结构示意图
Fig.2 Schematic diagram of ZIF, UiO, and MIL series structures
3.1.2 介孔二氧化硅
介孔二氧化硅材料凭借其独特的多孔架构,在生物催化与化学固定化领域作为一种载体而广泛使用[27]。然而,在实际应用中暴露出机械稳定性不足的缺陷,导致负载的催化剂易发生结构崩解,同时活性组分易从载体表面脱落。针对这些局限性,通过表面功能化修饰或孔道结构调控等手段对介孔二氧化硅进行改性优化,已成为提升其工程适用性的核心研究方向。WANG等[28]创新性地利用卤素及卤烷烃修饰的介孔硅材料SBA-15作为载体,将多种脂肪酶通过界面激活机制固定在功能化载体表面,并研究了固定化脂肪酶的水解活性和甘油解性能(图3-a)。SBA-15经卤素和卤代烷烃改性后,具有优异的水解活性和稳定性。然而,二氧化硅在酶固定化中一般需要对其结构进行二次修饰以改善酶浸出现象,其表面具有丰富的羟基,可以与各种试剂反应从而得到亲水-疏水的表面[29]。硅烷醇基团改性二氧化硅对脂肪酶固定化的影响主要体现在载体表面性质调控与酶活性保留的协同优化上。通过硅烷偶联剂对二氧化硅表面硅烷醇基团(—Si—OH)进行功能化修饰,可引入氨基、环氧基或疏水基团等活性官能团,从而调节载体的亲疏水性及化学亲和力。同时,硅烷醇基团与硅烷偶联剂形成的化学键(如Si—O—Si)可提高载体机械稳定性,减少酶脱落现象(图3-b)[30]。
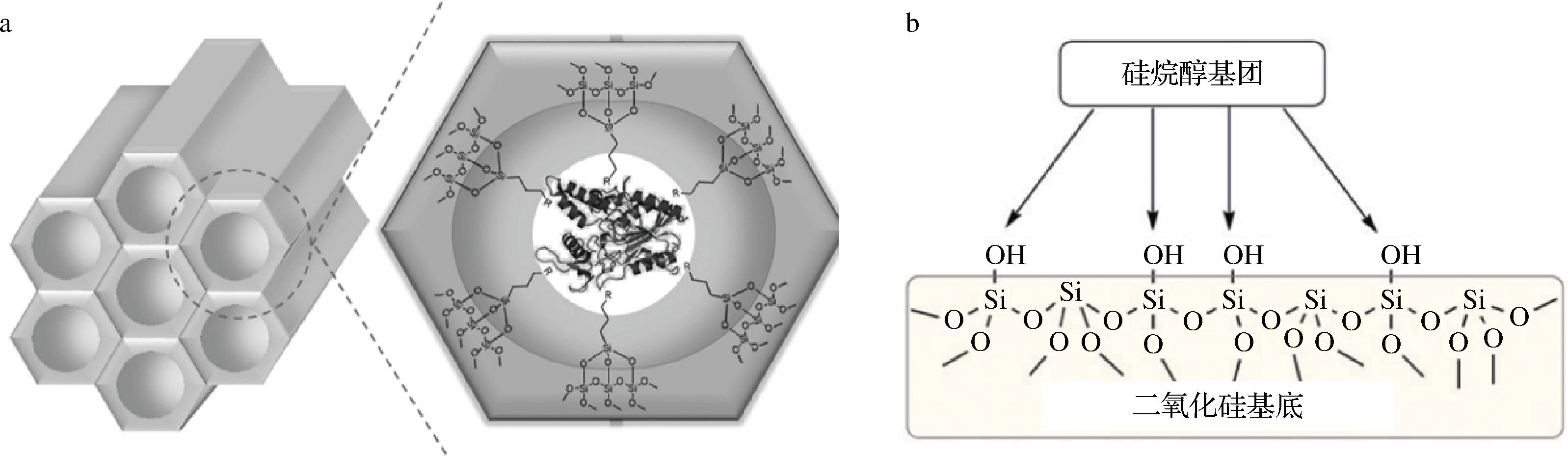
a-脂肪酶固定化载体SBA-15结构示意图;b-硅烷醇基团修饰二氧化硅表面
图3 不同载体固定脂肪酶示意图
Fig.3 Schematic diagram of lipase immobilization on different carriers
3.2 有机载体
3.2.1 天然高分子
在各种酶固定化载体中,壳聚糖(chitosan,CTS)、几丁质、海藻酸盐、纤维素等生物聚合物由于其独特的特性(如无毒、可生物降解、对蛋白质具有良好的亲和力)而更具实用性[31]。此外,这些天然生物聚合物由于具有生物相容性,能够最大程度地减少对脂肪酶多肽链的不利影响。而且,这些聚合物的化学成分中具有羟基、羰基和氨基等多种活性基团,这使得聚合物载体与酶之间能够直接反应,并简化了表面的调节[32]。
CTS是甲壳素(第二丰富的生物聚合物)的N-脱乙酰化衍生物(图4-a),甲壳素主要从真菌的细胞壁和甲壳类动物(主要是蟹、虾、龙虾和磷虾)的外壳中获得。由于CTS的游离氨基和羟基,其具有多功能性、生物相容性、生物降解性、低成本、环境友好等特性。然而,CTS也存在低机械强度、低耐热性、低吸附选择性和其仅在稀酸溶液中具有溶解性等缺点,这限制了其大规模应用。通过物理及化学改性能够使其具有更高的孔隙率和表面积,更好地作为固定脂肪酶的载体。DOS SANTOS等[33]提出一种基于聚醛淀粉(polyoxymethylene starch, PAS)交联方法,将荧光假单胞菌脂肪酶共价固定于CTS载体的策略,用于非对称二醇的动力学分辨研究(图4-b)。结果表明,在以PAS支持体系为固定化底物的动力学分辨反应中,(RS)-1-苯乙醇与(RS)-1-苯丙醇的转化率分别为43%(24 h)和36%(36 h),其产物手性纯度(eep)均高于99%。纤维素因其聚合度低、比表面积大而被用作脂肪酶固定载体。作为其改性形式,二醛纤维素由于其活性醛基团与磁性纳米粒子被用于交联和固定根霉脂肪酶。为了尽可能保持原有的酶活性,提高脂肪酶的稳定性,GUO等[34]将根霉脂肪酶成功固定在磁性二醛纤维素纳米粒子上(图4-c)。在最佳工艺条件下可以获得最大的固定化产率[(60.03±0.49)%]和回收活性[(88.88±0.61)%]。此外,固定化酶在储存30 d后的恢复活性仍达到(50.60±0.59)%,在6个循环后保留为(52.10±0.57)%。
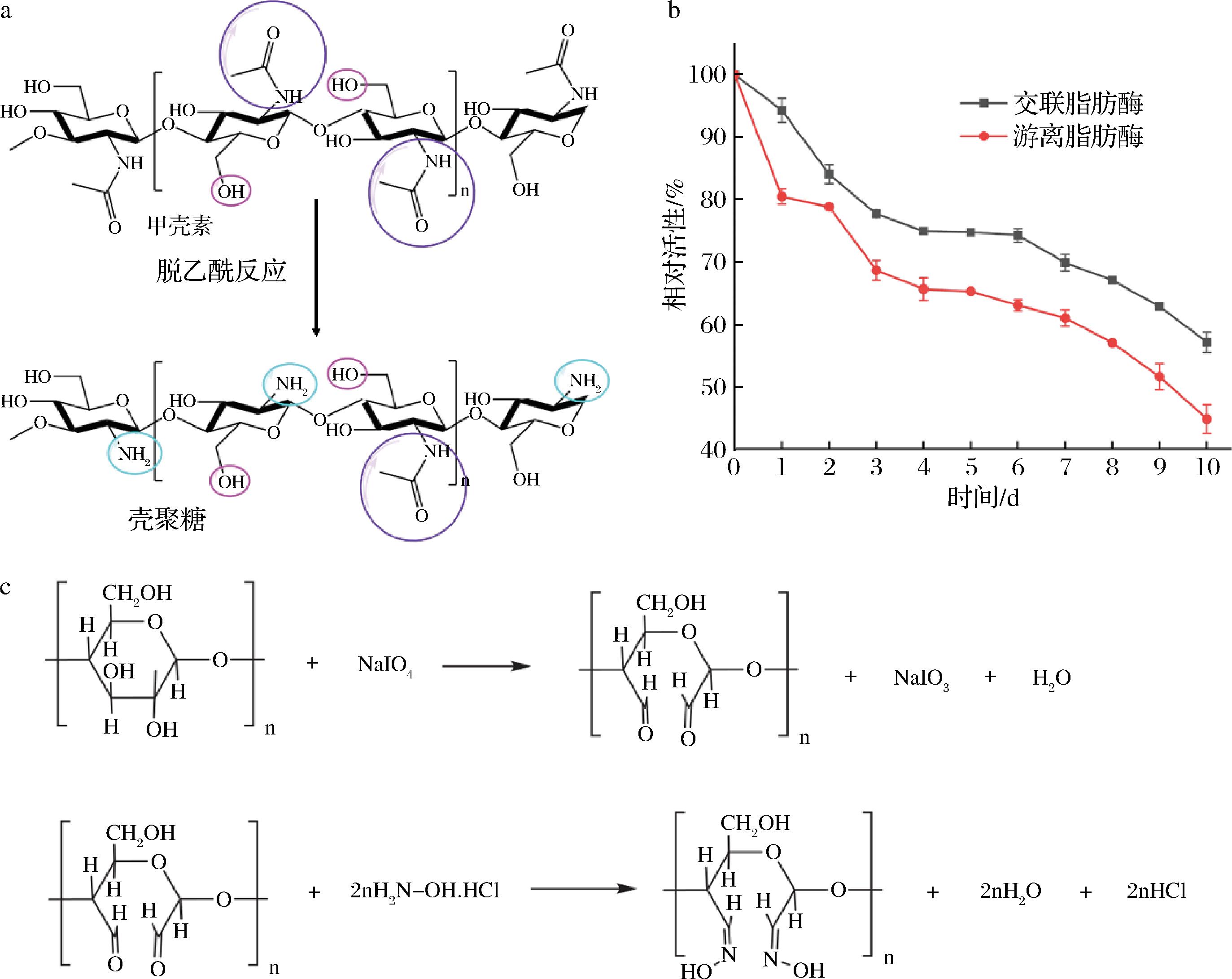
a-甲壳素和CTS的结构;b-游离脂肪酶和交联脂肪酶在40 ℃下的储存稳定性;c-二醛纤维素的制备方案和盐酸羟胺与二醛纤维素的反应机理图
图4 天然高分子示意图及固定脂肪酶机理
Fig.4 Schematic diagram of natural polymers and mechanism of immobilized lipase
3.2.2 合成聚合物
合成聚合物作为有机载体在脂肪酶固定化中的应用原理主要基于其可调控的化学结构与物理性质,通过功能基团与酶分子的定向结合及多孔结构的传质优化实现高效固定[35]。以丙烯酸类聚合物为例,王宁[36]通过静电纺丝技术制备甲基丙烯酸甲酯-丙烯酸共聚纳米纤维,利用CTS对其改性,并在CTS上生长聚甲基丙烯酸钠聚合物刷,研究了改性纳米纤维对脂肪酶的固载量以及稳定性的影响。结果表明:当甲基丙烯酸钠浓度为0.1 mol/L时,酶载达到165 mg/g。相比于游离酶,固定化酶在最低点的相对活性相比游离酶提升325%和400%;60 ℃下储存10 h后固定化酶的相对活性相比游离酶提升17%。环氧基大孔树脂则依赖环氧基的高反应活性,在温和条件下与脂肪酶的氨基、巯基或羟基发生开环反应,形成共价键[37]。通过引入第三单体(如丙烯酸丁酯)优化树脂疏水性和孔径分布,可形成双孔结构,既增加酶负载量又促进底物扩散[38]。刘文涛[39]以乙酸正戊酯和正辛醇为致孔剂采用悬浮聚合合成环氧基大孔树脂用于脂肪酶的固定化。环氧基大孔树脂通过调节交联剂比例,使固定化酶的最适温度提升10~15 ℃,并在宽pH范围内保持高活性恢复率(83.3%以上)。
4 固定化脂肪酶的应用领域
4.1 生物柴油
当前,生物柴油的生产方式主要采用化学催化法。这种方法借助酸或碱作为催化剂推动催化转酯反应的进行。但该方法存在一定局限性,它对原料的酸值有着较高要求,同时还伴有醇油比高、催化剂难以回收再利用等问题,并且会腐蚀生产设备、对环境造成污染。酶法生产生物柴油则是依靠脂肪酶的催化功能,促使油脂与短链醇发生酯交换反应。这一方法是生物柴油实现工业化生产的未来发展趋势。与化学催化法相比,酶法具有诸多优势,其反应条件较温和,纯化程序简单,产物相对容易回收,而且对含水量和酸值不敏感,因此受到了广泛的关注。
RAHIM等[40]使用磁性碳化Macro-MIL-88A进行脂肪酶固定用于生产生物柴油。结果表明,与Micro-Fe3O4-C相比,固定在Macro-Fe3O4-C上的脂肪酶(Macro-Fe3O4-C-TLL)在生物柴油生产过程中表现出更高的甲醇耐受性。研究发现,聚二甲基硅氧烷修饰在生物柴油生产过程中保持了固定化脂肪酶的高酶负载量和良好的可重复使用性。JIANG等[41]构建了一种通过自由基聚合合成的聚合物微凝胶固定化脂肪酶催化系统。金属可以与多个位点配位并从微凝胶表面接枝。脂肪酶活性结果表明,锌和脂肪酶微凝胶表现出最佳的催化效率,锌/脂肪酶微凝胶共催化体系在不同温度和pH下均表现出快速稳定的催化作用。该作用有助于酶/金属微凝胶的界面结构。此外,锌/脂肪酶微凝胶可以完成生物柴油的生产和开环聚合。不同载体固定不同脂肪酶在生物柴油生产中的部分应用如表3所示。
表3 不同载体固定化脂肪酶催化生产生物柴油
Table 3 Production of biodiesel catalyzed by immobilized lipase on different carriers
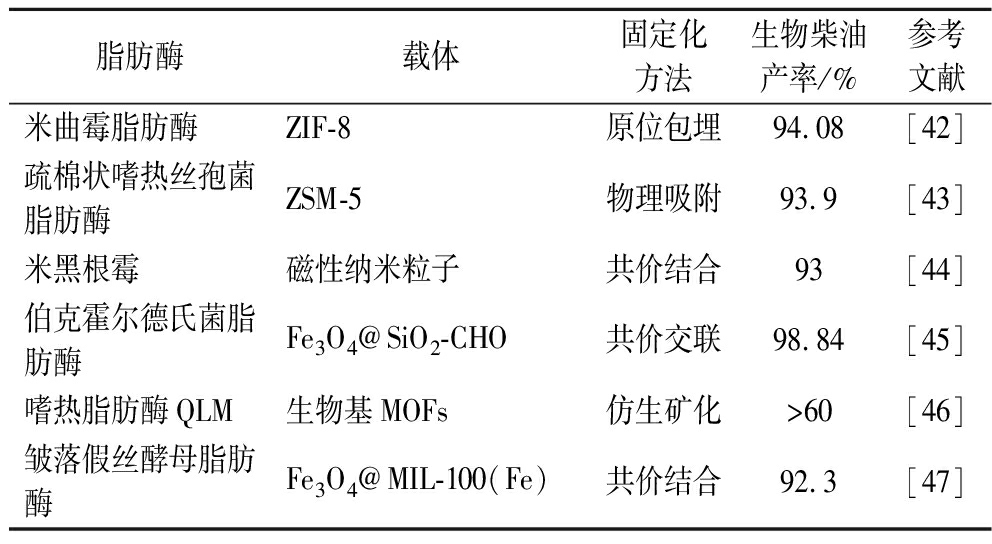
脂肪酶载体固定化方法生物柴油产率/%参考文献米曲霉脂肪酶ZIF-8原位包埋94.08[42]疏棉状嗜热丝孢菌脂肪酶ZSM-5物理吸附93.9[43]米黑根霉磁性纳米粒子共价结合93[44]伯克霍尔德氏菌脂肪酶Fe3O4@SiO2-CHO共价交联98.84[45]嗜热脂肪酶QLM生物基MOFs仿生矿化>60[46]皱落假丝酵母脂肪酶Fe3O4@MIL-100(Fe)共价结合92.3[47]
4.2 食品工业
固定化脂肪酶技术在食品工业中的应用涵盖多个关键领域,包括天然风味物质及香精的酶催化制备、油脂结构改性技术开发、废弃油脂的资源化转化处理,以及功能性食品添加剂的合成等。
芳香味酯类物质是短链脂肪酸与醇类化合物的酯化产物,这类化合物作为食品风味特征的核心成分,在食品加工领域应用广泛。通过固定化脂肪酶的酶促酯交换技术,可在温和条件下定向合成具有水果特征香气的短链酯类,例如丁酸甲酯(菠萝/苹果风味)、丁酸乙酯(菠萝/草莓风味),以及乙酸异戊酯/丁酸异戊酯(香蕉风味)等典型风味物质。相较于化学合成法,固定化酶催化反应具有产物天然安全的优势,且酶制剂可重复利用,能显著提升工业生产的可持续性。JI等[48]以肉桂醛-壳聚糖(cinnamaldehyde-chitosan, CA-CS)偶联物以对碳纳米管进行改性作为载体对猪胰脂肪酶(porcine pancreatic lipase, PPL)进行固定化(图5-a)。结果表明,肉桂醛-壳聚糖-碳纳米管-猪胰脂肪酶(CA-CS-CNTs-PPL)具有良好的热稳定性,重复使用7次后仍保持69%的酶活性。使用CA-CS-CNTs-PPL作为生物催化剂制备了具有浓郁芳香酒特征的己酸乙酯,最高产率为88%。有研 究发现,固定化脂肪酶能够有效提高肉桂酸苄酯、乙酸香叶酯等香精原料的转化率。为了提高脂肪酶在肉桂酸苄酯生物合成中的性能,CAO等[49]设计了一种包埋到纳米分子笼中的新型固定化脂肪酶(图5-b)。固定化的脂肪酶比游离脂肪酶具有更高的活性,将固定化的脂肪酶用于肉桂酸苄酯的生物合成,经过7个循环后,固定化脂肪酶催化肉桂酸苄酯的产率保持在70.2%。CHEN等[50]研究了使用自制固定化脂肪酶CSL@OMS-C8的超声波辅助生物合成肉桂酰乙酸酯。结果表明,超声波强化酶促反应促进了肉桂醇的96.6%转化率。CSL@OMS-C8的催化稳定性在10次重复使用后相对活性为60.1%。
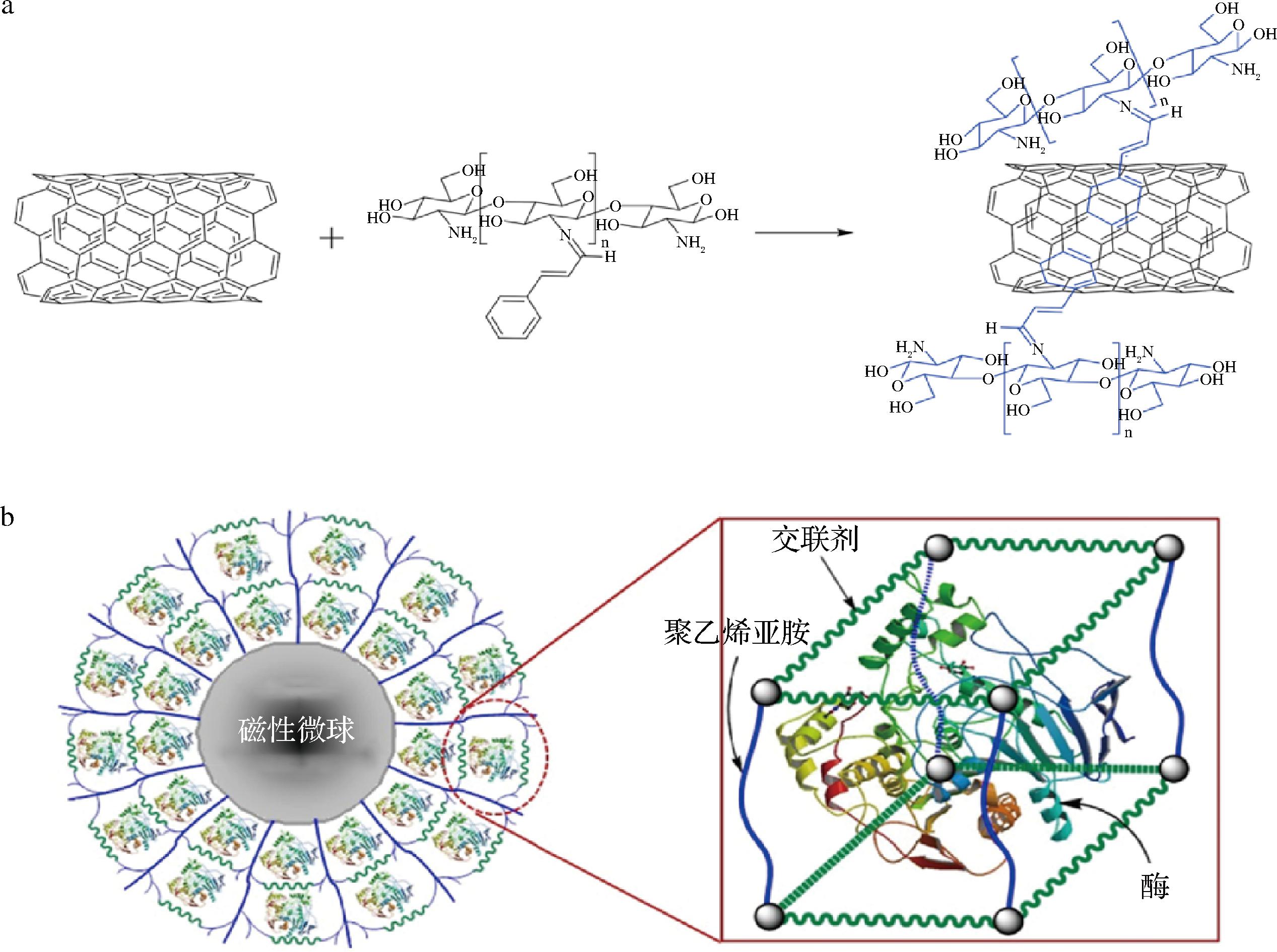
a-CA-CS功能化碳纳米管的合成机理;b-磁性微球表面分子笼包埋脂肪酶的示意图
图5 碳纳米管和纳米分子笼在脂肪酶固定的应用
Fig.5 The application of carbon nanotubes and nanoscale molecular cages in the immobilization of lipase
在油脂改性方面,为了解决酶合成中长链三酰基甘油反应时间长和适应范围有限的问题,LAI等[51]提出了一种广泛适用的无溶剂酶促酯交换策略。将念珠菌属脂肪酶(Candida lipase, CSL)固定在疏水性空心介孔二氧化硅球(hydrophobic hollow mesoporous silica spheres, HHSS)上,成功构建了CSL@HHSS固定化生物催化剂,实现了15.3%的固定率与94.0 mg/g的酶负载量,其比活性与表达活性分别比游离酶高5.6倍(173.62 U/g)与4.6倍(20.14 U/g)。该催化剂在20 min内实现多种植物油(如亚麻油、向日葵油、紫苏籽油、藻油、马来尼亚油)与中链三酰甘油的互酯化,产物中长链三酰基甘油收率达69.6%~78.0%。
随着废弃油脂(如地沟油、餐厨废油和过期植物油)的产生过剩,其高能量和低成本特性使其成为制备生物柴油和高值脂类产物的重要原料。然而,由于其杂质复杂、氧化程度高,传统化学催化剂在转化过程中易受抑制,且副产物多、操作条件苛刻。固定化脂肪酶因其高选择性、反应条件温和及良好的环境适应性,逐渐成为废弃油脂资源化的理想催化体系。杨建斌[52]研究了复合固定化脂肪酶在催化餐厨废弃油脂合成生物柴油中的应用效果,通过对不同脂肪酶组合的催化性能进行比较,系统优化了反应条件与酶剂搭配。结果显示,单独使用1,3位专一性根霉脂肪酶,反应18 h可实现70%的生物柴油转化率;而采用非专一性曲霉毛状脂肪酶,尽管反应延长至30 h,转化率仅为20%。为提高整体催化效率,研究进一步将两者进行复合固定化,构建出协同催化体系。在优化条件下,反应21 h内即可获得高达96.5%的生物柴油产率,显著优于单酶体系。同时,该复合固定化脂肪酶表现出良好的操作稳定性,连续催化10个批次(累计300 h)后,转化率仍保持在80%以上,表明其具有餐厨废弃油脂绿色转化的应用潜力与工业推广价值。许多功能性成分难以通过直接提取或化学方法生产,酶法合成需使用有害试剂,易引起了人们对食品安全和环境可持续性的担忧。
脂肪酶固定化技术在功能性食品成分的合成中展现出卓越的催化性能。DA S PEREIRA等[53]利用游离及CTS-海藻酸盐复合载体固定的曲霉毛状脂肪酶,催化合成具有功能食品潜力的β-谷甾醇油酸酯。研究比较了游离酶与固定化酶在催化效率、酯化率及操作稳定性方面的差异,结果表明,固定化脂肪酶在反应性能上表现出更高的催化活性和重复使用性,且在连续反应中能保持良好酶活力。
4.3 生物医药
固定化脂肪酶作为一种高效生物催化剂,凭借其优异的立体专一性和催化效能,可精准实现手性药物的不对称催化拆分,特别是在手性醇、手性胺及手性酯等关键化合物的催化制备中,因其优异的区域/立体选择性、高催化效率及绿色反应条件,广泛应用于医药、农药和精细化工等领域。相较于传统化学合成工艺,该技术具有显著优势,通过酶促反应路径的优化,可实现工艺路线简化;反应过程在温和条件下进行,有效抑制副产物生成;同时,其催化特异性保障了手性底物向目标对映体的定向转化,能够实现高纯度单一对映体的高效制备,同时确保产物收率。
在手性醇方面,SPELMEZAN等[54]将南极念珠菌的脂肪酶B(Candida antarctica lipase B, CALB)通过共价方式固定于CTS包覆的磁性纳米粒子,开发出一个高效动力学拆分体系,用于分离手性异芳基乙醇。该固定化体系在无溶剂条件下实现优异的对映选择性,3~16 h内转化率为49.2%~50%,对映体过量(enantiomeric excess,ee)>96%,在最佳条件下(乙酸乙烯酯、正己烷、45 ℃),生物催化剂在10次循环后仍保持活性。在手性胺方面,PINTOR等[55]报道了一个双酶连续流动反应器用于联合固定CALB与(R)-选择性ω-转氨酶,在乙酸乙酯有机介质中实现(R)-苯氧基丙-2-酰胺的级联合成,产物呈现高对映体纯度(>98% ee)和优良连续流稳定性。在手性酯方面,ZHANG等[56]开发了一种酶催化绿色合成技术,利用脂肪酶选择性聚合D-/L-天冬氨酸(Asp)二酯与二醇,制备具有螺旋手性结构和功能性聚酯。与D-Asp二酯相比,反应速度快的L-Asp二酯容易与二醇反应,从而提供一系列含有N-取代L-Asp重复单元的手性聚酯。
4.4 生物传感器
生物传感器由于其简单、快速、灵敏、专一且成本较低的特点,目前在传感器领域研究广泛。将脂肪酶固定在载体上,当传感器接触到含有特定氧化底物的样品时,脂肪酶会催化化学反应的发生,产生的信号可被传感器检测,进而实现对底物浓度等的快速、准确测定。
CHEN等[57]利用MOFs的可设计结构优势,以氧化亚铜(Cu2O)作为模板固定脂肪酶,显著提高了酶的负载能力,约为微孔Cu-BTC的1.89倍(图6-a)。与游离脂肪酶相比,空心分层(hollow hierarchical,HH)-Cu-BTC固定化皱褶假丝酵母脂肪酶(Candida rugosa lipase, CRL)(CRL@HH-Cu-BTC)表现出优异的耐pH性、热稳定性和可回收性。应用于二苯醚农药(硝基芬)的电化学生物传感器中,具有(0~78 μmol/L)的线性检测范围,1.15 μmol/L的检测限和良好的回收率,具有成本低、响应快、装置组装方便等优点。血液中高水平的甘油三酯会导致动脉硬化和阻塞,从而增加心脏病和中风的患病风险。甘油三酯是各种食物中使用的油脂的重要成分。为了特异性识别和灵敏检测甘油三酯,YANG等[58]提出了一种利用共价结合技术固定脂肪酶技术的强芯直径失配传感器(图6-b)。该传感器在3 min内显示出最佳响应,并在37 ℃,0~8 mg/mL表现出0.993 3 nm/(mg/mL)的高灵敏度和0.082 2 mg/mL的检测限,pH值为7.4。该生物传感器对甘油三酯具有高度特异性,并且基本不受其他物质的干扰。THAKKAR等[59]开发了一种脂肪酶固定的新型导电聚合物膜的电化学生物传感器,用于测量各种产品中的甘油三酯含量。结果表明,甘油三酯电极的线性范围为100~500 mg/dL。该传感器成功用于测定多个实际样品中的甘油三酯含量,平均回收率值为95.47%~101.05%。
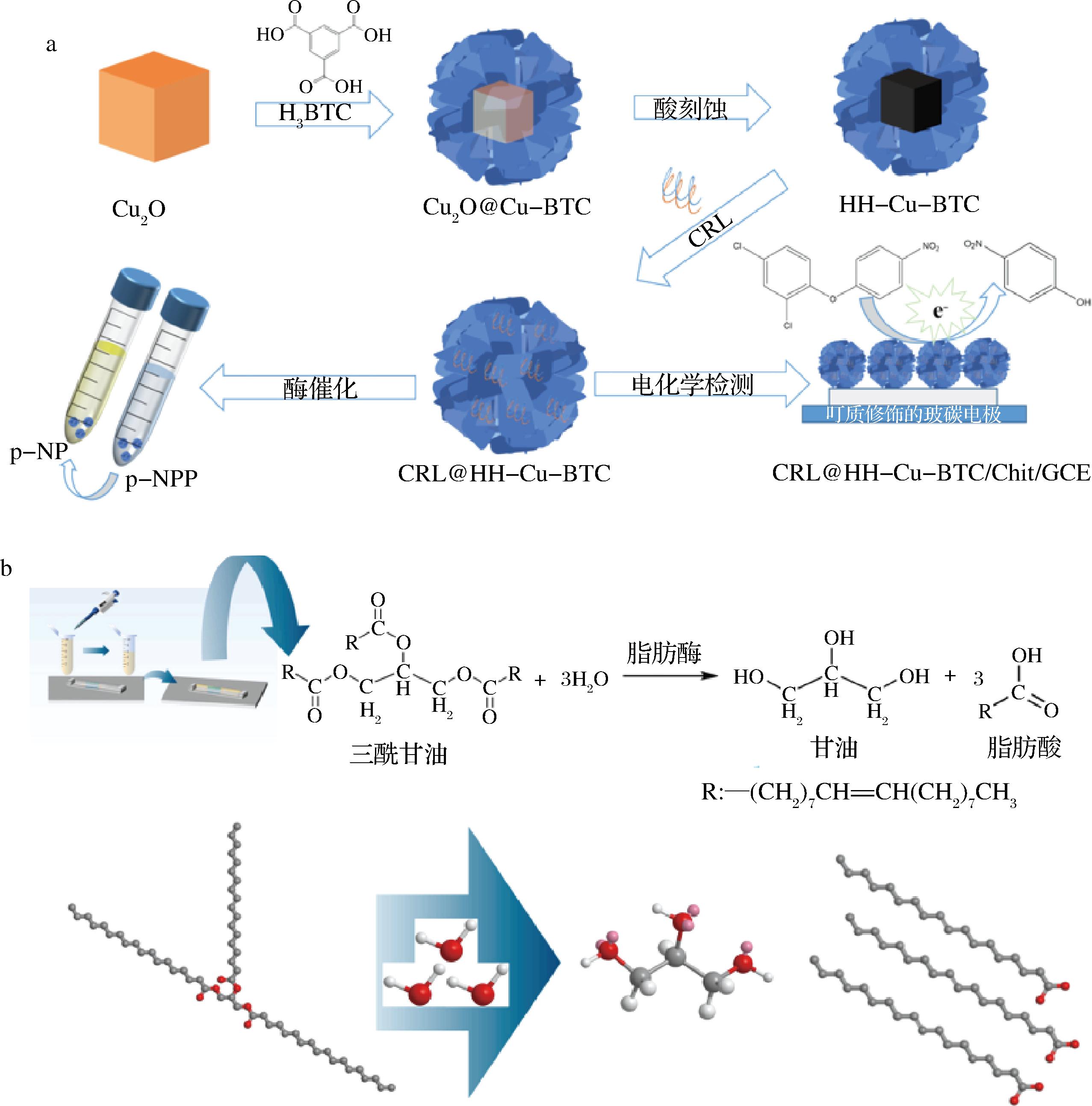
a-CRL@HH-Cu-BTC电化学生物传感器的合成示意图;b-固定脂肪酶用于检测甘油三酯原理
图6 脂肪酶固定在传感领域的应用
Fig.6 Application of immobilized lipase in the field of sensing
5 结语与展望
脂肪酶固定化技术通过载体与酶分子间的物理/化学作用,显著提升了酶的稳定性、重复利用性及环境耐受性,已成为推动酶工程产业化应用的核心策略。尽管固定化技术在酶工程领域已取得显著进展,但其应用仍受普适性不足与作用机理认知不清的双重瓶颈制约。首先,当前固定化策略的适配范围存在明显局限性。由于不同酶分子的活性位点构象、表面电荷分布及底物通道结构存在显著差异,而载体材料的孔径尺寸、官能团密度及表面亲疏水性亦千差万别,导致针对特定酶-载体组合的固定化工艺往往难以直接移植至其他体系。更根本的挑战在于,对固定化过程中酶-载体互作机制的解析仍停留在宏观层面。现有研究多聚焦于固定化后酶活性、稳定性等表观参数,而对载体界面如何诱导酶构象重排、活性中心微环境扰动、传质动力学演变等分子尺度机制缺乏系统性认知。未来应在以下方面开展深入研究:
1)载体材料创新:基于机器学习与高通量计算,建立载体的拓扑结构与酶构象稳定性的多尺度关联模型,开发具有动态自适应孔径的载体,以适配酶催化过程中的构象涨落。2)智能化设计:结合计算生物学与工智能技术,可构建“载体-酶-反应”三位一体的智能优化体系;利用AlphaFold2预测脂肪酶三维构象,通过分子动力学模拟解析载体界面与酶分子关键残基的相互作用位点,筛选最优固定化位点以避免活性中心屏蔽。3)多学科交叉研究:加强化学、生物学、材料科学等多学科的交叉合作,深入研究固定化脂肪酶的催化机制、构效关系等,为其性能优化和新应用开发提供理论支持。与纳米技术、光催化技术等联用,实现多功能系统融合,拓展其在生物传感、医学、环境修复、食品加工等领域的应用,开发具有特定功能的固定化脂肪酶产品。
[1] 林佳乐, 夏率博, 冯笑笑, 等.金属有机骨架固定化脂肪酶的构筑及其催化制备生物柴油的研究进展[J].中国油脂, 2023, 48(7):39-43.LIN J L, XIA S B, FENG X X, et al.Progress on immobilization of lipase on metal organic framework and its catalytic preparation of biodiesel[J].China Oils and Fats, 2023, 48(7):39-43.
[2] 张尧, 王佳欣, 温婵婵, 等.微生物源蛋白酶和脂肪酶分类、特性及在食品工业中的应用进展[J].食品工业科技, 2025, 46(3):415-424.ZHANG Y, WANG J X, WEN C C, et al.Progress on the classification, characteristics and food industry application of microbial proteases and lipases in food industry:A review[J].Science and Technology of Food Industry, 2025, 46(3):415-424.
[3] 张月华. 脂肪酶的固定化及在药物合成中的应用探究[J].工业微生物, 2023, 53(6):38-40.ZHANG Y H.Research on immobilization of lipase and its application in drug synthesis[J].Industrial Microbiology, 2023, 53(6):38-40.
[4] LANKAGE U M, HOLT S A, BRIDGE S, et al.Triglyceride-tethered membrane lipase sensor[J].ACS Applied Materials &Interfaces, 2023, 15(45):52237-52243.
[5] 柯彩霞, 范艳利, 苏枫, 等.酶的固定化技术最新研究进展[J].生物工程学报, 2018, 34(2):188-203.KE C X, FAN Y L, SU F, et al.Recent advances in enzyme immobilization[J].Chinese Journal of Biotechnology, 2018,34(2):188-203.
[6] YAO W T, LIU K Q, LIU H L, et al.A valuable product of microbial cell factories:Microbial lipase[J].Frontiers in Microbiology, 2021, 12:743377.
[7] SALGADO C A, DOS SANTOS C I A, VANETTI M C D.Microbial lipases:Propitious biocatalysts for the food industry[J].Food Bioscience, 2022, 45:101509.
[8] NAVVABI A, RAZZAGHI M, FERNANDES P, et al.Novel lipases discovery specifically from marine organisms for industrial production and practical applications[J].Process Biochemistry, 2018, 70:61-70.
[9] TOLDR -REIG F, MORA L, TOLDR
-REIG F, MORA L, TOLDR F.Developments in the use of lipase transesterification for biodiesel production from animal fat waste[J].Applied Sciences, 2020, 10(15):5085.
F.Developments in the use of lipase transesterification for biodiesel production from animal fat waste[J].Applied Sciences, 2020, 10(15):5085.
[10] LIM S Y, STEINER J M, CRIDGE H.Lipases:It’s not just pancreatic lipase![J].American Journal of Veterinary Research, 2022, 83(8):48.
[11] 陈莉莉, 张建国, 丛文杰, 等.脂肪酶固定化常用载体及方法的研究进展[J].工业微生物, 2024, 54(2):110-123.CHEN L L, ZHANG J G, CONG W J, et al.Research progress on common carriers and methods for lipase immobilization[J].Industrial Microbiology, 2024,54(2):110-123.
[12] QIN Z Q, FENG N, LI Y, et al.Hydrogen-bonded lipase-hydrogel microspheres for esterification application[J].Journal of Colloid and Interface Science, 2022, 606:1229-1238.
[13] 林海蛟, 张继福, 张云, 等.基于大孔吸附树脂先交联后吸附法固定化脂肪酶[J].广西师范大学学报(自然科学版), 2020, 38(4):100-108.LIN H J, ZHANG J F, ZHANG Y, et al.Immobilization of lipase by crosslinking and then adsorption method using macroporous adsorbent resin[J].Journal of Guangxi Normal University (Natural Science Edition), 2020, 38(4):100-108.
[14] TANG W, LI H X, ZHANG W, et al.Site-specific and covalent immobilization of lipase on natural polyphenol-modified magnetic nanoparticles for effective biodiesel production[J].ACS Sustainable Chemistry &Engineering, 2022, 10(17):5384-5395.
[15] 朱红莉, 王香亭, 张曼, 等.Co/Ni双金属-有机框架物及其衍生物在超级电容器中的研究进展[J].现代化工, 2024, 44(10):26-29;33.ZHU H L, WANG X T, ZHANG M, et al.Research progress on application of Co/Ni bimetallic-organic frameworks and their derivatives in supercapacitor[J].Modern Chemical Industry, 2024,44(10):26-29;33.
[16] 谷建霞, 王海璇, 贺敬婷, 等.金属有机框架复合材料在环境污染物电化学检测中的应用研究进展[J].分析化学, 2024, 52(8):1061-1071.GU J X, WANG H X, HE J T, et al.Advances of metal-organic framework composites in electrochemical detection of environmental pollutants[J].Chinese Journal of Analytical Chemistry,2024,52(8):1061-1071.
[17] 郑炜琼, 刘习奎, 李爽, 等.巯基配位的金属有机框架在高效电催化析氧中的应用[J].高分子材料科学与工程, 2024, 40(6):106-114.ZHENG W Q, LIU X K, LI S, et al.Metal-organic frameworks with sulfhydryl coordination for efficient electrocatalytic oxygen evolution reaction[J] Polymer Materials Science &Engineering, 2024,40(6):106-114.
[18] 宋瑞利, 范丽丹, 苗现华, 等.MOFs衍生的碳基电催化剂的研究进展[J].现代化工, 2024, 44(8):44-47;53.SONG R L, FAN L D, MIAO X H, et al.Progress in MOFs derived carbon-based electrocatalysts[J].Modern Chemical Industry, 2024,44(8):44-47;53.
[19] 都峙烨, 王德超, 汪静雯, 等.MOFs基多孔液体的合成及其气体吸附分离的应用[J].化工新型材料, 2024, 52(10):220-228.DU Z Y, WANG D C, WANG J W, et al.Advances in the synthesis of MOFs-based porous liquids and their application for gas adsorption and separation[J].New Chemical Materials, 2024,52(10):220-228.
[20] 王宇轩, 谢雯佳, 高会乐, 等.金属有机框架纳米药物载体胞吞途径的研究进展[J].药学学报, 2024, 59(5):1196-1209.WANG Y X, XIE W J, GAO H L, et al.Research progress on the endocytosis pathway of nanoscale metalorganic frameworks drug carriers[J] Acta Pharmaceutica Sinica,2024, 59(5):1196-1209.
[21] BIBI S, PERVAIZ E, ALI M.Synthesis and applications of metal oxide derivatives of ZIF-67:A mini-review[J].Chemical Papers, 2021, 75(6):2253-2275.
[22] ZHONG L, WANG Z J, YE X H, et al.Molecular simulations guide immobilization of lipase on nest-like ZIFs with regulatable hydrophilic/hydrophobic surface[J].Journal of Colloid and Interface Science, 2024, 667:199-211.
[23] 曹轩铭, 丛玉凤, 黄玮, 等.功能性金属有机骨架材料催化应用的研究进展[J].化工新型材料, 2022, 50(3):23-28;34.CAO X M, CONG Y F, HUANG W, et al.Research progress on catalytic application of functional MOFs[J].New Chemical Materials, 2022,50(3):23-28;34.
[24] RAMSAHYE N A, GAO J, JOBIC H, et al.Adsorption and diffusion of light hydrocarbons in UiO-66(Zr):A combination of experimental and modeling tools[J].The Journal of Physical Chemistry C, 2014, 118(47):27470-27482.
[25] ZHONG L J, JIANG B H, TANG K W.Efficient resolution of 4-chlormandelic acid enantiomers using lipase@UiO-67(Zr) zirconium-organic frameworks in organic solvent[J].Chirality, 2023, 35(5):323-333.
[26] GHASEMI S, YOUSEFI M, NIKSERESHT A, et al.Covalent binding and in situ immobilization of lipases on a flexible nanoporous material[J].Process Biochemistry, 2021, 102:92-101.
[27] 宋聪, 喻晓蔚, 钱丹, 等.KH560修饰的溶胶-凝胶法二氧化硅载体用于脂肪酶的固定化[J].无机材料学报, 2016, 31(3):311-316.SONG C, YU X W, QIAN D, et al.Immobilization of lipase on KH560 modified silica by Sol-gel process[J].Journal of Inorganic Materials,2016,31(3):311-316.
[28] WANG X, HE L H, HUANG J R, et al.Immobilization of lipases onto the halogen &haloalkanes modified SBA-15:Enzymatic activity and glycerolysis performance study[J].International Journal of Biological Macromolecules, 2021, 169:239-250.
[29] 罗艺献, 苏愉, 杨金花, 等.纳米二氧化硅固定化酶的研究进展[J].药物生物技术, 2022, 29(3):315-319.LUO Y X, SU Y, YANG J H, et al.Research progress of immobilized enzyme on nano-silica[J].Pharmaceutical Biotechnology, 2022,29(3):315-319.
[30] GHOLAMZADEH P, MOHAMMADI ZIARANI G, BADIEI A.Immobilization of lipases onto the SBA-15 mesoporous silica[J].Biocatalysis and Biotransformation, 2017, 35(3):131-150.
[31] HORCHANI H, AISSA I, OUERTANI S, et al.Staphylococcal lipases:Biotechnological applications[J].Journal of Molecular Catalysis B:Enzymatic, 2012, 76:125-132.
[32] ORREGO C E, SALGADO N, VALENCIA J S, et al.Novel chitosan membranes as support for lipases immobilization:Characterization aspects[J].Carbohydrate Polymers, 2010, 79(1):9-16.
[33] DOS SANTOS L A, ALNOCH R C, SOARES G A, et al.Immobilization of Pseudomonas fluorescens lipase on chitosan crosslinked with polyaldehyde starch for kinetic resolution of sec-alcohols[J].Process Biochemistry, 2022, 122:238-247.
[34] GUO H, LEI B S, YU J W, et al.Immobilization of lipase by dialdehyde cellulose crosslinked magnetic nanoparticles[J].International Journal of Biological Macromolecules, 2021, 185:287-296.
[35] JASI SKA K, ZIENIUK B, JANKIEWICZ U, et al.Bio-based materials versus synthetic polymers as a support in lipase immobilization:Impact on versatile enzyme activity[J].Catalysts, 2023, 13(2):395.
SKA K, ZIENIUK B, JANKIEWICZ U, et al.Bio-based materials versus synthetic polymers as a support in lipase immobilization:Impact on versatile enzyme activity[J].Catalysts, 2023, 13(2):395.
[36] 王宁. 聚合物改性的纳米载体固定化脂肪酶的研究[D].芜湖:安徽工程大学, 2018.WANG, N.Research on preparation of nanocale modified by polymer and its application for enzyme immobilization[D].Wuhu:Anhui Polytechnic University, 2018.
[37] 周亚梅, 刘佳, 陆丹, 等.脂肪酶的固定化及其在药物合成中的应用进展[J].生物技术进展, 2023, 13(2):220-227.ZHOU Y M, LIU J, LU D, et al.Progress on lipase immobilization and its application in pharmaceutical synthesis[J].Current Biotechnology, 2023,13(2):220-227.
[38] 段洪东, 刘文涛, 孟霞, 等.三组分大孔树脂的合成及其在脂肪酶固定中的应用[J].山东科技大学学报(自然科学版), 2012, 31(3):90-4.DUAN H D, LIU W T, MENG X, et al.Synthesis of three-component macroporous resins and their application in lipase immobilization.Journal of Shandong University of Science and Technology (Natural Science), 2012,31(3):90-94.
[39] 刘文涛. 环氧基大孔树脂的合成及其应用性能研究[D].济南:山东轻工业学院, 2012.LIU W T.Synthesis of porous resins with epoxy groups and study on its application[D].Jinan:Shandong Polytechnic University, 2012.
[40] RAHIM M, ZOU Z Q, DU Z Y, et al.Lipase immobilization over hierarchically carbonized macro-MIL-88A for biodiesel production[J].ACS Applied Nano Materials, 2024, 7(16):19163-19174.
[41] JIANG L, TONG X L, AO Q, et al.Mobilization of lipase and metal in microgel for biodiesel production and ring-opening polymerization[J].Surfaces and Interfaces, 2024, 44:103783.
[42] 吕珍珍, 邢世友, 王超, 等.ZIF-8固定化米曲霉脂肪酶并催化制备生物柴油[J].新能源进展, 2024, 12(6):656-63.LYU Z Z, XING S Y, WANG C, et al.Immobilization of lipase from Aspergillus oryzae on ZIF-8 and catalytic preparation of biodiesel[J].Advances in New and Renewable Energy, 2024, 12(6):656-663.
[43] 季骁彦, 许蕊, 王飞, 李迅.VKT多肽介导的固定化疏棉状嗜热丝孢菌脂肪酶催化制备生物柴油[J].化工进展, 2024, 43(6):3285-3292.JI X Y, XU R, WANG F, et al.Direct immobilization of Thermomyces lanuginosus lipase mediated by VKT-peptide for efficient biodiesel production from Jatropha curcas oil[J].Chemical Industry and Engineering Progress, 2024, 43(6):3285-3292.
[44] ZHANG W W, YANG H X, LIU W Y, et al.Improved performance of magnetic cross-linked lipase aggregates by interfacial activation:A robust and magnetically recyclable biocatalyst for transesterification of Jatropha oil[J].Molecules, 2017, 22(12):2157.
[45] 马晓瑞, 秦家亮, 吴海珍, 等.Fe3O4@SiO2-CHO共价固定脂肪酶条件的响应面优化及固定化酶催化生产生物柴油[J].应用与环境生物学报, 2017, 23(2):256-263.MA X R, QIN J L, WU H Z, et al.Preparation of a Fe3O4@SiO2-CHO carrier and immobilized lipase as a recyclable catalyst for biodiesel production[J].Chinese Journal of Applied and Environmental Biology, 2017, 23(2):256-263.
[46] LI Q, CHEN Y X, BAI S W, et al.Immobilized lipase in bio-based metal-organic frameworks constructed by biomimetic mineralization:A sustainable biocatalyst for biodiesel synthesis[J].Colloids and Surfaces B:Biointerfaces, 2020, 188:110812.
[47] XIE W L, HUANG M Y.Enzymatic production of biodiesel using immobilized lipase on core-shell structured Fe3O4@MIL-100(Fe) composites[J].Catalysts, 2019, 9(10):850.
[48] JI S P, LIU W, SU S Y, et al.Chitosan derivative functionalized carbon nanotubes as carriers for enzyme immobilization to improve synthetic efficiency of ethyl caproate[J].LWT, 2021, 149:111897.
[49] CAO Y P, ZHI G Y, HAN L, et al.Biosynthesis of benzyl cinnamate using an efficient immobilized lipase entrapped in nano-molecular cages[J].Food Chemistry, 2021, 364:130428.
[50] CHEN J H, LIU T L, ZHANG Y, et al.Ultrasound-assisted enzymatic synthesis of cinnamyl acetate by immobilized lipase on ordered mesoporous silicon with CFD simulation and molecular docking analysis[J].Food Chemistry, 2025, 464:141843.
[51] LAI Y D, LI D M, LIU T L, et al.Preparation of functional oils rich in diverse medium and long-chain triacylglycerols based on a broadly applicable solvent-free enzymatic strategy[J].Food Research International, 2023, 164:112338.
[52] 杨建斌. 复合固定化脂肪酶催化餐厨废弃油脂合成生物柴油[J].精细与专用化学品, 2020, 28(2):5-9.YANG J B.Synthesis of biodiesel from waste cooking oil using a compound of immobilized lipases[J].Fine and Specialty Chemicals, 2020, 28(2):5-9.
[53] DA S PEREIRA A, FRAGA J L, SOUZA C P L, et al.β-sitosterol oleate synthesis by Candida rugosa lipase in a solvent-free mini reactor system:Free and immobilized on chitosan-alginate beads[J].Catalysts, 2023, 13(4):780.
[54] SPELMEZAN C G, BENCZE L C, KATONA G, et al.Efficient and stable magnetic chitosan-lipase B from Candida antarctica bioconjugates in the enzymatic kinetic resolution of racemic heteroarylethanols[J].Molecules, 2020, 25(2):350.
[55] PINTOR A, MATTEY A P, LAVANDERA I, et al.Development of an amine transaminase-lipase cascade for chiral amide synthesis under flow conditions[J].Green Chemistry, 2023, 25(15):6041-6050.
[56] ZHANG Y, XIA B, LI Y Y, et al.Substrate engineering in lipase-catalyzed selective polymerization of D-/L-aspartates and diols to prepare helical chiral polyester[J].Biomacromolecules, 2021, 22(2):918-926.
[57] CHEN Y X, YUAN G S, TAN L C, et al.Hollow hierarchical Cu-BTC as nanocarriers to immobilize lipase for electrochemical biosensor[J].Journal of Inorganic and Organometallic Polymers and Materials, 2022, 32(11):4401-4411.
[58] YANG W L, TAN Z Z, YU S, et al.A highly sensitive optical fiber sensor enables rapid triglycerides-specific detection and measurement at different temperatures using convolutional neural networks[J].International Journal of Biological Macromolecules, 2024, 256:128353.
[59] THAKKAR J B, AGHERA D J, TRIVEDI B, et al.Design and characterization of a biosensor with lipase immobilized nanoparticles in polymer film for the detection of triglycerides[J].International Journal of Biological Macromolecules, 2023, 229:136-145.