透明质酸又称为玻尿酸或玻璃酸,是一种天然线性多糖,广泛分布于人体皮肤、关节、眼玻璃体等组织中。作为重要的天然保湿因子,透明质酸对维持皮肤的水分和弹性起着至关重要的作用。随着年龄的增长,人体内的透明质酸合成逐渐减少,导致皮肤水分流失加剧,进而引发干燥、细纹、皱纹等一系列皮肤老化问题。近年来,透明质酸在医药、化妆品等领域的应用研究取得了显著进展,不仅为抗衰老、保湿提供了有效手段,还在创伤愈合等方面展现出巨大潜力。本文旨在系统总结透明质酸与皮肤健康关系的研究进展,包括透明质酸的生物功能、作用功效以及应用现状,为进一步探索透明质酸在皮肤健康领域的应用提供理论支持。
1 透明质酸的基本性质
1.1 透明质酸的化学结构
1934年,美国哥伦比亚大学的Karl Meyer和John W.Palmer从牛眼晶状体中首先发现并分离了透明质酸[1]。透明质酸是由N-乙酰-D-葡萄糖胺及D-葡萄糖醛酸构成的双糖单位重复连结形成的一种无支链的线性多聚体结构,每个重复单元由1个N-乙酰-D-葡萄糖胺和1个D-葡萄糖醛酸分子由β-1,3-配糖键相连,这些单元进一步通过β-1,4-配糖键连接,形成长链结构[2]。透明质酸属于糖胺聚糖,其分子质量可以从数千到数百万Da不等[3]。透明质酸的部分子链上单糖与单糖间存在氢键,使其在空间结构上呈一种刚性柱形螺旋结构,柱形内侧存在大量的羟基,水分子可以通过极性键和氢键与透明质酸分子结合,使透明质酸能够吸收和保持大量水分子[4]。不同分子质量的透明质酸保水性不同,就其在皮肤中的保湿作用而言,一般情况下寡聚透明质酸钠的分子质量较小,能够透过皮肤到达皮肤深层,增加皮肤内部的水分含量;高分子质量的透明质酸在皮肤表层形成一层透明的水化膜,具有防止内部水分流失的作用[5]。
1.2 透明质酸的来源和分布
天然来源的透明质酸分布广泛,从原核细胞到真核生物均有存在。在人体中,透明质酸含量最丰富的部位是皮肤。研究表明,大鼠皮肤中透明质酸的含量几乎是全身透明质酸总量的50%,人皮肤中透明质酸的总量约为5 g[6]。除皮肤外,眼睛的玻璃体、脐带和滑膜液中也含有丰富的透明质酸。其他组织和器官,如骨骼组织、心脏瓣膜、肺、主动脉、前列腺等,具有少量透明质酸[7]。在其他脊椎动物和微生物中,透明质酸也广泛存在,其中雄鸡冠是迄今为止已知透明质酸含量最高的动物组织。
1.3 透明质酸的安全性
透明质酸被认为是一种安全的食品原料。通过小鼠、大鼠、家兔等多种实验动物模型及人体临床试验的综合评估,结果显示透明质酸具有较高的安全性[8-9]。具体而言,在一项双盲对照人体试验中,分别观察了连续12个月每日摄入200 mg透明质酸和连续8周每日摄入240 mg透明质酸的受试者情况,结果均证实无任何不良反应或副作用的发生[10-11]。动物急性毒性试验显示,小鼠、大鼠和兔口服透明质酸的半数致死量分别高达2 400、800、1 000 mg/kg[12-13],远高于平均日常摄入水平。此外,一项为期28 d的口服透明质酸毒性试验进一步揭示,大鼠口服梯度浓度的透明质酸后[0、34、235、3 536 mg/(kg BW·d)],无死亡率,大鼠体重、进食量、食物利用率、主要脏器质量及组织病理学指标等与对照组相比均未发生显著变化[14]。90 d的亚慢性毒性试验表明,透明质酸钠的无观察不良效应水平(no observed adverse effect level,NOAEL)超过48 mg/(kg·d)[15]。同时,在被动皮肤过敏反应系统的抗原性试验中,透明质酸钠均为阴性[16],表明透明质酸非过敏原。
2 透明质酸的合成和降解
2.1 透明质酸合成
透明质酸的合成路径在生物体内显得尤为独特,它并不遵循其他糖胺聚糖在高尔基体内合成并通过胞吐作用分泌到细胞外的常规模式。相反,透明质酸是在质膜内侧,由一类特定的酶——透明质酸合成酶(hyaluronan synthase,HAS)催化完成的[17]。这一过程中,在HAS作用下,葡萄糖胺残基和葡萄糖醛酸残基交替连结,逐渐产生聚合物链,随着聚合物链的延长构建出透明质酸产物。HAS家族由3种不同的同工酶组成:透明质酸合成酶1(hyaluronan synthase 1,HAS1)、透明质酸合成酶2(hyaluronan synthase 2,HAS2)和透明质酸合成酶3(hyaluronan synthase 3,HAS3),它们均属于跨膜酶类,这意味着它们能够跨越细胞膜,一端位于细胞内,另一端则暴露于细胞外环境[18]。这种结构特性使得它们能够直接在质膜内侧合成透明质酸,并通过其结构中的特定孔道将合成的透明质酸链转移到细胞外空间。
尽管这3种HAS在功能上相似,都能独立催化透明质酸的合成,但它们在活性和产物分子质量上却存在显著差异。其中HAS1活性最低,其合成的透明质酸分子质量相对较小,通常在2×105~2×106 Da。相比之下,HAS3则展现出最高的活性,但其产物透明质酸的分子质量却相对较低,一般不超过3×105 Da。而HAS2的活性则介于HAS1和HAS3之间,其合成产物的分子质量一般大于2×106 Da[19]。这种分子质量上的差异对于透明质酸在生物体内的功能具有重要影响。不同分子质量的透明质酸在机体中扮演着不同的角色,参与调节细胞的增殖、迁移、分化以及组织修复等多种生理过程[20]。因此,HAS家族的不同成员通过调节透明质酸的合成速率和分子质量,为生物体提供了精细调控细胞外基质结构和功能的能力。
2.2 透明质酸降解
透明质酸在人体中的降解主要通过2种不同的机制进行:一种是特异性的,由透明质酸酶(hyaluronidase,HYAL)介导,而另一种是非特异性的,由活性氧(reactive oxygen,ROS)引起的氧化损伤决定[21]。
具体而言,透明质酸的降解首要依赖于HYAL这一特异性酶家族的介导作用,HYAL能够水解透明质酸结构中N-乙酰-D-氨基葡萄糖和D-葡糖醛酸残基之间的β(1→4)糖苷键连接,促使透明质酸裂解为不同长度的片段。截至目前,在人类基因组中已经发现了6种HYAL亚型,分别为HYAL-1、HYAL-2、HYAL-3、HYAL-4、PH-20和HYALP1[22]。其中,HYAL-1和HYAL-2在多种组织中广泛表达,协同降解透明质酸长链。在细胞表面,HYAL-2与透明质酸结合并将其内化到囊泡中,透明质酸分子被切割成20 kDa的片段并递送至溶酶体,HYAL-1进一步将其消化成低聚糖。此外,PH-20主要存在于精子中,是活性最强的哺乳动物HYAL。相比之下,HYAL-3、HYAL-4和HYALP1的活性仍然知之甚少,尚待深入探索。
另一方面,透明质酸还受到非特异性机制调控,这一过程主要由ROS介导。ROS是氧代谢过程中产生的一类高度活跃的化学物质,包括超氧化物、H2O2、NO、过氧亚硝酸盐和次盐酸等分子,这些物质在紫外线照射、炎症反应、组织损伤和肿瘤发生过程中大量产生。这些ROS分子通过攻击透明质酸的糖胺聚糖骨架,诱发糖苷键的断裂,进而导致透明质酸分子质量的急剧减少,甚至彻底降解为低分子碎片[23]。此降解路径反映了生物体在应对外界刺激时复杂的代谢调控机制。ROS也能够通过p38MAPK通路刺激HYAL-2基因表达[24]。综上所述,透明质酸在人体内的降解是一个高度协调且动态变化的过程,既依赖于HYAL的特异性酶解作用,也受到ROS介导的非特异性氧化损伤的调控,这种降解机制确保了透明质酸在维持组织稳态、促进细胞间通讯及参与多种生理病理过程中的灵活性与高效性。
3 透明质酸的微生物发酵工艺制备
传统上,透明质酸是从动物组织中提取的,如雄鸡冠等。但这种方法面临多重挑战:透明质酸与蛋白聚糖在动物组织中的紧密络合导致提取效率低下,工艺流程复杂,生产成本高;同时,动物源性透明质酸存在伦理相关问题[25]。鉴于此,微生物发酵法逐渐取代传统动物组织提取法,成为透明质酸制备的主流技术。
微生物发酵法的发展历程可追溯到二十世纪三十年代,其里程碑式的发现源自KENDALL等[26]在1937年的研究,他们揭示了溶血性链球菌(Streptococcus haemolyticus)具有合成与代谢以透明质酸为主要成分的荚膜的能力,这一发现为微生物发酵产生透明质酸奠定了理论基础。随后,1983年日本资生堂公司首次提出了利用链球菌发酵生产透明质酸的方法,之后英美等国家也相继开展以微生物发酵生产透明质酸的研究[27]。微生物发酵法相较于传统提取法产量有不受动物原料资源限制、成本较低、易于大规模生产等优点,已成为工业化生产透明质酸的主要方式[28]。
产生透明质酸的菌株主要是链球菌属的A群菌和C群菌。尽管A群中的酿脓链球菌(Streptococcus pyogenes)具备优良的透明质酸合成能力,但其较强的致病性限制了其在工业上的应用;相比之下,C群链球菌,特别是兽疫链球菌(Streptococcus zooepidemicus)与马链球菌(Streptococcus equi),因其较弱的致病性成为生产透明质酸的优选菌株[29]。但两者均为β-溶血性链球菌,为了克服链球菌溶血素毒素可能带来的安全风险,一般都要通过诱变处理来获得工业用透明质酸产生菌株[30]。经过诱变选育的菌株,在合适的温度、营养条件、pH值等生产条件下,进行一定时间的发酵后,经一系列下游提取工艺,能够较简便的获得高纯度透明质酸。
随着分子生物学的快速发展,基因工程技术为透明质酸的生产开辟了新路径。研究者们利用基因工程技术构建安全的重组菌株来生产透明质酸,旨在通过异源表达透明质酸来降低致病风险并提升生产效率。其中枯草芽孢杆菌(Bacillus subtilis)和大肠杆菌(Escherichia coli)作为异源表达透明质酸的主要宿主,分别具有不同的优势:B. subtilis作为非致病性革兰氏阳性菌,主要产生分子质量较低的透明质酸;而E. coli,尽管其透明质酸产量相对较低,但作为一种经过充分研究的革兰氏阴性菌,拥有丰富的遗传工具库,便于基因操作与优化。此外,毕赤酵母(Pichia pastoris)作为透明质酸生产的新兴微生物,能够产生高产低分子质量透明质酸,生产效益高,并且易于扩大规模,使其成为大规模生产的有前途的候选者[31]。综上所述,微生物发酵法凭借其多方面的优势,不仅克服了传统动物源提取法的局限,还通过持续的技术创新与优化,不断推动透明质酸生产向更高效、更安全、更环保的方向发展。
4 透明质酸和皮肤健康的关系
4.1 透明质酸在皮肤衰老中的作用
4.1.1 透明质酸抗皮肤自然衰老
世界卫生组织预测,到2050年全球60岁及以上人口数量将激增至21亿,随之而来的是皮肤老化正在成为一个日益凸显的全球健康挑战。皮肤衰老是一个不可避免的自然生理过程,其表现形式包括皮肤松弛、皱纹加深、弹性下降等。这一生理过程的内在机制不仅涉及真皮层成纤维细胞数量的减少,还伴随着细胞内胞质明显减少,形态塌陷。同时细胞外基质的关键成分——透明质酸、胶原蛋白及弹力蛋白等的合成减少,基质金属蛋白酶(matrix metalloproteinase,MMP)表达增加,进一步加剧了皮肤老化的程度[32]。研究表明,外源补充透明质酸具有改善皮肤衰老的效果。一项包括40名具有轻度至中度皮肤老化临床症状的女性的随机对照试验显示,连续30 d外用透明质酸后,相比安慰剂组,受试者的皮肤皱纹数量和皱纹深度显著减少[33]。进一步地,PAVICIC等[34]探究了不同分子质量(50、130、300、800、2 000 kDa)的透明质酸抗眼周皮肤衰老的效果,为期60 d的局部涂抹试验结果表明,50、130 kDa透明质酸能够显著减少眼周皮肤皱纹,改善皮肤水合作用和增强皮肤弹性。此外,周成霞等[35]的研究纳入了106名具有明显皮肤老化临床表现的志愿者,采用面部外用5 g/L透明质酸联合0.5 g/L视黄醛,经过90 d持续治疗,受试者的皮肤老化症状显著改善,包括改善皮肤干燥、皱纹、皮肤弹性等。此外,KAYA等[36]的研究证实,局部涂抹透明质酸30 d能够改善皮肤萎缩症状,增加真皮层的胶原蛋白、弹性纤维和血管含量。
4.1.2 透明质酸抗皮肤光老化
皮肤光老化是由长期暴露在紫外线下引起的,主要表现为皮肤粗糙、干燥、松弛,皮肤皱纹加深等,研究表明,超过80%的面部皮肤老化是由暴露于紫外线引起的[37-38]。皮肤光老化主要由长波紫外线(ultraviolet A,UVA)和短波紫外线(ultraviolet B,UVB)引起:UVA可以到达真皮的深层,能够激发细胞内自由基的生成,促进脂质过氧化反应,进而破坏真皮层中至关重要的胶原纤维与弹性纤维结构。尽管UVA不直接损伤DNA,但它诱导产生的ROS却可间接引发DNA的氧化性损伤。相比之下,UVB主要导致表皮和浅层真皮的病变,并可能被细胞中的蛋白质和DNA吸收,造成细胞损伤和突变。紫外线辐射的另一重要影响在于促进皮肤内源性透明质酸的降解,这一过程通过上调多种HYALs的表达实现,导致透明质酸分子链的断裂与降解加速[39]。
补充外源性透明质酸已被证明可改善皮肤光老化。一项细胞试验结果表明,970 kDa透明质酸能够抑制UVB暴露诱导的HaCaT细胞活力下降,并降低IL-6、IL-8等促炎细胞因子水平[40]。膳食补充透明质酸也是改善皮肤光老化的有效途径。研究表明,给予UVB诱导的小鼠皮肤光老化模型14周透明质酸后,能够显著改善皮肤皱纹水平,增加胶原蛋白表达,降低MMP-1、IL-6的表达[41]。KAWADA等[42]利用慢性UVB诱导的小鼠皮肤光老化模型,小鼠每日口服200 mg/kg两种分子质量大小的透明质酸(300 kDa 和<10 kDa),6周后发现小鼠皮肤水分含量显著增加,表皮厚度显著减少。同时,相比于300 kDa透明质酸,较低分子质量的透明质酸(<10 kDa)不仅具有更优的效果,而且能够增加皮肤中Has2基因表达量,促进内源性透明质酸合成。膳食摄入外源性透明质酸改善皮肤光老化的潜在机制可能涉及3个方面:1)口服透明质酸可能穿过肠道屏障,转移至皮肤发挥作用。研究表明,通过使用放射性同位素标记法,发现透明质酸(5~1 000 kDa)口服后会被吸收并转移到大鼠和犬的皮肤上[43-44]。2)摄入的透明质酸有助于内源性透明质酸产生[42]。3)外源性透明质酸可通过影响肠道菌群,间接调节炎症等过程进而改善皮肤光老化[45]。
4.2 透明质酸促进皮肤保湿
皮肤的水合状态是维持皮肤健康、弹性和光泽的关键因素,也是维持皮肤屏障的重要指标。透明质酸独特的化学结构,使其能够结合1 000倍其体积的水分子,形成强大的水合网络,显著提高皮肤的水合能力[46]。透明质酸的渗透性主要与其分子质量紧密相关:高分子质量透明质酸,受限于其体积,主要停留在皮肤表面,形成一层保护性水合作用层,从而减少水分流失,增强皮肤屏障功能;低分子质量透明质酸可以渗透到表皮层和更深的真皮层,增加水分含量,并起到调节水平衡、渗透压和离子流动的作用[47]。随着年龄增长,皮肤内源性透明质酸含量逐渐减少,导致皮肤水合作用减弱,出现干燥、细纹等老化现象。因此,通过外源性途径补充透明质酸,成为改善皮肤状态、对抗老化的有效策略。多项研究有力支持了这一观点:OE等[48]研究表明,透明质酸在提升皮肤水分含量方面的良好效果,持续8周每日摄入120 mg透明质酸能够显著降低皱纹体积比。TOSHIHIDE[49]对39名年龄在37~59岁的日本女性受试者进行了透明质酸口服补充试验,每日接受120 mg透明质酸,6周试验结束后发现受试者面部皮肤含水量显著增加。HSU等[50]设计了一项随机、双盲、安慰剂对照试验,深入探讨了透明质酸对亚洲人群皮肤健康的影响。该试验对40名年龄在35~64岁的健康个体(男∶女=11∶29)进行为期12周每日120 mg透明质酸的口服补充,结果显示,与安慰剂组相比,补充透明质酸的受试者皮肤皱纹、角质层含水量、经表皮水分流失和皮肤弹性均有明显改善。
4.3 透明质酸促进皮肤创面愈合
皮肤创面愈合是一个高度精细且多阶段协同的生物过程,分为止血期、炎症期、增殖期和重塑期4个阶段,涉及各种细胞功能,如细胞迁移、增殖、基底膜再生和肉芽组织的形成。伤口本身是一个过渡性器官或结构,其功能是逐步重塑一系列日益复杂和有序的细胞外基质。在众多促进伤口愈合的生物活性物质中,透明质酸因其在皮肤及黏膜组织中浓度较高,被认为在皮肤或黏膜伤口愈合中具有重要的生物学作用[8]。伤口愈合需要足够的营养和新陈代谢帮助组织进行修复和重建,而新血管形成则是营养运输的前提和基础。许多研究表明透明质酸能够刺激血管内皮生长因子(vascular endothelial growth factor,VEGF)分泌,促进血管新生,从而加速伤口愈合。具体而言,近年来的研究成果进一步证实了透明质酸在伤口愈合领域的应用潜力,ZHOU等[51]发现硫化铜纳米颗粒结合透明质酸(copper sulfide nanoparticles/hyaluronic acid,CuS/HA)水凝胶在大鼠伤口愈合的早期阶段,能够显著上调VEGF和内皮细胞标志物CD31的表达水平,这一发现说明CuS/HA在促进伤口愈合阶段中血管生成的重要作用。此外,除VEGF之外,碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF)同样在血管生成过程中发挥重要作用。有研究表明,在大鼠烧伤创面模型中,透明质酸联合脂肪干细胞能够显著增强bFGF表达,从而加速烧伤创面的愈合过程[52]。
4.4 透明质酸与特应性皮炎(atopic dermatitis,AD)
AD是一种慢性炎症性皮肤病,其特征是皮肤干燥、剧烈瘙痒、皮疹和炎症反应。AD的发病机制复杂,涉及遗传、环境、免疫等多种因素,至今尚无根治AD的有效手段[53]。目前,临床上针对AD的治疗策略主要依赖于局部外用皮质类固醇药物,如糖皮质激素类药物,以其缓解患者症状。然而,长期使用皮质类固醇会产生不良反应,如表皮变薄、萎缩、溃疡和面部红斑等[54]。
一项双盲、随机研究招募了20名患有轻度至中度AD的女性受试者,通过连续4周涂抹含透明质酸的乳液,结果显示,补充透明质酸受试者的AD临床体征和症状显著改善,包括减缓皮肤红斑、脱屑、瘙痒、刺痛等[55]。不同分子质量的透明质酸在改善皮肤AD症状方面均显示出积极效果,但具体机制不完全相同。在一项基于2,4-二硝基氟苯诱导的小鼠皮肤AD模型中,通过连续20 d在小鼠背部皮肤涂抹0.5%浓度、不同分子质量的透明质酸(2 310~2×106 Da),研究人员观察到小鼠皮炎评分显著下降、表皮厚度降低及炎症细胞浸润程度显著降低[56]。进一步的研究揭示了透明质酸分子质量与其免疫调节功能之间的微妙关系:较低分子质量透明质酸主要调控Th1免疫应答,而高分子质量透明质酸则主要调节Th2免疫应答[56]。这一发现不仅为透明质酸在AD治疗中的应用提供了新的理论依据,也为未来开发基于透明质酸的个性化治疗方案开辟了道路。
4.5 透明质酸与皮肤玫瑰痤疮
玫瑰痤疮是一种主要累及面中部血管、神经和毛囊皮脂腺单位的顽固性、慢性、复发性、炎症性皮肤病。临床上呈现出多样化的临床表现。患者常面临阵发性潮红、持续性红斑、丘疹与脓疱的困扰,同时伴随毛细血管扩张等直观症状,以及灼热感、刺痛、皮肤干燥与脱屑、瘙痒等不适感,严重影响生活质量。
近年来,透明质酸作为一种生物相容性良好的天然多糖,在玫瑰痤疮的治疗中展现出独特优势。在皮内注射LL-37诱导皮肤玫瑰痤疮小鼠模型中,透明质酸低聚糖的应用可显著改善小鼠皮肤经皮失水率,减少发红面积和红斑指数,减少炎症细胞浸润,为透明质酸在玫瑰痤疮治疗中的应用提供了实验依据[57]。临床实践中,一项研究显示,2 g/L低分子质量透明质酸外用4周后,玫瑰痤疮患者的临床症状,包括皮肤丘疹、红斑、灼热、刺痛和干燥等,均得到显著改善[58]。进一步地,谢成树等[59]通过一项随机对照试验,深入探讨了透明质酸联合传统药物治疗玫瑰痤疮的效果。他们将72例丘疹脓疱型玫瑰痤疮患者均分为透明质酸组和对照组,透明质酸组在常规治疗(多西环素和夫西地酸乳膏)的基础上,每日额外涂抹2次透明质酸。结果显示,透明质酸联合夫西地酸乳膏的治疗方案能够更快速地改善患者的临床症状,减轻炎症反应,并有助于皮肤屏障的修复,为玫瑰痤疮的综合治疗提供了新的思路与策略。
5 透明质酸作为功能性食品的应用现状
由于其良好的保湿性和安全性,透明质酸首先被广泛添加于各种护肤产品中,如面霜、精华液、面膜等。透明质酸已成为现代护肤品中不可或缺的重要成分之一。近年来,随着研究的深入,透明质酸作为功能性食品的潜力逐渐凸显。通过口服途径摄入透明质酸,经过消化、吸收等过程,能够直接补充体内因自然衰老或环境因素导致的内源性透明质酸的流失,增加皮肤水分含量,减少皱纹的形成,使肌肤更加水润饱满、紧致有弹性。
我国在2008年批准透明质酸钠为新资源食品,主要用于保健食品领域。随着食品安全标准不断更新和完善,2021年1月,国家卫生健康委正式将透明质酸钠纳入新食品原料目录,其适用范围扩展至乳及乳制品、饮料、酒类、可可及巧克力制品以及糖果、冷冻饮品等多个领域,进一步推动了透明质酸在食品工业中的广泛应用。透明质酸在食品中的潜在应用在其他国家也受到相当大的关注[60]。日本自1992年起批准透明质酸作为膳食补充剂,用以缓解皮肤健康。随后,韩国批准透明质酸作为健康功能食品。美国、加拿大、意大利、比利时等国家也将透明质酸作为食品添加剂使用[13]。据英敏特全球新产品数据库统计显示,截至2020年,全球含透明质酸钠的食品共有1 000多个,其中美国有近600种膳食补充剂含有透明质酸,日本有160余种产品含有透明质酸,产品种类涵盖软糖、果冻、饮料、方便食品等多个品类。此外,透明质酸还被认为在维持肠道健康方面起着关键作用,多项研究显示口服透明质酸能够缓解葡聚糖硫酸钠盐诱导的小鼠结肠炎,起到维护肠道屏障和调节肠道菌群的有益作用[2],表明透明质酸可作为益生元产品发挥作用,为开发含有透明质酸的功能性食品提供见解和思路。
6 展望
本文主要对透明质酸在皮肤健康领域的多方面作用及其研究进展进行了系统性综述。当前研究表明,透明质酸在抵御皮肤衰老、促进皮肤保湿以及加速创面愈合等方面具有显著潜力,能够有效缓解并改善多种皮肤问题,甚至对部分炎症性皮肤疾病具有一定的辅助治疗作用。
近年来,透明质酸的应用领域不断拓展,已作为天然原料广泛应用于功能性食品、保健品及化妆品中。全球范围内,尤其是日本、韩国及北美地区,透明质酸产业蓬勃发展,各大企业竞相研发相关产品,推动了市场的繁荣与技术的进步。尽管透明质酸在皮肤健康中的作用已得到广泛研究和认可,但现有研究仍存在一些不足和缺点。首先,许多研究主要集中在透明质酸的保湿和抗衰老效果,而对其在皮肤屏障功能、创伤愈合及免疫调节等方面的研究相对较少。其次,透明质酸的作用机制尚未完全明确,不同分子质量的透明质酸在皮肤中的具体生理作用和代谢途径需要进一步探讨。今后研究应更加注重以下几个方面:首先,需进一步验证不同类型和分子质量的透明质酸在皮肤健康中的具体效果和安全性。其次,应加强对透明质酸作用机制的研究,特别是其在细胞和分子水平上的调控途径。最后,结合先进的生物技术,如基因编辑和生物打印,探索透明质酸在皮肤再生和组织工程中的新应用,从而为皮肤健康的维护和治疗提供更加全面和科学的依据。
[1] KOSI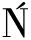 SKI J, JARECKI J, PRZEPIORKA-KOSI
SKI J, JARECKI J, PRZEPIORKA-KOSI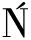 SKA J, et al.Hyaluronic acid in orthopedics[J].Wiadomosci Lekarskie, 2020, 73(9 cz.1):1878-1881.
SKA J, et al.Hyaluronic acid in orthopedics[J].Wiadomosci Lekarskie, 2020, 73(9 cz.1):1878-1881.
[2] ZHENG X L, WANG B T, TANG X, et al.Absorption, metabolism, and functions of hyaluronic acid and its therapeutic prospects in combination with microorganisms:A review[J].Carbohydrate Polymers, 2023, 299:120153.
[3] LI J M, QIAO M, JI Y, et al.Chemical, enzymatic and biological synthesis of hyaluronic acids[J].International Journal of Biological Macromolecules, 2020, 152:199-206.
[4] 蔡同凯, 刘谋治, 邓婕, 等.透明质酸的作用机制及临床应用研究进展[J].药学实践杂志, 2022, 40(2):103-107;131.CAI T K, LIU M Z, DENG J, et al.Research progress on action mechanism and clinical application of hyaluronic acid[J].Journal of Pharmaceutical Practice, 2022, 40(2):103-107;131.
[5] GHATGE A S, GHATGE S B.The effectiveness of injectable hyaluronic acid in the improvement of the facial skin quality:A systematic review[J].Clinical, Cosmetic and Investigational Dermatology, 2023, 16:891-899.
[6] 何祯平. 外源性透明质酸对皮肤创面愈合作用的研究[D].北京:中国协和医科大学, 2000.HE Z P.Studies on the effect of exogenous hyaluronate in skin wound healing[D].Beijing:Peking Union Medical College, 2000.
[7] KOBAYASHI T, CHANMEE T, ITANO N.Hyaluronan:Metabolism and function[J].Biomolecules, 2020, 10(11):1525.
[8] GUPTA R C, LALL R, SRIVASTAVA A, et al.Hyaluronic acid:Molecular mechanisms and therapeutic trajectory[J].Frontiers in Veterinary Science, 2019, 6:192.
[9] OE M, TASHIRO T, YOSHIDA H, et al.Oral hyaluronan relieves knee pain:A review[J].Nutrition Journal, 2016, 15:11.
[10] SATO T, IWASO H.An effectiveness study of hyaluronic acid [Hyabest®(J)] in the treatment of osteoarthritis of the knee on the patients in the United States[J].Journal of New Remedies and Clinics, 2009, 58(3):249-256.
[11] TASHIRO T, SEINO S, SATO T, et al.Oral administration of polymer hyaluronic acid alleviates symptoms of knee osteoarthritis:A double-blind, placebo-controlled study over a 12-month period[J].The Scientific World Journal, 2012, 2012(1):167928.
[12] NAGANO K, GOTO S, ABE Y, et al.Acute toxicity test of sodium hyaluronate[J].Pharmacology &Therapeutics, 1984, 12:37-45.
[13] 王钊, 徐康, 王方, 等.经口给予透明质酸的生理功能及其作用机制研究进展[J].食品科学, 2021, 42(23):1-10.WANG Z, XU K, WANG F, et al.Progress in research on physiological function and mechanism of oral hyaluronic acid[J].Food Science, 2021, 42(23):1-10.
[14] OE M, YOSHIDA T, KANEMITSU T, et al.Repeated 28-day oral toxicological study of hyaluronic acid in rats[J].Pharmacometrics, 2011, 81(1):11.
[15] ISHIHARA M, INOUYE T, ISHIYAMA Y, et al.Toxicity study on sodium hyaluronate (Na-HA) in rats by repeated oral administration for 90 days followed by a 28-day recovery study[J].Pharmacometrics, 1996, 51(2):97-113.
[16] TAKEMOTO M, OHZONE Y, ASAHI K.Antigenicity test of sodium hyaluronate (SH)[J].Yakuri to Chiry, 1992, 20(3):761-766.
[17] CAON I, PARNIGONI A, VIOLA M, et al.Cell energy metabolism and hyaluronan synthesis[J].The Journal of Histochemistry and Cytochemistry, 2021, 69(1):35-47.
[18] MALONEY F P, KUKLEWICZ J, COREY R A, et al.Structure, substrate recognition and initiation of hyaluronan synthase[J].Nature, 2022, 604(7904):195-201.
[19] GIRISH K S, KEMPARAJU K.The magic glue hyaluronan and its eraser hyaluronidase:A biological overview[J].Life Sciences, 2007, 80(21):1921-1943.
[20] SNETKOV P, ZAKHAROVA K, MOROZKINA S, et al.Hyaluronic acid:The influence of molecular weight on structural, physical, physico-chemical, and degradable properties of biopolymer[J].Polymers, 2020, 12(8):1800.
[21] FALLACARA A, BALDINI E, MANFREDINI S, et al.Hyaluronic acid in the third millennium[J].Polymers, 2018, 10(7):701.
[22] SALIH A R C, FAROOQI H M U, AMIN H, et al.Hyaluronic acid:Comprehensive review of a multifunctional biopolymer[J].Future Journal of Pharmaceutical Sciences, 2024, 10(1):63.
[23] BERDIAKI A, NEAGU M, SPYRIDAKI I, et al.Hyaluronan and reactive oxygen species signaling—novel cues from the matrix [J].Antioxidants, 2023, 12(4):824.
[24] PETREY A C, DE LA MOTTE C A.Hyaluronan, a crucial regulator of inflammation[J].Frontiers in Immunology, 2014, 5:101.
[25] CRISTIANO L, GUAGNI M.Zooceuticals and cosmetic ingredients derived from animals[J].Cosmetics, 2022, 9(1):13.
[26] KENDALL F, HEIDELBERGER M, DAWSON M. A serologically inactive polysaccharide elaborated by mucoid strains of group a hemolytic streptococcus[J]. Journal of Biological Chemistry, 1937, 118(1): 61-69.
[27] UCM R, AEM M, LHB Z, et al.Comprehensive review on biotechnological production of hyaluronic acid:Status, innovation, market and applications[J].Bioengineered, 2022, 13(4):9645-9661.
[28] 滕薇, 刘树滔, 吴金鸿, 等.透明质酸的制备、功能特性及其调节肠道健康的研究进展[J].中国食品学报, 2024, 24(7):401-413.TENG W, LIU S T, WU J H, et al.Recent advances on the preparation, cell functions and absorption of hyaluronic acid and its regulatory effect on intestinal homeostasis and inflammation[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(7):401-413.
[29] WEI M M, HUANG Y, ZHU J Y, et al.Advances in hyaluronic acid production:Biosynthesis and genetic engineering strategies based on Streptococcus:A review[J].International Journal of Biological Macromolecules, 2024, 270:132334.
[30] LIU L, LIU Y F, LI J H, et al.Microbial production of hyaluronic acid:Current state, challenges, and perspectives[J].Microbial Cell Factories, 2011, 10:99.
[31] SERRA M, CASAS A, TOUBARRO D, et al.Microbial hyaluronic acid production:A review[J].Molecules, 2023, 28(5):2084.
[32] GENG R X, KANG S G, HUANG K L, et al.Boosting the photoaged skin:The potential role of dietary components[J].Nutrients, 2021, 13(5):1691.
[33] NOBILE V, BUONOCORE D, MICHELOTTI A, et al.Anti-aging and filling efficacy of six types hyaluronic acid based dermo-cosmetic treatment:Double blind, randomized clinical trial of efficacy and safety[J].Journal of Cosmetic Dermatology, 2014, 13(4):277-287.
[34] PAVICIC T, GAUGLITZ G G, LERSCH P, et al.Efficacy of cream-based novel formulations of hyaluronic acid of different molecular weights in anti-wrinkle treatment[J].Journal of Drugs in Dermatology, 2011, 10(9):990-1000.
[35] 周成霞, 李咏, 何黎, 等.视黄醛联合透明质酸抗皮肤老化功效及安全性评价[J].临床皮肤科杂志, 2010, 39(7):420-422.ZHOU C X, LI Y, HE L, et al.Anti-aging efficacy and safety of topical preparations containing retinaldehyde and hyaluronate fragments[J].Journal of Clinical Dermatology, 2010, 39(7):420-422.
[36] KAYA G, TRAN C, SORG O, et al.Hyaluronate fragments reverse skin atrophy by a CD44-dependent mechanism[J].PLoS Medicine, 2006, 3(12):e493.
[37] TONG T, GENG R X, KANG S G, et al.Revitalizing photoaging skin through eugenol in UVB-exposed hairless mice:Mechanistic insights from integrated multi-omics[J].Antioxidants, 2024, 13(2):168.
[38] GENG R X, FANG J J, KANG S G, et al.Chronic exposure to UVB induces nephritis and gut microbiota dysbiosis in mice based on the integration of renal transcriptome profiles and 16S rRNA sequencing data[J].Environmental Pollution, 2023, 333:122035.
[39] YOSHIDA H, NAGAOKA A, KOMIYA A, et al.Reduction of hyaluronan and increased expression of HYBID (alias CEMIP and KIAA1199) correlate with clinical symptoms in photoaged skin[J].British Journal of Dermatology, 2018, 179(1):136-144.
[40] HA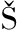 OV
OV M, CRH
M, CRH K T,
K T, 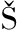 AFR
AFR NKOV
NKOV B, et al.Hyaluronan minimizes effects of UV irradiation on human keratinocytes[J].Archives of Dermatological Research, 2011, 303(4):277-284.
B, et al.Hyaluronan minimizes effects of UV irradiation on human keratinocytes[J].Archives of Dermatological Research, 2011, 303(4):277-284.
[41] YUN M K, LEE S J, SONG H J, et al.Protein expression level of skin wrinkle-related factors in hairless mice fed hyaluronic acid[J].Journal of Medicinal Food, 2017, 20(4):420-424.
[42] KAWADA C, KIMURA M, MASUDA Y, et al.Oral administration of hyaluronan prevents skin dryness and epidermal thickening in ultraviolet irradiated hairless mice[J].Journal of Photochemistry and Photobiology B:Biology, 2015, 153:215-221.
[43] BALOGH L, POLYAK A, MATHE D, et al.Absorption, uptake and tissue affinity of high-molecular-weight hyaluronan after oral administration in rats and dogs[J].Journal of Agricultural and Food Chemistry, 2008, 56(22):10582-10593.
[44] KIMURA M, MAESHIMA T, KUBOTA T, et al.Absorption of orally administered hyaluronan[J].Journal of Medicinal Food, 2016, 19(12):1172-1179.
[45] DE LA MOTTE C A, KESSLER S P.The role of hyaluronan in innate defense responses of the intestine[J].International Journal of Cell Biology, 2015, 2015:481301.
[46] JUNCAN A M, MOIS D G, SANTINI A, et al.Advantages of hyaluronic acid and its combination with other bioactive ingredients in cosmeceuticals[J].Molecules, 2021, 26(15):4429.
D G, SANTINI A, et al.Advantages of hyaluronic acid and its combination with other bioactive ingredients in cosmeceuticals[J].Molecules, 2021, 26(15):4429.
[47] ZHU J Y, TANG X D, JIA Y, et al.Applications and delivery mechanisms of hyaluronic acid used for topical/transdermal delivery-A review[J].International Journal of Pharmaceutics, 2020, 578:119127.
[48] OE M, SAKAI S, YOSHIDA H, et al.Oral hyaluronan relieves wrinkles:A double-blinded, placebo-controlled study over a 12-week period[J]. Clinical, Cosmetic and Investigational Dermatology, 2017, 10:267-273.
[49] TOSHIHIDE S.Clinical effects of hyaluronic acid diet for moisture content of dry skin[J].Aesthetic Dermatology, 2007, 17(1):33-39.
[50] HSU T F, SU Z R, HSIEH Y H, et al.Oral hyaluronan relieves wrinkles and improves dry skin:A 12-week double-blinded, placebo-controlled study[J].Nutrients, 2021, 13(7):2220.
[51] ZHOU W C, ZI L, CEN Y, et al.Copper sulfide nanoparticles-incorporated hyaluronic acid injectable hydrogel with enhanced angiogenesis to promote wound healing[J].Frontiers in Bioengineering and Biotechnology, 2020, 8:417.
[52] ALEMZADEH E, ORYAN A, MOHAMMADI A A.Hyaluronic acid hydrogel loaded by adipose stem cells enhances wound healing by modulating IL-1β, TGF-β1, and bFGF in burn wound model in rat[J].Journal of Biomedical Materials Research Part B:Applied Biomaterials, 2020, 108(2):555-567.
[53] LANGAN S M, IRVINE A D, WEIDINGER S.Atopic dermatitis[J].The Lancet, 2020, 396(10247):345-360.
[54] HOW K N, YAP W H, LIM C L H, et al.Hyaluronic acid-mediated drug delivery system targeting for inflammatory skin diseases:A mini review[J].Frontiers in Pharmacology, 2020, 11:1105.
[55] DRAELOS Z D.A clinical evaluation of the comparable efficacy of hyaluronic acid-based foam and ceramide-containing emulsion cream in the treatment of mild-to-moderate atopic dermatitis[J].Journal of Cosmetic Dermatology, 2011, 10(3):185-188.
[56] ZHENG B W, WANG B Y, XIAO W L, et al.Different molecular weight hyaluronic acid alleviates inflammation response in DNFB-induced mice atopic dermatitis and LPS-induced RAW 264.7 cells[J].Life Sciences, 2022, 301:120591.
[57] GU L, SOO Y, HYUN K, et al.Hyaluronan oligosaccharides improve rosacea-like phenotype through anti-inflammatory and epidermal barrier-improving effects[J].Annals of Dermatology, 2020, 32(3):189-196.
[58] SCHLESINGER T E, POWELL C R.Efficacy and tolerability of low molecular weight hyaluronic acid sodium salt 0.2% cream in rosacea[J].Journal of Drugs in Dermatology, 2013, 12(6):664-667.
[59] 谢成树, 周顶峰, 李敏, 等.2%夫西地酸乳膏联合透明质酸治疗丘疹脓疱型玫瑰痤疮的临床观察[J].皮肤性病诊疗学杂志, 2023, 30(5):428-432.XIE C S, ZHOU D F, LI M, et al.Clinical observation on the treatment of papular pustular rosacea with 2% fusidic acid cream combined with hyaluronic acid[J].Journal of Diagnosis and Therapy on Dermato-venereology, 2023, 30(5):428-432.
[60] CHENG Q, LIU C Q, ZHAO J, et al.Unlocking the potential of hyaluronic acid:Exploring its physicochemical properties, modification, and role in food applications[J].Trends in Food Science &Technology, 2023, 142:104218.