蛋白质作为维持人类生命的基本营养素,随着世界人口的增长(预计到2050年将达到97亿)和生活水平的提高,人类对蛋白质的需求将会快速增长[1]。动物蛋白即传统肉类的生产主要依靠传统畜牧业,这不但对土地和水资源有极高需求,产生的温室气体排放对气候变化也有着不可忽视的影响[2]。例如,仅牛场生产的牛肉,就占据了全球畜牧业25%的温室气体排放总量(约合13亿吨二氧化碳当量),土地占用率更是高达61%(约 9.5 亿公顷)[3]。因此,确保蛋白质的广泛可及性、经济可负担性、安全性以及可持续性,对于满足未来全球食物保障需求、推动生态环境保护具有至关重要的意义。目前,肉类替代品主要包括植物蛋白(如大豆蛋白)、细胞培养肉、微生物蛋白。其中,微生物蛋白是从细菌、真菌、微藻和酵母培养的生物质中获得[4]。植物蛋白,作为替代蛋白最广泛的来源,具有高蛋白、高膳食纤维、不含胆固醇,价格低廉等优势,截至2021年,豆类衍生蛋白已成为肉类替代品的主要来源,约占据63.6%的市场份额[5]。然而,大豆、芸豆及其他谷物豆类来源的植物蛋白中,往往含有较高水平的胰蛋白酶抑制剂等抗营养因子。这类物质的存在,会显著降低蛋白质与氨基酸的消化吸收率,并对蛋白质的营养价值产生不利影响[6]。同时,种植豆类需要更多的耕地,将豆类蛋白转化成模拟动物肉的性状效率也相对较低。而与传统肉类相比,细菌培养肉被认为“不够天然”,这种看法导致大众对这种新型食物的接受度较低[7]。因此,为满足未来蛋白市场日益增长且多元化的需求,真菌蛋白已成为除传统动物蛋白、植物蛋白之外,极具潜力的优质替代蛋白来源。
狭义的真菌蛋白是指丝状真菌发酵获得的低热量且富含蛋白质的全食物来源[8],本综述中真菌蛋白采用此定义,真菌蛋白具有纤维状结构,氨基酸组成接近人体需求,同时具有蛋白含量高、制造效率高、CO2排放低、资源消耗少等优势,能够通过发酵过程优化营养成分,从而提高营养价值,被视为一种有潜力的替代蛋白来源[9]。作为食品和饲料行业的新兴原料,2024年全球替代蛋白质市场价值为905亿美元,预计到2034年将达到2 387亿美元,复合年均增长率增长9.8%,展现出显著的环境和社会经济效益[10-11]。
本文重点阐述了丝状真菌蛋白的生产、营养价值、健康效应,同时对真菌蛋白的安全风险、控制措施及其在国内外的监管现状进行综述,并分析了目前真菌蛋白在替代蛋白应用方面亟待解决的问题和未来发展方向,为真菌替代蛋白产品的开发和推广提供参考依据。
1 真菌蛋白概述
基于本文中狭义真菌蛋白的概念,目前的研究表明红曲霉(Monascus purpureus)、米曲霉(Aspergillus oryzae)、盐渍副霉菌(Paradendryphiella salina)、米根霉(Rhizopus oryzae)、间型脉孢菌(Neurospora intermedia)、威尼斯镰刀菌(Fusarium venenatum)等丝状真菌可以通过深层发酵、固态发酵或表面培养方法来生产真菌蛋白[4]。供人类消费的真菌蛋白主要由食品级的发酵底物生成,研究发现一些食品加工的副产物也可以作为发酵底物,比如豌豆加工副产品、啤酒糟、葡萄渣、奶酪乳清等,既能提高糖化产量和木糖利用率,也能让真菌蛋白的生产环境更加友好[12]。国外在真菌替代蛋白开发方面起步较早,其中最早进入市场的是来自英国Marlow Foods公司的真菌蛋白品牌Quorn。Quorn蛋白是由Fusarium venenatum通过有氧发酵得到的真菌蛋白产品,于1985年获准上市,此后被欧洲等国家接受[4]。此外,美国 Nature’s Fynd公司研发生产的 Fy ProteinTM,其生产菌株为Fusarium flavolapis[13]。通常,真菌替代蛋白产品是通过在确定的培养基中发酵收获菌丝体后,与蛋清、色素和风味化合物混合以得到类似动物肉的产品。真菌蛋白的生产过程如图1所示,以Fusarium venenatum为例,先进行菌种准备、发酵,菌丝富集后在65 ℃条件下处理20 min以去除RNA,接着通过过滤或离心获得真菌生物质,将其制型后85~90 ℃下蒸制30 min,-18 ℃冷冻30 min,使其更接近动物肉的质地,最终得到肉饼、肉肠、肉丸等真菌蛋白产品[14]。
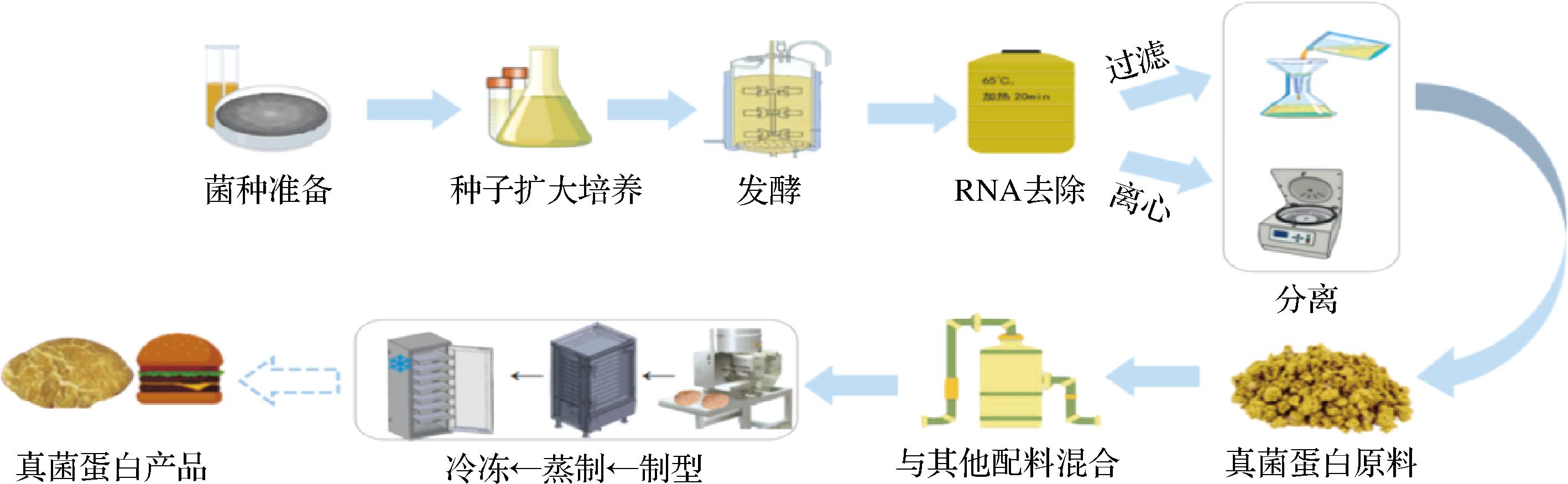
图1 真菌蛋白产品的生产过程
Fig.1 Production process of mycoprotein products
2 真菌蛋白的营养特性
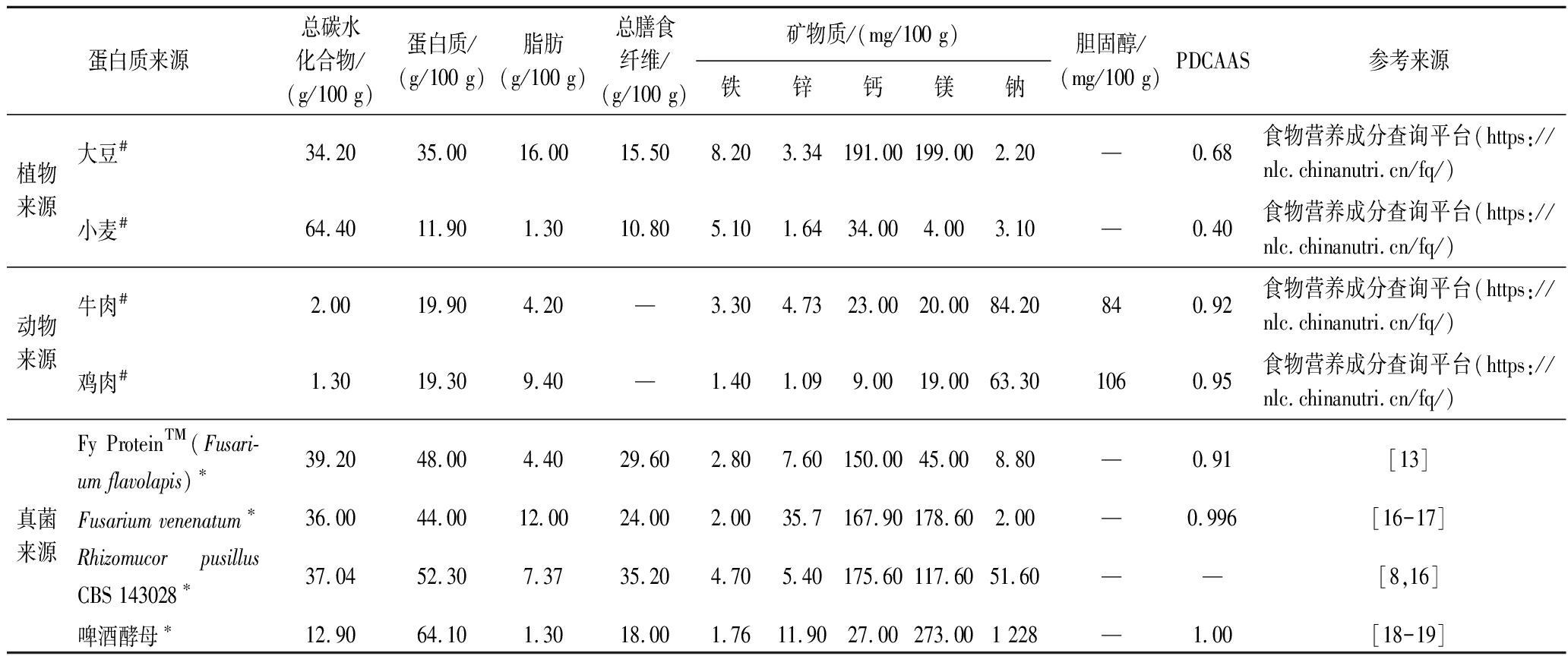
真菌蛋白不仅富含蛋白质、膳食纤维,还具有低脂肪的特点,是一种健康的蛋白质来源,在营养特性上展现出显著优势[15],它含有人体所需的全部必需氨基酸种类,其蛋白质消化率校正氨基酸评分(protein digestibility corrected amino acids score,PDCAAS)接近1,超越了大部分传统蛋白。表1列出以大豆、小麦为代表的植物蛋白,以鸡肉、牛肉为代表的动物蛋白和以Fusarium strain flavolapis、Fusarium venenatum、Rhizomucorpusillus CBS 143028为代表的真菌蛋白以及啤酒酵母的营养成分含量情况。
表1 不同蛋白来源的营养成分含量
Table 1 Nutrient content of different protein sources
蛋白质来源总碳水化合物/(g/100 g)蛋白质/(g/100 g)脂肪(g/100 g)总膳食纤维/(g/100 g)矿物质/(mg/100 g)铁锌钙镁钠胆固醇/(mg/100 g)PDCAAS参考来源植物来源大豆#34.2035.0016.0015.508.203.34191.00199.002.20—0.68食物营养成分查询平台(https://nlc.chinanutri.cn/fq/)小麦#64.4011.901.3010.805.101.6434.004.003.10—0.40食物营养成分查询平台(https://nlc.chinanutri.cn/fq/)动物来源牛肉#2.0019.904.20—3.304.7323.0020.0084.20840.92食物营养成分查询平台(https://nlc.chinanutri.cn/fq/)鸡肉#1.3019.309.40—1.401.099.0019.0063.301060.95食物营养成分查询平台(https://nlc.chinanutri.cn/fq/)真菌来源Fy ProteinTM(Fusari-um flavolapis)∗39.2048.004.4029.602.807.60150.0045.008.80—0.91[13]Fusarium venenatum∗36.0044.0012.0024.002.0035.7167.90178.602.00—0.996[16-17]Rhizomucor pusillus CBS 143028∗37.0452.307.3735.204.705.40175.60117.6051.60——[8,16]啤酒酵母∗12.9064.101.3018.001.7611.9027.00273.001 228—1.00[18-19]
注:“食物营养成分查询平台”是由中国营养学会和中国疾病预防控制中心营养与健康所联合发布的权威查询网站,该平台的数据来源于中国疾病预防控制中心营养与健康所建立的中国食物成分数据库;“#”表示以湿重计,“*”表示以干重计;“—”表示未测出。
2.1 蛋白质
在蛋白质含量上,真菌蛋白相较于传统的植物来源蛋白具有一定优势[20]。真菌来源中Rhizomucor pusillus CBS 143028菌株的蛋白质含量为52.30 g/100 g[8],高于植物蛋白(大豆35.00 g/100 g)。在蛋白质消化吸收率方面,通常使用PDCAAS进行评估。其中Fusarium venenatum的PDCAAS为0.996[18],优于大多数植物蛋白和动物蛋白。
2.2 脂肪
脂肪是人体必需的营养素,对维持健康至关重要。但脂肪摄入过多可能会对心血管系统造成一定影响。真菌蛋白的脂肪主要由单不饱和脂肪酸和多不饱和脂肪酸组成,其饱和脂肪酸含量低,脂肪酸组成更健康[21]。其中Rhizomucor pusillus CBS 143028的脂肪含量为7.37 g/100 g[8],低于植物蛋白和动物蛋白(大豆16.00 g/100 g、鸡肉9.40 g/100 g)。因此,真菌蛋白相较于动物蛋白对心血管健康可能更为有益。
2.3 膳食纤维
膳食纤维在提高消化能力、促进肠道健康等方面发挥重要作用[22]。真菌蛋白中的膳食纤维主要由β-葡聚糖和几丁质组成,其中不溶性膳食纤维占比相对较大[23]。真菌蛋白的膳食纤维含量(Rhizomucor pusillus CBS 143028含量为35.20 g/100 g)大都高于植物蛋白(小麦10.80 g/100 g)[8],真菌蛋白高膳食纤维含量符合健康饮食的要求。
2.4 维生素和矿物质
真菌蛋白含有丰富的矿物质,比如钙(Rhizomucor pusillus CBS 143028为175.60 mg/100 g、Fusarium venenatum为167.90 mg/100 g)、镁(Rhizomucor pusillus CBS 143028为117.60 mg/100 g、啤酒酵母为273.00 mg/100 g)等矿物质含量都比较丰富。但真菌蛋白的铁和维生素B12含量有限,如Fusarium venenatum中仅为2.00 mg/100 g,而动物蛋白却是铁和维生素B12的重要来源,如牛肉中铁含量为12.13 mg/100 g(以干重计)高于Fusarium venenatum的2.00 mg/100 g(以干重计),牛肝中维生素B12含量为83.10 μg/100 g,素食人群可搭配营养补充剂及营养强化食品食用[24]。
从营养成分数据来看,真菌蛋白的氨基酸组成、PDCAAS优于植物蛋白,脂肪组成和膳食纤维的含量也显著优于动物蛋白。这可能是由于丝状真菌细胞壁中包含近2/3的β-葡聚糖和1/3的甲壳素聚N-乙酰氨基葡萄糖,且含有亮氨酸、谷氨酰胺、谷氨酸、天冬氨酸、天冬酰胺和瓜氨酸等必需氨基酸和非必需氨基酸[8]。
3 真菌蛋白的健康效应
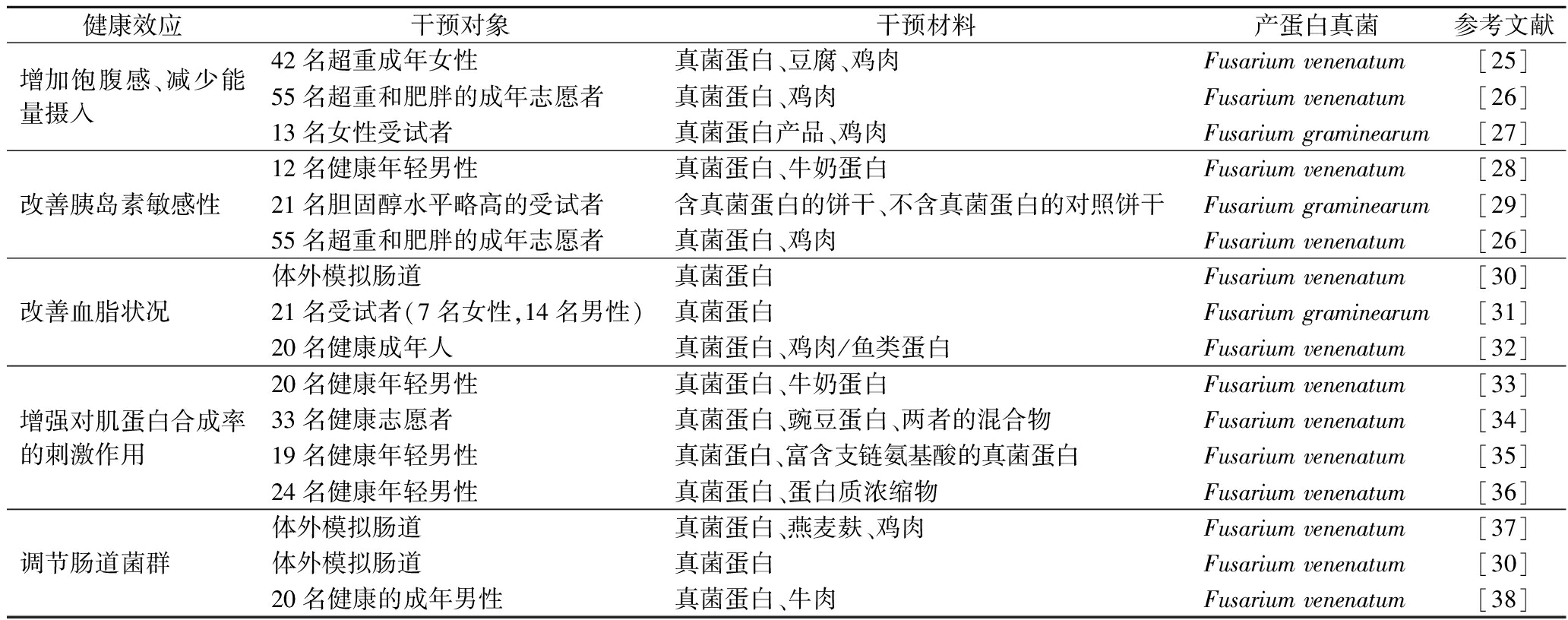
近年来,在营养与功能食品领域,真菌蛋白因其高蛋白、高膳食纤维及低脂肪等特性引发诸多关注。研究者通过临床随机对照实验、体外模拟消化模型及代谢组学分析,揭示了其在增强饱腹感、减少能量摄入、改善血糖血脂、肌肉质量维持和调节肠道健康等多方面的健康效应,如表2所示,其中Fusarium graminearum后期经研究更名为Fusarium venenatum。因为Fusarium venenatum发酵生产的Quorn蛋白,有较长的食用历史和较多的食用人数,目前很多研究都以其为研究对象探索潜在的健康促进作用。
表2 真菌蛋白的健康效应
Table 2 Health effects of mycoprotein
健康效应干预对象干预材料产蛋白真菌参考文献增加饱腹感、减少能量摄入42名超重成年女性真菌蛋白、豆腐、鸡肉Fusarium venenatum[25]55名超重和肥胖的成年志愿者真菌蛋白、鸡肉Fusarium venenatum[26]13名女性受试者真菌蛋白产品、鸡肉Fusarium graminearum[27]改善胰岛素敏感性12名健康年轻男性真菌蛋白、牛奶蛋白Fusarium venenatum[28]21名胆固醇水平略高的受试者含真菌蛋白的饼干、不含真菌蛋白的对照饼干Fusarium graminearum[29]55名超重和肥胖的成年志愿者真菌蛋白、鸡肉Fusarium venenatum[26]改善血脂状况体外模拟肠道真菌蛋白Fusarium venenatum[30]21名受试者(7名女性,14名男性)真菌蛋白Fusarium graminearum[31]20名健康成年人真菌蛋白、鸡肉/鱼类蛋白Fusarium venenatum[32]增强对肌蛋白合成率的刺激作用20名健康年轻男性真菌蛋白、牛奶蛋白Fusarium venenatum[33]33名健康志愿者真菌蛋白、豌豆蛋白、两者的混合物Fusarium venenatum[34]19名健康年轻男性真菌蛋白、富含支链氨基酸的真菌蛋白Fusarium venenatum[35]24名健康年轻男性真菌蛋白、蛋白质浓缩物Fusarium venenatum[36]调节肠道菌群体外模拟肠道真菌蛋白、燕麦麸、鸡肉Fusarium venenatum[37]体外模拟肠道真菌蛋白Fusarium venenatum[30]20名健康的成年男性真菌蛋白、牛肉Fusarium venenatum[38]
3.1 增强饱腹感与减少能量摄入
真菌蛋白含有高膳食纤维,相较于鸡肉等动物蛋白,具有更强的饱腹特性且能减少后续能量摄入[39]。在一项随机对照实验中,给55名志愿者分别食用真菌蛋白(分为高、中、低3种含量)和等能量的鸡肉。发现真菌蛋白相比较鸡肉能减少能量摄入和降低胰岛素浓度,且代谢组学分析也显示餐后代谢物与饱腹感相关[26]。此后,TURNBULL等[27]对13名健康女性开展了非限制性饮食随机交叉实验,WILLIAMSON等[25]对超重的绝经前女性进行了随机交叉对照实验,均进一步证实了真菌蛋白能够增加机体饱腹感,减少后续能量摄入。
3.2 改善血脂状况
真菌蛋白中的膳食纤维能通过改变胆固醇代谢或与肠道内的中性甾体、胆汁酸和胆固醇结合,降低胆盐活性,减少脂肪乳化和吸收,从而降低血脂水平[30]。COELHO等[32]对健康成年人进行了1周饮食干预实验,对比鱼肉或鸡肉,发现营养均衡的真菌蛋白餐可显著降低肥胖和超重个体的血浆总胆固醇、甘油三酯、低密度脂蛋白和极低密度脂蛋白水平。也有研究表明,真菌蛋白对血浆脂质组有显著影响,可以减少脂质降解和结合胆汁盐来降低血液脂质水平,对长期心血管代谢健康有益[30-32]。
3.3 改善胰岛素敏感性
近年来,血糖代谢紊乱的发病率呈上升趋势[40],而真菌蛋白富含膳食纤维,有助于控制食欲和能量摄入,能够很好地平衡血糖代谢。其中的黏性多糖可以降低餐后血糖和高胰岛素血症,β-葡聚糖先前在高碳水化合物负荷下食用时被证明可调节血糖和高胰岛素血症[17]。TURNBULL等[29]和DUNLOP等[28]的研究结果进一步表明,真菌蛋白不仅能够减少超重和肥胖个体的能量摄入,还可以改善胰岛素的敏感性,降低胰岛素浓度,控制体重和改善血糖代谢。真菌蛋白对胰岛素的影响或许对治疗和改善Ⅱ型糖尿病、高胰岛素血症等血糖代谢疾病提供一条新路径。
3.4 有利于肌肉的合成
真菌蛋白作为一类富含蛋白质和氨基酸的新型营养来源,在促进肌肉合成和生长方面具有显著的潜力。首先,真菌蛋白富含亮氨酸,作为全食物基质的组成部分,真菌蛋白与其他营养物质具有协同作用,能够延缓胃排空,并为身体提供连续的氨基酸[36];MONTEYNE等[33]在20名健康青年男性参与的随机、双盲、平行组研究中发现,服用单剂量真菌蛋白能加快静息和运动后肌肉蛋白质合成速率,且比服用亮氨酸匹配的牛奶蛋白能更大程度上促进肌肉蛋白质合成。一项针对不同非动物蛋白(含真菌蛋白、豌豆蛋白及其混合物)对肌肉蛋白合成率影响的研究进一步证实,真菌蛋白不仅能够有效支持长期的肌肉蛋白质周转,还能助力机体对训练产生适应性反应,其在促进肌肉蛋白质合成增长方面的效果,甚至优于牛奶蛋白[34]。
3.5 调节肠道菌群
肠道菌群对人类健康起着至关重要的作用,能够维持肠道屏障的完整性、促进新陈代谢和调节免疫系统等。肠道微生物群失调可能导致人体免疫系统异常、代谢功能紊乱,导致慢性炎症等各种病理状况[41]。据报道,肠道菌群组成已显示出与代谢紊乱(如心血管疾病和Ⅱ型糖尿病)有关的证据[42]。且肠道菌群中Bacteroides uniformis的增加可能通过减缓肥胖进展和限制脂质的肠道吸收来调节小鼠的代谢反应[43]。2024年,COLOSIMO等[37]研究了真菌蛋白纤维发酵造成的微生物种群和代谢物的变化。在这个模拟发酵系统中,真菌蛋白质和燕麦、鸡肉相比,造成了微生物群的显著差异,出现了如Bacteroides ovatus、Bacteroides uniformis 和 Bacteroides xylanisolvens等会大量分解β-葡聚糖的杆菌。在一项针对20名健康成年男性的盲法、随机、交叉饮食干预实验中发现,摄入真菌蛋白可显著降低粪便中遗传毒性物质、亚硝基化合物的排泄量及短链脂肪酸水平,同时显著提升Lactobacillus属、Roseburia属、Akkermansia属等有益肠道微生物群的丰度[38]。
4 真菌蛋白的安全风险及控制措施
丝状真菌发酵产生的大量生物质是真菌替代蛋白的主要供应形式,但霉菌在生长过程中可能会产生黄曲霉毒素、赭曲霉毒素等真菌毒素,同时其中的蛋白成分可能是潜在的致敏原,这会对消费者的健康带来安全风险。因此,在真菌蛋白资源的开发及生产,需要采取各种必要的风险控制措施。
4.1 潜在毒性与毒素控制
曲霉属、青霉属和镰孢属等真菌属在生长过程中可能产生毒素,如黑毛霉素、细胞松弛素、抗生素Y、肽类麦角生物碱、棒麦角碱生物碱和简单麦角生物碱等,这些毒素会影响中枢神经系统,导致肌肉收缩、血压变化、幻觉和四肢坏疽,甚至致癌[44]。因此选择在合适生长条件下无毒素产生的菌株极其重要,比如Quorn蛋白的生产使用的菌种是Fusarium venenatum,但在早期的研发中,通过安全性评估发现NRRL22198菌株会产生4 -单乙酰氧基角鲨烯醇、双乙酸基草镰刀菌醇和脱氧雪腐镰刀菌醇等毒素,但是ATCC PTA-2684菌株在类似的生长条件下却不会产生任何毒素[45]。
同时还要严格控制发酵条件(如温度、pH和通气量)、在生产过程中定期检测毒素含量,以有效控制真菌蛋白中的潜在毒素。比如在Quorn蛋白的发酵过程中,每6 h检测1次真菌毒素含量,以确保产品的安全性[4]。近年来,在挖掘真菌蛋白资源时,研究者还充分运用生物信息学手段,以评估生产真菌蛋白菌株的产毒性和致病性,比如SCAIFE等[46]在对Rhizomucor pusillus strain CBS 143028菌株的基因组进行测序注释后,用CGE(Center for Genomc Epidemiology,https://genomicepidemiology.org/)网站上的表型预测工具ToxFinder、VirulenceFinder 和PathogenFinder 等识别基因组中的产毒基因和获得性致病基因,同时预测真菌编码蛋白对人类宿主的致病概率。
4.2 潜在致敏性与致敏蛋白
真菌蛋白可能含有过敏原,给消费者带来一定过敏风险[47]。2001年,一名27岁的霉菌过敏女性患者在食用Quorn汉堡后几分钟内出现I型超敏反应[48]。2018年JACOBSON等[49]在Quorn真菌蛋白模拟肉食品的1 752例过敏反应案例中,发现312人出现了荨麻疹等皮肤过敏症状,有1 692人在进食8 h内出现呕吐、腹泻等胃肠道症状。此外,在一项双盲安慰剂对照评估真菌蛋白食物过敏的研究中,也有个体出现了对真菌蛋白的不良反应[39]。
所以在真菌蛋白的生产中,要优先选择已知致敏性低的菌种进行发酵生产,从源头上降低致敏风险;在产品上市前,可通过血清学、细胞和动物实验对真菌蛋白进行严格的致敏性评估,对其致敏性风险进行有效控制;此外,还可以运用生物信息学工具,如使用Algpred工具预测过敏原蛋白,通过UniprotKB/Swiss-Prot数据库筛选非过敏原蛋白,通过AllergenOnline数据库评估IgE交叉反应性可能。比如对Neurospora crassa真菌蛋白进行安全性评估时,就综合运用了上述方法,为该真菌蛋白的安全性提供更全面的支持[50]。
4.3 高嘌呤风险与RNA含量
膳食嘌呤作为核酸、核苷酸或游离碱基的成分存在于大多数食物中。嘌呤含量较高的食物会提高体内尿酸水平,增加患高尿酸血症的风险。SUN等[51]研究发现,素食肉类替代品中的嘌呤含量差异显著,主要取决于其蛋白质来源。谷物、坚果、薯类和豆制品中的嘌呤含量大多低于50 mg/100 g,而食用菌干品中的嘌呤含量则为178~780 mg/100 g,接近甚至超过动物肝脏中的嘌呤含量(如猪肝284.8 mg/100 g、牛肝219.8 mg/100 g)[10]。丝状真菌生物质中也有较高的嘌呤含量,如Quorn产品的嘌呤含量可达226.4 mg/100 g[52]。
为了避免因食用丝状真菌蛋白而导致尿酸水平过高,可在发酵过程结束后,对丝状真菌蛋白进行加热,激活内源性RNA酶以降低RNA含量,从而避免膳食中过多嘌呤的摄入[53]。
5 真菌替代蛋白的监管现状
真菌替代蛋白作为一种新兴食品,不同国家和地区的审批监管政策不同。如果生产的真菌运用了转基因技术,那么其监管主要依据该国转基因生物产品的管理法规。本文主要分析欧盟、美国和中国的真菌蛋白食品(非转基因)监管现状。
5.1 欧盟
世界上第一种丝状真菌替代蛋白产品诞生于英国,产品上市前经历了10年的评估,最终基于Fusarium venenatum A3/5(ATCC PTA-2684)菌株生产的真菌蛋白经系统评估证实其食用安全性,成功获批上市。1983年,相关团队向英国农业渔业与食品部提交了一份逾200万字的安全性评估报告。最终,由 Marlow Foods 公司研发生产的 Quorn®品牌真菌蛋白产品,于1985年正式获批上市[4,16],此后销往世界多个国家。
欧盟对替代蛋白的监管政策较为严格,审批评估较为完善。根据微生物作为生产工具及作为产品原材料的不同用途,管理不同。生产用微生物需要通过QPS(qualified presumption of safety)的安全资格认证后方可作为工具进行生产;而产品原材料使用微生物的食品,按照《新食品法案》进行管理[54]。欧盟委员会于2015年12月11日颁布《新食品法案(EU)2015/2283》。2021年3月,欧洲食品安全局(European Food Safety Authority,EFSA)发布了新型食品申请的指南 (guidance on the preparation and submission of an application for authorization of a novel food in the context of Regulation(EU)2015/2283)[55],真菌蛋白食品的审批按此流程。首先,向欧盟委员会提交申请;由EFSA进行风险评估并给出安全评估意见(通常为9个月),将评估意见提交欧盟成员国听取异议,由欧盟委员会做出最终决定。
5.2 美国
在美国,真菌蛋白食品由美国食品药品监督管理局(Food and Drug Administration,FDA)管理,主要以GRAS(generally recognized as safe)认证进行审批。根据美国《联邦食品、药品和化妆品法》,任何有意添加到食品中的物质都是食品添加剂,必须经过FDA的上市前审查和批准,除非该物质得到有资质专家的普遍认可,在其预期用途条件下已被充分证明是安全的,或者该物质的使用不属于食品添加剂的定义。《联邦食品、药品和化妆品法》第201(s)和409条的规定,以及《美国联邦法规》21 CFR 170.3和21 CFR 170.30的规定,食品成分的使用既可以通过科学程序被认定为GRAS,也可以通过在食品中使用的经验被认定为GRAS(对于1958年以前在食品中使用的成分),通过科学程序认定GRAS与食品添加剂的审批要求一致[56]。
GRAS还可以分为GRAS自我声明(Self-affirmed GRAS)和FDA GRAS认证两类。后者需要向FDA正式提交备案材料,并经过FDA官方审核和批准。若FDA的结论为“没有疑问”,即可纳入GRAS名单,并且可在FDA官网上查证,因此FDA GRAS认证更具权威性。目前多种真菌蛋白产品获得FDA GRAS认证,例如Quron真菌蛋白(GRN NO.91)2002年在美国通过GRAS认证,Natures Fynd公司备案的Fusarium strain flavolapis产蛋白(Fungal protein from fermented Fusarium sp.mycelia,GRN No.904)2021年通过GRAS认证。
5.3 中国
与欧盟和美国相比,中国真菌替代蛋白的研发及应用相对较晚。在中国真菌替代蛋白食品可以依照食品原料或食品添加剂的相关法规进行审批及管理。中国于2010年和2011年分别发布了《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》,国家卫生健康委于2022年发布了更新公告,其中除了1种马克斯克鲁维酵母,都属于细菌。公告规定《可用于食品的菌种名单》以外的新菌种要按照《新食品原料安全性审查管理办法》进行审查。2023年以酿酒酵母为原料生产的酵母蛋白获批新食品原料(2023年第10号公告),2024年克鲁维毕赤酵母获批新食品原料,并列入《可用于食品的菌种名单》(2024第2号公告)。但目前我国尚无丝状真菌发酵蛋白获批新食品原料。
5.4 其他国家
在新加坡替代蛋白属于新食品类别,被划分在“定义食品”的1个子类别,由新加坡食品局(Singapore Food Agency,SFA)统一负责与食品相关的监管工作。SFA 对每个新型食品申请个案均进行独立的安全性审核,每项评估需时 9~12个月[57]。在新西兰则由新西兰食品标准局(Food Standards Australia New Zealand, FSANZ)负责监管,而相关安全性评估则由新食品原料咨询委员会进行[58]。
6 展望
在全球优质蛋白需求激增的背景下,真菌蛋白作为一种新兴替代蛋白来源,因其突出的营养价值、对健康的有益效应及其环境友好性,在食品开发和应用上已获得了一定关注,但发展之路仍需面临诸多挑战。
6.1 技术瓶颈与创新方向
在技术研发层面,尽管已成功筛选出镰刀菌等优质生产菌种,但真菌蛋白产业化仍面临诸多亟待突破的瓶颈,具体包括:产品色泽的自然度与稳定性欠佳、菌种选育及改良技术亟待升级、发酵模式创新性不足,以及产品在口感与质地上的表现尚未达到商业化应用的理想标准[17]。后续应积极选育优良菌株、探索新型发酵模式、优化发酵条件、提高传质和传热效率,如混菌培养可通过离心和新鲜培养基重悬实现菌体标准化,再按一定比例接种菌种来构建可控微生物群落,以此优化发酵模式[59];同时深入研究蛋白结构与功能的关系,未来还可以通过CRISPR-Cas9基因编辑技术对丝状真菌的色泽、质地的相关基因进行编辑,以提升产品的感官属性。
6.2 生产成本与可持续性
真菌蛋白生产成本高,一方面在利用农业和工业废弃物作为替代原料时,部分原料成本高昂,还面临收集困难和预处理、供应和质量不稳定等难题[60]。另一方面,生产工艺复杂,发酵和分离提取能耗大、试剂消耗多。所以,后续应加大在低成本、可持续原料开发方面的投入,完善废弃物的收集和预处理体系,以确保原料供应的稳定性和质量的可靠性。需进一步研发高效节能生产工艺,创新设备和提取技术,从而降低生产成本。
6.3 消费者认知与市场推广
部分消费者对真菌蛋白产品了解有限,对其营养价值和安全性仍存在疑虑[61]。持续以消费者需求为导向,优化产品品质,改进配方和加工工艺,解决风味、口感等问题;并构建全方位科普宣传体系,利用多种渠道普及真菌蛋白知识,消除消费者顾虑。
总之,面对全球对可持续食品需求增加的环境,真菌蛋白或可成为未来食品市场替代蛋白的重要组成部分。真菌蛋白作为在功能性食品或药物开发方面应用的健康促进替代蛋白,未来需持续优化菌种选育和发酵工艺,提高生产效率和产品质量;深入探索新的发酵模式和加工技术,降低成本并开发针对特定健康需求的营养补充剂来提升市场竞争力。政府和国际组织应完善真菌蛋白研发和应用的相关政策和标准,同时加强国际合作,促进真菌蛋白微生物资源挖掘、安全性评价、产品开发方面的技术交流和资源共享,加速其在全球范围内的推广和应用。
[1] TILMAN D, BALZER C, HILL J, et al.Global food demand and the sustainable intensification of agriculture[J].Proceedings of the National Academy of Sciences of the United States of America, 2011, 108(50):20260-20264.
[2] HENCHION M, HAYES M, MULLEN A M, et al.Future protein supply and demand:Strategies and factors influencing a sustainable equilibrium[J].Foods, 2017, 6(7):53.
[3] POORE J, NEMECEK T.Reducing food’s environmental impacts through producers and consumers[J].Science, 2018, 360(6392):987-992.
[4] AHMAD M I, FAROOQ S, ALHAMOUD Y, et al.A review on mycoprotein:History, nutritional composition, production methods, and health benefits[J].Trends in Food Science &Technology, 2022, 121:14-29.
[5] MARKET G M S.Global Meat Substitutes Market Size, Share, and COVID-19 Impact Analysis, By Source (Plant-based Protein, Mycoprotein, Soy-based, and Others), By Distribution Channel (Foodservice and Retail), By Region (North America, Europe, Asia-Pacific, Latin America, Middle East, and Africa), Analysis and Forecast 2022-2032.[EB/OL].(2023-9)[2024-7-16].https://www.sphericalinsights.com/reports/meat-substitutes-market
[6] SARWAR GILANI G, XIAO C W, COCKELL K A.Impact of antinutritional factors in food proteins on the digestibility of protein and the bioavailability of amino acids and on protein quality[J].British Journal of Nutrition, 2012, 108(Suppl 2):S315-S332.
[7] SIEGRIST M, HARTMANN C.Perceived naturalness, disgust, trust and food neophobia as predictors of cultured meat acceptance in ten countries[J].Appetite, 2020, 155:104814.
[8] SCAIFE K, PHIPPS K R, SCALISE D, et al.Subchronic toxicity evaluation of dietary administration of a fungal biomass from Rhizomucor pusillus[J].Journal of Applied Toxicology, 2025, 45(3):400-417.
[9] KUREK M A, ONOPIUK A, POGORZELSKA-NOWICKA E, et al.Novel protein sources for applications in meat-alternative products:Insight and challenges[J].Foods, 2022, 11(7):957.
[10] 蔡路昀, 张滋慧, 曹爱玲, 等.食品中的嘌呤含量分布及在贮藏加工中变化研究进展[J].食品科学, 2018, 39(19):260-265.CAI L Y, ZHANG Z H, CAO A L, et al.Advances in research on purine distribution in foods and its changes during storage and processing[J].Food Science, 2018, 39(19):260-265.
[11] AYODELE T, TIJANI A, LIADI M, et al.Biomass-based microbial protein production:A review of processing and properties[J].Frontiers in Bioscience, 2024, 16(4):40.
[12] UPCRAFT T, JOHNSON R, FINNIGAN T, et al.Protein from renewable resources:Mycoprotein production from agricultural residues[J].Computer Aided Chemical Engineering, 2020, 48:985-990.
[13] FUREY B, SLINGERLAND K, BAUTER M R, et al.Safety evaluation of Fy ProteinTM (Nutritional Fungi Protein), a macroingredient for human consumption[J].Food and Chemical Toxicology, 2022, 166:113005.
[14] HASHEMPOUR-BALTORK F, KHOSRAVI-DARANI K, HOSSEINI H, et al.Mycoproteins as safe meat substitutes[J].Journal of Cleaner Production, 2020, 253:119958.
[15] DERBYSHIRE E J, DELANGE J.Fungal protein-what is it and what is the health evidence? a systematic review focusing on mycoprotein[J].Frontiers in Sustainable Food Systems, 2021, 5:581682.
[16] 康定荣, 李明瑕, 张伟.一株间型脉胞菌菌株及其在替代蛋白中的应用:中国, CN116162554B[P].2023-07-28.KANG D R, LI M X, ZHANG W.A strain of mesocystis and its application in alternative proteins:China, CN116162554B[P].2023-07-28.
[17] COELHO M O C, MONTEYNE A J, DUNLOP M V, et al.Mycoprotein as a possible alternative source of dietary protein to support muscle and metabolic health[J].Nutrition Reviews, 2020, 78(6):486-497.
[18] 周凯, 李乔智, 胡新, 等.真菌蛋白模拟肉研究现状及未来展望[J].中国食品学报, 2023, 23(12):323-336.ZHOU K, LI Q Z, HU X, et al.Research status and future outlook of fungal protein based meat analogues[J].Journal of Chinese Institute of Food Science and Technology, 2023, 23(12):323-336.
[19] PULIGUNDLA P, MOK C, PARK S.Advances in the valorization of spent brewer’s yeast[J].Innovative Food Science &Emerging Technologies, 2020, 62:102350.
[20] FINNIGAN T J, WALL B T, WILDE P J, et al.Mycoprotein:The future of nutritious nonmeat protein, a symposium review[J].Current Developments in Nutrition, 2019, 3(6):nzz021.
[21] HASHEMPOUR-BALTORK F, HOSSEINI S M, ASSAREHZADEGAN M A, et al.Safety assays and nutritional values of mycoprotein produced by Fusarium venenatum IR372C from date waste as substrate[J].Journal of the Science of Food and Agriculture, 2020, 100(12):4433-4441.
[22] 胡文凯, 王艳丽, 彭镰心, 等.谷物膳食纤维和酚类物质结合对肠道健康影响的研究进展[J].保鲜与加工, 2024, 24(9):147-156.HU W K, WANG Y L, PENG L X, et al.Research progress on the effects of cereal dietary fiber and phenolic substances on gut health[J].Storage and Process, 2024, 24(9):147-156.
[23] BADEN M Y, LIU G, SATIJA A, et al.Changes in plant-based diet quality and total and cause-specific mortality[J].Circulation, 2019, 140(12):979-991.
[24] DERBYSHIRE E, AYOOB K T.Mycoprotein[J].Nutrition Today, 2019, 54(1):7-15.
[25] WILLIAMSON D A, GEISELMAN P J, LOVEJOY J, et al.Effects of consuming mycoprotein, tofu or chicken upon subsequent eating behaviour, hunger and safety[J].Appetite, 2006, 46(1):41-48.
[26] BOTTIN J H, SWANN J R, CROPP E, et al.Mycoprotein reduces energy intake and postprandial insulin release without altering glucagon-like peptide-1 and peptide tyrosine-tyrosine concentrations in healthy overweight and obese adults:A randomised-controlled trial[J].British Journal of Nutrition, 2016, 116(2):360-374.
[27] TURNBULL W, WALTON J, LEEDS A.Acute effects of mycoprotein on subsequent energy intake and appetite variables[J].The American Journal of Clinical Nutrition, 1993, 58(4):507-512.
[28] DUNLOP M V, KILROE S P, BOWTELL J L, et al.Mycoprotein represents a bioavailable and insulinotropic non-animal-derived dietary protein source:A dose-response study[J].British Journal of Nutrition, 2017, 118(9):673-685.
[29] TURNBULL W, WARD T.Mycoprotein reduces glycemia and insulinemia when taken with an oral-glucose-tolerance test[J].The American Journal of Clinical Nutrition, 1995, 61(1):135-140.
[30] COLOSIMO R, MULET-CABERO A I, WARREN F J, et al.Mycoprotein ingredient structure reduces lipolysis and binds bile salts during simulated gastrointestinal digestion[J].Food &Function, 2020, 11(12):10896-10906.
[31] TURNBULL W H, LEEDS A R, EDWARDS D G.Mycoprotein reduces blood lipids in free-living subjects[J].The American Journal of Clinical Nutrition, 1992, 55(2):415-419.
[32] COELHO M O C, MONTEYNE A J, DIRKS M L, et al.Daily mycoprotein consumption for 1 week does not affect insulin sensitivity or glycaemic control but modulates the plasma lipidome in healthy adults:A randomised controlled trial[J].British Journal of Nutrition, 2021, 125(2):147-160.
[33] MONTEYNE A J, COELHO M O, PORTER C, et al.Mycoprotein ingestion stimulates protein synthesis rates to a greater extent than milk protein in rested and exercised skeletal muscle of healthy young men:A randomized controlled trial[J].The American Journal of Clinical Nutrition, 2020, 112(2):318-333.
[34] WEST S, MONTEYNE A J, WHELEHAN G, et al.Ingestion of mycoprotein, pea protein, and their blend support comparable postexercise myofibrillar protein synthesis rates in resistance-trained individuals[J].American Journal of Physiology.Endocrinology and Metabolism, 2023, 325(3):E267-E279.
[35] MONTEYNE A J, COELHO M O, PORTER C, et al.Branched-chain amino acid fortification does not restore muscle protein synthesis rates following ingestion of lower- compared with higher-dose mycoprotein[J].The Journal of Nutrition, 2020, 150(11):2931-2941.
[36] WEST S, MONTEYNE A J, WHELEHAN G, et al.Mycoprotein ingestion within or without its wholefood matrix results in equivalent stimulation of myofibrillar protein synthesis rates in resting and exercised muscle of young men[J].British Journal of Nutrition, 2023, 130(1):20-32.
[37] COLOSIMO R, HARRIS H C, AHN-JARVIS J, et al.Colonic in vitro fermentation of mycoprotein promotes shifts in gut microbiota, with enrichment of Bacteroides species[J].Communications Biology, 2024, 7:272.
[38] FARSI D N, GALLEGOS J L, KOUTSIDIS G, et al.Substituting meat for mycoprotein reduces genotoxicity and increases the abundance of beneficial microbes in the gut:Mycomeat, a randomised crossover control trial[J].European Journal of Nutrition, 2023, 62(3):1479-1492.
[39] DEAN D, ROMBACH M, DE KONING W, et al.Understanding key factors influencing consumers’ willingness to try, buy, and pay a price premium for mycoproteins[J].Nutrients, 2022, 14(16):3292.
[40] CHEW N W S, NG C H, TAN D J H, et al.The global burden of metabolic disease:Data from 2000 to 2019[J].Cell Metabolism, 2023, 35(3):414-428.e3.
[41] WAN M L Y, LING K H, EL-NEZAMI H, et al.Influence of functional food components on gut health[J].Critical Reviews in Food Science and Nutrition, 2019, 59(12):1927-1936.
[42] YANG L, KANG X C, DONG W J, et al.Prebiotic properties of Ganoderma lucidum polysaccharides with special enrichment of Bacteroides ovatus and B.uniformis in vitro[J].Journal of Functional Foods, 2022, 92:105069.
[43] L PEZ-ALMELA I, ROMAN
PEZ-ALMELA I, ROMAN -PÉREZ M, BULLICH-VILARRUBIAS C, et al.Bacteroides uniformis combined with fiber amplifies metabolic and immune benefits in obese mice[J].Gut Microbes, 2021, 13(1):1-20.
-PÉREZ M, BULLICH-VILARRUBIAS C, et al.Bacteroides uniformis combined with fiber amplifies metabolic and immune benefits in obese mice[J].Gut Microbes, 2021, 13(1):1-20.
[44] SULYOK M, KRSKA R, SCHUHMACHER R.A liquid chromatography/tandem mass spectrometric multi-mycotoxin method for the quantification of 87 analytes and its application to semi-quantitative screening of moldy food samples[J].Analytical and Bioanalytical Chemistry, 2007, 389(5):1505-1523.
[45] KIM K, CHOI B, LEE I, et al.Bioproduction of mushroom mycelium of Agaricus bisporus by commercial submerged fermentation for the production of meat analogue[J].Journal of the Science of Food and Agriculture, 2011, 91(9):1561-1568.
[46] SCAIFE K, VO T D, DOMMELS Y, et al.In silico and in vitro safety assessment of a fungal biomass from Rhizomucor pusillus for use as a novel food ingredient[J].Food and Chemical Toxicology, 2023, 179:113972.
[47] 向霞, 朱恩恒, 韩楠玉.三种主要真菌毒素及其毒素降解酶的研究进展[J].生物技术通报, 2024, 40(1):45-56.XIANG X, ZHU E H, HAN N Y.Research progress in three major mycotoxins and their toxin-degrading enzymes[J].Biotechnology Bulletin, 2024, 40(1):45-56.
[48] KATONA S J, KAMINSKI E R.Sensitivity to Quorn mycoprotein (Fusarium venenatum) in a mould allergic patient[J].Journal of Clinical Pathology, 2002, 55(11):876-877.
[49] JACOBSON M F, DEPORTER J.Self-reported adverse reactions associated with mycoprotein (Quorn-brand) containing foods[J].Annals of Allergy, Asthma &Immunology, 2018, 120(6):626-630.
[50] BARTHOLOMAI B M, RUWE K M, THURSTON J, et al.Safety evaluation of Neurospora crassa mycoprotein for use as a novel meat alternative and enhancer[J].Food and Chemical Toxicology, 2022, 168:113342.
[51] SUN Y W, ZHANG P H, LI Y, et al.Association of sodium, potassium and sodium-to-potassium ratio with urine albumin excretion among the general Chinese population[J].Nutrients, 2021, 13(10):3456.
[52] HAVLIK J, PLACHY V, FERNANDEZ J, et al.Dietary purines in vegetarian meat analogues[J].Journal of the Science of Food and Agriculture, 2010, 90(14):2352-2357.
[53] 陈献忠, 沈微, 樊游, 等.后基因组时代的丝状真菌基因组学与代谢工程[J].遗传, 2011, 33(10):1067-1078.CHEN X Z, SHEN W, FAN Y, et al.Genomics and metabolic engineering of filamentous fungi in the post-genomics era[J].Hereditas, 2011, 33(10):1067-1078.
[54] 李德茂, 曾艳, 周桔, 等.生物制造食品原料市场准入政策比较及对我国的建议[J].中国科学院院刊, 2020, 35(8):1041-1052.LI D M, ZENG Y, ZHOU J, et al.Regulation and guidance for marketing of food ingredients from biomanufacturing and policy suggestions for China[J].Bulletin of Chinese Academy of Sciences, 2020, 35(8):1041-1052.
[55] NUTRITION, NDA A, TURCK D, et al.Guidance on the preparation and submission of an application for authorisation of a novel food in the context of regulation (EU) 2015/22831 (revision 1)2[J].EFSA Journal, 2021, 19(3):e06555.
[56] FDA.Generally Recognized as Safe (GRAS)[S].America:FDA, 2023.
[57] ONLINE S S.Singapore Food Agency Act 2019[J].Singapore Statutes Online, 2019.
[58] 龙伽雯, 李跃辉.新食品原料的审批及应用现状研究[J].食品与发酵工业, 2025, 51(8):394-404.LONG J W, LI Y H.Research on approval and application status of new food raw materials[J].Food and Fermentation Industries, 2025, 51(8):394-404.
[59] 何诗微, 杨波, 郭敏, 等.双歧杆菌对2′-FL和LNT的菌株特异性代谢探究[J].食品与发酵工业, 2025,51(24):314-321.HE S W, YANG B, GUO M, et al.Strain-specific metabolism of 2′-FL and LNT by bifidobacteria[J].Food and Fermentation Industries, 2025,51(24):314-321.
[60] 汪超, 夏路, 李兆丰, 等.微生物蛋白的关键生产技术体系与食品产业应用[J].中国工程科学, 2024, 26(2):121-131.WANG C, XIA L, LI Z F, et al.Key manufacturing technologies of microbial protein and its application in food industry[J].Strategic Study of CAE, 2024, 26(2):121-131.
[61] 陈洪雨, 令狐昌丽, 罗颖, 等.食用真菌蛋白制备及其应用研究进展[J].食用菌学报, 2021, 28(6):188-198.CHEN H Y, LINGHU C L, LUO Y, et al.Research progress on preparation and application of fungal protein[J].Acta Edulis Fungi, 2021, 28(6):188-198.