在过去数年间,高脂高糖高热量的西式膳食模式所引发的代谢健康危机,已成为实施“大健康”战略过程中面临的重大公共卫生挑战。此类营养失衡的饮食不仅易导致肥胖、胰岛素抵抗和脂代谢紊乱,研究还表明,它可通过降低海马区神经元树突棘密度、激活小胶质细胞炎症通路等机制,诱发空间记忆缺陷等不可逆神经损伤[1]。鉴于肠道菌群在代谢性认知障碍中发生的潜在作用,靶向微生物群的干预策略已成为热门的研究方向。通过特异性富集拟杆菌(Bacteroides)、乳酸杆菌(Lactobacillus)及普雷沃菌(Prevotella)等功能菌群,促产短链脂肪酸(short-chain fatty acids,SCFAs),通过循环系统穿透血脑屏障,调控中枢神经炎症与突触可塑性[2]。此外,具有抑炎功效的益生菌补充剂(如Prevotella),被证实可通过抑制TLR4/MyD88等炎症相关信号轴的方式,显著降低阿尔茨海默病模型海马区Aβ斑块沉积密度,为代谢性认知障碍干预开辟了多靶点调控的新范式[3]。
后生元,即“对宿主健康有益的无活性微生物和/或其成分的制剂”,因其良好的加工稳定性、贮藏稳定性及安全性成为研究热点。现有研究表明,后生元在肥胖防控、炎症调节、肿瘤抑制等方面具有显著功效[4-5]。罗伊氏粘液乳杆菌因其显著的抑炎活性、肠道菌群调节功能及免疫增强特性而备受关注[6-7]。前期研究发现源自健康人粪便的罗伊氏粘液乳杆菌WX-94(Lactobacillus reuteri WX-94)具有健康效应,以益生元为发酵底物可进一步改善其代谢谱,促产吲哚乳酸、吲哚丙酸、苯乳酸等有益代谢物,显著增强其抗氧化能力[4-5,8]。然而,活菌制剂在产业化加工中面临热稳定性差、贮存条件严苛、肠道定殖程度波动大等诸多技术瓶颈,严重制约其产业化应用。
黄精(Polygonatum kingianum Coll.et Hemsl.)是我国著名的药食同源植物,《本草纲目》载其“补诸虚、填精髓”。现代药理学研究揭示,黄精粉末、不同极性提取物及多糖均具有显著的健康保护作用。其中,黄精多糖(Polygonatum kingianum polysaccharides, PKP)作为黄精核心活性成分,可通过多种途径发挥抗氧化、免疫调节、抗炎及神经递质调控等生理功能[9-11]。先前研究结果揭示,PKP为杂多糖,具有多糖的羟基和烷基特征,主链可能是葡萄糖、甘露糖通过β-(1→2)、(1→4)、(1→6)等糖苷键连接的吡喃酰基单元,支链常含有半乳糖和阿拉伯糖。这种复杂结构是其抗氧化活性的来源,也是作为有益菌碳源的基础[11]。其余研究中值得注意的是,黄精多糖在血管性痴呆、东莨菪碱诱导认知障碍、自然衰老记忆损伤等多种认知损伤模型中均表现出显著的认知改善功效[12-13]。
本研究创新性地以PKP与L.reuteri共培养制备后生元,通过整合生理生化指标、行为学、组织病理学、分子生物学和微生物组学分析,系统解析其对长期高脂高蔗糖(high-fat-high-sugar, HFHS)饮食诱导的大鼠认知功能障碍的改善作用及机制,为开发兼具代谢调节与神经保护功能的后生元营养干预策略提供理论依据。
1 材料与方法
1.1 材料与试剂
本研究采用L. reuteri WX-94,深圳华大应用农业研究所,细菌菌落总数1×1010CFU/g。
总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、血清低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)、肿瘤坏死因子-α(tumor necrosis factor,TNF-α)、白介素-10(interleukin-10,IL-10)、白介素-6(interleukin-6,IL-6)、白介素-1β(interleukin-1β,IL-1β)、脂多糖(lipopolysaccharide,LPS)、超氧化物歧化酶(superoxide dismutase,SOD)、还原型谷胱甘肽(glutathione,GSH)、丙二醛(malondialdehyde,MDA)、酶联免疫吸附分析(enzyme linked immunosorbent assay,ELISA)试剂盒,南京建成生物工程研究所;Trizol、逆转录、PCR试剂盒及引物,武汉爱博泰克生物科技有限公司;德氏乳杆菌保加利亚亚种用MRS培养基、MRS无糖培养基,青岛海博生物技术有限公司。
1.2 仪器与设备
高压灭菌锅,浙江新丰医疗器械有限公司;KEMaze 动物行为轨迹分析系统,南京卡尔文生物科技有限公司;JA2003 电子分析天平,上海精密科学仪器有限公司;高速冷冻离心机,德国 SIGMA 公司;倒置荧光显微镜,日本尼康;梯度PCR仪,德国Eppendorf;BioDrop 超微量分光光度计,上海奥然科贸有限公司;CFX96 荧光实时定量PCR仪,山东风途物联网科技有限公司;Thermo 全波长酶标仪,美国Thermo公司;厌氧工作站 IPAN A610,上海磐麦科技有限公司;旋涡振荡器,无锡沃信仪器公司。
1.3 实验方法
1.3.1 样本制备
取15 g滇黄精粉末(过200目筛)按1∶10(g∶mL)料液比加入体积分数95%乙醇,于80 ℃提取1 h。残渣用120 mL蒸馏水回流提取1 h,滤液在60 ℃下减压浓缩。浓缩液用体积分数80%乙醇于4 ℃沉淀24 h,随后通过活性炭和Sevage试剂(氯仿与正丁醇按体积比5∶1混合)进行纯化,获得粗多糖PKP并冷冻干燥[13]。采用高效凝胶渗透色谱法测定PKP分子量,通过高效液相色谱分析其单糖组成。结果表明,PKP呈现3个洗脱峰:其重均分子量(Mw)分别为297.81、32.3、24.51 kDa(对数分子量拟合方程:Log Mw=-0.192 3x+12.115,R2=0.993);峰位分子量(Mp)分别为208.78、31.23、23.54 kDa(拟合方程:y=-0.222x+11.34,R2=0.995)。组分分析显示,PKP主要由半乳糖(46.55%)、葡萄糖(16.82%)、甘露糖(1.89%)和阿拉伯糖(0.66%)以摩尔百分比构成。经鉴定,PKP主要由半乳糖(49.01%)、葡萄糖(17.25%)、甘露糖(1.93%)和阿拉伯糖(0.60%)组成[4,13]。
将L.reuteri活化后分别接种至MRS液体培养基或含50 g/L PKP的无糖MRS液体培养基中,放置于厌氧工作站实现厌氧发酵,待菌株发酵达到稳定期后(24 h,1×108 CFU/mL),将发酵液在6 000 r/min,4 ℃条件下离心20 min,取离心后的上清液于60 ℃巴氏杀菌30 min,即可获得以MRS培养基制备的后生元(MRS-L.reuteri)和以PKP为碳源制备的后生元(PKP- L.reuteri)。此外,称取50 g/L PKP及1×108 CFU/mL 的L.reuteri WX-94活菌,用蒸馏水溶解并旋涡混匀即可得到合生元(PKP+L.reuteri)。
1.3.2 动物实验方案
50只6周龄SPF级健康雄性SD大鼠[体质量(200±10) g]购自北京维通利华实验动物有限公司,许可证号SCXK(京)2021-0006。本实验严格遵守陕西师范大学《实验动物管理条例》相关规定(陕西师范大学学术委员会伦理号No.202416040)。实验动物饲养在陕西师范大学动物实验中心,饲养环境光照/黑暗12 h交替,温度保持在(22±2)℃,相对湿度(60±5)%,自由摄取食物和水。
大鼠适应性喂养1周后,如图1-a所示随机分为5组,每组10只,分别为正常对照组(NC组)、模型组(20%高脂饲料,10%蔗糖水喂养)、PKP+L.reuteri(HFHS饮食并灌胃PKP+L.reuteri)、PKP-L.reuteri(HFHS饮食并灌胃PKP-L.reuteri)、MRS-L.reuteri(HFHS饮食并灌胃MRS-L.reuteri)。按大鼠体质量确定干预药物量,给药体积约为0.1 mL/10 g,每天1次给药,共计干预8周,记录各组大鼠初始体质量和处死前体质量,计算体质量增长量。
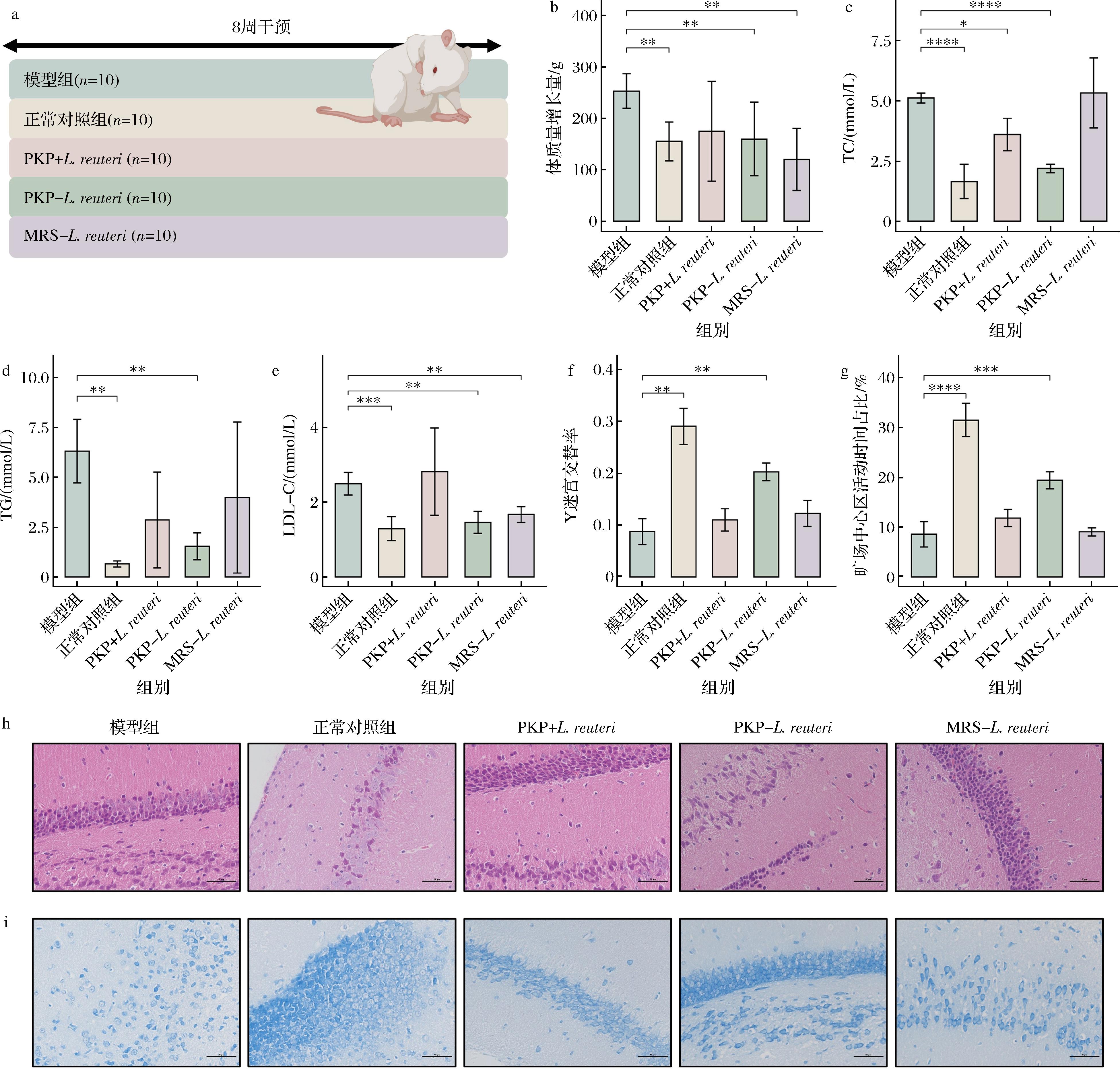
a-实验设计图;b-体质量增长量;c-血清TC水平;d-血清TG水平;e-血清LDL-C水平;f-Y迷宫自发交替率;g-旷场中心区域活动时间;h-海马体HE染色;i-海马体尼氏体染色
图1 PKP-L.reuteri缓解HFHS喂养大鼠体质量增加、改善大鼠认知功能障碍
Fig.1 PKP-L.reuteri attenuated body mass gain and improved cognitive dysfunction in HFHS diet-fed rats
注:*表示统计学上差异显著(P<0.05),**表示统计学上差异高度显著(P<0.01),***表示统计学上差异极显著(P<0.001),****表示统计学上具有极高的显著性(P<0.000 1)(下同)。
1.3.3 血生化指标测定
根据ELISA试剂盒说明书进行操作,定量检测大鼠血清中TC、TG以及LDL-C含量。
1.3.4 行为学实验
分别采用旷场实验和Y迷宫自发交替实验评估大鼠的自主活动水平、短期记忆和空间工作记忆[14]。实验开始前将待测大鼠放置于实验场地中适应环境,测试前及测试间隔需使用酒精清理排泄物以消除气味干扰。旷场实验测定时将大鼠放入周壁为黑色,长宽高均为100 cm的敞箱中,使其自由探索5 min,由KEMaze软件监测大鼠的行动轨迹和总路程,中心区域停留时间占比用来评价大鼠的自主活动能力。Y迷宫由3个完全相同,臂间夹角为120°的机械臂组成。实验开始时将大鼠放入三臂交汇处,使其自由探索迷宫5 min,记录大鼠的进臂次数。连续3次进入不同臂,记为1次正确自发交替,自发交替率计算如公式(1)所示:
自发交替率![]()
(1)
1.3.5 海马切片病理学观察
大鼠脑组织存放于4%(体积分数)多聚甲醛溶液中,随后进行石蜡包埋和切片处理,参考LIU等[15]的方法分别采用苏木精-伊红(hematoxylin and eosin,H&E)染色和尼氏(Nissl)染色法评估大鼠海马组织病理损伤情况和尼氏体数量,通过光学显微镜观察海马组织病理学变化。
1.3.6 脑组织炎症因子及mRNA表达测定
取适量大鼠海马组织样本,按照ELISA试剂盒检测海马中TNF-α、IL-10、IL-6、IL-1β、LPS、SOD、GSH和MDA含量。使用Trizol试剂盒提取海马组织总RNA,按照逆转录试剂盒操作步骤合成cDNA,以cDNA为模板参照试剂盒说明书进行RT-qPCR。以β-actin作为内参基因,使用实时荧光定量PCR仪器检测TLR4、NLRP3、MyD88和BDNF基因的相对转录水平,引物序列见表1。
表1 RT-qPCR引物序列
Table 1 Sequence of primers used in RT-qPCR
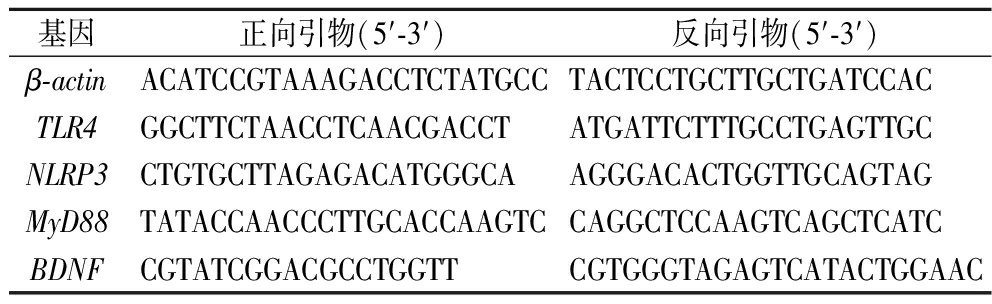
基因正向引物(5′-3′)反向引物(5′-3′)β-actinACATCCGTAAAGACCTCTATGCCTACTCCTGCTTGCTGATCCACTLR4GGCTTCTAACCTCAACGACCTATGATTCTTTGCCTGAGTTGCNLRP3CTGTGCTTAGAGACATGGGCAAGGGACACTGGTTGCAGTAGMyD88TATACCAACCCTTGCACCAAGTCCAGGCTCCAAGTCAGCTCATCBDNFCGTATCGGACGCCTGGTTCGTGGGTAGAGTCATACTGGAAC
1.3.7 肠道菌群16S rRNA高通量测序
采用16S rRNA基因测序技术分析大鼠肠道菌群和微生物群落结构的多样性。提取大鼠粪便中的总DNA,对DNA的质量和浓度进行测定并构建高通量测序文库,以细菌基因组为模板利用高保真酶扩增16S rDNA的V3~V4区,引物为V3F:5′-ACTCCTA-CGGGAGGCAGCA-3′;V4R:5′-GGACTACHVGGGTWTCTAAT-3′, 肠道菌群测序工作由美吉生物科技有限公司进行,采用α多样性指数(Shannon指数,Observed指数,Simpson指数以及Chao1指数)和主坐标分析(principal coordinates analysis,PCoA)研究肠道微生物群丰度和多样性的种群差异,肠道菌群中性模型参考CHENG等[16]的方法以评估肠道细菌的稳态与平衡。
1.4 数据统计与分析
实验结果以“平均值±标准差”的方式表示,组间均值比较采用ANOVA 方差分析进行数据统计,P<0.05 认为差异具有统计学意义。采用R软件(v3.3.2)软件作图,运用SPSS 22.0 软件进行相关性分析,将被PKP-L.reuteri显著调控的菌群与生化指标之间建立相关性*P<0.05,**P<0.01,***P<0.001,****P<0.000 1。
2 结果与分析
2.1 PKP-L.reuteri缓解HFHS喂养大鼠体质量增加、脂代谢紊乱、改善大鼠认知功能障碍
如图1-b~图1-e所示,在为期8周的饲养中,相较于NC组,HFHS喂养的大鼠体质量显著增加了63%(P<0.01),其TC水平升高至正常对照组的3.1倍(P<0.000 1),TG水平升高至9.6倍(P<0.01),LDL-C水平显著升高93%(P<0.001)。与HFHS模型组相比,PKP+L. reuteri与PKP-L. reuteri干预均能显著降低大鼠的TC(P<0.05,P<0.000 1)和TG水平(P<0.01,P<0.01),且后者的降脂效果更为显著。具体而言,PKP+L. reuteri组TC和TG水平分别降低30%和55%,而PKP-L. reuteri组的降低幅度更大,TC和TG水平分别显著降低57%和76%。MRS-L. reuteri组并没有表现出显著的脂代谢紊乱功效(P>0.05)。与NC组相比,HFHS组大鼠的自主活动水平及短期记忆和空间工作记忆能力显著降低,大鼠的旷场中心区停留时间占比降低了70%(P<0.000 1),Y迷宫交替率降低了73%(P<0.01),而PKP-L. reuteri组的大鼠的旷场中心区停留时间占比与Y迷宫交替率相较模型组分别提高了131%(P<0.001)和126%(P<0.01),表明PKP-L. reuteri可有效缓解高脂高糖饮食引发的认知障碍,且效果优于PKP+L. reuteri和MRS-L. reuteri(图1-f~图1-g)。
2.2 PKP-L.reuteri对HFHS饮食致认知障碍的大鼠海马组织的影响
因HFHS饮食造成的全身性炎症积累、血脑屏障损伤、海马体炎症浸润以及尼氏体萎缩是饮食诱导神经炎症的主要机制[17]。本研究通过海马体HE染色与尼氏体染色实验进一步探究PKP-L.reuteri对HFHS饮食大鼠的海马炎症浸润修复以及尼氏体保护功效。如图1-h、图1-i所示,正常对照组海马组织神经元细胞结构完整,排列规整紧密,核质界限清晰,未见明显炎性浸润,尼氏体分布均匀且结构完整。而HFHS大鼠的脑组织神经元胞体固缩,细胞核、质分界不清,可见纤维细胞增生,炎性细胞浸润,尼氏体衰退严重且结构模糊。经PKP-L.reuteri干预,上述病理变化可得到显著改善,表现为神经元细胞完整性恢复,炎症浸润减轻和尼氏体数量显著增加,而PKP+L.reuteri以及MRS-L.reuteri均未呈现出显著的改善效果。
2.3 PKP-L.reuteri改善HFHS饮食导致的神经炎症及氧化应激损伤
海马体炎症浸润与神经炎症反应是造成认知功能衰退的重要诱因,在众多的炎症因子中,TNF-α作为炎症反应的标志物,可透过血脑屏障进入脑区,上调小胶质细胞miR-342表达,进而激活NF-κB信号通路,最终引发炎症因子级联释放,从而加重脑损伤[18-19]。IL-6作为一种多效性细胞炎症因子,可通过反式信号传导与可溶性IL-6受体结合从而介导炎症反应,加剧认知功能损伤。如图2所示, PKP-L.reuteri组和PKP+L.reuteri组的大鼠的TNF-α和IL-6表达水平有所下降(P<0.05),其中PKP-L.reuteri组效果最为显著。此外,与模型组相比,PKP-L.reuteri组大鼠的IL-1β水平降低了40%(图2-c,P<0.01),同时IL-10水平显著升高至200%(图2-d,P<0.000 1)。
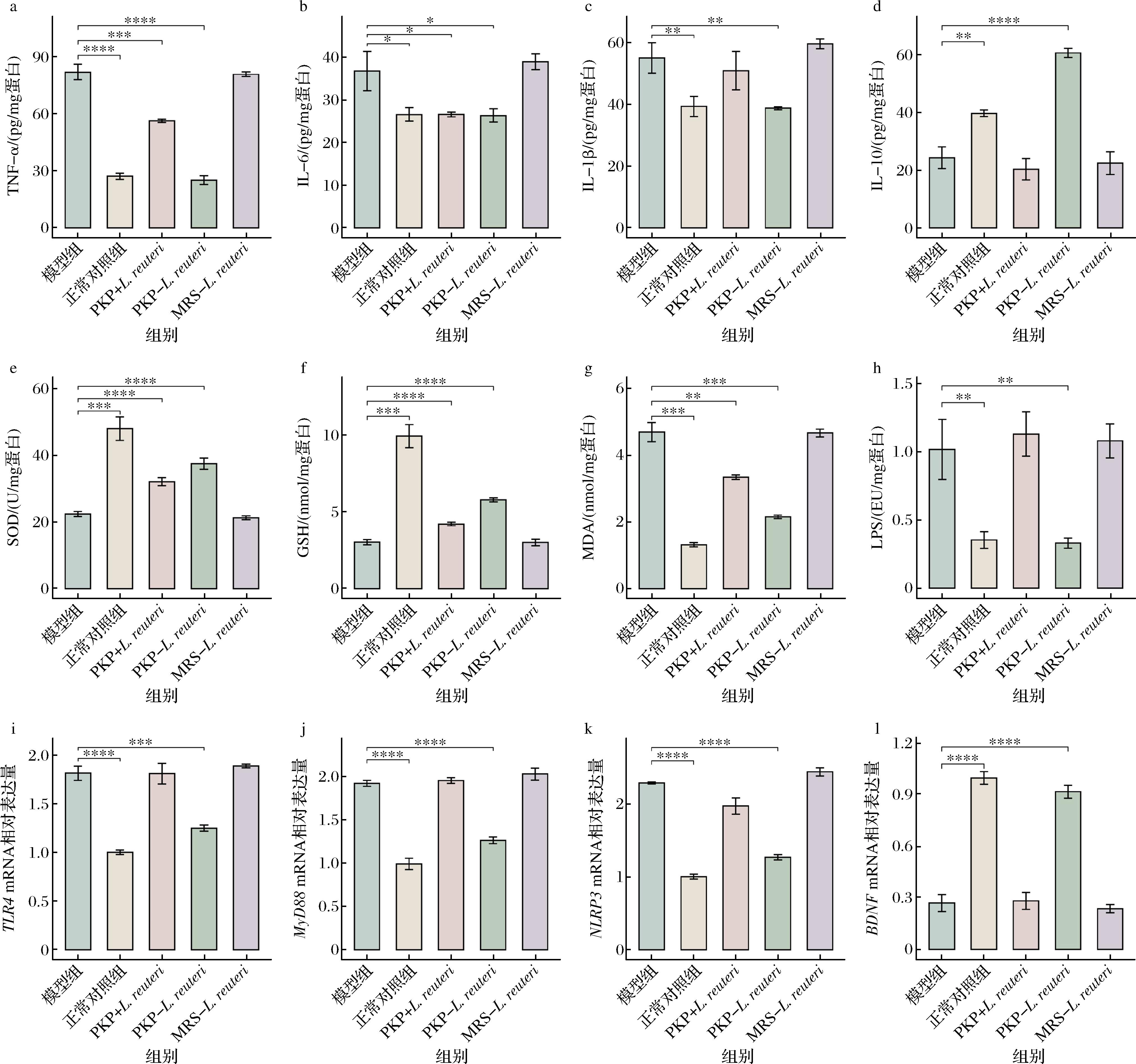
a-TNF-α含量;b-IL-6含量;c-IL-1β含量;d-IL-10含量;e-SOD活性;f-GSH含量;g-MDA含量;h-LPS含量;i-TLR4 mRNA相对表达量;j-MyD88 mRNA相对表达量;k-NLRP3 mRNA相对表达量;l- BDNF mRNA相对表达量
图2 PKP-L.reuteri抑制HFHS饮食导致的神经炎症及氧化应激损伤
Fig.2 PKP-L.reuteri suppressed neuroinflammation and attenuated oxidative stress damage induced by a high-fat and high-sucrose diet
LPS易位是高脂饮食诱导的主要肠道代谢紊乱指标之一。通过激活TLR4/NF-κB信号通路,LPS易位可诱发剧烈的神经炎症反应,促使IL-6等炎症因子大量分泌,进而降低突触可塑性,最终导致认知障碍发生[20]。此外,NF-κB还是炎症反应的核心调控节点,参与炎症介质的调控、炎症因子的产生和NLRP3炎症小体的激活。在中枢神经系统中,抑制NF-κB通路可有效缓解TNF-α和IL-6介导的神经炎症性疾病,而NF-κB磷酸化则会促进炎症因子的产生和释放,从而加剧认知功能损伤[21]。本研究发现,模型组大鼠海马区LPS表达量显著提升至NC组的2.6倍,而PKP-L.reuteri组大鼠LPS表达量与NC组一致,表现出明显的恢复功效。而PKP+L.reuteri组与MRS-L.reuteri组未见显著改善效果(图2-h)。
认知功能损伤常伴有神经兴奋性毒性、氧化应激与细胞凋亡等过程,这些过程会加剧脑组织损伤,并导致大量的细胞氧化自由基的积累。SOD和GSH能够清除内源性氧化自由基以减轻氧化损伤,故其活性水平可作为评估机体自由基清除能力的关键指标[22]。图2-e、图2-f表明,PKP-L.reuteri组大鼠的SOD活性及GSH含量相比于模型组显著提升,分别提升了91%(P<0.000 1)和67%(P<0.000 1)。MDA作为脂质氧化反应的代谢产物,其含量可有效反映细胞的损伤程度[23]。相比于模型组,PKP-L.reuteri组大鼠海马体中的MDA含量显著降低了54%(图2-g,P<0.001)。
综上,PKP-L.reuteri能显著改善HFHS饮食导致的海马体神经炎症、神经性毒性及氧化应激水平。
2.4 PKP-L.reuteri抑制TLR4/NLRP3/MyD88信号通路改善脑源性神经营养因子
抑郁症患者海马组织中炎症因子与海马小胶质细胞膜上的TLR4结合,进而募集下游的信号蛋白MyD88,形成TLR4-MyD88复合体,驱动炎症免疫相关基因转录,促进炎症因子分泌,完成炎症信号传递。此过程促进神经毒性A1型星形胶质细胞的形成,诱发抑郁样行为和海马神经元细胞损伤[19]。图2-i~图2-l表明,相较于正常对照组,模型组大鼠海马体中TLR4、NLRP3、MyD88 mRNA表达显著上调,分别上调81%(P<0.000 1),94%(P<0.000 1)和128%(P<0.000 1),同时脑源性神经营养因子(BDNF)的mRNA表达降低73%(P<0.000 1),而PKP-L.reuteri干预可显著恢复上述基因表达异常并使其恢复至接近正常水平,这表明PKP-L.reuteri可能通过抑制TLR4/NLRP3/MyD88信号通路的过度激活,抑制促炎因子产生,恢复BDNF表达,最终改善HFHS饮食导致的大鼠神经毒性作用。
2.5 PKP-L.reuteri重塑肠道菌群并提升SCFAs含量
肠道菌群作为体内多条代谢途径的枢纽,已成为膳食干预的重要研究靶点。随着“肠-脑轴”机制研究的深入,恢复“肠-脑轴”功能稳态有望成为改善肥胖相关认知障碍的潜在靶点[24-25]。相关研究表明,PKP可以调节肠道微生物群的平衡并促进肠道中SCFAs的产生,还能够提高罗伊氏粘液乳杆菌代谢物丰度,这些代谢物的生物靶点多与炎症和脂质调控有关,可以改善认知障碍和肥胖问题[4,11]。
本研究首先通过PCoA评估组间肠道微生物群组成的相似性和差异性,结果表明模型组与正常对照组的肠道菌群结构形成显著差异(图3-a),PKP-L.reuteri组与模型组形成显著差异且在PC1维度趋同于正常组,其中f_Lactobacillaceae、g_Prevotella、c_clostridia是造成组间差异的主要贡献菌群(图3-b)。
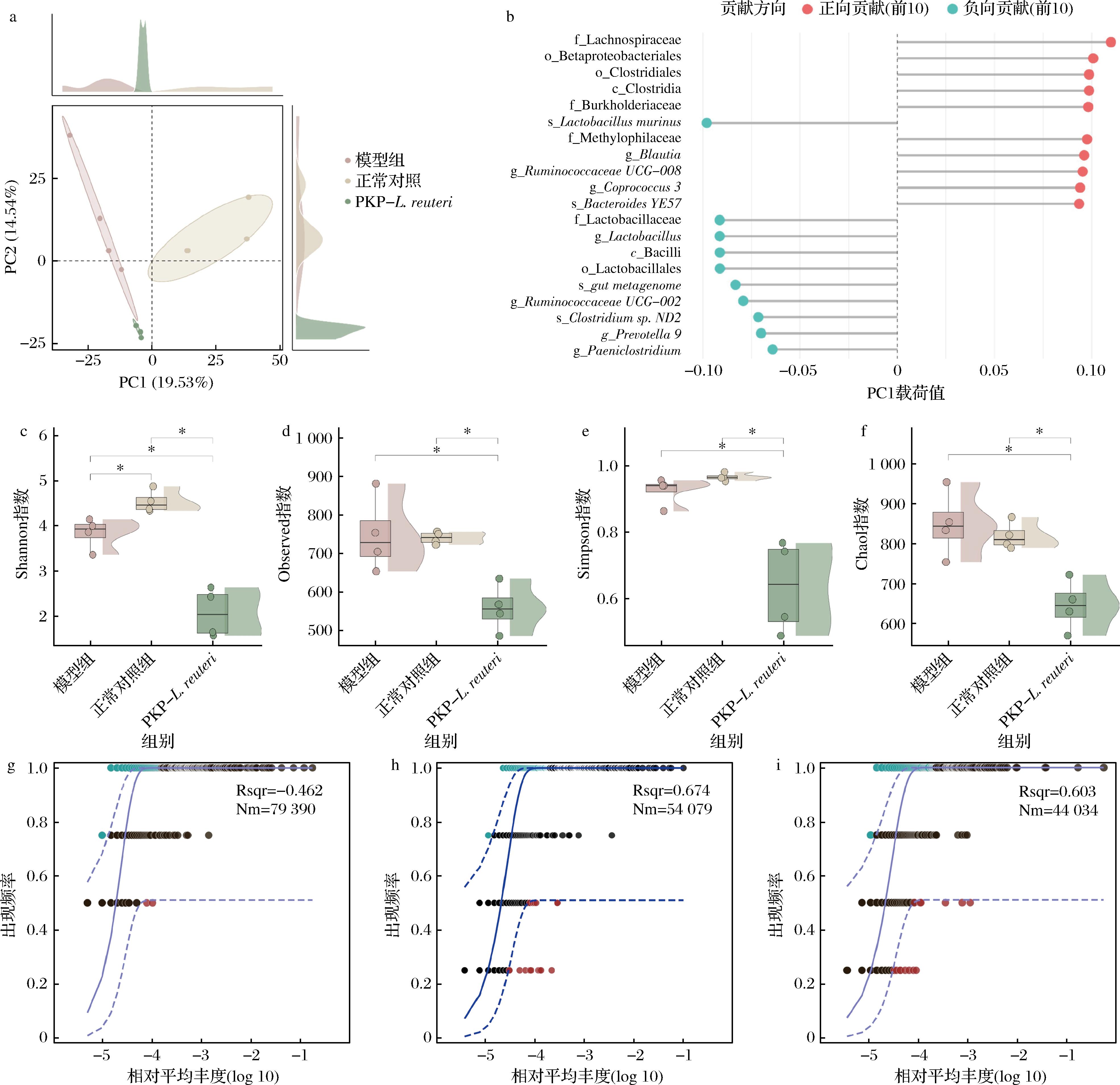
a-肠道菌群PCoA结果;b-肠道菌群贡献度;c-Shannon指数;d-Observed指数;e-Simpson指数;f-Chao1指数;g-HFHS组大鼠肠道菌群中性模型;h-对照组大鼠肠道菌群中性模型;i-PKP-L.reuteri组大鼠肠道菌群中性模型
图3 PKP-L.reuteri缓解HFHS饮食大鼠肠道菌群失调
Fig.3 PKP-L.reuteri alleviated gut dysbiosis in HFHS diet rats
α-多样性是评估微生物群落丰度和多样性的关键指标,研究发现PKP-L.reuteri组表现出独特的调节特性:Shannon、Simpson、Observed及Chao1指数均显著降低(图3-c~图3-f),而模型组与NC组间未见显著差异。中性群落模型(neutral community model,NCM)是基于中性理论的数学公式,通过随机过程来预测物种丰度分布,用以解释生态系统中物种多样性和分布格局,其拟合度表明微生物符合随机分布的程度[26]。结果表明,模型组相比于正常对照组出现明显混杂(图3-g),其拟合度低于正常对照组(图3-h),而经PKP-L.reuteri干预后,物种分布趋向于恢复至接近中性预期,拟合度显著提高(图3-i)。
螺杆菌科(f_Helicobacteraceae)感染是心脑血管疾病的独立危险因素,能够诱发多种炎症反应,破坏血脑屏障并导致脑神经元细胞坏死,从而增加阿尔茨海默病等神经退行性疾病的发病率[12]。此外,一项孟德尔随机化研究从基因因果效应层面进一步证实了螺杆菌科丰度与帕金森等脑部疾病存在显著因果关系,明确螺杆菌科作为“肠-脑轴”认知干预策略的重要潜在靶点[27]。图4-a~图4-c表明,模型组中螺杆菌科、颤螺菌属(g_Oscillospira)及螺杆菌属(g_Helicobacter)等条件致病菌的相对丰度显著升高,分别升高至正常对照组的4.8倍(P<0.01),2.9倍(P<0.05),3.2倍(P<0.01),而PKP- L.reuteri显著降低了以上有害菌群的丰度,相对于模型组分别降低了96%(P<0.01),89%(P<0.01)和87%(P<0.001),表明PKP-L.reuteri可有效抑制潜在神经毒性菌群的增殖,且为解释其特异性降低菌群多样性提供了机制线索。
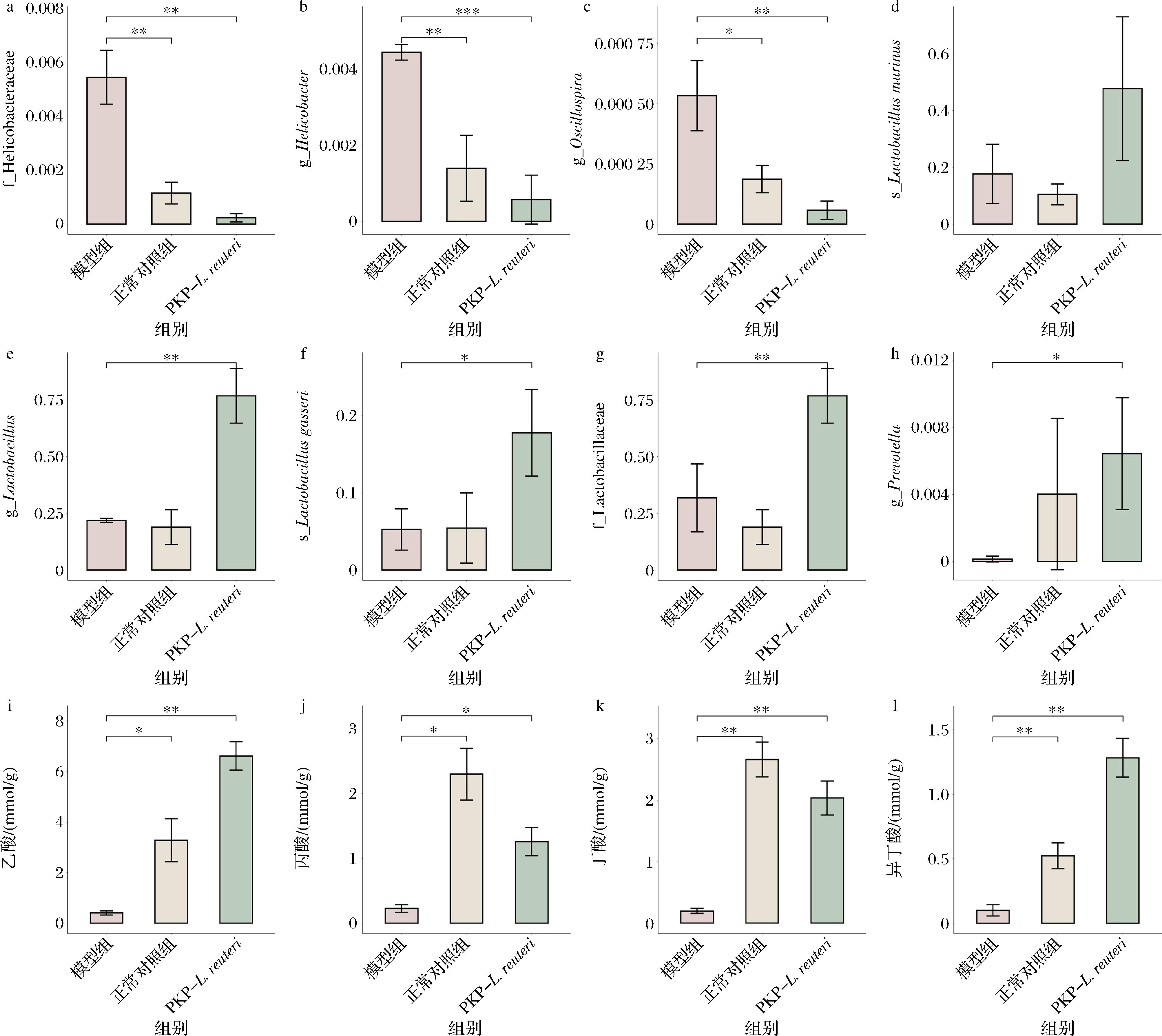
a-f_Helicobacteraceae丰度;b-g_Helicobacter丰度;c-g_Oscillospira丰度;d-s_Lactobacillus murinus丰度;e-g_Lactobacillus丰度;f-s_Lactobacillus gasseri丰度;g-f_Lactobacillaceae丰度;h-g_Prevotella丰度;i-乙酸丰度;j-丙酸丰度;k-丁酸丰度;l-异丁酸丰度
图4 PKP-L.reuteri重塑HFHS饮食大鼠肠稳态激活肠-脑轴协同
Fig.4 PKP-L.reuteri restored intestinal homeostasis and activated the gut-brain axis in HFHS diet rats
此外,PKP-L.reuteri干预显著提升了乳杆菌科(f_Lactobacillaceae)、乳杆菌属(g_Lactobacillus)、普雷沃菌属(g_Prevotella)及格氏乳杆菌(s_Lactobacillus gasseri)的相对丰度,分别提高至模型组的2.4倍(P<0.01),3.5倍(P<0.01),45.4倍(P<0.05)和3.4倍(P<0.05)(图4-d~图4-h)。普雷沃菌与乳杆菌皆为益生菌,具有调节脂代谢、恢复肠屏障及改善认知功能等作用,其中格氏乳杆菌能够改善宿主肠道微生态平衡,促进有益菌定植,并通过产生有益代谢物促进宿主的脂代谢功能[28]。普雷沃氏菌可通过调控TLR4/MyD88通路抑制炎症因子产生,进而促进脑部神经功能并上调BDNF表达[29]。图4-i~图4-l表明,模型组粪便中乙酸、丁酸、丙酸及异丁酸含量较正常对照组显著降低,而PKP-L.reuteri干预能显著恢复SCFAs水平。
如图5-a所示,普雷沃菌属(Prevotella)、乳杆菌科(Lactobacillaceae)的丰度与短链脂肪酸(如丁酸)水平呈显著正相关(r≥0.5,P<0.05);而螺杆菌科(Helicobacteraceae)等条件致病菌则与血清促炎因子(TNF-α、IL-6)及海马TLR4/MyD88信号通路关键分子的表达呈强正相关(r>0.5,P<0.05)。此外,普雷沃菌属(Prevotella)的丰度与抗氧化指标(SOD、GSH)显著正相关,而与脂代谢紊乱标志物(总胆固醇、LDL-C)呈负相关。这些结果进一步支持PKP-L. reuteri可能通过富集功能有益菌,同步改善氧化应激与脂代谢紊乱,从而发挥协同保护作用(图5-b)。进一步相关分析还表明,丁酸和丙酸水平与海马区NLRP3炎症小体表达呈显著负相关。
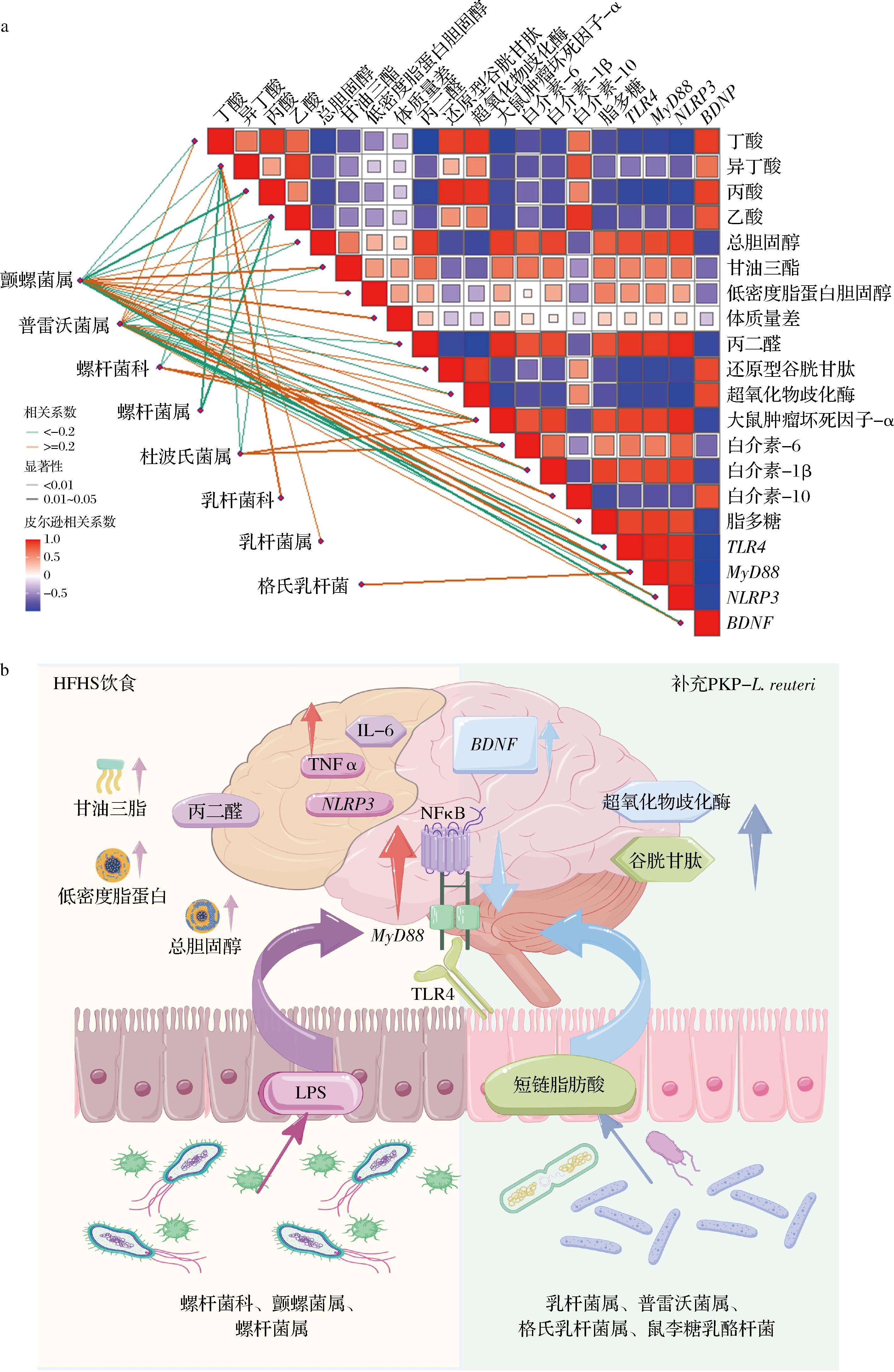
a-相关性分析;b-PKP重塑HFHS诱导认知障碍机制图
图5 基于皮尔逊相关矩阵的肠-脑轴多靶点互作分析
Fig.5 Multi-target interaction analysis of the gut-brain axis based on Pearson correlation matrix
相较于MRS 与L.reuteri 的共培养物,PKP 与L.reuteri共培养物中提取的上清液中的有益代谢物明显更高,其中的丁二酸等代谢物被证实具有维持厌氧环境的作用,有利于厌氧菌生长,可以富集乳杆菌科、乳杆菌属等功能有益菌,并抑制螺杆菌科等条件致病菌[4,11]。同时这些代谢物被厚壁菌门等肠道菌群利用后可代谢转化为丁酸、丙酸等SCFAs,并通过脂质转运突破血脑屏障,最终促进突触基因表达,抑制NF-κB通路,进而改善认知障碍。此外,在抑制TLR4/NLRP3/MyD88信号通路机制上,普雷沃菌属和PKP-L.reuteri具有协同作用。结果显示,普雷沃菌属和PKP-L.reuteri可抑制TLR4/NLRP3/MyD88 mRNA表达,从而可减少TLR4-MyD88复合体形成,抑制炎症免疫相关基因转录,进而减少神经促炎因子分泌,改善神经炎症,缓解认知障碍[29]。
3 讨论与结论
HFHS的西式饮食是肥胖及相关代谢性疾病的主要风险因素,其不仅直接诱发代谢紊乱,还可通过破坏激素稳态加剧认知功能损伤,而海马体与前额皮质依赖的学习记忆功能对此类损伤尤为敏感[30-31]。近年来,靶向“肠-脑轴”的微生态干预策略,如益生菌、益生元与合生元,在改善认知障碍方面展现出潜力。例如,ZHU等[32]报道短双歧杆菌HNXY26M4可通过增加Akkermansia、Lachnoclostridium等的相对丰度,促产SCFAs,改善APP/PS1小鼠的认知障碍、神经炎症和脑氧化损伤。CHUNCHAI等[33]研究发现,含有副干酪乳酪杆菌HII01和低聚木糖的合生元制剂可以通过肠-脑轴减轻海马炎症、改善小胶质细胞激活、增加树突棘密度,从而改善高脂饮食导致的大鼠海马发育障碍和脑线粒体功能障碍。尽管益生元、益生菌和合生元具有潜在的治疗益处,但在稳定性、个体反应的可变性和安全性等方面存在局限性[34]。而后生元主要由微生物代谢物、菌体成分等对宿主有利的活性物质组成,因其能够直接调节神经炎症和免疫反应,稳定安全的特性成为研究重点。
在各类益生元中,天然多糖因其显著的神经保护活性备受关注。杜仲、沙棘、枸杞等来源的多糖已被证实可缓解高热量饮食引起的神经炎症与认知衰退[35-37]。黄精的主要活性成分多糖在调节免疫、抗氧化、降血糖及改善认知功能方面具有明确功效。许云聪等[38]发现PKP可通过调控PPARα/UCP1通路促进脂肪分解,改善肥胖小鼠的脂代谢紊乱与脑功能损伤;LIU[39]等与LUO[12]等的研究进一步表明,PKP能有效缓解衰老及阿尔茨海默病模型小鼠的氧化应激、突触丢失及Aβ病理沉积,这些发现为本研究提供了重要的理论支持。
本研究将PKP与一株源自健康人粪便、具有显著抗炎效果的L.reuteri WX-94结合,制备新型后生元PKP-L.reuteri,并系统比较其与合生元(PKP+L.reuteri)及未添加PKP培养基制备的后生元MRS-L.reuteri的干预效果。结果表明,PKP-L.reuteri在改善HFHS饮食诱导的脂代谢紊乱、认知功能下降、海马组织病理损伤、神经炎症及氧化应激方面均表现出更全面的优势。前期研究显示,PKP不仅能作为碳源促进L.reuteri增殖,还可特异性诱导其产生吲哚乳酸、吲哚丙酸、苯乳酸等具有抗炎与抗氧化活性的代谢物[40],这可能是PKP增强后生元认知保护作用的关键物质基础。
TLR4作为天然免疫的关键受体,其激活会启动下游MyD88依赖性信号转导,进而触发海马组织NLRP3炎症小体的组装与活化,导致促炎细胞因子(如IL-1β、IL-18)的成熟与释放,诱发神经炎症。SCFAs,尤其是丁酸和丙酸,已被证实是G蛋白偶联受体(G protein-coupled receptors,GPCRs,如GPR41、GPR43、GPR109a)的激动剂,可以通过激活海马神经元特定GPCRs,干扰TLR4的寡聚化或内化,从而在源头上阻断其与MyD88的结合,抑制下游炎症信号的启动[41]。研究发现,PKP-L.reuteri调控肠道菌群结构,促进普雷沃菌属等产SCFAs功能菌的丰度,有效提升了小鼠体内丁酸与丙酸丰度,抑制海马区内TLR4/MyD88/NLRP3炎症通路基因表达。进一步地,TLR4/MyD88信号通路的被抑制,阻碍了NLRP3炎症小体的组装与活化,最终减少促炎细胞因子的释放,为关键神经营养因子BDNF的表达上调创造了有利条件。这些发现强烈提示PKP-L.reuteri神经保护作用是通过“菌群-SCFAs-脑轴”介导的。尽管本研究在基因转录水平上获得了TLR4/MyD88/NLRP3通路被抑制及BDNF表达上调的一致证据,但缺乏蛋白水平的验证确实是本研究的一个局限性。
综上所述,本研究证实了PKP-L.reuteri在干预HFHS诱发认知障碍中的显著效果,更从“菌群-代谢物-脑”轴角度阐明了PKP通过调控菌群代谢、增强后生元活性,进而协同发挥神经保护作用,为认知健康的营养干预策略提供了新思路。立足我国全面推进“大健康”战略的时代背景,结合持续增长的肠道健康市场需求与多元化的消费者诉求,以PKP为碳源制备后生元展现出良好的产业化转化前景和潜在应用价值。
[1] FIXEMER S, MIRANDA DE LA MAZA M, HAMMER G P, et al.Microglia aggregates define distinct immune and neurodegenerative niches in Alzheimer’s disease hippocampus[J].Acta Neuropathologica, 2025, 149(1):19.
[2] YU L C, ZHONG X, HE Y, et al.Butyrate, but not propionate, reverses maternal diet-induced neurocognitive deficits in offspring[J].Pharmacological Research, 2020, 160:105082.
[3] KIM T Y, KIM J M, LEE H L, et al.Codium fragile suppresses PM2.5-induced cognitive dysfunction by regulating gut-brain axis via TLR-4/MyD88 pathway[J].International Journal of Molecular Sciences, 2023, 24(16):12898-12927.
[4] LIU T Q, ZHOU L Q, LI X Q, et al.Polygonatum kingianum polysaccharides enhance the preventive efficacy of heat-inactivated limosilactobacillus reuteri WX-94 against high-fat-high-sucrose-induced liver injury and gut dysbacteriosis[J].Journal of Agricultural and Food Chemistry, 2024, 72(17):9880-9892.
[5] ZHOU L Q, SONG W, LIU T Q, et al.Multi-omics insights into anti-colitis benefits of the synbiotic and postbiotic derived from wheat bran Arabinoxylan and Limosilactobacillus reuteri[J].International Journal of Biological Macromolecules, 2024, 278:134860.
[6] ZHU T, MAO J D, ZHONG Y F, et al.L.reuteri ZJ617 inhibits inflammatory and autophagy signaling pathways in gut-liver axis in piglet induced by lipopolysaccharide[J].Journal of Animal Science and Biotechnology, 2021, 12(1):110.
[7] SHAN S H, QIAO Q Q, YIN R P, et al.Identification of a novel strain Lactobacillus reuteri and anti-obesity effect through metabolite indole-3-carboxaldehyde in diet-induced obese mice[J].Journal of Agricultural and Food Chemistry, 2023, 71(7):3239-3249.
[8] GU W, WANG Y F, ZENG L X, et al.Polysaccharides from Polygonatum kingianum improve glucose and lipid metabolism in rats fed a high fat diet[J].Biomedicine &Pharmacotherapy, 2020, 125:109910.
[9] ZHANG Y W, CHEN F, LI X Y, et al.Gastrodia elata, Polygonatum sibiricum, and Poria cocos as a functional food formula:Cognitive enhancement via modulation of hippocampal neuroinflammation and neuroprotection in sleep-restricted mice[J].Foods, 2025, 14(7):1103-1126.
[10] ZHOU L Q, LIU T Q, YAN T, et al.‘Nine Steaming Nine Sun-drying’ processing enhanced properties of Polygonatum kingianum against inflammation, oxidative stress and hyperglycemia[J].Journal of the Science of Food and Agriculture, 2024, 104(5):3123-3138.
[11] LIU T Q, LV J Y, BIAN B, et al.Postbiotic Limosilactobacillus reuteri cultured with Polygonatum kingianum polysaccharides ameliorates high-fat-high-sugar-deteriorated colitis and associated hepatobiliary disorders[J].International Journal of Biological Macromolecules, 2025, 322:147065.
[12] LUO S L, ZHANG X, HUANG S, et al.A monomeric polysaccharide from Polygonatum sibiricum improves cognitive functions in a model of Alzheimer’s disease by reshaping the gut microbiota[J].International Journal of Biological Macromolecules, 2022, 213:404-415.
[13] ZHANG X L, NI L, HU S S, et al.Polygonatum sibiricum ameliorated cognitive impairment of naturally aging rats through BDNF-TrkB signaling pathway[J].Journal of Food Biochemistry, 2022, 46(12):e14510.
[14] 艾孜古丽·木拉提.沙棘黄酮改善高热能膳食诱导小鼠糖脂代谢紊乱及认知障碍作用与机制研究[D].杨凌:西北农林科技大学,2022.AIZIGULI·M.Effects of konjac glucomannan on cognitive dysfunction and brain oxidative stress state in mice induced by a high-calorie diet[D].Yangling:Northwest A&F University,2022.
[15] LIU T Q, ZHOU L Q, DONG R, et al.Isomalto-oligosaccharide potentiates alleviating effects of intermittent fasting on obesity-related cognitive impairment during weight loss and the rebound weight gain[J].Journal of Agricultural and Food Chemistry, 2024, 72(43):23875-23892.
[16] CHENG M Y, LUO S, ZHANG P, et al.A genome and gene catalog of the aquatic microbiomes of the Tibetan Plateau[J].Nature Communications, 2024, 15(1):1438.
[17] TAN B L, NORHAIZAN M E, TAN B L, et al.Effect of high-fat diets on oxidative stress, cellular inflammatory response and cognitive function[J].Nutrients, 2019, 11(11):2579-2590.
[18] CHENG B, CHRISTAKOS S, MATTSON M P.Tumor necrosis factors protect neurons against metabolic-excitotoxic insults and promote maintenance of calcium homeostasis[J].Neuron, 1994, 12(1):139-153.
[19] WANG Y, SADIKE D, HUANG B, et al.Regulatory T cells alleviate myelin loss and cognitive dysfunction by regulating neuroinflammation and microglial pyroptosis via TLR4/MyD88/NF-κB pathway in LPC-induced demyelination[J].Journal of Neuroinflammation, 2023, 20(1):41.
[20] BELARBI K, JOPSON T, TWEEDIE D, et al.TNF-α protein synthesis inhibitor restores neuronal function and reverses cognitive deficits induced by chronic neuroinflammation[J].Journal of Neuroinflammation, 2012, 9:23.
[21] HENEKA M T, KUMMER M P, STUTZ A, et al.NLRP3 is activated in Alzheimer’s disease and contributes to pathology in APP/PS1 mice[J].Nature, 2013, 493(7434):674-678.
[22] KEYSER D O, ALGER B E.Arachidonic acid modulates hippocampal calcium current via protein kinase C and oxygen radicals[J].Neuron, 1990, 5(4):545-553.
[23] HEGADOREN K M, BAKER G B, BOURIN M.3, 4-Methylenedioxy analogues of amphetamine:Defining the risks to humans[J].Neuroscience &Biobehavioral Reviews, 1999, 23(4):539-553.
[24] LIANG X X, FU Y Q, CAO W T, et al.Gut microbiome, cognitive function and brain structure:A multi-omics integration analysis[J].Translational Neurodegeneration, 2022, 11(1):49.
[25] WANG X T, WANG Z X, CAO J, et al.Gut microbiota-derived metabolites mediate the neuroprotective effect of melatonin in cognitive impairment induced by sleep deprivation[J].Microbiome, 2023, 11(1):17.
[26] LU Q, ZHANG S Y, DU J Q, et al.Multi-group biodiversity distributions and drivers of metacommunity organization along a glacial-fluvial-limnic pathway on the Tibetan Plateau[J].Environmental Research, 2023, 220:115236.
[27] WANG X, JIANG D M, ZHANG X, et al.Causal associations between Helicobacter pylori infection and the risk and symptoms of Parkinson’s disease:A Mendelian randomization study[J].Frontiers in Immunology, 2024, 15:1412157.
[28] CHEN C Y, FANG S M, WEI H, et al.Prevotella copri increases fat accumulation in pigs fed with formula diets[J].Microbiome, 2021, 9(1):175.
[29] LU X, XUE Z Y, QIAN Y, et al.Changes in intestinal microflora and its metabolites underlie the cognitive impairment in preterm rats[J].Frontiers in Cellular and Infection Microbiology, 2022, 12:945851.
[30] CHAKRABORTY P, DROMARD Y, ANDRÉ E M, et al.Meal scheduling corrects obesogenic diet induced-uncoupling of cortico-hippocampal activities supporting memory[J].eBioMedicine, 2025, 117:105783.
[31] PENG L, XIANG Q W, JIA G, et al.Association between sarcopenic obesity and dementia in the Chinese elderly using different definitions of obesity:Evidence from the CHARLS[J].Frontiers in Aging Neuroscience, 2025, 17:1540272.
[32] ZHU G S, ZHAO J X, WANG G, et al.Bifidobacterium breve HNXY26M4 attenuates cognitive deficits and neuroinflammation by regulating the gut-brain axis in APP/PS1 mice[J].Journal of Agricultural and Food Chemistry, 2023, 71(11):4646-4655.
[33] CHUNCHAI T, THUNAPONG W, YASOM S, et al.Decreased microglial activation through gut-brain axis by prebiotics, probiotics, or synbiotics effectively restored cognitive function in obese-insulin resistant rats[J].Journal of Neuroinflammation, 2018, 15(1):11.
[34] BASHIR B, GULATI M, VISHWAS S, et al.Bridging gap in the treatment of Alzheimer’s disease via postbiotics:Current practices and future prospects[J].Ageing Research Reviews, 2025, 105:102689.
[35] WANG M L, SUN P H, CHAI X J, et al.Reconstituting gut microbiota-colonocyte interactions reverses diet-induced cognitive deficits:The beneficial of eucommiae cortex polysaccharides[J].Theranostics, 2024, 14(12):4622-4642.
[36] LAN Y, MA Z Y, CHANG L L, et al.Sea buckthorn polysaccharide ameliorates high-fat diet induced mice neuroinflammation and synaptic dysfunction via regulating gut dysbiosis[J].International Journal of Biological Macromolecules, 2023, 236:123797.
[37] TIAN X Y, DONG W, ZHOU W T, et al.The polysaccharides from the fruits of Lycium barbarum ameliorate high-fat and high-fructose diet-induced cognitive impairment via regulating blood glucose and mediating gut microbiota[J].International Journal of Biological Macromolecules, 2024, 258(Pt 2):129036.
[38] 许云聪, 闫巧娟, 朱春华, 等.滇黄精多糖对肥胖小鼠脂代谢紊乱及脑功能损伤的改善作用[J].食品科学, 2025, 46(1):64-73.XU Y C, YAN Q J, ZHU C H, et al.Ameliorative effects of Polygonatum kingianum polysaccharides on lipid metabolism disorders and brain function impairments in obese mice[J].Food Science, 2025, 46(1):64-73.
[39] LIU Z, FAYYAZ S, ZHAO D, et al.Polygonatum sibiricum polysaccharides improve cognitive function in D-galactose-induced aging mice by regulating the microbiota-gut-brain axis[J].Journal of Functional Foods, 2023, 103:105476.
[40] HUANG J, CHAI X J, WU Y J, et al.β-Hydroxybutyric acid attenuates heat stress-induced neuroinflammation via inhibiting TLR4/p38 MAPK and NF-κB pathways in the hippocampus[J].The FASEB Journal, 2022, 36(4):e22264.
[41] GUO T T, ZHANG Z, SUN Y, et al.Neuroprotective effects of sodium butyrate by restoring gut microbiota and inhibiting TLR4 signaling in mice with MPTP-induced Parkinson’s disease[J].Nutrients, 2023, 15(4):930-947.