近年来,饮酒的人日渐严重威胁人类健康,而过量饮酒是导致酒精性肝损伤(alcoholic liver injury,ALI)的一个重要原因,因为肝脏负责90%以上的酒精代谢[1]。如果不能及时治疗,它将从最初的可逆性脂肪肝转变为酒精性肝炎,再发展为慢性纤维化或者肝硬化,严重的会发展为肝细胞癌[2]。ALI是由炎症反应、氧化应激、肠源性内毒素和炎症介质之间的相互作用引起的,酒精及其衍生物会直接或间接诱导这些炎症介质[3]。酒精的主要代谢发生在肝脏,需要不同的亚细胞器。乙醇通过微粒体乙醇氧化系统内质网中的乙醇脱氢酶和线粒体中的醛氧化酶代谢[4]。该过程会产生活性氧物质(reactive oxygen species,ROS),ROS在肝脏中的积累导致细胞膜、蛋白质和DNA氧化的功能障碍,最终导致肝细胞损伤[5]。因此,迫切需要有效和安全的用于治疗肝脏疾病的替代来源。然而,目前国内关于柑橘多酚(citrus polyphenol,CP)在保护肝损伤,特别是ALI方面鲜见报道。
柑橘类水果因其营养成分和次生代谢产物,如维生素和黄酮类物质,是人们饮食中的重要组成部分[6]。柑橘的保健作用主要与其维生素C和黄酮类化合物的含量有关[7]。CP类物质已经被证明在抗炎、降血糖、抗氧化、神经保护甚至抗肿瘤方面有很强的生物学作用[8-9]。有研究表明柑橘类水果中的酚类物质对肝脏的保护起重要作用[10]。因此,本研究通过建立慢性ALI小鼠模型,初步探究CP提取物对乙醇诱导肝损伤的潜在防护作用,旨在为柑橘资源的深度开发利用以及护肝功能性食品的研究提供理论依据。
1 材料与方法
1.1 材料和仪器
SPF级雄性KM小鼠(4周龄),成都达硕实验动物有限公司,生产许可号:SCXK(川)2020-030;56°北京红星二锅头,北京红星股份有限公司;柑橘,四川顺溜现代农业发展有限公司;超氧化物歧化酶(superoxide dismutase, SOD)测定试剂盒、过氧化氢酶(catalase, CAT)测定试剂盒、谷胱甘肽过氧化物酶(glutathione peroxidase, GSH-Px)测定试剂盒,白细胞介素-6(interleukin-6, IL-6)、白细胞介素-1β(interleukin-1 beta, IL-1β)、α肿瘤坏死因子(tumor necrosis factor-α, TNF-α)酶联免疫吸附试验(ELISA)试剂盒,南京建成生物工程研究所;谷丙转氨酶(alanine aminotransferase, ALT)、谷草转氨酶(aspartate aminotransferase, AST)、甘油三酯(triglycerides, TG)、总胆固醇(total cholesterol, TC)测定试剂盒,深圳迈瑞生物医疗电子股份有限公司;甲醛(分析纯),四川西陇科学有限公司;二甲苯(分析纯),国药集团化学试剂有限公司;苏木素染液,武汉塞维尔生物科技有限公司;伊红染液,合肥博美生物科技有限责任公司。
LG-16M立式高速冷冻离心机,蜀科仪器有限公司;HAD-D2508转轮式切片机,北京恒奥德仪器仪表有限公司;PHY-Ⅲ型病理组织漂烘仪,常州市中威电子仪器有限公司;BMJ-A型组织包埋机,常州郊区中威电子仪器厂;JT-12P自动脱水机,武汉俊杰电子有限公司。
1.2 实验方法
所有动物实验均按照中华人民共和国国家科学技术委员会制定的《实验动物管理条例》进行,并获得了西华大学实验动物伦理委员会的批准(伦理批件:XH-2024-09-02)。
1.2.1 CP提取物的制备
将柑橘取皮烘干、粉碎过筛,称取柑橘粉末。参考文献[11]的方法提取CP。按照纤维素酶质量分数0.6%,在45 ℃水浴锅中,使纤维素酶与柑橘反应30 min,在水浴锅100 ℃高温水浴5 min进行灭酶处理,取出冷却至室温后再按照料液比1∶15(g∶mL)加入乙醇,置于360 W、40 ℃超声波处理一段时间。冷却后3 000 r/min离心10 min,收集上清液。提取液经AB-8大孔树脂纯化,并经过不同体积分数(20%、30%、40%、50%、60%、70%、80%、90%)乙醇溶液洗脱后,旋蒸出乙醇溶剂并回收,冷冻干燥得到CP提取物冻干粉末。最终得到纯度为50.67%的CP。
1.2.2 CP成分分析
1.2.2.1 测试样品前处理
称取适量样品于2 mL离心管中,加入600 μL甲醇,涡旋混匀。随后室温下超声波处理15 min,12 000 r/min、4 ℃离心5 min。取适量上清液加入体积分数80%甲醇稀释20倍,上清液过0.22 μm滤膜,过滤液加入到检测瓶中。
1.2.2.2 色谱条件
采用 ACQUITY UPLC BEH C18 色谱柱(2.1 mm×100 mm,1.7 μm),进样量5 μL,柱温40 ℃,流动相A为质量分数0.1%甲酸水溶液,流动相B为甲醇,流速0.25 mL/min。洗脱梯度:0~1 min,10% B;1~3 min,10%~33%B;3~10 min,33% B;10~15 min,33%~50% B;15~20 min,50%~90% B;20~21 min,90% B;21~22 min,90%~10%B;22~25 min,10%B。
1.2.2.3 质谱条件
采用ESI离子源,负离子电离模式对样品进行多重反应监测扫描。优化后质谱参数如下:离子源温度500 ℃,离子源电压-4 500 V,碰撞气6 psi,气帘气30 psi,雾化气和辅助气均为50 psi。
1.2.3 实验动物分组与处理
小鼠ALI模型的建立参考文献[12]的方法。将48只雄性KM小鼠随机分成6组,分别为:空白对照组、酒精模型组、阳性对照组、低剂量组、中剂量组、高剂量组,每组8只。在经过7 d的饲养适应期后(温度25 ℃,光照/黑暗周期12 h/12 h),阳性对照组、低、中和高剂量组分别依次灌胃50 mg/(kg·d)水飞蓟素以及100、200、400 mg/(kg·d) CP,空白对照组和酒精模型组分别灌胃相同体积的生理盐水。除空白组外,所有小鼠30 min后均灌胃10 mL/(kg·d) 56°红星二锅头,空白对照组灌胃相同体积生理盐水。连续21 d后,所有小鼠禁食12 h,麻醉后眼眶取血,于-80 ℃冷冻备用。取肝组织后,将部分肝脏浸入质量分数4%多聚甲醛固定液中,另一部分贮存在-80 ℃下备用。
1.2.4 小鼠肝脏指数的测定
解剖后迅速对肝脏组织进行称重并记录,并根据公式(1)计算肝脏指数[13]。
(1)
式中:W,肝脏指数,%;m,小鼠肝脏质量,g;m0,小鼠体重,g。
1.2.5 血清指标测定
小鼠眼球取血后,将血液在4 ℃、3 500 r/min离心10 min,然后从上清液中收集血清。采用试剂盒的方法直接测定小鼠血清中AST、ALT水平。
1.2.6 肝脏生化指标测定
小鼠肝脏按照脏器∶生理盐水=1∶9(g∶mL)用匀浆器将肝组织匀浆,将匀浆液在3 500 r/min、4 ℃离心10 min,取上清液。采用试剂盒上的方法测定小鼠CAT、SOD、GSH-Px活力以及小鼠肝脏中细胞因子IL-6、IL-1β和TNF-α含量。
1.2.7 小鼠肝脏病理学观察
用质量分数4%多聚甲醛溶液固定肝脏组织,脱水后进行石蜡包埋、切片。切片进行脱蜡,苏木精染色5~10 min,自来水冲洗至无色,盐酸酒精分化3 s,自来水冲洗至无色,放入50 ℃的温水中返蓝,自来水冲洗至无色,伊红染色3 min,梯度酒精脱水,并在二甲苯中脱蜡后,使用光学显微镜进行观察。
1.3 数据处理
所有实验均重复3次,实验数据以“平均值±标准差”表示,使用IBM SPSS Statistics 24软件对数据进行单因素方差分析(one-way ANOVA),P<0.05表示差异显著,P<0.01、P<0.001、P<0.000 1表示差异极显著。采用Graphpad Prism 10.1.2进行图表绘制。
2 结果与分析
2.1 CP成分分析
采用超高效液相色谱串联质谱(ultra performance liquid chromatography-tandem mass spectrometry,UPLC-MS/MS)对CP进行定性定量分析。将混标(图1-a)和样品(图1-b)的总离子流图(total ion chromatogram, TIC)进行对比,再结合质谱数据进行成分分析。
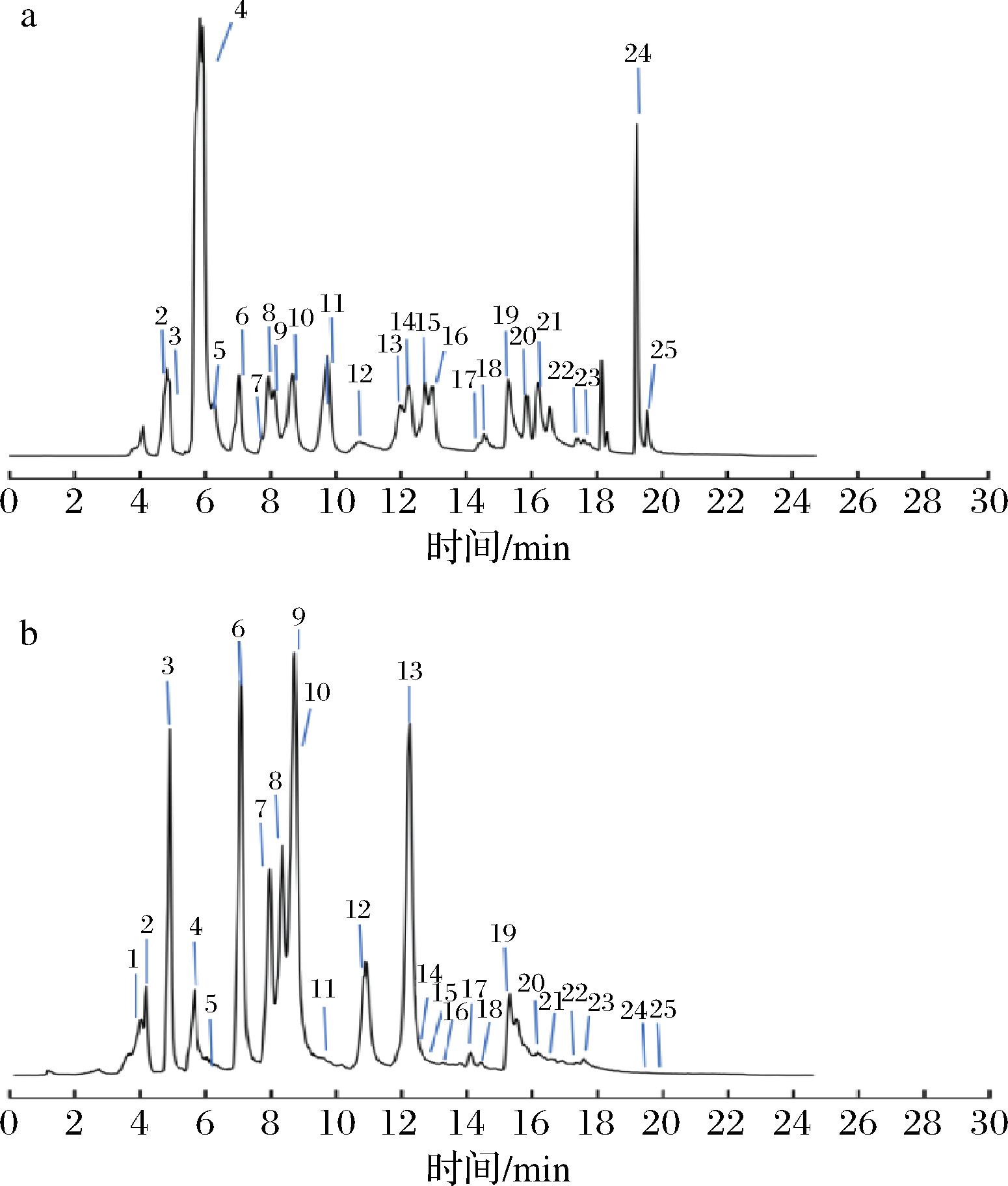
a-混标;b-CP样品
图1 混标和CP样品的TIC
Fig.1 TIC of mixed standard and CP
2.2 CP成分鉴定
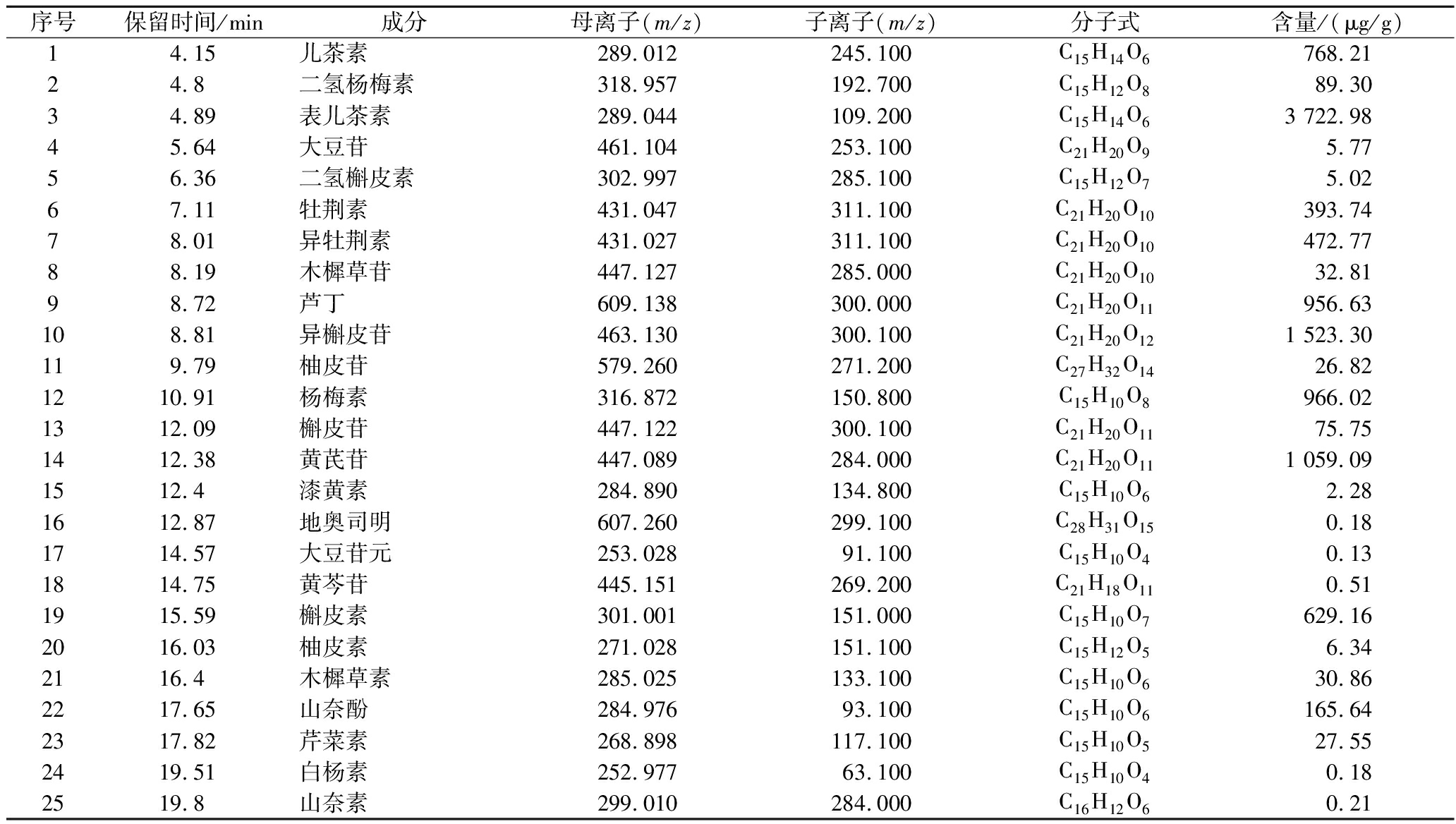
采用UPLC-MS/MS对CP进行定量分析,结果如表1所示。对多酚组成进行了分离检测,共分离鉴定出25种化合物,主要有表儿茶素、异槲皮苷、黄芪苷、槲皮素、芦丁、杨梅素、儿茶素等,其中表儿茶素相对含量最高。
表1 CP主要成分
Table 1 Main components of CP
序号保留时间/min成分母离子(m/z)子离子(m/z)分子式含量/(μg/g)14.15儿茶素289.012245.100C15H14O6768.2124.8二氢杨梅素318.957192.700C15H12O889.3034.89表儿茶素289.044109.200C15H14O63 722.9845.64大豆苷461.104253.100C21H20O95.7756.36二氢槲皮素302.997285.100C15H12O75.0267.11牡荆素431.047311.100C21H20O10393.7478.01异牡荆素431.027311.100C21H20O10472.7788.19木樨草苷447.127285.000C21H20O1032.8198.72芦丁609.138300.000C21H20O11956.63108.81异槲皮苷463.130300.100C21H20O121 523.30119.79柚皮苷579.260271.200C27H32O1426.821210.91杨梅素316.872150.800C15H10O8966.021312.09槲皮苷447.122300.100C21H20O1175.751412.38黄芪苷447.089284.000C21H20O111 059.091512.4漆黄素284.890134.800C15H10O62.281612.87地奥司明607.260299.100C28H31O150.181714.57大豆苷元253.02891.100C15H10O40.131814.75黄芩苷445.151269.200C21H18O110.511915.59槲皮素301.001151.000C15H10O7629.162016.03柚皮素271.028151.100C15H12O56.342116.4木樨草素285.025133.100C15H10O630.862217.65山奈酚284.97693.100C15H10O6165.642317.82芹菜素268.898117.100C15H10O527.552419.51白杨素252.97763.100C15H10O40.182519.8山奈素299.010284.000C16H12O60.21
2.3 CP对酒精肝损伤小鼠体重和肝脏指数的影响
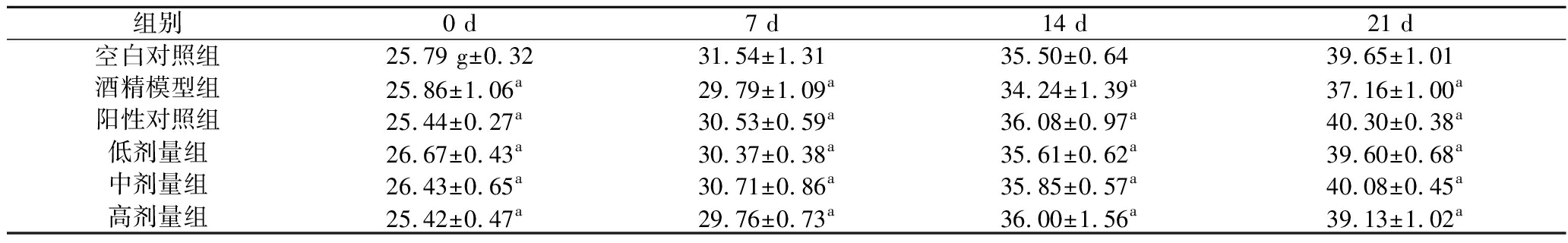
由表2可知,试验期间各剂量组动物体重增长趋势与空白对照组基本一致,且组间比较未出现统计学差异(P>0.05)。在整个试验期间,CP 各剂量组的小鼠均未出现死亡现象。基于上述实验结果可知,给小鼠灌胃不同剂量的CP,对其健康状况并未产生明显的负面影响。
表2 实验期间小鼠体重变化 单位:g
Table 2 Body weight changes of mice during the experiment
组别0 d7 d14 d21 d空白对照组25.79 g±0.3231.54±1.3135.50±0.6439.65±1.01酒精模型组25.86±1.06a29.79±1.09a34.24±1.39a37.16±1.00a阳性对照组25.44±0.27a30.53±0.59a36.08±0.97a40.30±0.38a低剂量组26.67±0.43a30.37±0.38a35.61±0.62a39.60±0.68a中剂量组26.43±0.65a30.71±0.86a35.85±0.57a40.08±0.45a高剂量组25.42±0.47a29.76±0.73a36.00±1.56a39.13±1.02a
注:同列相同小写字母代表不具有显著性差异(P>0.05)。
肝脏作为机体代谢中枢,在稳态调控与生理功能协调中承担关键作用。乙醇经消化道摄入后,约90%需通过肝细胞进行生物转化,其代谢中间产物乙醛会造成肝细胞损伤,因此过量饮酒是引发肝脏损伤的主要原因。肝脏系数可反映肝脏损伤的程度,而肝肿大是ALI临床上常见的症状[14]。由图2可知,模型组肝脏系数相较于空白组显著(P<0.05)上升,上升的原因可能是酒精的过量摄入导致肝损伤严重,引起了肝脏肿大,说明模型建立成功。与模型组相比,阳性组和中高剂量组均显著降低(P<0.05),说明CP的干预缓解了小鼠肝肿大。结果表明CP与水飞蓟素均能减轻酒精引起的小鼠肝损伤,而且中高剂量CP减轻ALI效果较好。
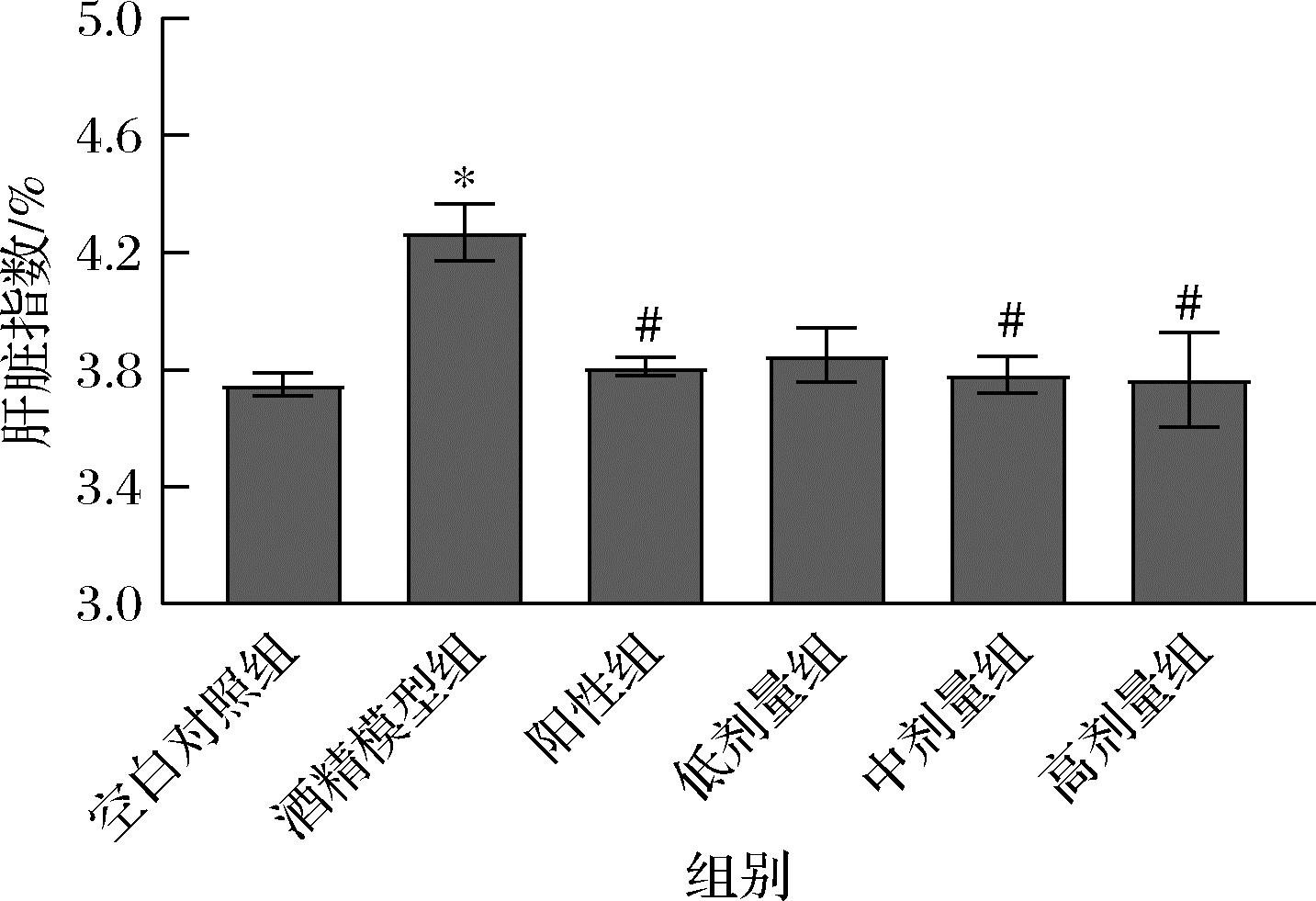
图2 CP对小鼠肝脏指数的影响
Fig.2 Effect of CP on liver index in mice
注:与空白组相比,*P<0.05;**P<0.01;***P<0.001;****P<0.000 1,与模型组相比,#P<0.05;##P<0.01;###P<0.001;####P<0.000 1(下同)。
2.4 CP对酒精肝损伤小鼠肝脏TC和TG的影响
肝损伤可导致脂肪酸肝内扩散,导致肝脏TG、TC含量升高。TG和TC的水平反映了肝脏中的脂质过氧化程度[15]。由图3可知,相较于空白对照组,模型组小鼠肝脏中TC和TG水平均极显著升高(P<0.01),这可能是由于酒精的摄入导致肝脏内脂滴过量积累。与模型组相比,中剂量和高剂量CP灌药后,小鼠的TG、TC含量均显著降低(P<0.05或P<0.001),且呈现剂量依赖性。ZHOU等[16]研究发现,白芍多酚能够上调肝损伤小鼠TG、TC水平,这与本研究结果相似。以上结果均表明,CP可以改善ALI小鼠脂质代谢紊乱和防止脂肪变性。
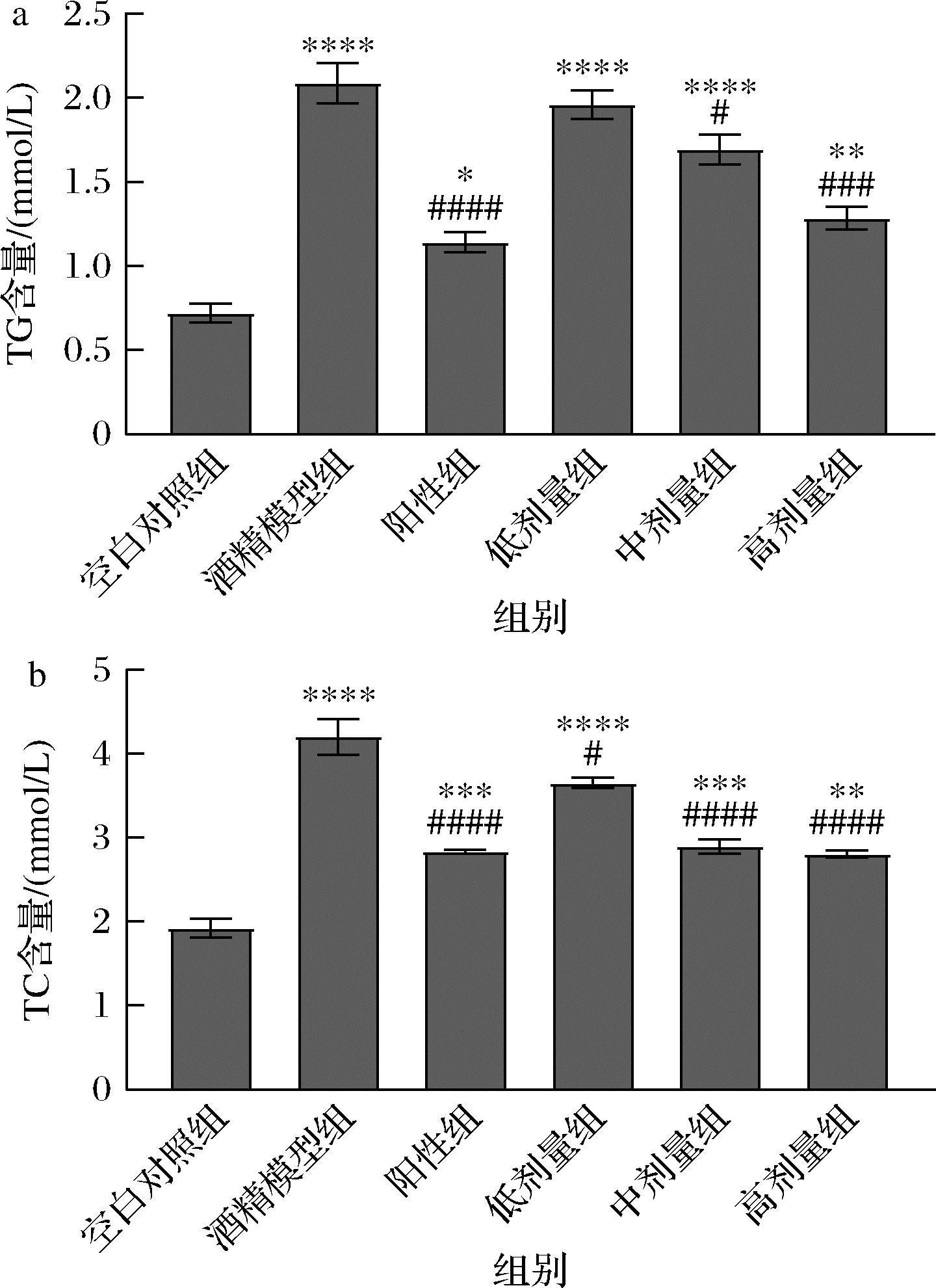
a-TG;b-TC
图3 CP对ALI小鼠TG、TC的影响
Fig.3 Effect of CP on TG and TC in mice with ALI
2.5 CP对酒精肝损伤小鼠血清AST、ALT的影响
AST主要分布于肝细胞血浆和线粒体中,ALT主要存在于肝细胞血浆中[17]。血清中ALT和AST水平的增加分别表明肝中的细胞膜损伤和细胞线粒体损伤[18]。如图4所示,与空白组相比,模型组小鼠的血清中AST、ALT水平均极显著增高(P<0.001)。这是由于肝脏中乙醇脱氢酶浓度较高,该酶将乙醇催化为相应的醛,从而使肝脏损伤[19]。与模型组相比,高剂量组小鼠AST水平极显著下降(P<0.001);而中剂量组、高剂量组的小鼠ALT水平极显著下降(P<0.001),二者差异不显著。结果表明,CP对酒精诱导的肝损伤具有一定的保护作用,且随剂量的增加,对肝脏保护作用效果越好,呈现出一定的剂量效应。
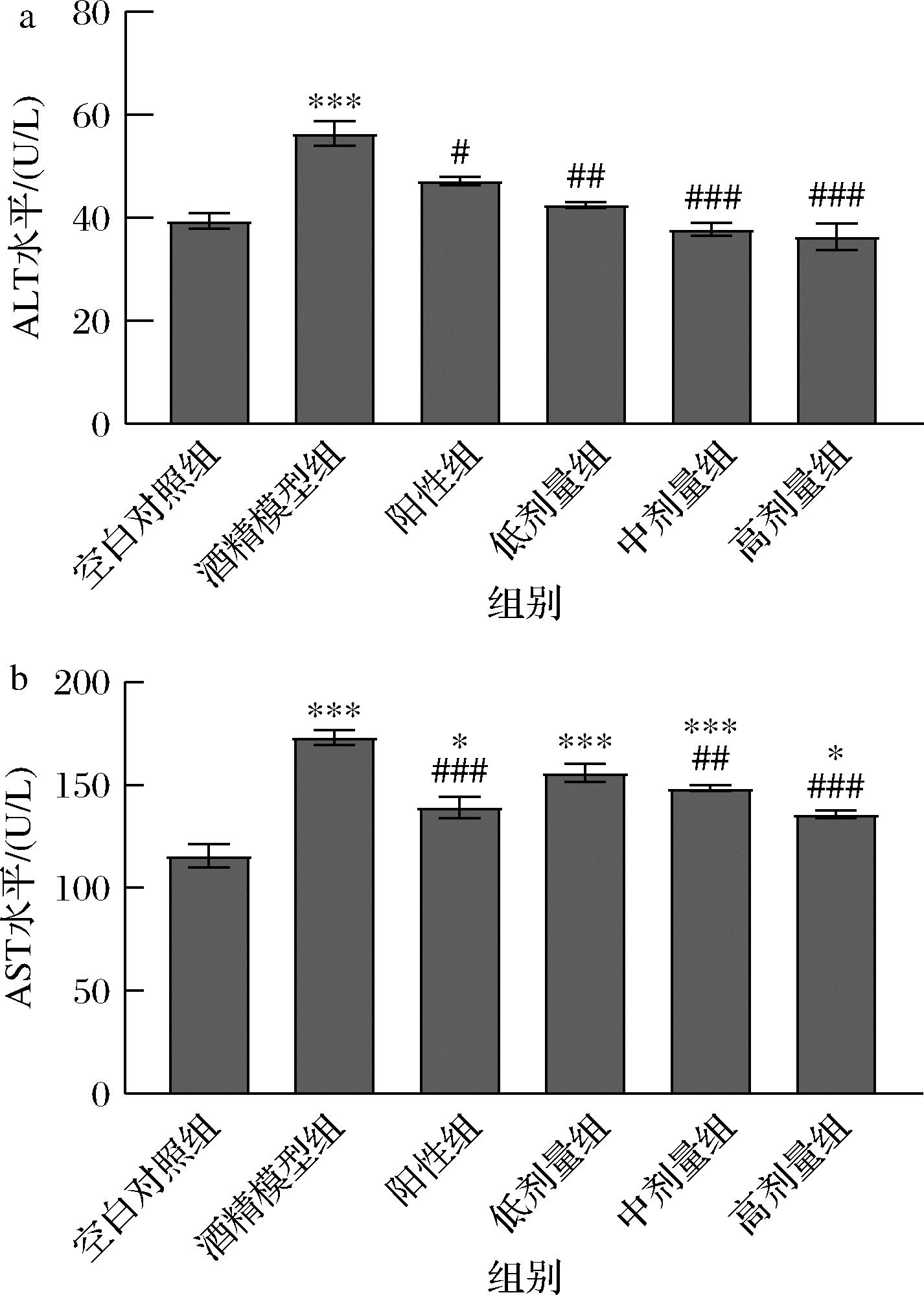
a-ALT;b-AST
图4 CP对ALI小鼠血清ALT、AST的影响
Fig.4 Effect of CP on AST and ALT in mice with ALI
2.6 肝脏组织的病理学变化分析
在图5中可观察到小鼠肝脏形态。正常小鼠的肝细胞显示出完整的细胞结构和有丝分裂细胞,即均匀的细胞层、清晰排列的核和肝索,以及围绕核仁均匀排列的中心静脉(图5-a)。相比之下,模型组的肝组织表现出明显的异常形态变化,细胞间隙增加,细胞边界丧失,细胞内空泡,伴有细胞核周围大量脂肪沉积、细胞坏死和炎症(图5-b)。然而,在阳性对照组中,脂肪空泡化有所改善,病变得到了有效缓解,肝组织损伤得到了成功抑制(图5-c)。与模型组相比,CP减轻了细胞萎缩,减少了脂滴,减轻了细胞坏死的程度,使细胞核和脉络膜清晰(图5-d~5-f)。CP干预的小鼠肝组织发生了明显变化,且呈现剂量-效应关系。
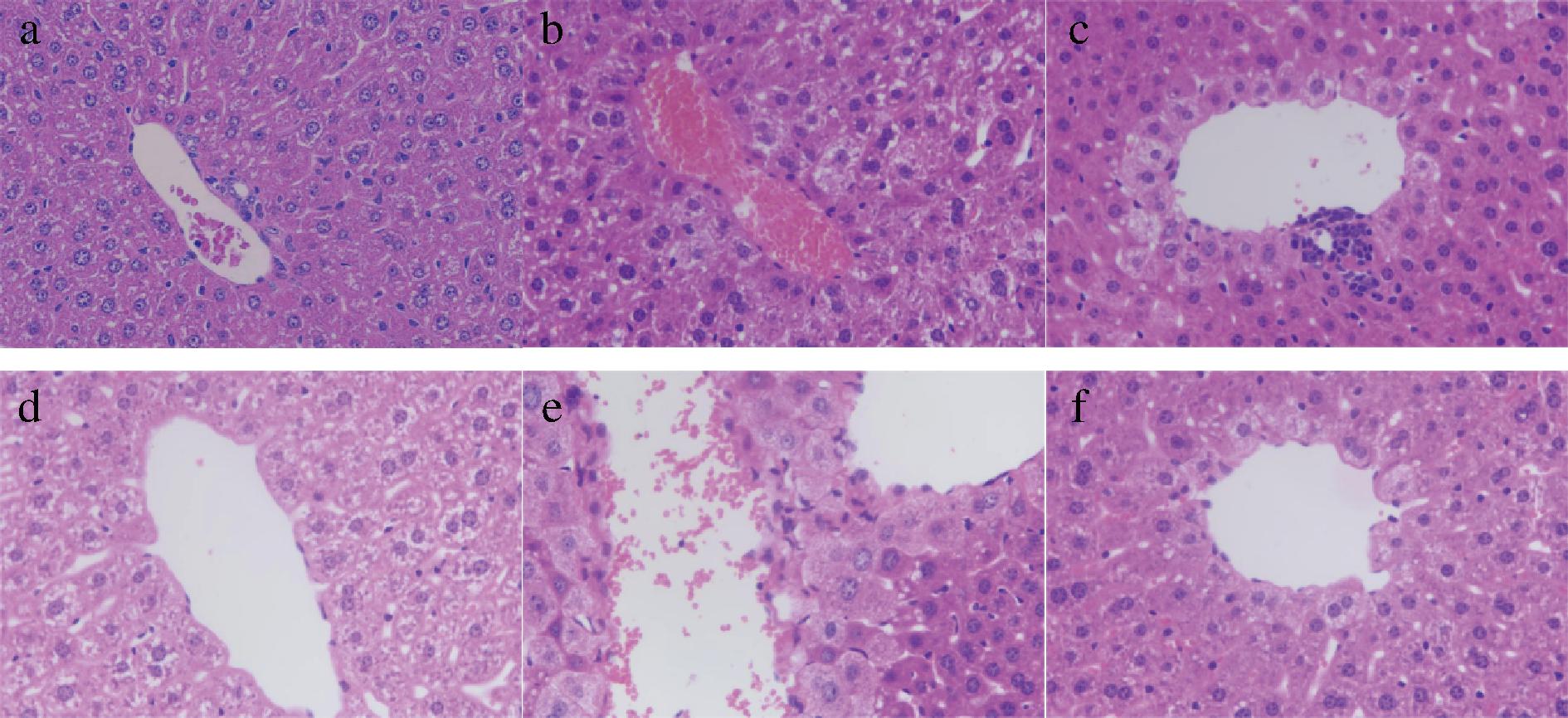
a-空白组;b-模型组;c-阳性组;d-低剂量组;e-中剂量组;f-高剂量组
图5 CP对酒精诱导的小鼠肝组织组织病理学变化的影响(400×)
Fig.5 Effect of CP on alcohol-induced histopathological changes in liver tissue in mice(400×)
2.7 CP对小鼠肝组织中氧化应激水平的影响
酒精的摄入会诱导氧化应激,从而使ROS过量积累引起肝脏组织器官损伤[20]。SOD和CAT是体内重要的抗氧化酶,CAT可以将H2O2从体内清除,从而抑制氧化应激,减少体内酒精诱导的氧化,抑制肝损伤[21]。SOD可以与CAT协同从而防止自由基引起的氧化应激[22]。GSH-Px催化H2O2分解。通过催化H2O2的还原,它可以保护细胞膜,避免细胞损伤[23]。由图6可知,与空白组相比,模型组SOD、CAT、GSH-Px水平极显著下降(P<0.001),表明ALI小鼠氧化应激状态明显,模型建立成功。与酒精模型组相比,高剂量组SOD、CAT、GSH-Px水平均极显著提高(P<0.01或P<0.001),且与阳性组均无显著性差异,说明CP提取物与水飞蓟素对肝损伤的影响相似。以上结果表明,对酒精诱导的肝损伤具有保护作用的可能机制之一是由于CP的抗氧化活性和抑制脂质过氧化。
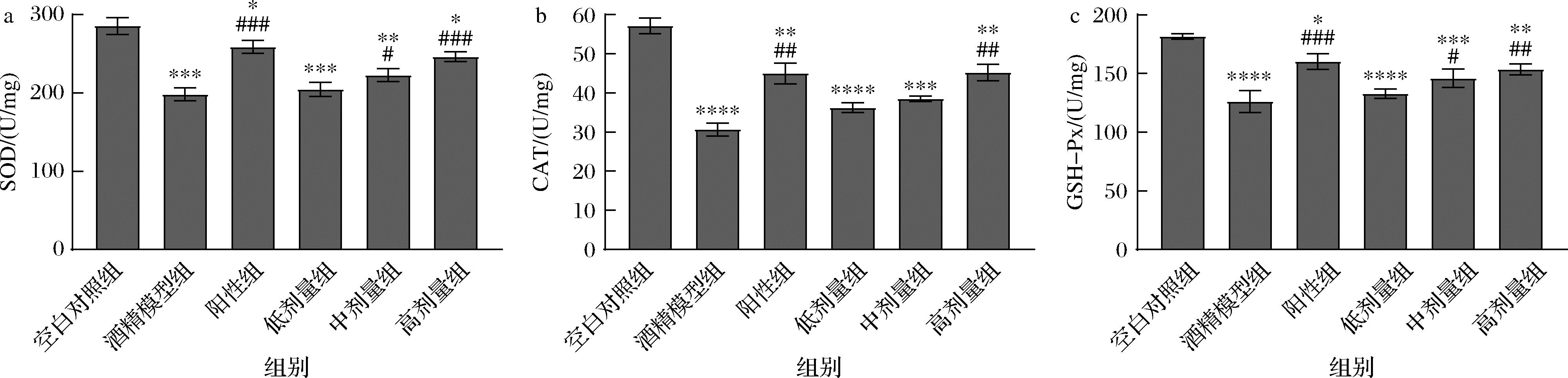
a-SOD;b-CAT;c-GSH-Px
图6 CP对ALI小鼠肝组织氧化应激水平的影响
Fig.6 Effect of CP on oxidation stress level in liver tissue of mice with ALI
2.8 CP对酒精肝损伤小鼠肝脏细胞炎症因子水平的影响
乙醇的过量摄入会诱导炎症因子和内毒素进入肝脏,从而导致炎症水平的升高[24]。肝组织损伤后出现的氧化应激可导致体内炎症因子(包括IL-6、IL-1β和TNF-α)的失衡,从而增加其在肝脏中的含量[25]。由图7可知,相较于空白组,模型组小鼠肝脏IL-6、IL-1β和TNF-α的含量均极显著升高(P<0.01或P<0.001)。说明ALI会诱导小鼠肝脏中的炎症反应。与模型组相比,高剂量组小鼠肝脏IL-1β、IL-6和TNF-α含量极显著下降(P<0.01或P<0.001),且呈现剂量依赖性,其作用效果与水飞蓟素效果相似。以上结果说明,CP可以通过调节肝损伤小鼠IL-6、IL-1β和TNF-α的水平,从而减轻肝损伤,维持肝脏的正常代谢。
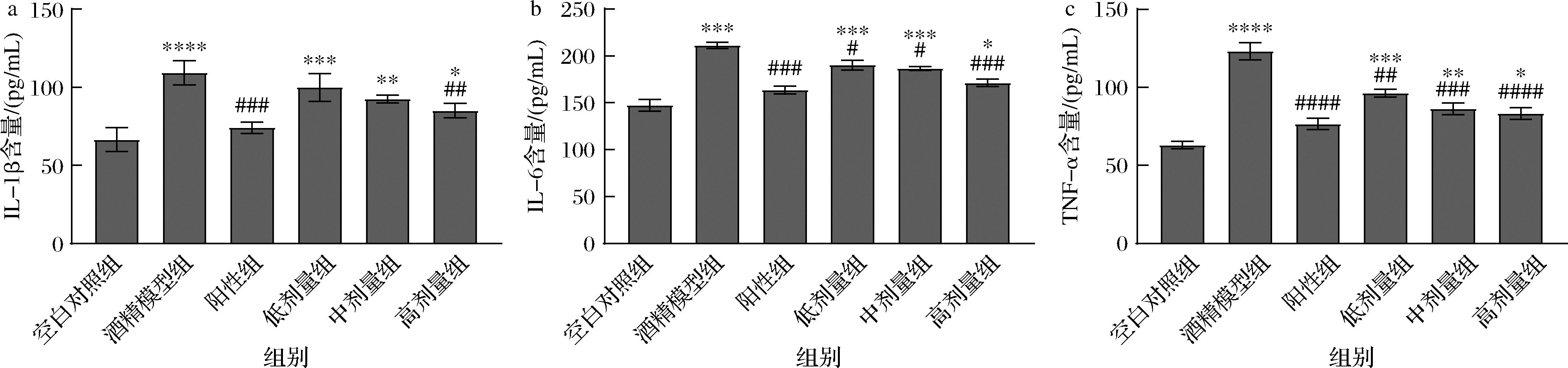
a-IL-6;b-IL-1β;c-TNF-α
图7 CP对ALI小鼠肝脏细胞炎症因子水平的影响
Fig.7 Effect of CP on inflammatory cytokine level in liver tissue of mice with ALI
3 结论
本研究从体内生化指标、病理学形态变化和体内炎症因子水平等方面分析了CP对酒精诱导的小鼠肝损伤的改善作用。结果表明,CP能够通过降低肝脏指数、肝脏脂质代谢水平(TG、TC)、转氨酶水平(AST、ALT)及提高氧化应激(SOD、CAT、GSH-Px)的水平来改善肝脏细胞和组织的损伤;肝脏病理学切片显示CP可以减轻肝损伤程度;CP干预能降低小鼠肝脏炎症因子水平,且各剂量组呈剂量依赖关系。综上所述,CP对ALI具有保护作用,其作用效果和水飞蓟素相似。CP是一种具有多种功效的自然资源,在功能性食品、保健品以及医药领域将具有广阔的发展前景,研究结果也为CP护肝产品的开发提供了理论依据。尽管证明了CP对小鼠ALI具有保护作用,但对于CP干预小鼠ALI的作用机制仍需要进一步的研究,未来可在后续研究中进行验证。
[1] SUN F R, WANG B Y.Alcohol and metabolic-associated fatty liver disease[J].Journal of Clinical and Translational Hepatology, 2021, 9(5):719-730.
[2] REN J N, YANG S, SHEN N, et al.Screening alcohol degrading function probiotics and protective effect of fermented apple juice on alcoholic liver injury in mice[J].Food Bioscience, 2024, 58:103786.
[3] SEITZ H K, BATALLER R, CORTEZ-PINTO H, et al.Alcoholic liver disease[J].Nature Reviews Disease Primers, 2018, 4:16.
[4] 丁晓波, 张华, 刘世尧, 等.柑橘果品营养学研究现状[J].园艺学报, 2012, 39(9):1687-1702.DING X B, ZHANG H, LIU S Y, et al.Current status of the study in citrus nutriology[J].Acta Horticulturae Sinica, 2012, 39(9):1687-1702.
[5] TOH M R, WONG E Y T, WONG S H, et al.Global epidemiology and genetics of hepatocellular carcinoma[J].Gastroenterology, 2023, 164(5):766-782.
[6] SEBGHATOLLAHI Z, GHANADIAN M, AGARWAL P, et al.Citrus flavonoids:Biological activities, implementation in skin health, and topical applications:A review[J].ACS Food Science &Technology, 2022, 2(9):1417-1432.
[7] SHARMA K, MAHATO N, LEE Y R.Extraction, characterization and biological activity of citrus flavonoids[J].Reviews in Chemical Engineering, 2019, 35(2):265-284.
[8] PONTIFEX M G, MALIK M M A H, CONNELL E, et al.Citrus polyphenols in brain health and disease:Current perspectives[J].Frontiers in Neuroscience, 2021, 15:640648.
[9] DI LORENZO C, COLOMBO F, BIELLA S, et al.Polyphenols and human health:The role of bioavailability[J].Nutrients, 2021, 13(1):273.
[10] LI C Y, SCHLUESENER H.Health-promoting effects of the citrus flavanone hesperidin[J].Critical Reviews in Food Science and Nutrition, 2017, 57(3):613-631.
[11] 胡霞, 王顺风, 白玉英, 等.超声辅助纤维素酶法提取辣木籽多酚的工艺优化及其体外活性[J].食品工业科技, 2023, 44(7):207-214.HU X, WANG S F, BAI Y Y, et al.Process optimization of the extraction of Moringa oleifera seed polyphenols by ultrasound-assisted cellulase and its in vitro activity[J].Science and Technology of Food Industry, 2023, 44(7):207-214.
[12] 赵婷婷, 戴映笛, 舒昉, 等.灵芝菌丝体多糖提取工艺优化及其对慢性酒精肝损伤的保护作用[J].食品工业科技, 2023, 44(5):388-396.ZHAO T T, DAI Y D, SHU F, et al.Optimization of extraction technology of polysaccharides from Ganoderma lingzhi mycelium and its protective effect on alcoholic liver injury[J].Science and Technology of Food Industry, 2023, 44(5):388-396.
[13] ZHAO X, ZHANG J, YI S, et al.Lactobacillus plantarum CQPC02 prevents obesity in mice through the PPAR-α signaling pathway[J].Biomolecules, 2019, 9(9):407.
[14] WANG D J, LV J, FU Y, et al.Optimization of microwave-assisted extraction process of total flavonoids from Salicornia bigelovii Torr.and its hepatoprotective effect on alcoholic liver injury mice[J].Foods, 2024, 13(5):647.
[15] WU E Y, SUN W J, WANG Y, et al.Optimization of ultrasonic-assisted extraction of total flavonoids from Abrus cantoniensis (abriherba) by response surface methodology and evaluation of its anti-inflammatory effect[J].Molecules, 2022, 27(7):2036.
[16] ZHOU Y L, TAN F, LI C, et al.White peony (fermented Camellia sinensis) polyphenols help prevent alcoholic liver injury via antioxidation[J].Antioxidants, 2019, 8(11):524.
[17] GUI Y Y, ZHENG B, HUANG H R, et al.Protective effects of polysaccharides from Polygonatum cyrtonema on the acute alcohol induced liver damage[J].Food Bioscience, 2024, 61:104879.
[18] ZHOU B J, LIU P P, YAO X G, et al.Hepatoprotective effects of peach gum polysaccharides against alcoholic liver injury:Moderation of oxidative stress and promotion of lipid metabolism[J].Frontiers in Nutrition, 2024, 10:1325450.
[19] LAI W W, ZHOU S P, BAI Y, et al.Glucosamine attenuates alcohol-induced acute liver injury via inhibiting oxidative stress and inflammation[J].Current Research in Food Science, 2024, 8:100699.
[20] PENG Q, YANG K M, HOU Q F, et al.Alleviation of alcoholic liver injury through composite postbiotics regulation of intestinal flora and promotion of bile acid metabolism[J].Food Bioscience, 2024, 62:105379.
[21] GUAN S, ZHANG S Z, LIU M T, et al.Preventive effects of lactoferrin on acute alcohol-induced liver injury via iron chelation and regulation of iron metabolism[J].Journal of Dairy Science, 2024, 107(8):5316-5329.
[22] ZHANG X, DONG Z C, FAN H, et al.Scutellarin prevents acute alcohol-induced liver injury via inhibiting oxidative stress by regulating the Nrf2/HO-1 pathway and inhibiting inflammation by regulating the AKT, p38 MAPK/NF-κB pathways[J].Journal of Zhejiang University:Science B, 2023, 24(7):617-631.
[23] WANG M, JIANG Y S, WANG S Y, et al.Yak milk protects against alcohol-induced liver injury in rats[J].Food &Function, 2023, 14(21):9857-9871.
[24] WANG X, DONG K, MA Y J, et al.Hepatoprotective effects of chamazulene against alcohol-induced liver damage by alleviation of oxidative stress in rat models[J].Open Life Sciences, 2020, 15(1):251-258.
[25] TANG Z, ZHAN L, HE R R, et al.Hepatoprotective effect of tea composite solid beverage on alcohol-caused rat liver injury[J].Foods, 2023, 12(22):4126.