近年来,2型糖尿病(type 2 diabetes mellitus, T2DM)作为一种常见的代谢性疾病,其与甲状腺结节(thyroid nodule, TN)和甲状腺癌(thyroid cancer, TC)的关联性受到越来越多的关注[1]。流行病学研究表明,糖尿病患者合并甲状腺功能异常的患病率是非糖尿病患者的2~3倍[2]。然而,T2DM患者甲状腺癌发生发展的具体机制尚未完全阐明。越来越多的研究表明,免疫炎症反应在T2DM及甲状腺癌的发生发展中起着重要作用[3-4]。
炎症小体是由胞浆内模式识别受体(pattern recognition receptors,PRRs)参与组装的多蛋白复合物,是天然免疫系统的重要组成部分[5]。NOD样受体蛋白3(NOD-like receptor family pyrin domain containing 3,NLRP3)炎症小体在多种疾病发生发展过程中扮演着重要角色,包括自身免疫性疾病、T2DM、炎症性肠病以及甲状腺疾病等[6]。NLRP3炎症小体可被多种刺激因素激活,包括细菌成分、尿酸晶体、ATP等,激活后促进前炎症因子IL-1β和IL-18的成熟和释放,参与组织损伤和炎症反应[7]。
干扰素基因刺激因子(stimulator of interferon genes, STING)是天然免疫信号通路中的关键调控分子,在调节机体应答病原体、肿瘤或自身DNA方面发挥重要作用[8-9]。近年研究表明,STING可能参与调控NLRP3炎症小体的活化。研究显示,脂多糖(lipopolysaccharide,LPS)刺激可触发STING核易位,进而与IRF3结合并磷酸化IRF3,活化的IRF3转移到细胞核中并增加NLRP3的表达[10]。另有研究表明,在线粒体DNA(mitochondrial DNA,mtDNA)刺激后,STING/TANK结合激酶1(TBK1)信号通路增强活化,而STING抑制可阻断NLRP3信号的过度激活[11]。这些研究提示STING-NLRP3信号轴在免疫调控中具有重要作用。
Th9细胞是近年发现的一类新型CD4+辅助T细胞亚群,主要分泌IL-9,在过敏性疾病、自身免疫性疾病以及抗肿瘤免疫中发挥重要作用[12]。越来越多的研究表明,Th9细胞还在多种代谢性疾病和内分泌疾病中参与炎症调控作用。在apoE-/-小鼠动脉粥样硬化模型中,Th9/IL-9水平与动脉粥样硬化发展程度呈正相关[13]。基于MAANIITTY等[14]的最新研究,通过对452名接受冠状动脉造影的患者进行分析,发现IL-9水平升高与冠状动脉疾病呈显著正相关(OR 1.359, P=0.022),表明Th9/IL-9信号通路在冠状动脉粥样硬化发生发展中发挥重要作用。SIMONOVIC等[15]通过对13名DTC患者和13名健康对照者的外周血细胞进行比较分析,首次证实分化型甲状腺癌患者外周血细胞产生的Th2/Th9相关细胞因子(IL-5、IL-13和IL-9)浓度显著高于健康对照组,且放射性碘治疗后这些细胞因子水平明显下降,提示Th2/Th9介导的免疫反应可能参与甲状腺癌的发生发展过程。值得关注的是,慢性炎症状态是连接T2DM与甲状腺疾病的重要桥梁。T2DM患者长期处于低度炎症状态,血清中多种促炎因子水平升高,这些炎症因子不仅影响胰岛β细胞功能,还可影响甲状腺激素的合成、释放和外周代谢,从而增加甲状腺疾病的发生风险。Th9细胞作为重要的促炎细胞亚群,通过分泌IL-9等细胞因子参与这一病理过程,可能成为连接T2DM与甲状腺疾病的重要免疫学机制。目前已知转录因子PU.1、IRF4和BATF等参与Th9细胞的分化过程,然而,先天性免疫信号通路如何调控Th9细胞分化仍需进一步探索。STING-NLRP3信号轴作为重要的先天性免疫调控通路,是否参与调控Th9细胞分化尚不明确。探索STING-NLRP3信号轴对Th9细胞分化的调控作用,有助于深入理解Th9细胞在代谢性疾病和甲状腺疾病中的作用机制,为相关疾病的防治提供新的理论依据。
植物乳植杆菌(Lactiplantibacillus plantarum)是一种重要的益生菌,具有调节肠道菌群平衡、增强肠道屏障功能和调节免疫反应等多种生物学功能。WANG等[16]研究表明,通过增强上皮细胞防御机制、上调紧密连接蛋白表达、调节炎症因子产生以及重塑肠道微生态组成,从而显著增强肠道屏障功能,这些作用机制为其在多种肠道疾病防治中的应用提供了科学依据。近年来研究表明,L. plantarum可通过调节肠道菌群组成及其代谢产物短链脂肪酸(short chain fatty acids,SCFAs)参与多种疾病的免疫调节。ZENG等[17]在免疫抑制小鼠模型中证实,L. plantarum可显著恢复环磷酰胺处理后肠道菌群的平衡,增加SCFAs的产生,从而促进肠道免疫功能恢复,包括炎症因子表达水平的上调和肠道杯状细胞数量的增加。然而,L. plantarum是否可通过STING-NLRP3信号轴调控Th9细胞分化尚未有报道。
本研究旨在探讨L. plantarum通过STING-NLRP3信号轴调控Th9细胞分化的分子机制,以及在糖尿病相关甲状腺疾病中的潜在免疫调节作用,为相关疾病的防治提供新的思路和方法。
1 材料与方法
1.1 材料与试剂
6~8周龄雄性C57BL/6小鼠,体重20~25 g,购自上海绪海生物科技有限公司,饲养于上海市胸科医院实验动物中心SPF级环境中,温度(22±2)℃,湿度(55±5)%,12 h明暗循环。动物实验方案经上海市安亭医院伦理委员会批准(批准号:HXQK-2025-14)。
RPMI 1640培养基和胎牛血清,Gibco公司;小鼠CD4+初始T细胞分离试剂盒,Miltenyi Biotec公司;重组小鼠TGF-β1、IL - 4,PeproTech公司;抗CD3和抗CD28抗体,eBioscience公司;此外,实验中使用的L. plantarum菌株为ATCC 14917,后文简称LP。小鼠IL-9和IL-1β ELISA试剂盒,R&D Systems公司;STING、NLRP3、Caspase-1、PU.1以及β-actin抗体,Cell Signaling Technology公司;TRIzol试剂、SYBR GreenERTM qPCR SuperMix Universal,Invitrogen公司。
1.2 仪器与设备
AutoMACS Pro 磁珠分选仪,Miltenyi Biotec 公司;Thermo Heracell VIOS 160i CO2培养箱、Thermo Multiskan FC 51119000-7001585 酶标仪、Thermo Scientific Sorvall ST16R 高速冷冻离心机,Thermo Fisher Scientific 公司;Bio-Rad Mini-PROTEAN Tetra 1658005EDU垂直电泳仪、Bio-Rad ChemiDoc XRS+ 1708265EDU 凝胶成像仪,Bio-Rad 公司;Eppendorf Research Plus 移液器、Eppendorf 5424R 低速离心机,Eppendorf 公司;BD FACSCanto Ⅱ 流式细胞仪,BD Biosciences 公司;QuantStudio5 荧光定量 PCR 仪,ABI公司。
1.3 实验方法
1.3.1 小鼠Th9细胞的诱导与LP干预
采用磁珠分选法从小鼠脾脏中分离纯化CD4+初始T细胞。将细胞以5×105个/孔接种于预先包被抗CD3(2 μg/mL)和抗CD28(2 μg/mL)抗体的24孔板中,加入TGF-β1(2.0 ng/mL)和IL-4(20 ng/mL)诱导Th9细胞分化。根据实验分组加入LP(107 CFU/mL)或PBS,培养48 h。
1.3.2 流式细胞术检测
收集细胞,用PBS洗涤2次,加入细胞固定/渗透试剂盒(eBioscience公司)处理。加入PE标记的抗小鼠IL-9抗体和PerCP/Cy5.5标记的抗小鼠CD4抗体,4 ℃孵育30 min,PBS洗涤后流式细胞仪检测CD4+IL-9+细胞比例。
1.3.3 RT-PCR分析
采用TRIzol试剂提取总RNA,逆转录为cDNA。使用SYBR Green PCR Master Mix进行实时荧光定量PCR,以β-actin为内参基因。
1.3.4 Western Blot分析
提取细胞总蛋白,BCA法测定蛋白浓度。等量蛋白样品经SDS-PAGE分离后转移至PVDF膜,将样品用50 g/L脱脂奶粉溶液封闭1小时,加入相应一抗4 ℃孵育过夜,TBST洗涤后加入HRP标记的二抗室温孵育1 h,ECL法显影。
1.3.5 T2DM合并TN小鼠模型的构建与LP干预
小鼠随机分为对照组、T2DM+TN组和T2DM+TN+LP组,每组8只。T2DM模型采用高脂饮食(脂肪质量分数60%)联合链脲佐菌素(streptozotocin,STZ,40 mg/kg)腹腔注射建立;TN模型通过甲状腺刺激素(thyroid stimulating hormone,TSH)刺激联合碘过量诱导建立。LP干预组给予LP悬液(1×109 CFU/只/d)灌胃,对照组给予等体积PBS,连续干预4周。
1.3.6 血清炎症因子检测
小鼠眼眶取血,分离血清,ELISA法测定IL-9、IL-1β、IL-6、TNF-α水平。
1.4 数据处理
采用Prism软件进行统计分析,数据以“平均数±标准差”表示,多组间比较采用单因素方差分析(one-way analysis of variance,one-way ANOVA),P<0.05为差异有统计学意义。
2 结果与分析
2.1 LP抑制体外诱导的Th9细胞分化及IL-9表达
为观察LP对Th9细胞分化的影响,采用TGF-β1和IL-4共同诱导小鼠CD4+初始T细胞向Th9细胞分化,并给予LP干预。流式细胞术结果显示,与对照组相比,LP干预组CD4+IL-9+细胞比例显著降低(P<0.01),提示LP可抑制Th9细胞的分化(图1-a、图1-b)。同时,ELISA结果显示LP干预组培养上清液中IL-9水平较对照组显著降低(P<0.01)(图1-c)。
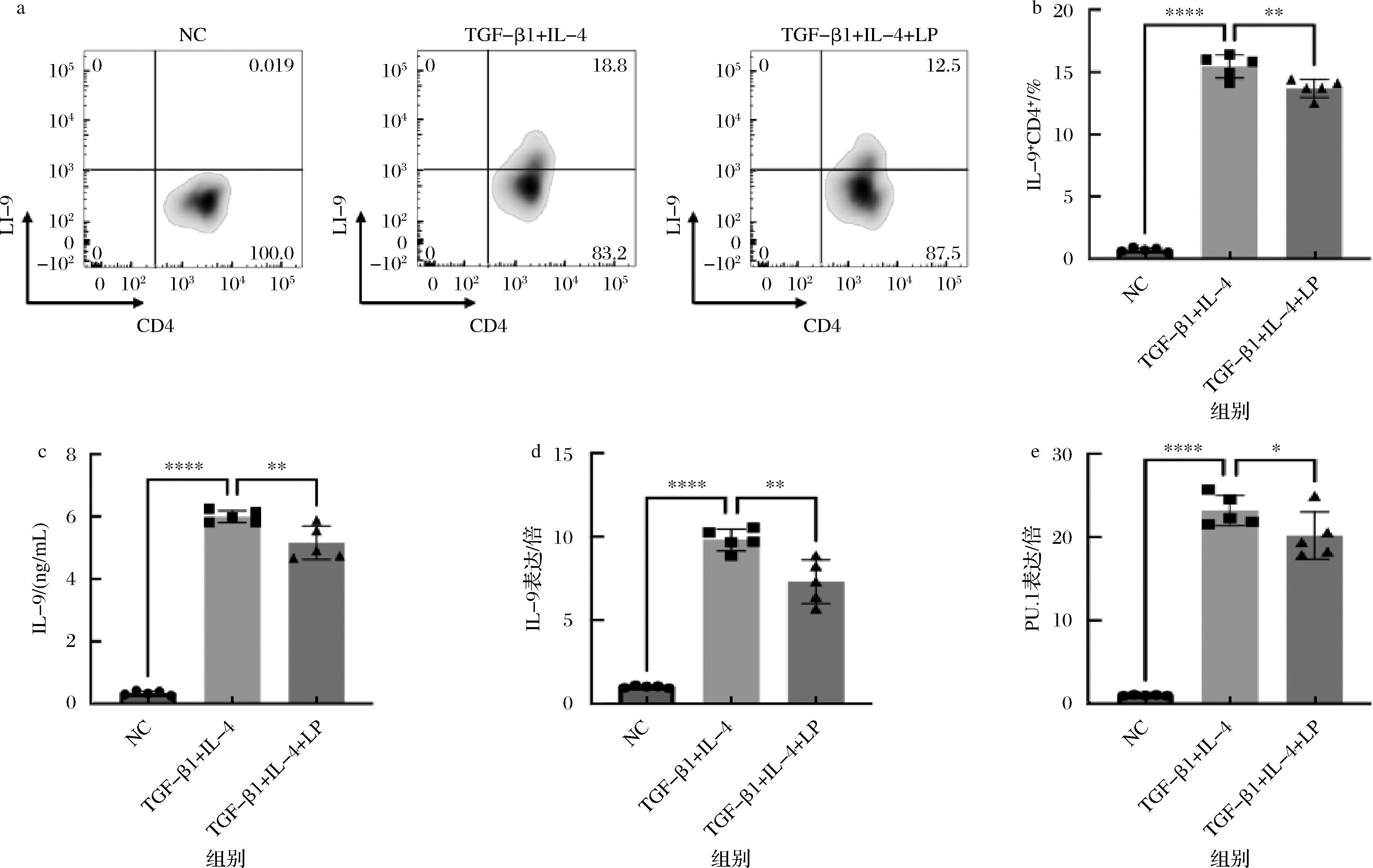
a-流式细胞术检测CD4+IL-9+细胞百分比;b-不同处理组CD4+IL-9+细胞百分比统计分析;c-ELISA检测培养上清液中IL-9浓度;d-实时荧光定量PCR检测IL-9 mRNA表达水平;e-实时荧光定量PCR检测PU.1 mRNA表达水平
图1 植物乳植杆菌抑制Th9细胞分化及IL-9和PU.1表达
Fig.1 L. plantarum inhibits Th9 cell differentiation and expression of IL-9 and PU.1
注:NC:阴性对照组;TGF-β1+IL-4:Th9细胞诱导组;TGF-β1+IL-4+LP:植物乳植杆菌干预组。数据以“平均数±标准差”表示(n=5),*P<0.05,**P<0.01,****P<0.000 1(下同)。
进一步通过RT-PCR检测Th9细胞特异性转录因子PU.1和效应分子IL-9的表达,结果显示LP干预可显著降低PU.1和IL-9的mRNA表达水平(IL-9:P<0.01;PU.1:P<0.05) (图1-d、图1-e)。
2.2 LP通过调控STING-NLRP3信号轴抑制Th9细胞分化
Western Blot结果显示,与对照组相比,LP干预组Th9细胞中STING、NLRP3以及pro-caspase-1的蛋白表达水平显著降低 (图2-a)。同时,LP干预可抑制Caspase-1的活化和IL-1β的产生(图2-b、图2-c)。为进一步验证STING-NLRP3信号轴在LP调控Th9细胞分化中的作用,采用STING特异性激动剂DMXAA和抑制剂H-151处理Th9细胞。结果显示,DMXAA可逆转LP对Th9细胞分化的抑制作用,而H-151可增强LP的抑制效应(图2-d、图2-e)。这些结果表明,LP通过调控STING-NLRP3信号轴抑制Th9细胞分化及IL-9的产生。
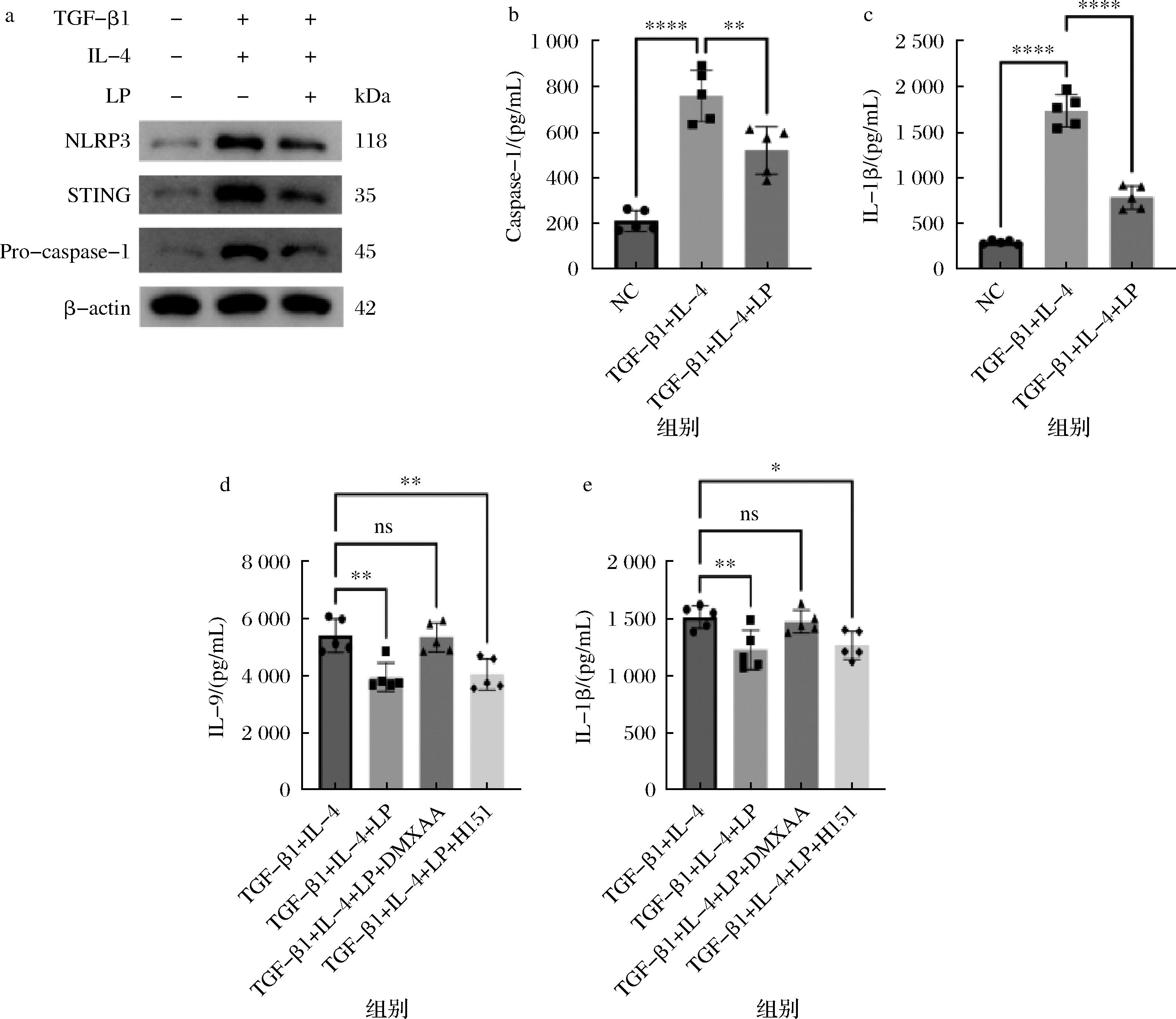
a-Western blot检测不同处理组STING、NLRP3、Pro-caspase-1蛋白表达水平(β-actin作为内参);b-ELISA检测培养上清液中Caspase-1蛋白水平;c-ELISA检测培养上清液中IL-1β水平;d-不同处理组培养上清液中IL-9水平,加入STING抑制剂(H-151)或NLRP3抑制剂(MCC950);e-不同处理组培养上清液中IL-1β水平,加入STING抑制剂或NLRP3抑制剂
图2 植物乳植杆菌抑制STING-NLRP3炎症小体通路激活及相关细胞因子分泌
Fig.2 L. plantarum inhibits the activation of the STING-NLRP3 inflammasome pathway and the secretion of related cytokines
注:****P<0.000 1,ns表示无显著差异(下同)。
2.3 LP通过调控STING-NLRP3-Th9轴改善T2DM合并TN小鼠模型的炎症反应
血清学检测结果显示,与对照组相比,T2DM+TN组小鼠血清中IL-9、IL-1β、IL-6、和TNF-α水平显著升高(P<0.000 1),而LP干预可显著降低这些炎症因子水平(P<0.01)(图3-a~图3-d)。流式细胞术结果显示,T2DM+TN组小鼠脾脏组织中CD4+IL-9+细胞比例显著增加(P<0.000 1),而LP干预可显著降低Th9细胞比例(P<0.001)(图3-e)。进一步通过Western Blot检测甲状腺组织中STING-NLRP3信号轴相关分子的表达,结果显示LP干预可显著降低STING、NLRP3、活化的Caspase-1在甲状腺组织中的表达 (图3-f)。这些结果表明,LP可通过调控STING-NLRP3-Th9轴改善T2DM合并TN小鼠模型的炎症反应。
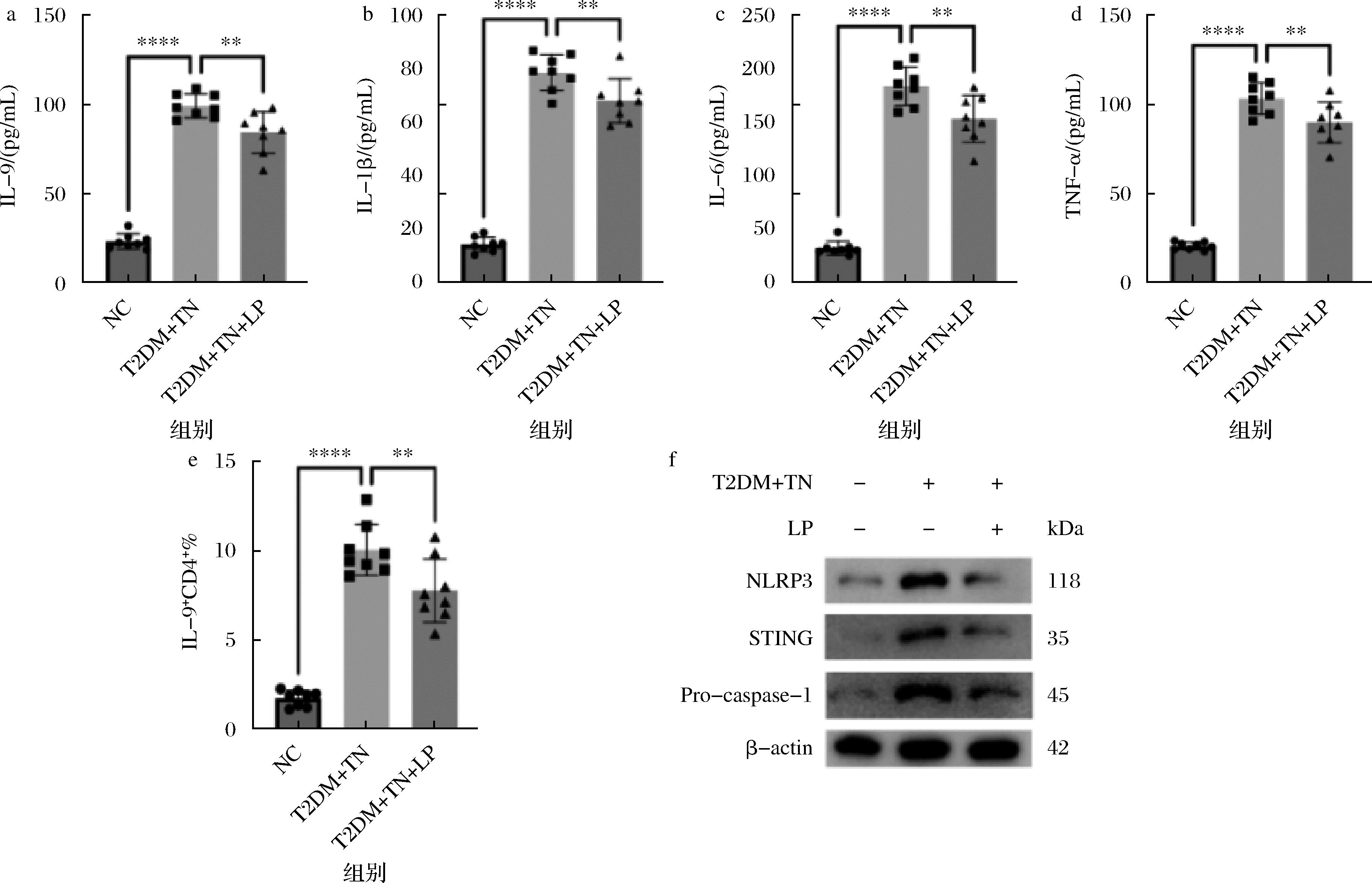
a-IL-9;b-IL-1β;c-IL-6;d-TNF-α;e-流式细胞术检测外周血中CD4+IL-9+细胞百分比;f-Western blot检测外周血单个核细胞中STING、NLRP3及Pro-caspase-1蛋白表达水平(β-actin作为内参)
图3 植物乳植杆菌降低T2DM合并甲状腺结节患者炎症因子水平及STING-NLRP3通路激活
Fig.3 L. plantarum reduces the levels of inflammatory factors and activation of the STING-NLRP3 pathway in T2DM patients with thyroid nodules
注:NC:健康对照组;T2DM+TN:2型糖尿病合并甲状腺结节模型组;T2DM+TN+LP:植物乳植杆菌干预治疗组。
数据以“平均数±标准差”表示(n=8),***P<0.001。
3 讨论与结论
本研究发现L. plantarum可以有效抑制Th9细胞分化及功能,并在T2DM合并TN小鼠模型中发挥免疫调节作用。研究结果提示,这一作用可能与STING-NLRP3信号通路的调节有关,为理解益生菌在免疫调节中的作用提供了新的机制,也为糖尿病相关甲状腺疾病的防治提供了新的潜在靶点。
NLRP3炎症小体是天然免疫系统的重要组成部分,在多种疾病的发生发展中起关键作用[5]。本研究发现,L. plantarum可显著抑制Th9细胞中NLRP3的表达及其下游Caspase-1的活化和IL-1β的产生。L. plantarum AR113株可通过下调TLR4/MyD88/NF-κB信号通路来抑制DSS诱导的结肠炎症反应,该信号通路与NLRP3炎症小体激活密切相关[18]。近年来,STING被认为是调控NLRP3炎症小体活化的重要上游分子。有研究证实,STING可以直接与NLRP3相互作用,促进NLRP3在内质网中的定位,并通过降低NLRP3的泛素化水平来促进炎症小体的活化[19]。此外,LI等[20]通过免疫共沉淀实验进一步证实了STING与NLRP3存在直接的物理结合,这种相互作用是激活NLRP3炎症小体途径的关键机制。研究发现,L. plantarum干预可降低Th9细胞中STING的表达,并减弱STING与NLRP3的相互作用,提示L. plantarum可能通过抑制STING-NLRP3信号轴调控Th9细胞分化。
Th9细胞是一类新型的CD4+辅助T细胞亚群,主要分泌IL-9,在多种炎症性疾病中发挥重要作用[21]。多项研究表明,Th9细胞参与多种疾病的发生发展过程,包括过敏性疾病、自身免疫性疾病、炎症性肠病和肿瘤等[22]。在炎症性肠病中,Th9细胞通过分泌促炎因子IL-9增强肠道炎症反应,破坏肠道屏障功能,促进疾病进展。本研究发现,L. plantarum干预可显著抑制体外诱导的Th9细胞分化及IL-9的表达,这可能与L. plantarum抑制STING-NLRP3信号轴活化有关。进一步研究发现,STING特异性激动剂DMXAA可逆转L. plantarum对Th9细胞分化的抑制作用,而STING抑制剂H-151可增强L. plantarum的抑制效应,证实了STING-NLRP3信号轴在L. plantarum调控Th9细胞分化中的关键作用。
T2DM与甲状腺疾病之间确实存在复杂而密切的联系,这种关联已被多项研究证实[23]。在T2DM患者中,促炎细胞因子如IL-6和高敏C反应蛋白(high-sensitivity C-reactive protein,hsCRP)水平升高,这些炎症因子不仅参与胰岛素抵抗的形成,也能影响甲状腺功能[24]。本研究构建了T2DM合并TN小鼠模型,发现模型小鼠血清中IL-9、IL-1β等炎症因子水平升高,脾脏组织中Th9细胞比例增加,甲状腺组织中STING、NLRP3表达增加。L. plantarum干预可改善这些炎症指标,降低Th9细胞比例,提示L. plantarum通过调控STING-NLRP3-Th9轴改善T2DM合并TN的炎症反应。
L. plantarum作为益生菌可通过多种机制调节免疫反应,包括调节肠道菌群组成、促进短链脂肪酸产生、增强肠道屏障功能等[17,25-27]。虽然观察到L. plantarum干预可以调节STING-NLRP3信号通路相关分子的表达,但这一现象可能是L. plantarum调节Th9细胞功能的结果之一,而非唯一的作用机制。益生菌发挥免疫调节作用是一个复杂的多因素过程,涉及肠道菌群平衡、代谢产物调节、肠道屏障功能改善等多个方面。L. plantarum可能通过产生特定的代谢产物如短链脂肪酸,或通过调节肠道微环境pH值、竞争性抑制病原菌生长等机制,间接影响免疫细胞的分化和功能。研究显示,L. plantarum调节STING-NLRP3信号轴可能是其免疫调节作用的新机制之一。此外,小肠微生态环境的稳态对维持全身免疫平衡至关重要[28],L. plantarum可能通过改善肠道微生态环境间接影响甲状腺功能。
本研究存在一些局限性:首先,主要在体外和小鼠模型中观察了L. plantarum对STING-NLRP3-Th9轴的调控作用,这些发现是否可以外推到人体尚需进一步研究;其次,L. plantarum调控STING-NLRP3信号轴的具体分子机制还需深入探究;最后,L. plantarum干预的最佳剂量和时间窗尚未确定,这需要更多的实验来优化。
综上所述,本研究首次揭示了植物乳植杆菌可通过调控STING-NLRP3信号轴抑制Th9细胞分化及功能,减轻T2DM合并TN的炎症反应。这一发现为益生菌在免疫相关疾病中的应用提供了新的理论基础,也为糖尿病相关甲状腺疾病的防治提供了新的思路和方法。未来研究应进一步探究L. plantarum调控STING-NLRP3信号轴的分子机制,以及在临床应用中的可行性。
[1] TOULIS K, TSEKMEKIDOU X, POTOLIDIS E, et al.Thyroid autoimmunity in the context of type 2 diabetes mellitus:Implications for vitamin D[J].International Journal of Endocrinology, 2015, 2015:710363.
[2] ZHENG Y, LEY S H, HU F B.Global aetiology and epidemiology of type 2 diabetes mellitus and its complications[J].Nature Reviews Endocrinology, 2018, 14(2):88-98.
[3] WANG X, BAO W, LIU J, et al.Inflammatory markers and risk of type 2 diabetes:A systematic review and meta-analysis[J].Diabetes Care, 2013, 36(1):166-175.
[4] FERRARI S M, FALLAHI P, GALDIERO M R, et al.Immune and inflammatory cells in thyroid cancer microenvironment[J].International Journal of Molecular Sciences, 2019, 20(18):4413.
[5] SWANSON K V, DENG M, TING J P Y.The NLRP3 inflammasome:Molecular activation and regulation to therapeutics[J].Nature Reviews Immunology, 2019, 19(8):477-489.
[6] REN W X, SUN Y, ZHAO L, et al.NLRP3 inflammasome and its role in autoimmune diseases:A promising therapeutic target[J].Biomedicine &Pharmacotherapy, 2024, 175:116679.
[7] KELLEY N, JELTEMA D, DUAN Y H, et al.The NLRP3 inflammasome:An overview of mechanisms of activation and regulation[J].International Journal of Molecular Sciences, 2019, 20(13):3328.
[8] ZHANG Z L, ZHOU H F, OUYANG X H, et al.Multifaceted functions of STING in human health and disease:From molecular mechanism to targeted strategy[J].Signal Transduction and Targeted Therapy, 2022, 7:394.
[9] HE X, WEDN A, WANG J, et al.IUPHAR ECR review:The cGAS-STING pathway:Novel functions beyond innate immune and emerging therapeutic opportunities[J].Pharmacological Research, 2024, 201:107063.
[10] LI N, ZHOU H, WU H M, et al.STING-IRF3 contributes to lipopolysaccharide-induced cardiac dysfunction, inflammation, apoptosis and pyroptosis by activating NLRP3[J].Redox Biology, 2019, 24:101215.
[11] ZHONG W Z, RAO Z Q, RAO J H, et al.Aging aggravated liver ischemia and reperfusion injury by promoting STING-mediated NLRP3 activation in macrophages[J].Aging Cell, 2020, 19(8):e13186.
[12] LI J H, CHEN S Q, XIAO X, et al.IL-9 and Th9 cells in health and diseases:From tolerance to immunopathology[J].Cytokine &Growth Factor Reviews, 2017, 37:47-55.
[13] ZHANG W C, TANG T T, NIE D A, et al.IL-9 aggravates the development of atherosclerosis in ApoE-/ - mice[J].Cardiovascular Research, 2015, 106(3):453-464.
[14] MAANIITTY E, SINISILTA S, JALKANEN J, et al.Distinct circulating cytokine levels in patients with angiography-proven coronary artery disease compared to disease-free controls[J].International Journal of Cardiology Cardiovascular Risk and Prevention, 2024, 22:200307.
[15] SIMONOVIC S Z, MIHALJEVIC O, MAJSTOROVIC I, et al.Cytokine production in peripheral blood cells of patients with differentiated thyroid cancer:Elevated Th2/Th9 cytokine production before and reduced Th2 cytokine production after radioactive iodine therapy[J].Cancer Immunology, Immunotherapy, 2015, 64(1):75-82.
[16] WANG J, JI H F, WANG S X, et al.Probiotic Lactobacillus plantarum promotes intestinal barrier function by strengthening the epithelium and modulating gut microbiota[J].Frontiers in Microbiology, 2018, 9:1953.
[17] ZENG Z B, HUANG Z H, YUE W, et al.Lactobacillus plantarum modulate gut microbiota and intestinal immunity in cyclophosphamide-treated mice model[J].Biomedicine &Pharmacotherapy, 2023, 169:115812.
[18] XIA Y J, CHEN Y, WANG G Q, et al.Lactobacillus plantarum AR113 alleviates DSS-induced colitis by regulating the TLR4/MyD88/NF-κB pathway and gut microbiota composition[J].Journal of Functional Foods, 2020, 67:103854.
[19] SPECTOR L, SUBRAMANIAN N.Revealing the dance of NLRP3:Spatiotemporal patterns in inflammasome activation[J].Immunometabolism, 2025, 7(1):e00053.
[20] LI W Y, SHEN N, KONG L Q, et al.STING mediates microglial pyroptosis via interaction with NLRP3 in cerebral ischaemic stroke[J].Stroke and Vascular Neurology, 2024, 9(2):153-164.
[21] CHEN J, GUAN L, TANG L, et al.T helper 9 cells:A new player in immune-related diseases[J].DNA and Cell Biology, 2019, 38(10):1040-1047.
[22] VYAS S P, GOSWAMI R.A decade of Th9 cells:Role of Th9 cells in inflammatory bowel disease[J].Frontiers in Immunology, 2018, 9:1139.
[23] MOHAMMED HUSSEIN S M, ABDELMAGEED R M.The relationship between type 2 diabetes mellitus and related thyroid diseases[J].Cureus, 2021, 13(12):e20697.
[24] EOM Y S, WILSON J R, BERNET V J.Links between thyroid disorders and glucose homeostasis[J].Diabetes &Metabolism Journal, 2022, 46(2):239-256.
[25] YANG B, YUE Y, CHEN Y, et al.Lactobacillus plantarum CCFM1143 alleviates chronic diarrhea via inflammation regulation and gut microbiota modulation:A double-blind, randomized, placebo-controlled study[J].Frontiers in Immunology, 2021, 12:746585.
[26] WU Y Q, LI A, LIU H W, et al.Lactobacillus plantarum HNU082 alleviates dextran sulfate sodium-induced ulcerative colitis in mice through regulating gut microbiome[J].Food &Function, 2022, 13(19):10171-10185.
[27] KIM H I, KIM J K, KIM J Y, et al.Lactobacillus plantarum LC27 and Bifidobacterium longum LC67 simultaneously alleviate high-fat diet-induced colitis, endotoxemia, liver steatosis, and obesity in mice[J].Nutrition Research, 2019, 67:78-89.
[28] ZHENG D P, LIWINSKI T, ELINAV E.Interaction between microbiota and immunity in health and disease[J].Cell Research, 2020, 30(6):492-506.