作为一种传统的蒸馏酒精饮料,白酒有着2 000多年的历史,是中国发酵产品的重要组成部分[1]。根据香气特征的差异,白酒被划分为12种香型[2],其中酱香型白酒以其独特风味特征占据了中国白酒市场30%左右的份额[3]。作为酱香型白酒酿造的核心因素,高温大曲主要以小麦为原料,经周围环境和原材料中自然引入的多样化微生物固态发酵而成[4],该过程通常包括40 d的自然发酵阶段和3~6个月的储存阶段[5]。因此,在发酵过程中,由于环境以及温度、水分和酸度等条件的不同,大曲微生物群落结构演替存在显著差异。王晓丹等[6]对遵义地区3个不同酒厂高温大曲菌落组成进行研究发现,珍酒高温大曲样品中细菌物种比较丰富,优势菌属的含量较茅台高温大曲样品存在明显差异;ZHANG等[7]对采集自湖北省和贵州省高温大曲的微生物群落结构对比发现,解淀粉芽孢杆菌(Bacillus amyloliquefaciens)、贝莱斯芽孢杆菌(Bacillus velezensis)和索诺拉沙漠芽胞杆菌(Bacillus sonorensis)在贵州省高温大曲中显著富集。由此可见,地域因素显著影响大曲微生物群落结构,而微生物作为发酵食品的重要组成部分,其代谢活动对白酒质地和风味至关重要[8]。
作为“中国酒城”,四川省泸州市凭借其温和的气候、充沛的雨量以及“地球同纬度上最适合酿造优质纯正蒸馏酒的生态区”这个独特的地理位置,成为了长江上游名酒带的核心区域[9]。山东省作为中国白酒黄淮产区的重要组成部分,是白酒产销大省之一[10],其中济宁市坐落于山东省西南部,地处黄淮海平原与鲁中南山地交接地带,降水相对较少、气温偏低、四季分明[11]。由此可见,泸州和济宁的地理位置和环境气候存在明显差异,这些差异决定了两地微生物群落的构成,从而影响了当地白酒的品质与风味特征。基于此,为探究地域因素对高温大曲微生物群落结构的影响,并探讨微生物与大曲质量指标之间的相关性,本研究首先从泸州市和济宁市2个地区分别采集了10份高温大曲样品,采用纯培养技术、Pacific Biosciences(PacBio)公司的单分子实时(single molecule real-time, SMRT)测序技术和常规理化分析手段对细菌群落结构和理化指标进行了测定,以期为解析地域因素对高温大曲品质影响提供数据支撑,同时为强化大曲提供菌株支持。
1 材料与方法
1.1 材料与试剂
营养琼脂培养基(nutrient agar, NA)、MRS培养基、CaCO3,国药集团化学试剂有限公司;菌株扩增引物27F/1495R,上海桑尼生物科技有限公司;TGuide S96磁珠法土壤/粪便基因组DNA提取试剂盒,天根生化科技(北京)有限公司;SMRTbell Template Prep Kit建库试剂盒、SMRTbell Template Prep Kit建库试剂盒,PacBio公司;16S全长引物27F(16S-F)和1492R(16S-R),北京百灵克生物科技有限责任公司;NaOH、HCl、次甲基蓝、葡萄糖、碘、可溶性淀粉、无水乙醇、甲醛溶液(均为分析纯),国药集团化学试剂有限公司。
1.2 仪器与设备
DG250厌氧工作站,英国Don Whitley公司;梯Veriti96-Well度基因扩增仪,美国Applied Biosystems公司;Synergy HTX酶标仪,Gene Company Limited公司;DYCP-31E电泳仪,北京六一仪器厂;TA.XT Plus物性测试仪,英国Stable Micro System公司;UltraScan PRO全自动多功能色度仪,美国Hunterlab公司;NMI20-025V-I型核磁共振成像分析仪,上海纽迈电子科技有限公司;K1100凯氏定氮仪,海能未来技术集团股份有限公司;AND日本MS-70快速水分测定仪,上海右一仪器有限公司;AW-1水分活度仪,无锡碧波电子设备厂;R920机架式服务器,美国DELL公司。
1.3 实验方法
1.3.1 样本采集
本研究从四川省泸州市和山东省济宁市收集了20份高温大曲样品,分别标记为LZ1~10和JN1~10,考虑到样品的科学性和代表性,从曲房的中间和四周进行随机取样。将大曲样品使用小型粉碎机破碎混合后,分装入无菌自封袋进行包装和标记,储存于-40 ℃冰箱备用。
1.3.2 乳酸菌和芽孢杆菌的分离鉴定
首先通过连续稀释和平板涂布分离出各种乳酸菌和芽孢杆菌菌落,其次通过三区域划线,将单菌落分别接种在MRS和NA培养基平板上进行菌落纯化。纯化菌落经过试剂盒进行DNA提取后,使用通用引物27F/1495R对乳酸菌和芽孢杆菌菌株进行16S序列分析。测序序列返回进行拼接和去除引物后,在美国国立生物技术信息中心(national center for biotechnology information, NCBI)网站上进行BLAST比对。最后将菌株序列上传至GenBank数据库中,乳酸菌登录号为PQ312749~PQ312762和PQ312770~PQ312771,泸州高温大曲芽孢杆菌登录号为PQ312809~PQ312839,济宁高温大曲芽孢杆菌登录号为PQ314936~PQ314973和PQ314981~PQ314983。
1.3.3 微生物计数
参照GB 4789.2—2022《食品安全国家标准 食品微生物学检验 菌落总数测定》和GB 4789.35—2023《食品安全国家标准 食品微生物学检验 乳酸菌检验》分别对纳入本研究20份高温大曲的菌落总数和乳酸菌总数进行统计。
1.3.4 PacBio SMRT测序与生物信息学处理
使用TGuide S96 磁珠法土壤/粪便基因组DNA提取试剂盒,根据说明书对大曲粉末样品的DNA进行提取。为确保DNA提取的质量和数量,使用酶标仪进行浓度检测。随后使用16S全长引物27F(16S-F)和1492R(16S-R)对DNA进行PCR,使用1.8%的琼脂糖凝胶电泳对产物完整性进行检测。PCR产物进行分级混样后,使用SMRTbell Template Prep Kit建库试剂盒进行文库构建,反应产物进行纯化后置于Sequel II测序仪上进行上机测序。测序下机数据基于QIIME(v1.9.0)平台进行生物信息学处理,首先使用PyNAST软件根据标签将序列进行分配,然后通过FLASH软件进行序列拼接,使用uclust工具将相似度≥97%的序列聚类到相同的操作分类单元(operational taxonomic units, OTU),通过UCHIME算法(v8.1)去除嵌合体序列,最后选用Silva数据库(http://www.arb-silva.de)对OTU代表序列进行注释。采用Chao1指数和Shannon指数评估2个地区高温大曲细菌群落结构的α多样性,采用主坐标分析(principal coordinates analysis, PCoA)对β多样性进行分析,运用PERMANOVA比较组间差异。
1.3.5 高温大曲质构、色度、水分及理化指标的测定
使用物性测试仪的P2N探头对大曲样品的曲皮和曲心硬度进行测定;使用色度仪的反射模式对大曲样品的色泽指标(L*值、a*值、b*值)进行测定;参照GB 5009.5—2025《食品安全国家标准 食品中蛋白质的测定》使用凯氏定氮仪对大曲样品的蛋白质含量进行测定;使用水分活度仪和水分测定仪对水分活度和水分含量进行测定;参照QB/T 4257—2011《酿酒大曲通用分析方法》对大曲样品的理化指标进行测定。
使用核磁共振成像分析仪对结合水、不易流动水和自由水含量进行测定,参考王智伟等[12]的方法并稍作修改,样品为粉碎混匀的大曲粉末,测试条件为:重复采样等待时间(time wait, TW)为2 500 ms,样品采集频率(sampling bandwidth, SW)为250 kHz,抽样次数(number sampling, NS)为2,回波时间(echo time, TE)为0.200 ms,回波个数(number of echoes, NECH)为2 000。样品测试数据经系统软件反演后,获得对应大曲的水分分布结果。
1.4 数据处理与可视化
使用MEGA 5.0中的邻接法(neighbor-joining method, NJ)构建系统发育树,以确定乳酸菌和芽孢杆菌分离株的分类学地位;使用多元方差分析(multivariate analysisof variance, MANOVA)对物种含量及理化数据进行显著性分析;使用Prism进行微生物计数、α多样性指数和大曲质量指标柱形图的绘制;使用R软件包ggplot2对优势细菌门和种进行堆积柱形图的绘制;使用R软件包microeco进行线性判别分析(linear discriminant analysis effect size,LEfSe),以识别2个地区高温大曲之间存在显著差异的物种;使用R软件包vegan进行菌群与品质指标之间相关性的普氏分析;使用SAS软件进行相关性R和P值的计算,使用Gephi软件进行相关性网络图的绘制。
2 结果与分析
2.1 两个地区高温大曲中可培养乳酸菌和芽孢杆菌分析
从泸州和济宁地区采集的20份高温大曲样品中共分离得到88个分离株,经PCR扩增、测序、引物去除和BLAST分析后,结果显示72株属于芽孢杆菌,16株属于乳酸菌。本研究进一步将代表分离株序列与其模式菌株构建了系统发育树,同时对2个地区分离株多样性进行统计分析,结果如图1所示。
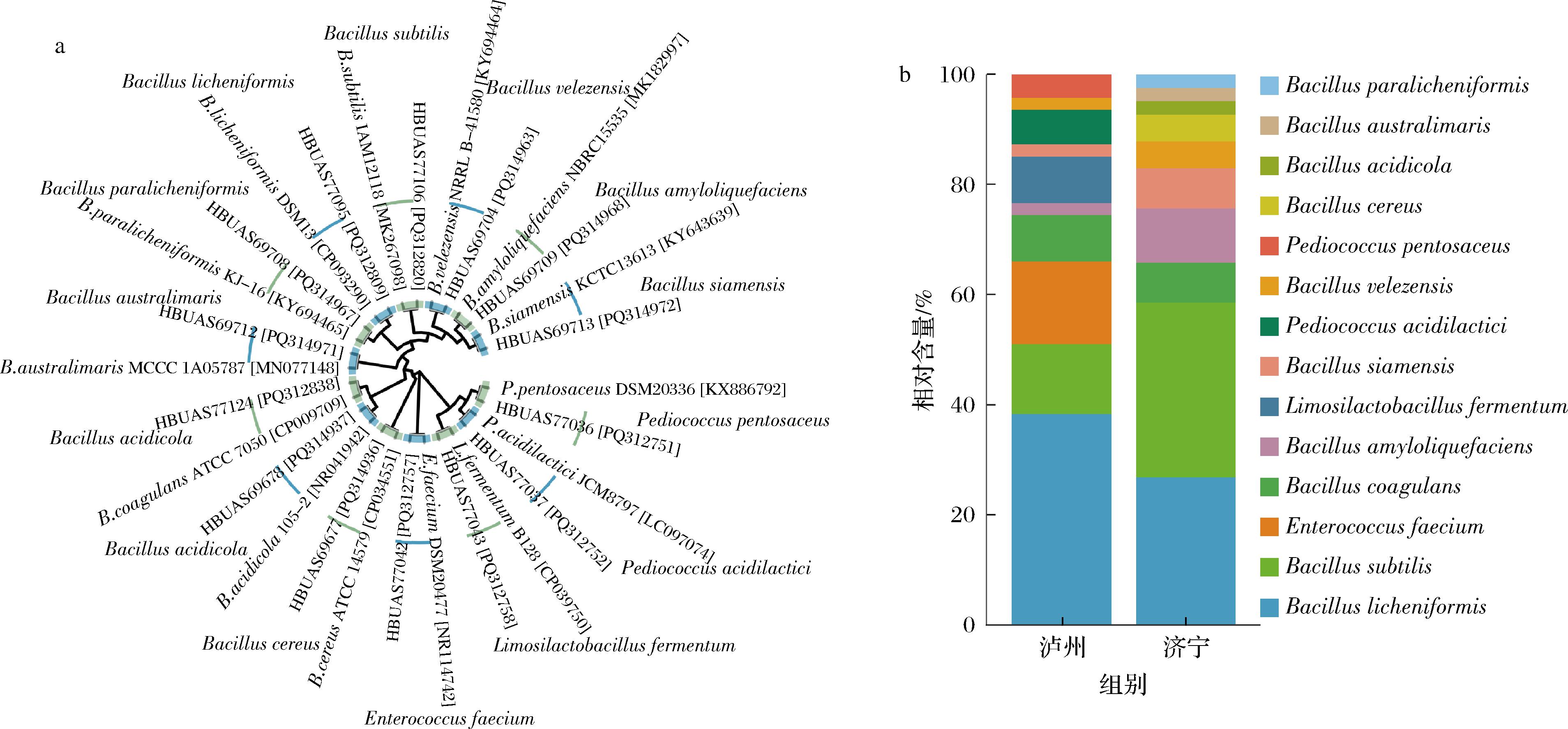
a-系统发育树;b-各地区分菌情况
图1 系统发育树和各地区分菌情况统计
Fig.1 Phylogenetic tree and statistical analysis of bacterial distribution in different regions
由图1-a可知,88个分离株隶属于4个属下的14个种,分别是隶属于肠球菌属(Enterococcus)的粪肠球菌(E.faecium);隶属于粘液乳杆菌属(Limosilactobacillus)的发酵粘液乳杆菌(L.fermentum);隶属于片球菌属(Pediococcus)的乳酸片球菌(P.acidilactici)和戊糖片球菌(P.pentosaceus);隶属于芽孢杆菌属(Bacillus)的地衣芽孢杆菌(B.licheniformis)、枯草芽孢杆菌(B.subtilis)、凝结芽孢杆菌(B.coagulans)、暹罗芽胞杆菌(B.siamensis)、B.velezensis、B.amyloliquefaciens、蜡样芽孢杆菌(B.cereus)、酸居芽孢杆菌(B.acidicola)、南中国海芽胞杆菌(B.australimaris)和副地衣芽孢杆菌(B.paralicheniformis)。为分析不同地区大曲样品可培养微生物的多样性和丰富度,本研究进一步对2个地区不同菌种的相对含量进行了计算。由图1-b可知,采集自泸州地区的高温大曲中分离得到47株菌隶属于4个属下的10个种,分别为E.faecium、L.fermentum、P.acidilactici、P.pentosaceus、B.licheniformis、B.subtilis、B.coagulans、B.siamensis、B.velezensis和B.amyloliquefaciens,分别占总分离株的14.89%、8.51%、6.38%、4.25%、38.30%、12.77%、8.51%、2.13%、2.13%和2.13%。由此可见,E.faecium和B.licheniformis分别为泸州地区高温大曲的优势可培养乳酸菌和芽孢杆菌。相比之下,从济宁地区高温大曲样品分离的41株菌中,未发现乳酸菌的存在,而芽孢杆菌的种类更为丰富,共计分离得到10个菌种,分别为B.subtilis、B.licheniformis、B.amyloliquefaciens、B.coagulans、B.siamensis、B.velezensis、B.cereus、B.acidicola、B.australimaris和B.paralicheniformis,分别占总分离株的31.71%、26.83%、9.76%、7.31%、7.31%、4.88%、4.88%、2.44%、2.44%和2.44%。由此可见,济宁地区高温大曲的优势可培养芽孢杆菌为B.subtilis。芽孢杆菌属(Bacillus)微生物具有良好的耐热性、耐酸性和耐氧性,并且具有分泌淀粉酶、蛋白酶、脂肪酶的能力,在风味化合物的产生中起着重要作用[13]。YAN等[14]研究发现,将B.licheniformis和B.subtilis接种到液体大曲培养基中会增加培养基中有机酸的产生;WANG等[15]还发现,大曲中芳香化合物的增加可能与B.licheniformis的含量有关。因此,芽孢杆菌的丰度对高温大曲的品质具有重要影响。
综上可知,不同来源高温大曲中可培养微生物存在一定差异,如乳酸菌仅在采集自泸州地区的高温大曲中分离得到,而B.cereus、B.acidicola、B.australimaris、B.paralicheniformis仅在采集自济宁地区的高温大曲中分离得到。据报道,一般情况下乳酸菌对于高温的耐受性较差[16],而芽孢杆菌因孢子的特性更易在高温条件下存活[17],基于此我们推测,相较于泸州地区高温大曲样品,济宁地区高温大曲样品的制曲温度或者贮藏温度可能更低,所以给乳酸菌的生长创造了条件。可见地域因素对可培养微生物种类分布存在影响,说明对不同地区高温大曲细菌群落结构进行解析是极为必要的。
2.2 两个地区高温大曲细菌群落α和β多样性分析
由微生物计数结果可知(图2-a、图2-b),2种大曲的菌落总数和乳酸菌总数存在显著差异(P<0.05)。因此,为了进一步分析不同地区高温大曲微生物群落的差异,本研究应用PacBio SMRT测序技术,对20份高温大曲样品细菌群落结构进行测序,最后共获得268 335条高质量序列,按照97%的相似度,所有序列被划分为5 240个OTU。为解析微生物群落的多样性特征,本研究进一步计算了基于OTU水平的α和β多样性指数,结果如图2所示。α多样性指数主要用于评估微生物群落的丰富度和均匀度,β多样性指数则反映了不同分组之间微生物群落的差异程度。
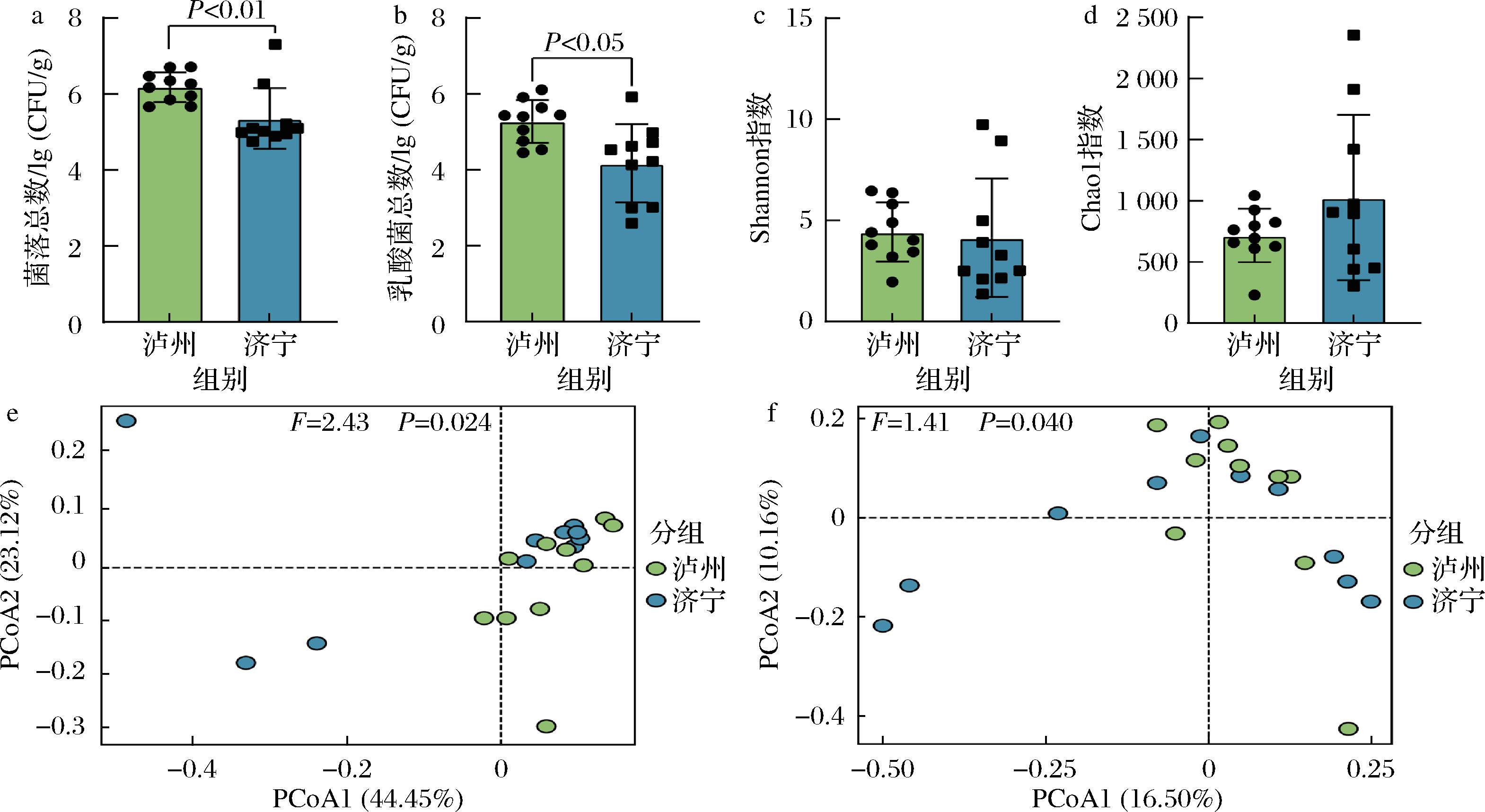
a-菌落总数;b-乳酸菌总数;c-Shannon指数;d-Chao1指数;e-基于加权UniFrac距离PCoA;f-基于非加权UniFrac距离PCoA
图2 高温大曲微生物计数、α和β多样性指数分析
Fig.2 Analysis of microbial counts, α-diversity, and β-diversity indices in high-temperature Daqu
由图2-c和图2-d可知,泸州地区高温大曲样品的Shannon和Chao1指数平均值分别为4.43和717.29,济宁地区高温大曲样品的Shannon和Chao1指数平均值分别为4.15和1 026.54,经Mann-Whitney检验获得的组间总体差异的P>0.05,表明2个地区高温大曲细菌群落多样性和丰富度之间没有显著差异。由图2-e和图2-f可知,PERMANOVA检验显示,无论是否将物种丰度纳入考虑范围,2个地区高温大曲样品细菌群落结构均存在显著差异(P<0.05),表明在2个地区高温大曲样品之间,无论是低丰度物种还是高丰度物种,其分布和组成均存在显著差异。
2.3 两个地区高温大曲细菌群落结构分析
基于SILVA数据库在门、纲、目、科、属和种分类水平上对高温大曲获得的OTU进行物种注释,结果显示5 240个OTU被鉴定为39个门、70个纲、108个目、255个科、620个属和760个种。将平均相对含量大于1%的物种定义为优势物种,基于门和种水平高温大曲细菌群落结构分析如图3所示。
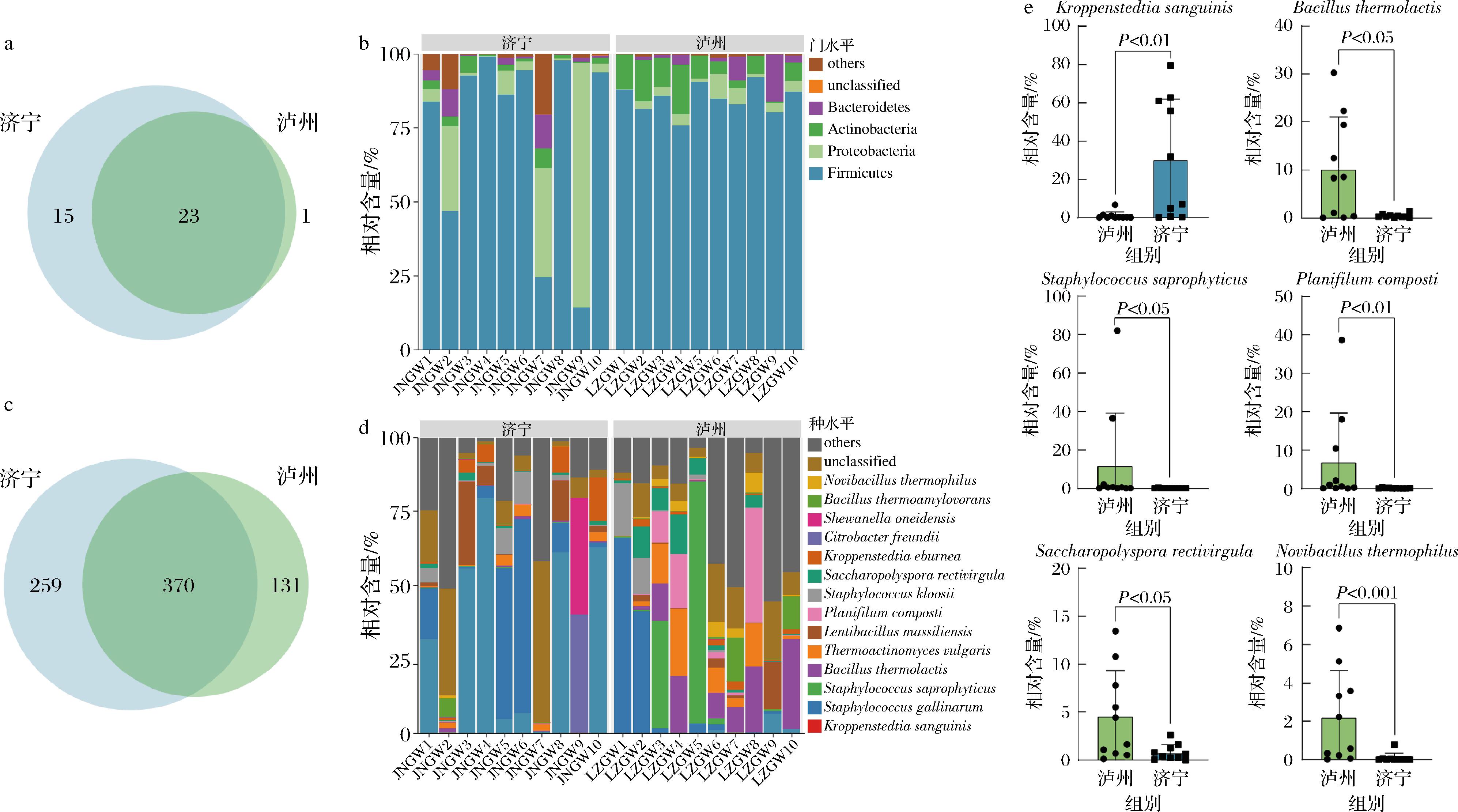
a-门水平韦恩图;b-门水平堆积柱形图;c-种水平韦恩图;d-种水平堆积柱形图;e-存在显著差异优势细菌种柱形图
图3 高温大曲群落结构分析
Fig.3 Analysis of community structure of high-temperature Daqu
由图3-a可知,高温大曲样品共检测出39个细菌门,其中2个地区共有细菌门有23个,占细菌门总数的58.97%,采集自泸州地区的高温大曲具有1个特有细菌门,而采集自济宁地区的高温大曲具有15个特有细菌门,亦证明济宁地区高温大曲细菌群落丰富度大于泸州地区高温大曲。由图3-b可知,在细菌门水平上,共有4个优势细菌门,分别为厚壁菌门(Firmicutes)、变形菌门(Proteobacteria)、放线菌门(Actinobacteria)和拟杆菌门(Bacteroidetes),平均相对含量分别为79.27%、10.04%、5.22%和3.15%。由此可见,在高温大曲细菌菌群的组成上,Firmicutes占绝对优势。经Mann-Whitnay检验发现,采集自泸州地区的高温大曲中Actinobacteria的相对含量显著偏高(P<0.05),平均相对含量为7.90%,而在采集自济宁地区的高温大曲中仅为2.54%。
由图3-c可知,在细菌种水平上,从20份大曲样本中共检测到760个细菌种,其中2个地区共有细菌种有370个,占细菌种总数的48.68%,采集自泸州地区的高温大曲独有细菌种131个,采集自济宁地区的高温大曲独有细菌种259个,进一步说明济宁地区高温大曲细菌群落丰富度较高。由图3-d可知,从20份大曲样本中共检测到14个优势细菌种,其中采集自泸州地区的高温大曲主要以腐生葡萄球菌(S.saprophyticus)、鸡葡萄球菌(S.gallinarum)和热乳芽孢杆菌(B.thermolactis)为主,平均相对含量分别为12.25%、11.55%和10.29%。Staphylococcus广泛分布在土壤、空气、水、灰尘和各种食物中[18],ZHENG等[19]研究亦发现S.saprophyticus在被视为南方大曲的生物标志物,泸州位于四川省东南部川渝黔滇结合部,在地理位置上属于我国南方,所以在大曲细菌结构上检测到S.saprophyticus的存在,而济宁位于山东省,属于我国北方,测序结果显示,纳入本研究的10份济宁地区高温大中S.saprophyticus的平均相对含量为0.07%,与ZHENG等[19]的结论一致。此外,XU等[20]研究发现,Staphylococcus可以产生芳香化合物,如3-甲基-1-丁醇、苯基乙醛、苯乙醇和异戊醇等,改善产品风味,同时Staphylococcus也会分泌酯酶,加速酯的形成。然而,目前还没有关于白酒酿造过程中S.saprophyticus的功能和安全性的报道。采集自济宁地区的高温大曲主要以血液克罗彭施泰特氏菌(Kroppenstedtia sanguinis)和S.gallinarum为主,平均相对含量分别为30.44%和15.09%。克罗彭斯特菌属(Kroppenstedtia)隶属于高温放线菌科(Thermoactinomycetaceae),能够代谢产生多种耐高温酶系,被认定为与脂肪酸生物合成相关的核心微生物[21],楚京嬴等[22]研究亦发现,Kroppenstedtia与有机杂环化合物、脂类及类脂分子以及苯环类等芳香类化合物含量均呈显著正相关。由图3-e可知,进一步经Mann-Whitney检验发现,采集自泸州地区的高温大曲中S.saprophyticus、B.thermolactis、Planifilum composti、直杆糖多孢菌(Saccharopolyspora rectivirgula)和嗜热新芽孢杆菌(Novibacillus thermophilus)的平均相对含量显著偏高(P<0.05),K.sanguinis的平均相对含量显著偏低(P<0.05),平均相对含量分别为12.25%、10.29%、7.10%、4.61%、2.23%和1.02%,其在采集自济宁地区的高温大曲中平均相对含量分别为0.07%、0.42%、0.07%、0.79%、0.09%和30.44%。
为进一步找到2个地区高温大曲的差异性细菌菌种,本研究进行了基于OTU水平的LEfSe分析,结果如图4所示。
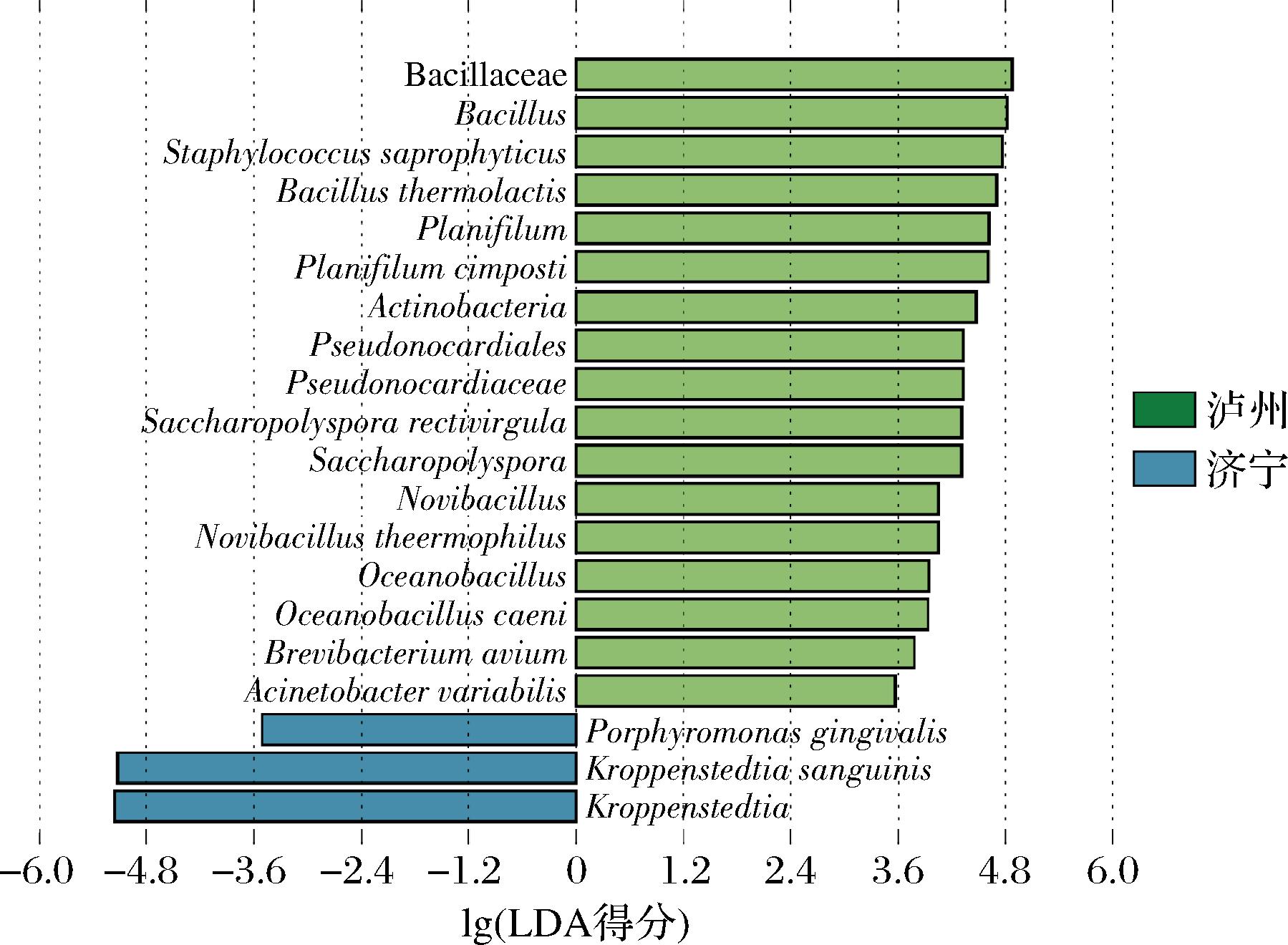
图4 两个地区差异物种分析
Fig.4 Analysis of species differences between two regions
由图4可知,当LDA>3.5分时,S.saprophyticus、B.thermolactis、P.composti、S.rectivirgula、N.theermophilus、淤泥大洋芽孢杆菌(Oceanobacillus caeni)、鸟短杆菌(Brevibacterium avium)和可变不动杆菌(Acinetobacter variabilis)等在采集自泸州地区的高温大曲中显著富集(P<0.05)。克罗彭斯特菌属(Kroppenstedtia)、牙龈卟啉单胞菌(Porphyromonas gingivalis)和K.sanguinis在采集自济宁地区的高温大曲中显著富集(P<0.05)。根据物种的LDA得分,可以将S.saprophyticus和K.sanguinis分别作为采集自泸州和济宁地区高温大曲的生物标志物。
2.4 两个地区高温大曲质构和色度指标分析
本研究首先对2个地区高温大曲的质构和色度进行了检测,结果如图5所示。
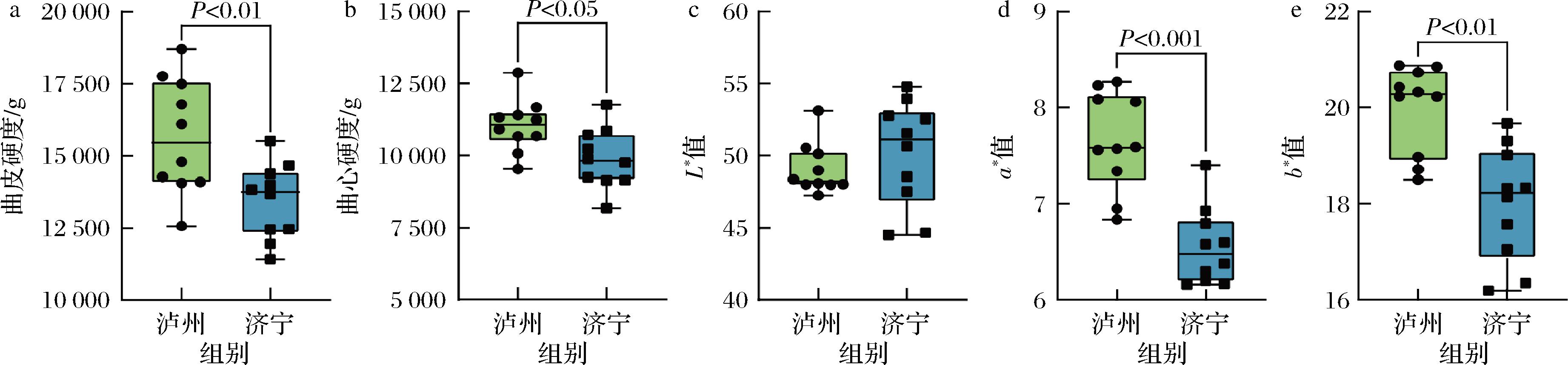
a-曲皮硬度;b-曲心硬度;c-L*;d-a*;e-b*
图5 高温大曲质构和色度指标分析
Fig.5 Analysis of texture and chromaticity indices of high-temperature Daqu
由图5-a和图5-b可知,泸州地区高温大曲样品的曲皮和曲心硬度较高,平均值分别为15 665、11 035 g,显著高于济宁地区高温大曲的13 436、9 891 g(P<0.05),说明泸州地区高温大曲的硬度更大。曲皮和曲心的硬度变化,一定程度上反映了制曲温度的高低,随着温度的升高,曲块整体变得更加坚硬,这可能是由于高温诱导的蛋白质变性、淀粉糊化等生物化学变化所致[23]。基于此我们推测,泸州地区高温大曲样品的制曲温度更高,与纯培养推测结果存在一致性。由图5-c~图5-e可知,泸州地区高温大曲样品的a*值和b*值极显著偏高(P<0.01),平均值分别为7.65和19.99,其在济宁地区高温大曲样品中平均值分别为6.55和18.00,说明相较于济宁高温大曲,采集自泸州地区的高温大曲在外观上偏绿偏蓝。随着温度的升高,美拉德反应加剧,促使黑色素沉积[24],因此制曲温度更高的泸州地区高温大曲的L*值偏低,而a*值、b*值显著偏高。综上可知,2个地区高温大曲样品在质构及色度上存在显著差异。
2.5 两个地区高温大曲水分指标分析
由图6-a和图6-b可知,泸州地区高温大曲样品的水分活度和水分含量之间差异不显著(P>0.05)。由图6-c和图6-d可知,2个地区高温大曲样品在结合水和不易流动水含量上存在显著差异(P<0.05),具体而言,泸州地区高温大曲样品的结合水含量为92.42%,不易流动水含量为5.68%,而济宁地区高温大曲样品的结合水含量为93.37%,不易流动水含量为4.34%。究其原因可能是,硬度的提升导致大曲结构更为紧密,透气性减弱,内部水分蒸发受阻[25],进而促进了不易流动水的累积。由图6-e可知,2个地区高温大曲样品自由水含量之间差异不显著(P>0.05)。
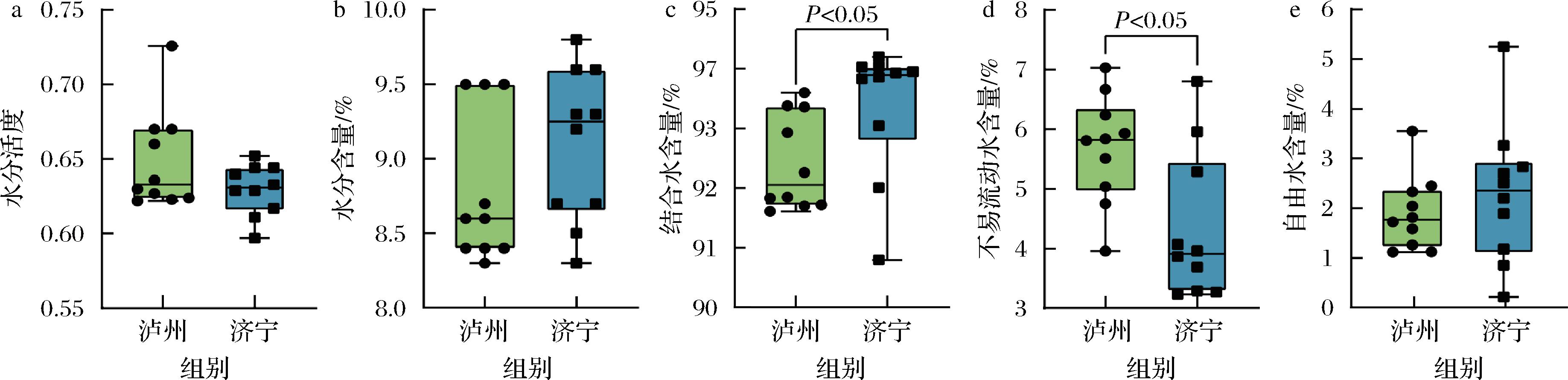
a-水分活度;b-水分含量;c-结合水含量;d-不易流动水含量;e-自由水含量
图6 高温大曲水分指标分析
Fig.6 Analysis of water content in high-temperature Daqu
2.6 两个地区高温大曲理化指标分析
由图7可知,仅有3个理化指标在2个地区高温大曲样品之间存在显著差异(P<0.05)。具体而言,济宁地区高温大曲的发酵力平均值为0.11 U,淀粉含量平均值为77.42 g/100 g,这2项指标均极显著高于泸州地区的0.03 U和74.14 g/100 g(P<0.01)。大曲淀粉含量可以反映大曲中能水解利用淀粉的微生物水平[22],通过对微生物群落结构分析我们发现,采集自泸州地区的高温大曲中蕴含着更多元化的芽孢杆菌,作为白酒功能微生物之一,Bacillus常见于各种类型的大曲中,能够促进淀粉的转化,从而产生用于酒精发酵的合适底物[26],这也解释了泸州地区高温大曲淀粉含量显著偏低的现象。同时,泸州地区高温大曲的灰分显著偏高(P<0.000 1),平均值为2.11 g/100 g,而济宁地区高温大曲样品的灰分平均值为1.54 g/100 g。
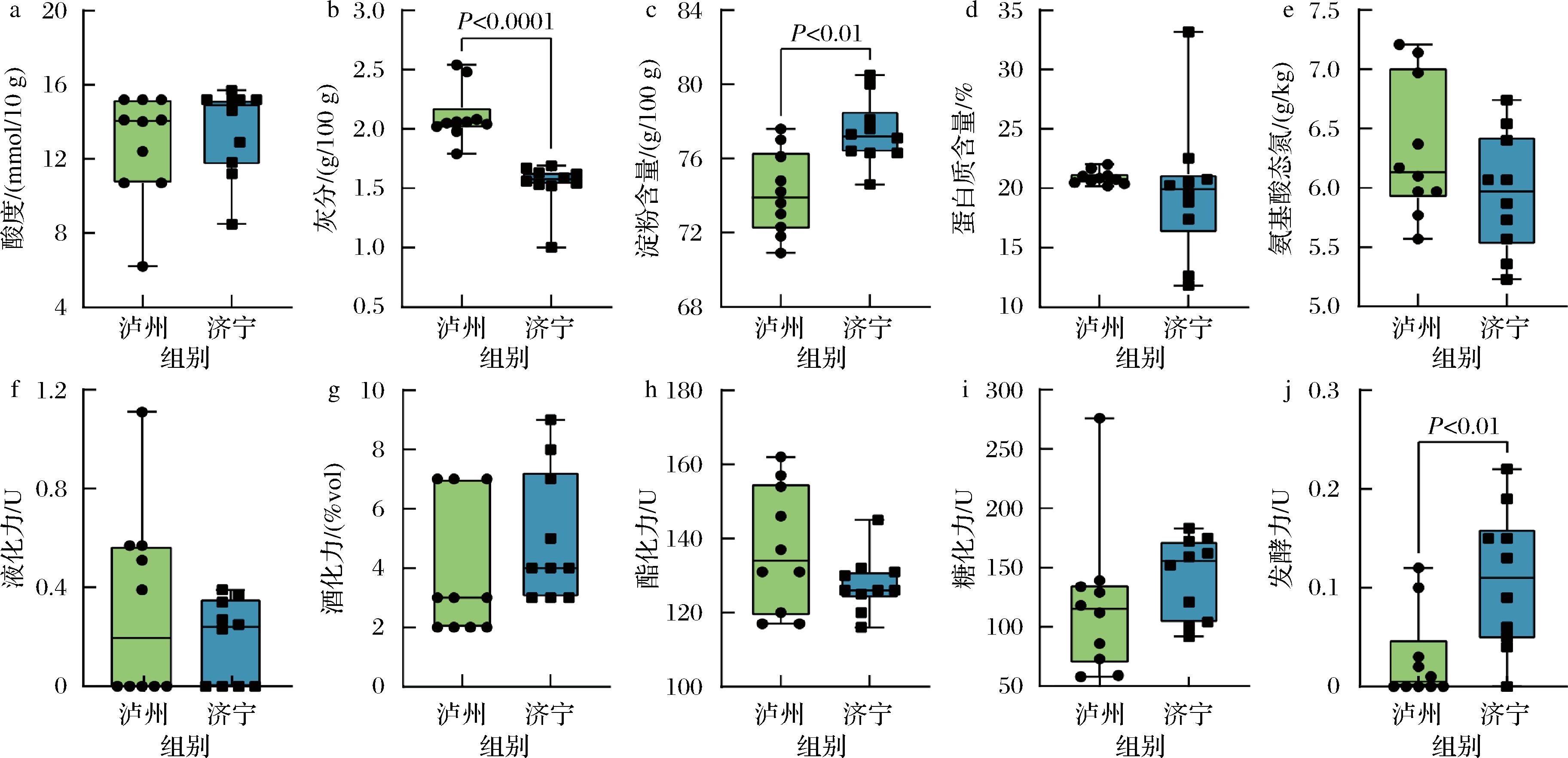
a-酸度;b-灰分;c-淀粉含量;d-蛋白质含量;e-氨基酸态氮;f-液化力;g-酒化力;h-酯化力;I-糖化力;J-发酵力
图7 高温大曲理化指标分析
Fig.7 Analysis of physicochemical indicators in high-temperature Daqu
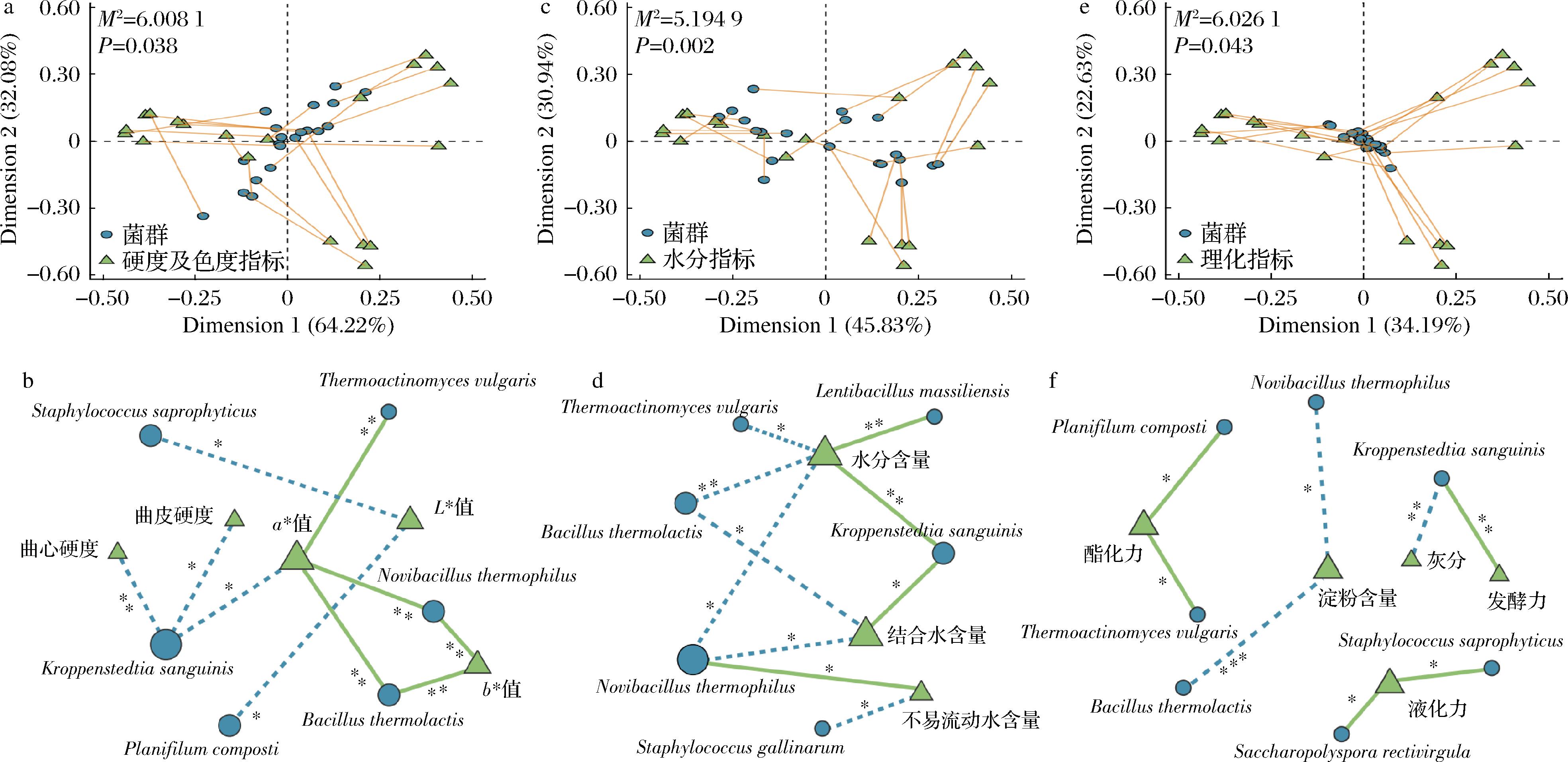
a-菌群与硬度及色度指标的普氏分析;b-菌群与硬度及色度指标的相关性网络图;c-菌群与水分指标的普氏分析;d-菌群与水分指标的相关性网络图;e-菌群与理化指标的普氏分析;f-菌群与理化指标的相关性网络图
图8 高温大曲优势细菌种与品质指标关联性分析
Fig.8 Correlation analysis between dominant bacterial species and quality indicators of high-temperature Daqu
注:图8-b、图8-d、图8-e中绿色实线表示正相关,蓝色虚线表示负相关;*表示P<0.05,**表示P<0.01,***表示P<0.001。
2.7 高温大曲优势细菌种与品质指标关联性分析
2个地区高温大曲优势细菌种与品质指标之间的相关性分析结果如图8所示。由图8-a、图8-c、图8-e可知,纳入本研究2个地区高温大曲优势细菌种与质构、色度、水分和理化指标之间存在显著相关性(P<0.05)。由图8-b、图8-d、图8-f可知,Spearman相关性分析结果显示,K.sanguinis与曲皮硬度、曲心硬度、a*值和灰分呈显著负相关(P<0.05),与水分含量、结合水含量和发酵力呈显著正相关(P<0.05);S.saprophyticus与液化力呈显著正相关(P<0.05),与L*值呈显著负相关(P<0.05);B.thermolactis与淀粉含量呈极显著负相关(P<0.001)。综上可知,微生物的种类对大曲的整体质量具有重要影响。
3 结论
采集自济宁和泸州地区的高温大曲细菌菌群和理化指标之间存在明显差异,其中泸州高温大曲的生物标志物是S.saprophyticus,其曲皮和曲心硬度、结合水含量、不易流动水含量和灰分显著偏高,济宁高温大曲的生物标志物为K.sanguinis,其发酵力、淀粉含量显著偏高。相关性研究发现优势细菌种对高温大曲理化指标具有显著影响,其中K.sanguinis与水分含量、结合水含量和发酵力显著正相关,S.saprophyticus与液化力显著正相关,B.thermolactis与淀粉含量极显著负相关。本研究为进一步了解地域因素对高温大曲细菌群落结构和理化品质的差异提供了数据支撑。
[1] LIU S P, ZHOU Y, MA D N, et al.Environment microorganism and mature Daqu powder shaped microbial community formation in mechanically strong-flavor Daqu[J].Food Bioscience, 2023, 52:102467.
[2] JIA W, FAN Z B, DU A, et al.Characterisation of key odorants causing honey aroma in Feng-flavour Baijiu during the 17-year ageing process by multivariate analysis combined with foodomics[J].Food Chemistry, 2022, 374:131764.
[3] 段旭林,冯杰利,田栋伟,等.酱香型白酒品质提升技术研究进展[J].食品工业科技,2025,46(20):478-487.DUAN X L, FENG J L, TIAN D W, et al.Research progress on quality enhancing for sauce-flavor Baijiu[J].Science and Technology of Food Industry, 2025,46(20):478-487.
[4] MA S Y, LUO H B, ZHAO D, et al.Environmental factors and interactions among microorganisms drive microbial community succession during fermentation of Nongxiangxing Daqu [J].Bioresource Technology, 2022, 345:126549.
[5] 史凤, 马楷雨, 史改玲, 等.酱香型高温大曲发酵过程中风味物质分析[J].中国酿造, 2025, 44(1):52-59.SHI F, MA K Y, SHI G L, et al.Analysis of flavor compounds of sauce-flavor high-temperature Daqu during fermentation process[J].China Brewing, 2025, 44(1):52-59.
[6] 王晓丹, 班世栋, 周鸿翔, 等.贵州省遵义地区3个酱香型大曲细菌群落的比较分析[J].食品科学, 2016, 37(7):110-116.WANG X D, BAN S D, ZHOU H X, et al.Comparative analysis of bacterial populations of three Maotai-flavored daqus in Zunyi, Guizhou[J].Food Science, 2016, 37(7):110-116.
[7] ZHANG Z D, MENG Y L, WANG Y R, et al.Understanding the factors influencing high-temperature Daqu from different geographical regions[J].Food Bioscience, 2024, 62:105528.
[8] WANG W Y, LIU R L, SHEN Y, et al.The potential correlation between bacterial sporulation and the characteristic flavor of Chinese Maotai liquor[J].Frontiers in Microbiology, 2018, 9:1435.
[9] 欧阳宏虹. 泸州建设世界优质白酒产业集群的SWOT分析及发展战略研究[J].全国流通经济, 2024(19):173-176.OUYANG H H.SWOT analysis of building a world-class high-quality liquor industry cluster in Luzhou and its development strategies[J].China Circulation Economy, 2024(19):173-176.
[10] 孟镇, 吕志远, 牛邦彦, 等.山东地区浓香型白酒窖池中细菌群落与理化指标相关性[J].食品与发酵工业, 2024, 50(23):70-76;86.MENG Z, LYU Z Y, NIU B Y, et al.Correlation between bacterial community and physicochemical indexes in Nongxiangxing Baijiu cellars in Shandong[J].Food and Fermentation Industries, 2024, 50(23):70-76;86.
[11] 薛红燕, 崔莹, 杨鑫, 等.薄壳山核桃品种‘威奇塔’在山东济宁的引种表现与栽培要点[J].中国果树, 2020(1):104-106;116;141.XUE H Y, CUI Y, YANG X, et al.Introduction performance and cultivation technique essentials of pecan cultivar ‘Wichita’ in Jining, Shandong Province[J].China Fruits, 2020(1):104-106;116;141.
[12] 王智伟, 李茜, 张民.富硒豌豆苗粉理化性质及抗氧化活性分析[J].食品科学, 2024, 45(6):8-14.WANG Z W, LI Q, ZHANG M.Physicochemical properties and antioxidant activity in vitro of selenium-enriched pea seedling powder[J].Food Science, 2024, 45(6):8-14.
[13] XU B Y, XU S S, CAI J, et al.Analysis of the microbial community and the metabolic profile in medium-temperature Daqu after inoculation with Bacillus licheniformis and Bacillus velezensis[J].LWT, 2022, 160:113214.
[14] YAN Z, ZHENG X W, CHEN J Y, et al.Effect of different Bacillus strains on the profile of organic acids in a liquid culture of Daqu[J].Journal of the Institute of Brewing, 2013, 119(1-2):78-83.
[15] WANG P, WU Q, JIANG X J, et al.Bacillus licheniformis affects the microbial community and metabolic profile in the spontaneous fermentation of Daqu starter for Chinese liquor making[J].International Journal of Food Microbiology, 2017, 250:59-67.
[16] SHI C, MAKTABDAR M.Lactic acid bacteria as biopreservation against spoilage molds in dairy products-A review[J].Frontiers in Microbiology, 2021, 12:819684.
[17] DELBRÜCK A I, ZHANG Y F, HEYDENREICH R, et al.Bacillus spore germination at moderate high pressure:A review on underlying mechanisms, influencing factors, and its comparison with nutrient germination[J].Comprehensive Reviews in Food Science and Food Safety, 2021, 20(4):4159-4181.
[18] XU P, YANG H, TIAN L, et al.Function and safety evaluation of Staphylococcus epidermidis with high esterase activity isolated from strong flavor Daqu[J].LWT, 2023, 176:114534.
[19] ZHENG X W, YAN Z, ROBERT NOUT M J, et al.Characterization of the microbial community in different types of Daqu samples as revealed by 16S rRNA and 26S rRNA gene clone libraries[J].World Journal of Microbiology and Biotechnology, 2015, 31(1):199-208.
[20] XU P, WU Y J, CHEN H, et al.Promoting microbial community succession and improving the content of esters and aromatic compounds in strong-flavor Daqu via bioaugmentation inoculation[J].Food Bioscience, 2023, 56:103299.
[21] ZHANG J, DU R B, NIU J, et al.Daqu and environmental microbiota regulate fatty acid biosynthesis via driving the core microbiota in soy sauce aroma type liquor fermentation[J].International Journal of Food Microbiology, 2024, 408:110423.
[22] 楚京嬴, 吕嘉枥, 曹丹, 等.三种凤香型大曲中心区域细菌群落、理化特性及非靶向代谢物的差异性和相关性分析[J].陕西科技大学学报, 2024, 42(6):40-51.CHU J Y, LYU J L, CAO D, et al.Differential and correlation analysis of bacterial communities, physicochemical properties and untargeted metabolites in the central region of three kinds of Fengxiangxing Daqu[J].Journal of Shaanxi University of Science &Technology, 2024, 42(6):40-51.
[23] WANG Y, CHEN L, YANG T Y, et al.A review of structural transformations and properties changes in starch during thermal processing of foods[J].Food Hydrocolloids, 2021, 113:106543.
[24] 王凡, 山其木格, 卢君, 等.基于红外光谱技术的高温大曲模式识别与类黑素快速定量[J].现代食品科技, 2024, 40(9):325-332.WANG F, SHAN Q M G, LU J, et al.Pattern recognition of high-temperature daqu and rapid infrared spectroscopy-based melanoidin quantification[J].Modern Food Science and Technology, 2024, 40(9):325-332.
[25] PANG Z M, LI W W, HAO J, et al.Correlational analysis of the physicochemical indexes, volatile flavor components, and microbial communities of high-temperature Daqu in the northern region of China[J].Foods, 2023, 12(2):326.
[26] SODHI H K, SHARMA K, GUPTA J K, et al.Production of a thermostable α-amylase from Bacillus sp.PS-7 by solid state fermentation and its synergistic use in the hydrolysis of malt starch for alcohol production[J].Process Biochemistry, 2005, 40(2):525-534.