在白酒的酿造中,微生物菌群通过差异化的代谢途径来调控酒体的风味品质,故而有“糖化靠霉菌、发酵靠酵母、生香靠细菌”的说法[1]。作为酱香型白酒的糖化发酵剂,高温大曲为酱香型白酒的酿造提供了丰富的微生物类群,其中芽孢杆菌(Bacillus)是高温大曲中的主要细菌类群之一[2]。有研究指出,Bacillus可以显著提高大曲中淀粉酶的含量并改善苯乙醛、苯乙醇和其他芳香族化合物的产生,从而增加大曲中风味物质的丰度[3]。通过全基因组测序技术,YANG等[4]发现地衣芽孢杆菌(Bacillus licheniformis)中约69.95%的基因与风味化合物的生成密切相关,TANG等[5]亦发现通过强化接种B.licheniformis可以提高大曲中吡嗪类物质的含量。由此可见,对以B.licheniformis为代表的Bacillus进行分离、鉴定和保藏,进而为具有白酒提质增效作用的菌株筛选提供支持是极为必要的。
通过对培养基营养和培养条件的组合,纯培养技术实现了酒曲中可培养微生物类群的分离、纯化和培养[6],然而由于酒曲中还存在无法实现纯培养的未培养微生物,因而该技术无法对酒曲微生物类群进行全面的解析[7]。在对酒曲微生物类群进行解析的过程中,宏基因组测序技术不仅能精确到“种”水平,而且可通过基因组组装的非选择性基因对检测到的微生物进行功能注释[8]。基于宏基因组测序技术,侯强川等[9]发现相较于白酒曲,增香酒曲含有更多的蜡样芽孢杆菌(Bacillus cereus);ZHANG等[10]发现与湖北枝江相比,贵州茅台高温大曲中含有更多隶属于Bacillus的索诺拉沙漠芽孢杆菌(Bacillus sonorensis)、解淀粉芽孢杆菌(Bacillus amyloliquefaciens)和贝莱斯芽孢杆菌(Bacillus velezensis),可提高大曲中芳香类化合物的含量。虽然实现了对酒曲微生物类群的全面解析,但宏基因组测序技术无法获得可培养的菌株。王玉荣等[11]采用宏基因组测序技术发现,采自茅台镇高温大曲中Bacillus类群主要由B.sonorensis和B.amyloliquefaciens构成,并以此结果为指导,进一步采用纯培养技术从酒曲中分离到了B.sonorensis和B.amyloliquefaciens等20个种的Bacillus。由此可见,首先使用宏基因组技术对酒曲中微生物类群进行全面解析,在明确酒曲中Bacillus类群的基础上,通过对培养基类型和培养温度进行选择和组合,可显著提高酒曲中Bacillus的分离效率。
高温大曲可分为黑色、黄色和白色高温大曲3大类,其中黑色高温大曲主要分布于曲房的底层,最高温度可达到60 ℃,因而更适合芽孢杆菌等耐热微生物的繁殖[2]。本研究以采集自5个地区的黑色高温大曲为研究对象,首先基于宏基因组测序技术对其中蕴含的微生物类群和功能进行了解析,随后采用5种培养温度和4种培养基对样品中的芽孢杆菌菌株进行了分离。通过本研究的开展,在明确黑色高温大曲微生物类群及其功能的基础上,筛选适于芽孢杆菌分离的纯培养方法,以期为后续酿酒微生物的分离鉴定提供方法支持。
1 材料与方法
1.1 材料与试剂
于2024年3~4月分别从山东省淄博市、山东省济宁市、四川省泸州市、贵州省遵义市和湖北省枝江市酿酒公司的曲房中随机采集黑色高温大曲各10块,装于自封袋中运回实验室。经粉碎后将采自同一个企业的10块高温大曲混合成1个样品,共计5份样品,编号分别记为A、B、C、D和E。
DNeasy mericon Food Kit DNA基因组提取试剂盒,德国QIAGEN公司;NovaSeq 6000高通量测序平台配套试剂,美国Illumina公司;胰蛋白酶大豆琼脂培养基(tryptic soy agar,TSA)、脑心浸液培养基(brain heart infusion agar,BHI)、营养琼脂培养基(nutrient agar,NA),青岛海博生物技术有限公司;特级马血清,北京索莱宝科技有限公司;十六烷基三甲基溴化铵(cetyltrimethylammonium bromide, CTAB)、酚、氯仿、异戊醇、NaCl、乙酸钠、乙醇,国药集团化学试剂有限公司;PCR buffer、dNTP mix、rTaq酶、pMD18-T载体,宝生物工程(大连)有限公司;清洁试剂盒,艾思进生物技术(杭州)公司;引物27F/1495R、M13F(-47)/M13R(-48),武汉天一辉远生物科技有限公司;大肠杆菌(Escherichia coli)TOP10,鄂西北传统发酵食品研究所保藏。
1.2 仪器与设备
LRH-150生化培养箱,上海一恒科学仪器有限公司;QYC-2102C全温培养摇床,上海新苗医疗器械制造有限公司;ECLIPSE Ci生物显微镜,日本Nikon公司;Veriti FAST梯度PCR仪,美国ABI公司;164-5050基础电泳仪,美国Bio-Rad公司;UVPCDS8000凝胶成像分析系统,美国Protein Simple公司;NovaSeq 6000高通量测序平台,美国Illumina公司;R920型机架式服务器,美国DELL公司。
1.3 实验方法
1.3.1 宏基因组DNA提取、测序及生物信息学分析
参照DNeasy mericon Food Kit DNA基因组提取试剂盒的方法提取5份样品的宏基因组DNA,将通过0.1 g/L凝胶电泳检测的DNA送往上海赛恒生物科技有限公司使用Illumina NovaSeq 6000平台进行了宏基因组测序。本研究使用fastp(v0.20.0)软件[12]去除宏基因组测序所得原始序列中长度<50 bp、平均质量值<20及含有N碱基的低质量序列,同时将高质量序列与人体的DNA序列进行比对,去除人体污染。使用MEGAHIT(v1.1.2)软件[13]对序列进行了拼接,随后使用kraken2(v2.1.1)[14]和Bracken(v2.5)软件[15]注释5份高温大曲的微生物信息。最后,使用HUMAnN(v3.0)软件[16]和UniRef 90数据库[17]对黑色高温大曲中微生物的功能及代谢通路进行了注释。
1.3.2 芽孢杆菌的分离纯化
根据芽孢杆菌对于氮源、碳源、无机盐和生长因子等营养物质的需求,以及其好氧且耐高温的生长特性。参照以往的研究[18],分别使用TSA+5%马血清(体积分数)、TSA[19]、BHI[20]和NA[20]等4种培养基,以及40、45、50、55、60 ℃等5种培养温度对5份黑色高温大曲中蕴含的芽孢杆菌进行了分离纯化。具体方法为:称取10 g大曲粉末于装有90 mL 8.5 g/L生理盐水(瓶内装入8~10颗玻璃珠)的三角瓶中,在30 ℃摇床中振荡混匀30 min。随后,吸取1 mL混匀液体于9 mL生理盐水试管中,得到10-2梯度稀释液,以此类推稀释至10-5梯度,将10-3、10-4和10-5梯度稀释液分别涂布于4种培养基中,并放置在5个温度下正置培养1 d。依据《伯杰细菌鉴定手册》[21]中芽孢杆菌的菌落形态特征,对疑似芽孢杆菌菌株进行了挑取及纯化,在连续划线3次后挑取单菌落于对应的液体培养基中,在各培养温度下振荡培养1 d后使用30%甘油(体积分数)管藏,冻存于-80 ℃冰箱备用。
1.3.3 疑似芽孢杆菌分离株的DNA提取、PCR扩增和测序
使用CTAB法提取疑似芽孢杆菌菌株的DNA,以提取的DNA为模板、27F(5′-AGAGTTTGATCCTGGCTCAG-3′)和1495R(5′-CTACGGCTACCTTGTTACGA-3′)为引物,参照WANG等[22]的体系及方法进行了PCR扩增。对通过凝胶成像系统检验的扩增产物进行清洁,随后连接到T载体并转化至E.coli TOP10中,最后将阳性克隆子寄往上海赛恒生物科技有限公司进行了测序。对测序返回的序列进行拼接及去引物后在美国国家生物技术信息中心(National Center for Biotechnology Information,NCBI)进行比对(https://blast.ncbi.nlm.nih.gov/Blast.cgi),并申请了登录号,为PV123981~PV124030。
1.4 数据处理
本研究使用R软件(v4.3.2)进行了气泡图和热图的绘制,使用Origin软件(v2018)进行了柱状图的绘制,使用MEGA5.0与R软件进行了系统发育树的绘制。
2 结果与分析
2.1 基于宏基因组测序技术黑色高温大曲中微生物类群构成解析
通过序列拼接及物种注释后,本研究发现所有样品中共存在1 580个属和3 746个种,平均相对含量>1.0%的属如图1所示。
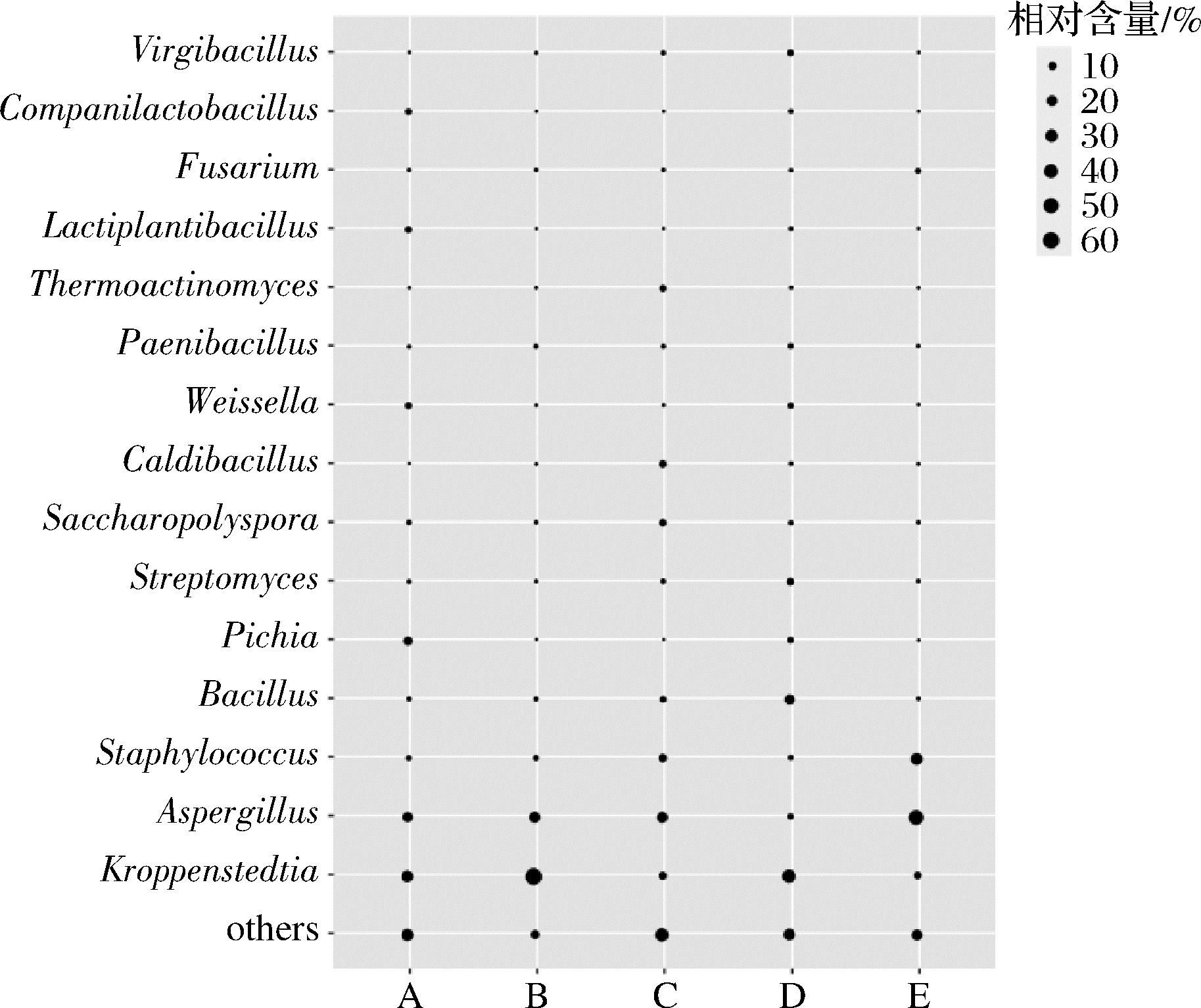
图1 黑色高温大曲中平均相对含量>1.0%属的气泡图
Fig.1 Bubble plot of microbial genera with an average relative abundance >1.0% in black high-temperature Daqu
由图1可知,纳入本研究的黑色高温大曲样品中平均相对含量>1.0%的菌属共有15个,分别为克罗彭斯泰特氏菌属(Kroppenstedtia)、曲霉属(Aspergillus)、葡萄球菌属(Staphylococcus)、芽孢杆菌属(Bacillus)、毕赤酵母菌属(Pichia)、链霉菌属(Streptomyces)、糖多孢菌属(Saccharopolyspora)、热芽孢杆菌属(Caldibacillus)、魏斯氏菌属(Weissella)、类芽孢杆菌属(Paenibacillus)、高温放线菌属(Thermoactinomyces)、乳植物杆菌属(Lactiplantibacillus)、镰刀菌属(Fusarium)、伴生乳杆菌属(Companilactobacillus)和枝芽孢杆菌属(Virgibacillus),平均相对含量分别为26.87%、21.17%、8.16%、4.89%、2.78%、1.94%、1.83%、1.46%、1.44%、1.25%、1.09%、1.03%、1.02%、1.02%和1.01%。本研究进一步对平均相对含量>1.0%的种进行了分析,结果如图2所示。
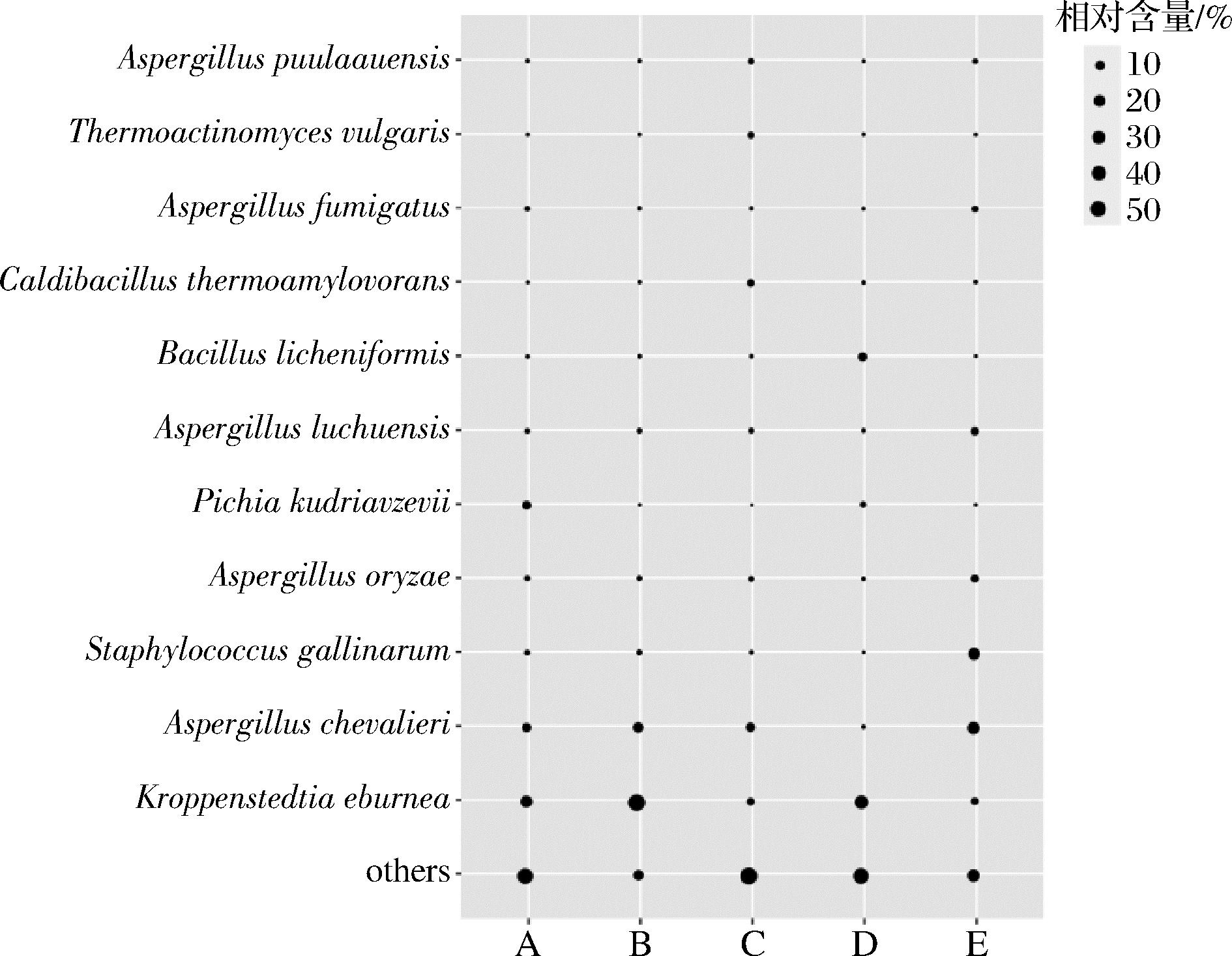
图2 黑色高温大曲中平均相对含量>1.0%种的气泡图
Fig.2 Bubble plot of microbial species with an average relative abundance >1.0% in black high-temperature Daqu
由图2可知,纳入本研究的黑色高温大曲样品中平均相对含量>1.0%的种共有11个,分别为象牙色克罗彭斯泰特氏菌(K.eburnea)、谢瓦曲霉(A.chevalieri)、鸡葡萄球菌(S.gallinarum)、米曲霉(A.oryzae)、库德里阿兹威毕赤酵母(P.kudriavzevii)、琉球曲霉(A.luchuensis)、地衣芽孢杆菌(B.licheniformis)、热噬淀粉芽孢杆菌(C.thermoamylovorans)、烟曲霉(A.fumigatus)、普通高温放线菌(T.vulgaris)和普乌拉曲霉(A.puulaauensis),平均相对含量分别为26.78%、13.28%、5.78%、2.83%、2.80%、2.32%、2.20%、1.47%、1.31%、1.09%和1.00%。由此可见,B.licheniformis是纳入本研究大曲中含量最高的芽孢杆菌菌种。此外,基于种水平,本研究解析出隶属于Bacillus的47个细菌种,对其中平均相对含量>0.1%的细菌种进行了解析,如图3所示。
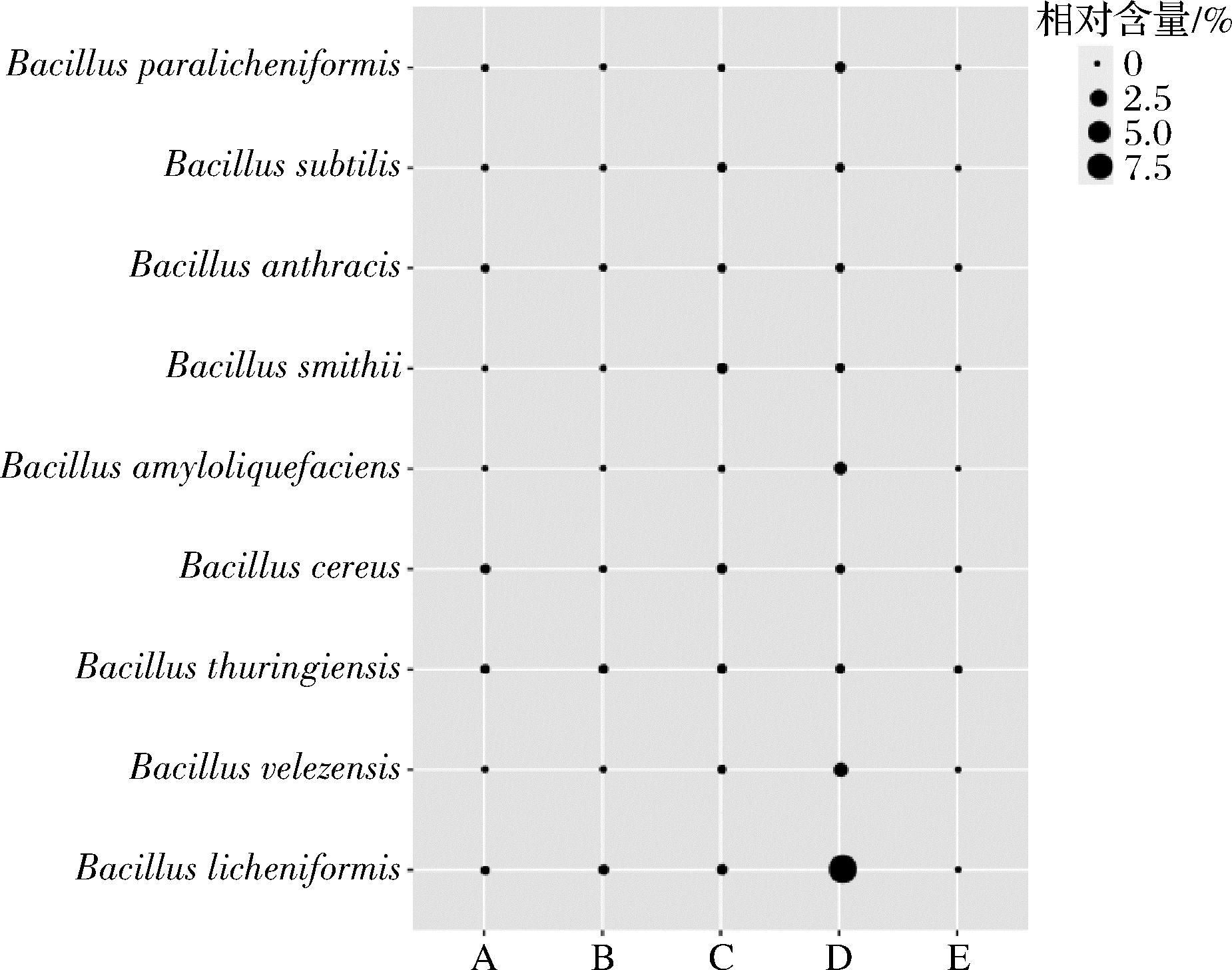
图3 黑色高温大曲中平均相对含量>0.1%芽孢杆菌种的气泡图
Fig.3 Bubble plot of Bacillus species with an average relative abundance >0.1% in black high-temperature Daqu
由图3可知,隶属于Bacillus且平均相对含量>0.1%的菌种共有9个,累计平均相对含量为3.79%,分别为B.licheniformis、B.velezensis、苏云金杆菌(B. thuringiensis)、B. cereus、B. amyloliquefaciens、史氏芽胞杆菌(B. smithii)、炭疽芽胞杆菌(B. anthracis)、枯草芽孢杆菌(B. subtilis)和副地衣芽孢杆菌(B. paralicheniformis),平均相对含量分别为2.20%、0.32%、0.25%、0.24%、0.20%、0.16%、0.15%、0.14%和0.13%。
2.2 黑色高温大曲中微生物的功能分析
为了揭示黑色高温大曲中微生物所蕴含的基因功能,本研究基于KEGG对微生物的基因功能进行了解析,共发现452条代谢通路,选取其中相对含量>0.02%的优势代谢通路进行了分析,结果如图4所示。
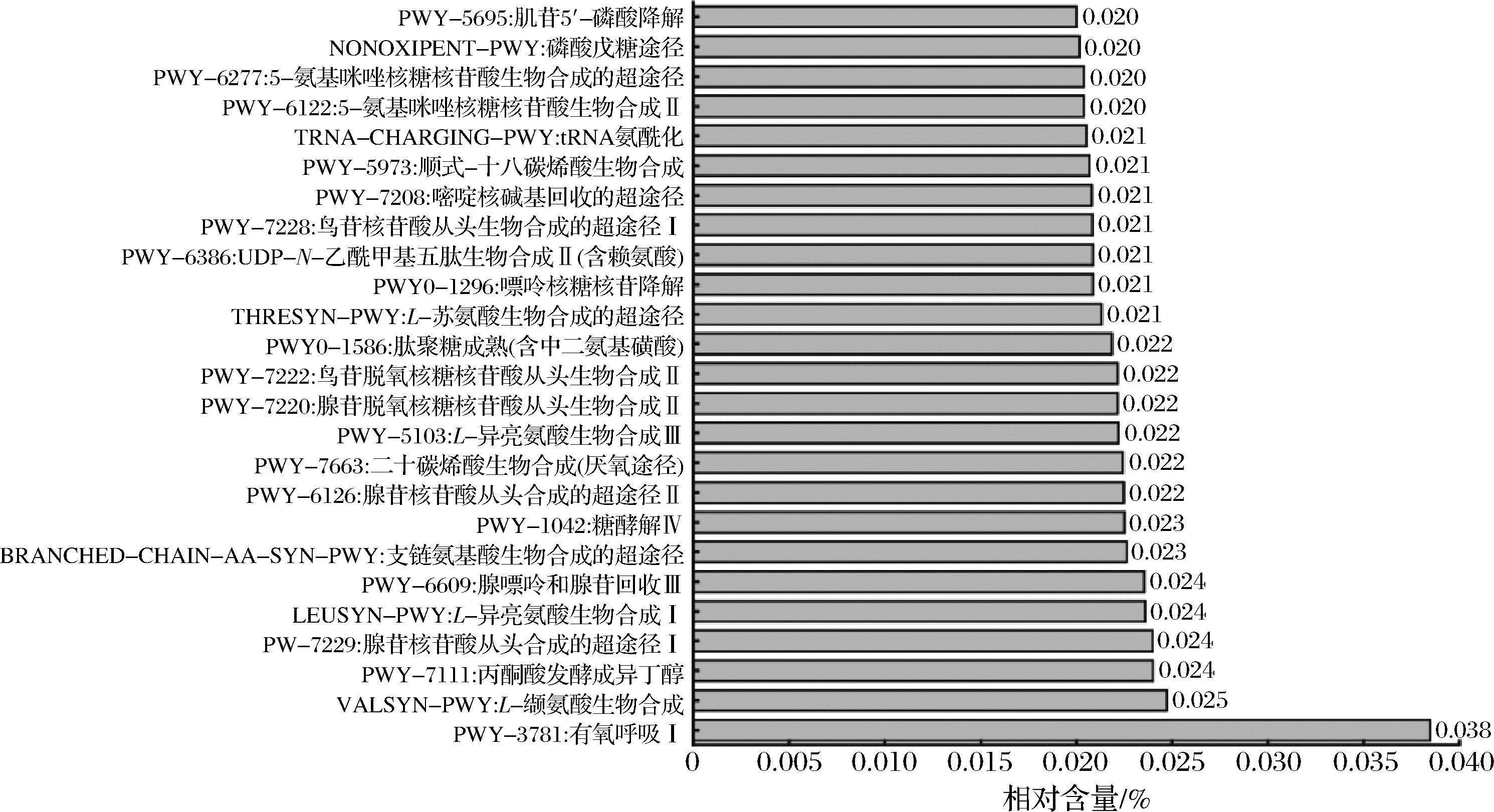
图4 黑色高温大曲中微生物的优势代谢通路相对含量的柱状图
Fig.4 Bar chart of relative content of dominant metabolic pathways of microorganisms in black high-temperature Daqu
由图4可知,纳入本研究的所有高温大曲样品中优势代谢通路共有25条,其中有氧呼吸(PWY-3781)、腺苷核苷酸从头合成的超途径(PWY-7229、PWY-6126)和L-异亮氨酸生物合成(ILEUSYN-PWY、PWY-5103)等3个通路的相对含量最高,累计相对含量分别为0.038%、0.046%和0.046%。有氧呼吸代谢通路的相对含量较高表明,大曲中好氧微生物的生长代谢较为活跃,这进一步促使了大曲中好氧菌成为其优势菌群,该研究结果与上述优势菌种中大多数均能在好氧条件下生长相对应。
由图4亦可知,纳入本研究的黑色高温大曲中腺苷核苷酸从头合成通路的相对含量较高,表明大曲中的微生物可能具有较强的核酸合成能力,能够促进微生物的生长繁殖。有研究表明,充足的氧气供应为腺苷核的生物合成提供了良好的条件[23],且腺苷核苷酸从头合成通路表达活跃时促进了大曲中芽孢杆菌等微生物的代谢,从而产生四甲基吡嗪等风味物质[24]。此外,本研究亦发现黑色高温大曲中L-异亮氨酸生物合成通路的相对含量较高,表明大曲中微生物可能具有高效的氨基酸合成能力。REN等[25]研究表明,Kroppenstedtia、Streptomyces和Bacillus均与L-异亮氨酸呈显著正相关,并且异亮氨酸等氨基酸的合成途径主要为四甲基吡嗪的合成提供氨,从而引起果香和焙烤香,促进白酒风味的形成[26]。由此可见,在纳入本研究的黑色高温大曲中微生物的生长代谢较为旺盛,这有利于推进发酵的进程并产生风味及风味前体物质。
2.3 黑色高温大曲中芽孢杆菌的分离鉴定
本研究选取不同的培养基和温度的组合对高温大曲中芽孢杆菌进行了分离鉴定,共分离得到了50株疑似芽孢杆菌菌株,在对其16S rDNA进行测序的基础上进行了系统发育树绘制,结果如图5所示。
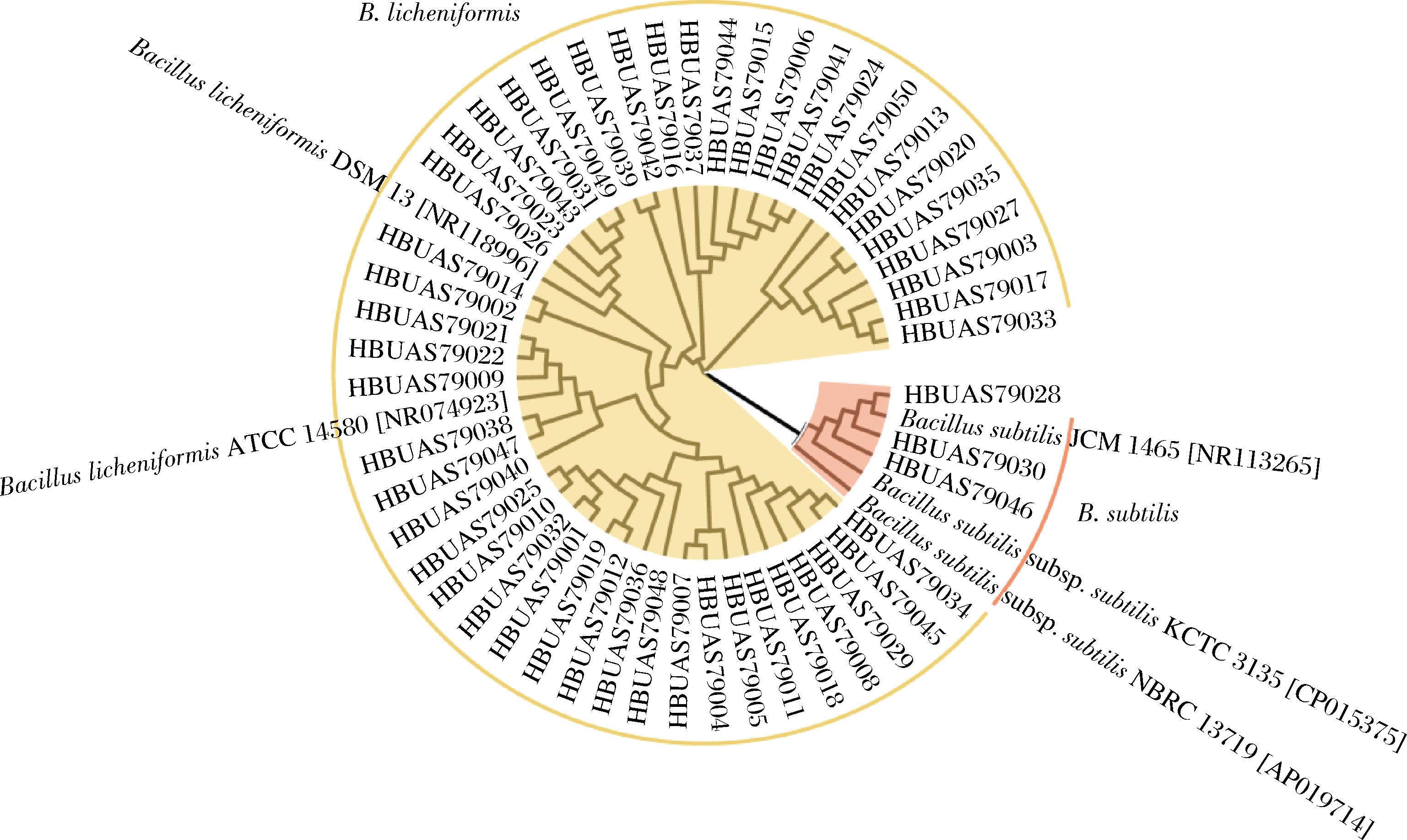
图5 黑色高温大曲中芽孢杆菌分离株的系统发育树
Fig.5 Phylogenetic tree of Bacillus isolates from black high-temperature Daqu
由图5可知,50个分离株被鉴定为B.licheniformis和B.subtilis 2个种,分离数分别为47株和3株,占比分别为94%和6%。由此可见,B.licheniformis是纳入本研究黑色高温大曲中占绝对优势的芽孢杆菌分离株。与此结果不同的是,宏基因组测序表明纳入本研究的高温大曲中亦存在除B.licheniformis和B.subtilis外的其他7个平均相对含量>0.1%的芽孢杆菌菌种,然而在40~60 ℃的培养温度和4种培养基条件下并未分离出来。造成这种现象的原因可能主要为宏基因组测序技术可直接提取样本中的总DNA进行检测,该方法亦能对未降解DNA的死亡微生物以及活性较低的微生物进行解析[27],从而导致2种方法对于高温大曲中芽孢杆菌组成的检测结果存在部分差异。与本研究类似,ZHANG等[6]在对高温大曲中微生物组成进行解析时亦发现了测序与纯培养结果存在不同的情况。虽然2种检测方式的结果存在差异,但值得一提的是,宏基因组测序和纯培养技术均证明了B.licheniformis是纳入本研究黑色高温大曲中主要的芽孢杆菌菌群。
本研究进一步对分离株的菌落形态和显微镜细胞形态图进行了绘制和分析,结果如图6所示。由图6可知,隶属于B.licheniformis的分离株菌落呈现灰白色,表面干燥,边缘扁平且呈不规则状,中央隆起具有褶皱。革兰氏染色后呈现蓝紫色,表明其为革兰氏阳性细菌,细胞形态为杆状。而隶属于B.subtilis分离株的菌落呈现灰白且略带黄色,表面干燥且具有褶皱,边缘呈不规则状。但相较于B.licheniformis,B.subtilis菌株的粗糙度和褶皱均更小。通过革兰氏染色后呈现蓝紫色,表明其亦为革兰氏阳性细菌,细胞形态也为杆状。2种芽孢杆菌分离株的菌落和形态特征均符合《伯杰细菌鉴定手册》中的描述[21]。当前,隶属于B.licheniformis[5]和B.subtilis[28]的芽孢杆菌菌株可用做优质酿酒微生物资源,通过生物强化接种的方法来提高大曲和白酒的风味品质及产量。由此可见,后续可进一步对本研究分离出的芽孢杆菌菌株进行发酵力和酶活力等指标的筛选,并将筛选出的优质菌株通过强化接种至大曲或酒醅中,进一步探究其发酵特性,以期获得具有较好酿酒能力的芽孢杆菌菌株资源。
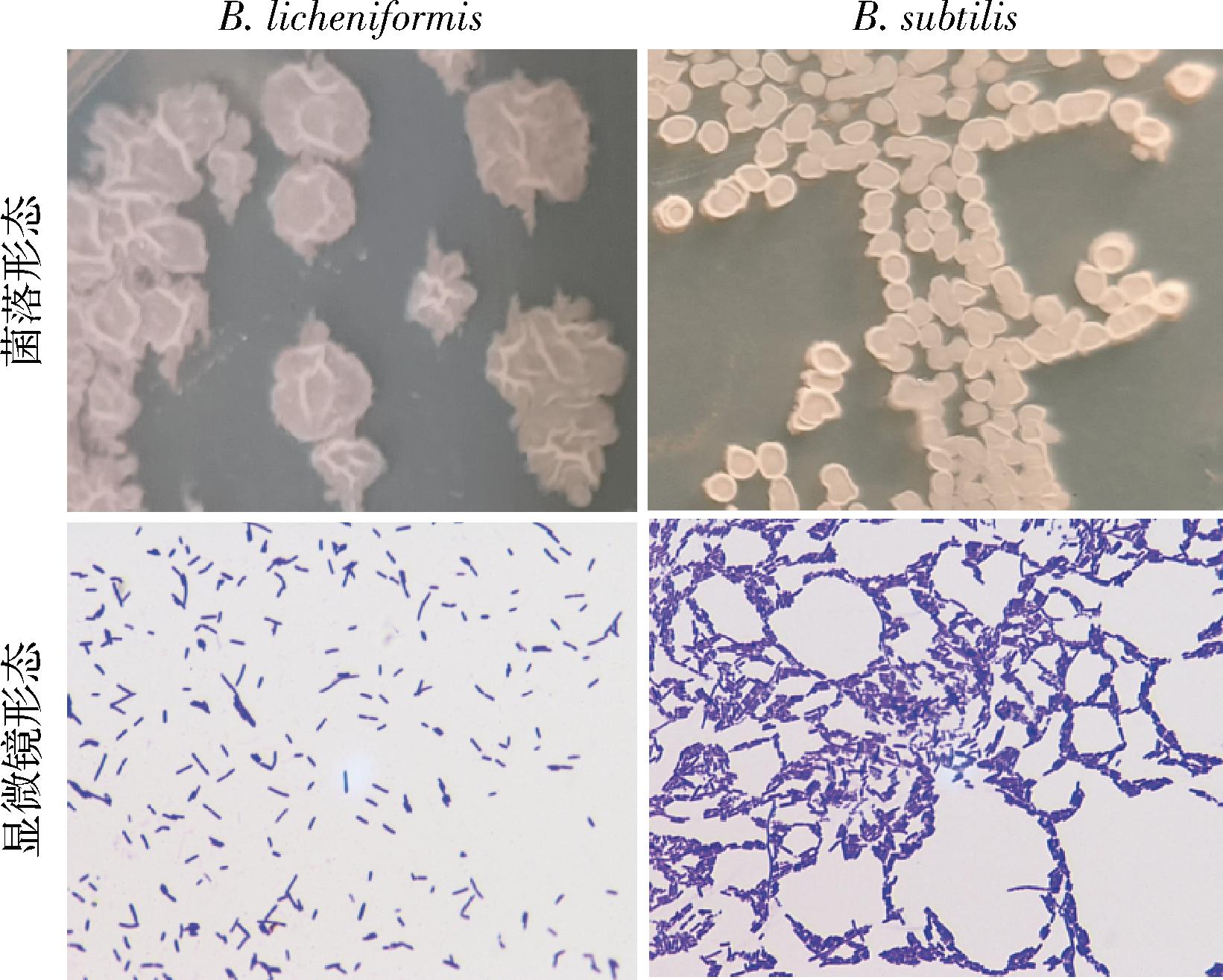
图6 芽孢杆菌分离株的菌落和细胞形态图
Fig.6 Colony and cell morphology of Bacillus isolates
2.4 黑色高温大曲中B.licheniformis最佳分离条件的确定
本研究进一步对不同培养基质和不同培养温度下B.licheniformis的分离株数进行了统计,结果如图7所示。
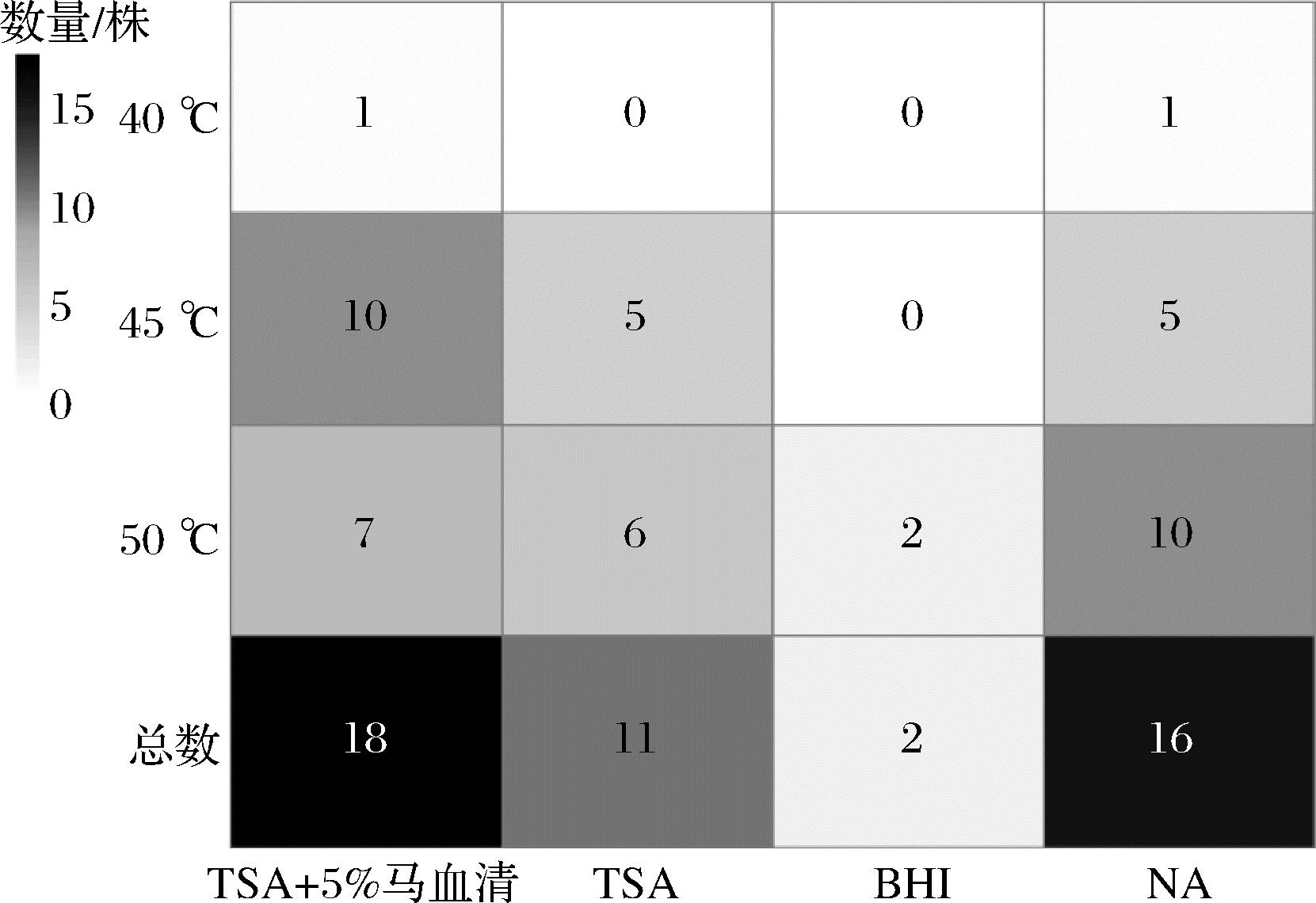
图7 不同培养基质和不同培养温度下B.licheniformis分离株数的比较
Fig.7 Comparison of the number of B.licheniformis isolates under different culture media and temperatures
由图7可知,使用TSA+5%马血清、TSA、BHI和NA培养基对黑色高温大曲样品中B.licheniformis进行分离时,分别得到了18、11、2、16个分离株。由此可见,TSA+5%马血清和NA培养基相对更适于B.licheniformis菌株的分离。由图7亦可知,在40、45、50 ℃下对分离株进行培养时,分别得到2、20、25个分离株。由此可见,45 ℃和50 ℃的培养温度适宜B.licheniformis菌株的分离。综上所述,培养温度为45 ℃和50 ℃,且选用NA或添加马血清的TSA培养基可较好地对高温大曲中B.licheniformis进行分离。与本研究类似,XIANG等[29]使用NA培养基在37 ℃下从湖北和山西地区清香型大曲中分离出的芽孢杆菌中B.licheniformis的占比高达54.90%。与本研究不同的是,魏子涵等[18]在对大熊猫肠道中的芽孢杆菌进行分离时,发现TSA培养基的分离效果最好,BHI培养基次之,而NA培养基的分离效果较差。造成这种差异的原因可能是样品的种类不同,NA培养基中富含的营养物质可能与大曲中微生物的生长需求更接近。值得一提的是,在 55 ℃ 和60 ℃的培养条件下,所有的培养皿均没有菌落生长。
3 结论
依托宏基因组测序技术,本研究发现隶属于Bacillus的微生物在纳入本研究的黑色高温大曲中占比较高,为4.89%,其中B.licheniformis是平均相对含量最高的芽孢杆菌菌种,占比为2.20%。培养温度为45 ℃和50 ℃,使用NA和添加5%马血清的TSA培养基更适合高温大曲中B.licheniformis的分离。本研究可为后续具有优良发酵特性芽孢杆菌菌株的验证提供菌种资源和分离方法的支持。
[1] CHEN Y R, LI K M, LIU T, et al.Analysis of difference in microbial community and physicochemical indices between surface and central parts of Chinese special-flavor Baijiu Daqu[J].Frontiers in Microbiology, 2021, 11:592421.
[2] GUO Z, XIANG F S, HOU Q C, et al.Analysis of bacterial community structure and taste quality of different colored high-temperature Daqu in the Xiangyang region, China[J].LWT, 2023, 188:115411.
[3] XU B Y, XU S S, CAI J, et al.Analysis of the microbial community and the metabolic profile in medium-temperature Daqu after inoculation with Bacillus licheniformis and Bacillus velezensis[J].LWT, 2022, 160:113214.
[4] YANG F, LIU Y F, CHEN L Q, et al.Genome sequencing and flavor compound biosynthesis pathway analyses of Bacillus licheniformis isolated from Chinese Maotai-flavor liquor-brewing microbiome[J].Food Biotechnology, 2020, 34(3):193-211.
[5] TANG Q X, CHEN X R, HUANG J, et al.Mechanism of enhancing pyrazines in Daqu via inoculating Bacillus licheniformis with strains specificity[J].Foods, 2023, 12(2):304.
[6] ZHANG Y R, ZHANG L J, XU Y.Enhanced bacterial cultivation supports the identification and function evaluation of cultured but not sequenced (CBNS) bacteria of high-temperature Daqu[J].Food Bioscience, 2025, 68:106488.
[7] HOU Q C, WANG Y R, QU D W, et al.Microbial communities, functional, and flavor differences among three different-colored high-temperature Daqu:A comprehensive metagenomic, physicochemical, and electronic sensory analysis[J].Food Research International, 2024, 184:114257.
[8] HOU Q C, WANG Y R, CAI W C, et al.Metagenomic and physicochemical analyses reveal microbial community and functional differences between three types of low-temperature Daqu[J].Food Research International, 2022, 156:111167.
[9] 侯强川, 王玉荣, 田龙新, 等.基于宏基因组测序技术解析市售强化酒曲微生物群落结构和功能特征[J].食品与发酵工业, 2023, 49(10):100-107.HOU Q C, WANG Y R, TIAN L X, et al.Microbial community structure and functional characteristics of commercial intensified Jiuqu based on metagenomic sequencing technology[J].Food and Fermentation Industries, 2023, 49(10):100-107.
[10] ZHANG Z D, MENG Y L, WANG Y R, et al.Understanding the factors influencing high-temperature Daqu from different geographical regions[J].Food Bioscience, 2024, 62:105528.
[11] 王玉荣, 侯强川, 田龙新, 等.基于纯培养和超高深宏基因组测序技术分析茅台镇两企业高温大曲微生物多样性差异[J].食品科学, 2024, 45(4):108-115.WANG Y R, HOU Q C, TIAN L X, et al.Pure culture and ultra-high deep metagenomic sequencing for analysis of the differences in microbial diversity of high temperature Daqu from two distilleries in Maotai town[J].Food Science, 2024, 45(4):108-115.
[12] CHEN S F.Ultrafast one-pass FASTQ data preprocessing, quality control, and deduplication using fastp[J].iMeta, 2023, 2(2):e107.
[13] LI D H, LUO R B, LIU C M, et al.MEGAHIT v1.0:A fast and scalable metagenome assembler driven by advanced methodologies and community practices[J].Methods, 2016, 102:3-11.
[14] LU J, SALZBERG S L.Ultrafast and accurate 16S rRNA microbial community analysis using Kraken 2[J].Microbiome, 2020, 8(1):124.
[15] LU J, BREITWIESER F P, THIELEN P, et al.Bracken:Estimating species abundance in metagenomics data[J].PeerJ.Computer Science, 2017, 3:e104.
[16] YANG C C, PENG C T, JIN H, et al.Comparison of the composition and function of the gut microbiome in herdsmen from two pasture regions, Hongyuan and Xilingol[J].Food Science &Nutrition, 2021, 9(6):3258-3268.
[17] SUZEK B E, WANG Y Q, HUANG H Z, et al.UniRef clusters:A comprehensive and scalable alternative for improving sequence similarity searches[J].Bioinformatics, 2015, 31(6):926-932.
[18] 魏子涵, 秦向宁, 邓雯文, 等.圈养大熊猫肠道可培养芽孢杆菌分离及多样性[J].应用与环境生物学报, 2025, 31(6):1000-1012.WEI Z H, QIN X N, DENG W W, et al.Isolation and diversity of culturable Bacillus from the intestinal tract of captive giant pandas[J].Chinese Journal of Applied and Environmental Biology, 2025, 31(6):1000-1012.
[19] 江地科, 项明源, 王印, 等.猪源蜡样芽孢杆菌的分离鉴定与部分生物学特性分析[J].中国预防兽医学报, 2019, 41(10):1063-1066.JIANG D K, XIANG M Y, WANG Y, et al.Identification and biological characteristics analysis of a Bacillus cereus strain from swine[J].Chinese Journal of Preventive Veterinary Medicine, 2019, 41(10):1063-1066.
[20] SHU L J, YANG Y L.Bacillus classification based on matrix-assisted laser desorption ionization time-of-flight mass spectrometry:Effects of culture conditions[J].Scientific Reports, 2017, 7:15546.
[21] R E 布坎南, N E 吉本斯.伯杰细菌鉴定手册[M].北京:科学出版社, 1984.R E BUCHANAN, N E GIBBONS.Bergey’s Manual of Systematic Bacteriology[M].Beijing:Science Press, 1984.
[22] WANG Y R, XIANG F S, ZHANG Z D, et al.Characterization of bacterial community and flavor differences of different types of Douchi[J].Food Science &Nutrition, 2021, 9(7):3460-3469.
[23] YU W B, GAO S H, YIN C Y, et al.Comparative transcriptome analysis of Bacillus subtilis responding to dissolved oxygen in adenosine fermentation[J].PLoS One, 2011, 6(5):e20092.
[24] LIU Y B, LI M K, HONG X F, et al.Screening and identification of high yield tetramethylpyrazine strains in Nongxiangxing liquor Daqu and study on the mechanism of tetramethylpyrazine production[J].Journal of the Science of Food and Agriculture, 2023, 103(14):6849-6860.
[25] REN H W, SUN Y F, YANG Y F, et al.Unraveling the correlations between microbial communities and metabolic profiles of strong-flavor Jinhui Daqu with different storage periods[J].Food Microbiology, 2024, 121:104497.
[26] WANG X D, HUANG W, HUANG J, et al.The mechanism of Laceyella sacchari FBKL4.010 produced tetramethylpyrazine in the liquid fermentation by comparative transcriptomic techniques[J].Frontiers in Microbiology, 2024, 15:1414203.
[27] TRINGE S G, RUBIN E M.Metagenomics:DNA sequencing of environmental samples[J].Nature Reviews Genetics, 2005, 6(11):805-814.
[28] LIU Y B, LI H D, LIU W X, et al.Bioturbation analysis of microbial communities and flavor metabolism in a high-yielding cellulase Bacillus subtilis biofortified Daqu[J].Food Chemistry:X, 2024, 22:101382.
[29] XIANG F S, CAI W C, HOU Q C, et al.Comparative analysis of the microbial community structure in light-flavor Daqu in Taiyuan and Suizhou regions, China[J].LWT, 2023, 177:114599.