L-苯丙氨酸(L-phenylalanine,L-Phe)是一种具有关键生物学功能和广泛工业应用价值的芳香族氨基酸,其分子式为C9H11NO2。近年来,L-苯丙氨酸在医药、食品以及化工等多个领域均发挥着不可或缺的作用[1]。在医药产业,它是合成多种重要药物的关键前体,如抗癌药物、抗艾滋病药物等;在食品工业,它是人工合成甜味剂阿斯巴甜的核心原料;在化工领域,其可用于制备新型高分子材料。目前,L-苯丙氨酸的生产方法主要包括蛋白质水解法、化学合成法和微生物发酵法。蛋白质水解法工艺简单,但产量有限且成本较高;化学合成法可实现大规模生产,但产物为需要拆分的外消旋体;微生物发酵法具有原料来源广泛、环境友好等优点,成为当前生产L-苯丙氨酸的主要方法[2]。在L-苯丙氨酸生物合成过程中,代谢改造的主要研究方向聚焦于优化合成途径、解除反馈抑制以及增强前体物质供应等方面[3]。
大肠杆菌作为一种模式菌株,其优点是遗传背景清晰、基因操作简单、在廉价培养基中生长快等,被广泛用于生产L-苯丙氨酸等芳香族化合物[4]。在大肠杆菌中,L-苯丙氨酸生物合成途径的2个前体是磷酸烯醇式丙酮酸(phosphoenolpyruvate,PEP)和赤藓糖-4-磷酸(erythrose-4-phosphate,E4P),其生物合成经过莽草酸途径,如图1所示,3种3-脱氧-D-阿拉伯庚酮糖酸-7-磷酸(3-deoxy-D-arabino-heptulosonate-7-phosphate synthase,DAHP)合成酶同工酶由基因aroF、aroG和aroH编码,负责L-苯丙氨酸生物合成途径的第一步,也是关键的限速酶,它们分别受到L-酪氨酸、L-苯丙氨酸和L-色氨酸的反馈抑制。同时aroG占DAHP总活性的80%,而aroF和aroH占DAHP总活性的比例仅分别为15%和5%左右[5]。PEP和E4P形成中间产物分支酸需要7个酶促反应。然后,分支酸进入通路,进行L-色氨酸、L-酪氨酸和L-苯丙氨酸的单独生物合成。L-苯丙氨酸途径中的另一个限速酶是由pheA基因编码的分支酸变位酶-预苯酸脱氢酶(chorismate mutase-prephenate dehydratase,CM-PDT),该酶与L-苯丙氨酸结合引起反馈抑制。L-苯丙氨酸形成的最后一步是以谷氨酸为氨基供体的转氨反应,主要由pheA基因编码的分支酸变位酶/预苯酸脱水酶及tyrB基因编码的酪氨酸转氨酶生成L-苯丙氨酸[3]。
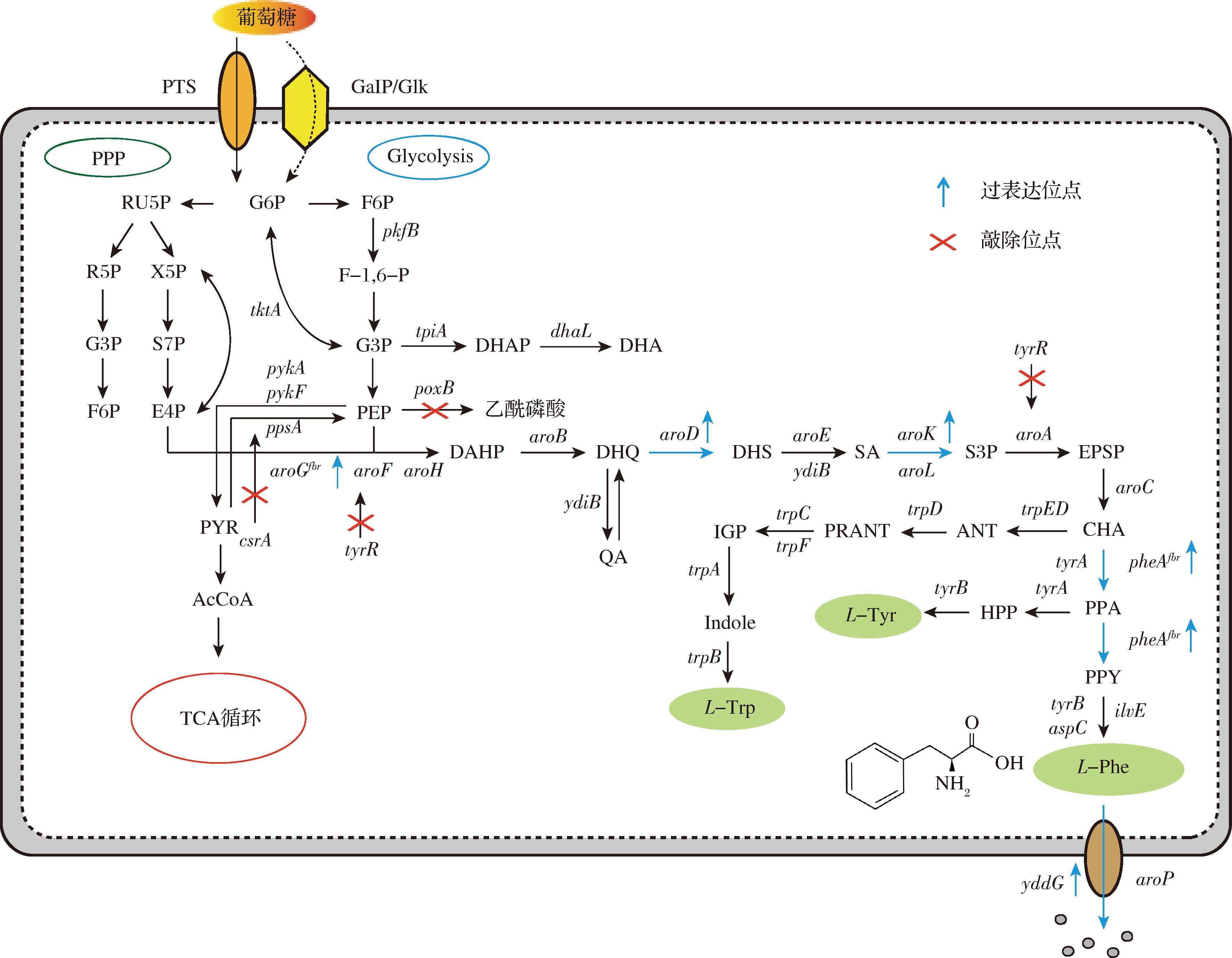
图1 大肠杆菌中L-苯丙氨酸、酪氨酸及色氨酸合成路径
Fig.1 The biosynthetic pathways of L-phenylalanine, L-tyrosine, and L-tryptophan in Eschrichia coli
注:G6P(glucose 6-phosphate):葡萄糖-6-磷酸;RU5P(ribulose 5-phosphate):核酮糖-5-磷酸;R5P(ribose 5-phosphate):核糖-5-磷酸;X5P(xylulose 5-phosphate):木酮糖-5-磷酸;G3P(glyceraldehyde 3-phosphate):甘油醛-3-磷酸;F6P(fructose 6-phosphate):果糖-6-磷酸;S7P(sedoheptulose 7-phosphate):景天庚酮糖-7-磷酸;E4P(erythrose 4-phosphate):赤藓糖-4-磷酸;F-1,6-P(fructose 1,6-bisphosphate):果糖-1,6-二磷酸;DHAP(dihydroxyacetone phosphate):二羟基丙酮磷酸;DHA(dihydroxyacetone):二羟基丙酮;PEP(phosphoenolpyruvate):磷酸烯醇式丙酮酸;PYR(pyruvate):丙酮酸;AcCoA(acetyl-CoA):乙酰辅酶A;DAHP(3-deoxy-D-arabino-heptulosonate7-phosphate):3-脱氧-D-阿拉伯庚酮糖酸-7-磷酸;DHQ(3-dehydroquinate):3-脱氢莽草酸;QA(quinic acid):奎宁酸;DHS(3-dehydroshikimate):3-脱氢莽草酸;SA(shikimic acid):莽草酸;S3P(shikimate 3-phosphate):莽草酸-3-磷酸;EPSP(5-enolpyruvylshikimate-3-phosphate):5-烯醇丙酮酸莽草酸-3-磷酸;CHA(chorismate):分支酸;ANT(anthranilate):邻氨基苯甲酸;PRANT(5-phospho-D-ribosyl-1-pyrophosphate):5-磷酸-D-核糖-1-焦磷酸;IGP(indole-3-glycerol phosphate):吲哚-3-甘油磷酸; indole(indole):吲哚;PPA(prephenate):预苯酸;HPP(4-hydroxyphenylpyruvic acid):对羟基苯丙酮酸;PPY(phenylpyruvic acid):苯丙酮酸。
KONSTANTINOV等[6]以葡萄糖为碳源,在3 L发酵罐中发酵L-苯丙氨酸,产量达到46 g/L,糖酸转化率≥17%。曾小冰等[7]利用葡萄糖与糖蜜在5 L发酵罐内生产了27.7 g/L的L-苯丙氨酸。门佳轩等[8]以大肠杆菌W3110为出发菌,通过基因改造的方式适量表达了关键基因pheA和aroG,强化aroA和aroD,敲除pykF,最终改造菌株在5 L发酵罐内发酵48 h,L-苯丙氨酸产量达到81.8 g/L,糖酸转化率为24%。近期,WANG等[9]在一株产莽草酸的大肠杆菌菌株中,选取多种启动子进行关键基因的过表达,同时优化莽草酸途径,过表达L-苯丙氨酸生物合成相关的内源和外源基因,培育出一株产L-苯丙氨酸菌株,同时利用适应性实验室进化分离出对L-苯丙氨酸具有高耐受性的大肠杆菌菌株,过表达对L-苯丙氨酸具有耐受性的基因marA,在5 L发酵罐中产生了约80 g/L的L-苯丙氨酸。CHEN等[10]首次通过合理设计工业方法,通过系统代谢工程改造得到大肠杆菌PHE 17,其能够积累103.15 g/L的L-苯丙氨酸,是目前报道中大肠杆菌生产L-苯丙氨酸的最高产量。
虽然已有研究报道了与L-苯丙氨酸相关的不同基因对产量的影响,但没有量化相关菌株改造后基因型与表型之间的直接关联,验证代谢工程改造对目标基因的转录水平变化。需要经过相关改造后基因转录水平变化的具体数据,来识别代谢流重新分配过程中表达水平显著变化的基因,发现潜在的限速步骤或调控枢纽,为后续多基因协同调控提供依据[11]。
本研究利用代谢工程手段构建并优化了一条以葡萄糖为底物生产L-苯丙氨酸的途径(图1),研究中以野生型大肠杆菌W3110作为底盘菌株,首先解除L-苯丙氨酸对酶AroG和PheA的反馈抑制,接下来提高前体的积累量、扩大L-苯丙氨酸生产途径的碳流量、促进L-苯丙氨酸排出胞外。为了明确代谢改造后相关基因的表达效果,通过逆转录聚合酶链式反应(reverse transcription polymerase chain reaction,RT-PCR)的手段,揭示了L-苯丙氨酸合成途径中相关基因的转录水平变化,量化了改造菌株基因型与表型之间的关系,揭示了关键基因的调控效果,为突破L-苯丙氨酸生物合成瓶颈提供支撑。
1 材料与方法
1.1 菌株、质粒与引物
Escherichia coli W3110由实验室保藏,用于本研究的出发菌株。E.coli BL21用于质粒的构建,质粒pcrEG和pCRISPR-Cas12a(Cpf1)均由本实验室保藏,本研究使用的菌株、质粒见表1,所涉及到的引物见电子版增强出版附表1(https://doi.org/10.13995/jcnki.11-1802/ts.042772)。
表1 本研究所用的菌株和质粒
Table 1 Strains and plasmids used in this study
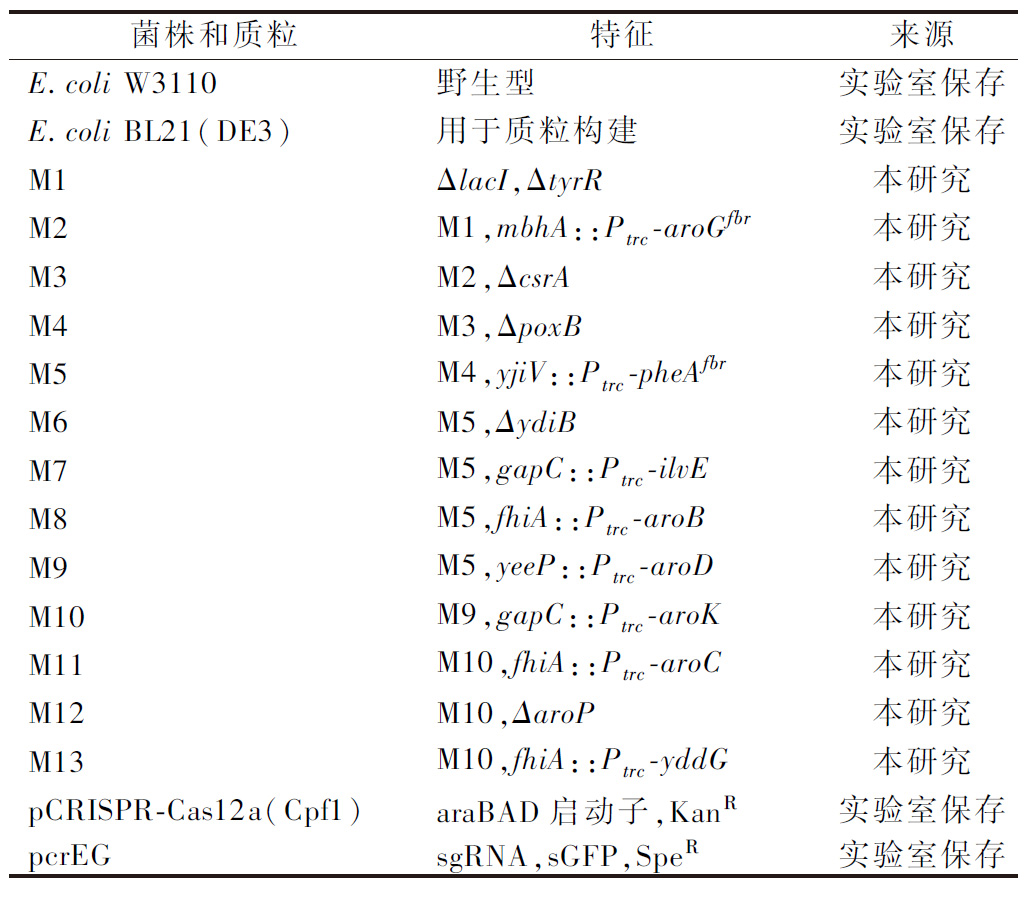
菌株和质粒特征来源E.coli W3110野生型实验室保存E.coli BL21(DE3)用于质粒构建实验室保存M1ΔlacI,ΔtyrR本研究M2M1,mbhA::Ptrc-aroGfbr本研究M3M2,ΔcsrA本研究M4M3,ΔpoxB本研究M5M4,yjiV::Ptrc-pheAfbr本研究M6M5,ΔydiB本研究M7M5,gapC::Ptrc-ilvE本研究M8M5,fhiA::Ptrc-aroB本研究M9M5,yeeP::Ptrc-aroD本研究M10M9,gapC::Ptrc-aroK本研究M11M10,fhiA::Ptrc-aroC本研究M12M10,ΔaroP本研究M13M10,fhiA::Ptrc-yddG本研究pCRISPR-Cas12a(Cpf1)araBAD启动子,KanR实验室保存pcrEGsgRNA,sGFP,SpeR实验室保存
1.2 工具酶与试剂
Dpn Ⅰ限制性内切酶、PrimerSTAR MAX DNA聚合酶和2×Taq DNA聚合酶,宝生物工程(大连)有限公司;RNA提取试剂盒,武汉爱博泰克生物科技有限公司;高保真DNA聚合酶、同源重组酶、琼脂糖凝胶DNA回收试剂盒,南京诺唯赞生物科技股份有限公司;质粒快速提取试剂盒,北京全式金生物技术有限公司;阿拉伯糖、卡那霉素、壮观霉素,生工生物工程(上海)股份有限公司;蛋白胨、酵母粉,OXOID公司;NaCl及其他试剂,国药集团化学试剂有限公司。
1.3 培养基
LB培养基(g/L):NaCl 10、蛋白胨10、酵母提取物5,固体培养基在其基础上添加16~18 g/L琼脂粉。
摇瓶发酵培养基(g/L):酵母提取物4.5、蛋白胨1.5、(NH4)2SO4 2.5、KH2PO4·3H2O 3、MgSO4·7H2O 2、柠檬酸钠2、NaCl 1、CaCl2·2H2O 0.015、FeSO4·7H2O 0.03、维生素B2 0.005、谷氨酸1.2、维生素H 0.000 2、维生素B混合物(维生素B1、维生素B3、维生素B5、维生素B7,各0.000 2),金属离子混合溶液1 mL/L,苯酚红溶液20 mL/L,用稀释后的氨水将培养基的pH值调为6.8~7.0,115 ℃,高温蒸汽灭菌15 min,底糖质量浓度为15 g/L葡萄糖。
发酵罐种子培养基(g/L):酵母提取物5、(NH4)2SO4 5、KH2PO4 3H2O 4、MgSO4·7H2O 1.5、柠檬酸钠2、FeSO4·7H2O 0.002 8、MgSO4·7H2O 0.001 2、维生素H 0.000 2、维生素B混合物(维生素B1、维生素B3、维生素B5、维生素B7,各0.000 2),金属离子混合溶液1 mL/L。用稀释后的氨水将培养基pH值调为6.8~7.0,115 ℃,高温蒸汽灭菌15 min,底糖质量浓度为30 g/L葡萄糖。
发酵罐发酵培养基(g/L):酵母提取物4.5、蛋白胨1.5、(NH4)2SO4 2.5、KH2PO4·3H2O 6.5、MgSO4·7H2O 1.5、柠檬酸钠2、维生素B2 0.005、谷氨酸1.2、维生素H 5×10-7、维生素B混合物(维生素B1、维生素B3、维生素B5、维生素B7, 各0.000 25),金属离子混合溶液1 mL/L。用稀释后的氨水将培养基的pH值调为6.8~7.0,灭菌条件为115 ℃、15 min,底糖质量浓度为15 g/L葡萄糖。
金属离子混合溶液(g/L):CaCl2·2H2O 10,CuSO4·5H2O 0.45,CoCl2·6H2O 6,ZnSO4 0.6,FeSO4·7H2O 28,MnSO4·H2O 14,NiCl2·6H2O 6,AlCl3·6H2O 2.5,NiSO4·6H2O 2.5。
1.4 仪器与设备
ETC821D型PCR仪,北京东胜创新生物科技有限公司;EP300核酸胶电泳仪,韦克斯科技(北京)有限公司;S-10生物传感分析仪,深圳西尔曼科技有限公司;Intelli-Ferm A G2型5 L发酵罐,迪必尔生物工程(上海)有限公司;AF103制冰机,斯科茨曼制冰系统有限公司;411BR14129电转仪、Centrifuge 5425R台式高速微量小型离心机,德国Eppendorf公司;1260 Infinity Ⅱ高效液相色谱仪,安捷伦科技(中国)有限公司;CR21N冷冻离心机,日本日立公司;StepOnePlus实时荧光定量PCR仪,美国应用生物系统公司;Diamonsil C18色谱柱(4.6 mm×250 mm,5 μm),北京迪科马科技有限公司。
1.5 实验方法
1.5.1 代谢改造菌株的构建
本研究将特异性靶向的crRNA连接到稳定的pcrEG质粒上,其间隔序列有23个核苷酸,形成了靶向识别的sgRNA。Cas12a质粒含有AraC蛋白,其是一种具有双重功能的调节蛋白,在没有阿拉伯糖存在时,AraC蛋白会抑制相关基因编码λ-Red酶系的表达,所以需要终浓度为10 mmol/L的阿拉伯糖诱导λ-Red酶系的表达。Cas12a质粒具备RuvC核酸酶结构域,能够特异性识别碱基TTTV(V=A/C/G)的PAM序列,当Cas12a的RuvC结构域依次切割DNA的2条链形成黏性末端时,此时加入相应的目的片段,就能实现基因的定向编辑[12]。
目的片段的获取是以对应的特异性引物通过PCR扩增上下游同源臂及待整合的基因,将其与启动子连接后,与上下游同源臂连接得到。为了确保编辑的高效性,左右同源臂分别设计为500个碱基对,电转时将目的片段DNA与特异性pcrEG共转化,转入质粒的浓度约为500 ng/μL,目的片段浓度约为2 000 ng/μL。电转化后的菌体涂布在卡那霉素和壮观霉素双抗性平板上。对发出绿色荧光的菌落进行PCR检测,使用对应的上下游引物,根据条带大小的不同选取正确的阳性转化子进行测序确认。
pcrEG质粒上携带可以靶向自身的crRNA序列,其表达由PrhaB启动子驱动,添加鼠李糖后,被诱导的crRNA引导Cas12a蛋白对pcrEG质粒进行切割,从而促进pcrEG质粒的消除。Cas12a质粒携带sacB基因,通过在添加终质量浓度为10 g/L蔗糖的LB培养基中培养以消除质粒[12]。
1.5.2 摇瓶发酵方法
将改造菌株接入10 mL的LB小瓶中,37 ℃、220 r/min摇床培养8~12 h,随后按3%接种量接种到30 mL的摇瓶发酵培养基中,每次发酵设置3个平行,37 ℃、220 r/min摇瓶发酵48 h,每6 h取样一次,每次取样1 mL,取样后,迅速向摇瓶中补充1 mL无菌的对应发酵培养基,补充后充分摇匀,维持发酵体系总体积恒定。
1.5.3 5 L发酵罐发酵方法
将重组菌株在5 L发酵罐上进行补料分批发酵培养。将菌株在LB平板上划线活化后,依次接种至一级LB培养基及二级发酵罐种子培养基中,二级种子液在发酵罐中37 ℃培养,搅拌转速300 r/min,生长至OD600值达15左右时,按20%接种量进行罐上接种。控制发酵温度37 ℃,气流速率保持在3 L/min,通过自动添加体积分数50%的氨水将pH值保持在7.0左右,发酵过程中控制溶氧在30左右。
1.5.4 分析方法
将发酵液稀释至合适倍数后,在600 nm处使用分光光度计测量吸光度以确定细菌细胞密度。取1 mL发酵液,以梯度稀释法稀释成合适的浓度,以12 000 r/min低温冷冻离心10 min,获取稀释好的发酵上清液,过0.22 μm聚醚砜膜。本实验用HPLC测L-苯丙氨酸含量,仪器配备光子二极管阵列紫外检测器,使用C18色谱柱(4.6 mm×250 mm,5 μm)进行检测。检测条件:柱温35 ℃,检测波长210 nm,流动相为10%体积分数的乙腈,流速1 mL/min[8]。
2 结果与分析
2.1 解除菌株的反馈调节抑制
为了使L-苯丙氨酸合成途径通畅,积累更多产量,解除终产物对关键酶的反馈抑制是重要步骤之一[10]。tyrR基因编码的酶是L-苯丙氨酸生物合成途径中基因的主要转录调节因子,不仅参与L-酪氨酸的合成调控,也影响L-苯丙氨酸的代谢,同时该酶的转录会阻遏基因aroA的表达[13]。tyrR基因编码的酶可以结合效应物分子L-苯丙氨酸、L-酪氨酸和L-色氨酸,根据胞内氨基酸的浓度变化对不同基因的转录进行调控,所以经常对其进行失活处理[3,14]。aroG基因参与编码DAHP合成酶,催化PEP和E4P缩合生成DAHP,是L-苯丙氨酸合成途径的重要限速步骤,DAHP受到L-苯丙氨酸的反馈抑制,是重要的调控靶点,将其进行突变以解除L-苯丙氨酸对aroG编码的DAHP的反馈抑制[2]。同时,通过敲除乳糖操纵子阻遏基因lacI,解除乳糖操纵子的抑制,实现莽草酸途径相关酶的高效表达[8]。
在野生型大肠杆菌W3110的基础上,敲除基因lacI和tyrR,得到菌株M1,在M1的基础上整合突变后的基因aroGfbr,得到菌株M2,突变位点为P150L,该突变通过改变酶活性中心的α-螺旋结构,增强了DAHP合成酶的稳定性,解除了L-苯丙氨酸对DAHP合成酶的反馈抑制[15]。结果如图2所示,野生型大肠杆菌在摇瓶发酵条件下L-苯丙氨酸的产量仅为0.4 g/L,M1菌株产量为2.8 g/L,经过tyrR基因敲除后的突变株M1表现出了显著的产量提升,表明tyrR基因的敲除有效地解除了TyrR酶对基因aroA的阻遏作用,使得细胞内的代谢流更多地流向了L-苯丙氨酸的合成方向。而菌株M2的L-苯丙氨酸摇瓶产量达到4.1 g/L,相比于菌株M1的产量提高了46.4%。表明基因aroG同样是关键限速步骤。从代谢调控的角度来看,当tyrR基因被敲除后,关键酶基因的表达不再受到阻遏,同时基因aroGfbr既解除了一部分L-苯丙氨酸对DAHP的反馈抑制,也加强了莽草酸途径,促进了L-苯丙氨酸的合成。
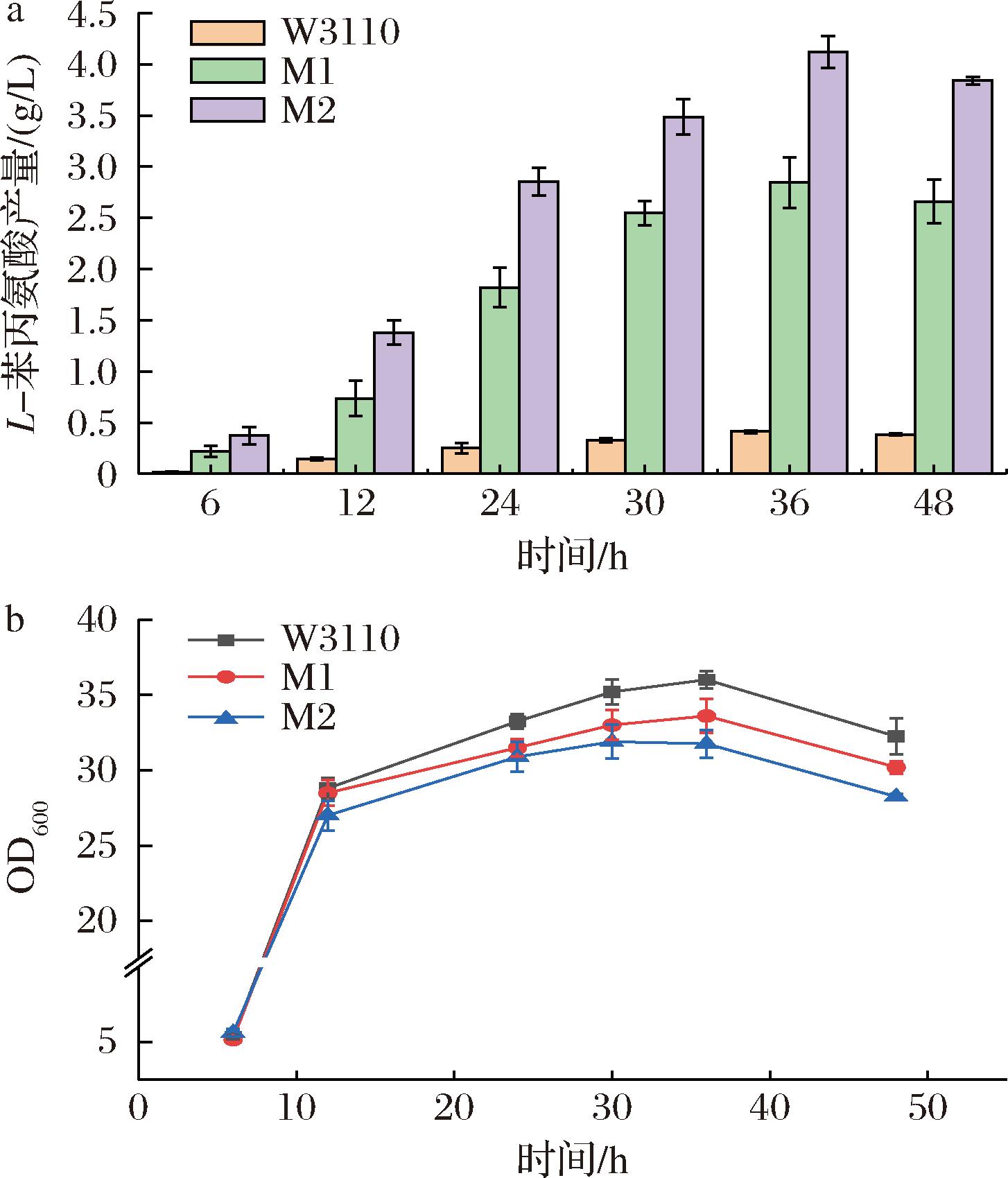
a-L-苯丙氨酸产量;b-OD600值
图2 野生型W3110、M1、M2菌株摇瓶发酵生产L-苯丙氨酸产量及OD600值
Fig.2 The yield of L-phenylalanine and the OD600 values during the shake flask fermentation of the wild-type W3110, M1, and M2 strains
2.2 提高前体物质的胞内水平
另外,前体物质的通量大小是影响终产物产量的重要因素。csrA是一种全局转录调控因子,其正调控丙酮酸激酶基因pykF,负调控PEP羧激酶基因pykA和PEP合成酶基因ppsA,从而影响细胞内PEP的通量。PEP作为L-苯丙氨酸生物合成途径中的重要前体物质,其通量的改变会直接影响L-苯丙氨酸的合成效率[3,13]。
在菌株M2的基础上敲除csrA基因,得到M3,菌株M3在发酵结束后,L-苯丙氨酸的产量提高到5.6 g/L(图3),终产量提高了约36.6%。csrA基因敲除后,由于其对ppsA的负调控作用消失,使得更多的PEP得以保留,同时,csrA对pckA的负调控作用解除,PEP羧激酶基因pckA和PEP合成酶基因ppsA的表达水平升高,进一步增加了细胞内PEP的含量和通量,为L-苯丙氨酸的合成提供了更充足的原料[3]。
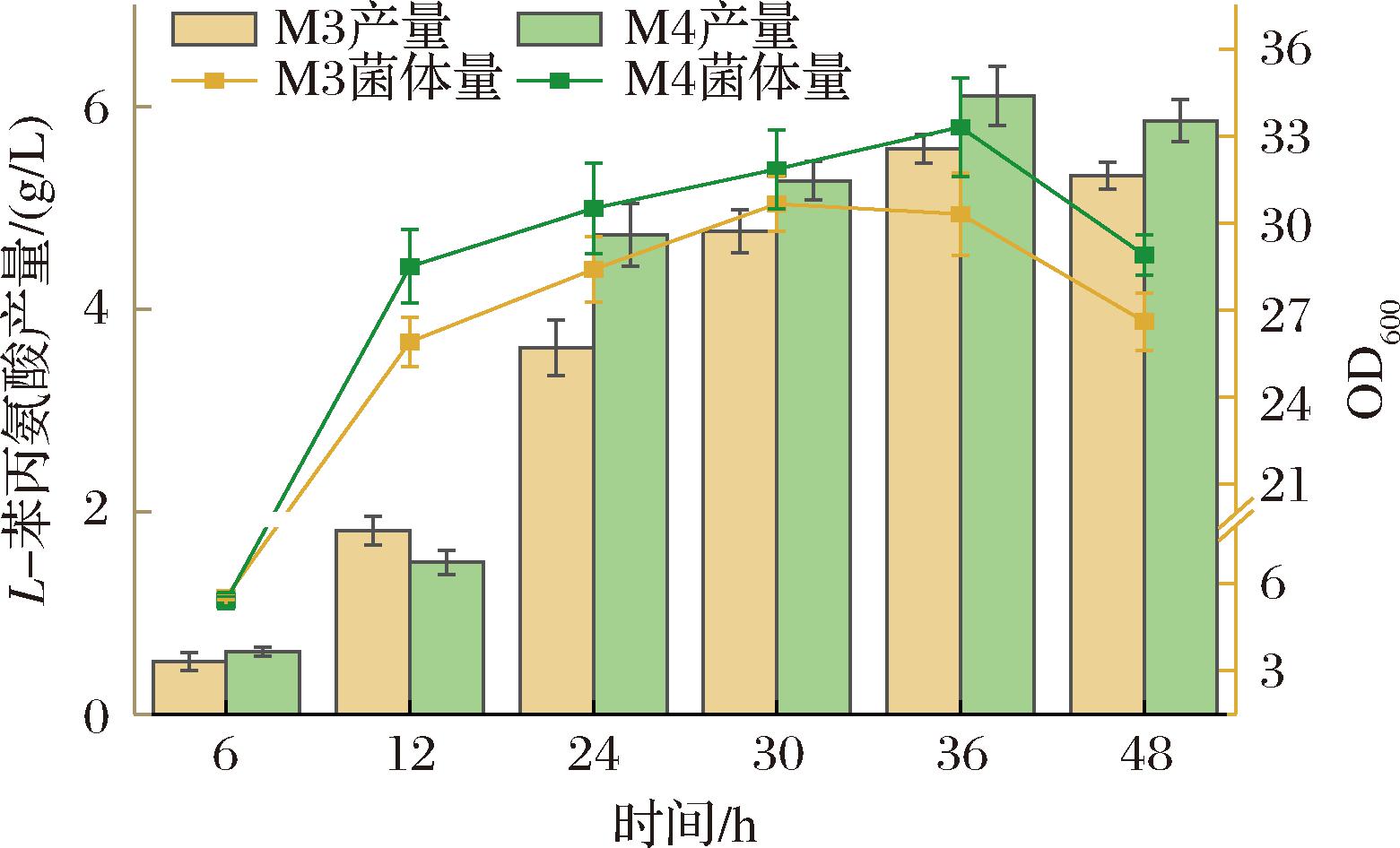
图3 M3、M4菌株摇瓶发酵生产L-苯丙氨酸产量及OD600值
Fig.3 The yield of L-phenylalanine and the OD600 value in the shake-flask fermentation of strain M3,M4
根据前期改造转录水平调节因子的摇瓶实验结果,菌体生长量有所下降。为进一步提升菌体生长量并优化L-苯丙氨酸的合成,本研究针对基因poxB进行了改造[6]。poxB基因编码丙酮酸氧化酶,敲除该基因能够使PEP合成丙酮酸的代谢流减弱,从而增加了芳香族氨基酸合成的前体供应[4]。同时它催化丙酮酸直接氧化脱羧生成乙酸,其与乙酸激酶(由ackA基因编码)共同影响乙酸的合成过程。基因poxB编码的酶所在的途径是丙酮酸代谢的一个主要分流,对其进行改造能够减少乙酸的生成,优化碳代谢流,此外,基因ackA还参与细胞内的能量代谢过程,考虑敲除ackA可能会对细胞的能量平衡产生较大影响,不对其进行改动[4]。对丙酮酸脱氢酶poxB基因进行敲除,验证成功后得到菌株M4,测定改造菌株的L-苯丙氨酸产量变化。实验结果显示,菌株M4的L-苯丙氨酸的摇瓶产量相对于M3提高到了6.1 g/L,提高了约8.9%,同时菌株的OD600值提高到33.3(图3)。
2.3 加大L-苯丙氨酸合成路径碳流量
在L-苯丙氨酸的生物合成中,pheA基因编码的CM-PDT的双功能酶是关键的催化酶,它催化分支酸转化为预苯酸,再进一步将预苯酸脱水生成苯丙酮酸,最终通过转氨作用形成L-苯丙氨酸,该酶与L-苯丙氨酸结合引起反馈抑制,其表达水平和酶活性直接影响L-苯丙氨酸的合成效率[4]。将基因pheA的309位谷氨酰胺(Gln)替换为赖氨酸(Lys),得到基因pheAfbr,Q309K突变解除了L-苯丙氨酸对其编码的双功能酶反馈抑制[16]。在菌株M4的基础上,整合基因pheAfbr,摇瓶验证L-苯丙氨酸产量变化,结果显示,菌株M5的L-苯丙氨酸的摇瓶产量提高到了8.7 g/L(图4),相比于M4提高了约42.6%,pheAfbr基因的整合使催化反应更高效,将更多的碳通量引导到了L-苯丙氨酸的合成途径中。
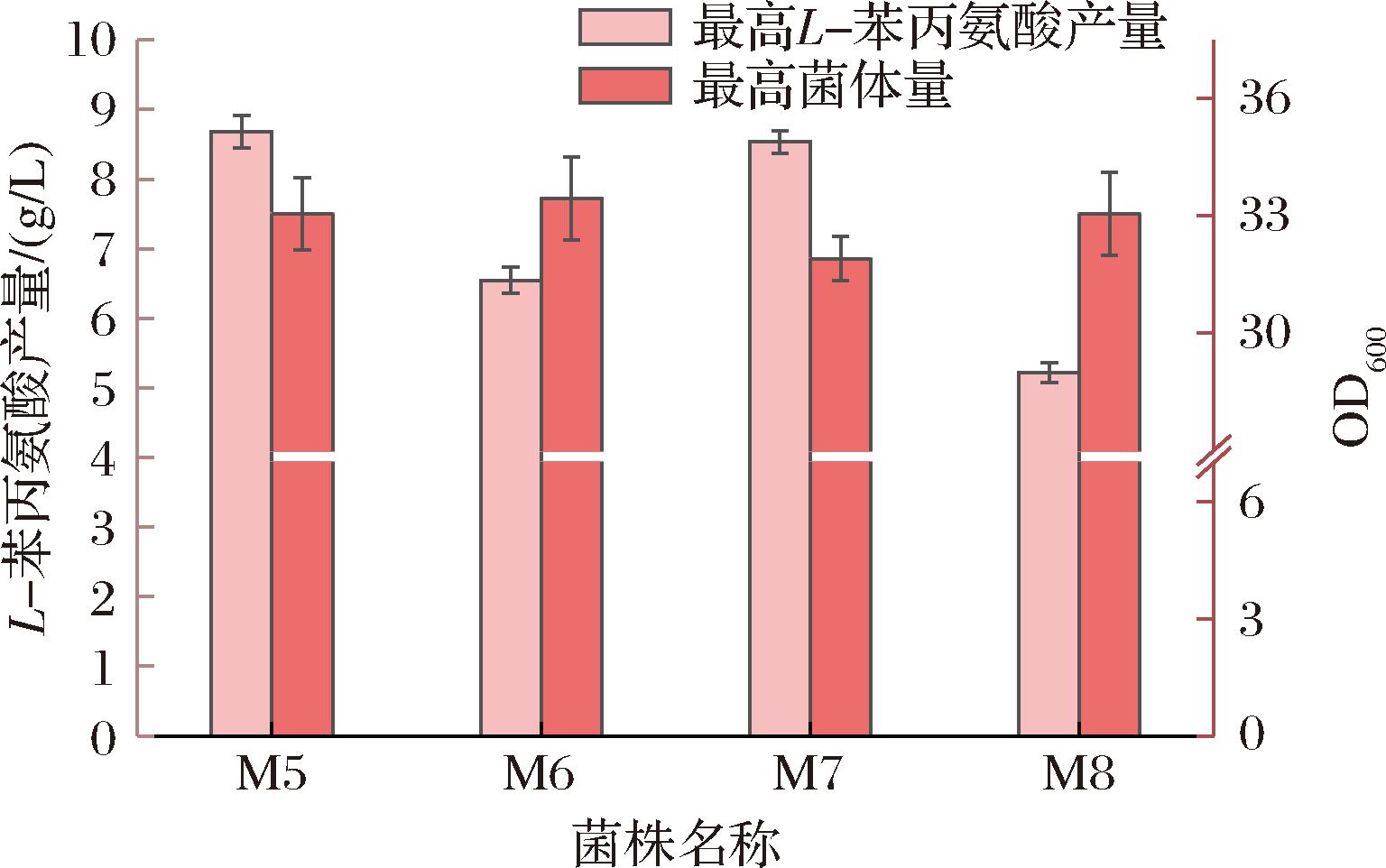
图4 M7、M8、M9和M10菌株摇瓶发酵生产得到的最高L-苯丙氨酸产量及最高的OD600值
Fig.4 The highest L-phenylalanine production and maximum OD600 values obtained from shake flask fermentation of strains M7, M8, M9, and M10
为了进一步提高L-苯丙氨酸合成路径中的碳流量,敲除未改造过的支路莽草酸脱氢酶编码的基因ydiB,基因ydiB与发挥主要作用的aroE基因同时参与L-苯丙氨酸合成途径中莽草酸的生成,同时ydiB参与生成奎宁酸[16]。在M5的基础上,对莽草酸脱氢酶ydiB基因实施敲除操作,得到菌株M6。实验结果显示,菌株M6的L-苯丙氨酸的摇瓶产量相对于M5降低到了6.5 g/L(图4)。结果证明虽然生产莽草酸主要由aroE基因发挥作用,但敲除ydiB基因加强的中心碳通量不足以弥补敲除ydiB基因后所减少的碳通量,而使产量大幅降低。
ilvE基因编码支链氨基酸转氨酶,参与多种氨基酸的合成与分解代谢,而aspC基因编码天冬氨酸转氨酶,这2个基因与编码芳香族氨基酸转氨酶的基因tyrB一起,参与合成L-苯丙氨酸[4,17]。同时由于基因tyrB和aspC同时参与L-酪氨酸的合成,为了不强化L-酪氨酸的合成,选择在假基因位点gapC处整合单基因ilvE,得到菌株M7。由图4可知,单独整合ilvE基因L-苯丙氨酸产量几乎没有变化,证明基因ilvE并不是促进L-苯丙氨酸合成的主要基因。
在莽草酸途径中,aroB基因编码的3-脱氢莽草酸合酶催化DAHP转化为3-脱氢莽草酸,是莽草酸途径中的关键步骤之一[18]。在菌株M5的基础上整合3-脱氢莽草酸合酶编码基因aroB,得到菌株M8,摇瓶发酵后测定其L-苯丙氨酸产量。实验结果显示,菌株M8的L-苯丙氨酸的摇瓶产量相对于M5降低到了5.2 g/L(图4)。aroB基因编码的酶通常参与莽草酸途径的早期步骤,aroB基因整合后L-苯丙氨酸产量下降,说明额外整合的aroB基因打破了原有代谢网络的平衡,原本的菌株已经达到最优表达量,使得L-苯丙氨酸合成减少。
aroD基因编码3-脱氢奎尼酸脱水酶(3-dehydroquinate dehydratase),它催化3-脱氢奎尼酸转化为3-脱氢莽草酸,是L-苯丙氨酸合成途径中的重要限速步骤[14,19]。在M5的基础上整合基因aroD,得到M9。摇瓶结果显示,菌株M9的L-苯丙氨酸的摇瓶产量上升到了10.6 g/L(图5),提高了约原产量的21.8%,结果证明,在代谢工程中aroD基因控制的酶是关键限速步骤,过表达基因aroD可以提高前体物质的供应,进而大幅度促进L-苯丙氨酸的合成[16,20]。
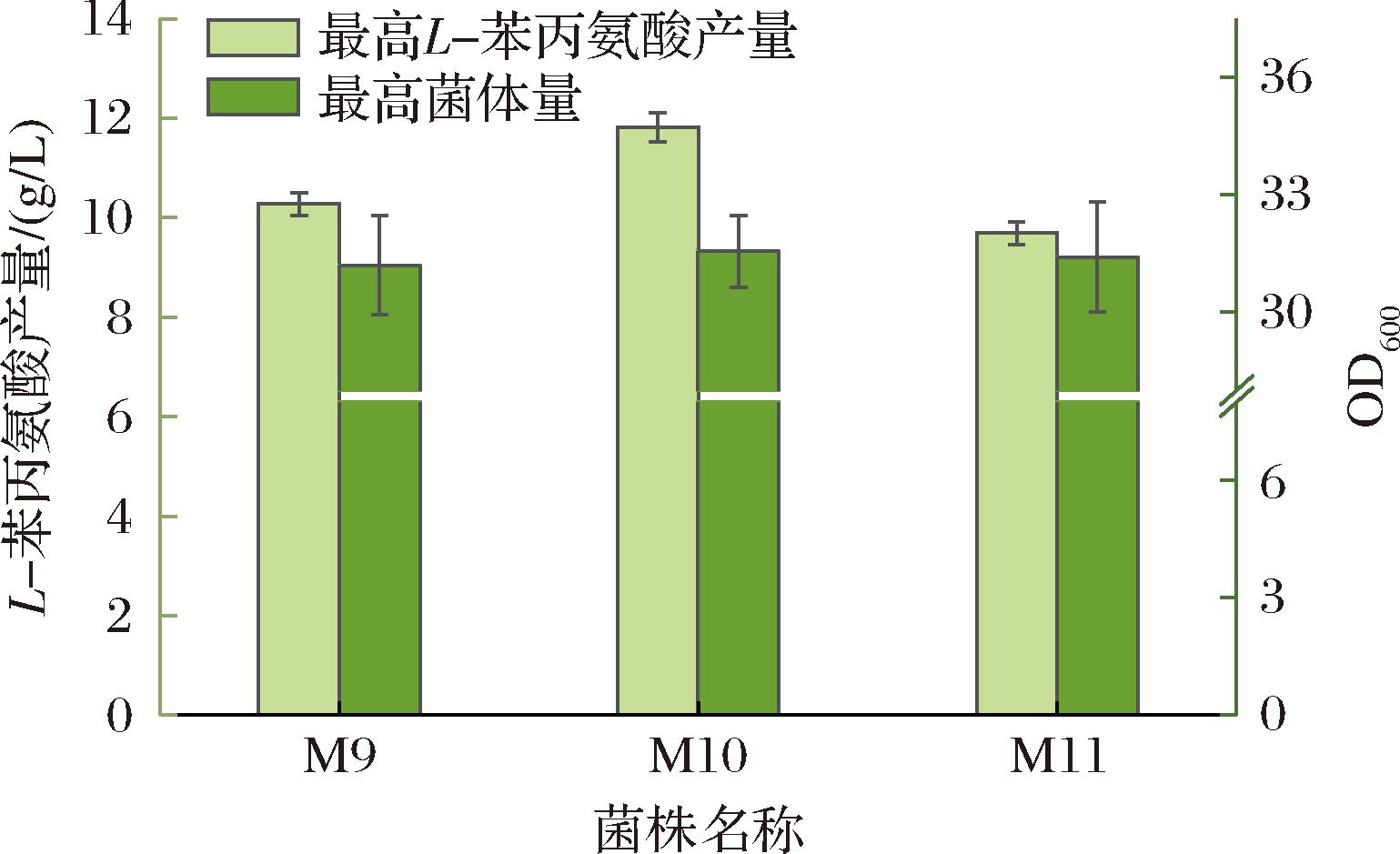
图5 M9、M10和M11菌株摇瓶发酵生产得到的最高L-苯丙氨酸产量及最高的OD600值
Fig.5 The highest L-phenylalanine production and maximum OD600 values obtained from shake flask fermentation of strains M9, M10, and M11
aroK基因编码莽草酸激酶,它与基因aroL一起催化莽草酸与ATP反应生成莽草酸-3-磷酸,OLDIGES等[21]发现基因aroK的加强比基因aroL对L-苯丙氨酸积累的促进效果更加显著。因此本研究针对aroK基因进行过表达,得到菌株M10,其L-苯丙氨酸的摇瓶产量上升到了11.8 g/L(图5)。
aroC基因编码分支酸合成酶,它催化5-烯醇式丙酮酰莽草酸-3-磷酸转化为分支酸,这是芳香族氨基酸合成途径中的最后一步共同反应[22-23]。在M10的基础上整合aroC基因,得到M11,结果显示L-苯丙氨酸的摇瓶产量出现了小幅度下降,为9.7 g/L(图5),说明过表达的aroC基因扰乱了原有代谢网络的稳态,在该基因整合前已实现最优表达,达到平衡状态。
2.4 促进L-苯丙氨酸分泌转运
在大肠杆菌中,氨基酸转运蛋白基因aroP能够将胞外的L-苯丙氨酸转运至胞内供应菌体生长,而氨基酸转运蛋白基因yddG能够转运L-苯丙氨酸到胞外[24]。在菌株M10的基础上对芳香族氨基酸转运蛋白aroP基因进行敲除,得到菌株M12,摇瓶发酵测定其L-苯丙氨酸产量变化。实验结果显示,菌株M12的L-苯丙氨酸的摇瓶产量相对于M10降低到了8.6 g/L(图6)。aroP基因控制芳香族氨基酸逆浓度梯度转运进入细胞,但敲除后L-苯丙氨酸产量下降,表明其参与维持细胞的正常生理功能和代谢平衡,敲除反而影响了细胞本身的代谢平衡。
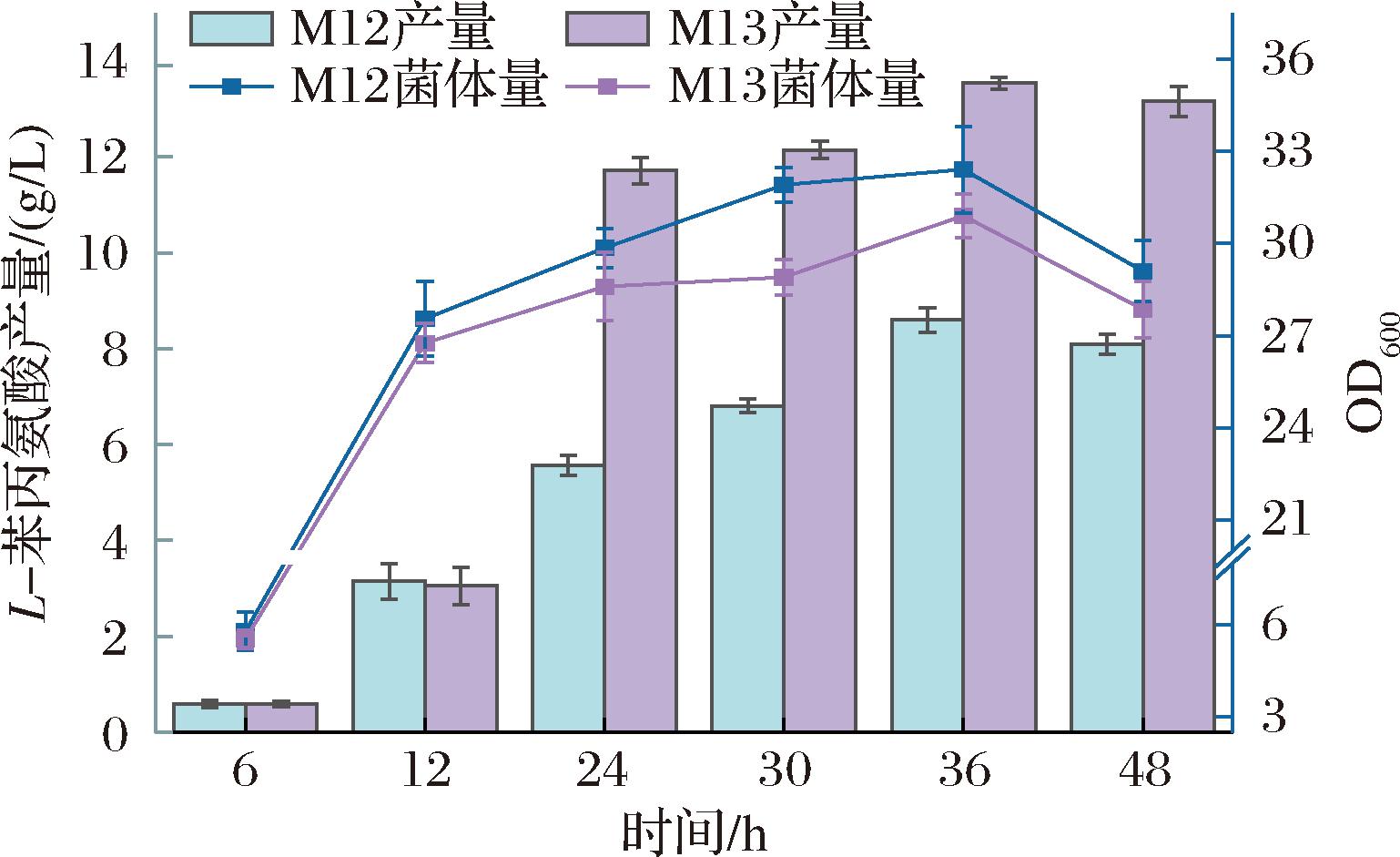
图6 M12、M13菌株摇瓶发酵生产L-苯丙氨酸产量及OD600
Fig.6 The yield of L-phenylalanine and the OD600 value in the shake-flask fermentation of strain M12, M13
在菌株M10的基础上整合氨基酸转运蛋白基因yddG,得到菌株M13,摇瓶发酵后测定其L-苯丙氨酸产量。结果显示,菌株M13的L-苯丙氨酸的摇瓶产量上升到了13.5 g/L(图6),相比M10提高了14.4%。结果表明yddG基因确实能够促进L-苯丙氨酸蛋白排出胞外,对L-苯丙氨酸的积累有着正向作用。
最终得到改造菌株M13,其摇瓶产量在36 h时达到最高的13.5 g/L,其关键改造步骤的产量变化见表2。
表2 关键改造步骤L-苯丙氨酸产量变化
Table 2 The changes in the yield of L-phenylalanine during key modification steps
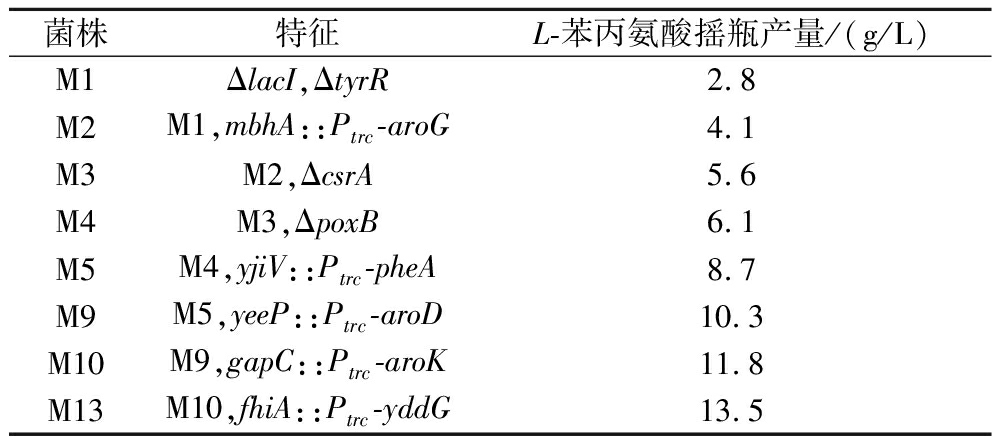
菌株特征L-苯丙氨酸摇瓶产量/(g/L)M1ΔlacI,ΔtyrR2.8M2M1,mbhA::Ptrc-aroG4.1M3M2,ΔcsrA5.6M4M3,ΔpoxB6.1M5M4,yjiV::Ptrc-pheA8.7M9M5,yeeP::Ptrc-aroD10.3M10M9,gapC::Ptrc-aroK11.8M13M10,fhiA::Ptrc-yddG13.5
2.5 RT-PCR量化L-苯丙氨酸相关基因的作用
上述结果为深入理解L-苯丙氨酸代谢调控网络提供了实验依据,明确了这些代谢物水平调节因子基因对L-苯丙氨酸生产的影响。为了确定靶基因是否在转录水平有调整,与野生型W3110菌株相比,在M13菌株中进行了RT-PCR[11,25]。
相对表达水平分析表明,在最终构建的M13菌株中,aroD、tyrA、pheA、aroG、aroK基因的表达量均显著上调3倍及以上,提示这些基因为限制L-苯丙氨酸合成的关键上调基因。其中,tyrA基因在未改造背景下本底表达水平较高,经改造后表达进一步提升,表明其在L-苯丙氨酸生物合成中具有重要作用。而基因tyrB、aroA、yddG的表达水平上调;csrA、tyrR、poxB基因敲除后表达明显消失;而基因pykF和ppsA在没有改造的情况下表达下降,推测是因为基因csrA的敲除抑制了其显性表达[3](图7);同时基因tktA在没有改造情况下表达被抑制。如果想进一步得到更高的L-苯丙氨酸产量,替换更高表达的相关关键基因的启动子可能是较好的方案。分析结果通过比较野生型与工程菌株在转录组层面的差异,从分子水平验证了代谢工程策略的实际效果,即M13菌株主要在转录后水平调节这些靶点。通过量化关键基因的mRNA丰度,验证了代谢工程改造对目标基因的转录调控效果,建立了高产L-苯丙氨酸菌株基因型与表型之间的直接关联。相对表达水平的分析表明,过表达后的基因表达明显上调,敲除的基因则明显不再表达;而未被改动的基因tyrA、tyrB被促进了表达;基因tktA、pykF和ppsA在没有改造的情况下表达下降。
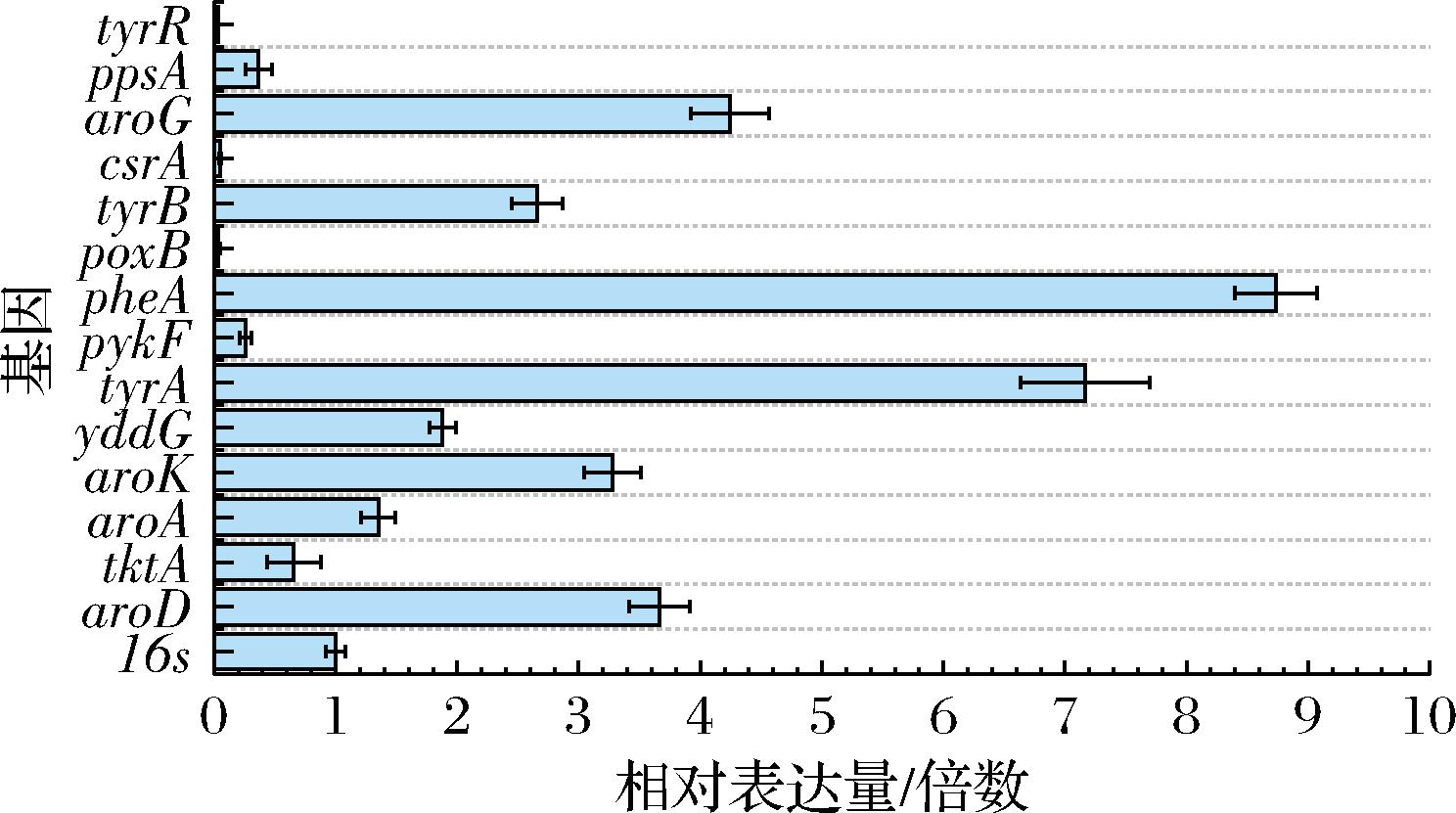
图7 RT-PCR在W3110和M13中测量预测的靶基因相对表达水平
Fig.7 Measurement of relative expression levels of predicted target genes in W3110 and M13 using RT-PCR
2.6 5 L发酵罐发酵培养及发酵液氨基酸成分分析
将重组菌株M13在5 L发酵罐上进行补料分批发酵培养[17]。根据实验数据可知,发酵到3.5 h左右,发酵液溶氧上升,底糖消耗干净,开始指数流加葡萄糖进行补料。结果表明,M13在60 h时达到最高产量62.7 g/L,糖酸转化率为22.3%,36 h后菌体生长速度缓慢,48 h后菌体开始裂解,72 h时OD600值下降到99.26(图8)。
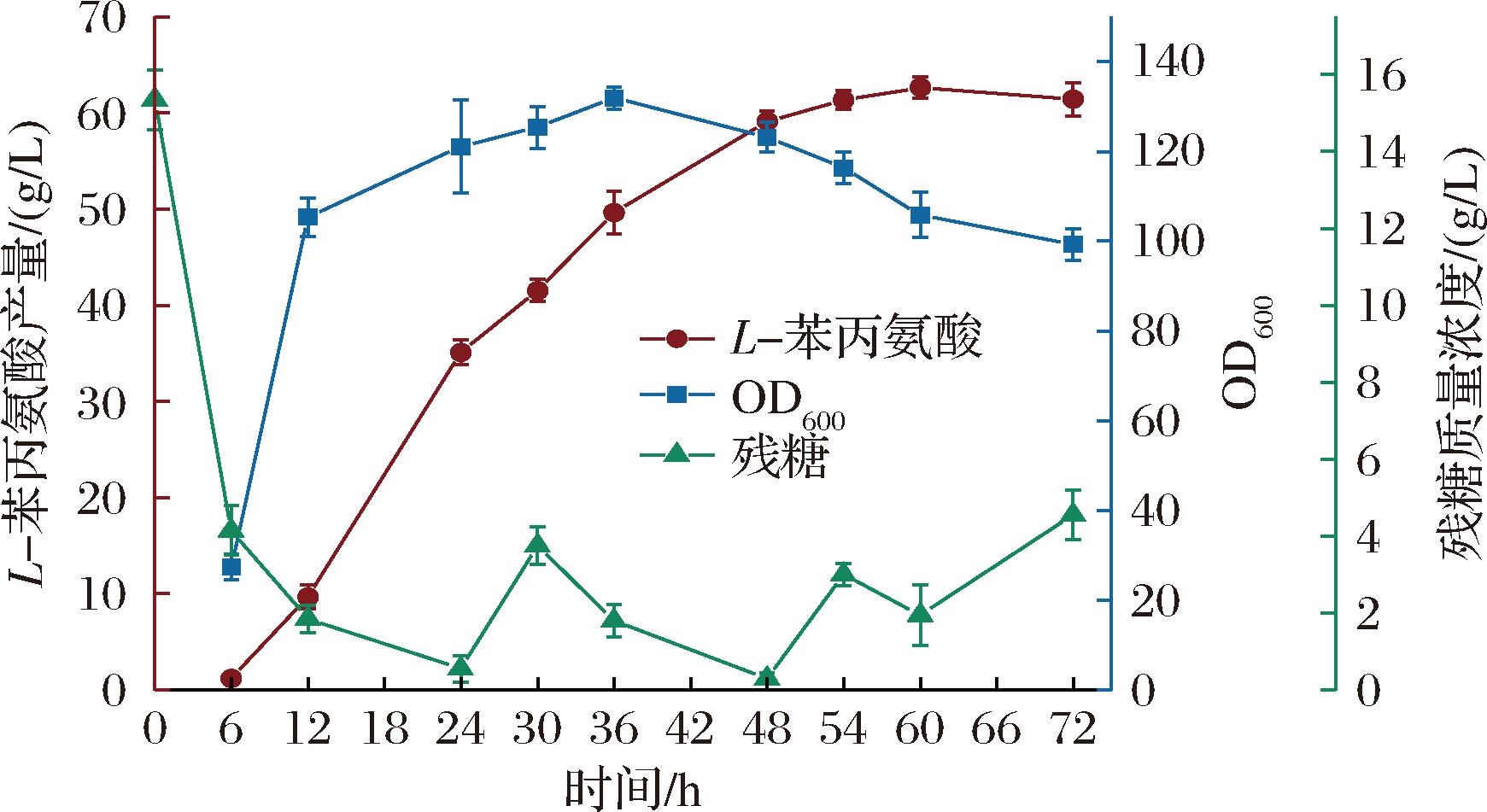
图8 M13菌株在5 L发酵罐内发酵生产L-苯丙氨酸产量随时间变化的曲线
Fig.8 The curve of L-phenylalanine production over time during the fermentation of strain M13 in a 5 L fermenter
使用氨基酸分析仪对发酵液成分进行分析,在对5 L发酵罐的发酵液进行氨基酸成分分析后,除L-苯丙氨酸以外,检测出酪氨酸(Tyr)含量约为1.12 g/L,赖氨酸(Lys)含量约为2.43 g/L(图9)。从结果可以看出,该顺序的基因改造最终并没有过多地促进L-酪氨酸的合成,可能是由于基因pheA的突变,使得更多的碳通量流向了L-苯丙氨酸,同时L-酪氨酸对关键酶的反馈抑制并没有被解除;Lys的含量相对较高,说明该发酵过程可能对于赖氨酸的合成具有较好的促进作用。较高的赖氨酸含量可能是由于改造后的M13菌株特性;也可能是发酵条件,如温度、pH值以及营养物质配比等,恰好符合了赖氨酸合成相关酶的活性需求,从而促使其生成。而发酵液中其他氨基酸成分的含量都较低,说明该菌株是一株较优的L-苯丙氨酸生产菌株。具体氨基酸及含量成分如表3所示。
表3 5 L发酵罐的发酵液中各氨基酸含量
Table 3 The contents of various amino acids in the fermentation broth of a 5 L fermenter
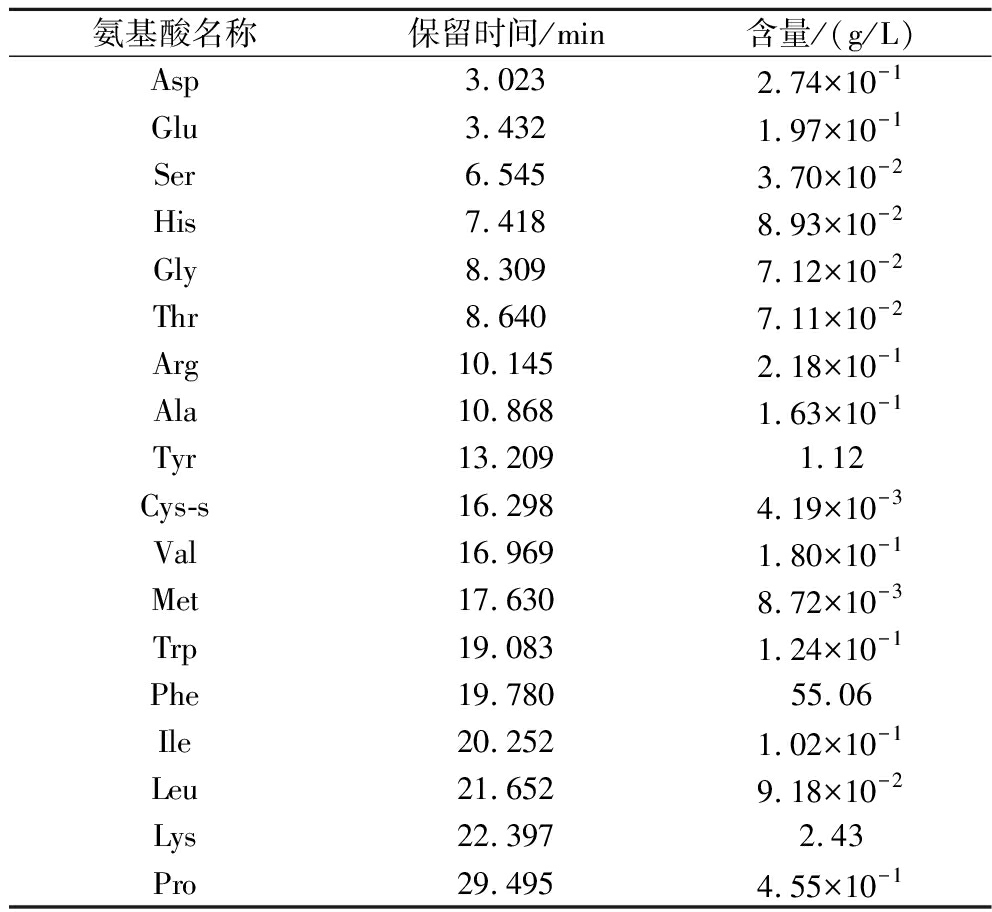
氨基酸名称保留时间/min含量/(g/L)Asp3.0232.74×10-1Glu3.4321.97×10-1Ser6.5453.70×10-2His7.4188.93×10-2Gly8.3097.12×10-2Thr8.6407.11×10-2Arg10.1452.18×10-1Ala10.8681.63×10-1Tyr13.2091.12Cys-s16.2984.19×10-3Val16.9691.80×10-1Met17.6308.72×10-3Trp19.0831.24×10-1Phe19.78055.06Ile20.2521.02×10-1Leu21.6529.18×10-2Lys22.3972.43Pro29.4954.55×10-1
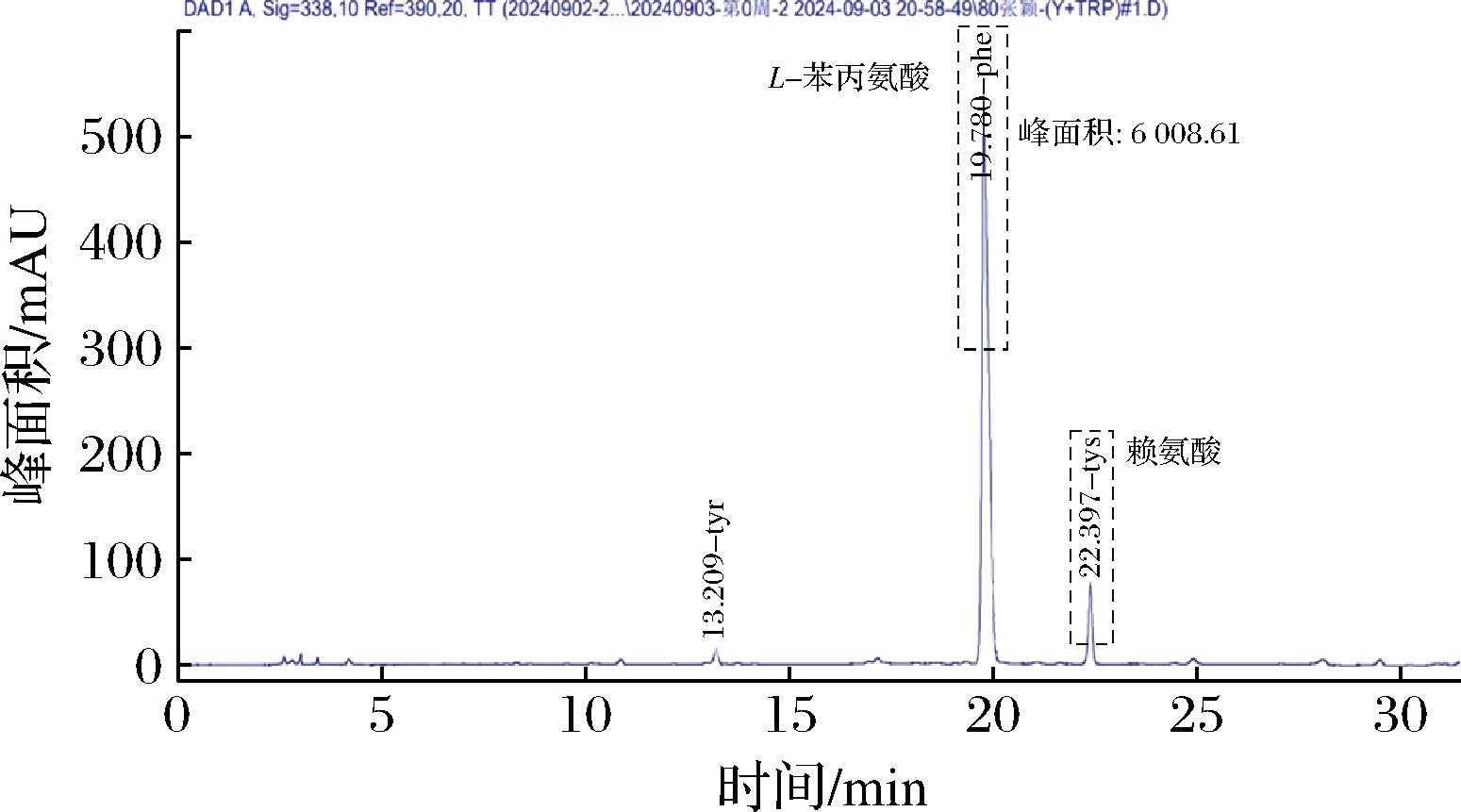
图9 M13菌株经5 L发酵罐发酵后所得发酵液的氨基酸成分图谱
Fig.9 Amino acid composition profile of the fermentation broth obtained from the fermentation of strain M13 in a 5 L fermenter
3 结论与展望
L-苯丙氨酸作为一种重要的芳香族氨基酸,目前主要通过微生物发酵法进行生产,但目前不确定代谢流重新分配过程中表达水平显著变化的基因,本研究结合已报道的L-苯丙氨酸生物合成途径,在优化代谢路径的基础上引入RT-PCR的验证手段,揭示了该代谢改造顺序对L-苯丙氨酸生产的影响,为突破L-苯丙氨酸生物合成的瓶颈提供数据支持,同时为其他氨基酸和天然产物的高产菌株开发提供方法论参考。本研究以野生型E.coli W3110作为底盘菌株,首先敲除乳糖操纵子阻遏基因lacI和转录水平调节因子基因tyrR,过表达经过点突变得到的限速酶调控基因![]() 接下来加强合成前体PEP和E4P的供给效率,敲除全局调控因子基因csrA,敲除基因poxB以上调菌体量,得到摇瓶产量为6.1 g/L的菌株M4;接下来对关键限速酶基因pheA进行点突变,得到
接下来加强合成前体PEP和E4P的供给效率,敲除全局调控因子基因csrA,敲除基因poxB以上调菌体量,得到摇瓶产量为6.1 g/L的菌株M4;接下来对关键限速酶基因pheA进行点突变,得到![]() 并将其整合,该步骤解除了L-苯丙氨酸结合引起的该酶的反馈抑制,敲除基因poxB,整合基因pheA、aroD、aroK,此时摇瓶产量上升到11.8 g/L;为了加强L-苯丙氨酸的分泌,整合了yddG基因,得到菌株M13,其摇瓶产量达到13.5 g/L。为了建立基因型与表型的最终联系,结合RT-PCR手段,量化大肠杆菌W3110通过代谢改造后与L-苯丙氨酸生产相关基因的表达情况,相对表达水平分析表明改动tyrA,tyrB后其表达促进;基因tktA、pykF和ppsA在没有改造的情况下表达下降,这些结果有助于加深对L-苯丙氨酸在大肠杆菌中生产的理解。最终在5 L发酵罐中对M13进行发酵,M13菌株最高OD600值达到131.9,在5 L发酵罐中发酵60 h时积累了最高的L-苯丙氨酸(62.7 g/L),糖酸转化率达到22.3%。
并将其整合,该步骤解除了L-苯丙氨酸结合引起的该酶的反馈抑制,敲除基因poxB,整合基因pheA、aroD、aroK,此时摇瓶产量上升到11.8 g/L;为了加强L-苯丙氨酸的分泌,整合了yddG基因,得到菌株M13,其摇瓶产量达到13.5 g/L。为了建立基因型与表型的最终联系,结合RT-PCR手段,量化大肠杆菌W3110通过代谢改造后与L-苯丙氨酸生产相关基因的表达情况,相对表达水平分析表明改动tyrA,tyrB后其表达促进;基因tktA、pykF和ppsA在没有改造的情况下表达下降,这些结果有助于加深对L-苯丙氨酸在大肠杆菌中生产的理解。最终在5 L发酵罐中对M13进行发酵,M13菌株最高OD600值达到131.9,在5 L发酵罐中发酵60 h时积累了最高的L-苯丙氨酸(62.7 g/L),糖酸转化率达到22.3%。
由于产量仍有提高的空间,可能是负责前体合成的相关基因tktA受到了抑制,考虑替换不同的启动子以提高其表达量,另外,菌株在发酵后期菌体量下降,可以考虑增加菌株对L-苯丙氨酸的耐受抗性方向进行改造,增强菌株生产效率,并通过培养基优化寻找最佳发酵条件等策略,持续提升L-苯丙氨酸的合成效率。
[1] SALMAHAMINATI, ROCA-SANJU N D.The photophysics and photochemistry of phenylalanine, tyrosine, and tryptophan:A CASSCF/CASPT2 study[J].ACS Omega, 2024, 9(33):35356-35363.
N D.The photophysics and photochemistry of phenylalanine, tyrosine, and tryptophan:A CASSCF/CASPT2 study[J].ACS Omega, 2024, 9(33):35356-35363.
[2] BANG H B, CHOI I H, JANG J H, et al.Engineering of Escherichia coli for the economic production L-phenylalanine in large-scale bioreactor[J].Biotechnology and Bioprocess Engineering, 2021, 26(3):468-475.
[3] LIU X Z, NIU H, LI Q, et al.Metabolic engineering for the production of L-phenylalanine in Escherichia coli[J].3 Biotech, 2019, 9(3):85.
[4] LIU L W, LIU X Z, MA Q Q, et al.Construction of recombinant Escherichia coli for production of L-phenylalanine-derived compounds[J].World Journal of Microbiology and Biotechnology, 2021, 37(5):84.
[5] HIRASAWA T, SATOH Y, KOMA D.Production of aromatic amino acids and their derivatives by Escherichia coli and Corynebacterium glutamicum[J].World Journal of Microbiology and Biotechnology, 2025, 41(2):65.
[6] KONSTANTINOV K B, NISHIO N, SEKI T, et al.Physiologically motivated strategies for control of the fed-batch cultivation of recombinant Escherichia coli for phenylalanine production[J].Journal of Fermentation and Bioengineering, 1991, 71(5):350-355.
[7] 曾小冰, 范长胜, 江培翃, 等.外源基因pheA、aroG和tyrB在苯丙氨酸合成途径中的共表达[J].生物工程学报, 2000, 16(6):671-674.ZENG X B, FAN C S, JIANG P H, et al.Co-expression of heterologous genes pheA, aroG and tyrB for biosynthesis pathway of L-phenylalanine[J].Chinese Journal of Biotechnology, 2000, 16(6):671-674.
[8] 门佳轩, 熊博, 郝亚男, 等.代谢工程优化大肠杆菌高效合成L-苯丙氨酸[J].食品科学, 2021, 42(2):114-120.MEN J X, XIONG B, HAO Y N, et al.Metabolic engineering of Escherichia coli for efficient synthesis of L-phenylalanine[J].Food Science, 2021, 42(2):114-120.
[9] WANG X G, QIU C, CHEN C H, et al.Metabolic engineering of Escherichia coli for high-level production of L-phenylalanine[J].Journal of Agricultural and Food Chemistry, 2024, 72(19):11029-11040.
[10] CHEN M L, HAN C, ZHOU P, et al.Rational metabolic engineering of Escherichia coli for the industrial-scale production of L-phenylalanine [J].Bioresource Technology, 2025, 426:132325.
[11] ZHANG M H, ZHAO S J.Different transcriptomic and metabolomic analysis of Saccharomyces cerevisiae BY4742 and CEN.PK2-1C strains[J].Archives of Microbiology, 2024, 206(12):460.
[12] ZHU X W, WU Y K, LV X Q, et al.Combining CRISPR-Cpf1 and recombineering facilitates fast and efficient genome editing in Escherichia coli[J].ACS Synthetic Biology, 2022, 11(5):1897-1907.
[13] NIE M Z, WANG J Y, CHEN Z Y, et al.Systematic engineering enables efficient biosynthesis of L-phenylalanine in E.coli from inexpensive aromatic precursors[J].Microbial Cell Factories, 2024, 23(1):12.
[14] SUN W, DING D Q, BAI D Y, et al.Transcriptomics and metabolomics analysis of L-phenylalanine overproduction in Escherichia coli[J].Microbial Cell Factories, 2023, 22(1):65.
[15] TYAGI N, SAINI D, GULERIA R, et al.Designing an Escherichia coli strain for phenylalanine overproduction by metabolic engineering[J].Molecular Biotechnology, 2017, 59(4):168-178.
[16] LIU S P, XIAO M R, ZHANG L, et al.Production of L-phenylalanine from glucose by metabolic engineering of wild type Escherichia coli W3110[J].Process Biochemistry, 2013, 48(3):413-419.
[17] NISHIMURA A, ISOGAI S, MURAKAMI N, et al.Isolation and analysis of a sake yeast mutant with phenylalanine accumulation[J].Journal of Industrial Microbiology and Biotechnology, 2022, 49(3):kuab085.
[18] YE D, XU H J, XIA H W, et al.Targeting SERT promotes tryptophan metabolism:Mechanisms and implications in colon cancer treatment[J].Journal of Experimental &Clinical Cancer Research, 2021, 40(1):173.
[19] LIU Y F, XU Y R, DING D Q, et al.Genetic engineering of Escherichia coli to improve L-phenylalanine production[J].BMC Biotechnology, 2018, 18(1):5.
[20] FATUR K, KREFT S.Common anticholinergic solanaceaous plants of temperate Europe - A review of intoxications from the literature (1966-2018)[J].Toxicon, 2020, 177:52-88.
[21] OLDIGES M, KUNZE M, DEGENRING D, et al.Stimulation, monitoring, and analysis of pathway dynamics by metabolic profiling in the aromatic amino acid pathway[J].Biotechnology Progress, 2004, 20(6):1623-1633.
[22] YOO H, SHRIVASTAVA S, LYNCH J H, et al.Overexpression of arogenate dehydratase reveals an upstream point of metabolic control in phenylalanine biosynthesis[J].The Plant Journal, 2021, 108(3):737-751.
[23] CHEN M L, LIANG H Y, HAN C, et al.Engineering of global transcription factor FruR to redirect the carbon flow in Escherichia coli for enhancing L-phenylalanine biosynthesis[J].Microbial Cell Factories, 2022, 21(1):222.
[24] CHEN S H, JIN C H, OHGAKI R, et al.Structure-activity characteristics of phenylalanine analogs selectively transported by L-type amino acid transporter 1 (LAT1)[J].Scientific Reports, 2024, 14:4651.
[25] ZAO C L, YANG Y C, TOMANEK L, et al.PCR monitoring of parasitemia during drug treatment for canine Chagas disease[J].Journal of Veterinary Diagnostic Investigation, 2019, 31(5):742-746.