曲乃酒之骨,大曲是白酒酿造的糖化发酵剂,在白酒生产中起提供菌源、糖化发酵、投粮、生香等重要作用。大曲断面局部区域常出现红、黄、黑等不同颜色菌斑(本研究中“菌斑”指在大曲培菌发酵过程中,因特定条件差异从而在大曲断面形成的肉眼可见,且颜色或形态上明显区别于常规曲心的局部区域),这些局部差异主要受大曲中微生物种类、生长环境、生长阶段影响[1],是微生物及其代谢活动的体现。例如,“红心曲”中心区域的红色、“槐瓤曲”的金黄色[2]以及中高温大曲断面出现的黑色斑点[3],均表明相应区域的微生物组成和代谢产物存在一定差异。
目前,大曲质量评定普遍采用感官评价与理化指标检测相结合的方式,其中,大曲断面色泽及香气作为感官评价的关键指标在大曲质量评定中具有较高权重[3]。然而,现有研究多数聚焦于对大曲整体微生物群落和挥发性风味物质的解析,鲜少关注大曲色泽形成机制。红菌斑(RJB)和黑菌斑(BJB)是中高温大曲断面较为常见的典型形态特征,与大曲断面色泽、感官评价相关。同时,RJB、BJB作为中高温大曲断面中具有鲜明典型性和代表性的特征菌斑,是理解微生物-环境-代谢物-感官品质的突破口。
因此,本研究以中高温大曲断面常见的RJB、BJB为研究对象,以常规曲心(CG)作为对照,利用高通量测序及气相色谱-质谱联用技术,解析RJB、BJB和CG区域的微生物群落、挥发性风味物质组成及差异,探讨大曲断面微生物与挥发性风味物质之间的关联性,为传统大曲感官评价提供科学依据,对完善大曲质量评价体系和生产工艺优化具有一定理论价值和实践意义。
1 材料与方法
1.1 材料与试剂
样品采自四川某中高温大曲半成品曲房,从同一时间生产、同一时间出房的3间曲房中各抽取3块带有RJB的大曲、3块带有BJB的大曲,并从每块大曲中采集CG样品。如图1所示,使用无菌镊子分别挑取每块大曲的RJB区域、BJB区域以及CG区域样品,粉碎、混合均匀后编号为RJB1~3、BJB1~3、CG1~3。将每份混合样品等分为2份,密封于无菌自封袋中,1份用于挥发性风味物质检测,另1份用于高通量测序。

a-RJB区域;b-BJB区域;c-CG
图1 中高温大曲断面特征菌斑与CG形态
Fig.1 Morphological characteristics of characteristic microbial colonies and conventional Qu core in the cross-section of medium-high temperature Daqu
1.2 仪器与设备
7890B-5977B气相色谱-质谱联用仪、DB-WAX色谱柱(60 m×0.25 mm×0.25 μm)、50/30 μm DVB/CAR/PDMS三相萃取头,安捷伦科技公司;PAL多功能自动进样器,瑞士斯特分析仪器。
1.3 实验方法
1.3.1 大曲断面微生物群落结构检测
通过Illumina NovaSeq 6000测序系统(天津诺禾致源科技有限公司)进行高通量测序。采用CTAB法提取样品总DNA后,针对细菌16S rRNA基因V3~V4区(引物515F/806R)和真菌ITS1区(引物ITS5-1737F/ITS2-2043R)进行PCR扩增。扩增产物经纯化后构建文库,使用PE250双端测序模式进行分析。
1.3.2 大曲断面风味物质检测
样品前处理:准确称取10 g大曲样品,加入30 mL饱和NaCl溶液,超声浸泡提取1 h,4 000 r/min离心5 min后过滤。上清液经乙腈振荡萃取5 min后取下层有机液(重复萃取2次),合并有机相后使用5 g无水Na2SO4干燥过夜,氮吹浓缩至1 mL,待测。
气相色谱条件:DB-WAX色谱柱;载气为高纯He(1 mL/min);进样量1 μL,分流比10∶1;进样口温度250 ℃;程序升温:35 ℃(初始,保持5 min)→3 ℃/min→90 ℃(保持1 min)→3 ℃/min→150 ℃(保持1 min)→5 ℃/min→190 ℃(保持1 min)→10 ℃/min→220 ℃(最终,保持8 min)。
质谱条件:离子源(electron ionization,EI),电离能量70 eV,离子源温度230 ℃,四极杆温度150 ℃,离子检测(selected ion monitor,SIM),质谱扫描范围20~300 m/z。
定性定量分析:通过NIST20谱库和保留指数比对定性,内标法定量。所有样品平行测定3次。
1.4 数据处理
使用SIMCA 14.0软件对数据进行正交偏最小二乘判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA),使用联川生物云平台(https://www.omicstudio.cn)进行线性判别分析(Linear discriminant analysis Effect Size,LEfSe),使用Origin 2024、Metware Cloud (https://cloud.metware.cn)作图。
2 结果与分析
2.1 大曲断面特征菌斑微生物群落差异
2.1.1 微生物属水平差异
在RJB、BJB和CG样品中共检测到245个细菌属和18个真菌属(图2-a、图2-b)。其中,细菌共有属(3组样品均检出)有63个;CG、RJB、BJB特有细菌属(仅在对应组检出)数量分别为71、33、17个;真菌共有属有2个;RJB和BJB中检出的真菌特有属数量分别为9个和1个。CG中细菌物种丰富度最高,RJB中真菌物种丰富度最高。
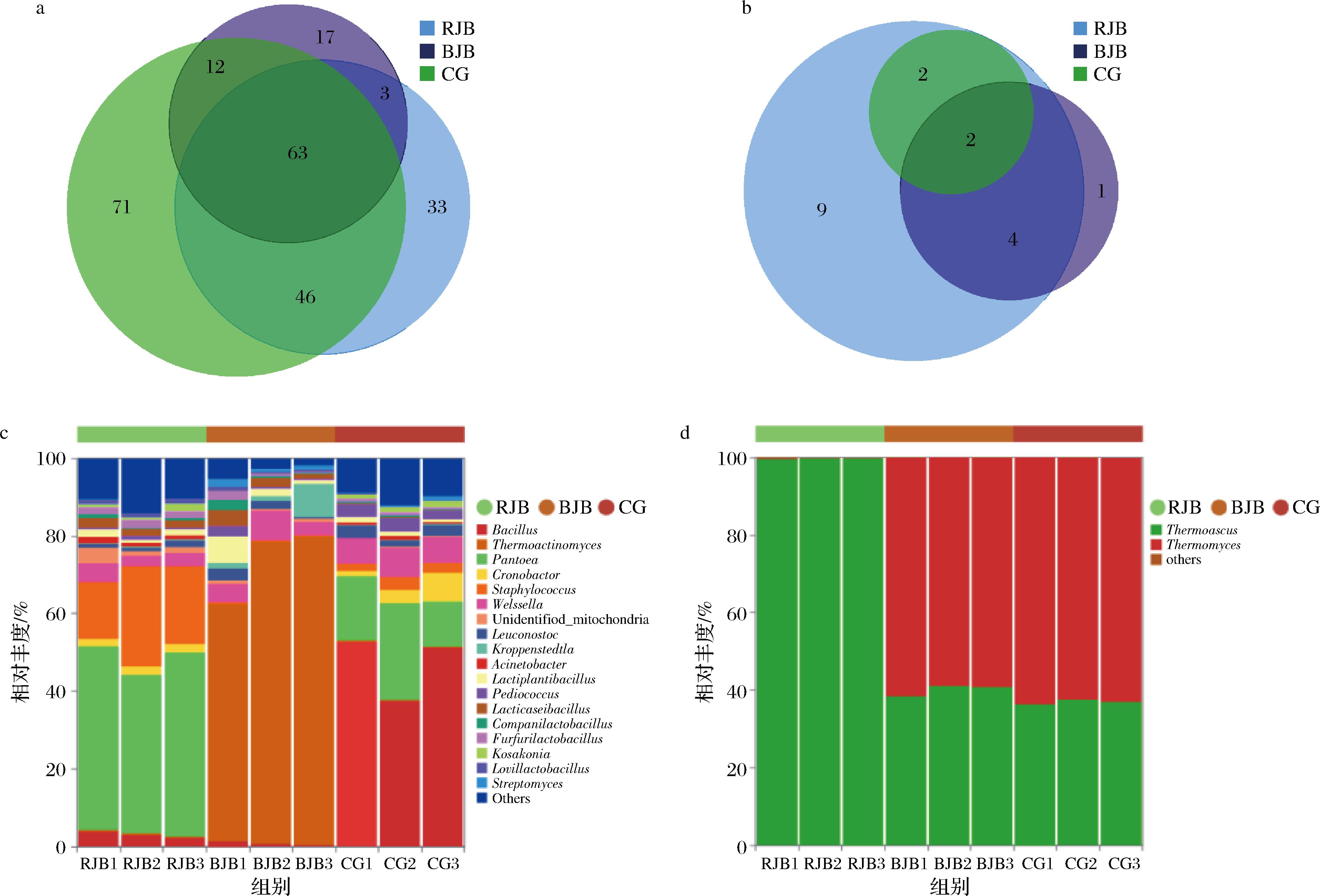
a-细菌韦恩图;b-真菌韦恩图;c-细菌丰度;d-真菌丰度
图2 中高温大曲断面特征菌斑微生物差异(属水平)
Fig.2 Microbial differences (at genus level) in characteristic colonies from the cross-section of medium-high temperature Daqu
将样品中平均相对丰度<1%的微生物归为“others”。3组样品的细菌群落主要由芽孢杆菌属(Bacillus)、高温放线菌属(Thermoactinomyces)、泛菌属(Pantoea)、葡萄球菌属(Staphylococcus)、魏斯氏菌属(Weissella)组成(图2-c),其中,RJB中细菌群落以泛菌属、葡萄球菌属为主,平均相对丰度分别为45.12%、20.24%,远高于BJB和CG,相关研究表明,泛菌属、葡萄球菌属与大曲酯化力、发酵力、氨基酸态氮含量呈正相关[4],可能导致RJB与CG在理化方面呈现一定差异;BJB中高温放线菌属以平均相对丰度72.95%占绝对优势,高温放线菌属具有耐高温特性,是大曲中主要细菌之一[5],能够分泌淀粉酶和酯化酶,是大曲香气生成的前体物[6];CG中细菌群落则以芽孢杆菌属、泛菌属为主,平均相对丰度分别为47.13%、17.61%,芽孢杆菌属是中高温大曲中优势细菌属,有利于浓香型白酒主体香味物质己酸乙酯的生成[7],CG中芽孢杆菌为主要优势细菌,充分说明CG对白酒风味形成的重要作用。
真菌群落主要以嗜热子囊菌属(Thermoascus)、嗜热真菌属(Thermomyces)为主(图2-d),嗜热子囊菌属在RJB、BJB、CG中相对丰度分别为99.81%、40.12%、36.93%,嗜热真菌属在RJB、BJB、CG中相对丰度分别为0.05%、59.87%、63.07%。已有研究表明,嗜热子囊菌属、嗜热真菌属等为高温优势真菌,能增强美拉德反应和焦糖化反应,形成黑色或深褐色化合物[8],可能与大曲断面RJB、BJB区域的颜色形成有关。
2.1.2 微生物种水平差异
基于种水平中细菌平均相对丰度>1%,真菌平均相对丰度>0.5%,筛选出12种细菌、3种真菌。细菌群落中(图3-a),相对丰度最高的为普通高温放线菌(Thermoactinomyces vulgaris)(BJB:14.47%>CG:0.40%>RJB:0.36%),其最适生长温度为50 ℃,能够水解淀粉、纤维素等[9];其次为食窦魏斯氏菌(Weissella cibaria)(CG:6.07%>BJB:3.87%>RJB:2.73%),其在中高温大曲中相对丰度较高[10],是RJB、BJB、CG共有的优势菌种。真菌种水平中橙色嗜热子囊菌(Thermoascus aurantiacus)(RJB:99.81%>BJB:40.12%>CG:36.93%)占据绝对优势(图3-b),已有研究证实该菌种存在橙黄或红棕的闭囊壳[11],一定条件下可代谢产生红色色素,可能是RJB形成的关键微生物[12],其次为疏绵状嗜热丝孢菌(Thermomyces lanuginosus)(CG:63.00%>BJB:59.86%>RJB:0.05%),该菌种能够产生具有高活性和稳定性的半纤维素酶和淀粉水解酶[13],能够在55~60 ℃的条件下维持稳定的酶活性[14],鉴于其在CG和BJB中相对丰度占据绝对优势,推测其可能发挥重要作用。
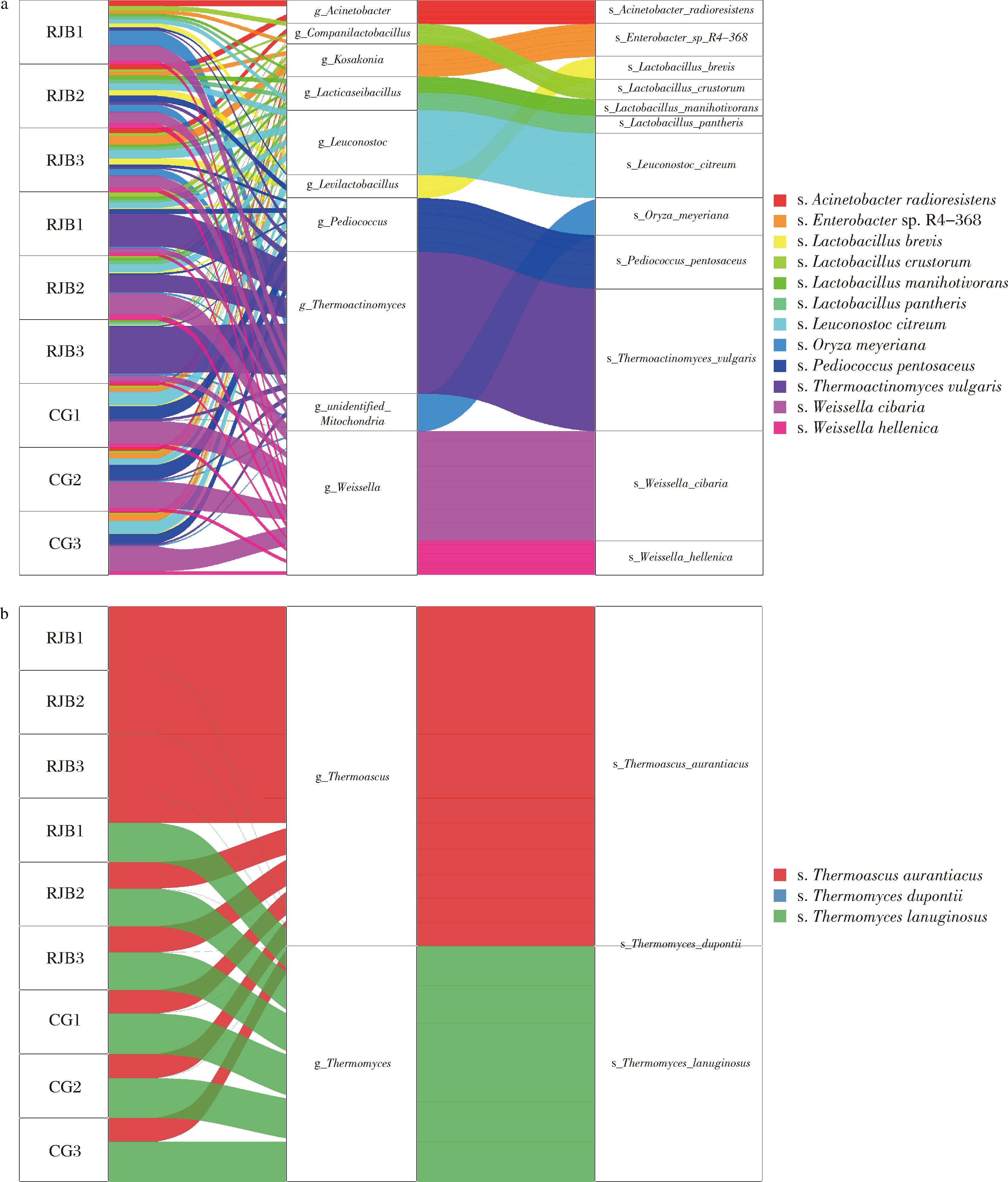
a-细菌桑基图;b-真菌桑基图
图3 中高温大曲断面特征菌斑微生物差异(种水平)
Fig.3 Microbial differences (at species level) in characteristic colonies from the cross-section of medium-high temperature Daqu
2.1.3 差异微生物筛选
采用LEfSe分析筛选差异微生物[LDA(linear discriminant analysis)>3,P<0.05]。如图4所示,共鉴定出14个差异细菌属和2个差异真菌属。其中RJB中鉴定出9个差异细菌属、1个差异真菌属。差异细菌属有泛菌属、葡萄球菌属、Unidentified mitochondria、不动杆菌属(Acinetobacter)、轻乳杆菌属(Levilactobacillus)、假单胞菌属(Pseudomonas)、Unidentified chloroplast、寡养单胞菌属(Stenotrophomonas)、类芽孢杆菌属(Paenibacillus),差异真菌属为嗜热子囊菌属。BJB中差异细菌属有链霉菌属(Streptomyces)、慢乳杆菌属(Lentilactobacillus)、粘液乳杆菌属(Limosilactobacillus),其中链霉菌属(BJB∶1.16%>CG∶0.52%>RJB∶0.08%)可能产生黑色素,是导致BJB呈现黑色的原因之一[15]。CG中差异细菌属为芽孢杆菌属、宽乳酸杆菌属(Latilactobacillus),差异真菌属为嗜热真菌属。这些微生物在不同菌斑的差异分布可能是RJB、BJB与CG在颜色、形态上表现出差异的主要原因,同时为大曲呈现出不同的风味特征奠定了微生物学基础。
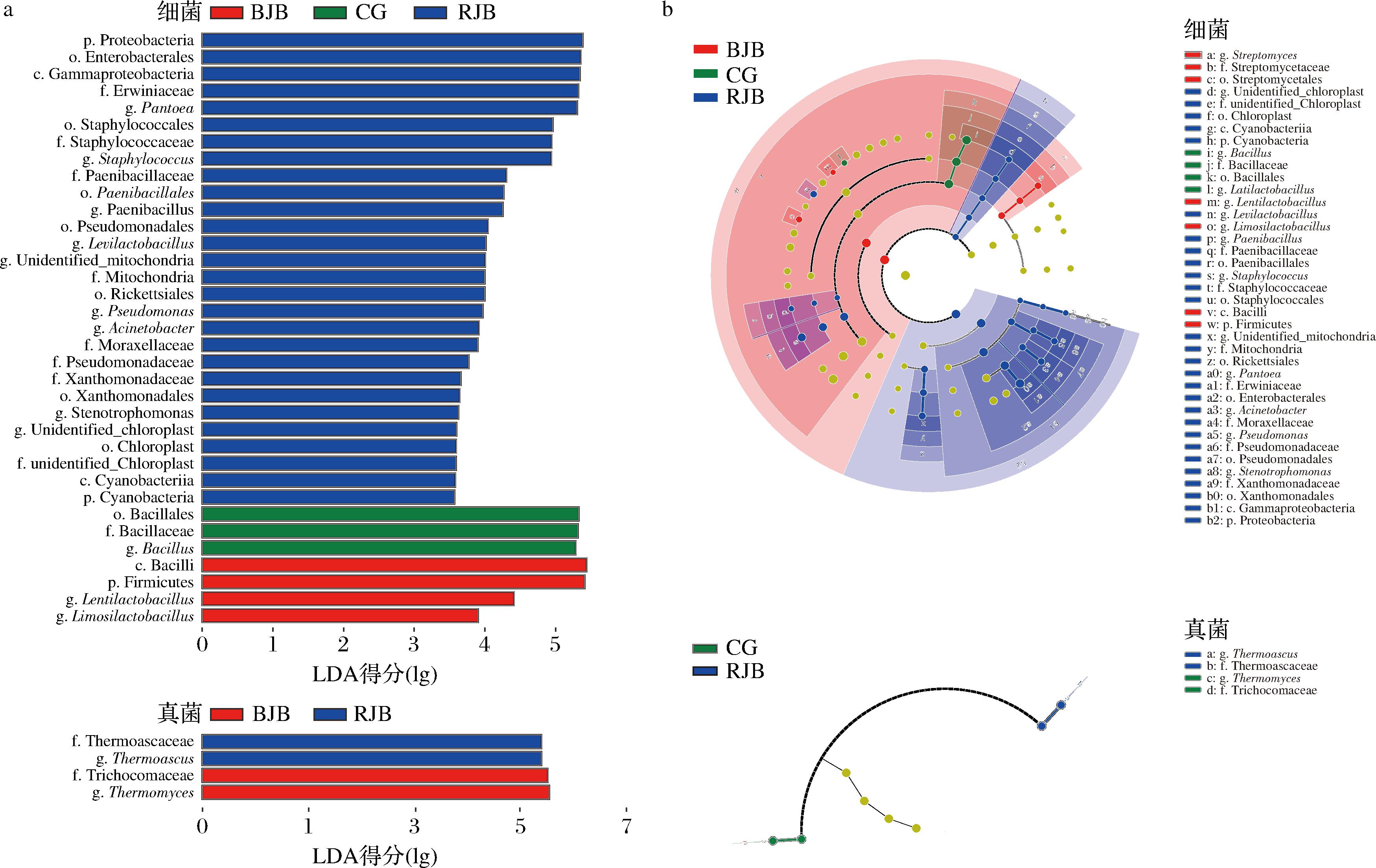
a-LDA得分图;b-分支图
图4 中高温大曲断面特征菌斑差异微生物
Fig.4 Differential microorganisms in characteristic colonies from the cross-section of medium-high temperature Daqu
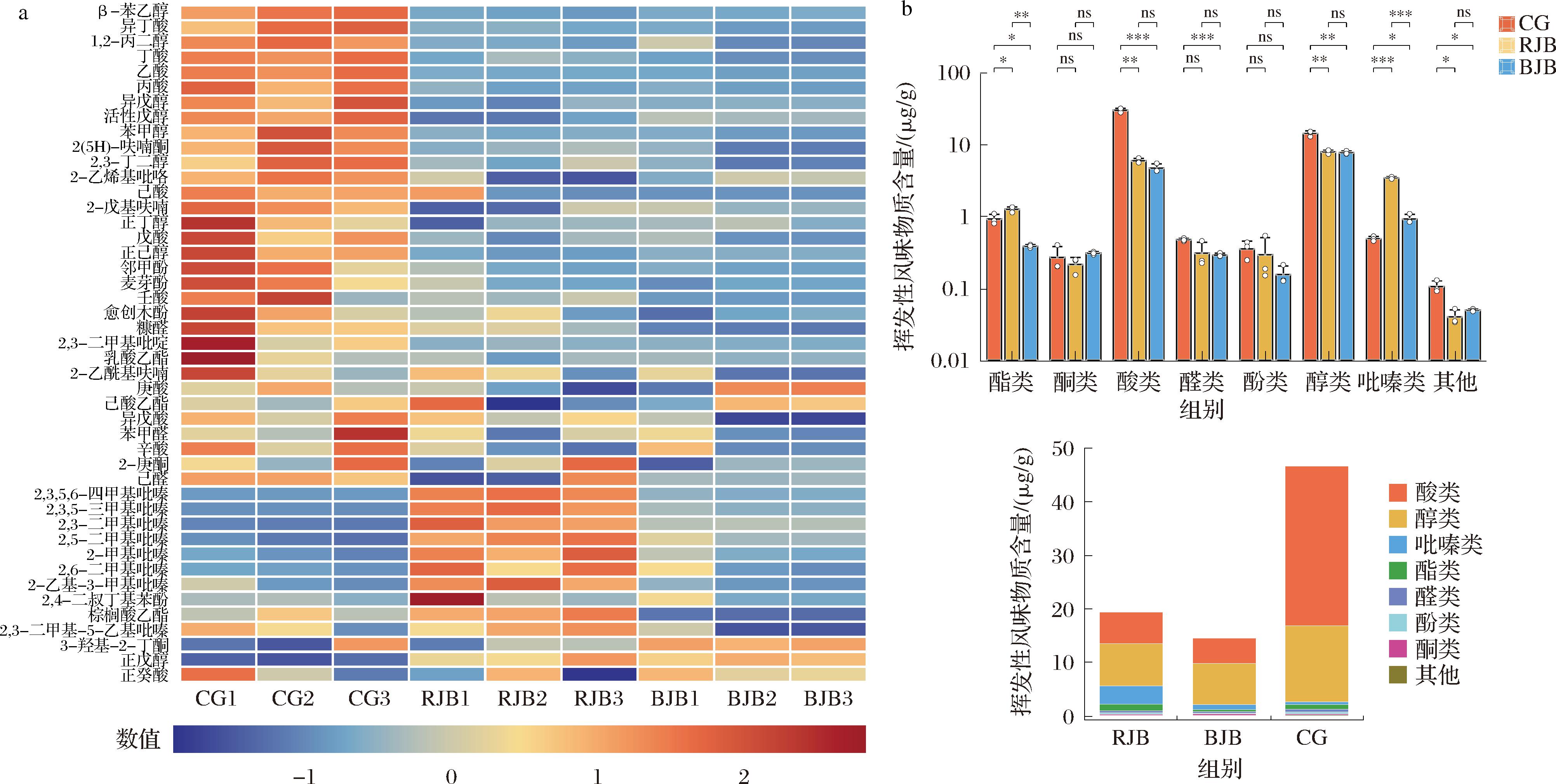
a-不同菌斑挥发性风味物质;b-风味物质种类含量差异
图5 中高温大曲断面特征菌斑挥发性风味物质组成
Fig.5 Composition of volatile flavor compounds in characteristic colonies from the cross-section of medium-high temperature Daqu
注:ns表示不显著;*表示P<0.05;**表示P<0.01;***表示P<0.001(下同)。
2.2 大曲断面特征菌斑挥发性风味物质
2.2.1 挥发性风味物质组成
如图5-a所示,共鉴定出45种挥发性化合物,包括酸类11种、吡嗪类8种、醇类9种、酚类4种、醛类3种、酮类3种、酯类3种、其他4种。如图5-b所示,CG中酸类、醇类化合物显著(P<0.05)高于RJB和BJB,醛类化合物显著(P<0.05)高于BJB;RJB中酯类、吡嗪类化合物显著(P<0.05)高于CG和BJB;酮类化合物在3组样品间无显著差异。已有研究表明,优质中高温曲醇类、酯类、酸类、醛酮类等化合物含量通常高于普通曲[16],本研究中CG酸类、醇类化合物总含量显著高于RJB和BJB,且酯类、醛类、酮类化合物含量亦相对较高,故推测断面色泽一致的CG区域其整体挥发性风味物质组成更符合优质曲特征。吡嗪是大曲中重要挥发性风味物质,赋予大曲烘焙、吐司和坚果等香气[17],RJB中吡嗪含量显著高于CG和BJB,说明大曲断面RJB区域能够提升大曲此类香气;BJB中挥发性风味物质总含量在3组样品中最低,说明大曲BJB区域香气呈现可能较弱。
2.2.2 挥发性风味物质差异
为进一步确定2种大曲挥发性物质差异,构建OPLS-DA模型,模型体现了2组样品在得分图中呈现显著分离趋势(R2Y=0.982,Q2Y=0.898),且模型未过拟合(置换检验结果Q2=-0.576)。基于VIP>1筛选出22种关键差异物质(图6),其中,吡嗪类化合物(2,3,5,6-四甲基吡嗪、2,3,5-三甲基吡嗪、2,3-二甲基吡嗪等)、棕榈酸乙酯与RJB落点距离较近,在RJB中相对含量较高,可视为RJB区别于CG和BJB的特征风味物质;正戊醇与BJB落点距离较近,在BJB中相对含量较高,为BJB的特征风味物质;β-苯乙醇、异丁酸、丁酸、乙酸、丙酸、活性戊醇、苯甲醇、2(5H)-呋喃酮、2,3-丁二醇、正己醇、糠醛、异戊酸与CG落点距离较近,在CG中相对含量较高,为CG特征风味物质。
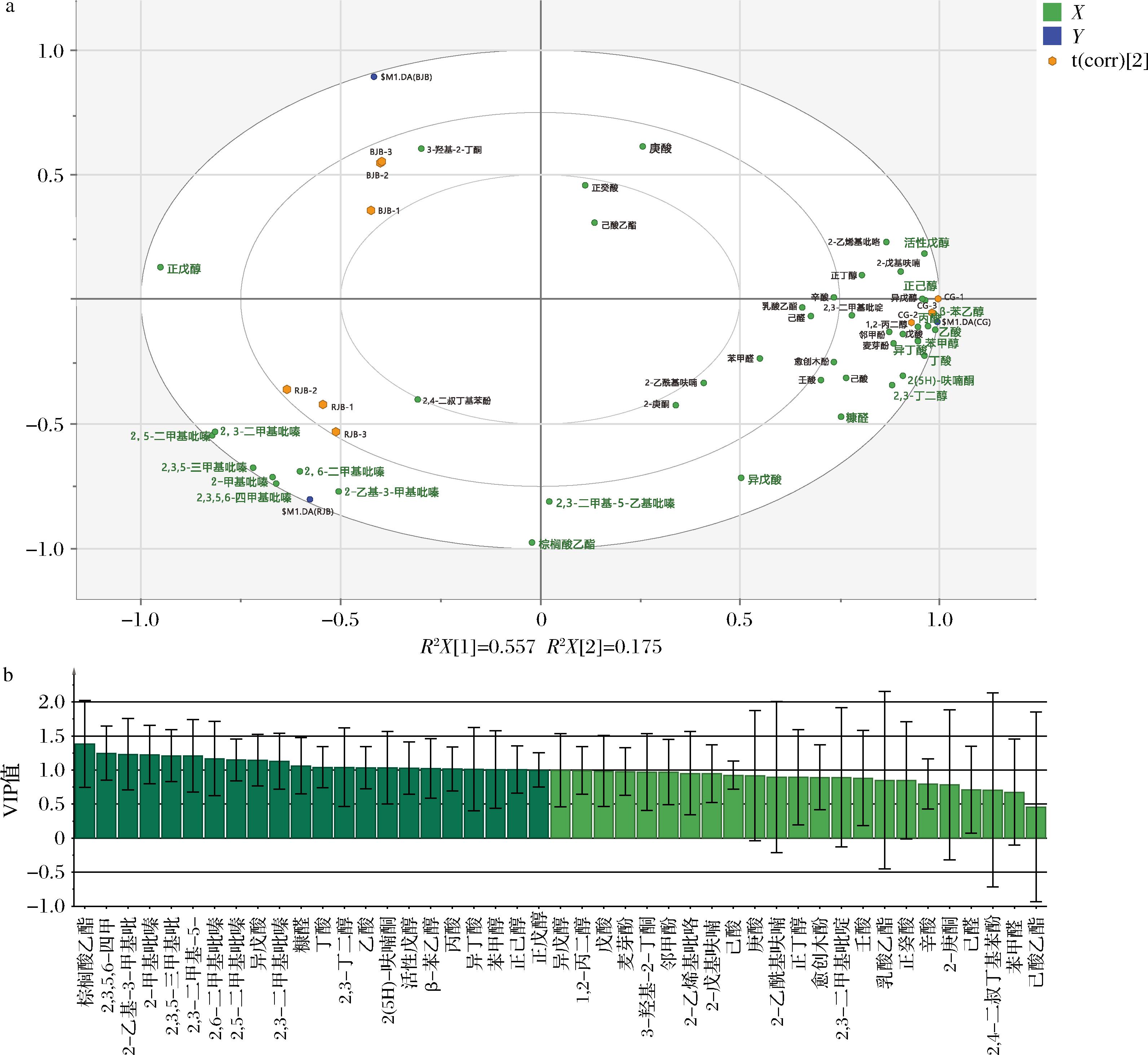
a-OPLS-DA得分图;b-变量重要性投影(variable importance in projection,VIP)值图
图6 挥发性风味物质差异
Fig.6 Differences in volatile flavor compounds
2.3 大曲断面特征菌斑差异微生物与挥发性风味物质相关性分析
为了解大曲中不同菌斑微生物与不同类别化合物之间的差异,采用冗余分析 (redundancy analysis,RDA)解析差异微生物与大曲不同类别化合物的相关性。如图7-a所示,RJB中吡嗪类、酯类、酚类化合物与轻乳杆菌属(Levilactobacillus)、Unidentified mitochondria、Unidentified chloroplast、嗜热子囊菌属(Thermoascus)、假单胞菌属(Pseudomonas)、葡萄球菌属(Staphylococcus)、类芽孢杆菌属(Paenibacillus)、寡养单胞菌属(Stenotrophomonas)、泛菌属(Pantoea)、不动杆菌属(Acinetobacter)呈正相关。BJB中链霉菌属(Streptomyces)、慢乳杆菌属(Lentilactobacillus)、粘液乳杆菌属(Limosilactobacillus)、嗜热真菌属(Thermomyces)与酮类化合物呈正相关。CG中芽孢杆菌属(Bacillus)、宽乳酸杆菌属(Latilactobacillus)、嗜热真菌属(Thermomyces)与酸类、醇类、醛类及其他化合物呈正相关。
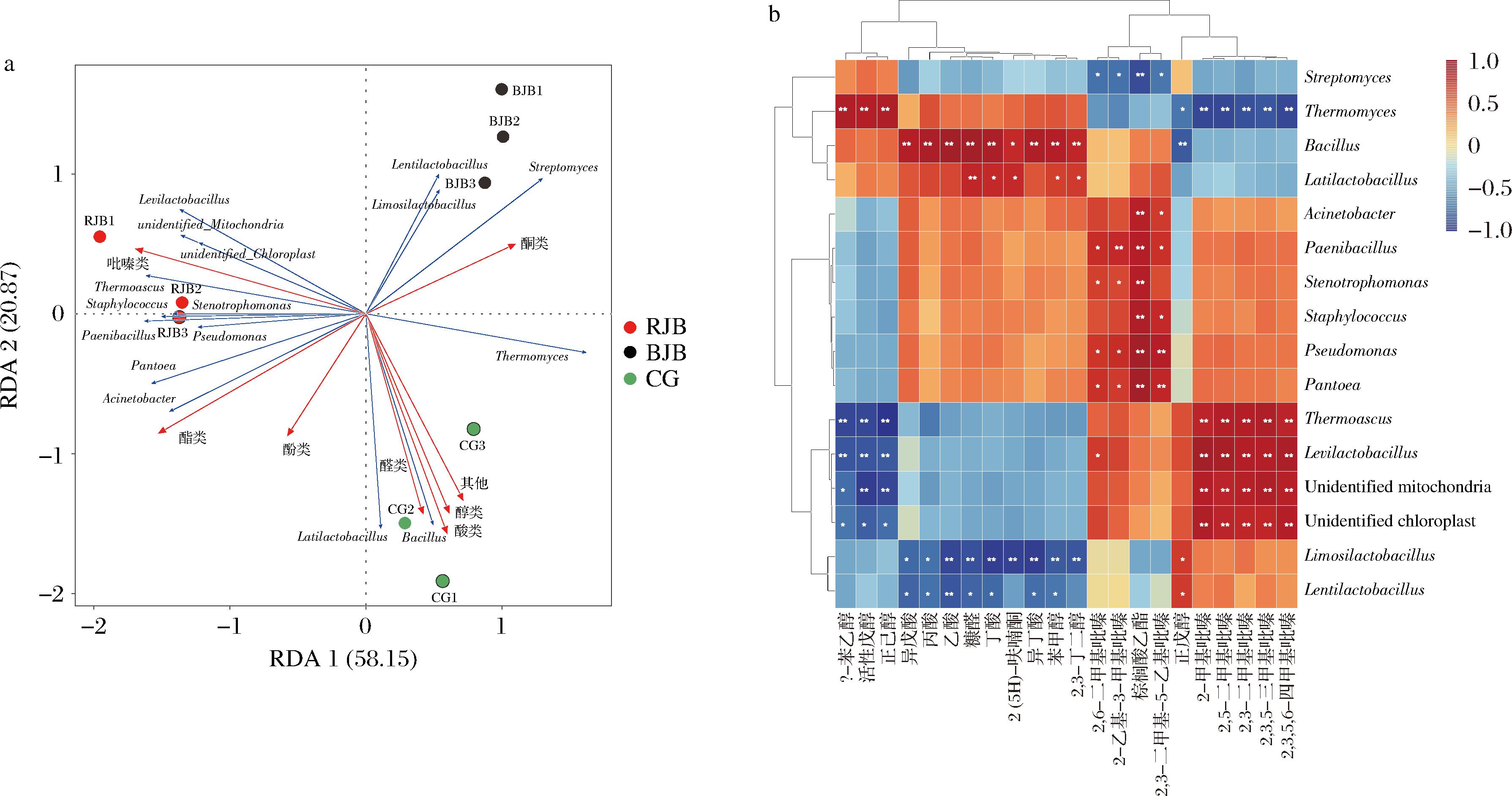
a-RDA图;b-相关性热图
图7 微生物与挥发性风味物质相关性分析
Fig.7 Correlation analysis between microorganisms and volatile flavor compounds
基于Spearman法进一步揭示差异微生物与特征风味物质的显著相关性,如图7-b所示,链霉菌属(Streptomyces)与2,6-二甲基吡嗪、2-乙基-3-甲基吡嗪、棕榈酸乙酯、2,3-二甲基-5-乙基吡嗪呈显著负相关;嗜热真菌属(Thermomyces)与β-苯乙醇、活性戊醇、正己醇呈显著正相关,与2-甲基吡嗪、2,5-二甲基吡嗪、2,3-二甲基吡嗪、2,3,5-三甲基吡嗪、2,3,5,6-四甲基吡嗪呈显著负相关;芽孢杆菌属(Bacillus)与异戊酸、丙酸、乙酸、糠醛、丁酸、2(5H)-呋喃酮、异丁酸、苯甲醇、2,3-丁二醇呈显著正相关,与正戊醇呈显著负相关;类芽孢杆菌属(Paenibacillus)、假单胞菌属(Pseudomonas)、泛菌属(Pantoea)与2,6-二甲基吡嗪、2-乙基-3-甲基吡嗪、棕榈酸乙酯、2,3-二甲基-5-乙基吡嗪呈显著正相关;嗜热子囊菌属(Thermoascus)、明串珠菌属(Levilactobacillus)、Unidentified mitochondria、Unidentified chloroplast与2-甲基吡嗪、2,5-二甲基吡嗪、2,3-二甲基吡嗪、2,3,5-三甲基吡嗪、2,3,5,6-四甲基吡嗪呈显著正相关,与β-苯乙醇、活性戊醇、正己醇呈显著负相关;粘液乳杆菌属(Limosilactobacillus)、缓乳杆菌属(Lentilactobacillus)与正戊醇呈显著正相关,与异戊酸、丙酸、乙酸、糠醛、丁酸、2(5H)-呋喃酮、异丁酸、苯甲醇、2,3-丁二醇呈显著负相关。
3 结论与讨论
本研究通过对中高温大曲断面RJB、BJB和CG区域的微生物群落及挥发性风味物质进行系统分析,揭示了不同特征菌斑的微生物组成与风味特征之间的关联性。微生物群落方面,RJB以泛菌属(45.12%)、葡萄球菌属(20.24%)和嗜热子囊菌属(99.81%)为优势菌群,Thermoascus_aurantiacus可能与RJB颜色形成相关;BJB中高温放线菌属(72.95%)占主要优势,链霉菌属为主要差异细菌,可能与BJB颜色形成有关;CG中芽孢杆菌属(47.13%)为主要优势微生物。风味物质方面,RJB中酯类及吡嗪类化合物含量显著高于CG和BJB(P<0.05),吡嗪类化合物赋予RJB区域突出的烘焙、吐司和坚果香气;BJB中挥发性风味物质总含量在最低,表明其局部香气可能相对较弱;CG中, 酸类和醇类化合物总含量显著高于RJB和BJB(P<0.05),且其酯类、醛类及酮类化合物含量亦相对较高,结合优质中高温曲风味特征,表明断面色泽一致的CG整体风味相对较优。相关性分析结果表明,RJB中泛菌属、葡萄球菌属、嗜热子囊菌等微生物与吡嗪类、酯类、酚类化合物呈正相关;BJB中链霉菌属、慢乳杆菌属、粘液乳杆菌属、嗜热真菌属与酮类化合物呈正相关。CG中芽孢杆菌属、宽乳酸杆菌属、嗜热真菌属与酸类、醇类、醛类化合物呈正相关。本研究从微生物群落角度解析了大曲断面菌斑颜色差异的原因,为完善大曲质量评价体系提供了理论依据。
[1] 肖冬光. 白酒生产技术[M].北京:化学工业出版社, 2023.XIAO D G.Baijiu Production Technology[M].Beijing:Chemical Industry Press, 2023.
[2] 曹丹, 吕嘉枥, 楚京嬴, 等.3种凤香型大曲中心区域特性的多维度表征及其差异性和相关性分析[J].食品科学, 2024, 45(20):123-135.CAO D, LYU J L, CHU J Y, et al.Central regions of three types of Fengxiangxing Daqu:Multidimensional characterization and difference and correlation analysis[J].Food Science, 2024, 45(20):123-135.
[3] 余乾伟. 传统白酒酿造技术[M].第2版.北京:中国轻工业出版社, 2017.YU Q W.Traditional Baijiu Brewing Technology[M].2nd ed.Beijing:China Light Industry Press, 2017.
[4] 任海伟, 李云帆, 阿丽米热·克热穆, 等.不同等级金徽酒大曲贮藏过程中的细菌群落演替规律和组装机制[J].食品科学, 2025, 46(10):108-119.REN H W, LI Y F, KEREMU A, et al.Succession and assembly mechanism of bacterial communities in different grades of Jinhui Baijiu Daqu during storage[J].Food Science, 2025, 46(10):108-119.
[5] WANG Z M, WANG C T, SHEN C H, et al.Microbiota stratification and succession of amylase-producing Bacillus in traditional Chinese Jiuqu (fermentation starters)[J].Journal of the Science of Food and Agriculture, 2020, 100(8):3544-3553.
[6] ZHENG X W, YAN Z, ROBERT NOUT M J, et al.Microbiota dynamics related to environmental conditions during the fermentative production of Fen-Daqu, a Chinese industrial fermentation starter[J].International Journal of Food Microbiology, 2014, 182:57-62.
[7] ZHENG X W, YAN Z, ROBERT NOUT M J, et al.Characterization of the microbial community in different types of Daqu samples as revealed by 16S rRNA and 26S rRNA gene clone libraries[J].World Journal of Microbiology and Biotechnology, 2015, 31(1):199-208.
[8] DENG L, MAO X, LIU D, et al.Comparative analysis of physicochemical properties and microbial composition in high-temperature Daqu with different colors[J].Frontiers in Microbiology, 2020, 11:588117.
[9] 王芙蓉. 酱香型大曲中高温放线菌的筛选及其产酶条件的优化[D].贵阳:贵州大学,2017.WANG F R.Screening of high temperature actinomycetes in Maotai Daqu and optimization of enzyme-producing conditions[D].Guiyang:Guizhou University, 2017.
[10] 赵佳宇,王玉荣,侯强川,等.高温和中高温大曲品质差异分析[J].中国酿造,2025,44(6):55-61.ZHAO J Y, WANG Y R, HOU Q C, et al.Analysis of quality differences between high-temperature and medium-high-temperature Daqu[J].China Brewing, 2025, 44(6):55-61.
[11] HOUBRAKEN J, KOCSUBÉ S, VISAGIE C M, et al.Classification of Aspergillus, Penicillium, Talaromyces and related genera (Eurotiales):An overview of families, genera, subgenera, sections, series and species[J].Studies in Mycology, 2020, 95:5-169.
[12] 唐艺婧, 来欢欢, 赵微, 等.红心曲来源Thermoascus aurantiacus QH-1的生长代谢特征[J].食品工业科技, 2023, 44(22):117-124.TANG Y J, LAI H H, ZHAO W, et al.Characteristics of growth and metabolism of Thermoascus aurantiacus QH-1 derived Hongxinqu[J].Science and Technology of Food Industry, 2023, 44(22):117-124.
[13] 杨阳, 牛曼思, 戴秋涟, 等.同一地区中温和高温大曲理化性质及真菌群落组成的比较研究[J].食品工业科技, 2023, 44(13):150-159.YANG Y, NIU M S, DAI Q L, et al.A comparative study on physicochemical indices and fungal community composition of medium-temperature and hightemperature Daqus from the same region[J].Science and Technology of Food Industry, 2023, 44(13):150-159.
[14] LOKHA Y, ARANA-PE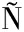 A S, RIOS N S, et al.Modulating the properties of the lipase from Thermomyces lanuginosus immobilized on octyl agarose beads by altering the immobilization conditions[J].Enzyme and Microbial Technology, 2020, 133:109461.
A S, RIOS N S, et al.Modulating the properties of the lipase from Thermomyces lanuginosus immobilized on octyl agarose beads by altering the immobilization conditions[J].Enzyme and Microbial Technology, 2020, 133:109461.
[15] SAKR A A, GHALY M F, EDWARDS H G M, et al.Involvement of Streptomyces in the deterioration of cultural heritage materials through biomineralization and bio-pigment production pathways:A review[J].Geomicrobiology Journal, 2020, 37(7):653-662.
[16] 孙亮霞, 王淑珍, 林一心, 等.不同等级中高温大曲理化性质、微生物群落结构及挥发性风味物质的研究[J].食品与发酵工业, 2025,51(24):284-290.SUN L X, WANG S Z, LIN Y X, et al.Research on physicochemical properties, microbial community structure and volatile flavour substances of different grades of medium and high temperature Daqu[J].Food and Fermentation Industries, 2025,51(24):284-290.
[17] 胡金喆, 韩业慧, 谌琦月, 等.基于多维度的大曲关键风味代谢菌群判定与调控应用研究[J].食品与发酵工业, 2025,52(1):366-375.HU J Z, HAN Y H, CHEN Q Y, et al.Identification and regulatory application of key flavor metabolism microorganismsof Daqu based on multi-dimension[J].Food and Fermentation Industries,2025,52(1):366-375.