酱油是赋予食物鲜味和良好风味的重要调味品,目前酱油大多采用高盐稀态发酵工艺酿造[1]。食盐摄入量过高会导致血压升高,增加发生脑溢血、心脏病等疾病的风险[2]。酱油发酵体系中高盐环境限制了部分产香酵母和有益乳酸菌的生长,使发酵食品的香气化合物均来自耐盐以及嗜盐微生物,导致整体产品风味较为单一[3]。因此,减少酱油中的盐含量对提升酱油风味有重要意义,但酱油的减盐发酵由于盐浓度降低常导致酱油中腐败微生物过度生长和风味失调等问题[4-5]。因此,研究在酱油发酵过程中抑制影响酱油发酵和风味的腐败菌生长的方法,对于实现酱油减盐发酵具有重要意义。
酱油发酵体系中富含营养物质,高浓度的盐能有效抑制微生物,特别是腐败细菌的快速增殖。升高或降低发酵温度、使用超声处理等方式可在一定程度上抑制大多数细菌的生长。但是,在酱油减盐发酵过程采用这些方法不仅抑制腐败菌的生长,也影响了有益或功能微生物的生长。因此,有效抑制腐败菌且不影响功能微生物发挥作用是实现酱油减盐发酵的重要前提。已有研究证实,在酱油减盐发酵过程中添加一种或多种功能菌株协同发酵能有效提高酱油的风味和抑制腐败微生物的生长[4]。例如,在低盐(盐质量浓度为80~ 140 g/L)酱油中接种毕赤酵母(Pichia guilliermondii)和德氏酵母(Torulaspora delbrueckii),可以有效抑制腐败微生物的生长,并生成更多的挥发性风味物质,与高盐酱油获得的风味特征模式相同[5]。另外,在减盐酱油(盐质量浓度为120 g/L)中接入鲁氏接合酵母(Zygosaccharomyces rouxii A22)、P.guilliermondii EM1Y52和嗜盐四芽球菌(Tetragenococcus halophilus TS71)进行协同发酵,可增加酱油中主要风味物质苯乙醇和愈创木酚等物质的含量,同时降低生物胺的含量,提升减盐酱油的品质[6]。同时,克氏库克菌(Kocuria kristinae)和Z. rouxii 协同发酵可显著增加3-甲硫基丙醛、乙酸乙酯和苯乙醛等多种关键风味物质的含量[7]。乳酸菌在酱油中种类多、占比大,可利用葡萄糖转化生成多种有机酸,是影响酱油发酵的重要微生物[8]。魏斯氏菌(Weissella)作为其中重要的乳酸菌之一,广泛应用于酱油、泡菜、豆豉等食品发酵中[9-10]。而类肠膜魏斯氏菌(Weissella paramesenteroides)作为酱油发酵过程中的优势细菌,不但能够产生酱油所需的风味物质,同时还能分泌肽酶和产生细菌素,抑制减盐酱油发酵过程中的部分腐败菌[11]。前期研究证实,利用W. paramesenteroides 和解淀粉芽孢杆菌(Bacillus amyloliquefaciens)进行协同发酵,成功实现了减盐酱油的发酵,并且能抑制腐败菌的生长,协调减盐酱油的微生物群落以及改善减盐酱油的品质和香气[12]。但目前对W. paramesenteroides 在发酵前期低温的条件下协同发酵减盐酱油,对减盐酱油中的微生物及品质影响尚不清楚。
本研究旨在筛选获得一株可耐受低温且可有效抑制酱油发酵腐败菌的功能乳酸菌,并探究W. paramesenteroides 与鲁式接合酵母协同发酵对减盐酱油品质与风味的影响,以期为进一步研究酱油减盐发酵机理与方法提供理论参考。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
本研究所用菌株均分离自高盐稀态酱油的酱醪,其 中 Bacillus megaterium、 Bacillus subtilis、 Bacillus halotolerans、腐生葡萄球菌(Staphylococcus saprophyticus)、Z. rouxii ZQ01和部分W. paramesenteroides 为本研究室保藏菌株(表1)。
表1 本研究所用菌株
Table 1 Microbial strains used in this work

注:“—”表示在文中无缩写名称。
1.1.2 培养基
MRS培养基(g/L):葡萄糖20.0,牛肉浸粉8.0,酵母浸粉4.0,蛋白胨10.0,磷酸氢二钾2.0,柠檬酸氢二铵2.0,吐温80 1.0 mL,乙酸钠5.0,硫酸镁0.2,硫酸锰0.04,pH值为6.5。在培养基中加入那他霉素10 mg/L、山梨酸1 000 mg/L得到MRS复配培养基。
LB培养基(g/L):蛋白胨10.0,酵母粉5.0,氯化钠10.0,pH值为7.4。在培养基中加入那他霉素10 mg/L得到LB复配培养基。
Z.rouxii 用YPD培养基(g/L):酵母粉10.0,蛋白胨20.0,葡萄糖20.0,氯化钠60.0,pH值调整为5.0。
1.1.3 试剂
氨基酸标样、有机酸和邻苯二甲醛(o-phthalaldehyde,OPA)(色谱纯),美国Agilent公司;高浓度甲醛(体积分数为37%)、3,5-二硝基水杨酸,国药集团化学试剂有限公司;氢氧化钠标准溶液、硝酸银标准溶液、仲辛醇(色谱纯),上海麦克林生化科技有限公司。
1.2 仪器与设备
LHP-100恒温恒湿培养箱,常州首创仪器设备公司;T100 DNA engine PCR,美国伯乐公司;HDPN-55恒温培养箱、YJY-206T恒温摇床,上海跃进医疗器械厂;TG-WAMS色谱柱(60 m × 250 μm × 0.25 μm,Thermo Fisher Scientific)、ODS HYPERSIL色谱柱(250 mm × 4.6 mm,2.5 μm),美国赛默飞公司;Aminex-HPX-87H色谱柱(300 mm ×7.8 mm,9 μm),美国伯乐公司;岛津20A,岛津企业管理有限公司;Agilent 1260高效液相色谱仪,美国安捷伦公司。
1.3 实验方法
1.3.1 菌株分离与鉴定
取酱醪样品(25 g)加入225 mL无菌生理盐水,混匀后取100 μL悬浮液梯度稀释并涂布于复配MRS培养基,在37 ℃下培养24 h。挑取单菌落划线分离纯化3次后用分离培养基培养至对数后期,然后保藏于-80 ℃。随后用上海生工生物公司细菌基因组提取试剂盒提取菌株的基因组DNA,并用16S rRNA通用引物27 F(5′-AGAGTTTGATCCTGGCTCAG-3′)和1492 R(5′-GGTTACCTTGTTACGACTT-3′)进 行PCR扩增。PCR产物送至天霖生物科技无锡有限公司测序,测序结果在NCBI进行BLAST比对。
1.3.2 酱醪微生物定量分析
取酱醪样品(25 g)加入225 mL无菌生理盐水,于37 ℃、220 r/min,振荡1 h,取100 μL梯度稀释液涂布于复配的MRS固体培养基及复配的LB固体培养基,培养后进行平板活菌计数[13]。其中W. paramesenteroides 在复配MRS培养基上37 ℃静置培养24 h;腐败菌(B. megaterium、B. halotolerans、B. subtilis和S.saprophyticus)在复配LB固体培养基上于37 ℃,220 r/min摇床中培养12 h;Z. rouxii 在含60 g/L NaCl的YPD培养基上于30 ℃,220 r/min摇床中培养48 h。
W.paramesenteroides 定量分析采用菌落PCR计数的方法:挑取平板上的全部单菌落至PCR管中,利用特异性引物WPF(5′-GCTCTGAAGTGATTTTATCTGAC-3′)和WPR(5′-AACCATGCGGTTGTTGGTA-3′)扩增。PCR体系为DNA模板0.5 μL(50 ng/μL),Taq 酶10 μL,上下游引物各0.5 μL(10 μmol/L),ddH2O 8.5 μL;扩增条件:94 ℃持续3 min,94 ℃持续30 s,58 ℃持续20 s,72 ℃持续1 min,12 ℃持续10 min。
1.3.3 理化指标测定
取5.0 g酱醪,加入45 mL生理盐水振荡30 min,于6 000 r/min离心5 min取上清液进行理化分析。总酸和氨基酸态氮采用滴定法测定[12]。
1.3.4 酱油发酵工艺
将蒸熟(121 ℃,30 min)的大豆与面粉混匀(质量比为3∶2),以原料总质量的1.5‰接种米曲霉(Aspergillus oryzae)沪酿3.042;在湿度95%、30 ℃培养48 h制得成曲。将成曲与160~200 g/L的盐水按1∶2质量比混合,使得酱醪中盐含量为120~180 g/L,然后在如表2所示条件下进行酱油发酵。
表2 酱油发酵工艺
Table 2 Procedures of soy sauce fermentation

1.3.5 非挥发性风味物质的测定
有机酸含量和氨基酸含量测定采用高效液相色谱法[13]。
有机酸的测定。液相系统:岛津20A,色谱柱:Aminex-HPX-87H(300 mm × 7.8 mm,9 μm);流动相:5 mmoL/L稀硫酸,进样体积10 μL,洗脱速度0.5 mL/min,洗脱时间30 min,柱温40 ℃,检测器UV210 nm。
游离氨基酸的测定。样品采用OPA进行柱前衍生。液相系统:安捷伦1260,色谱柱ODS HYPERSIL(250 mm ×4.6 mm,2.5 μm);流动相A相:无水乙酸钠5 g,四氢呋喃5 mL,三乙胺200 μL,超纯水1 L,冰醋酸调节pH值至7.2;流动相B相:无水乙酸钠5 g,超纯水200 mL,甲醇400 mL,乙腈400 mL,pH值调至7.2。进样体积10 μL,洗脱速度1 mL/min,洗脱时间45 min,柱温40 ℃,检测器UV338 nm。
1.3.6 挥发性风味物质的测定
挥发性风味物质采用固相微萃取联合气质联用技术(solid-phase micro extraction-gas chromatographymass spectrometry,SPME-GC-MS) 进行测定[14]。取5 mL酱油样品,50 ℃水浴30 min后,用萃取头吸附30 min,插入气相色谱进样口,240 ℃ 解吸15 min。气相色谱条件:进样口250 ℃,载气为高纯氦气,不分流进样;梯度升温程序为:45 ℃ 保持1 min,以每分钟3 ℃升至130 ℃,以每分钟6 ℃升至200 ℃,再以每分钟8 ℃升至230 ℃ 恒温10 min。质谱条件:电离源(EI),离子源温度为220 ℃,界面温度为250 ℃,离子源能量为70 eV,电子扫描范围为全扫描,通过NIST标准谱库对保留指数(retention index,RI)和相似指数(similarity index,SI)大于800的风味物质进行检索鉴定,以内标2-辛醇的峰面积对化合物进行半定量分析。
1.4 数据分析
采用SPSS 26和OriginPro软件进行数据分析和绘图,数据以“平均值±标准差”表示,以P <0.05表示数据之间的显著性差异,所有数据平行测定3次。
2 结果与分析
2.1 适合低温生长的W.paramesenteroides 菌株筛选
一般来说,低温(15~25 ℃)不是乳酸菌的最适生长温度,对其生长有一定的影响。为获得可在低温下生长良好的W. paramesenteroides 菌株,本研究首先从酱油发酵的酱醪中分离获得了7株W.paramesenteroides。通过比较这7株W. paramesenteroides 和课题组保藏的14株W. paramesenteroides 在低温下的生长情况发现(图1),温度对W. paramesenteroides 生长的影响较小,W. paramesenteroides JL-5在15 ℃和20 ℃的低温条件下生长优于其他菌株,活菌数达到9.5 ×109 CFU/g以上。因此,本研究选择W. paramesenteroides JL-5菌株进行后续研究。
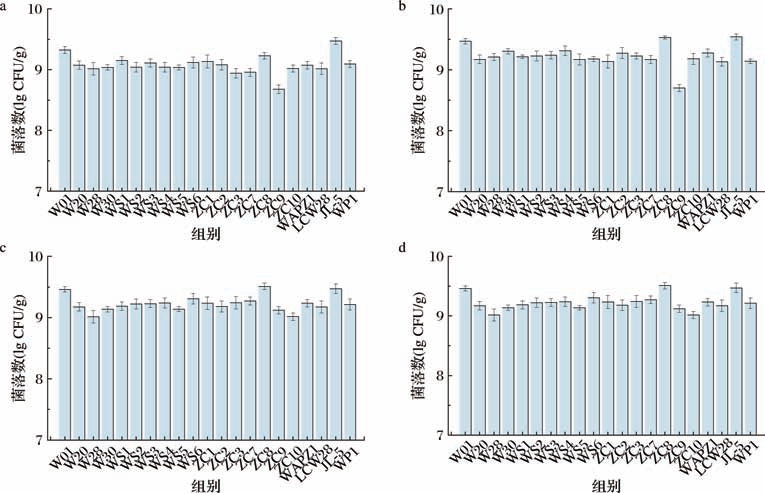
图1 温度对类肠膜魏斯氏菌生长的影响
Fig.1 Effect of temperature on growth of W.paramesenteroides
a-15 ℃;b-20 ℃;c-25 ℃;d-30 ℃
2.2 W. paramesenteroides JL-5对酱油减盐体系中腐败菌的抑制作用
为了研究W. paramesenteroides JL-5菌株对酱油发酵过程中腐败菌的抑制作用,考察了在不同培养温度下,酱油中主要腐败菌(Bacillus 和S. saprophyticus)[12]单独培养和与JL-5菌株共培养对腐败菌生长的影响。由图2可知,降低温度可有效抑制Bacillus(B.subtilis、B.halotolerans、B.megaterium)的生长。当温度低于30 ℃(15~20 ℃)时, Bacillus 的数量下降了3.3~4.3个数量级。但降低温度对S. saprophyticus 的抑制效果并不明显。当与W. paramesenteroides JL-5菌株共培养时,S. saprophyticus 的生长明显得到抑制,与S.saprophyticus 单独培养相比其菌落数下降了4.3~4.7个数量级。此外,与W. paramesenteroides JL-5共培养也可显著抑制Bacillus 的生长(P <0.05)。这些结果表明,W.paramesenteroides JL-5显示出在低温条件下抑制Bacillus 和S. saprophyticus 生长的能力。因此,酱油减盐发酵前期选择低温并添加W. paramesenteroides JL-5与Z.rouxii ZQ01进行协同发酵,有望对腐败菌进行有效减控,最终实现酱油减盐发酵。
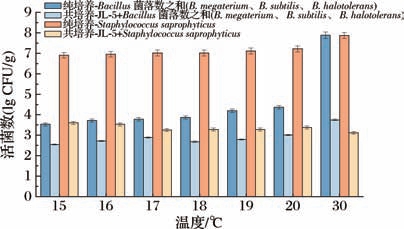
图2 不同培养温度下类肠膜魏斯氏菌JL-5对腐败菌生长的影响
Fig.2 Effect of W.paramesenteroides JL-5 on the growth of spoilage bacteria at different cultivation temperatures
2.3 W. paramesenteroides JL-5协同对酱油减盐发酵的影响
2.3.1 酱油发酵过程主要细菌的数量变化
为确定W. paramesenteroides JL-5菌株是否有助于酱油减盐发酵,首先研究了该菌株对协同发酵中主要细菌数量的影响。由图3-a可知,在30 ℃的减盐发酵体系中非乳酸菌细菌(腐败菌主体)数量明显上升,且稳定在108 CFU/g。虽然在发酵前期(0~15 d)降低温度可减少非乳酸菌细菌的数量,但发酵后期(15~45 d)非乳酸菌细菌数量迅速增加。采用W.paramesenteroides JL-5协同发酵可使酱醪中非乳酸菌细菌(腐败菌主体)的数量下降3.0~3.7个数量级;发酵第35天时,W. paramesenteroides JL-5协同发酵组酱醪中非乳酸细菌数量与高盐对照组(30 ℃,180 g/L NaCl,下同) 基本相同,但比减盐对照组(30 ℃,120 g/L NaCl,下同)低3.0~3.5个数量级。与减盐对照组和高盐对照组相比,W. paramesenteroides JL-5协同发酵组中乳酸菌数量较高,在0~30 d均可维持在107~108 CFU/g (图3-b)。这些结果表明,酱油减盐发酵会导致非乳酸菌细菌数量明显增加,发酵前期降低温度只在发酵前期对非乳酸菌细菌的抑制效果较为明显,而发酵前期降低温度的同时在发酵体系中加入W. paramesenteroides JL-5对非乳酸菌细菌的生长有良好的抑制作用,同时可增加酱油体系中以W.paramesenteroides JL-5为主的乳酸菌数量。
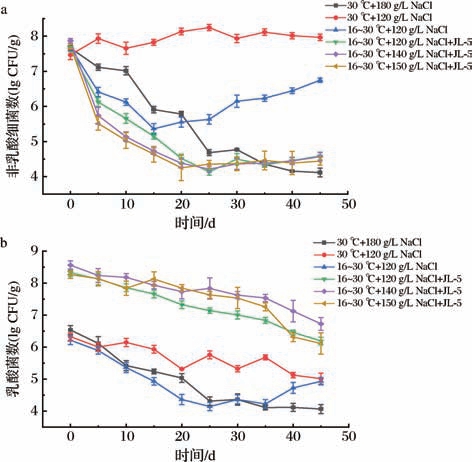
图3 酱油发酵过程中主要细菌的数量变化
Fig.3 Changes in main bacteria population during soy sauce fermentation
a-非乳酸细菌;b-乳酸菌
2.3.2 酱油发酵过程中理化指标变化
为了探究前低温处理且W.paramesenteroides JL-5与Z. rouxii ZQ01协同发酵对减盐酱油品质的影响,研究了减盐酱油的相关理化指标。由图4-a所示,添加W.paramesenteroides JL-5且盐质量浓度为140 g/L和150 g/L NaCl的发酵组的总酸含量与高盐对照组接近,均显著低于减盐对照组(P <0.05)。由图4-b可知,减盐发酵组酱醪中氨基酸态氮的含量均高于高盐对照;降低酱油发酵前期温度和添加W. paramesenteroides JL-5协同发酵组的氨基酸态氮含量变化更接近高盐对照组。其中,盐质量浓度为140 g/L并添加W.paramesenteroides JL-5的发酵组与高盐对照组氨基酸态氮含量变化最相似,发酵45 d时氨基酸态氮含量为1.10 g/100 mL。添加W.paramesenteroides JL-5的发酵组氨基酸态氮含量高于高盐对照组可能与耐盐乳酸菌分泌的寡肽酶增加游离氨基酸含量有关[15-16]。
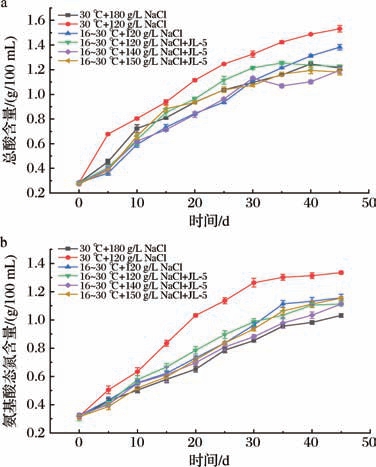
图4 酱油发酵过程中理化指标变化
Fig.4 Changes in physicochemical indexes during soy sauce fermentation
a-总酸;b-氨基酸态氮
2.3.3 酱油减盐发酵过程中非挥发性物质变化
为了探究前低温处理且W.paramesenteroides JL-5与Z. rouxii ZQ01协同发酵对减盐酱油非挥发性物质的影响,比较了减盐酱油中有机酸和氨基酸的含量。由图5-a可知,在前期低温处理且添加JL-5的发酵组有机酸含量显著高于高盐对照组(P <0.05),其中盐度140 g/L的发酵组有机酸总量最高为30.96 g/L,较高盐对照组提高了32.62%。其中乳酸、琥珀酸含量显著增加(P <0.05),乳酸是发酵后期参与酯类物质形成的重要有机酸之一,而琥珀酸能提升酱油的鲜味,改善酱油的品质[17]。酒石酸、苹果酸和乙酸含量在各发酵组中无明显差异。
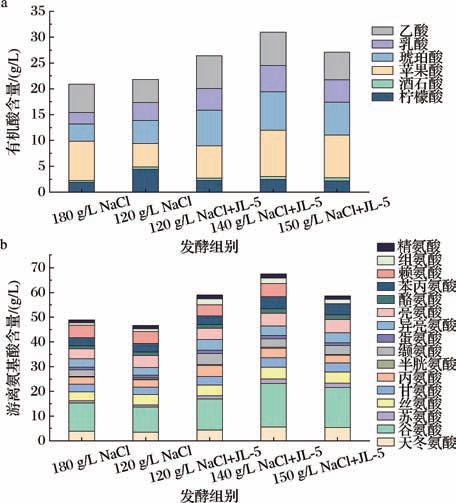
图5 酱油中非挥发物质含量的比较
Fig.5 Comparison of non-volatile substances in soy sauce
a-有机酸;b-游离氨基酸
游离氨基酸变化如图5-b所示,添加W. paramesenteroides JL-5且盐质量浓度为120 g/L时,鲜味氨基酸(天冬氨酸、谷氨酸)的含量与高盐对照组无显著差异。盐质量浓度为140 g/L和150 g/L时的发酵组的鲜味氨基酸含量显著增加(P <0.05),其中140 g/L盐质量浓度的发酵组鲜味氨基酸总量为23.17 g/L,较高盐对照组提高了33.75%,较低盐对照组提高了40.74%;盐质量浓度为140 g/L发酵组酱醪中甜味氨基酸(丝氨酸、丙氨酸、苏氨酸和甘氨酸)总量为14.31 g/L,较高盐对照组和低盐对照组均提高了27%左右。此外,添加W. paramesenteroides JL-5之后苦味氨基酸也有所增加,但盐质量浓度对苦味氨基酸的含量影响不显著。上述结果表明W. paramesenteroides JL-5与Z. rouxii ZQ01在协同发酵前期低温处理有助于有机酸和游离氨基酸的生成,且在盐质量浓度为140 g/L的条件下效果更为显著。
2.3.4 酱油中挥发性风味物质的比较
为了探究在发酵前期低温且添加W.paramesenteroides JL-5与Z. rouxii ZQ01在协同发酵过程中对减盐酱油中挥发性风味物质的影响,分析了不同发酵组酱油中的挥发性风味物质含量。从表3可以看出,减盐对照组中挥发性风味物质总量最低,而低温处理后添加JL-5协同发酵可显著增加挥发性风味物质总量(P <0.05)。其中,盐质量浓度为140 g/L的发酵组挥发性风味物质总量含量最高,相对总含量达到(440.89± 33.56) μg/L,比高盐对照组增加了44.60%。苯乙醇和异戊醇是酱油中主要的风味物质,它们不仅能为酱油提供酒香、花香等重要香气特征,还能抑制杂菌的生长[18]。添加W. paramesenteroides JL-5和Z. rouxii ZQ01且盐质量浓度为140 g/L的协同发酵组酱油中苯乙醇和异戊醇含量较高盐对照组分别提高99.18%和85.70%。此外,乳酸乙酯、棕榈酸乙酯和乙酸乙酯是酱油中重要的酯类物质,它通常能增加酱油的果香和甜香[19],盐质量浓度为140 g/L的W.paramesenteroides JL-5协同发酵组中这3种物质含量较高盐对照组分别提高了76.51%、47.77%和78.57%。低盐对照组中未检测到酚类物质,在盐质量浓度为140 g/L且添加W. paramesenteroides JL-5协同发酵组中,4-乙基愈创木酚和愈创木酚的含量比高盐对照组分别高89.19% 和90.75%,它们主要为酱油提供坚果香和烟熏香[20]。这些结果表明,酱油经前期低温处理后,加入W. paramesenteroides JL-5和Z. rouxii ZQ01进行协同发酵能增加挥发性风味物质的含量,在盐质量浓度为140 g/L时更有利于挥发性风味物质的生成。
表3 不同工艺酱油中挥发性风味物质相对含量的比较
Table 3 Comparison of the relative contents of volatile flavor compounds in soy sauce with different processes
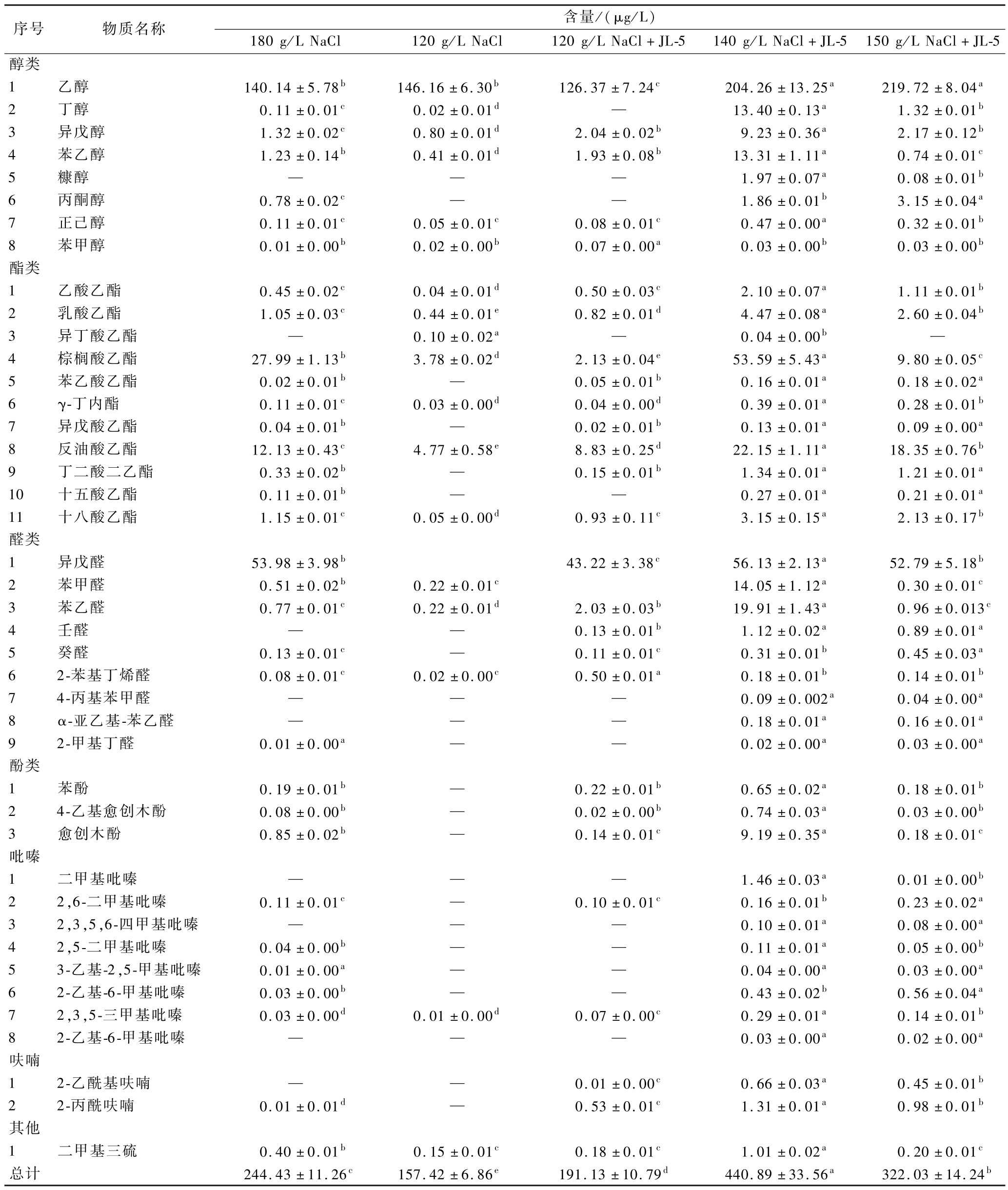
注:“—”表示未检出;不同字母表示同一物质在不同发酵组存在显著性差异(P <0.05)。
3 结论
传统酱油通常含有大量的盐分,过量食用会对人体健康产生不良影响,因此研究酱油的减盐发酵具有重要意义,但腐败菌增殖引起菌群失衡和发酵停滞是酱油减盐发酵较难实现的主要问题。在发酵过程中添加具有协同生长特性优势的发酵菌株是提高酱油的品质及微生物安全的有效手段之一。本研究通过分离筛选到一株W. paramesenteroides JL-5,在前期低温的条件下协同发酵减盐酱油,并探究其对减盐酱油品质的影响。研究结果显示,W.paramesenteroides JL-5菌株在低温条件下(15~25 ℃)生长良好且能显著抑制非乳酸细菌(主体腐败菌)的生长,同时能强化发酵体系中乳酸菌的数量。利用W. paramesenteroides JL-5进行协同发酵,总酸含量与高盐对照组无明显差异,而氨基酸态氮的含量显著提高,有机酸和游离氨基酸的含量在盐质量浓度为140 g/L时含量最高,分别为30.96 g/L和67.48 g/L。此外,140 g/L盐质量浓度的协同发酵组挥发物含量最高为(440.89±33.56) μg/L。同时,酱油的重要风味物质苯乙醇、异戊醇和愈创木酚较高盐对照组分别提高了99.18%、85.70%和90.75%。本研究筛选得到一株可耐受低温且可有效抑制酱油发酵腐败菌的功能乳酸菌W.paramesenteroides JL-5,前期低温处理同时利用W.paramesenteroides JL-5和Z. rouxii ZQ01进行协同发酵成功实现了减盐酱油的酿造,后续还可以深入探究W. paramesenteroides JL-5在减盐酱油中的抑菌机制和风味物质代谢途径。
[1]徐新玉,李心智,吴昌正,等.接种产酯酵母结合梯度升温工艺对低盐稀态发酵酱油的风味提升研究[J].食品与发酵工业,2025,51(12):149-157.XU X Y,LI X Z,WU C Z,et al.Inoculation with ester-producing yeast and combination of gradient heating process to improve flavor of low-salt liquid fermented soy sauce[J].Food and Fermentation Industries,2025,51(12):149-157.
[2]SUN C X,ZHOU X L,HU Z N,et al.Food and salt structure design for salt reducing[J].Innovative Food Science &Emerging Technologies,2021,67:102570.
[3]ELHALIS H,CHIN X H,CHOW Y.Soybean fermentation:Microbial ecology and starter culture technology[J].Critical Reviews in Food Science and Nutrition,2024,64(21):7648-7670.
[4]LIN X,TANG Y,HU Y,et al.Sodium reduction in traditional fermented foods:Challenges,strategies,and perspectives[J].Journal of Agricultural and Food Chemistry,2021,69(29):8065-8080.
[5]SONG Y R,JEONG D Y,BAIK S H.Effects of indigenous yeasts on physicochemical and microbial properties of Korean soy sauce prepared by low-salt fermentation[J].Food Microbiology,2015,51:171-178.
[6]SINGRACHA P,NIAMSIRI N,VISESSANGUAN W,et al.Application of lactic acid bacteria and yeasts as starter cultures for reduced-salt soy sauce (moromi) fermentation[J].LWT,2017,78:181-188.
[7]赵谋明,陈涛,王靖雯,等.酱油发酵过程中细菌的分离鉴定及其特性与交互作用[J].现代食品科技,2020,36(5):148-154;222.ZHAO M M,CHEN T,WANG J W,et al.Identification of bacteria during soy sauce fermentation and the study on their characteristics and interactions[J].Modern Food Science and Technology,2020,36(5):148-154;222.
[8]房峻,刘佳乐,彭玉慧,等.强化嗜盐四联球菌对模拟低盐酱油发酵的影响[J].中国酿造,2020,39(12):146-152.FANG J,LIU J L,PENG Y H,et al.Effect of enrichment of Tetragenococcus halophilus on simulated fermentation of low-salt soy sauce[J].China Brewing,2020,39(12):146-152.
[9]李巧玉,陈坚,曾伟主,等.酱醪中魏斯氏菌的分离及特性分析[J].微生物学通报,2018,45(11):2449-2462.LI Q Y,CHEN J,ZENG W Z,et al.Isolation and characterization of Weissella strains from soy sauce moromi mash[J].Microbiology China,2018,45(11):2449-2462.
[10]KOTW,NEVE H,HELLER K J,et al.Bacteriophages of Leuconostoc, Oenococcus,and Weissella[J].Frontiers in Microbiology,2014,5:186.
[11]李巧玉.魏斯氏菌在酱油发酵过程的含量变化及特性研究[D].无锡:江南大学,2018.LI Q Y.Detection of characteristics of Weissella strains and their contents in soy sauce moromi mash during soy sauce fermentation[D].Wuxi:Jiangnan University,2018.
[12]HU G Y,WANG Y J,CHEN J,et al.Synergistic fermentation with functional bacteria for production of salt-reduced soy sauce with enhanced aroma and saltiness[J].Food Bioscience,2024,57:103459.
[13]刘书亮,詹莉.纳他霉素与山梨酸复配改良MRS培养基的研究[J].中国酿造,2008,27(1):33-35.LIU S L,ZHAN L.Improvement of MRS medium by co-addition of natamycin and sorbic acid[J].China Brewing,2008,27(1):33-35.
[14]HARADA R,YUZUKI M,ITO K,et al.Microbe participation in aroma production during soy sauce fermentation[J].Journal of Bioscience and Bioengineering,2018,125(6):688-694.
[15]王涛,胡光耀,方芳.足球菌协同发酵对低盐固态酱油风味与品质的影响[J].食品与发酵工业,2023,49(15):77-84.WANG T,HU G Y,FANG F.Effect of synergetic fermentation with Pediococcus on the aroma and quality of low-salt solid-state soy sauce[J].Food and Fermentation Industries,2023,49(15):77-84.
[16]李秀娟,王夫杰,鲁绯,等.一株戊糖片球菌在低盐固态酱油工艺中的应用[J].食品科学,2011,32(9):251-256.LI X J,WANG F J,LU F,et al.Application of a Pediococcus pentosaceus strain in low-salt solid-state fermentation of soy sauce[J].Food Science,2011,32(9):251-256.
[17]于江,于贞.琥珀酸高产菌株ASQ-1酱油发酵性能的初步研究[J].中国调味品,2019,44(11):37-39.YU J,YU Z.Preliminary study on soy sauce fermentation performance of succinic acid-producing strain ASQ-1[J].China Condiment,2019,44(11):37-39.
[18]ZHANG W W,HAN Y Q,SHI K X,et al.Effect of different sulfurcontaining compounds on the structure,sensory properties and antioxidant activities of Maillard reaction products obtained from Pleurotus citrinopileatus hydrolysates[J].Lwt,2022,171:114144.
[19]WANG Q F,CUI R R,LIU X L,et al.Examining the impact of Tetragenococcus halophilus, Zygosaccharomyces rouxii,and Starmerella etchellsii on the quality of soy sauce:A comprehensive review of microbial population dynamics in fermentation[J].Critical Reviews in Food Science and Nutrition,2024,64(29):10873-10884.
[20]冯云子,周婷,吴伟宇,等.酱油风味与功能性成分研究进展[J].食品科学技术学报,2021,39(4):14-28.FENG Y Z,ZHOU T,WU W Y,et al.Research progress on flavor and functional components of soy sauce[J].Journal of Food Science and Technology,2021,39(4):14-28.