副干酪乳酪杆菌(Lacticaseibacillus paracasei)作为重要的益生菌种,具有广泛益生特性,因其显著的免疫特性、抗氧化作用和抑菌作用等功效而备受关注[1]。近期研究发现,副干酪乳酪杆菌对黄曲霉毒素B1(aflatoxin B1,AFB1)展现出显著的降解能力,这一发现为其功能性质拓展了新的研究方向。研究表明,副干酪乳酪杆菌YS-816对花生粕中AFB1 的脱除率达54.08%,同时还能提高花生粕中的蛋白质和氨基酸含量[2];唐连群等[3]从36株乳酸菌中分离鉴定得到发酵乳杆菌BP-4~7等4种乳酸菌,这4种乳酸菌对AFB1降解上具有显著优势作用。本课题组前期已研究副干酪乳酪杆菌F50对AFB1 的去除能力,并优化了副干酪乳酪杆菌F50的高密度发酵工艺,显著提高了菌种密度以及对AFB1的清除率[4]。副干酪乳酪杆菌通常采用液体培养方式,但该方式存在运输和商业化应用不便的问题,严重限制了其实际应用效果。为促进其在医疗保健和生物防治领域的应用,需将菌种发酵液从实验室规模推向商业化生产。因此,如何实现菌液的高效利用与稳定贮存成为亟待解决的关键问题。目前,水凝胶、乳液和纳米涂层等技术可用于短期包埋菌液[5],但其长期稳定性有限。相比之下,微胶囊化技术被广泛认为是最具前景的保护手段之一。该技术不仅能提供长期稳定的贮存条件,还可包埋化合物等不稳定的活性成分,有效防止核心物质受温度、光照、氧气和水分等环境因素的影响。此外,微胶囊化技术还能实现活性成分的可控释放,进一步拓展其应用潜力。
微胶囊包埋技术主要包括喷雾干燥法、挤压法、凝聚法和静电液滴法等多种形式,各具特点。喷雾干燥法操作简便且适合大规模生产,但高温可能导致益生菌严重失活并且降低了其在最终产品中的活性[6]。相比之下,挤压法基于物理交联原理,在常温条件下通过层流挤压制备微胶囊,能有效规避高温和高速剪切力对菌体的损伤、并兼备设备简单和成本低廉的优势。研究显示,挤压法制备的副干酪乳酪杆菌微胶囊在冷冻干燥后,在4 ℃条件下贮存28 d,菌种存活率达58.97%;在模拟胃液中3 h的存活率为67.52%;在模拟肠液中45 min内可实现基本完全释放[7]。挤压法中冷冻干燥阶段冰晶的形成和渗透压的变化极易导致微胶囊内部形成疏松孔隙,可能加速芯材氧化或泄露,降低缓释效果,所以添加适当的冷冻保护剂成为关键。MORGAN等[8]介绍了多种物质可以作为冷冻干燥时的保护剂,例如脱脂乳固体、血清、海藻糖、甘油、甜菜碱等。ÜÇOK等[9]的研究中使用乳制品加工副产品酪蛋白,可以在冷冻干燥中对植物乳植杆菌进行保护并可以长期保存。ZHANG等[10]研究证明了添加保护剂在冷冻干燥时可以增强对益生菌的保护,在冷冻干燥后依然维持益生菌活性,并且30 d贮存期间内微胶囊活细胞没有密度上的明显变化。
基于此,本研究采用挤压法对具有AFB1 降解能力的副干酪乳酪杆菌进行微胶囊化包埋。并从壁材的选择及保护剂的选择上进行优化,通过扫描电镜、流变分析、粒径与电位分布表征、红外光谱以及差示扫描量热法阐明壁材组成对微胶囊微观结构的影响;此外,进一步探究了壁材成分刺激菌体产生生物膜的能力。
1 材料与方法
1.1 材料与试剂
副干酪乳酪杆菌F50(Lacticaseibacillus paracasei):由西南大学食品科学学院508实验室筛选与鉴定,并已经保藏在中国典型培养物保藏中心,保藏编号为CCTCC NO:M 20222039。
MRS液体培养基,北京奥博星生物技术有限责任公司;海藻酸钠、卡拉胶、无水氯化钙,上海麦克林生化科技有限公司;黄原胶,成都赛尔文思生物科技有限公司;低甲基果胶,新疆阜丰生物科技有限公司;海藻糖、麦芽糊精、乳糖,上海源叶生物科技有限公司。
1.2 仪器与设备
T6紫外可见分光光度计,北京普析通用仪器有限责任公司;85-2数显恒温磁力搅拌器,常州朗越仪器制造有限公司;t 10 basic s025手持式均质机,德国艾卡公司;B-395 BUCHI微胶囊造粒仪,步琦实验室设备贸易有限公司;SCIENTZ-30F/A冷冻干燥,宁波新芝冻干设备股份有限公司;Phenom Pro扫描电镜,荷兰赛默飞公司;Spectrum100傅立叶红外光谱、DSC4000差示扫描量热仪,珀金埃尔默公司;Nano ZS90纳米粒度及zeta电位分析仪,英国马尔文公司。
1.3 实验方法
1.3.1 副干酪乳酪杆菌F50菌悬液的制备
将驯化好的耐酸副干酪乳酪杆菌F50按0.3 g/L接种到MRS液体培养基中活化2次,采用本课题组的方法进行培养[4]并收集菌液,取45 mL(1.7 ×1010 CFU/mL)副干酪乳酪杆菌F50发酵液在4 ℃和5 500 × g 下离心8 min,弃去上清液培养液,保留菌泥沉淀,加入生理盐水(含8.5 g/L NaCl)洗涤,重复2次,重悬于5 mL生理盐水(1.53 ×1011 CFU/mL)摇匀待用。
1.3.2 微胶囊的制备
取15 mL制备好的副干酪乳酪杆菌F50菌悬液、10 mL 20 g/L海藻酸钠溶液及10 mL 10 g/L羧甲基纤维素钠溶液(作增稠稳定剂),置于无菌容器中,使用磁力搅拌器混匀至均质。用10 mL无菌注射器吸取混合溶液,固定于微胶囊造粒仪的进料架上(图1)。在无菌密封接料罐中加入10 g/L灭菌的CaCl2 溶液,并放入转子持续搅拌。采用同心圆喷嘴,调节推料速度,开启电磁场,使料液连续分散滴入CaCl2 固化液中。持续搅拌20 min,让Ca2+ 进入到微胶囊内部。接着放入灭菌MRS液体培养基中原位固化12 h。最终将微胶囊粒子倒入砂芯漏斗中,用去离子水润洗抽滤3遍,随后自然晾干。参照MGOMI等[11]的方法为长期稳定贮存,在-40 ℃冰箱预冻4 h后进行冷冻干燥12 h,真空压盖备用。
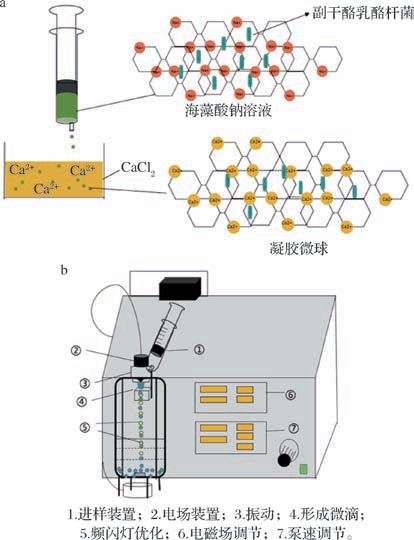
图1 微胶囊制备示意图
Fig.1 Schematic diagram of microcapsule preparation
a-凝胶微球原理图;b-微胶囊造粒仪制备微胶囊
1.3.3 微胶囊壁材选择
按照上述微胶囊制备方法,将海藻酸钠与低甲基果胶、卡拉胶、黄原胶进行复配,形成6种复配体系。二元复配:海-果、海-卡、海-黄(质量比为1 ∶1);三元复配:海-果-卡、海-果-黄、海-黄-卡(质量比为2∶1∶1),通过菌种包封率和冷冻干燥后的菌种存活率综合考察筛选壁材。
称取冷冻干燥后的微胶囊0.2 g,加入5 mL的30 g/L柠檬酸盐,稀释平板涂布并于37 ℃培养48 h,按照GB 4789.35—2023《食品安全国家标准 食品微生物学检验 乳酸菌检验》中的方法进行活菌计数,计算如公式(1)所示:
式中:X 为冻干存活率,%;A1 为冷冻干燥后的活菌数,CFU/g;A0 为冷冻干燥前的活菌数,CFU/g。
1.3.4 保护剂选择
分别以麦芽糊精、吐温80、脱脂乳、海藻糖、可溶性淀粉、乳糖、谷氨酸钠作为副干酪乳酪杆菌F50菌剂制备的保护剂,将其加入菌悬液充分混合,以菌种存活率为考察指标,再按1.3.2节等的方法制备微胶囊菌剂,筛选出合适的保护剂。
1.3.5 微胶囊壁材刺激生物膜产量的实验
生物膜对加强菌种的抗逆性起到关键作用,参照HE等[12]的方法,将2 mL 10 g/L低甲基果胶、卡拉胶、黄原胶加入到10 mL MRS液体培养基中,放入六孔板,接种副干酪乳酪杆菌F50培养18~20 h。转入96孔板检测,PBS洗涤3次,甲醇固定,结晶紫染色,再洗涤3次后,乙醇脱色并转入新的96孔板检测590 nm波长下的紫外吸光度值,用来表示生物膜的含量。
1.3.6 扫描电镜表征实验
使用扫描电镜,观察微胶囊粉末的表观形貌特点和粒径。放在黏在铝支架的双面碳带上,离子溅射喷金,在20 kV的加速电压下,扫描拍摄260倍数的显微照片[13]。
1.3.7 微胶囊复配壁材的流变分析
参考吴伟都等[14]的方法并稍作修改。将低甲基果胶、卡拉胶以及两者互相复配与海藻酸钠形成的微胶囊使用30 g/L柠檬酸三铵溶解后,选择直径为40 mm的平行板,在25 ℃下,剪切速率扫描范围在0.1~100 s-1下进行黏度曲线测试,观察黏度(mPa·s)与剪切速率(s-1)的关系。
1.3.8 粒径电位表征实验
称取0.2 g微胶囊,悬于5 mL蒸馏水中。将悬浮液在37 ℃的振荡器中孵育30 min,再使用激光粒度分析仪测定悬浮液的粒度分布和zeta电位[15]。
1.3.9 红外光谱实验
使用红外光谱仪确定固态副干酪乳酪杆菌F50菌剂内各种材料之间的交联效应。样品在4 000~400 cm-1 的波长进行了16次扫描。使用3 000~380 cm-1宽峰的高斯拟合来获得该范围内样品中各种类型氢键的比例和分布[16]。
1.3.10 差示扫描量热(differential scanning calorimetry,DSC)实验
按照KAMBLE等[17]概述的方法,将10 mg固态副干酪乳酪杆菌F50菌剂微胶囊置于铝盘中,加热速率为10 ℃/min。使用空铝盘作为参考,先从常温降到-30 ℃,再升温至60 ℃测定固态副干酪乳酪杆菌F50菌剂内各种材料的玻璃化转变以及熔融温度。
1.4 数据分析与处理
所有实验数据为3次实验平均值,结果取平均值。采用SPSS 27.0软件进行数据显著性分析处理,采用Origin 2021软件作图。
2 结果与分析
2.1 不同保护剂和包埋材料对固态副干酪乳酪杆菌F50菌剂活菌数的影响
由图2-a可知,黄原胶和海藻酸钠作为微胶囊壁材的包封率较高,但难以抵抗冷冻干燥的损失。冷冻干燥后,海藻酸钠单一壁材菌种存活率仅为2.73%,海藻酸钠、果胶和卡拉胶复配后菌种存活率最高,为12.12%。综上,在冷冻干燥保存时,选取海藻酸钠、果胶和卡拉胶作为壁材最佳。在此基础上,进一步筛选冻干保护剂。由图2-b可知采用7种包埋保护剂进行菌种存活率实验,其中添加保护剂脱脂乳、海藻糖、乳糖时,菌种存活率最高,分别为38%、35%、36.3%。因此可选取这3种保护剂为后续冷冻干燥中提供保护。脱脂乳可以在细菌细胞膜表面,形成保护性的包被层,减少冷冻干燥过程损伤,保护细胞结构[18]。海藻糖和乳糖中含有多个羟基,可以通过取代细胞膜中的磷酸基团或者菌体中的极性基团,形成氢键,保持细胞膜的结构完整[18]。
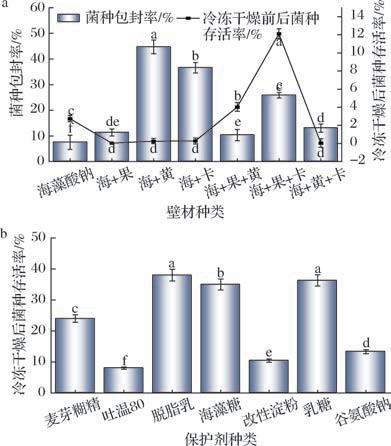
图2 不同包埋保护剂和壁材种类对活菌数的影响
Fig.2 Effects of different embedding protective agents and wall materials on bacterial density
注:不同小写字母表示差异显著(P <0.05)(下同)。
a-不同壁材种类;b-不同包埋保护剂
2.2 壁材刺激副干酪乳酪杆菌F50生物膜产生及含量
如图3所示,添加果胶组OD590 值(1.57)较对照组(0.253)显著提升了6.2倍,表明果胶有效促进副干酪乳酪杆菌F50生物膜形成。果胶中的特定组分可能通过激活生物膜形成相关基因,促进胞外多糖分泌,进而增强生物膜结构致密化[19]。基于此机制,研究采用果胶作为包封基质,结合海藻酸钠构建复合凝胶体系,利用离子交联技术制备微胶囊,并在MRS液体培养基中原位培养菌体。在此过程中,果胶不仅作为包埋材料提供物理屏障,还通过持续刺激菌体在微胶囊内部形成多层生物膜结构。这种原位生物膜强化策略有效提升了菌体对恶劣环境的耐受性,例如在模拟胃肠条件下,包埋菌体的存活率显著高于游离菌体,且能够在肠道环境中高效释放[19]。
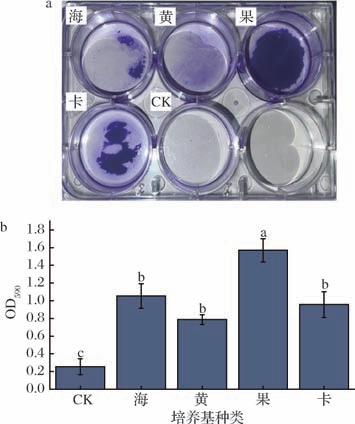
图3 不同胶体材料刺激培养菌种生物膜含量
Fig.3 The biofilm contents of cultured bacterial strains stimulated by different colloidal materials
a-培养20 h后照片;b-OD值
2.3 扫描电镜(scanning electron microscope,SEM)表征实验分析
如图4所示,在260倍放大倍数下观察发现,不同胶体壁材组合的微胶囊表面形貌及结构稳定性存在显著差异。单一海藻酸钠制备的微胶囊(图4-a)表面呈现明显凹陷和孔洞,结构松散且不均匀,表明其凝胶网络交联密度较低,难以抵抗干燥或温度变化导致的收缩开裂。相比之下,海藻酸钠与果胶复配体系(图4-c)通过Ca2+交联形成更紧密的凝胶网络,表面凹陷减少,但果胶的亲水性可能引入局部溶胀应力,导致干燥后仍残留微裂纹。而海藻酸钠与卡拉胶复配体系(图4-d)则表现出显著优势,微胶囊表面光滑致密,这得益于卡拉胶的硫酸酯基团与海藻酸钠羧基的静电相互作用形成的刚性双网络结构,其热可逆凝胶特性有效抑制了干燥收缩,提升了耐温性。图4-b进一步在三元复配体系(海藻酸钠+果胶+卡拉胶)中,微胶囊表面光滑均匀且无缺陷,综合性能最优。海藻酸钠提供基础凝胶骨架,果胶通过氢键增强网络韧性并优化缓释特性,卡拉胶则通过离子交联和疏水作用强化机械强度,三者协同形成多尺度分子互作网络[20]。该体系在抵御温度波动或机械应力方面展现出显著潜力,尤其适用于益生菌包埋或热敏性成分递送。

图4 SEM电镜扫描不同胶体壁材以及复配后的微胶囊表面(260 ×)
Fig.4 Different colloids and the surface of microcapsules after compounding by SEM (260 ×)
a-海藻酸钠;b-海藻酸钠+果胶+卡拉胶;c-海藻酸钠+果胶;d-海藻酸钠+卡拉胶
2.4 流变实验分析
流变学分析结果如图5所示,不同胶体材料的黏度随剪切速率的变化呈现显著差异。卡拉胶和海藻酸钠两者复配后的复合体系黏度最大。值得注意的是,复配体系表现出典型的剪切稀化现象,即黏度随剪切速率的增加而下降,复配体系的黏度高于纯卡拉胶,但其机械强度与包埋性能通过协同作用显著提升。卡拉胶的硫酸酯基团与海藻酸钠的羧酸基团通过静电相互作用形成双网络结构,增强了凝胶的刚性[21]。相比之下,低甲基果胶虽能刺激生物膜形成,但其黏度过低无法满足包封需求。卡拉胶的引入显著优化了复配体系的加工适用性。在挤压法制备微胶囊的工艺中,卡拉胶的引入使壁材体系在静置状态下有效包裹芯材,避免在输送至针头前发生壁材渗漏或芯材扩散;挤压过程中,针头处高剪切速率使黏度骤降,流动性增强;挤出后剪切力消失,黏度瞬时恢复,液滴迅速定型。这种协同作用在挤压法中对芯材的保护至关重要。
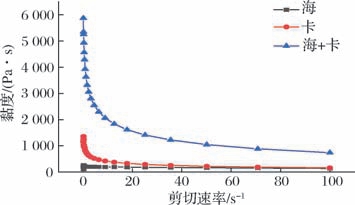
图5 不同胶体材料黏度随着剪切速率的变化
Fig.5 The variation of viscosity of different colloidal materials with shear rate
2.5 粒径以及电位实验分析
粒径、zeta电位及多分散指数(polydispersity index,PDI)分析结果如图6所示,海-果复配体系粒径分布区间最窄(459~1 990 nm),海-卡复配体系粒径分布最宽(825~2 670 nm)。海-果-卡复配体系(459~1 990 nm)较海藻酸钠单一体系(825~1 990 nm)集中在更窄的纳米区间。果胶加入后使海-卡组粒径分布进一步降低,表明果胶的引入通过其阴离子特性与卡拉胶的凝胶化能力产生协同效应,促进更小且均一颗粒的形成。同时,复配组的zeta电位绝对值接近-30 mV,显著高于海-果或海-卡单配组(如-20 mV以下),高表面负电荷通过静电排斥作用有效抑制颗粒聚集,从而提升胶体体系的物理稳定性[22]。此外,海-果-卡复配组的PDI(0.258)低于海-卡组(0.29),进一步验证了果胶的引入促进颗粒分布均匀。该体系的小粒径、高电荷稳定性及低PDI特性,使其在药物靶向递送、益生菌包埋等领域具备应用潜力,尤其在需长期贮存或抵抗环境胁迫的场景中可显著提升功能成分的生物利用度。
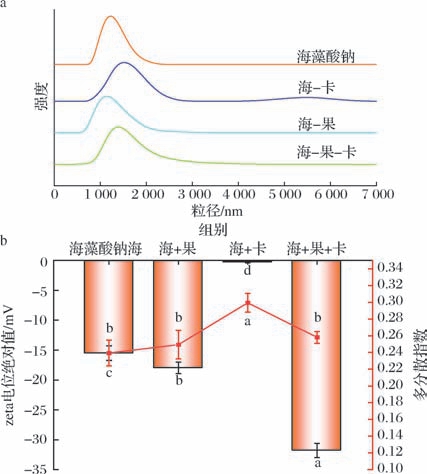
图6 不同胶体壁材微胶囊粒径分布、zeta电位与PDI
Fig.6 Particle size distribution,zeta potential,and PDI of microcapsules with different colloidal wall materials
a-粒径分布图;b-zeta电位及PDI图
2.6 红外光谱实验分析
红外光谱分析结果如图7所示,海-果-卡复配组在分子结构与相互作用上展现出显著优势。在3 400 cm-1处,复配组中羟基(—OH)伸缩振动峰强度较海-果组更高,表明果胶的羟基基团在复配体系中通过氢键与海藻酸钠、卡拉胶形成稳定的分子网络,有效保留其活性官能团。值得注意的是,在1 500~1 600 cm-1处,复配组的N—H伸缩振动峰强度显著高于海-果组,表明果胶中酰胺基团与卡拉胶的硫酸酯基团(—OSO3-)通过静电作用形成交联,增强了分子间相互作用。相较于海-果组在1 500 cm-1处出现的C—H振动特征峰,复配组在此区域的光谱呈现平滑过渡,暗示果胶的柔性链段与卡拉胶的刚性螺旋结构互补,形成均一的复合网络,而非简单物理混合。此外,复配组整体光谱基线平稳、峰形尖锐(如羟基与羰基峰半峰宽较窄),表明其分子排列有序,无相分离或聚集现象,与粒径、PDI实验中复配组更小粒径(纳米级)和更低多分散性(PDI <0.26)的结果一致。特别是光谱中未出现异常宽峰或杂峰(如1 600~1 650 cm-1 处的降解产物特征峰),证实复配过程未引发多糖降解或副反应,确保了材料的安全性[23]。
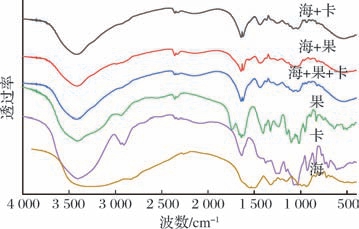
图7 不同包埋壁材红外光谱图
Fig.7 Infrared spectra of different embedding materials
2.7 DSC实验分析
DSC分析结果如图8所示,不同壁材微胶囊的热行为特征及其对菌种保护机制可解析如下,在低温区(-30~-10 ℃),海藻酸钠单独体系的DSC曲线在-24 ℃处呈现显著的吸热峰(向下峰)。当海藻酸钠与卡拉胶、果胶复配后,吸热峰温度向高温方向偏移至-19 ℃,分子链段运动受限程度增加。在高温区(-20~60 ℃),海-卡体系的DSC曲线显示其分子螺旋结构在高温下仍能维持稳定性,在高温环境胁迫下(如食品加工或贮存)为内部菌种提供物理保护[24]。此外,海-果-卡复配组的DSC曲线在高温区基线平稳,熔融峰形尖锐且无肩峰或杂峰,表明复配体系未发生相分离或组分聚集,分子网络均一性显著优于单一或二元体系。综上,复配体系实现了对菌种的双重保护机制,低温冷冻时减少冰晶损伤,高温环境下维持壁材完整性,为益生菌制剂在复杂加工及贮存条件下的活性保留提供了理论支持。
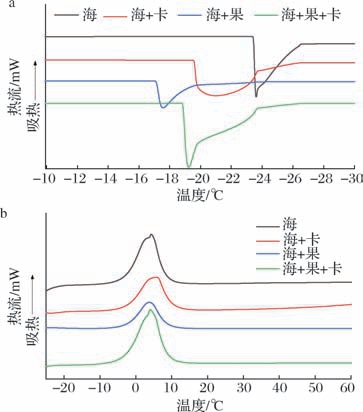
图8 不同壁材微胶囊差式扫描图
Fig.8 Microcapsule differential scanning of different wall materials
a-降温阶段;b-升温阶段
3 结论
本研究以海藻酸钠-果胶-卡拉胶三元复配体系作为壁材,添加脱脂乳、海藻糖和乳糖为保护剂,通过挤压法制备副干酪乳酪杆菌F50微胶囊,并针对该复配体系的生物膜产量、流变性质、表观形貌、粒径电位、分子结构和热稳定性进行研究分析。结果表明,三元壁材中,海藻酸钠提供凝胶骨架;果胶可以刺激生物膜形成;卡拉胶的引入赋予体系剪切稀化行为,三者复配构建稳定网络结构。SEM结果表明该复配体系表面光滑无缺陷。粒径以及电位分析可知该体系具有粒径小、电荷稳定性高和PDI低的特点。红外光谱进一步证明该体系形成了均一的复合网络结构。差示扫描热量结果显示复配体系低温冷冻时可以减少冰晶损伤,高温环境下可以保持壁材结构完整。综上,三元复配壁材以及保护剂的加入,显著提升了微胶囊抵抗冻干损伤的能力,为益生菌制剂工业化提供新策略。
[1]王一帆,薛云德,张宝平,等.副干酪乳杆菌的益生特性及其机制研究进展[J].食品研究与开发,2024,45(6):211-217.WANG Y F,XUE Y D,ZHANG B P,et al.Research progress on probiotic properties and mechanism of Lactobacillus paracasei[J].Food Research &Development,2024,45(6):211-217.
[2]袁芳,程玲,杨祥龙,等.副干酪乳杆菌YS-816的筛选及脱除花生粕中黄曲霉毒素B1 应用[J].现代食品科技,2025,41(4):316-325.YUAN F,CHENG L,YANG X L,et al.Screening of Lactobacillus paracasei YS-816 and its application in aflatoxin B1 detoxification from peanut meal[J].Modern Food Science &Technology,2025,41(4):316-325.
[3]唐连群,王茂全,陶学金,等.乳酸菌生物学特性及体外AFB1去除率的评价[J].中国饲料,2025(5):44-50.TANG L Q,WANG M Q,TAO X J,et al.Evaluation of biological characteristics and removal rate of AFB1 in vitro for forage derived lactic acid bacteria[J].China Feed,2025(5):44-50.
[4]张欣蕊,阳刚,李爱君,等.副干酪乳杆菌F50高密度发酵提升去除黄曲霉毒素能力及其非靶向代谢组学[J/OL].现代食品科技,2025.https://doi.org/10.13982/j.mfst.1673-9078.2026.1.1564.ZHANG X R,YANG G,LI A J,et al.High density fermentation of Lactobacillus paracasei F50 enhances the ability to remove aflatoxins and its non targeted metabolomics[J/OL].Modern Food Science &Technology,2025.https://doi.org/10.13982/j.mfst.1673-9078.2026.1.1564.
[5]BU W Y,MCCLEMENTS D J,ZHANG Z P,et al.Encapsulation method of probiotic embedded delivery system and its application in food[J].Food Hydrocolloids,2025,159:110625.
[6]ROKKA S,RANTAMÄKI P.Protecting probiotic bacteria by microencapsulation:Challenges for industrial applications[J].European Food Research and Technology,2010,231(1):1-12.
[7]邹盈,魏敏,谢琪,等.副干酪乳杆菌海藻酸钠微胶囊包埋工艺[J].食品与机械,2015,31(2):227-231.ZOU Y,WEI M,XIE Q,et al.Microencapsulation of Lactobacillus para casei with alignate[J].Food &Machinery,2015,31(2):227-231.
[8]MORGAN C A,HERMAN N,WHITE P A,et al.Preservation of micro-organisms by drying:A review[J].Journal of Microbiological Methods,2006,66(2):183-193.
[9]ÜÇOK G,SERT D.Trial productions of freeze-dried Lactobacillus plantarum culture using dairy by-products as cryoprotectants:Viability and characterization of cultures[J].Food Bioscience,2022,46:101541.
[10]ZHANG T,WANG C,SU S P,et al.Metal-phenolic networks enhanced the protection of excipients for probiotics during freeze-drying[J].Food Research International,2025,206:116097.
[11]MGOMI F C,YUAN L,FAROOQ R,et al.Survivability and characterization of the biofilm-like probiotic Pediococcus pentosaceus encapsulated in calcium alginate gel beads[J].Food Hydrocolloids,2024,156:110253.
[12]HE C A,SAMPERS I,VAN DE WALLE D,et al.Encapsulation of Lactobacillus in low-methoxyl pectin-based microcapsules stimulates biofilm formation:Enhanced resistances to heat shock and simulated gastrointestinal digestion[J].Journal of Agricultural and Food Chemistry,2021,69(22):6281-6290.
[13]RESENDE I F,MARTINS P M M,DE SOUZA MELO D,et al.Development and characterization of microencapsulated Pichia kluyveri CCMA 0615 with probiotic properties and its application in fermented beverages[J].International Journal of Food Microbiology,2025,427:110967.
[14]吴伟都,朱慧,王雅琼,等.质构仪及流变仪研究k-卡拉胶的凝胶特性[J].饮料工业,2016,19(1):10-13.WU W D,ZHU H,WANG Y Q,et al.Study on the gelling properties of k-carrageenan with textural analyzer and rheometer[J].Beverage Industry,2016,19(1):10-13.
[15]WANG X D,LYU W Q,ZHAI C Y,et al.Preparation and characterization of multilayered microcapsules of Lactobacillus rhamnosus encapsulated with sodium alginate,hyaluronic acid and carrageenan and their protective effects on the retina[J].International Journal of Biological Macromolecules,2025,305:141104.
[16]IPAR V S,SINGHAL R S,DEVARAJAN P V.An innovative approach using microencapsulated turmeric oleoresin to develop ready-to-use turmeric milk powder with enhanced oral bioavailability[J].Food Chemistry,2022,373(Pt A):131400.
[17]KAMBLE M,SINGH A,SINGH S V,et al.Effect of gastrointestinal resistant encapsulate matrix on spray dried microencapsulated Lacticaseibacillus rhamnosus GG powder and its characterization[J].Food Research International,2024,192:114804.
[18]刘开文,马雯,金刚.真空冷冻干燥提高乳酸菌存活率及延长贮藏期的研究进展[J].食品科学,2024,45(2):325-333.LIU K W,MA W,JIN G.Research progress on improving the survival rate and extending the storage period of lactic acid bacteria through vacuum freeze-drying[J].Food Science,2024,45(2):325-333.
[19]马蓝.干酪乳杆菌na-2胞外多糖抑制大肠杆菌O157:H7生物膜形成的机制研究[D].北京:中国农业科学院,2022.MA L.Study on the mechanism of exopolysaccharide from Lactobacillus casei NA-2 inhibiting the formation of biofilm in Escherichia coli O157[D].Beijing:Chinese Academy of Agricultural Sciences Thesis,2022.
[20]HUGHES M H,BRUGNONI L I,GENOVESE D B.Mixed κ/ιcarrageenan-LM pectin gels:Relating the rheological and mechanical properties with the capacity for probiotic encapsulation[J].International Journal of Biological Macromolecules,2024,273(Pt 1):133009.
[21]陈丽叶,许仁杰,林艳秋,等.海藻酸钠与κ-卡拉胶复配胶体的流变特性研究[J].现代食品,2022,28(10):191-196.CHEN L Y,XU R J,LIN Y Q,et al.Study on rheological properties of sodium alginate and κ-carrageenan complex gel[J].Modern Food,2022,28(10):191-196.
[22]ZHANG Z J,SUN W,WANG C,et al.Encapsulation of melatonin in zein/pectin composite nanoparticles:Fabrication,characterization,and in vitro release property[J].Food Chemistry,2025,465:142051.
[23]SAENGSUK N,LAOHAKUNJIT N,SANPORKHA P,et al.Comparative physicochemical characteristics and in vitro protein digestibility of alginate/calcium salt restructured pork steak hydrolyzed with bromelain and addition of various hydrocolloids (low acyl gellan,low methoxy pectin and κ-carrageenan)[J].Food Chemistry,2022,393:133315.
[24]GüNTER E A,MARTYNOV V V,ANANCHENKO B A,et al.The gel strength and swelling in the gastrointestinal environment of pectin/κ-carrageenan gel particles based on pectins with different degrees of methylesterification[J].Materials Today Communications,2022,33:104986.