肥胖是由能量摄入与消耗长期失衡诱发的慢性代谢性疾病,其发病机制复杂,涉及遗传、生理行为及环境因素的共同结果[1]。目前,在全球范围内肥胖问题愈发严峻,最新流行病学数据显示全球超重或肥胖成年人已达22亿,预计到2035年可上升至33亿,在我国超重和肥胖人群已逾3亿人,中国已成为全球肥胖人口最多的国家,且肥胖率仍在持续上升[2],肥胖问题已成为亟待解决的公共健康难题。在认知功能领域,肥胖的影响日益受到关注,临床神经影像学研究证实[3],肥胖患者的脑组织出现了灰质萎缩和白质纤维完整性受损等病理性变化,这些病理变化指向了肥胖对中枢神经系统功能的直接损害,是导致认知功能障碍的病理基础[4],因此改善肥胖已经成为防治认知障碍相关神经退行性疾病的重要举措。
肥胖诱导认知障碍主要归结于肥胖状态下全身低度炎症导致IL-1β、TNF-α 等促炎因子分泌增加,进而激活小胶质细胞引发神经炎症,干扰神经元正常功能;以及胰岛素抵抗导致大脑胰岛素信号通路受损影响神经元存活,造成突触可塑性受损[5]。上述认知障碍还会进一步诱导机体运动能力衰退,神经信号传导受到干扰会导致大脑对运动指令的处理速度和准确性下降,延长运动反应时间并降低运动协调性[6],而神经炎症会进一步损害神经信号传导,间接影响运动控制和协调能力,造成运动功能衰退[7]。值得注意的是,肠道微生物菌群和中枢神经系统之间的双向交流在肥胖认知障碍中发挥重要作用,研究发现肥胖能够通过“微生物-肠-脑”轴导致宿主肠道微生态失衡,增加条件致病菌(Enterobacteriales、Dubosiella[8]),减少有益菌(Faecalibaculum[9])的相对丰度,造成肠道通透性增加,使细菌代谢产物如内毒素脂多糖(lipopolysaccharide,LPS)经血液循环进入神经中枢,并通过激活Toll样受体4(toll-like receptors 4,TLR4)/核因子-κB(nuclear factor kappa B,NF-κB)信号通路诱发神经炎症,直接导致负责学习和记忆功能的海马区神经元受损[10];而TLR4/NF-κB炎症信号通路的持续活化会进一步激活核苷酸结合寡聚化结构域样受体蛋白3(NOD-like receptor family pyrin domain containing 3,NLRP3)/含半胱氨酸的天冬氨酸特异性蛋白酶-1(cysteine-dependent aspartate-specific protease1,Caspase-1)/Gasdermin D(GSDMD)信号通路,导致细胞焦亡发生,加剧认知功能障碍[11]。因此,恢复“微生物-肠-脑”轴正常功能有望成为肥胖相关认知障碍和运动能力衰退潜在的治疗靶点。
姜黄素(curcumin,CUR)是姜黄(Curcuma longa L.)根茎中结晶状多酚化合物(摩尔质量:368.39 g/mol)[12],可通过靶向多种信号通路,有效发挥抗炎、抗氧化、神经保护以及运动机能促进的药理学作用[13]。近些年,在认知障碍小鼠模型中发现CUR能够通过“微生物-肠-脑”轴减轻神经元损伤[14]。研究指出,低剂量[60 mg/(kg·d)]CUR通过增加短链脂肪酸(shortchain fatty acids,SCFAs) 的产生菌群(Turicimonas、Culturomica)相对丰度,有效降低丁酸/乙酸比值,并通过增强肠道屏障功能减少肠道通透性,避免LPS向神经中枢的过度分泌,削弱其介导的神经炎症信号通路表达[15];而中等剂量[100 mg/(kg·d)]CUR给药还能够显著增加有益菌(优杆菌科、里肯菌科等)的相对丰度、减少有害菌(Patescibacteria、肠杆菌科等)的相对丰度,并通过代谢产物重编程机制抑制神经炎症,减少α-突触核蛋白聚集,防治帕金森疾病(Parkinson’s disease,PD)进程[16]。而在阿尔兹海默症(Alzheimer’s disease,AD)模型中也发现,CUR(4 g/kg)干预能够增加肠道菌群α 多样性,富集有益菌群(振荡菌属、阿利斯特菌属等),减少条件致病菌(疣微菌门)的相对丰度,显著改善肠道屏障功能,减轻神经炎症反应。然而,上述研究主要围绕的是PD、AD等神经退行性疾病模型,对于肥胖相关认知障碍模型而言,CUR是否也能通过“微生物-肠-脑”轴产生疗效目前暂无报道,其抗炎作用是否进一步抑制细胞焦亡发生尚且不知。此外,新近研究指出CUR能够显著上调有益菌(木聚糖降解拟杆菌、戈尔德斯坦副拟杆菌)相对丰度,促进SCFAs水平增加,且两者的变化与小鼠力竭游泳时间和疲劳转棒时间呈显著正相关,提示CUR干预对宿主运动能力的提高与健康的肠道微生态有关。基于以上研究背景,本研究旨在探索CUR是否通过微生物-肠-脑轴调控NLRP3/Caspase-1/GSDMD通路抑制细胞焦亡发挥神经保护作用和运动能力提升作用,旨在为CUR干预防治肥胖相关认知障碍及运动能力衰退提供新的治疗思路。
1 材料与方法
1.1 材料与试剂
CUR,上海麦克林生化科技股份有限公司、甘油三酯(triglyceride,TG)、总胆固醇(total cholesterol,TC)、高密度脂蛋白(high-density lipoprotein cholesterol,HDL-C)、低密度脂蛋白(low density lipoprotein cholesterol,LDL-C)比色法检测试剂盒,南京建成生物;RIPA强裂解液、苯甲基磺酰氟蛋白酶抑制剂,碧云天生物技术有限公司;Gasdermin D(GSDMD)、IL-1β、Cleaved-Caspase1、NF-κB、紧密连接蛋白1(zonula Occludens-1,ZO-1)、兔源一抗,武汉三鹰生物技术有限公司。突触素(synaptophysin,SYP)、突触蛋白1(synapsin 1,SYN1)、NLRP3、β-actin、Tubulin兔源一抗和羊抗兔二抗,成都正能技术有限公司;TLR4抗体,湖南欧迈科博生物技术有限公司;BDNF抗体,Abcam;10%PAGE凝胶制备试剂盒、10% PAGE凝胶制备试剂盒、三色预染蛋白Mark,上海雅酶生物医药科技有限公司;LPS的酶联免疫吸附测定法(enzyme linked immunosorbent assay,ELISA)试剂盒,武汉伊莱瑞特生物科技股份有限公司。苏木精-伊红(hematoxylin and eosin,H&E)染色试剂盒,武汉赛维尔生物科技有限公司。
1.2 仪器与设备
ECO 48实时荧光定量聚合酶链式反应(polymerase chain reaction,PCR)仪,美国illumina公司;ZB-200小鼠疲劳转棒仪,成都泰盟软件有限公司;KT-213抓力测试仪,淮北鲲鹏软件有限公司;Y迷宫、新物体识别系统,北京天鸣宏远公司;Tissuelyer-24多样品组织研磨机,上海净信实业发展公司;PowerPac Basic电泳仪和转膜仪,Bio-Rad公司;Multiskan FC酶标仪、51029702超净工作台,赛默飞世尔科技公司;AG 5428高速离心机,Eppendorf公司;MiniChemi 420化学发光成像仪,北京赛智创业科技有限公司;RM 2126石蜡切片机,Leica公司;BX51显微镜,Olympus Corporation公司。
1.3 实验动物
8周龄SPF级雄性C57BL/6小鼠40只,购于湖南斯莱克景达实验动物有限公司,体重约为(17.73±0.59)g,实验动物使用许可编号:SCXK(湘)2019-0004。所有小鼠饲养于标准无病原体环境中,温度条件为(23±1) ℃,湿度条件为(55±5)%,光照条件为12 h光暗循环,饮食条件为自由摄食饮水,垫料每周更换2次。实验方案遵循动物研究“3R原则”,研究遵循的程序符合负责动物试验委员会(吉首大学)所制订的伦理学标准,并经吉首大学生物医学伦理委员会批准(审批号为JSDX-2024-0126)。
1.4 实验方法
1.4.1 肥胖认知障碍动物造模构建及干预方案
小鼠适应性喂养1周后,随机分为对照组(CON,n=12)和肥胖造模组(n=28),CON组以10% 脂肪供能的普通饲料喂养,而造模组以60% 脂肪供能的高脂饲料喂养,正常饲料即基础生长繁殖饲料,高脂饲料配方组成(质量分数):31.6% 猪油+25.8% 酪蛋白+16.1% 麦芽糊精+9.5% 蔗糖+6.5% 纤维素+6.5%混合矿物质+3.2%大豆油+0.4%L-胱氨酸+0.3%酒石酸氢胆碱+0.1%混合维生素;能量供应:60%脂肪+20%碳水化合物+20%蛋白质。持续12周喂养后,每组随机各取2只小鼠进行肝脏病理学检测,并结合肥胖指标(体重、血脂)评判模型造模结果,以体重增加不低于30%且血清TG水平显著高于CON组作为肥胖建模成功标准[17]。随后采用新物体识别(novel object recognition,NOR)和Y迷宫测试进一步筛选出患有认知功能障碍的小鼠,并剔除造模失败的小鼠。将上述造模成功小鼠(n=24)随机分为HFD组(n=12)和CUR组(n=12),CUR组以100 mg/kg[18]的剂量进行CUR灌胃,而其余组灌胃等体积生理盐水,1次/日。实验过程CUR组共排除1只因灌胃导致食道受损阻碍进食,导致状态不佳的小鼠。最终对照组保留10只,HFD组保留12只,CUR组保留11只用作后续实验分析。于实验干预结束后第21周进行认知及运动表现相关测试,不同测试之间间隔1 d以避免累积效应发生,完成所有测试后隔天进行组织取材,具体实验方案见图1。
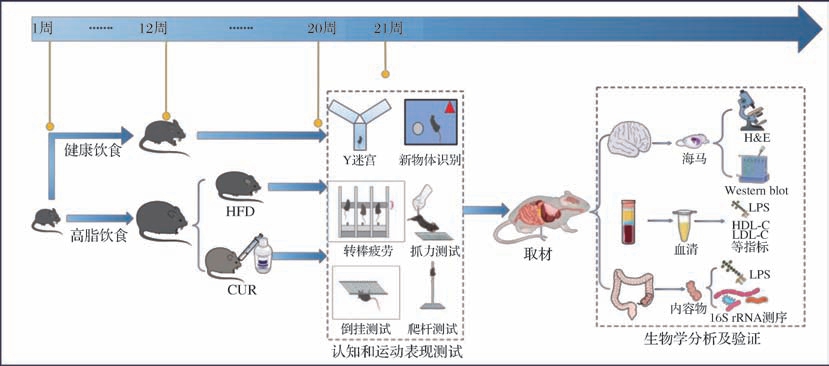
图1 实验流程图
Fig.1 The flowchart of experiment
1.4.2 认知行为学测试
第12周造模期间和第21周运动干预后进行Y迷宫和NOR认知行为学测试,评估各组小鼠认知功能的变化。采用Y迷宫测试检测各组小鼠空间记忆能力;Y型迷宫行为箱由3个的亚克力板(50 cm ×20 cm ×25 cm)组成,通道夹角为120°。实验前将3个臂分别随机定义为新异臂、起始臂和熟悉臂,然后进行2个阶段测试。第一阶段,关闭新异臂,从起始臂放入小鼠,使其自由探索10 min。第二阶段:将所有臂开放,再使小鼠自由探索5 min,并记录小鼠运动轨迹、各个臂探索时间和进入次数[19]。NOR实验可用于评价实验小鼠记忆能力的行为测试。实验包含3个阶段:适应阶段:小鼠置于实验箱自由探索10 min;训练阶段:在测试箱(A)中对角放置2个相同的物体,小鼠从2个物体中间放入,使其自由探索10 min;测试阶段:训练期结束后24 h,将其中1个物体替换为大小相似、颜色和形状易于区分的新物体(B),将小鼠从物体中间放入,使其自由探索5 min。采用Xeye Aba V3.2动物行为分析系统记录小鼠新旧物体探索次数,计算新物体识别指数,如公式(1)所示[20]:

1.4.3 运动表现测试
第21周采用转棒疲劳测试、倒挂测试、抓力测试、爬杆测试评价各组小鼠的运动能力。转棒疲劳测试用于评估小鼠的平衡能力、协调性和耐力,具体操作为将小鼠放置在旋转杆上,杆的转速从4 r/min逐渐增加到44 r/min,加速率为8 r/min,测试持续至小鼠从杆上掉落3次,记录其在杆上停留的平均时间,时间越长,表明小鼠的平衡能力、协调性和耐力越好[21];倒挂测试用于评估小鼠的抓握能力和肌肉力量,具体操作为将小鼠置于网格中心,随后翻转网格,测量小鼠从网格翻转至掉落的时间。悬挂时间越长,表明小鼠的抓握能力和肌肉力量越强[21];抓力测试用于评估小鼠前肢最大抓力,具体操作为将小鼠置于抓力计上,使其前肢抓住横杆,随后轻轻拉动小鼠身体,测量其前肢抓握时产生的最大拉力值。每个小鼠重复测量3次,测试间隔1 min,取平均值作为最终成绩;爬杆实验用于评估小鼠的运动协调性、肌肉力量和平衡能力。具体操作为将小鼠放置在竖直的爬杆底部,记录其从底部爬到顶部所需的时间。爬杆高度设定为50 cm,直径为1 cm,表面粗糙以提供足够的摩擦力。每个小鼠进行3次测试,取平均值作为最终结果[22]。
1.4.4 生化指标分析
认知行为学和运动表现测试结束后,将小鼠麻醉并进行眼球取血,血液常温静置2 h,离心(4 ℃,1 000 r/min,20 min)处理后取上层血清,采用ELISA试剂盒检测血清中LPS含量,采用微板法对血清中血脂指标(TG、TC、HDL-C、LDL-C)进行检测,检测试剂盒购自南京建成生物工程研究所。小鼠断颈处死后,使用无菌剪刀和镊子在盲肠的尖部进行横切,将盲肠内容物轻轻挤压至提前标记好的无菌冻存管中[23],采用ELISA试剂盒检测各组小鼠盲肠内容物中LPS含量。
1.4.5 组织H&E染色
小鼠取血后断颈处死,每组随机取3只小鼠,迅速分离出目标组织(肝脏、全脑和结肠),将分离出的组织分别置于4%(质量分数)多聚甲醛溶液中进行固定,随后进行石蜡包埋与切片处理。切片经二甲苯脱蜡、梯度酒精水化后,采用H&E染色法进行染色。染色完成后,将切片置于梯度乙醇溶液中进行脱水处理,并用中性树胶进行封片。对于结肠组织的H&E染色结果,进行如下组织学评分[24]:a)肠上皮细胞:形态正常,0分;杯状细胞丢失,1分;杯状细胞大面积丢失,2分;隐窝丢失,3分;隐窝大面积丢失,4分。b)炎症浸润:无炎症浸润,0分;浸润黏膜层,1分;浸润黏膜肌层,2分;广泛浸润黏膜肌层,并伴随黏膜肌层肿胀,3分;浸润黏膜下层,4分。
1.4.6 肠道微生物测序和生物信息学分析
小鼠经麻醉后采用颈椎脱臼法处死。使用无菌剪刀和镊子于盲肠尖部实施横切,确保切口平整且避免损伤内容物。将盲肠内容物轻柔挤压至预先标记的抗凝冻存管内。随后,利用QIAamp DNA Stool Mini试剂盒从盲肠内容物样本中提取总DNA,以338F (5′-ACTCCTACGGGAGGCAGCAG-3′) 和 806R(5′-GGACTACHVGGGTWTCTAAT-3′)[25]为引物扩增16S rRNA基因V3~ V4区。扩增产物经Illumina MiSeq PE300平台完成双端测序,测序服务由上海美吉生物医药科技有限公司提供。原始测序数据经QIIME 1.9.1软件进行预处理,以97%的序列相似度将序列聚类为操作分类单元(operational taxonomic units,OTUs),并利用RDP Classifier算法(置信度阈值设定为0.7)进行物种注释。基于Majorbio云平台开展生物信息学分析:α 多样性分析借助mothur 1.30.2软件计算多样性指数;β 多样性分析则采用Bray-Curtis距离矩阵进行主坐标分析(principal coordinates analysis,PCoA)和非度量多维尺度分析(non-metric multidimensional scaling,NMDS);组间差异菌群的筛选通过线性判别分析效应量(linear discriminant analysis effect size,LEfSe)分析完成,设定线性判别分析(linear discriminant analysis,LDA)值大于3且P <0.05为筛选条件,以鉴定从门到属水平的显著性差异分类单元。
1.4.7 Western blot检测
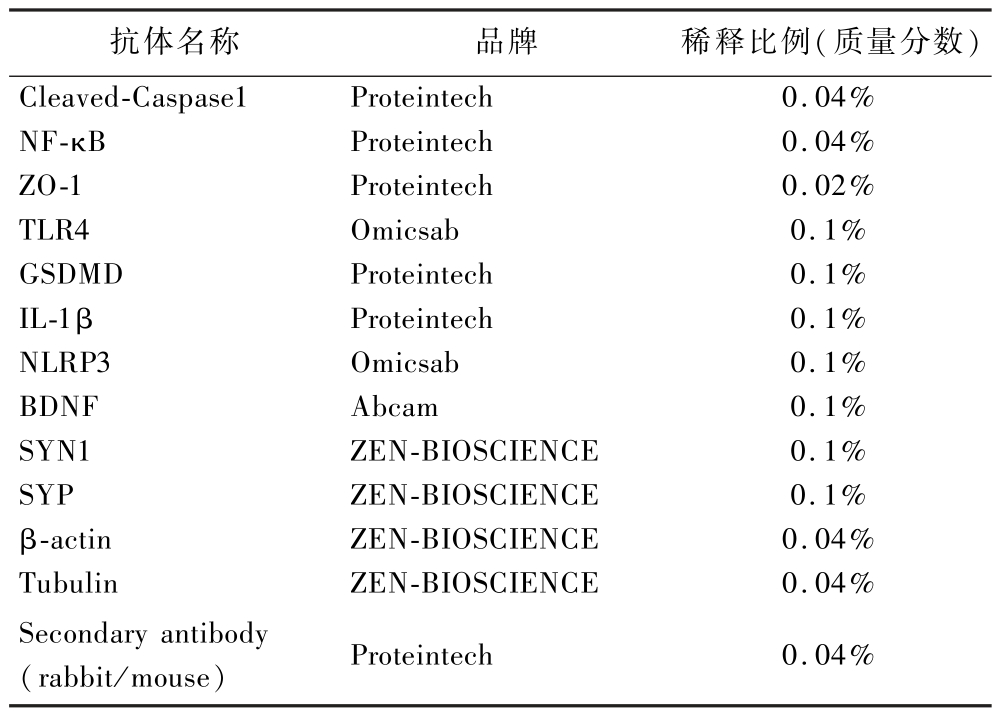
小鼠颈椎脱臼处死后,迅速分离两侧海马并置于-80 ℃冰箱保存。海马组织按每10 mg加入100 μL强裂解液,用多组织研磨机匀浆(60 Hz,1 min),4 ℃离心(10 000 r/min,10 min)取上清液。经BCA法蛋白定量后,加入SDS-PAGE蛋白上样缓冲液并100 ℃加热变性10 min。随后进行10% 分离胶电泳(浓缩胶80 V,20 min;分离胶100 V,70 min),湿转转膜(200 V,70 min)。室温下用5% 脱脂牛奶封闭1 h后,4 ℃孵育一抗过夜,TBST(Tris-buffered saline with Tween-20)洗膜3次(每次10 min)。加入二抗(山羊抗兔IgG,1∶5 000)室温孵育1 h,TBST洗膜3次(每次10 min)。滴加ECL(enhanced chemiluminescence)超敏显影液,化学发光成像仪曝光拍摄条带,ImageJ软件计算灰度值。抗体信息见表1。
表1 抗体基本信息
Table 1 Basic antibody information
1.4.8 实时荧光定量PCR
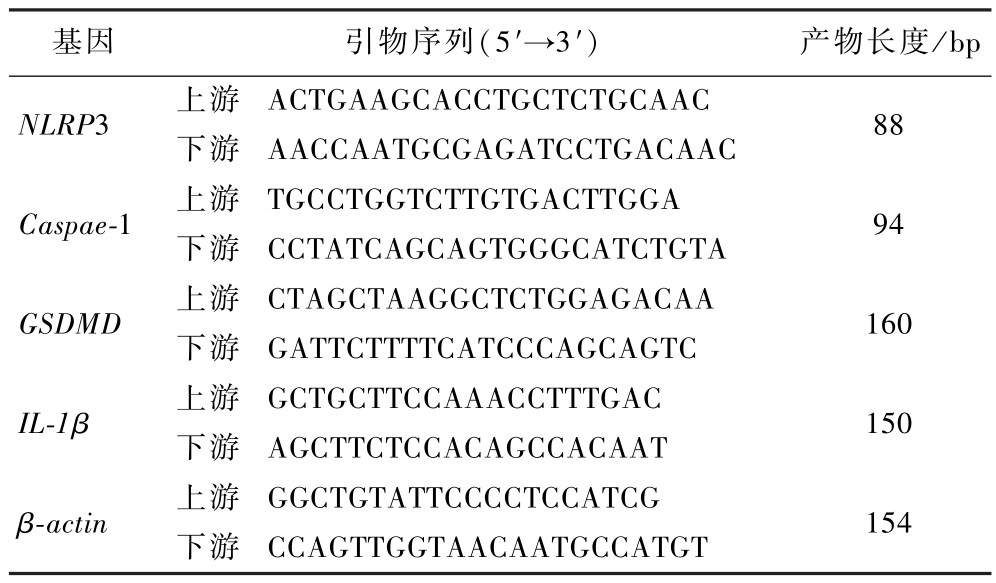
根据试剂盒说明书提取海马组织中的总mRNA,并将其反转录为cDNA。实时荧光定量PCR的反应条件如下:首先在95 ℃进行10 min的预变性;随后进行40个循环的三步法扩增,具体为95 ℃持续5 s、60 ℃持续20 s、72 ℃持续10 s;最后执行熔解曲线分析,程序为95 ℃持续15 s、55 ℃持续15 s、95 ℃持续15 s。通过测定得到的Ct值,采用2-ΔΔCt法计算细胞焦亡相关基因NLPR3、Caspae1、GSDMD和IL-1β 的mRNA表达水平,引物序列见表2。
表2 引物序列
Table 2 Basic antibody information
1.5 数据分析
实验结果所有数据以“平均值±标准差”表示,使用Image J,Graphpad Prism 8作图,采用SPSS 22.0对实验原始数据进行统计分析。数据进行方差齐性检验后,单变量分析部分,采用t 检验进行两两组间比较;多组间比较采用单因素方差分析(one way ANOVA)。P <0.05为显著性差异;P <0.01为极显著性差异。
2 结果与分析
2.1 12周高脂膳食诱导肥胖相关认知障碍小鼠模型的造模结果
研究结果显示(图2-a、图2-b),12周造模后,高脂饲养小鼠体重(P <0.05)、TG浓度(P <0.01)较对照组小鼠显著升高;图2-c结果显示,高脂膳食饲养的小鼠肝脏可见明显脂肪颗粒;综上,体重、血清TG指标和H&E染色结果表明,高脂饲养小鼠已形成高血脂和脂肪肝,即高脂膳食诱导肥胖小鼠模型造模成功。认知行为测试结果显示(图2-d、图2-e),造模组小鼠新物体识别指数(P <0.01)和新异臂探索时间占比(P <0.05)显著降低,说明造模组小鼠出现认知障碍。
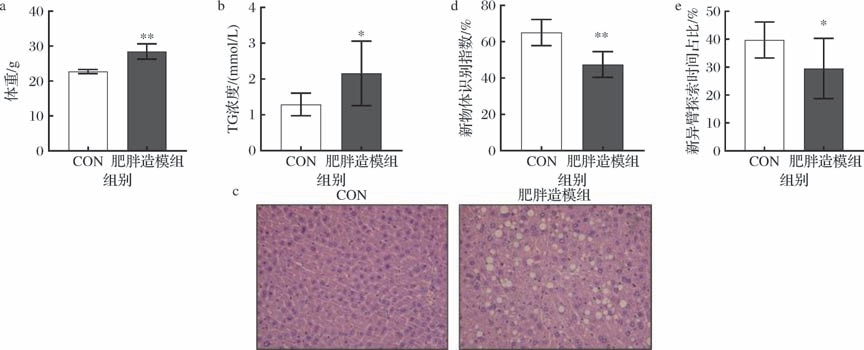
图2 高脂膳食诱导肥胖相关认知障碍模型的造模结果
Fig.2 Modeling results of high-fat diet induced obesity-related cognitive impairment model
注:∗代表显著性差异(P <0.05),∗∗代表极显著性差异(P <0.01)(下同)。
a-体重、b-TG;c-肝脏病理;d-新物体识别指数;e-新异臂探索时间占比
2.2 CUR干预对肥胖相关指标的影响
各组小鼠肥胖相关指标结果如图3所示,健康指数结果显示(图3-a~ 图3-d),与CON组相比,HFD组体重、肝指数、BMI和Lee’s指数显著增加(P <0.05);CUR组与HFD组相比,体重、肝指数、BMI和Lee’s指数显著减小(P <0.05)。血脂变化结果显示(图3-e~ 图3-h),与CON组相比,HFD组血清TG、TC、LDL-C浓度显著增加(P <0.01),HDL-C浓度显著降低(P <0.01);与HFD组相比,CUR组血清TG、TC、LDL-C浓度显著降低(P <0.05),HDL-C浓度显著增加(P <0.05)。
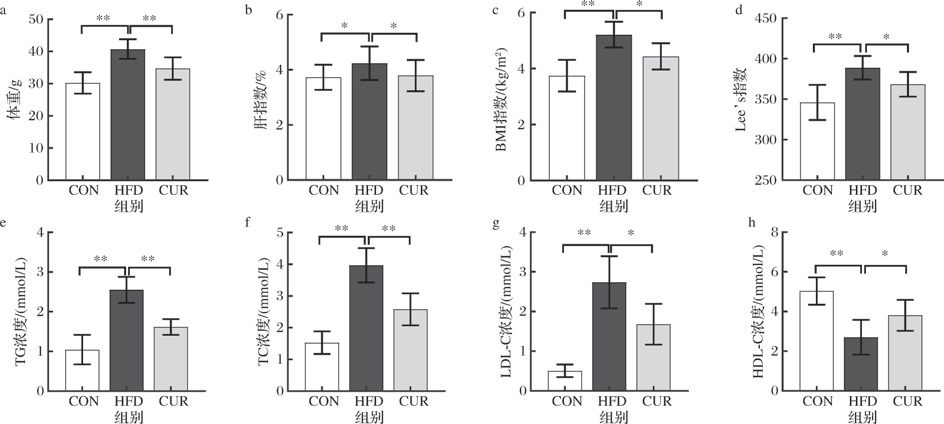
图3 CUR干预对肥胖相关指标的影响
Fig.3 Effect of CUR on obesity-related measures
a-体重;b-肝指数;c-BMI指数;d-Lee’s指数;e-TG;f-TC;g-LDL-C;h-HDL-C
2.3 CUR干预对认知行为和海马形态的影响
图4结果显示,与CON组相比,HFD组新异臂索时间占比显著降低(P <0.01)(图4-a、图4-b),新物体识别指数显著减少(P <0.01)(图4-c),同时,H&E染色结果显示,海马组织细胞结构排列松散(图4-d);与HFD组相比,CUR组新异臂探索时间占比显著增加(P <0.05),新物体识别指数显著升高(P <0.01),且海马细胞排列较为紧密,细胞数量明显增多。实验结果表明,8周CUR干预能够改善高脂膳食诱导的学习和记忆能力下降,并有效缓解肥胖相关认知障碍。
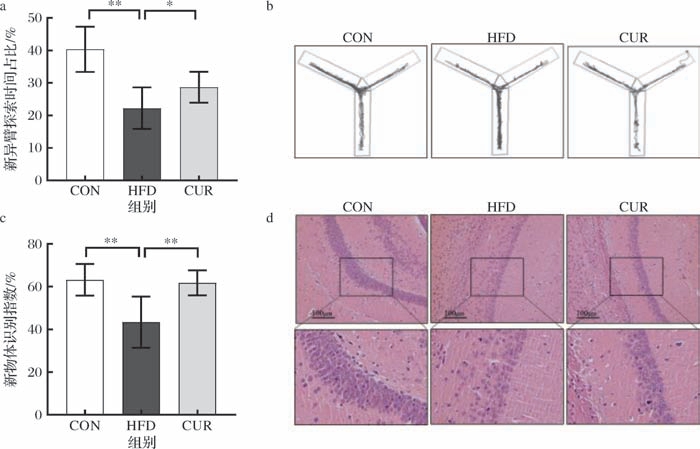
图4 CUR干预对认知行为和海马形态的影响
Fig.4 Effects of CUR intervention on cognitive behavior and hippocampal morphology
a-新异臂探索时间占比;b-Y迷宫轨迹图;c-新物体识别指数;d-海马组织H&E染色
2.4 CUR干预对运动表现的影响
爬杆实验结果表明,与CON组相比,HFD组爬杆实验完成时间显著延长(P <0.01);相较于HFD组,CUR组爬杆实验完成时间明显减少(P <0.05)(图5-a)。抓力和疲劳测试结果表明,与CON组相比,HFD组小鼠前肢抓力(P <0.05)、倒挂实验下落时间、转棒疲劳时间显著减少(P <0.01);与HFD组相比,CUR组小鼠前肢抓力无显著差异(P >0.05),CUR组小鼠倒挂实验下落时间、转棒疲劳时间显著延长(P <0.05)(图5-b~ 图5-d)。研究结果表明CUR干预可显著提高运动表现,缓解运动能力衰退。
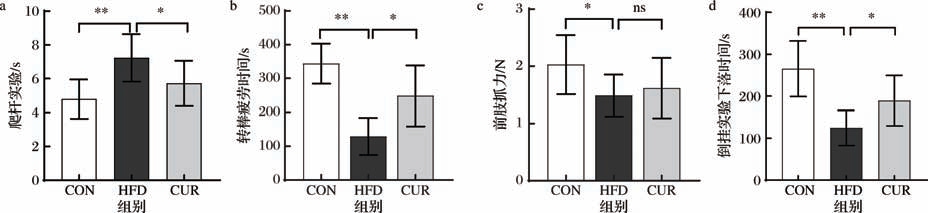
图5 CUR干预对运动表现的影响
Fig.5 Effect of CUR intervention on exercise performance
a-爬杆实验;b-转棒疲劳时间;c-前肢抓力;d-倒挂实验下落时间
2.5 CUR对肥胖小鼠肠道菌群的影响
2.5.1 CUR对肥胖小鼠肠道菌群α 多样性的影响
通过对盲肠内容物进行16S rRNA测序,以分析CUR干预对高脂膳食喂养小鼠肠道菌群结构和组成的影响。Venn图结果显示(图6-a),CON组,HFD组和CUR组分别包括548、139、207个OTUs,而3个组别共同包含364个OTUs。α 指数是评估肠道菌群物种多样性的有效指标,基于覆盖度(Coverage)指数(图6-b)及香农(Shannon)指数(图6-c)分析发现,随着物种数量增加,两指数的稀释曲线趋势均逐渐趋于平缓,表明本次菌群样本的群落丰富度、多样性及覆盖度良好,测序深度合理可靠,可充分反映小鼠盲肠内容物中绝大多数肠道微生物信息。对α 指数进行组间差异检验发现,Chao(P=0.014 8),Coverage(P=0.01)和Sob(P=0.02)和在3个组别中的差异具有统计学意义(图6-d~图6-f),且与CON组相比,HFD组Chao和Sob指标值均极显著降低(P <0.01),而Coverage指标值极显著增加(P <0.01),CUR组Coverage指标值也显著高于CON组。
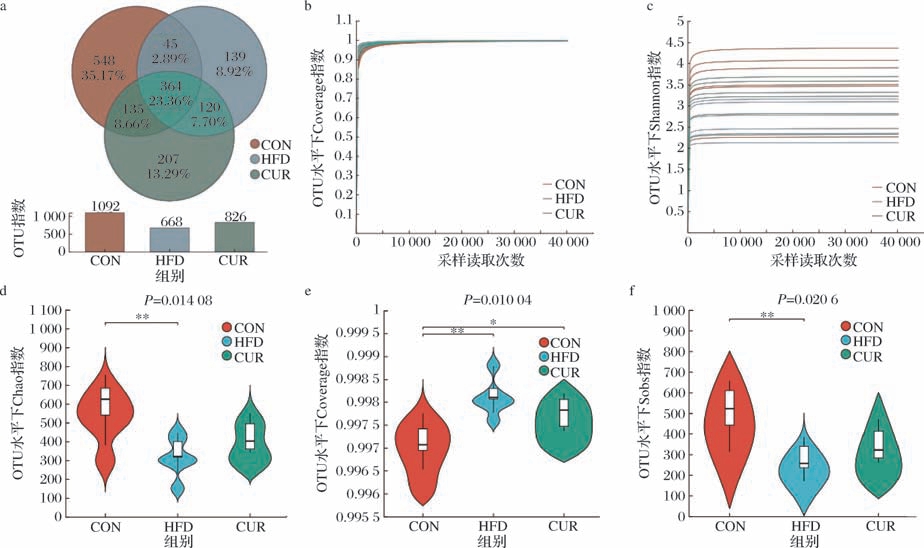
图6 CUR干预对肠道菌群α 多样性的影响
Fig.6 Effect of CUR intervention on alpha diversity of gut microbiota
a-Venn图;b-Coverage稀释曲线;c-Shannon稀释曲线;d-Chao组间差异;e-Coverage组间差异;f-Sobs组间差异
2.5.2 不同干预方式对肥胖小鼠肠道菌群β 多样性的影响
通过PCoA和NMDS分析各组肠道菌群β 多样性,评估组间肠道微生物群的组成的相似性和差异性。PCoA分析结果显示(图7-a~ 图7-c),在OTUs水平(R=0.644,P=0.001)和属水平(R=0.618,P=0.001)上,CON组与其他组别能够显著分离并独立成簇,而剩余2个组别样本相互聚集,无法彼此分离,在门水平上所有组别均无法分离(R=0.165,P=0.035);NMDS分析结果显示(图7-d~ 图7-f),在OTUs水平(R2=0.371,P=0.001)和属水平(R2=0.405,P=0.001)上,CON组也能够与其他组别显著分离并独立成簇,而剩余2个组别样本同样相互聚集无法分离,在门水平上所有组别均无法分离(R2=0.359,P=0.02),这说明CON组肠道菌群组成与其他组别之间存在显著差异,而HFD组和CUR组中的肠道菌群样本的多样性相似。
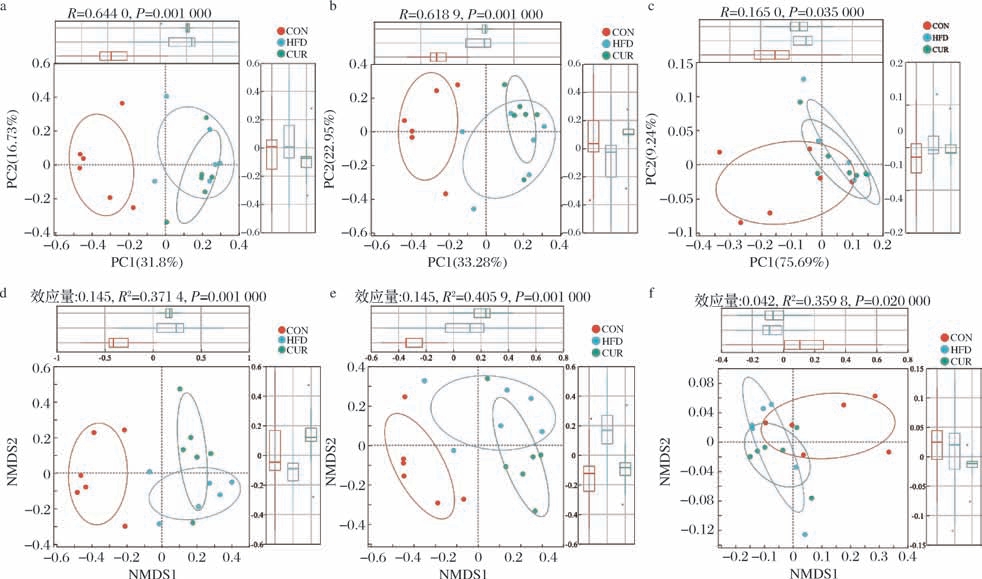
图7 CUR干预对肠道菌群β 多样性的影响
Fig.7 Effect of CUR intervention on beta diversity of gut microbiota
a-OTU水平PCoA分析;b-属水平PCoA分析;c-门水平PCoA分析;d-OTU水平NMDS分析;e-属水平NMDS分析;f-门水平NMDS分析
2.5.3 不同干预方式对肥胖小鼠肠道菌群组成的影响
门水平和属水平的肠道菌群群落分析结果显示,在门水平上,厚壁菌门、Desulfobacterota、拟杆菌门、放线菌门和变形菌门5个菌门在所有组别中最为丰富,为优势菌群(图8-a)。Firmicutes/Bacteroidota(F/B)比值在一定程度上可反映脂代谢紊乱程度[26],结果发现与CON组比,HFD组F/B比值极显著增加。而CUR组较HFD组显著降低(P <0.01)(图8-b),表明CUR干预能够改善肠道菌群稳态失衡。在属水平上,乳杆菌属、布劳氏菌属、Faecalibaculum、unclassified_f__Lachnospiraceae 等菌属在所有组别中为优势菌属(图8-c)。
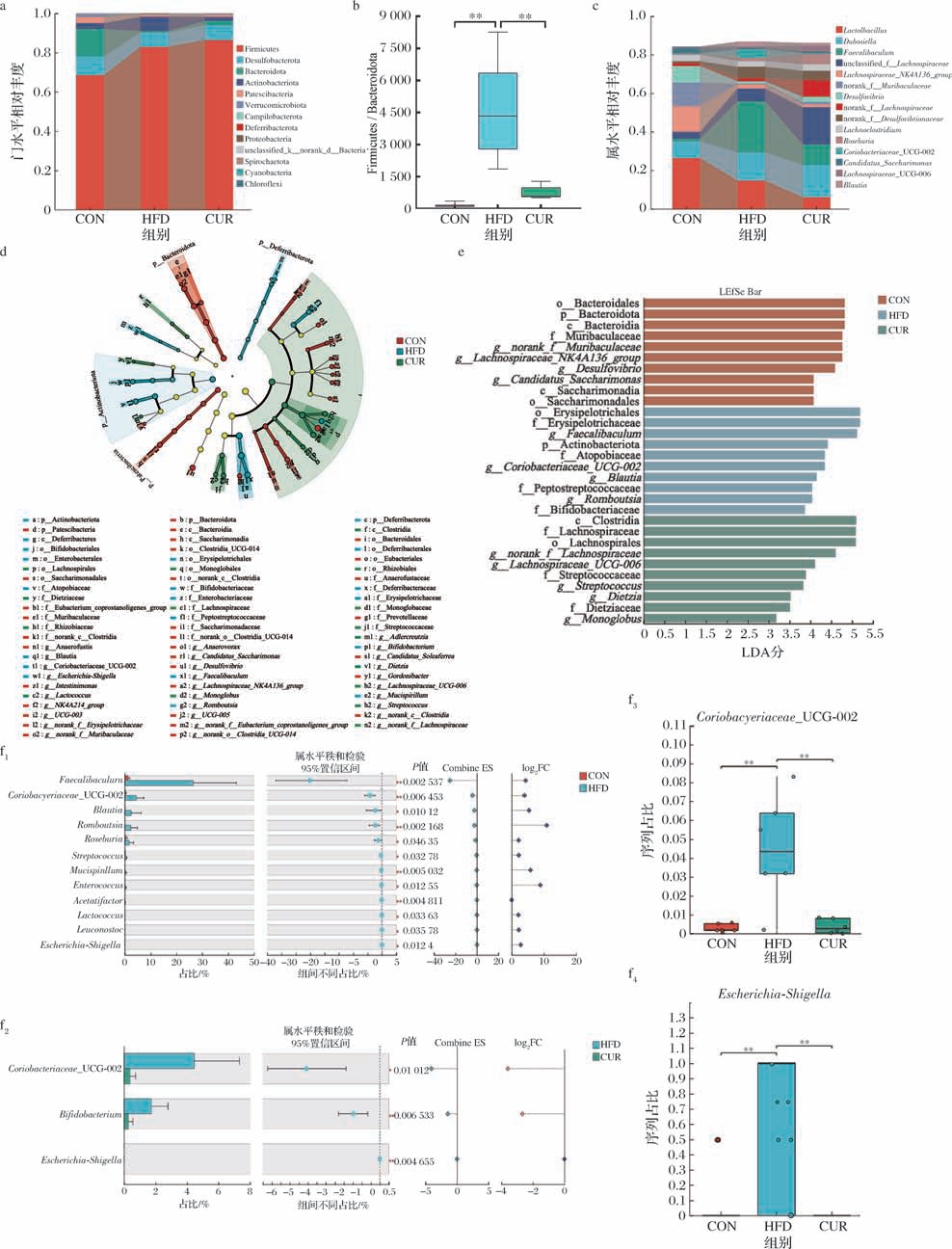
图8 CUR干预对肠道菌群组成的影响
Fig.8 Effects of CUR intervention methods on microflora composition
a-门水平组成;b-F/B比值;c-属水平组成;d-LEfSe分析进化树分支图;e-LDA评分图;f1-HFDvsCON;f2-HFDvsCUR;f3-Coriobacteriaceae_UCG-002组间比较;f4-Escherichia-Shigella 组间比较
利用LEfSe分析各组丰度显著变化的物种(图8-d、图8-e),设定LDA值大于3。结果发现,HFD组显著富集Faecalibaculum、Coriobacteriaceae_UCG-002、布劳氏菌属、Romboutsia 等菌属;CUR组显著富集了norank_f__Lachnospiraceae、_Lachnospiraceae_UCG-006、链球菌属等菌属。进一步采用Wilcoxon秩和检验对各组菌属进行两两组间差异分析,探究CUR干预对HFDvsCON组中显著变化的菌属是否具有回调效果,结果发现CUR干预可极显著缓解HFD组中Coriobacteriaceae_UCG-002和大肠杆菌-志贺菌属(Escherichia-Shigella)相对丰度异常增加,并降低至CON组相似水平(图8-f1~图8-f4)。
2.6 CUR干预对结肠组织形态、通透性和LPS的影响
研究结果显示,与CON组相比,HFD组结肠组织连接相关蛋白ZO-1显著降低(P <0.01);与HFD组相比,CUR组结肠组织ZO-1蛋白相对表达量显著上调(P <0.01)(图9-a、图9-b)。图9-c、图9-d结果显示,HFD组血清及盲肠内容物LPS含量相较于CON组显著增加(P <0.01);但与HFD组相比,CUR组血清及盲肠内容物LPS含量显著下调(P <0.01)。H&E结果显示,CON组小鼠结肠组织结构完整,细胞排列紧密,肠道黏膜上皮屏障完整,且无炎症细胞浸润;HFD组与CON组相比,组织病理评分显著增加(P <0.01),肠道出现明显炎症浸润,结构出现损伤;与HFD组相比,CUR干预组小鼠肠道结构得到明显改善,炎症症状明显减少,组织病理评分显著减小(P <0.01)(图9-c、图9-d)。
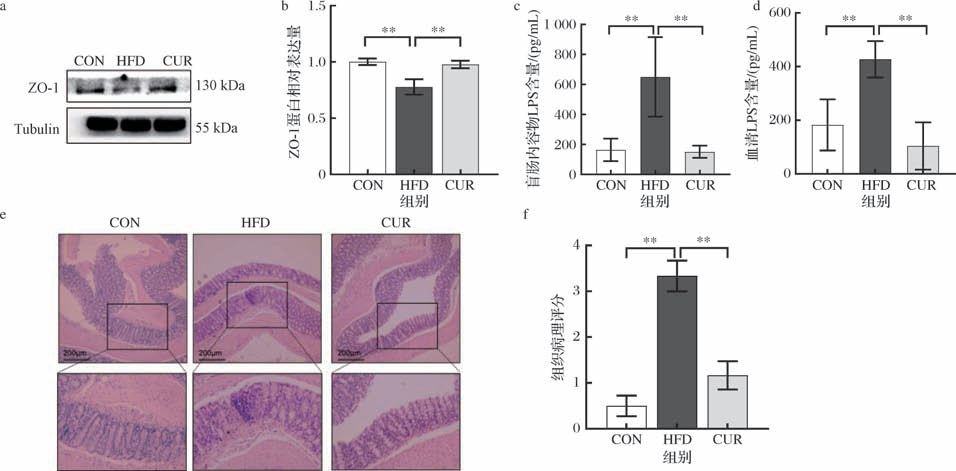
图9 CUR干预对结肠组织形态,通透性及LPS的影响
Fig.9 Effects of CUR intervention on colon morphology,permeability,and LPS
a-ZO-1蛋白原始条带(n=6);b-ZO-1蛋白相对表达量;c-盲肠内容物LPS含量;d-血清LPS含量;e-结肠组织H&E染色;f-组织病理评分
2.7 CUR干预对海马区神经元细胞焦亡和突触可塑性的影响
如图10所示,与CON组相比,HFD组海马体细胞焦亡相关基因NLRP3、GSDMD、IL-1β 的mRNA及蛋白表达水平均显著上调(P <0.05),Caspase1 的mRNA表达水平以及Cleaved-Caspase1 的mRNA及蛋白表达水平均显著上调(P <0.05) (图10-a~图10-d);突触可塑性相关蛋白SYN1、SYP及BDNF的表达水平显著下调(P <0.05);而在CUR干预后,上述细胞焦亡基因的mRNA及蛋白表达均显著下调(P <0.05),而突触可塑性相关基因蛋白表达水平显著上调(图10-e、图10-f),结果说明CUR干预能够减轻海马区神经元细胞焦亡,并提高突触可塑性。
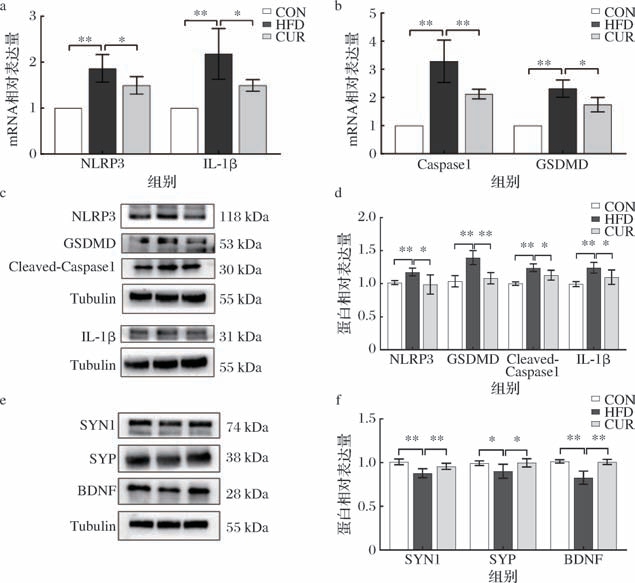
图10 CUR干预对海马区神经元细胞焦亡和突触可塑性的影响
Fig.10 Effects of CUR intervention on neuronal pyroptosis and synaptic plasticity in the hippocampus
a-焦亡相关基因NLRP3、IL-1β 的mRNA表达水平;b-Caspase1、GSDMD的mRNA表达水平;c-焦亡相关蛋白原始条带;d-焦亡相关蛋白相对表达量;e-突触可塑性相关蛋白;f-突触可塑性相关蛋白相对表达量
2.8 核心菌群与运动相关指标、细胞焦亡、突触可塑性蛋白的相关性分析
图11结果显示,Coriobacteriaceae_UCG-002与BDNF(r=-0.728)、SYN1(r=-0.523)呈显著负相关(P <0.05);与GSDMD、Cleaved-Caspase1、NLRP3、血清LPS以及爬杆实验下落时间呈显著正相关(r=0.569~ 0.708,P <0.05)。 Escherichia-Shigella 与ZO-1呈极显著负相关(r=-0.671,P <0.01);与BDNF、SYN1、疲劳转棒时间、倒挂时间呈显著负相关(r=-0.671~-0.493,P <0.05);与GSDMD、NLRP3、血清及盲肠内容物LPS呈显著正相关(r=0.477~0.656,P <0.05)。
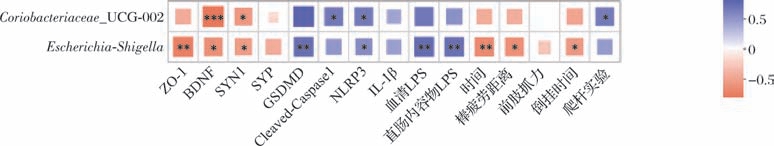
图11 核心菌群与运动相关指标、细胞焦亡、突触可塑性蛋白的相关性分析
Fig.11 Correlation analysis of core microbiota with exercise-related indicators,pyroptosis,and synaptic plasticity proteins
注:∗∗∗代表非常显著性差异,P <0.001。
3 讨论与结论
本研究通过长期高脂膳食喂养诱导肥胖相关认知障碍模型,发现12周高脂膳食能够成功诱导肥胖认知障碍模型。健康指数和血脂变化结果显示,HFD组出现血脂异常并伴随肥胖现象发生,而CUR组小鼠得到明显改善。前人研究表明,CUR在调节血脂和能量代谢方面展现出显著的潜力:在脂质代谢方面,CUR干预可通过抑制肠道尼曼-匹克C1样蛋白1表达减少胆固醇吸收[27];上调肝脏三磷酸腺苷结合盒转运子A1(ATP-binding cassette transporter A1,ABCA1),促进胆固醇逆向转运;抑制脂肪酸合成酶(fatty acid synthase,FAS)活性,减少脂肪酸合成;增强脂肪酸β-氧化,促进脂肪酸分解;激活脂蛋白脂酶(lipoprotein lipase,LPL),促进甘油三酯分解[28];在能量代谢方面,CUR干预激活成纤维细胞生长因子21(fibroblast growth factor 21,FGF21)/鸢尾素信号通路,增加能量消耗[29],此外CUR还可通过提高脂肪组织的产热和褐变能力[30]缓解脂质代谢紊乱。本研究结果同样说明CUR干预可有效减轻血脂异常,改善健康指数,恢复健康状况。
本研究中认知行为学测试发现,高脂膳食会诱导肥胖小鼠发生认知功能障碍。有研究发现,短期(3 d)或长期(3个月)高脂膳食均会诱导认知障碍发生,造成肥胖动物模型出现学习记忆能力下降并伴随脑部炎症[31],但短期高脂膳食主要导致轻度且可逆的认知功能损伤,虽然会影响空间记忆和情景记忆等特定认知领域,但这种损伤通常具有可逆性,对物体记忆等其他认知能力影响较小;而长期高脂膳食则通过累积的炎症反应、神经退行性变化(Tau蛋白过度磷酸化)以及小胶质细胞激活等机制,导致更严重的认知功能障碍,包括空间记忆、情景记忆等多领域的下降,且这种损伤难以逆转[32]。本研究结果同样证实,持续12周高脂膳食会导显著损害小鼠的识别记忆能力,减少其对新物体的探索偏好,导致认知功能下降。然而,8周的CUR干预能够显著改善肥胖相关认知障碍,与HFD组比较,CUR组小鼠在NOR和Y迷宫测试中表现出较好的学习和记忆能力,且海马神经元细胞数量明显增多,提示CUR能够改善肥胖相关认知障碍。突触可塑性相关蛋白变化结果显示,HFD组BDNF、SYP、SYN1表达水平均 显著降 低,BDNF信号通路与神经元发育、分化、再生以及突触传递和可塑性有关,该通路受损参与认知功能障碍发病进程,前人研究发现肥胖小鼠海马中BDNF水平降低,神经元树突棘密度显著减少[33],而上述蛋白在CUR组中表达显著增加,提示CUR干预可通过促进BDNF信号通路表达提高突触可塑性,继而改善肥胖相关认知障碍。运动学测试结果表明,HFD组小鼠协调能力、肌肉力量和运动耐力均出现显著衰退,CUR干预则显著改善协调能力和运动耐力,但对肌肉力量的提升效果不佳,研究结果支持前人研究成果[18],进一步论证了CUR对运动能力的影响主要为耐力和协调能力,而非肌肉力量。
高脂膳食会导致肠道菌群微生态失衡并继而破坏肠道屏障功能[34],在门水平上F/B比值是评估肠道菌群稳态的重要指标之一,Firmicutes能够增加能量获取效率并导致能量摄取过量,而Bacteroidota与免疫系统有关,而肥胖状态下全身慢性炎症会间接抑制其生长,因此F/B比值增加通常意味着代谢紊乱现象发生[26,35]。研究结果显示,HFD组F/B比值显著增加而CUR组比值则显著降低,说明CUR干预能够有效逆转高脂膳食对肠道菌群的不良影响,维持肠道菌群微生态平衡。在属水平上,Coriobacteriaceae_UCG-002和Escherichia-Shigella 为CUR干预后的回调菌群,其相对丰度在HFD组中显著增加,但在CUR组中显著下调。前人研究发现,高脂膳食喂养小鼠体内Coriobacteriaceae_UCG-002显著增加,并与血清LPS水平呈正相关[36]。尽管Coriobacteriaceae_UCG-002自身并不产生LPS,但作为一种产生苯酚和对甲酚的革兰氏阳性菌,该菌属能够通过自身代谢产物直接损伤肠上皮细胞,并通过抑制紧密连接蛋白表达来破坏肠道黏膜屏障的完整性[37],肠道中的LPS则更容易通过受损的肠道屏障进入血液循环,继而促进炎症发生。而Escherichia-Shigella 作为直接产生LPS的革兰氏阴性促炎菌,不仅会通过其自身产生的志贺毒素和肠毒素直接损伤肠上皮细胞,破坏肠道黏膜屏障[38],还会过度增殖产生大量LPS诱导炎症发生[39]。本研究结果证实,HFD组肠道出现明显炎症浸润,结构出现损伤,ZO-1表达显著降低,盲肠内容物和血清中的LPS显著增加,而CUR干预则显著降低2种菌属的相对丰度,并改善肠道通透性,降低LPS的水平,说明CUR能够有效减少有害菌对肠道屏障的损伤。相关性分析发现,Escherichia-Shigella 与ZO-1及血清/盲肠内容物的LPS呈强烈正相关,进一步说明菌群的组成变化对肠道微生态平衡具有重要影响。值得注意的是,对棕榈酸处理的BV2小胶质细胞体外研究发现[40],NLRP3炎症小体被显著活化,流式细胞术检测Caspase-1表达水平可观察到焦亡率显著增加,提示NLRP3/Caspase-1/GSDMD细胞焦亡信号通路在肥胖相关认知障碍中发挥重要作用。本研究发现,HFD组中NLRP3、GSDMD、IL-1β 的mRNA及蛋白表达水平显著增加,Caspase1的 mRNA和 Cleaved-Caspase1蛋白表达显著增加,但CUR干预则显著逆转上述基因的表达变化,说明CUR干预能够抑制NLRP3/Caspase-1/GSDMD信号通路减少神经元细胞焦亡,抑制炎症因子IL-1β 表达,从而改善肥胖相关认知障碍。
本研究存在一定局限,尽管相关性分析发现,Coriobacteriaceae_UCG-002和Escherichia-Shigella 均与突触可塑性相关蛋白BDNF、SYN1呈显著负相关,与细胞焦亡蛋白GSDMD、NLRP3等呈显著正相关,而前者与爬杆实验下落时间呈显著正相关,后者则与疲劳转棒时间、倒挂时间呈显著负相关,暗示菌群的变化与细胞焦亡、突触可塑性及运动能力之间高度相关,然而尚不清楚其原理机制,后续研究需要通过菌群移植实验探究2种菌属在肥胖相关认知障碍及运动能力衰退中的作用及其潜在机制。
综上所述,CUR干预通过调节肠道菌群组成维持肠道微环境稳态,抑制高脂膳食诱导Coriobacteriaceae_UCG-002和Escherichia-Shigella 的过度增殖,减少肠道屏障损伤以及LPS的分泌与循环水平,进而通过“微生物-肠-脑”轴下调NLRP3/Caspase-1/GSDMD通路表达抑制细胞焦亡,减轻炎症因子IL-1β 表达,进而增加突触可塑性,改善外周代谢紊乱水平,从而减轻肥胖相关认知障碍和运动能力衰退。
[1]LEI Y,LIANG X,SUN Y N,et al.Region-specific transcriptomic responses to obesity and diabetes in macaque hypothalamus[J].Cell Metabolism,2024,36(2):438-453.e6.
[2]XIAO N,DING Y,CUI B,et al.Navigating obesity:A comprehensive review of epidemiology,pathophysiology,complications and management strategies [ J].The Innovation Medicine,2024,2(3):100090.
[3]KULLMANN S,HENI M,HALLSCHMID M,et al.Brain insulin resistance at the crossroads of metabolic and cognitive disorders in humans[J].Physiological Reviews,2016,96(4):1169-1209.
[4]LIVINGSTON G,HUNTLEY J,LIU K Y,et al.Dementia prevention,intervention,and care:2024 report of the Lancet standing Commission[J].Lancet,2024,404(10452):572-628.
[5]ZHANG D,SHEN C Y,CHEN N G,et al.Long-term obesity impacts brain morphology,functional connectivity and cognition in adults[J].Nature Mental Health,2025,3(4):466-478.
[6]WANG C M,CHAN J S Y,REN L J,et al.Obesity reduces cognitive and motor functions across the lifespan[J].Neural Plasticity,2016,2016(1):2473081.
[7]SCHMITT L O,GASPAR J M,SCHMITT L O,et al.Obesity-induced brain neuroinflammatory and mitochondrial changes[J].Metabolites,2023,13(1):86.
[8]INABA T,YAMASHIRO K,KURITA N,et al.Microbial lipopolysaccharide-induced inflammation contributes to cognitive impairment and white matter lesion progression in diet-induced obese mice with chronic cerebral hypoperfusion[J].CNS Neuroscience &Therapeutics,2023,29(S1):200-212.
[9]MURPHY E A,VELAZQUEZ K T,HERBERT K M.Influence of high-fat diet on gut microbiota:A driving force for chronic disease risk[J].Current Opinion in Clinical Nutrition and Metabolic Care,2015,18(5):515-520.
[10]CHEN J L,XIAO Y H,LI D M,et al.New insights into the mechanisms of high-fat diet mediated gut microbiota in chronic diseases[J].iMeta,2023,2(1):e69.
[11]HUANG P T,ZHANG Z Y,ZHANG P,et al.TREM2 deficiency aggravates NLRP3 inflammasome activation and pyroptosis in MPTP-induced Parkinson’ s disease mice and LPS-induced BV2 cells[J].Molecular Neurobiology,2024,61(5):2590-2605.
[12]ZHANG H J,KANG R,SONG T C,et al.Advances in relieving exercise fatigue for curcumin:Molecular targets,bioavailability,and potential mechanism[J].Journal of Food Science,2024,89(8):4604-4619.
[13]HANDU D,STOTE K,PIEMONTE T,et al.Evaluating bioactivesubstance-based interventions for adults with MASLD:Results from a systematic scoping review[J].Nutrients,2025,17(3):453.
[14]CERULLO M,ARMELI F,MENGONI B,et al.Curcumin modulation of the gut-brain axis for neuroinflammation and metabolic disorders prevention and treatment[J].Nutrients,2025,17(9):1430.
[15]CAI B C,ZHONG L F,WANG Q T,et al.Curcumin alleviates 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine-induced Parkinson’s disease in mice via modulating gut microbiota and short-chain fatty acids[J].Frontiers in Pharmacology,2023,14:1198335.
[16]CUI C,HAN Y Y,LI H X,et al.Curcumin-driven reprogramming of the gut microbiota and metabolome ameliorates motor deficits and neuroinflammation in a mouse model of Parkinson’s disease[J].Frontiers in Cellular and Infection Microbiology,2022,12:887407.
[17]HAO S,DEY A,YU X L,et al.Dietary obesity reversibly induces synaptic stripping by microglia and impairs hippocampal plasticity[J].Brain,Behavior,and Immunity,2016,51:230-239.
[18]颜惠敏,吕欣晨,宋雯燕,等.姜黄素调控肠道菌群及其代谢物提高小鼠运动表现的研究[J].食品与发酵工业,2025,51(8):37-44.YAN H M,LYU X C,SONG W Y,et al.Curcumin modulates gut microbiota and its metabolites to improve exercise performance in mice[J].Food and Fermentation Industries,2025,51(8):37-44.
[19]YOSHIZAKI K,ASAI M,HARA T,et al.High-fat diet enhances working memory in the Y-maze test in male C57BL/6 J mice with less anxiety in the elevated plus maze test[J].Nutrients,2020,12(7):2036.
[20]陈淑云,罗子清,王紫琪,等.基于网络药理学、分子对接及体内实验探讨二至丸改善认知障碍的作用机制[J].中药新药与临床药理,2023,34(10):1387-1397.CHEN S Y,LUO Z Q,WANG Z Q,et al.Exploring the mechanism of erzhi pills in improving cognitive impairment based on network pharmacology,molecular docking and in vivo experiments[J].Traditional Chinese Drug Research and Clinical Pharmacology,2023,34(10):1387-1397.
[21]ZHAO Q,JING Y,JIANG X Y,et al.SIRT5 safeguards against primate skeletal muscle ageing via desuccinylation of TBK1[J].Nature Metabolism,2025,7(3):556-573.
[22]OHNO Y,SHIMIZU S,IMAKI J,et al.Evaluation of the antibradykinetic actions of 5-HT1A agonists using the mouse pole test[J].Progress In Neuro-psychopharmacology and Biological Psychiatry,2008,32(5):1302-1307.
[23]刘瑞玲,李先辉,伍方佳,等.姜黄素联合抗阻运动干预对非酒精性脂肪性肝病的改善作用及对肠道菌群的影响[J].食品与发酵工业,2026,52(2):97-107.LIU R L,LI X H,WU F J,et al.Mechanism of curcumin combined with resistance exercise on high-fat diet-induced nonalcoholic fatty liver disease based on gut microbiota[J].Food and Fermentation Industries,2026,52(2):97-107.
[24]刘芸芸,张冬娜,李善智,等.4′-羟基查尔酮通过调节Th17/Treg平衡治疗溃疡性结肠炎[J].中国病理生理杂志,2025,41(1):81-89.LIU Y Y,ZHANG D N,LI S Z,et al.4′-Hydroxychalcone attenuates ulcerative colitis by regulating Th17/Treg homeostasis[J].Chinese Journal of Pathophysiology,2025,41(1):81-89.
[25]LIU C S,ZHAO D F,MA W J,et al.Denitrifying sulfide removal process on high-salinity wastewaters in the presence of Halomonas sp[J].Applied Microbiology and Biotechnology,2016,100(3):1421-1426.
[26]STOJANOV S,BERLEC A,ŠTRUKELJ B.The influence of probiotics on the firmicutes/bacteroidetes ratio in the treatment of obesity and inflammatory bowel disease [ J].Microorganisms,2020,8(11):1715.
[27]CHENG M J,DING F,LI L Y,et al.Exploring the role of curcumin in mitigating oxidative stress to alleviate lipid metabolism disorders[J].Frontiers in Pharmacology,2025,16:1517174.
[28]JABCZYK M,NOWAK J,HUDZIK B,et al.Curcumin in metabolic health and disease[J].Nutrients,2021,13(12):4440.
[29]ZOU T D,LI S,WANG B,et al Curcumin improves insulin sensitivity and increases energy expenditure in high-fat-diet-induced obese mice associated with activation of FNDC5/irisin[J].Nutrition,2021,90:111263.
[30]YANG C C,DU Y,ZHAO T,et al.Consumption of dietary turmeric promotes fat browning and thermogenesis in association with gut microbiota regulation in high-fat diet-fed mice[J].Food &Function,2024,15(15):8153-8167.
[31]刘玲馨,王阳,朱毅.高脂饮食造成认知功能损伤的机制探索[J].中国油脂,2025,50(7):75-81.LIU L X,WANG Y,ZHU Y.Mechanism exploration of cognitive impairment caused by high fat diet[J].China Oils and Fats,2025,50(7):75-81.
[32]MCLEAN F H,GRANT C,MORRIS A C,et al.Rapid and reversible impairment of episodic memory by a high-fat diet in mice[J].Scientific Reports,2018,8:11976.
[33]胡佳,许傲雪,胡锐,等.CXCL7/CXCR2轴调控突触可塑性在肥胖相关认知功能障碍中的作用[J].中国药理学通报,2024,40(5):881-886.HU J,XU A X,HU R,et al.Effect of CXCL7/CXCR2 axis on synaptic plasticity in obesity-related cognitive dysfunction[J].Chinese Pharmacological Bulletin,2024,40(5):881-886.
[34]AL MAMUN M A,RAKIB A,MANDAL M,et al.Impact of a high-fat diet on the gut microbiome:A comprehensive study of microbial and metabolite shifts during obesity[J].Cells,2025,14(6):463.
[35]LIU Y,JIN Y,LI J,et al.Small bowel transit and altered gut microbiota in patients with liver cirrhosis[J].Frontiers in Physiology,2018,9:470.
[36]HAN H,WANG M Y,ZHONG R Q,et al.Depletion of gut microbiota inhibits hepatic lipid accumulation in high-fat diet-fed mice[J].International Journal of Molecular Sciences,2022,23(16):9350.
[37]YU Z T,LI D G,SUN H X.Herba Origani alleviated DSS-induced ulcerative colitis in mice through remolding gut microbiota to regulate bile acid and short-chain fatty acid metabolisms[J].Biomedicine &Pharmacotherapy,2023,161:114409.
[38]PAKBIN B,BRÜCK W M,BRÜCK T B,et al.Molecular mechanisms of Shigella pathogenesis;recent advances[J].International Journal of Molecular Sciences,2023,24(3):2448.
[39]WANG N N,DILIXIATI Y,XIAO L,et al.Different short-chain fatty acids unequally modulate intestinal homeostasis and reverse obesity-related symptoms in lead-exposed high-fat diet mice[J].Journal of Agricultural and Food Chemistry,2024,72(34):18971-18985.
[40]YANG C X,SUI G H,WANG L,et al.miR-124 prevents the microglial proinflammatory response by inhibiting the activities of TLR4 and downstream NLRP3 in palmitic acid-treated BV2 cells[J].Journal of Molecular Neuroscience,2022,72(3):496-506.