大豆分离蛋白(soy protein isolate,SPI)因良好的功能特性及优质的营养价值被广泛应用于食品体系中。但SPI在贮运过程中溶解性会大幅下降[1]。如何将劣变后的低溶解度SPI实现高值化应用具有重大的现实意义,但目前相关研究鲜少报道。
近年来,由蛋白质稳定的内相体积分数占74%以上的高内相乳液(high internal phase emulsions,HIPEs)[2]和由天然大分子(例如蛋白质[3-4] 和多糖[5-6])或类似固体颗粒[7-8]稳定的高内相Pickering乳液(high internal phase pickering emulsions,HIPPEs)成为研究的热点。相较于上述2种乳液,中内相乳液(medium internal phase emulsions,MIPEs)是指内相体积分数为30%~74%。在MIPEs中,内相液滴浓度显著增加,导致液滴间距缩小,液滴间相互作用增强,并开始相互挤压[9]。这赋予了MIPEs独特的性质:相较于普通乳液,它们通常表现出更高的黏度、更好的物理稳定性以及开始出现类凝胶行为;而与HIPEs和HIPPEs相比,其制备过程对乳化剂的要求相对较低。这使得MIPEs在食品工业(如沙拉酱[10]、蛋黄酱替代品、冰淇淋[11]、奶油制品等需要特定质构和口感的领域)、化妆品(膏霜、乳液)、药物负载载体以及作为多孔材料前驱体[12]等方面具有广泛的应用潜力。特别是在食品体系中,MIPEs因其能平衡产品质地、口感、稳定性和健康属性(如降低脂肪含量),而备受关注。目前,高溶解性大豆蛋白[13]以及改性不溶大豆蛋白颗粒[14-15] 都被报道可以应用于HIPEs和HIPPEs,但其稳定性具有较大的环境局限性[16]。因此,大豆蛋白往往通过和其他稳定剂复配使用或者将蛋白分子改性以提高其在HIPPEs中的乳化及稳定性。已被报道的多糖类复配剂主要有卡拉胶(carrageenan,Car)[17-19]和黄原胶(xanthan gum,XG)[20-22],大豆分离蛋白与Car或XG的复合能够显著改善乳液的稳定性,但大部分使用的SPI为高溶解度,低溶解度SPI鲜有报道。
此外,体系的表面电荷对乳液体系稳定性也具有显著影响[23]。乳液中的液滴会因为电荷的静电斥力不容易发生聚集,这正是电荷对乳液稳定性的重要作用之一[24]。在不同的离子浓度下,离子可能会对液滴表面电荷产生屏蔽效应。TIAN等[25]发现增加蛋白溶液的NaCl浓度,可以改善界面吸附动力学,提升乳液稳定性,但乳液乳滴的聚集程度会增加,乳化活性也会降低。溶液的pH值对乳液的电荷特性也有影响,溶液在不同pH值下,制备的乳液中的电荷密度会不同。WU等[26]发现将pH值从4.7升到7.0,表面电荷从0.34 mmol/g提高到1.16 mmol/g,分散液滴间的静电排斥增加,乳液的稳定性也提高。
为获得稳定的MIPEs体系,本文研究了pH、离子强度和添加XG或Car对SPI-MIPEs贮藏稳定性的影响,为解决低溶解度大豆分离蛋白的高值化应用提供一个新的思路。
1 材料与方法
1.1 材料与试剂
低温脱脂豆粕,山东禹王有限公司;大豆油,益海嘉里食品营销有限公司;牛血清蛋白(bovine serum albumin,BSA),合肥博美生物技术有限公司;XG、Car、尼罗红和尼罗蓝,上海McLean生化科技公司。本研究中使用的所有其他试剂均为分析纯。
1.2 仪器与设备
H2100R离心机,湖南湘仪实验室仪器开发有限公司;ADL311-A喷雾干燥机,日本Yamato公司;T18高速剪切机,德国IKA公司;Nano-ZS型激光粒度仪,英国Malvern公司;LSM900激光共聚焦显微镜,德国Zeiss公司;MCR302流变仪,奥地利Anton Paar公司。
1.3 实验方法
1.3.1 不同溶解度SPI的制备
采用GUO等[27]的方法制备低溶解度的SPI。低温脱脂豆粕和去离子水固液比为1∶6(g∶mL),室温搅拌1 h,过程中用2 mol/L NaOH溶液调pH值至10.0,然后10 000 r/min离心25 min,得到上清液用2 mol/L HCl溶液调pH值至4.5,3 000 r/min离心10 min,将沉淀水洗后复溶,调整pH值至7.0。用双缩脲法[28]测定复溶后的SPI浓度,以BSA蛋白为标准蛋白,后稀释至蛋白浓度为50 mg/mL。上述SPI溶液90 ℃水浴加热15 min(中心温度达到90 ℃开始计时)后冰浴快速冷却,喷雾干燥(入口温度180 ℃,出口温度90 ℃,压力0.1 MPa,流速为2.5 mL/min)。未进行热处理直接喷雾干燥获得的SPI为高溶解度SPI。干燥后的SPI用真空袋包装,并在-20 ℃贮存。根据马天怡等[29]的方法测定SPI溶解度,得到低SPI溶解度为60.41%(质量分数),命名为SPI60,高溶解度SPI溶解度为80.23%(质量分数),命名为SPI80。
1.3.2 MIPEs制备
1.3.2.1 不同pH SPI-MIPEs制备
将SPI60以10 mg/mL的浓度用去离子水分散,室温搅拌2 h,4 ℃保存12 h使蛋白充分水化。后用0.02 mol/L的NaOH溶液将分散液调节到不同的pH值(8.0、9.0、10.0、11.0、12.0)。添加固定的大豆油比例(Φ=60%)到制备的SPI60分散液中,使用高速剪切机在12 000 r/min下均质2 min,得到不同pH值的SPI-MIPEs,未进行pH调节的SPI60和SPI80制备的MIPEs作为对照。
1.3.2.2 不同离子强度SPI-MIPEs制备
将SPI60以10 mg/mL的浓度用去离子水分散,室温搅拌2 h,4 ℃保存12 h使蛋白充分水化。后添加不同量的NaCl,使分散液离子强度分别为50、100、150、200 mmol/L。室温搅拌30 min后,添加固定的大豆油比例(Φ=60%)到制备的SPI60分散液中,使用高速剪切机在12 000 r/min下均质2 min,得到不同离子强度的SPI-MIPEs。
1.3.2.3 SPI-多糖复合物的制备及MIPEs制备
将SPI60以10 mg/mL的浓度用去离子水分散,室温搅拌2 h,4 ℃保存12 h使蛋白充分水化。将SPI60分散液在80 ℃保温30 min,冰浴冷却后备用。将XG和Car以5 mg/mL的浓度分别用去离子水溶解,80 ℃下搅拌1 h。将上述SPI60分散液与多糖溶液分别以体积比为1∶0.5、1∶1、1∶1.5、1 ∶2混合,调节pH值至8.0,并在65 ℃下保温1 h,得到SPI-XG溶液和SPI-Car溶液。取一定量溶液与大豆油混合,并保持油的比例为60%,使用高速剪切机在12 000 r/min下均质2 min,得到SPI-多糖复合物MIPEs[18,20]。
1.3.2.4 MIPEs外观观察
将新鲜制备的MIPEs转移至15 mL透明玻璃瓶中,利用相机对每种MIPEs进行拍照记录,确定是否有分层。
1.3.3 乳液性质测定
1.3.3.1 流变特性
为了研究用不同MIPEs的流变行为,使用流变仪进行动态黏弹性测量,采用PP25探头进行测试。进行振荡应力扫描,扫描范围为0.001~20 Pa,恒定频率10 Hz。然后在线性黏弹性范围内,以0.5% 的应变(在LVE区),从0.1~100 Hz进行动态频率扫描。随着剪切速率从0.10 s-1 增加到100 s-1 时,绘制黏度曲线[30]。所有测量均在25 ℃条件下进行。
1.3.3.2 Zeta电位测定
乳液在25 ℃下通过激光粒度仪测定Zeta电位。在测量之前,用PBS(0.01 mol/L,pH 7.0)将MIPEs稀释50倍,以防止多次散射[31]。
1.3.3.3 离心稳定性测定
将MIPEs转移到10 mL的离心管中,在4 000 r/min下离心5 min,离心完后拍照记录,并根据其状态计算乳析指数(emulsification index,EI)[32],如公式(1)所示:
式中:Hs 为乳液层的高度,Ht 分别为总高度。
1.3.3.4 热稳定性测定
将制备好的MIPEs样品密封在玻璃瓶中并在100 ℃水浴锅中加热30 min,拍照记录加热后MIPEs的形态。
1.3.3.5 冻融稳定性测定
将制备好的MIPEs样品密封在玻璃瓶中并在-20 ℃的冰箱存放24 h,取出后放入25 ℃水浴锅中水浴加热30 min,拍照记录加热后MIPEs的形态。
1.3.3.6 微观结构
采用激光共聚焦扫描显微镜来观察乳液的微观结构,按照MA等[31]的方法检测了不同MIPEs的形态。观察前,用10 mg/mL的尼罗红(大豆油) 和10 mg/mL的尼罗蓝(蛋白质)分别对MIPEs进行染色。尼罗红的激发波长为488 nm,尼罗蓝的激发波长为633 nm。使用ZEISS软件对图像进行处理。
1.4 数据处理
所有实验均重复3次,结果报告为“平均值± 标准差”。所有数据采用IBM SPSS Statistics 26软件进行邓肯和LSD检验(P <0.05)。采用Origin 2021软件进行分析绘图。
2 结果与分析
2.1 MIPEs外观评价
如图1所示,SPI80、SPI60、不同pH、离子强度、添加Car或XG均可以形成SPI-MIPEs,且未出现分层。刚制备的MIPEs从外观上来看基本无区别,但添加Car和XG的乳液黏着性增加。

图1 不同处理方法对SPI-MIPEs外观的影响
Fig.1 The effect of different processing methods on the appearance of SPI-MIPEs
a-pH;b-NaCl;c-Car;d-XG
2.2 流变学特性分析
2.2.1 SPI-MIPEs线性黏弹性区域(linear viscoelastic region,LVE)与屈服应力
LVE指乳液储能模量(G′)和损耗模量(G″)基本不变的区域,G′拐点表示乳液不发生结构破坏的情况下可以承受的最大应力,即屈服应力。如图2-a所示,SPI60-MIPEs的屈服应力和G′明显低于SPI80-MIPEs。SPI60分散液在pH 8~11,对应的MIPEs体系LVE基本无变化,屈服应力均略大于未经处理的SPI60-MIPEs。此现象在菜籽蛋白乳液中也有报道[33],这很可能归因于在pH 8~11,蛋白质部分展开,增强了界面吸附能力,静电排斥与疏水作用平衡,黏弹性稳定[34]。因此表现出LVE消失,G′大幅降低。
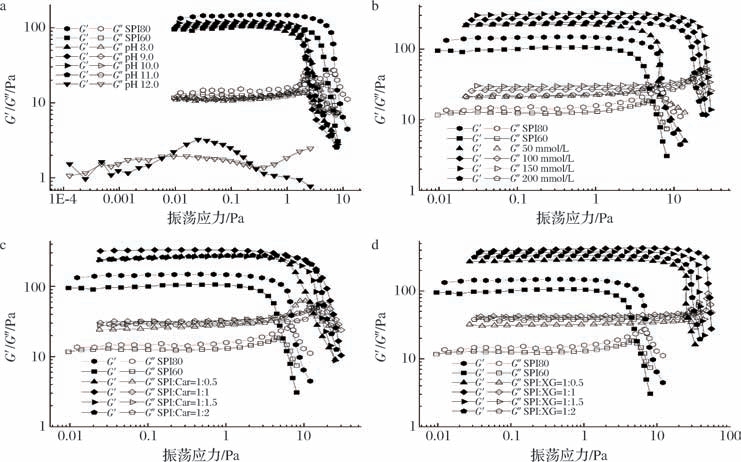
图2 不同处理方法对SPI-MIPEs储能模量(G′)与损耗模量(G″)应力扫描的影响
Fig.2 The effects of different processing methods on the storage modulus (G′) and loss modulus (G″) stress scanning of SPI-MIPEs
a-pH;b-NaCl;c-Car;d-XG
SPI分散液的离子强度可以直接影响SPI的溶解度和MIPEs电荷分布,从而影响MIPEs体系的稳定性。如图2-b所示,添加NaCl在0~ 200 mmol/L,SPI60-MIPEs屈服应力及动态模量均呈现先上升后略微下降的趋势,在150 mmol/L时达到最大值。这可能因为低浓度NaCl的通过电子屏蔽削弱了蛋白分子间的静电排斥,从而形成更致密的界面膜,而高浓度NaCl过度盐析导致SPI溶解度降低,部分蛋白质聚集,界面吸附能力下降[35]。
添加Car(图2-c)和XG(图2-d)也大幅提升了SPI60-MIPEs屈服应力和动态模量。随着多糖比例的增加,SPI60-MIPEs屈服应力及动态模量均呈现出先上升后下降的趋势,添加Car和XG与SPI60比例均在1∶1(体积比)达最大值,这可能因为Car和XG和SPI60在界面膜发生协同作用,形成连续的网状结构[18,22],而过量的多糖又会通过空间位阻减少了SPI60在界面的有效覆盖,导致界面膜的强度下降[36]。对比图2结果,XG的增效作用最显著,当SPI60∶XG为1∶1(体积比)时,SPI60-MIPEs的屈服应力能达到50 Pa,较未经处理SPI60-MIPEs提升9倍以上,且显著高于Car组同比例(P <0.05),表明MIPEs形成的网状结构更加稳定,这很可能由于XG的刚性网络与SPI柔性分子相互作用形成了更稳定的膜界面结构[37]。
2.2.2 MIPEs的黏弹性
流变的动态模量频率扫描可以显示乳液体系的黏弹性。如图3所示,所有样品G′都大于G″,在0.1~100 Hz内二者无交点,说明SPI-MIPEs均能形成一种弱凝胶结构[34]。如图3-a所示,SPI80-MIPEs的G′高于SPI60-MIPEs,这表明SPI溶解度降低,MIPEs网络结构减弱。pH 8.0~11.0时,SPI60-MIPEs在扫描频率范围内动态模量相对稳定,pH 10.0的SPI60-MIPEs G′值明显高于未经处理的SPI60-MIPEs,其他样品差别微小;同时,所有样品的G″值都低于未处理SPI60乳液。当pH 12.0时,SPI60-MIPEs的动态模量明显下降,且随着频率升高出现明显的先下降后上升趋势,说明该体系结构较为脆弱[38]。这一结果说明pH调节对主要影响乳液体系的弹性特性有一定改善作用(G′在pH 10升高)[39]。添加NaCl(图3-b),Car(图3-c)和XG(图3-d)的频率扫描结果中,其G′值随各自添加量的变化同应力扫描结果基本一致,分别在NaCl添加量为150 mmol/L时,SPI∶Car/XG为1∶1(体积比)获得最大值。
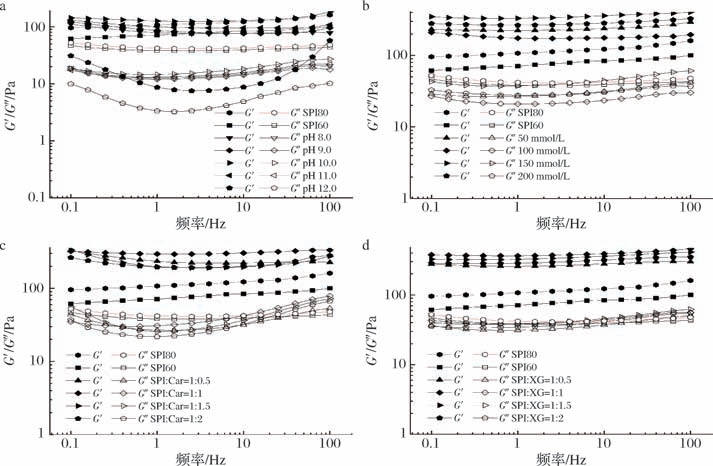
图3 不同处理方法对SPI-MIPEs储能模量(G′)与损耗模量(G″)频率扫描的影响
Fig.3 The effects of different processing methods on the storage modulus (G′) and loss modulus (G″) frequency scans of SPI-MIPEs
a-pH;b-NaCl;c-Car;d-XG
2.2.3 MIPEs的黏度
由图4可知,所有的SPI-MIPEs的黏度都随着剪切速率的增大而降低,表现出典型的剪切稀化行为[40]。SPI60-MIPEs的黏度明显低于SPI80-MIPEs,可能是由于液滴在MIPEs中的排列较为分散,形成了较弱的凝胶网络结构。且pH调节对SPI60形成的MIPEs体系黏度的影响较为有限(图4-a)。除pH 12.0在剪切初期因黏弹性下降导致更快的黏度下降,其他不同pH的SPI60-MIPEs黏度差异较小,这很可能是因为远离等电点(SPI等电点为4.5)时,蛋白质的带电状态达到饱和,pH进一步升高不会显著改变界面电荷密度或液滴间作用力。MCCLEMENTS等[40]也报道乳清蛋白(等电点为5)用于稳定乳液时,在pH 7~11时,体系黏度差异小于10%。随着NaCl添加量的增多,SPI60-MIPEs的黏度和G′(图3-b)的变化趋势一致,先上升后下降,添加量为150 mmol/L时,乳液体系黏度最大。添加Car和XG都大幅提升了SPI60-MIPEs黏度,不同添加比例的样品间差别较小,Car在添加比例为1∶1.5(体积比)时黏度最大,XG在添加比例为1∶1(体积比)时黏度最大,且后者黏度最大,主要是依赖于XG的分子结构是刚性螺旋链,能与SPI形成致密的网状结构,能够包裹住更多的油滴,从而提升乳液的黏度[41]。
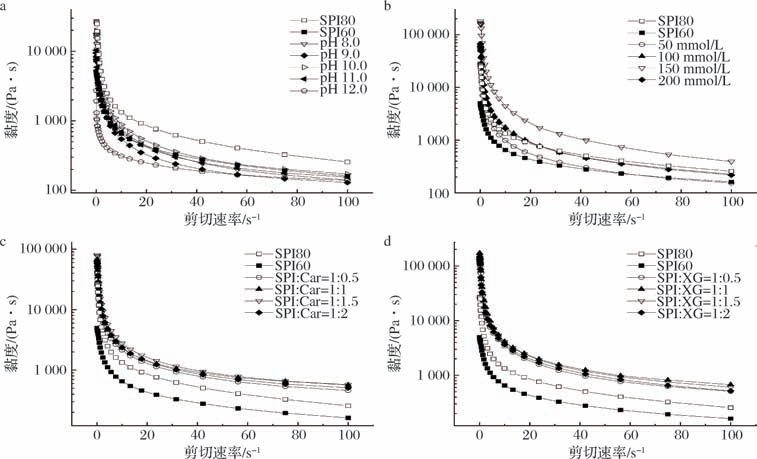
图4 不同处理方法对SPI-MIPEs黏度的影响
Fig.4 The effects of different processing methods on the viscosity of SPI-MIPEs
a-pH;b-NaCl;c-Car;d-XG
2.3 MIPEs的Zeta电位
Zeta电位是衡量胶体分散体系稳定性的重要参数,其绝对值越高,表明体系越稳定,高Zeta电位值意味着颗粒之间的静电排斥力较强,可防止颗粒聚集。如图5-a所示,SPI60-MIPEs的Zeta电位绝对值显著低于SPI80-MIPEs(P <0.05),这很可能是由于低溶解性SPI发生蛋白聚集,造成表面电荷下降[42]。SPI60-MIPEs的Zeta电位绝对值随着pH上升逐渐升高,在pH 10.0时,乳液体系的Zeta电位绝对值达到最大值,表明此时蛋白质表面电荷最多,静电排斥力最强,从而有利于乳液的稳定性。然而,当pH值进一步升高至12.0时,可能会出现过度的电荷排斥作用,导致蛋白质分子间的相互作用减弱,从而降低了Zeta电位的绝对值[43]。这一现象与流变特性结果一致,其中在pH 10时乳液的G′值较高,显示出较好的黏弹性和稳定性。图5-b显示了在不同NaCl含量测得的Zeta电位值。随着NaCl浓度的增加,由于电子屏蔽效应,Zeta电位绝对值持续降低。添加Car(图5-c)和XG(图5-d)的SPI60-MIPEs zeta电位绝对值均出现大幅升高,当添加比例为1∶1(体积比)时获得最大值,随后逐渐下降。这一变化与流变特性一致,均在添加比例为1∶1(体积比)时获得最大G′。添加XG的增效更突出:SPI∶XG=1∶1(体积比)时电位达-40.4 mV,显著高于Car组同比例(P <0.05)。这一影响趋势同前人报道一致,XU等[44]研究了Car对乳蛋白稳定乳液的影响,发现添加Car显著提高了乳液的Zeta电位绝对值,且在特定比例下达到最大值,过量添加Car会导致Zeta电位绝对值下降,DICKINSON[45]也指出,Car与蛋白质的静电相互作用是提高乳液稳定性的关键机制,过量添加会破坏静电平衡,导致Zeta电位下降。从Zeta电位绝对值来看,整体上XG和Car可以大幅提高电位绝对值,其中XG在添加比例1∶1(体积比)时获得最大值-40.4 mV,理论上更有利于乳液的长期稳定性。
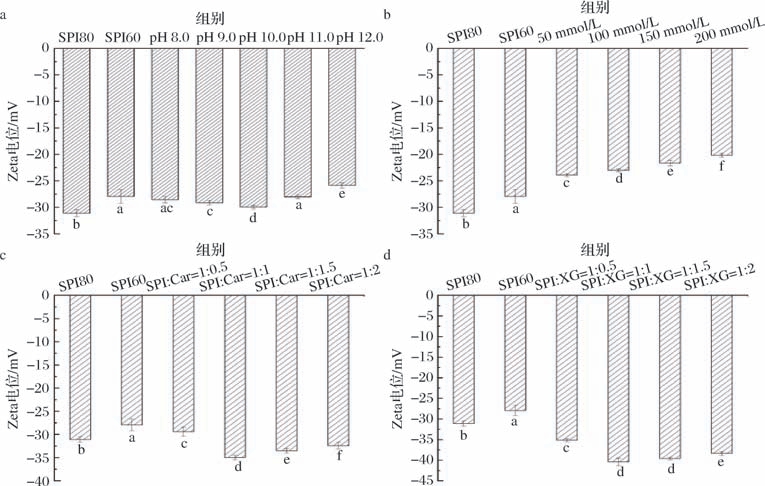
图5 不同处理方式对SPI-MIPEs Zeta电位的影响
Fig.5 The effects of different processing methods on the Zeta potential of SPI-MIPEs
注:不同小写字母表示差异显著(P <0.05)(下同)。
a-pH;b-NaCl;c-Car;d-XG
2.4 MIPEs的离心稳定性
通过离心力来加速液滴的沉降和聚结过程,在短时间内模拟乳液长期贮存可能发生的分层和破乳现象,来表征SPI-MIPEs的稳定性。如图6所示,SPI80-MIPEs的离心稳定性为52.145%,SPI60-MIPEs的离心稳定性为48.335%,说明低溶解度SPI不利于MIPEs的稳定性。除添加NaCl的图6-b外,其他SPIMIPEs离心稳定性基本与其相应的流变特性、黏度和Zeta电位结果一致,分别是在pH 10,Car和XG添加比例为1 ∶1(体积比)时获得最大的离心稳定性,且XG效果最佳。同时可以发现,pH和添加NaCl的离心稳定性均在45%~ 58%,而添加Car最大值为68.115%,添加XG最大值为93.05%,显著高于其他组(P <0.05),较未经处理的SPI60-MIPEs提高了44.715%,较Car最大值提高了24.935%,说明SPI60-MIPEs乳液黏弹性影响相对较大。对比图5-b中添加NaCl的SPI60-MIPEs Zeta电位绝对值随添加量的增加持续下降,图6-b中相应乳液的离心稳定性却变化微小,进一步说明了静电斥力对低溶解性SPIMIPEs稳定性影响较为有限。由于XG和Car均带有负电,与蛋白分子发生静电相互作用[46],因此对体系的G′、黏度和Zeta电位都有很大的影响,且XG由于除静电相互作用,还具有空间位阻效应[47],因此对MIPEs体系稳定性的提升效果最佳。
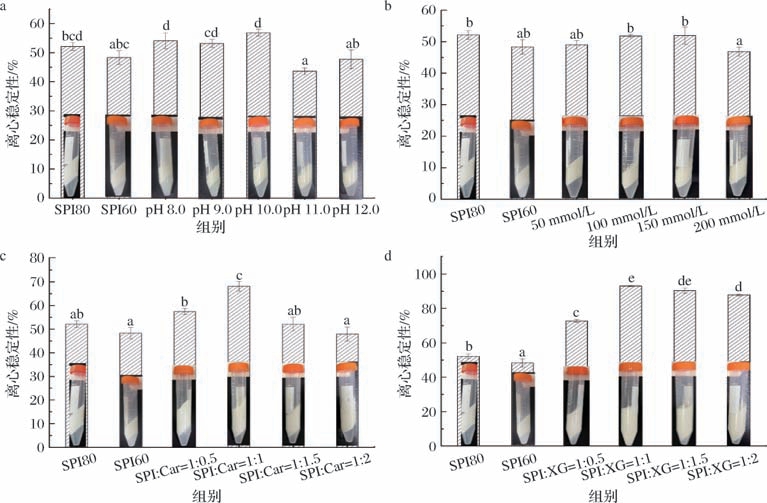
图6 不同处理方法对SPI-MIPEs离心稳定性的影响
Fig.6 The effects of different processing methods on the centrifugal stability of SPI-MIPEs
a-pH;b-NaCl;c-Car;d-XG
2.5 MIPEs的热和冻融稳定性
MIPEs的热稳定性如图7的左图所示,SPI80-MIPEs具有良好的热稳定性,在加热后仍具有乳液的形态,未有连续相析出,而SPI60-MIPEs的热稳定性不佳,在沸水浴下有大量连续相析出。左图7-a中,当pH为值8.0、10.0和11.0时,乳液的热稳定性有提高,但仍有少量连续相析出。图7-b中,添加不同浓度的NaCl对提升乳液的热稳定性都有一定的效果。图7-c中,当SPI∶Car=1∶0.5(体积比)时,乳液仍有连续相析出,继续增大Car浓度,乳液的热稳定性好,在100 ℃下仍能保持稳定。添加XG的乳液的热稳定性都较好。

图7 不同处理方法对SPI-MIPEs热稳定性(左)和冻融稳定性(右)的影响
Fig.7 The effects of different processing methods on the thermal stability (left) and freeze-thaw stability (right) of SPI-MIPEs
注:左图(图7-a~图7-d)为热稳定性(a:pH;b:NaCl;c:Car;d:XG);右图(图7-a′~图7-d′)为冻融稳定性(a′:pH;b′:NaCl;c′:Car;d′:XG)。
MIPEs的冻融稳定性如图7-c′所示,SPI60-MIPEs和SPI80-MIPEs都发生了严重的乳析现象,分层现象明显,表明乳液的冻融稳定性较差。添加NaCl后,乳液也出现了乳析现象,当添加量为150 mmol/L时,乳液的冻融稳定性相对最好。添加Car后,乳液的冻融稳定性也有所改善,当SPI∶Car=1∶1(体积比)时,乳液经过冻融后外观形态变化最小。4种添加不同比例的XG乳液,冻融后乳液的稳定性都较好,当SPI∶XG=1 ∶1(体积比)时,乳液外观没有变化,说明添加XG对SPI60的乳化稳定性调节效果最好。
2.6 MIPEs的微观结构
图8展示了采用激光共聚焦扫描显微镜对4种处理方式中具有最佳离心稳定性的SPI-MIPEs的微观结构分析结果。大豆油用尼罗红染色,蛋白质用尼罗蓝染色。通过与未经处理的SPI60-MIPEs(图8-a)的比较,可以观察到不同处理方式对乳液微观结构的显著影响。
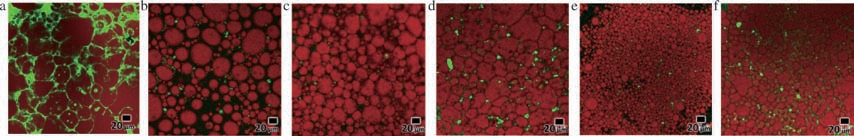
图8 不同处理方式对SPI-MIPEs微观结构的影响
Fig.8 The effects of different processing methods on the microstructure of SPI-MIPEs
a-SPI80-MIPEs;b-SPI60-MIPEs;c-pH 10.0;d-150 mmol/L NaCl;e-SPI∶Car=1∶1(体积比);f-SPI∶XG=1∶1(体积比)
SPI80-MIPEs(图8-a) 颗粒最大,未经处理的SPI60-MIPEs(图8-b)颗粒均匀度较前者明显下降,且分布较为分散,这种结构导致MIPEs的稳定性较差,和其对应的G′、黏度和离心稳定性变化趋势一致。这很可能是由于不可溶性蛋白的增加降低了颗粒之间相互作用[48]。一般来说,乳液颗粒间距离越小,布朗运动越剧烈,对应的黏度值越高;同时颗粒分布越均匀,颗粒排列越有序,可能在低剪切速率下形成弱网络结构,会进一步提升黏度,增加体系的屈服应力及离心稳定性[49]。和未经处理的SPI60-MIPEs相比,调节pH(图8-c)或添加NaCl(图8-d),SPI60-MIPEs颗粒均匀度都有较为明显的改善,且颗粒排列更为紧密,这很可能就是体系屈服应力、G′和黏度增加的主要原因,但对体系的离心稳定性改善较为有限。而添加Car(图8-e)后,SPI60-MIPEs粒径均明显变小,颗粒呈规则球状,分布紧密,这种微观结构的变化与离心稳定性的提升(较未经处理的SPI60-MIPEs提高了19.78%)相一致。虽然在微观结构上较为相似,但添加XG所形成的乳液离心稳定性较添加Car提高了约24.935%,对应的G′、黏度和Zeta电位绝对值均显著高于后者。XG和Car都可以提高体系黏度,且都因带负电荷可以和蛋白发生静电相互作用[46],但XG还被报道可以通过疏水相互作用和氢键和蛋白发生多种相互作用,从而形成更为稳定的界面膜和连续相的三维网状凝胶结构[50]。
3 结论与讨论
本研究聚焦于低溶解度SPI在MIPEs体系中的应用潜力,深入探究了pH、离子强度及多糖(Car、XG)对其稳定性的影响。研究发现,添加XG对低溶解度SPI稳定MIPEs体系起到了至关重要的作用。当SPI60与XG的添加比达到1∶1(体积比)时,体系的储能模量(G′)显著升高3倍,表观黏度也大幅提升,离心稳定性提升了44.715%,微观结构分析更直观地证实了该体系液滴粒径大幅减小,分布均匀且排列紧密,这为体系的长期稳定提供了有力的微观结构支撑。这一发现为低溶解度SPI在食品乳液体系中的应用提供了有力的理论依据,为低溶解性SPI实现高值化应用提供新的思路和方法。
[1]MARTINS V B,NETTO F M.Physicochemical and functional properties of soy protein isolate as a function of water activity and storage[J].Food Research International,2006,39(2):145-153.
[2]BAGO RODRIGUEZ A M,BINKS B P.High internal phase Pickering emulsions[J].Current Opinion in Colloid &Interface Science,2022,57:101556.
[3]LI X,XU X B,SONG L,et al.High internal phase emulsion for food-grade 3D printing materials[J].ACS Applied Materials &Interfaces,2020,12(40):45493-45503.
[4]JIAO B,SHI A M,WANG Q,et al.High-internal-phase Pickering emulsions stabilized solely by peanut-protein-isolate microgel particles with multiple potential applications[J].Angewandte Chemie(International Ed.in English),2018,57(30):9274-9278.
[5]ZENG T,WU Z L,ZHU J Y,et al.Development of antioxidant Pickering high internal phase emulsions (HIPEs) stabilized by protein/polysaccharide hybrid particles as potential alternative for PHOs[J].Food Chemistry,2017,231:122-130.
[6]CHEN Y,WANG Y S,LI Y H,et al.Extrusion-based 3D printing of Pickering high internal phase emulsions stabilized by flaxseed protein-sodium alginate complexes for encapsulating curcumin [ J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2023,673:131863.
[7]YI J,GAO L Y,ZHONG G T,et al.Fabrication of high internal phase Pickering emulsions with calcium-crosslinked whey protein nanoparticles for β-carotene stabilization and delivery[J].Food &Function,2020,11(1):768-778.
[8]ZHOU F Z,YU X H,LUO D H,et al.Facile and robust route for preparing Pickering high internal phase emulsions stabilized by bare zein particles[J].ACS Food Science &Technology,2021,1(8):1481-1491.
[9]ZHANG L,YU Y,ZHANG L,et al.Improving the stability of waterin-oil emulsions with medium internal phase by the introduction of gelatin[J].Foods,2023,12(15):2863.
[10]LI R N,TRUE A D,SHA L,et al.Structural modification of oat protein by thermosonication combined with high pressure for O/W emulsion and model salad dressing production[J].International Journal of Biological Macromolecules,2024,255:128109.
[11]MOHAMMED N K,MUHIALDIN B J,MEOR HUSSIN A S.Characterization of nanoemulsion of Nigella sativa oil and its application in ice cream[J].Food Science &Nutrition,2020,8(6):2608-2618.
[12]MATHIEU K,JÉRÔME C,DEBUIGNE A.Macro-and near-mesoporous monoliths by medium internal phase emulsion polymerization:A systematic study[J].Polymer,2016,99:157-165.
[13]金银霜.天然大豆分离蛋白稳定高内相乳液的制备及表征[J].现代食品科技,2019,35(8):55-61;41.JIN Y S.Fabrication and characterization of high internal phase emulsions stabilized by natural soy protein isolates[J].Modern Food Science and Technology,2019,35(8):55-61;41.
[14]ZHAO F,LIU J Q,ZHAO J X,et al.The mechanism of 3D-printed high internal phase Pickering emulsion gels improved by soybean protein isolate/bacterial cellulose co-assemblies[J].International Journal of Biological Macromolecules,2025,302:140435.
[15]ZHAO G L,WANG S N,LI Y Y,et al.Metal cation-induced conformational changes of soybean protein isolate/soybean soluble polysaccharide and their effects on high-internal-phase emulsion properties[J].Journal of the Science of Food and Agriculture,2024,104(6):3341-3351.
[16]SUN Y D,ZHONG M M,ZHAO X M,et al.Stability and digestion characteristics of Pickering high internal phase emulsions formed by acid-induced soy lipophilic protein,β-conglycinin,and globulin[J].LWT,2022,153:112554.
[17]QIAO D L,ZHANG Y Y,SUN F R,et al.Enhancement mechanism of ι-carrageenan on the network structure and gel-related properties of soy protein isolate/λ-carrageenan system[J].Food Chemistry,2025,468:142476.
[18]LIU X,MENG F J,YANG C,et al.Formation conditions of soy protein isolate-carrageenan complex particles and their stabilization effect on the relationship between structure and rheology of emulsions[J].Food Bioscience,2024,60:104341.
[19]MENG F J,LI J M,YANG C,et al.Rheological and tribological properties of high internal phase emulsions stabilized by pH-induced soy protein isolate-carrageenan complex coacervates[J].Food Hydrocolloids,2024,146:109191.
[20]LI L L,WANG W J,JI S P,et al.Soy protein isolate-xanthan gum complexes to stabilize Pickering emulsions for quercetin delivery[J].Food Chemistry,2024,461:140794.
[21]薛山,庄凌凌.大豆分离蛋白-卡拉胶-黄原胶三元复合Pickering乳液的制备与特性分析[J].食品工业科技,2023,44(15):16-24.XUE S,ZHUANG L L.Preparation and characterization of Pickering emulsion of soybean protein isolate-carrageenan-xanthan terpolymer[J].Science and Technology of Food Industry,2023,44(15):16-24.
[22]KRSTONOŠI V,PAVLOVI N,NIKOLI I,et al.Physicochemical properties and stability of oil-in-water emulsions stabilized by soy protein isolate and xanthan gum[J].International Journal of Biological Macromolecules,2024,260:129610.
[23]马焕塔,刘思彤,招亮羽,等.罗非鱼分离蛋白-卡拉胶复合乳液的稳定性研究[J].食品与发酵工业,2024,50(18):148-153.MA H T,LIU S T,ZHAO L Y,et al.Studies on stability of tilapia protein isolate-carrageenan composite emulsion[J].Food and Fermentation Industries,2024,50(18):148-153.
[24]HEIDARI-DALFARD F,TAVASOLI S,ASSADPOUR E,et al.Surface modification of particles/nanoparticles to improve the stability of Pickering emulsions;a critical review[J].Advances in Colloid and Interface Science,2025,336:103378.
[25]TIAN Y,TAHA A,ZHANG P P,et al.Effects of protein concentration,pH,and NaCl concentration on the physicochemical,interfacial,and emulsifying properties of β-conglycinin[J].Food Hydrocolloids,2021,118:106784.
[26]WU Y L,LI Y,LI B,et al.Effect of surface charge density of bacterial cellulose nanofibrils on the properties of O/W Pickering emulsions co-stabilized with gelatin[J].Food Hydrocolloids,2023,138:108447.
[27]GUO F X,XIONG Y L,QIN F,et al.Examination of the causes of instability of soy protein isolate during storage through probing of the heat-induced aggregation [J].Journal of the American Oil Chemists’ Society,2015,92(8):1075-1084.
[28]GORNALL A G,BARDAWILL C J,DAVID M M.Determination of serum proteins by means of the biuret reaction[J].Journal of Biological Chemistry,1949,177(2):751-766.
[29]马天怡,郭凤仙,何振东,等.L-精氨酸/L-赖氨酸改性大豆分离蛋白乳化性[J].精细化工,2022,39(1):150-157;163.MA T Y,GUO F X,HE Z D,et al.L-Arginine/L-lysine ameliorating the emulsifying properties of soy protein isolate [J].Fine Chemicals,2022,39(1):150-157;163.
[30]景成童,涂安,赵春昊,等.玉米醇溶蛋白-假酸浆子胶二元复合物的制备及在Pickering乳液中的应用[J].食品工业科技,2024,45(9):91-98.JING C T,TU A,ZHAO C H,et al.Preparation of zein-Nicandra physaloides gum binary complex and its application in Pickering emulsions[J].Science and Technology of Food Industry,2024,45(9):91-98.
[31]MA L,ZOU L Q,MCCLEMENTS D J,et al.One-step preparation of high internal phase emulsions using natural edible Pickering stabilizers:Gliadin nanoparticles/gum Arabic [J].Food Hydrocolloids,2020,100:105381.
[32]葛慧娟,肖军霞,黄国清.乳清分离蛋白-果胶复合物在Pickering乳液制备中的应用[J].中国食品学报,2021,21(3):161-172.GE H J,XIAO J X,HUANG G Q.The application of whey protein isolate-pectin complex in the preparation of Pickering emulsions[J].Journal of Chinese Institute of Food Science and Technology,2021,21(3):161-172.
[33]XU F R,PAN M M,LI J W,et al.Preparation and characteristics of high internal phase emulsions stabilized by rapeseed protein isolate[J].LWT,2021,149:111753.
[34]LIN D Q,KELLY A L,MIAO S.The impact of pH on mechanical properties,storage stability and digestion of alginate-based and soy protein isolate-stabilized emulsion gel beads with encapsulated lycopene[J].Food Chemistry,2022,372:131262.
[35]WANG Y S,MA T Y,LIU C Q,et al.L-histidine improves solubility and emulsifying properties of soy proteins under various ionic strengths[J].LWT,2021,152:112382.
[36]XU Y,WANG S N,XIN L W,et al.Interfacial mechanisms,environmental influences,and applications of polysaccharide-based emulsions:A review[J].International Journal of Biological Macromolecules,2025,293:139420.
[37]FANG F,LUO X,BEMILLER J N,et al.Neutral hydrocolloids promote shear-induced elasticity and gel strength of gelatinized waxy potato starch[J].Food Hydrocolloids,2020,107:105923.
[38]ESPERT M,GRACIA-FERNÁNDEZ C,SALVADOR A,et al.Linear and nonlinear viscoelasticity of edible o/w emulsions used as saturated fat replacers[J].LWT,2024,191:115609.
[39]BOOSTANI S,HOSSEINI S M H,GOLMAKANI M T,et al.The influence of emulsion parameters on physical stability and rheological properties of Pickering emulsions stabilized by hordein nanoparticles[J].Food Hydrocolloids,2020,101:105520.
[40]MCCLEMENTS D J,DECKER E A,WEISS J.Emulsion-based delivery systems for lipophilic bioactive components[J].Journal of Food Science,2007,72(8):R109-R124.
[41]WASHINGTON G E,BRANT D A.Model for the temperature-induced conformational change in xanthan polysaccharide[J].Biomacromolecules,2021,22(11):4691-4700.
[42]张相风.醇法加工对花生蛋白结构和功能特性的影响研究[D].郑州:河南工业大学,2024.ZHANG X F.Study on the structural andfunctional properties of peanut proteins byalcoholicprocessing[D].Zhengzhou:Henan University of Technology,2024.
[43]MAO J X,CUI L J,MENG Z.Stabilization of oil-in-water emulsion gels by pH-induced electrostatic interactions between soybean protein isolate microgel particles and xanthan gum[J].Journal of the American Oil Chemists’ Society,2024,101(11):1287-1298.
[44]XU H,GAO Z W,HUANG M C,et al.Static stability of partially crystalline emulsions stabilized by milk proteins:Effects of κ-carrageenan,λ-carrageenan,ι-carrageenan,and their blends[J].Food Hydrocolloids,2024,147:109387.
[45]DICKINSON E.Hydrocolloids at interfaces and the influence on the properties of dispersed systems[J].Food Hydrocolloids,2003,17(1):25-39.
[46]HUANG L R,YAN Y H,QU L L,et al.Structure,emulsifying and embedding characteristics of soy protein isolate induced by the complexation of carrageenan with different charge groups[J].Food Hydrocolloids,2024,157:110455.
[47]PETRI D F S.Xanthan gum:A versatile biopolymer for biomedical and technological applications[J].Journal of Applied Polymer Science,2015,132(23):42035.
[48]黄云.红外辅助复合酶解制备巴旦木乳及其稳定机制研究[D].无锡:江南大学,2024.HUANG Y.Study on infrared assisted composite enzymatic hydrolysis preparation and stability mechanism of almond-based milk.Wuxi:Jiangnan University,2024.
[49]PETSEV,DIMITER N,et al.Emulsions:Structure,Stability and Interactions[M].Elsevier,2004.
[50]CAI Y J,DENG X L,LIU T X,et al.Effect of xanthan gum on walnut protein/xanthan gum mixtures,interfacial adsorption,and emulsion properties[J].Food Hydrocolloids,2018,79:391-398.