莴苣(Lactuca sativa L.)又名莴笋,隶属于菊科植物,是一种一年生或二年生的蔬菜作物,是多个国家广泛种植的重要经济型蔬菜之一,广泛分布在中国、印度、以色列、泰国、日本及美国等地。其质地脆嫩、色泽翠绿,口感清爽,营养成分丰富,含有大量的莴苣素、维生素、无机盐以及锌、铁等微量元素[1]。此外,莴苣还具有显著的保健作用,包括抗氧化、抗肿瘤和调节血压等功能[2]。与其他果蔬相比,莴苣的外表皮更易发生纤维化,其叶亦较为娇嫩,极易受到机械性损伤,导致其贮藏性能较差,更适用于鲜切加工[3]。鲜切莴苣因其具备新鲜、营养丰富、食用便捷与卫生安全等优点,已成为现代消费者饮食结构中受欢迎的即食蔬菜之一。但去皮、切分等机械损伤会破坏莴苣细胞的膜结构完整性,打破细胞内的活性氧(reactive oxygen species,ROS)生成与清除的动态平衡,致使呼吸过程中产生的ROS不能及时被ROS清除系统迅速代谢,导致ROS积累,最终对组织细胞造成不可逆转的氧化损伤[4]。此外,非生物胁迫还会诱导“伤呼吸”和“伤乙烯”效应的发生,显著增加呼吸速率和乙烯生成,进一步加剧细胞膜脂氧化、ROS富集,破坏膜脂的稳定性,加速细胞衰老和组织褐变[1]。这些生理生化变化直接影响鲜切莴苣的感官品质、营养价值及货架期,成为制约其贮藏与加工品质的关键因素,显著降低了产品的市场商品价值。
肉桂醛主要提取自肉桂、风信子、玫瑰及藿香等植物,在抑制细菌滋生与真菌繁衍方面成效显著[5]。由于其对人体安全、无毒副作用[6],该化合物已获得中国国家食品安全标准[7]及美国食品药品监督管理局(Food and Drug Administration,FDA)的认证,被列为安全的食品添加剂之一,这为其在采后保鲜领域的应用奠定了基础。例如猕猴桃采后容易受到微生物感染,而通过使用肉桂醛对采后猕猴桃进行熏蒸或以其溶液喷洒处理时,便可破坏假单胞菌生物膜形成相关基因,从而有效抑制该病原菌及其他病原微生物的生长,达到延长果实货架期的效果[8]。除直接抑菌作用外,该化合物通过调控活性氧代谢网络发挥抗氧化功能。在“红阳”猕猴桃的采后保鲜研究中,何靖柳等[9]采用肉桂醛溶液处理果实便可使超氧化物歧化酶(superoxide dismutase,SOD)及过氧化物酶(peroxidase,POD)活性维持在较高水平,同时降低其他抗氧化物质的降解速率,使果实的抗氧化能力维持在较高水平。分子生物学研究进一步揭示,肉桂提取物可通过抑制脐橙膜脂过氧化关键酶脂氧合酶活性,提高贮藏稳定性,延缓果实的衰老[10]。此外,在新型保鲜材料开发方面,GUO等[11]构建的肉桂醛/纳米ZnO-羧甲基纤维素复合膜不仅可以使樱桃番茄贮藏期的硬度保持在较高水平,还可以控制其失重率,降低总酸度,从而提高樱桃番茄的整体品质。XIAO等[12]研发的壳聚糖-玉米醇溶蛋白纳米复合膜可以在室温条件下显著延缓芒果果实的黄化、抑制呼吸速率、减少水分和维生素C损失以及降低丙二醛的积累。综上,肉桂醛凭借其卓越的抑菌与抗氧化性能,在新鲜果蔬采后保鲜领域展现出广阔的应用潜力和发展前景。
截至目前,有关植物提取物对鲜切莴苣褐变及活性氧代谢的影响研究中,所使用的抗褐变剂主要有大蒜乙醇提取液[13]、黄连及连翘提取液[14]、竹叶提取物[15]、葡萄籽提取物及松叶精油[16]等,而对于肉桂醛的应用则鲜有报道。因此,本研究以莴苣为实验材料,通过测定褐变度、总酚、类黄酮及活性氧代谢等生理生化指标,多维度系统评价肉桂醛处理对酶促褐变进程的调控效应及其与活性氧代谢的机制,以期为开发鲜切莴苣的褐变控制手段提供理论参考,同时为鲜切果蔬产业可持续发展提供创新性技术支撑。
1 材料与方法
1.1 材料与试剂
供试材料:莴苣购于南昌市经开区农贸市场。挑选外形饱满、大小适中、颜色均匀、表皮洁净、无任何病害症状且表皮破损面积小于5%的新鲜莴苣。
供试试剂:肉桂醛、没食子酸、芦丁等标准品,上海蓝季源叶生物科技有限公司。上海蓝季源叶生物科技有限公司;双氧水、浓硫酸、愈创木酚、聚乙烯吡咯烷酮(polyvinyl pyrrolidone,PVP)、乙二胺四乙酸(ethylenediaminetetraacetic acid,EDTA)等均为分析纯试剂,国药集团化学试剂有限公司。
1.2 仪器与设备
果蔬切片机,杭州拜杰科技有限公司;HWS-12电热恒温水浴锅,上海一恒科仪器有限公司;FA2004B电子天平,上海精科天美科学仪器有限公司;UV-1600PC紫外可见分光光度计,上海美普达仪器有限公司;Centrifuge 5804R高速冷冻离心机,长沙湘锐离心机有限公司;DDS-307A电导率测定仪,上海仪电分析仪器有限公司;IM-F124制冰机,日本San Yo公司;冷冻柜,青岛海尔特种电冰柜有限公司。
1.3 实验方法
1.3.1 样品准备和处理
将挑选过的新鲜莴苣用200 μL/L次氯酸钠溶液浸泡2 min,然后用自来水冲洗。待莴苣表面水分风干后,将莴苣手动去皮,使用锋利的不锈钢刀切成厚度为(4± 1) mm的圆形切片。接着将片状莴苣混合,均匀随机分成4组,分别用蒸馏水(CK)和0.1、0.5、1.0 g/L肉桂醛溶液浸泡处理5 min,在室温下自然风干,置于经紫外线消毒的聚丙烯保鲜盒中(每盒装12片,共12盒/处理组),接着使用透明聚丙烯保鲜膜封膜并分别做好相应标记。在(5±1) ℃、85%~90%相对湿度下贮藏8 d。贮藏期间,分别于2、4、6、8 d取样观察,随后立即用液氮冷冻样品,转移至零下80 ℃超低温环境中保存,为后续生理生化指标的测定及分析提供可靠实验基础。
1.3.2 褐变度的测定
参考刘云芬等[17]的方法,稍作优化。最终测定值以420 nm特征波长下的吸光度值(OD420nm)进行表征。
1.3.3 总酚、类黄酮、醌类物质含量的测定
参照ZHOU等[18]的方法测量总酚含量,并作适当优化。通过没食子酸标准曲线计算总酚含量,结果以mg/kg表示。
参考曹建康等[19]的方法测定类黄酮含量,稍作修改。通过芦丁标准曲线计算总黄酮含量,结果以mg/kg表示。
醌类物质的定量分析采用比色法[20],稍作优化。对照组为2 mL 80% (体积分数)乙醇代替上清液。结果以OD437nm表示。
1.3.4 丙二醛(malondialdehyde,MDA)含量和相对电导率的测定
参照LIU等[21]的方法测定MDA含量,使用硫代巴比妥酸(thiobarbituric acid,TBA)比色法测定,并稍作优化。结果以μmol/g表示,计算如公式(1)所示:
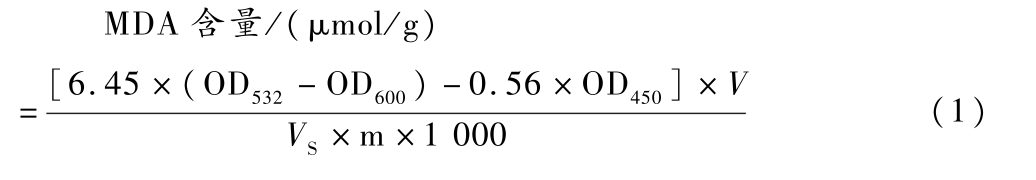
式中:V 为提取液总体积,mL;VS 代表测定时所取样品提取液体积,mL;m 代表样品质量,g。
参照WANG等[22]的方法测定相对电导率,稍作修改。
1.3.5 H2O2含量和超氧阴离子自由基(·O-2)产生速率的测定
参照LIU等[21]的方法测定H2 O2 含量,结果以μmol/g表示。
参照曹建康等[19]的方法测定·O-2含量,最终结果以每克鲜样每分钟生成的·O2- 微摩尔数[μmol/(min·g)]表示。
1.3.6 DPPH自由基、ABTS阳离子自由基和羟自由基(·OH)清除率的测定
准确称取2.0 g待测样品,按1∶10(g∶mL)比例加入68%(体积分数)乙醇水溶液,涡旋振荡30 s使其充分匀浆,接着转移至超声辅助提取系统于50 ℃下处理30 min。混合液经4 ℃低温条件下以12 000 r/min离心20 min,收集上清液待测。
参考谢晓宇等[23]的方法测定DPPH自由基清除率,稍作修改。对照组采用68%乙醇代替上清液,于517 nm处测量光吸收值。
依照李志晓等[24]的方法测定ABTS阳离子自由基、·OH清除率,并作适当优化。以734 nm处样品的光吸收值作为ABTS阳离子自由基清除率计算值,以510 nm处样品的光吸收值作为·OH清除率计算值。
1.3.7 SOD、过氧化氢酶(catalase,CAT)、抗坏血酸过氧化物酶(ascorbate peroxidase,APX)、谷胱甘肽还原酶(glutathione reductase,GR)活性的测定
准确称取1.0 g样品,按1∶8(g∶mL)比例加入预冷提取缓冲液(0.1 mol/L磷酸盐缓冲液,pH 7.8,含0.1 mol/L EDTA及50 g/L的PVP),立即进行涡旋振荡30 s使其充分匀浆。混合体系于冰浴条件下静置浸提10 min后,转移至4 ℃低温离心机以12 000 r/min离心20 min,最终收集上清液进行检测。
参照曹建康等[19]的方法测定SOD、CAT、APX、GR活性,酶活力单位(U)定义为每分钟吸光值变化0.01所对应的酶量,最终结果以U/g表示。
1.3.8 多酚氧化酶(polyphenol oxidase,PPO)、POD、苯丙氨酸解氨酶(phenylalanine ammonia-lyase,PAL)活性的测定
准确称取1.0 g鲜样,按1∶8(g∶mL)比例加入预冷提取缓冲液(0.1 mol/L磷酸盐缓冲液,pH 7.8,含0.1 mol/L EDTA及50 g/L的PVP),立即涡旋振荡30 s实现组织破碎。混合体系经4 ℃低温离心(12 000 r/min,20 min)后获取澄清酶提取液。
参照曹建康等[19]的方法测定PPO、POD、PAL活性。酶活力单位(U)定义为每分钟吸光值变化0.01所对应的酶量,最终结果以U/g表示。
1.3.9 抗坏血酸(ascorbic acid,AsA)含量的测定
参照LIN等[25]的方法,并作适当优化,于534 nm处测定吸光度。最终通过抗坏血酸标准曲线计算AsA含量,结果以mg/100 g表示。
1.4 数据分析
所有指标测定均重复3次,采用Microsoft Excel 2019软件对数据进行处理和显著性分析,采用Origin PRO 2021软件作图。
2 结果与分析
2.1 肉桂醛对鲜切莴苣外观品质的影响
外观品质是影响鲜切果蔬商品价值的直接指标。由图1可知,CK组和0.1 g/L肉桂醛处理组于4 d时便出现明显的褐变,并伴随着组织失水、红斑等现象出现,其商品价值大打折扣。随着贮藏时间的推移,8 d时CK组已完全褐变且水分流失严重,质地干软,丧失商品价值。0.1 g/L肉桂醛处理组较CK组褐变程度有所下降,但质地偏干,水分流失较严重,虽未出现红斑,在很大程度上也制约其商品价值。0.5 g/L与1.0 g/L肉桂醛处理组则分别在6 d与8 d时才出现轻微褐变现象。贮藏时间在8 d时,0.5 g/L肉桂醛处理组出现了组织失水、质地变软的现象,而1.0 g/L肉桂醛处理组则能较好保持鲜切莴苣原有外观品质。

图1 肉桂醛处理对鲜切莴苣外观品质的影响
Fig.1 Effects of cinnamaldehyde treatment on the appearance quality of fresh-cut lettuce
2.2 肉桂醛对鲜切莴苣褐变度的影响
褐变度是评价鲜切果蔬酶促褐变程度的重要指标,其数值越高表明酚类物质氧化聚合形成的褐色产物积累越显著,直接反映组织劣变程度[25]。由图2可知,随着贮藏时间的延长,处理组和对照组褐变度都呈上升趋势,其中1.0 g/L肉桂醛处理组,褐变度始终低于CK组,且在贮藏第8天呈极显著差异(P <0.01)。这与外观品质结果保持一致。
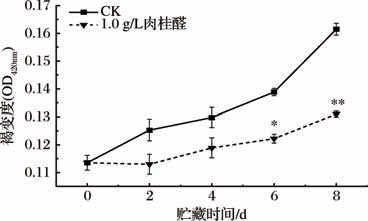
图2 肉桂醛处理对鲜切莴苣褐变度的影响
Fig.2 Effects of cinnamaldehyde treatment on the browning degree of fresh-cut lettuce
注:图中星号表示同一贮藏期2组之间的差异水平(∗P <0.05,∗∗P <0.01)(下同)。
2.3 肉桂醛对鲜切莴苣总酚、类黄酮及醌类物质含量的影响
酶促褐变作为果蔬采后品质劣变的重要机制,其本质是酚类代谢途径的异常激活过程。在完整细胞系统中,酚类底物与PPO受区室化分离调控,但当组织遭受机械损伤或环境胁迫时,细胞膜系统完整性破坏引发酶与底物接触,在酚代谢酶的作用下发生氧化反应生成醌类物质,经历多步非酶促聚合反应后形成黑色素聚合物,最终在表皮组织形成特征性褐变斑块,使果蔬呈现褐色或黑色[26]。
由图3-A可知,鲜切莴苣总酚含量在贮藏期呈现上升趋势,在贮藏时间2~8 d,1.0 g/L肉桂醛处理组与对照组,总酚含量呈极显著差异(P <0.01)。由图3-B可知,鲜切莴苣类黄酮含量在贮藏期间的增长趋势与总酚类似,CK组的类黄酮含量均高于1.0 g/L肉桂醛处理组,在贮藏6~8 d处理组和对照组,类黄酮含量呈极显著差异(P <0.01)。
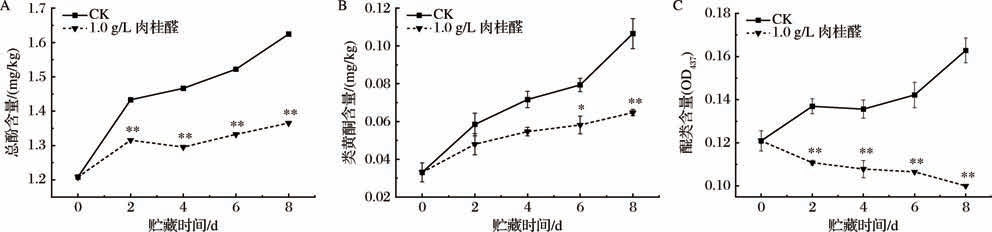
图3 肉桂醛处理对鲜切莴苣总酚含量、类黄酮含量及醌类物质含量的影响
Fig.3 Effects of cinnamaldehyde treatment on the total phenol content,flavonoid content,and quinone content of fresh-cut lettuce
A-总酚含量;B-类黄酮含量;C-醌类物质含量
机械损伤引发的信号转导网络激活会显著上调苯丙烷代谢关键节点酶活性,驱动酚类(如绿原酸)和类黄酮(如芦丁)等次生代谢产物的生物合成通量增加,加速褐变进程[27]。由此说明,肉桂醛处理在一定程度上可以降低鲜切莴苣中总酚、类黄酮含量的积累,延缓褐变。
结合图3-C可知,贮藏期间,CK组与1.0 g/L肉桂醛处理组的醌类物质含量随贮藏时间的延长呈现相反的趋势,且从贮藏2 d开始,1.0 g/L肉桂醛处理组醌类物质含量与贮藏时间呈负相关,而肉桂醛处理组始终显著低于CK组(P <0.01)。由此可知,肉桂醛处理可以有效降低醌类物质的积累,推测是由于肉桂醛降低了酚代谢酶的活性,使醌类物质含量降低,无法进一步氧化、聚合形成黑色素。
2.4 肉桂醛对鲜切莴苣相对电导率及MDA含量的影响
相对电导率又被称为细胞膜透性,是评估细胞膜完整性的关键指标,其值升高表明膜透性增大,离子外泄加剧,与氧化损伤导致的膜脂降解密切相关。由图4-A可知,贮藏期间,CK组的相对电导率整体上呈逐渐上升的趋势,而1.0 g/L肉桂醛处理组增长平缓,无明显变化,且始终低于CK组,达极显著差异(P <0.01)。MDA是膜脂过氧化的终产物,其含量直接反映细胞膜受活性氧攻击的损伤程度,MDA积累会破坏膜系统完整性并加剧褐变进程。结合图4-B可知,在贮藏期间,MDA含量呈现先下降后上升的变化趋势。其中,1.0 g/L肉桂醛处理组在整个贮藏期间的MDA含量均显著低于CK组。综上,1.0 g/L肉桂醛可以有效抑制细胞膜透性的增加并减少MDA含量的积累,从而维持膜脂稳定性,延缓细胞区室化功能丧失,为保持鲜切莴苣的品质提供了结构基础。
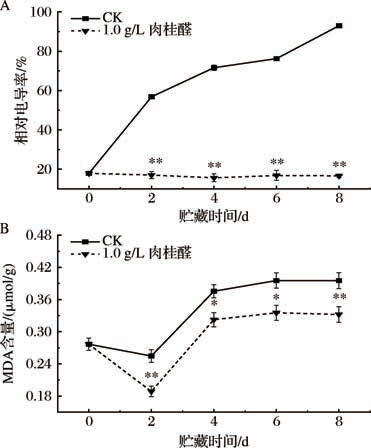
图4 肉桂醛处理对鲜切莴苣相对电导率、MDA含量的影响
Fig.4 Effects of cinnamaldehyde treatment on the relative electrical conductivity and MDA content of fresh-cut lettuce
A-相对电导率;B-MDA含量
2.5 肉桂醛处理对鲜切莴苣PPO及POD活性的影响
PPO作为酶促褐变的关键调控因子,如前所述,在有氧条件中,该酶可以利用氧气催化酚类底物生成醌类,而醌类物质又可经历多阶段非酶促联合反应形成黑色聚合物,最终导致果蔬褐变[25]。由图5-A可知,在贮藏期间,PPO活性整体呈逐渐上升的趋势,而1.0 g/L肉桂醛处理组PPO活性在贮藏4 d时便显著低于CK组(P <0.05)。当贮藏6~8 d时,1.0 g/L肉桂醛处理组与CK组呈极显著差异(P <0.01),说明肉桂醛可以有效抑制PPO活性的上升,从而显著延缓褐变发生。
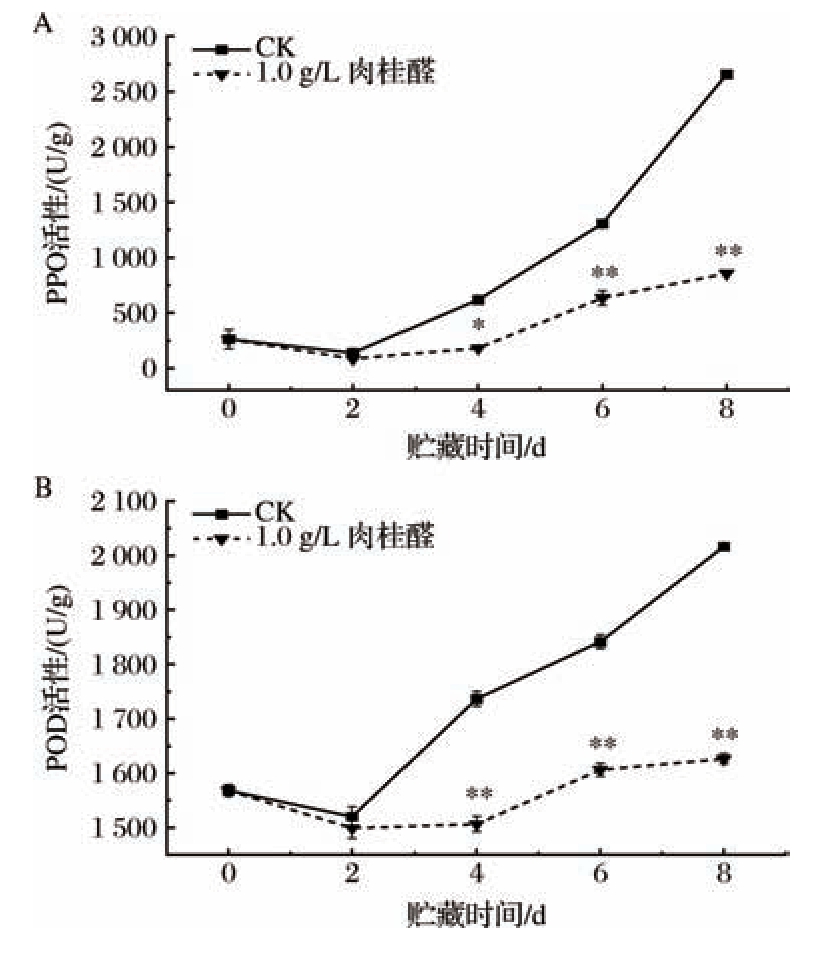
图5 肉桂醛处理对鲜切莴苣PPO及POD活性的影响
Fig.5 Effects of cinnamaldehyde treatment on the activities of PPO and POD in fresh-cut lettuce
A-PPO;B-POD
POD能够直接利用醌类化合物作为底物进行氧化反应,但需要在底物充足的条件下氧化反应才能发生,故POD在褐变中的实际影响受到底物种类及反应条件的限制,其作用强度通常低于PPO。由图5-B可知,贮藏2 d之后,POD活性逐渐上升,而1.0 g/L肉桂醛处理组的POD活性始终显著低于CK组(P <0.01)。说明肉桂醛处理可以有效抑制POD活性的增加,延缓醌类的氧化,减少莴苣中黑色素的积累。
2.6 肉桂醛处理对鲜切莴苣H2O2含量及·O2- 产生速率的影响
ROS主要包括H2O2、·O2-,机械损伤引发的氧化应激会导致细胞抗氧化防御体系活性失衡,导致H2O2、·O2- 等活性氧在细胞内积累进而引发氧化损伤[28]。由图6-A可知,整个贮藏过程中,CK组H2 O2含量均高于1.0 g/L肉桂醛处理组,且呈极显著差异(P <0.01)。由图6-B可知,贮藏期内,·O2- 产生速率与H2O2产生速率基本一致,均呈先上升后回落的趋势。在贮藏时间达4 d时,CK组和1.0 g/L肉桂醛处理组的·O2- 产生速率均达到峰值,之后便持续降低,而1.0 g/L肉桂醛处理组始终低于CK组(P <0.01)。
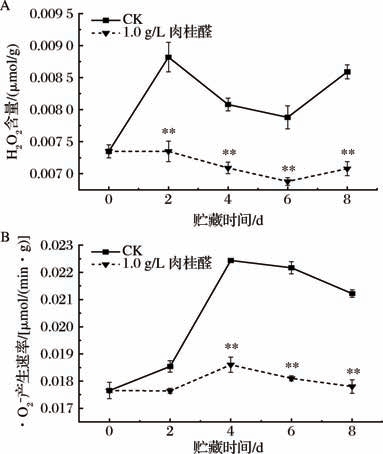
图6 肉桂醛处理对鲜切莴苣H2 O2 含量及·O2
-产生速率的影响
Fig.6 Effects of cinnamaldehyde treatment on H2 O2 content and ·O2- production rate in fresh-cut lettuce
A-H2 O2 含量;B-·O -2 产生速率
由此可知,肉桂醛处理可以显著减少H2 O2 的积累并减缓·O2- 产生速率的上升,降低因切割导致的ROS积累对莴苣组织细胞的伤害。
2.7 肉桂醛处理对鲜切莴苣DPPH自由基、ABTS阳离子自由基及·OH清除率的影响
鲜切果蔬体外抗氧化效能评估体系通常以DPPH自由基、ABTS阳离子自由基及·OH的清除率来反映样品供氢能力,进而得出果蔬清除自由基的总体能力[29]。根据图7-A分析可知,贮藏初期至中期(2~6 d)之前,CK组的DPPH自由基清除率呈下降趋势,直至8 d时才缓慢回升,1.0 g/L肉桂醛处理组在贮藏4 d前,DPPH自由基清除率逐渐增加,之后便逐渐降低,且始终高于CK组。在贮藏2 d后,处理组和CK组之间呈极其显著差异(P <0.01)。由图7-B、图7-C可知,贮藏期内,CK组与1.0 g/L肉桂醛处理组的ABTS阳离子自由基及·OH清除效率动态变化趋势相似,但处理组的ABTS阳离子自由基、·OH清除率在整个贮藏期内始终维持较高活性水平。贮藏中期(4 d),1.0 g/L肉桂醛处理组的ABTS阳离子自由基清除率为37.74% (P <0.05),同期·OH清除率为76.52%,与CK组存在着极其显著的差异(P <0.01)。
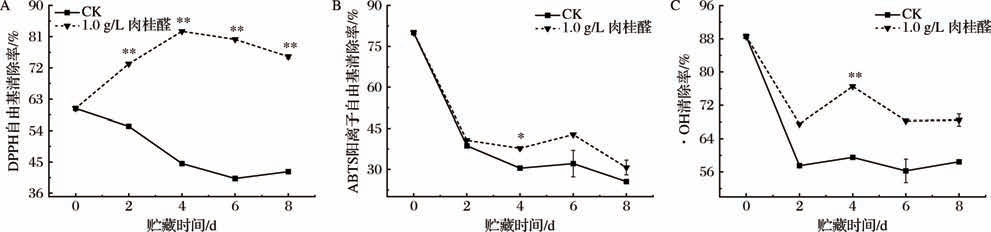
图7 肉桂醛处理对鲜切莴苣DPPH自由基、ABTS阳离子自由基及·OH清除率的影响
Fig.7 Effects of cinnamaldehyde treatment on the scavenging rates of DPPH radical,ABTS cationic radical,and ·OH in fresh-cut lettuce
A-DPPH自由基;B-ABTS阳离子自由基;C-·OH
综上可知,肉桂醛处理在一定程度上可以提高DPPH自由基、ABTS阳离子自由基及·OH的清除率,增强莴苣中的抗氧化物捕获自由基的能力以及对自由基的淬灭作用,从而提高莴苣的抗氧化能力,延缓褐变的发生,这与周晓斌[30]的研究结果相似。
2.8 肉桂醛处理对鲜切莴苣SOD及CAT活性的影响
SOD作为植物抗氧化系统的核心成员,与CAT、APX等构成协同作用网络。SOD作为一种自由基清除剂,可以将·O2- 歧化为H2 O2,后者由CAT再分解转化生成水分子与氧分子,共同维持细胞内ROS稳态[31]。据图8-A分析可知,贮藏期间SOD活性呈现时间依赖性激活模式,而1.0 g/L肉桂醛处理组的SOD活性始终高于CK组,表现出持续酶活优势。在贮藏8 d时,1.0 g/L肉桂醛处理组较CK组呈极显著差异(P <0.01)。由图8-B可知,贮藏期内,处理组的CAT活性始终优于对照组,且均在贮藏6 d时达最大值,而后下降。处理组与CK组的CAT活性在第2天和第8天呈极显著差异(P <0.01)。
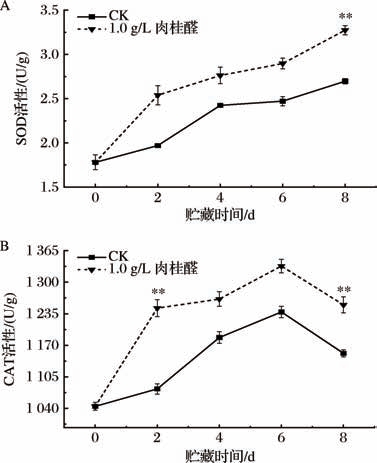
图8 肉桂醛处理对鲜切莴苣SOD及CAT活性的影响
Fig.8 Effects of cinnamaldehyde treatment on the activities of SOD and CAT in fresh-cut lettuce
A-SOD;B-CAT
综上,肉桂醛处理在一定程度上可以提高SOD及CAT的活性,增强鲜切莴苣的抗氧化能力,清除组织细胞内的ROS,维持ROS代谢平衡。
2.9 肉桂醛处理对鲜切莴苣APX及GR活性的影响
APX与GR是抗坏血酸-谷胱甘肽(AsA-GSH)循环中重要的活性氧清除酶,二者在果蔬中协同分解H2O2,以延缓因机械损伤引发的腐败过程,抑制褐变和组织细胞衰老,从而维持果蔬品质和延长保鲜期[32]。结合图9-A分析可知,整个贮藏期内,CK组与1.0 g/L肉桂醛处理组的APX活性呈逐渐下降的趋势,且CK组的APX活性下降幅度更大。在贮藏4 d之后,与1.0 g/L肉桂醛处理组相比,均呈现显著差异(P <0.05)。在贮藏6 d时,1.0 g/L肉桂醛处理组的APX活性为16.27 U/g,较CK显著提高了85.25%(P <0.01)。由图9-B可知,贮藏期间,GR活性呈现出先上升后回落的趋势,贮藏中期(6 d),1.0 g/L肉桂醛处理组的GR活性持续上升至最大值32.07 U/g,与CK组存在极显著差异(P <0.01)。
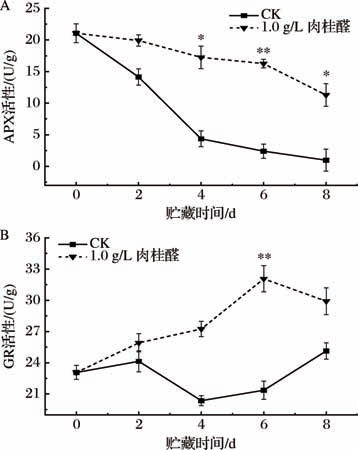
图9 肉桂醛处理对鲜切莴苣APX及GR活性的影响
Fig.9 Effects of cinnamaldehyde treatment on the activities of APX and GR in fresh-cut lettuce
A-APX;B-GR
由此说明,肉桂醛处理可以有效延缓鲜切莴苣APX及GR活性的降低,使二者的协同作用强度不会因非生物胁迫而迅速下降,从而维持莴苣组织细胞对ROS的清除能力,延缓品质劣变并延长贮藏期。
2.10 肉桂醛处理对鲜切莴苣AsA及GSH含量的影响
鲜切果蔬内源性抗氧化代谢网络研究揭示,AsA-GSH循环系统作为非酶促抗氧化防御体系,又称为ROS非酶清除系统。该系统主要通过淬灭活性氧、保护膜系统及修复损伤三方面维持细胞氧化还原稳态,从而延缓果蔬细胞衰老、抵抗逆境胁迫[31]。由图10-A可知,贮藏期间,CK组与1.0 g/L肉桂醛处理组的AsA含量变化趋势基本一致,均为先减少后增加,但1.0 g/L肉桂醛处理组始终高于CK组。在贮藏4~6 d内,1.0 g/L肉桂醛处理组的AsA含量显著高于CK组(P <0.05)。再结合图10-B分析可知,在整个贮藏期内,GSH含量均呈降低之势,猜测这可能是由于贮藏时间延长,莴苣组织逐渐衰老而导致的,但在整个贮藏期间,1.0 g/L肉桂醛处理组的GSH含量始终高于CK组,且贮藏2 d之后,与CK组的差异极其显著(P <0.01)。
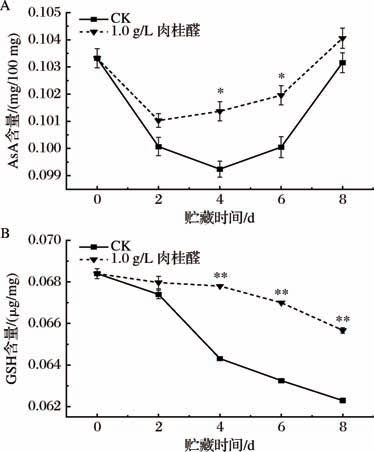
图10 肉桂醛处理对鲜切莴苣AsA及GSH含量的影响
Fig.10 Effects of cinnamaldehyde treatment on the contents of AsA and GSH in fresh-cut lettuce
A-AsA;B-GSH
综上,肉桂醛处理可以有效提高莴苣中AsA含量并延缓GSH含量的下降,增强ROS非酶清除系统,提高莴苣清除MDA和对抗自由基的能力,延缓衰老并保持品质。
2.11 肉桂醛处理对鲜切莴苣PAL活性的影响
PAL是苯丙烷类代谢通路的关键调控节点酶,通过生物催化脱氨作用将L-苯丙氨酸转化为反式肉桂酸,而后者又可作为合成酚类化合物(如绿原酸)的底物,为酶促褐变提供物质基础[33]。由图11可知,贮藏期间,1.0 g/L肉桂醛处理组的PAL活性始终高于CK组,且在贮藏8 d时提高到了17.27 U/g,是CK组的10.67倍(P <0.01),由此说明肉桂醛处理并不能抑制PAL活性,反而使其活性提高,原因可能是肉桂醛虽抑制了PPO及POD活性,使酚类物质氧化为醌的速率降低,但这会导致酚类物质的积累,而这种积累则通过反馈调节机制上调了PAL活性[34],以维持莴苣的代谢平衡。
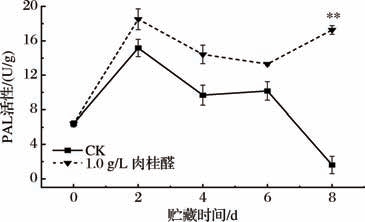
图11 肉桂醛处理对鲜切莴苣PAL活性的影响
Fig.11 Effects of cinnamaldehyde treatment on the activity of PAL in fresh-cut lettuce
3 结论与讨论
李静[35]研究表明,ROS与鲜切莴苣的褐变过程密切相关。莴苣在经过切割处理后,体内会迅速积累大量的ROS,同时一些与ROS代谢相关的酶类如SOD、APX和CAT的活性也会发生显著变化。在贮藏4 d内,对照组SOD活性在2 d时达到顶峰;CAT活性则在1 d时便达到峰值;而APX活性则一直处于下降状态。使用短波紫外线(ultraviolet-C,UV-C)处理后,一定程度上诱导SOD、CAT活性的升高,抑制APX活性的下降,削弱了ROS对莴苣组织的伤害。师聪等[36]的研究表明,外源褪黑素能够有效降低鲜切莴苣中H2O2含量的积累和·O-2 的生成速率,从而延缓其衰老过程。此外,已有研究证明,γ-氨基丁酸(γ-aminobutyric acid,GABA)作为新型采后处理剂,同样能够通过多靶点调控延缓鲜切莴苣的褐变,其作用机制主要通过调控ROS水平和膜脂代谢实现[37]。
本研究通过分析不同浓度肉桂醛处理对鲜切莴苣褐变及ROS代谢的影响,发现1.0 g/L肉桂醛处理可显著抑制褐变度的上升,并延缓总酚、类黄酮及醌类物质的积累,这与张林青等[13]的关于植物精油通过调控酚代谢酶活性抑制褐变的结论一致。同时,肉桂醛处理显著降低了H2O2 含量和·O-2 产生速率,表明其可通过抑制ROS的生成缓解氧化胁迫对细胞膜的损伤,这一结果与RU等[37]关于GABA调控ROS代谢的机制相似。但本研究进一步发现,肉桂醛处理可显著提高SOD和CAT的活性,并通过增强APX、GR活性及AsA再生效率、GSH含量以维持ROS清除系统的动态平衡,从而使细胞MDA积累量下降,最终实现延缓膜脂过氧化的效果。值得注意的是,尽管肉桂醛处理显著抑制了PPO和POD活性,却导致PAL活性升高至对照组的10.67倍。这一矛盾现象可能与酚类物质反馈调节有关,PPO活性被抑制后,酚类氧化速率降低,导致底物积累,从而激活苯丙烷代谢途径以维持代谢稳态[34]。
综上所述,肉桂醛处理通过抑制酚类氧化、增强ROS清除能力及维持细胞膜完整性,有效延缓了鲜切莴苣的褐变与衰老进程。然而,PAL活性的异常升高提示需进一步探究酚类代谢的反馈调控网络,并结合转录组或蛋白组学解析肉桂醛对苯丙烷途径的分子调控机制。未来研究可优化肉桂醛与其他保鲜技术,如与气调包装或UV-C技术协同应用,以提升其工业化应用潜力,为鲜切果蔬绿色保鲜技术的开发提供新思路。
[1]杨晓哲,胡文忠,姜爱丽,等.鲜切莴苣生理生化变化及其保鲜技术的研究进展[J].食品与发酵工业,2018,44(2):278-283.YANG X Z,HU W Z,JIANG A L,et al.Research progress on physiological and biochemical changes of fresh-cut lettuce and its preservation technology [ J].Food and Fermentation Industries,2018,44(2):278-283.
[2]李静,季悦,李美琳,等.切割方式对鲜切莴苣品质及抗氧化活性的影响[J].食品科学,2018,39(3):268-273.LI J,JI Y,LI M L,et al.Effects of cutting methods on quality and antioxidant activity of fresh-cut lettuce[J].Food Science,2018,39(3):268-273.
[3]祝竞芳,汤静,游万里,等.氯化钙处理对鲜切莴苣品质及γ-氨基丁酸代谢的影响[J].食品科学,2022,43(7):174-181.ZHU J F,TANG J,YOU W L,et al.Effects of calcium chloride treatment on quality and γ-aminobutyric acid metabolism of fresh-cut lettuce[J].Food Science,2022,43(7):174-181.
[4]NADARAJAH K K.ROS homeostasis in abiotic stress tolerance in plants[J].International Journal of Molecular Sciences,2020,21(15):5208.
[5]BLAKEMORE W M,THOMPSON H C Jr.Trace analysis of cinnamaldehyde in animal feed,human urine,and wastewater by electron capture gas chromatography[J].Journal of Agricultural and Food Chemistry,1983,31(5):1047-1052.
[6]孟康.肉桂醛对香菇采后品质及膜脂代谢调控研究[D].南京:南京农业大学,2021.MENG K.Study on the regulation of cinnamaldehyde on postharvest quality and membrane lipid metabolism of Lentinula edodes [D].Nanjing:Nanjing Agricultural University,2021.
[7]SHREAZ S,WANI W A,BEHBEHANI J M,et al.Cinnamaldehyde and its derivatives,a novel class of antifungal agents[J].Fitoterapia,2016,112:116-131.
[8]MALHEIRO J F,MAILLARD J Y,BORGES F,et al.Evaluation of cinnamaldehyde and cinnamic acid derivatives in microbial growth control[J].International Biodeterioration &Biodegradation,2019,141:71-78.
[9]何靖柳,李玉,杜小琴,等.肉桂精油处理对低温贮藏期间‘红阳’猕猴桃抗氧化活性的影响[J].现代食品科技,2016,32(3):211-217.HE J L,LI Y,DU X Q,et al.Effects of cinnamon essential oil on the antioxidant activity of ‘red sun’ kiwifruits during cold storage[J].Modern Food Science and Technology,2016,32(3):211-217.
[10]万春鹏,陈楚英,陈明,等.肉桂提取物对赣南脐橙的保鲜效果[J].食品工业科技,2015,36(17):317-321.WAN C P,CHEN C Y,CHEN M,et al.Effect of Cinnamomum cassia extractions on fresh-keeping of ‘Newhall’Navel orange[J].Science and Technology of Food Industry,2015,36(17):317-321.
[11]GUO X G,CHEN B R,WU X L,et al.Utilization of cinnamaldehyde and zinc oxide nanoparticles in a carboxymethylcellulosebased composite coating to improve the postharvest quality of cherry tomatoes[J].International Journal of Biological Macromolecules,2020,160:175-182.
[12]XIAO J Q,GU C Q,ZHU D X,et al.Development and characterization of an edible chitosan/zein-cinnamaldehyde nano-cellulose composite film and its effects on mango quality during storage[J].LWT,2021,140:110809.
[13]张林青,朱露露.大蒜乙醇提取液对生菜贮藏效果的影响[J].北方园艺,2016(11):135-137.ZHANG L Q,ZHU L L.Effect of garlic alcohol extract on lettuce storage[J].Northern Horticulture,2016(11):135-137.
[14]陈洲,王婷婷,姚颖斐,等.黄连、连翘提取物对鲜切莴苣保鲜效果的研究[J].食品工业,2013,34(11):180-183.CHEN Z,WANG T T,YAO Y F,et al.Research on the preservation effect of Coptis chinensis and Forsythia suspensa on fresh-cut lettuce[J].The Food Industry,2013,34(11):180-183.
[15]李铭桐,张增芹,李敏,等.不同保鲜剂处理对鲜切生菜贮藏品质的影响[J].北方园艺,2016(18):139-142.LI M T,ZHANG Z Q,LI M,et al.Effect of different preservatives and storage temperature on the quality of fresh-cut lettuce[J].Northern Horticulture,2016(18):139-142.
[16]KIM J H,KWON K H,OH S W.Effects of malic acid or/and grapefruit seed extract for the inactivation of common food pathogens on fresh-cut lettuce[J].Food Science and Biotechnology,2016,25(6):1801-1804.
[17]刘云芬,廖玲燕,段振华,等.不同处理对鲜切莴苣褐变及贮藏品质的影响[J].保鲜与加工,2020,20(4):15-20.LIU Y F,LIAO L Y,DUAN Z H,et al.Effects of different treatments on browning and storage quality of fresh-cut lettuce[J].Storage and Process,2020,20(4):15-20.
[18]ZHOU F H,XU D Y,LIU C H,et al.Ascorbic acid treatment inhibits wound healing of fresh-cut potato strips by controlling phenylpropanoid metabolism[J].Postharvest Biology and Technology,2021,181:111644.
[19]曹建康,姜微波,赵玉梅.果蔬采后生理生化实验指导[M].北京:中国轻工业出版社,2007.CAO J K,JIANG W B,ZHAO Y M.Guidance of Physiological and Biochemical Experiments on Postharvest Fruits and Vegetables[M].Beijing:China Light Industry Press,2007.
[20]李维嘉,王志强,许泽群,等.分光光度法测定灵芝孢子油中总三萜的含量[J].食品研究与开发,2019,49(17):165-170.LI W J,WANG Z Q,XU Z Q,et al.Determination of total triterpenoids in Ganoderma lucidum spore oil by spectrophotometry[J].Food Research and Development,2019,49(17):165-170.
[21]LIU Y F,LIU Y,CHEN Q M,et al.Methyl jasmonate treatment alleviates chilling injury and improves antioxidant system of okra pod during cold storage[J].Food Science &Nutrition,2023,11(4):2049-2060.
[22]WANG D,CHEN Q Y,CHEN W W,et al.Melatonin treatment maintains quality and delays lignification in loquat fruit during cold storage[J].Scientia Horticulturae,2021,284:110126
[23]谢晓宇,张飞,石洁,等.预冷处理结合低温贮藏对西兰花贮藏品质的影响[J].食品工业科技,2021,42(7):302-310.XIE X Y,ZHANG F,SHI J,et al.Effect of pre-cooling treatment and low temperature storage on storage quality of broccoli[J].Science and Technology of Food Industry,2021,42(7):302-310.
[24]李志晓,金青哲,叶小飞,等.精炼过程中油茶籽油活性成分和抗氧化性的变化[J].中国油脂,2015,40(8):1-5.LI Z X,JIN Q Z,YE X F,et al.Changes of bioactive constituents and antioxidant activity of oil-tea Camellia seed oil during refining[J].China Oils and Fats,2015,40(8):1-5.
[25]LIN D S,SHUAI L,XU X L,et al.Salicylic acid inhibition on browning of fresh-cut taro by regulating phenolic compounds and active oxygen metabolism[J].LWT,2024,206:116591.
[26]TILLEY A,MCHENRY M P,MCHENRY J A,et al.Enzymatic browning:The role of substrates in polyphenol oxidase mediated browning[J].Current Research in Food Science,2023,7:100623.
[27]CAI C,XU C J,LI X,et al.Accumulation of lignin in relation to change in activities of lignification enzymes in loquat fruit flesh after harvest[J].Postharvest Biology &Technology,2006,40(2):163-169.
[28]TAN Y X,WANG X W,LI L,et al.Postharvest combined chitosan and melatonin treatment maintain antioxidant capacity and cell membrane integrity of fresh-cut broccoli by inducing reactive oxygen species scavenging system[J].LWT,2025,220:117572.
[29]ALMUHAYAWI M S,HASSAN A H A,ABDEL-MAWGOUD M,et al.Laser light as a promising approach to improve the nutritional value,antioxidant capacity and anti-inflammatory activity of flavonoid-rich buckwheat sprouts [ J].Food Chemistry,2021,345:128788.
[30]周晓斌.控释型肉桂精油复合膜的制备及其在樱桃番茄保鲜中的应用研究[D].长春:吉林大学,2024.ZHOU X B.Preparation of controlled-release cinnamon essential oil composite films and their application in the preservation of cherry tomatoes[D].Changchun:Jilin University,2024.
[31]SHUAI L,WANG M,LIAO L Y,et al.Trisodium phosphate inhibits the shrinkage of passion fruit by suppressing ROS accumulation and mitigating oxidative damage [ J].LWT,2025,218:117480.
[32]MEITHA K,PRAMESTI Y,SUHANDONO S.Reactive oxygen species and antioxidants in postharvest vegetables and fruits[J].International Journal of Food Science,2020(1):8817778.
[33]XU D D,DENG Y Z,XI P G,et al.Fulvic acid-induced disease resistance to Botrytis cinerea in table grapes may be mediated by regulating phenylpropanoid metabolism [ J].Food Chemistry,2019,286:226-233.
[34]ZHANG X B,LIU C J.Multifaceted regulations of gateway enzyme phenylalanine ammonia-lyase in the biosynthesis of phenylpropanoids[J].Molecular Plant,2015,8(1):17-27.
[35]李静.切割方式和UV-C处理对鲜切莴苣品质及抗氧化活性的影响[D].南京:南京农业大学,2017.LI J.Effects of cutting methods and UV-C treatment on the quality and antioxidant activity of fresh-cut lettuce[D].Nanjing:Nanjing Agricultural University,2017.
[36]师聪,刘大豪,沈苏婉,等.外源褪黑素处理对鲜切莴苣品质与活性氧代谢的影响[J].北方园艺,2023(19):84-91.SHI C,LIU D H,SHEN S W,et al.Effects of exogenous melatonin treatment on quality and reactive oxygen species metabolism of fresh-cut lettuce[J].Northern Horticulture,2023(19):84-91.
[37]RU X Y,YOU W L,ZHANG J L,et al.γ-aminobutyric acid treatment inhibits browning and promotes storage quality by regulating reactive oxygen species and membrane lipid metabolism in fresh-cut stem lettuce[J].Food Chemistry,2024,459:140420.