中国白酒是世界上最古老的蒸馏酒之一,已有数千年的历史。其中,浓香型白酒因其香味浓郁,口感柔和甘甜,余味持久,深受消费者喜爱,目前占整个白酒市场的70%以上[1]。中高温大曲是浓香型白酒生产的主要糖化发酵剂,在发酵过程中起着重要作用,一方面,它作为白酒酿造原料提供发酵基质;另一方面,大曲提供发酵动力,在整个发酵过程中,各种微生物从环境和原料中逐渐引入大曲,形成了一个复杂的、多功能的微生物群落,产生各种酶和化合物,从而赋予白酒独特的风味[2]。因此,对中高温大曲发酵过程的研究很有必要。
理化参数是评价大曲质量的重要指标。长期以来,对大曲的研究主要以温度、酸度、水分、糖化力、液化力等理化指标为主[3-4]。目前,结合理化参数对中高温大曲中微生物群落演替及其环境驱动因素的研究越来越多。MAO等[5]在研究细菌多样性与理化指标的关联性时发现芽孢杆菌属Bacillus,泛菌属Pantoea 和片球菌属Pediococcus 是中高温大曲的主要微生物,与大曲的酸度、纤维素酶活性和水分密切相关。LEI等[6]发现中高温大曲的酸度偏高与乳酸杆菌属Lactobacillus、魏斯氏菌属Weissella 和Bacillus 息息相关。孙亮霞等[7]通过冗余分析发现一级中高温大曲中Bacillus 与酸度、酯化力及蛋白酶活性呈正相关。刘慧等[8]发现影响中高温大曲的关键微生物是根霉Rhizopus、根毛霉Rhizomucor、Weissella、Lactobacillus,与糖化力、液化力等呈正相关。这些研究都主要集中在微生物多样性分析上,缺乏对特定功能菌属的筛菌验证与分析,同时对于大曲发酵过程中的深入研究也较为有限。
本研究通过对中高温大曲发酵过程中6个样品的理化指标及高通量测序结果进行分析,确定功能菌属后,进一步探究中高温大曲发酵过程中理化指标与功能菌之间的关联性,对优化中高温大曲传统固态发酵条件、提升大曲质量具有重要实践价值。
1 材料与方法
1.1 材料与试剂
从四川水井坊有限公司采集发酵过程的中高温大曲样品。在大曲发酵1 d(发酵开始)、4 d(升温中期)、10 d(进入顶温期)、13 d(顶温期结束)、19 d(降温中期)、25 d(发酵结束),在同一发酵室的大曲堆上、中、下3层不同位置随机抽取大曲砖,粉碎成粉,充分混合,将同一发酵时间的样品混合均匀,一共采集6个大曲样品。每个样品分为2份,-20 ℃保存用于理化指标测定,-80 ℃保存用于高通量测序。
散曲培养基:小麦和麸皮按照4 ∶1的质量比混匀,加水控制最终水分含量为40%,混合均匀,装入30 g湿麸皮于500 mL锥形瓶中,121 ℃灭菌20 min。
1.2 仪器与设备
7890B气相色谱(gaschromatography,GC)仪,美国安捷伦科技公司;YXQ-75SII高压蒸汽灭菌锅,上海博讯实业有限公司;303-0AB电热恒温培养箱,天津赛得利实验分析以期制造公司;CF1524R高速冷冻型微量离心机,美国赛洛捷克有限公司;DZF-0B真空干燥箱,上海跃进医疗器械有限公司;LPH-A实验室pH计,北京兰杰柯科技有限公司。
1.3 实验方法
1.3.1 大曲发酵过程理化指标测定
测定的理化指标包括温度、水分、酸度、糖化力、液化力、酯化力、发酵力。温度通过插入温度计在发酵室内大曲中心来测定。水分含量通过重量法测定,在105 ℃下烘干4 h。酸度通过0.1 mol/L NaOH滴定测定,滴定终点为pH 8.2。糖化力、液化力、酯化力、发酵力参照QB/T 4257—2011《酿酒大曲通用分析方法》测定。每个指标做3次重复实验取平均值。
1.3.2 大曲发酵过程微生物多样性测定
根据E.Z.N.A.®土壤DNA试剂盒(Omega Biotek,Norcross,GA,U.S.)说明书进行大曲微生物群落总DNA提取。使用通用引物338F/806R(5′-ACTCCTACGGGAGGCAGCAGAG-3′/5′-GGACTACHVGGTWTCTAAT-3′)扩增细菌16S rRNA基因的V3~V4可变 区,ITS1F/2043R(5′-CTTGGTCATTAGGAAGA-3′/5′-GCTGCGTTCTTCATCGATGC-3′)扩增真菌rRNA基因的ITS1区,利用Illumina公司的Miseq PE250测序平台,最后交由上海凌恩科技有限公司进行测序。
1.3.3 大曲发酵过程功能菌株的筛选和酯化活性测定
通过传统分离方法进行筛菌,对其进行分子生物学鉴定,最终得到功能菌株。制备108 CFU/mL的细菌菌悬液/真菌孢子悬浮液,分别加入1 mL于发酵培养基中,30 ℃发酵5 d。称取发酵结束后的散曲5 g、无菌水15 mL、无水乙醇5 mL、正己酸0.3 mL于50 mL离心管中,在35 ℃下酯化反应5 d。酯化反应结束后吸取上清液0.5 mL于2 mL离心管中,再加入1 mL正己烷(已加乳酸乙酯作为内标,终质量浓度为0.48 μg/μL),涡旋振荡1 min后离心1 min。使用1 mL注射器吸取离心管中上层透明的有机层,经过0.22 μm微孔滤膜过滤后,转移至气相进样瓶中进行GC检测。
1.4 数据处理
采用Microsoft Office Excel 2016进行数据统计和处理;采用SPSS 22.0完成显著性分析;采用MEGA 11软件构建系统发育树;采用Origin 2024进行处理绘制理化指标动态图和功能菌株酯化活性图;丰度图、相关性热图通过在线平台https://www.chiplot.online/绘制。
2 结果与分析
2.1 发酵过程中大曲理化指标的动态变化
发酵过程中大曲的理化指标变化趋势见图1。在发酵过程中,温度逐渐上升,在10 d升至顶温,达到60 ℃,维持大约3 d,13 d后温度逐步下降,最终保持在室温26 ℃左右。在整个过程中,水分整体呈下降趋势。1~4 d水分保持在36% 左右,此时水分过高而温度适宜使大曲产生大量细菌。大曲酸度在4 d时达到最高值0.63 mmoL/10 g,可能是此时细菌大量积累,伴随产酸细菌(如乳酸菌、醋酸菌)的迅速繁殖,代谢产生酸类物质,促使酸度在短期内快速上升[9];而后随着发酵的进行大曲温度不断升高,一些不耐高温的产酸细菌被抑制,促使酸度下降[10]。
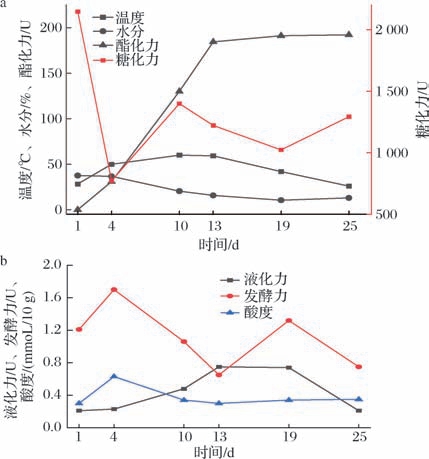
图1 理化指标的动态变化
Fig.1 Dynamic changes of physicochemical indexes
a-温度、水分、酯化力、糖化力变化;b-液化力、发酵力、酸度变化
糖化力、液化力、酯化力和发酵力反映了大曲的功能。在发酵过程中糖化力整体呈现先下降后波动上升的趋势,在1 d时最高,达2 146.06 U,表明大曲原料中本身含有较高的糖化酶。液化力和酯化力在10 d以后达到比较高的水平,这可能是在这期间发生了显著物种优势更替,此时优势微生物代谢产生的液化酶、酯化酶导致液化力、酯化力逐渐上升[11]。发酵力于4 d时达到最高,为1.70 U,这可能是酵母菌和细菌在利用糖类物质进行生长的同时启动酒精发酵[12]。
2.2 发酵过程中大曲微生物的丰富度和多样性
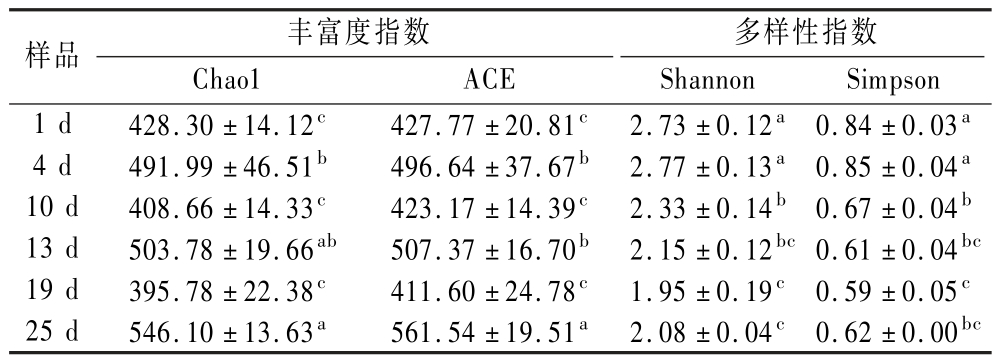
对发酵过程中大曲的Alpha多样性进行分析,结果如表1所示。表1中细菌群落的Chao1和ACE丰富度指数呈振荡上升趋势且整体处于较高水平,在13 d达到峰值(Chao1=1 643.26,ACE=1 708.52),其Shannon多样性指数在10~25 d维持在4.41~4.84高位区间,表明细菌群落具有较高的物种多样性及稳定性。反观表2真菌群落,其Chao1丰富度指数在13 d与25 d分别形成503.78和546.10的双峰特征,而Shannon多样性指数在4 d达到最高,而后呈下降趋势,表明真菌群落的丰富度上升而多样性下降,暗示真菌群落在发酵过程中发生了显著物种优势更替。由以上分析,根据真菌群落的演替特征,将整个发酵过程分为2个阶段,1~ 4 d记为发酵前期,10~25 d记为发酵中后期。
表1 发酵过程中大曲细菌的Alpha多样性指数
Table 1 Alpha diversity index of Daqu bacteria during fermentation
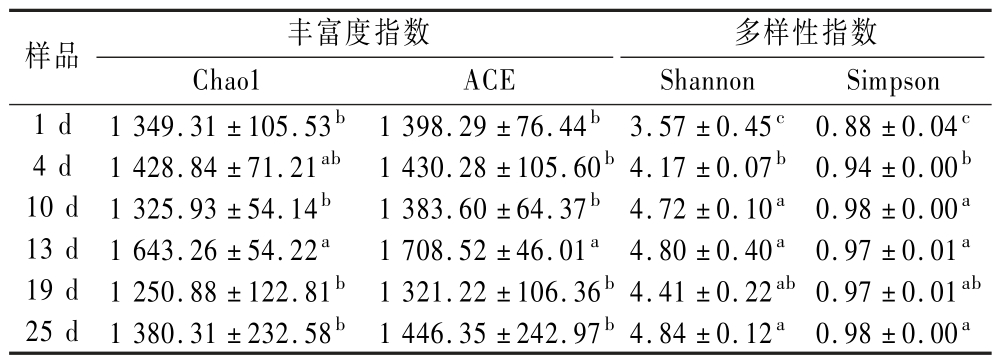
注:不同小写字母代表差异显著(P <0.05)(下同)。
表2 发酵过程中大曲真菌的Alpha多样性指数
Table 2 Alpha diversity index of Daqu fungi during fermentation
2.3 发酵过程中大曲微生物群落的变化情况
2.3.1 基于属水平的大曲细菌群落解析
本研究基于属水平对中高温大曲发酵过程中细菌多样性进行解析,6个大曲样品共检测到310个细菌属,将相对含量>1%的属定义为优势属,大曲发酵过程中优势细菌属的波动情况如图2所示。一共鉴定出16个优势细菌属,分别是Pantoea、Weissella、Lactobacillus、Thermoactinomyces(高温放线菌属)、Bacillus、Salmonella(沙门氏菌属)、Pediococcus、Lactococcus(乳球菌属)、Helicobacter(螺杆菌属)、Kosakonia(科萨克氏菌属)、Acinetobacter(不动杆菌属)、Bacteroides(拟杆菌属)、Kroppenstedtia (克罗彭斯特菌属)、Pseudomonas(假单胞菌属)、Leuconostoc(明串珠菌属)、Acetobacter(醋酸杆菌属)。主要优势属是Pantoea、Weissella、Lactobacillus、Thermoactinomyces、Bacillus。Pantoea 在1 d时占绝对优势,相对丰度为41.04%,随后丰度从4 d开始急剧下降,在发酵中后期相对丰度仅维持在6.34%~ 14.36%。 Lactobacillus 和Weissella均属于乳酸菌,适合在高酸以及湿度较大的环境中存在,代谢产生乳酸[13],它们均在4 d相对丰度达到峰值,这可能也是4 d酸度最高的原因。 Thermoactinomyces 和Bacillus 经过顶温期发酵,在19 d相对丰度达到最高,分别为14.96% 和8.16%,这可能与它们的耐热性有关。 Thermoactinomyces 具有发达的菌丝体、含有淀粉酶、蛋白酶等,有助于小麦等制曲原料的液化和糖化,提高原料的利用率[14]。 Bacillus 是中高温大曲中不可或缺的功能细菌,具有产生蛋白水解酶、淀粉酶、吡嗪类和有机酸的功能[15]。
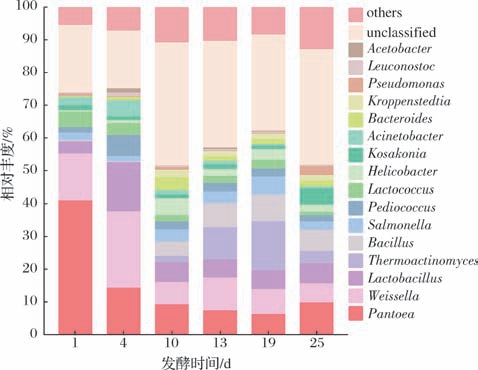
图2 属水平下大曲细菌群落结构
Fig.2 Bacterial community structure of Daqu at genus level
2.3.2 基于属水平的大曲真菌群落解析
本研究基于属水平对中高温大曲发酵过程中真菌多样性进行解析,6个大曲样品共检测到159个真菌属,将相对含量>1%的属定义为优势属,大曲发酵过程中优势真菌属的波动情况如图3所示。一共鉴定出11个优势真菌属,分别是Thermoascus(热子囊菌属)、Wickerhamomyces(威克汉逊酵母属)、Trichosporon(丝孢酵母属)、Thermomyces(嗜热真菌属)、Aspergillus(曲霉属)、Candida(念珠菌属)、Pichia(毕赤酵母属)、Fusarium(镰刀菌属)、Saccharomycopsis(复膜孢酵母属)、Diaporthe(间座壳属)、Epicoccum(附球霉属)。主要优势属是Thermoascus、Wickerhamomyces、Trichosporon、Thermomyces、Aspergillus。其中,Thermoascus 相对丰度为4.67%~73.12%,从4 d后开始迅速增殖,在发酵中后期占绝对优势。 Thermoascus在大曲发酵中可以参与编码与糖化和乙醇发酵的相关酶,具有产酒生香的能力[16]。 Wickerhamomyces 和Trichosporon 在发酵初期占绝对优势,随后相对丰度均出现明显下降。 Thermomyces 相对丰度为0.07%~16.68%,在1~13 d丰度很低,从19 d开始稳定成为第二优势菌株,含量稳定在10%以上,Thermomyces 能提供蛋白酶、纤维素酶等重要酶类,在白酒酿造过程中还具有产酯生香的作用[17-18]。 Aspergillus 相对丰度为2.34%~10.40%,在整个发酵过程中波动变化不大。
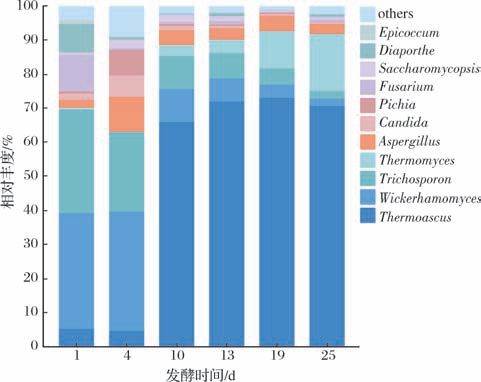
图3 属水平下大曲真菌群落结构
Fig.3 Fungal community structure of Daqu at genus level
2.4 发酵过程中大曲优势菌属与理化指标的关联性分析
为揭示理化指标对优势微生物群落的影响,选取相对丰度分别排名前10的优势细菌属、优势真菌属与发酵过程中理化指标进行相关性分析(图4)。在整个发酵过程中,很多优势菌属与酸度、水分呈正相关, Lactobacillus、 Pediococcus、 Aspergillus、 Candida、Pichia 与酸度的相关系数均>0.9,Wickerhamomyces和Trichosporon 与水分的相关系数>0.9。
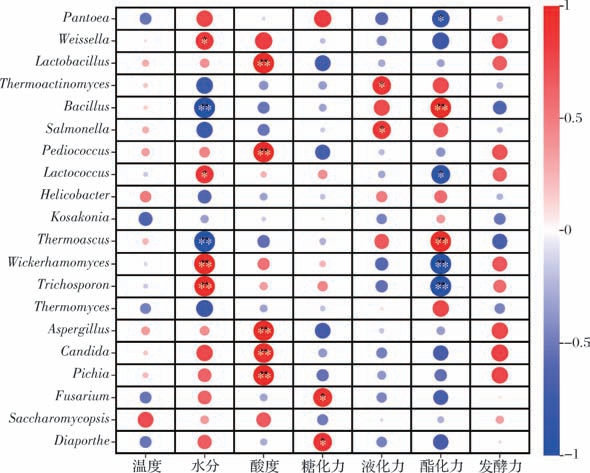
图4 理化指标与优势菌属之间的相关性分析
Fig.4 Correlation analysis between physicochemical indexes and dominant microorganisms
注:∗∗代表差异极显著(P <0.01),∗代表差异显著(P <0.05)。
Bacillus 和Thermoascus 是影响大曲功能的主要优势微生物,与酯化力、液化力均呈正相关,尤其体现在酯化力方面,Bacillus 和Thermoascus 与酯化力的相关系数分别高达0.98和0.97(P <0.01)。目前一些研究也报道了Bacillus、Thermoascus 在产酯方面的应用,ZHENG等[19]的研究表明,Bacillus 对浓香型白酒中己酸乙酯的生成有促进作用;ZHAO等[20]筛选出一株蜡样芽孢杆菌,可产生214.7 mg/100 mL的己酸乙酯;孙亮霞等[7]发现中高温大曲中己酸乙酯的生成与Thermoascus 呈正相关。TIE等[21]筛选到一株橙色嗜热子囊菌Thermoascus aurantiacus,其酯化力大概为7 μmol/g。
2.5 发酵过程中大曲功能菌属的筛选和酯化力验证
通过分离、纯培养和16S/ITS rRNA测序,从大曲中得到功能菌属下的6株常见菌株,分别命名为BV(Bacillus velezensis 贝莱斯芽孢杆菌)、BS(Bacillus subtilis 枯草芽孢杆菌)、BP(Bacillus pumilus 短小芽孢杆菌)、BC(Bacillus cereus 蜡样芽孢杆菌)、TC(Thermoascus crustaceus 坚脆嗜热子囊菌)、TA(Thermoascus aurantiacus)。系统发育树、菌落形态和酯化活性测试结果如图5所示,这6株菌经过散曲发酵均表现出一定的酯化力,总体来说真菌的酯化力明显强于细菌,细菌的酯化力比较微弱,这一结论与TIE等[21]的实验结论一致,丝状真菌能产较强的酯化酶,这与其酶的结构有关。
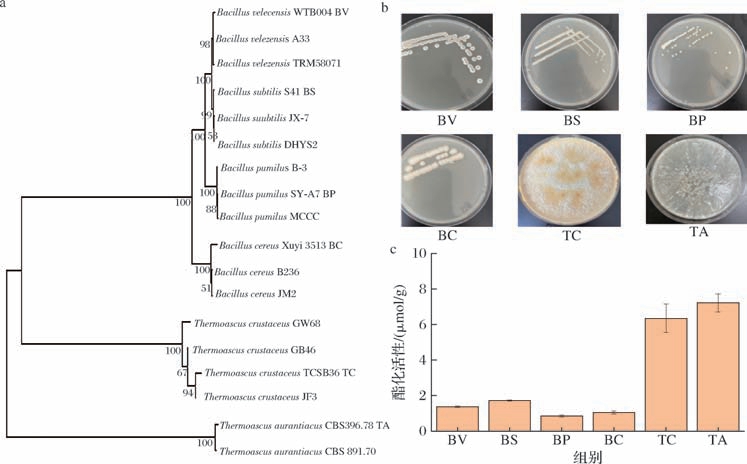
图5 功能菌株的筛选和验证
Fig.5 Screening and verification of functional microorganisms
a-系统发育树;b-菌株形态;c-菌株酯化活性
2.6 发酵过程中大曲优势菌属的关联性分析
如图6所示,为了解功能菌属Bacillus 和Thermoascus 与其他优势属之间的相互作用,对这20个优势属进行相关性分析,共鉴定出81对为正相关。其中,Bacillus 与Thermoascus(r=0.95)呈极显著正相关(P <0.01),Bacillus 与Thermoactinomyces(r=0.85)呈显著正相关(P <0.05),Thermoascus 与Lactococcus(r=0.89)呈显著正相关(P <0.05)、与Weissella(r=-0.87)呈显著负相关(P <0.05),Bacillus、Thermoascus 均与Wickerhamomyces、Trichosporon 呈极显 著负相关(P <0.01)。为进一步探究功能菌属Bacillus和Thermoascus 的演替驱动因素,选取以上相关菌属再次与理化指标进行RDA。
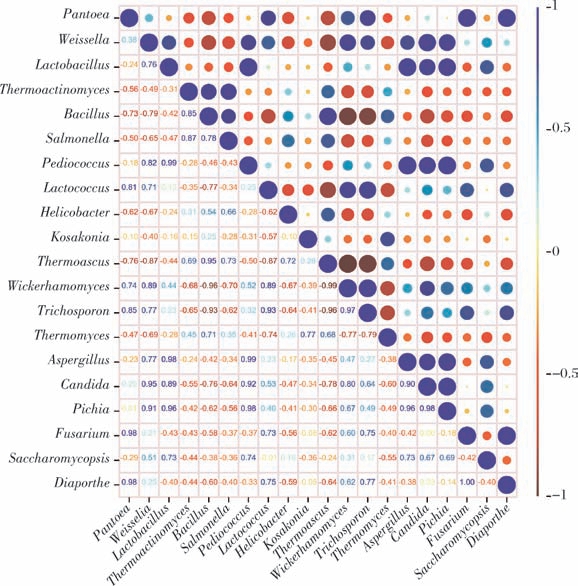
图6 大曲优势菌属相关性
Fig.6 Correlation of dominant microorganisms of Daqu
2.7 发酵过程中大曲功能菌属与理化指标的关联性分析
为深入了解发酵过程中大曲功能菌属与理化指标的相互作用及理化指标(其中Tem代表温度、Acid代表酸度、Moi代表水分、SP代表糖化力、LP代表液化力、EP代表酯化力、FP代表发酵力)之间的相关性,建立RDA相关性图。如图7-a可知,酯化力和水分对大曲微生物群落的影响最大,温度、糖化力、酸度影响较小。任海伟等[22]也发现酯化力、水分对大曲群落变化影响较强。酯化力与酸度、水分、糖化力、发酵力呈负相关,与温度、液化力呈正相关。发酵前期(A组)与发酵中后期(B组)分别位于坐标轴左右侧,B组随时间变化出现明显的生态位分化,与表2的Alpha多样性分析一致。
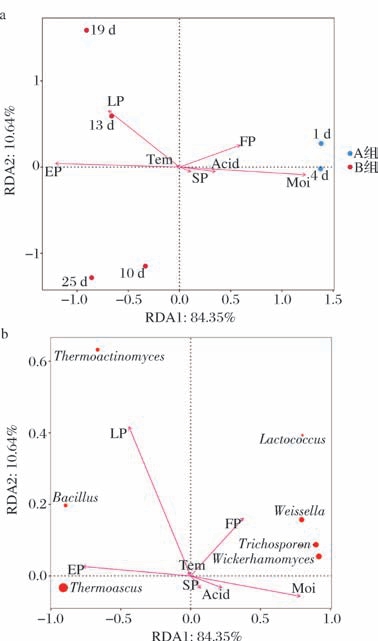
图7 大曲功能菌属RDA
Fig.7 RDA of functional microorganisms of Daqu
a-理化指标与发酵时间相关性;b-理化指标与菌属相关性
如图7-b所示,Bacillus 与Thermoascus 与酯化力呈正相关,其中Thermoascus 与酯化力之间的相关性更强,这与图5中的酯化力结果相符。分析功能菌属Bacillus、Thermoascus 和理化指标、其他菌属之间的相关性,试解释功能菌属演替的规律,结果发现:Bacillus 与Thermoascus 均与Wickerhamomyces、Trichosporon呈负相关,而Wickerhamomyces 和Trichosporon 与发酵前期(A组)呈正相关,与水分呈正相关,可能是在发酵前期,水分过重,Wickerhamomyces 和Trichosporon 优势生长,抑制了Bacillus 与Thermoascus 的生长,此时酯化力不高。后面由于升温,水分快速挥发,此时发生显著优势演替,酯化力逐渐上升。
3 结论
本研究对中高温大曲发酵过程中的理化指标进行了测定,并结合高通量测序技术对微生物群落的变化进行了系统的研究。研究发现,在发酵过程中,细菌群落具有较高的物种多样性及稳定性,而真菌群落在发酵中后期发生显著物种优势更替。在整个发酵过程中,细菌以Pantoea、Weissella、Lactobacillus、Thermoactinomyces、 Bacillus 为主,真菌以 Thermoascus、Wickerhamomyces、Trichosporon、Thermomyces、Aspergillus为主。通过相关性分析最终确定Bacillus 和Thermoascus 是影响大曲功能的主要微生物,主要体现在酯化力上。通过筛菌得到了6株功能菌,通过散曲发酵实验验证了它们的酯化能力,其中,Thermoascus 酯化能力更强,这与其酯化酶的结构有关。通过优势菌属之间相关性分析找到与Bacillus 和Thermoascus 相关的菌属后,与理化指标再次进行相关性分析,结果发现,酯化力和水分对大曲微生物群落的影响最大,在发酵前期,由于水分过重,Wickerhamomyces、Trichosporon 占优势地位,影响了Bacillus 和Thermoascus 的酯化优势,到了发酵中后期,水分迅速下降,功能菌属才得以占据优势而发挥作用,导致酯化力逐渐上升。因此,在实际生产应用中,尤其是发酵初期应注意控制大曲的水分含量,避免影响大曲功能。同时,虽然Pantoea、Weissella、Lactobacillus 等菌在相对丰度上占有优势,但它们对大曲的功能性质影响甚微甚至呈负相关,说明功能微生物与其在大曲中的相对丰度并不完全呈正相关。本研究通过对中高温大曲发酵过程理化指标及功能菌群的分析,进一步阐释了发酵过程中功能菌的驱动演替规律,找到关键控制点,为后续实际应用生产研究提供指导,同时筛到的功能菌株为大曲功能微生物的研究提供了菌株资源,为未来大曲功能微生物的深入研究打下基础。
[1]LIU H L,SUN B G.Effect of fermentation processing on the flavor of Baijiu[J].Journal of Agricultural and Food Chemistry,2018,66(22):5425-5432.
[2]侯强川,王文航,徐媛媛,等.徐坊中高温大曲发酵过程中理化品质、风味及真菌群落结构变化规律研究[J].食品工业科技,2024,45(19):133-141.HOU Q C,WANG W H,XU Y Y,et al.Dynamic changes of physicochemical quality,flavor and fungal community structure during mediumhigh temperature Daqu fermentation process in Xufang region[J].Science and Technology of Food Industry,2024,45(19):133-141.
[3]DENG J,ZHENG J,HUANG D,et al.Characterization of physicochemical properties,volatile compounds and microbial community structure in four types of Daqu[J].LWT,2023,184:115064.
[4]MA S Y,LUO H B,ZHAO D,et al.Environmental factors and interactions among microorganisms drive microbial community succession during fermentation of Nongxiangxing daqu[J].Bioresource Technology,2022,345:126549.
[5]MAO J J,LIU X L,GAO T,et al.Unraveling the correlations between bacterial diversity,physicochemical properties and bacterial community succession during the fermentation of traditional Chinese strong-flavor Daqu[J].LWT,2022,154:112764.
[6]LEI Y,CAI W C,WANG Y R,et al.Elucidating the physicochemical parameters,bacterial community structure,and correlation characteristics of medium-high temperature Daqu[J].Food Bioscience,2024,58:103679.
[7]孙亮霞,王淑珍,林一心,等.不同等级中高温大曲理化性质、微生物群落结构及挥发性风味物质的研究[J].食品与发酵工业,2025,51(24):284-290.SUN L X,WANG S Z,LIN Y X,et al.Research on physicochemical properties,microbial community structure,and volatile flavour substances of different grades of medium and high temperature Daqu[J].Food and Fermentation Industries,2025,51(24):284-290.
[8]刘慧,涂璇,吕育财,等.中高温大曲在制曲过程中微生物区系演替特征及功能研究[J].食品与发酵工业,2022,48 (22):180-186.LIU H,TU X,LYU Y C,et al.Succession of microbial communities and function of medium-high-temperature Daqu during the starter-making process[J].Food and Fermentation Industries,2022,48(22):180-186.
[9]孙亮霞,王生艳,林一心,等.中高温大曲贮存期间理化指标及微生物群落动态分析[J].食品与发酵工业,2025,51(7):122-128.SUN L X,WANG S Y,LIN Y X,et al.Analyzing dynamics of microbial community and physicochemical indicators during storage of medium-and high-temperature Daqu[J].Food and Fermentation Industries,2025,51(7):122-128.
[10]刘敏芳,王昊乾,唐艺婧,等.后火曲制作过程中理化、生化指标和微生物菌群变化及其相关性分析[J].中国酿造,2023,42(5):70-77.LIU M F,WANG H Q,TANG Y J,et al.Changes of physicochemical and biochemical indexes and microbial community and analysis during the preparation of Houhuoqu[J].China Brewing,2023,42(5):70-77.
[11]陈雪,张永利,闫宗科,等.凤香型酒醅微生物群落演替及其与理化指标的相关性分析[J].食品科学,2020,41(22):200-205.CHEN X,ZHANG Y L,YAN Z K,et al.Correlation analysis of microbial community succession in fermented grains of Xifeng-flavor Chinese liquor with its physicochemical indexes[J].Food Science,2020,41(22):200-205.
[12]薄涛,吕娜,杨凯环,等.白酒大曲发酵过程中微生物群落及功能研究进展[J].食品科学,2023,44(19):385-393.BO T,LYU N,YANG K H,et al.Recent advances in understanding the composition and functions of microbial community in the fermentation of Baijiu Daqu[J].Food Science,2023,44(19):385-393.
[13]YANG Y,WANG S T,LU Z M,et al.Metagenomics unveils microbial roles involved in metabolic network of flavor development in medium-temperature daqu starter[J].Food Research International,2021,140:110037.
[14]WANG Y R,CAI W C,WANG W P,et al.Analysis of microbial diversity and functional differences in different types of high temperature Daqu[J].Food Science &Nutrition,2020,9(2):1003-1016.
[15]HE G Q,DONG Y,HUANG J,et al.Alteration of microbial community for improving flavor character of Daqu by inoculation with Bacillus velezensis and Bacillus subtilis[J].LWT,2019,111:1-8.
[16]ZHU M,ZHENG J,XIE J,et al.Effects of environmental factors on the microbial community changes during medium-high temperature Daqu manufacturing[J].Food Research International,2022,153:110955.
[17]CAI W C,XUE Y A,WANG Y R,et al.The fungal communities and flavor profiles in different types of high-temperature daqu as revealed by high-throughput sequencing and electronic senses[J].Frontiers in Microbiology,2021,12:784651.
[18]DENG Y K,HUANG D,HAN B L,et al.Correlation:Between autochthonous microbial diversity and volatile metabolites during the fermentation of Nongxiang Daqu[J].Frontiers in Microbiology,2021,12:688981.
[19]ZHENG X W,YAN Z,ROBERT NOUT M J,et al.Characterization of the microbial community in different types of Daqu samples as revealed by 16S rRNA and 26S rRNA gene clone libraries[J].World Journal of Microbiology &Biotechnology,2015,31(1):199-208.
[20]ZHAO C Q,YAN X L,YANG S T,et al.Screening of Bacillus strains from Luzhou-flavor liquor making for high-yield ethyl hexanoate and low-yield propanol[J].LWT,2017,77:60-66.
[21]TIE Y,WANG L,DING B,et al.Investigating the main contributors to esterification activity and identifying the aqueous-phase ester synthases in Daqu[J].Food Bioscience,2025,66:106227.
[22]任海伟,李云帆,阿丽米热·克热穆,等.不同等级金徽酒大曲贮藏过程中的细菌群落演替规律和组装机制[J].食品科学,2025,46(10):108-119.REN H W,LI Y F,ALIMIRE·Keremu,et al.Succession and assembly mechanism of bacterial communities in different grades of Jinhui Baijiu Daqu during storage[J].Food Science,2025,46(10):108-119.