银杏(Ginkgo biloba L.)作为现存最古老的裸子植物之一,其演化历史可追溯至2亿年前,具有植物界“活化石”之称。我国作为全球银杏资源最丰富的国家,种植面积逾300万亩(占全球总量的70%),极具开发潜力[1]。其中,银杏叶作为药食同源的重要资源,具有活血化瘀等药用功效以及独特的食用价值。然而,目前大部分银杏叶仅作为原料出口或用于初级产品加工,高值化利用度低,导致这一特色资源未能充分开发[2]。
银杏叶富含多酚、多糖等活性成分。其中酚类化合物因其显著的抗氧化、抗炎及清除自由基等生物活性[3],从而在功能食品以及医药领域展现出重要应用价值。然而,目前对于银杏叶酚类化合物的加工利用方式仍停留在通过传统有机溶剂浸提酚类化合物的方法,存在污染严重、溶剂残留等问题。因此,亟待开发一种安全、环保的可替代传统浸提的提取方法。
低共熔溶剂(deep eutectic solvent,DES)作为一种新型绿色提取介质,凭借其低毒性、可降解性和可设计性等优势,为植物活性成分的提取提供了创新思路[4]。DES中的氢键供体或氢键受体可与酚类化合物中的酚羟基产生相互作用,从而增加了其在DES中的溶解度,提高其提取率[5]。现有研究虽在DES提取银杏叶黄酮工艺方面取得一定进展,但在DES体系构建、酚类成分鉴定及其抗氧化活性评价等方面仍缺乏系统研究[3,6]。
为此,本研究以氯化胆碱为氢键受体,苹果酸、乳酸、甘油、葡萄糖、山梨糖醇、乙二醇和尿素为氢键供体构建DES,通过考察不同DES对银杏叶酚类化合物提取率的影响筛选出最优提取溶剂;结合超声波辅助提取的方法,通过优化调整超声功率、料液比、加水量以及超声时间等关键因素,确定银杏叶酚类化合物的最佳提取工艺。同时,通过高效液相色谱鉴定了8种银杏叶酚类化合物,并对其进行DPPH自由基清除能力、ABTS阳离子自由基清除能力和总抗氧化能力(oxygen radical absorbance capacity,ORAC)等抗氧化能力评价。本研究成果为银杏叶酚类化合物的绿色高效提取及其在功能食品与医药领域的应用提供理论依据和技术支持。
1 材料与方法
1.1 材料与试剂
银杏叶,江苏恒天生物科技有限公司,经鉴定为晒干后的银杏叶,水分含量为7.99%;槲皮素、木犀草素、咖啡酸、香草酸、阿魏酸、没食子酸、芦丁、荧光素钠、偶氮二异丁脒盐酸盐[2,2′-azobis (2-methylpropionamidine) dihydrochloride,AAPH],上海阿拉丁公司;原儿茶酸、绿原酸,上海源叶生物科技有限公司;DPPH,梯希爱(上海)化成工业发展有限公司;ABTS,南京辛西亚生物科技有限公司;L(+)-抗坏血酸(维生素C)、AlCl3,国药集团化学试剂有限公司;氯化胆碱,麦克林试剂;其他试剂均为分析纯。
1.2 仪器与设备
SpectraMax® i3x酶标仪,美国美谷分子公司;Wizard 2.0冷冻干燥机,美国Virtis公司;SCIENTZIID超声波细胞粉碎机,宁波新芝生物科技股份有限公司;DZF-6050真空干燥箱,上海一恒科学仪器有限公司;MB120水分含量测定仪,奥豪斯仪器(常州)有限公司;C-MAG HS 7 control IKA磁力搅拌器,德国艾卡集团;LC-20A高效液相色谱仪,日本岛津公司。
1.3 实验方法
1.3.1 银杏叶酚类提取与工艺优化
1.3.1.1 DES的制备
采用氯化胆碱为氢键受体,乳酸、甘油、乙二醇、葡萄糖、苹果酸、尿素、山梨糖醇为氢键供体,按一定的摩尔比(比例见电子版增强出版附表1,https://doi.org/10.13995/j.cnki.11-1802/ts.043613,下同)于85~90 ℃下反应一段时间,待反应溶液澄清透明,且冷却至室温后仍呈均一稳定、无晶体析出状态即为稳定的DES。
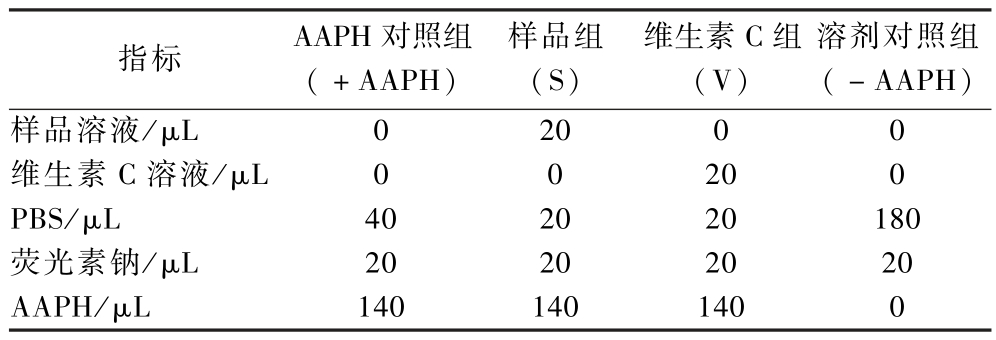
表1 银杏叶酚类化合物的ORAC抗氧化评价
Table 1 ORAC antioxidant evaluation of phenolic compounds from G.biloba leaves
1.3.1.2 DES的筛选
银杏叶干燥、粉碎、过0.25 mm筛后备用。分别称取1 g银杏叶粉加入到30 mL含水量20%(质量分数)的不同种类的DES中,室温下超声提取40 min后,离心取上清液,分别用提取时所用的DES定容至50 mL。以不同DESs提取所得的8种酚类化合物的含量为指标筛选出最优提取溶剂。采用多次提取的方式确定银杏叶8种酚类化合物的总含量。提取率的计算如公式(1)所示:
式中:mD,不同DESs单次提取后8种酚类化合物的总质量,mg;m,多次提取得到的银杏叶中8种酚类化合物的总质量,mg。
1.3.1.3 超声波辅助DES提取单因素试验
称取1 g样品加入100 mL烧杯中,按不同的料液比[1∶10、1∶15、1∶20、1∶25、1∶30(g∶mL)],加入不同含水量(20%、25%、30%、35%、40%,质量分数)的DES,在不同的超声功率(100、150、200、250、300 W)下,提取一段时间(5、10、15、20、25 min)。待提取结束后,提取液于8 000 r/min下离心5 min,取上清液用对应的DES定容至50 mL,得到溶液即为银杏叶粗提液。
1.3.1.4 银杏叶酚类化合物的分离、定量
将1 g银杏叶加入30 mL水分含量为30%的筛选得到的最佳的DES中,在最优提取条件下(超声功率为200 W,超声提取时间为10 min)的下,得到粗提液定容后,通过高效液相色谱进行检测与收集[7]。液相收集的条件为梯度洗脱0~6 min:90%~70% B,6~13 min:70%~60% B,13~17 min:60%~55% B,17~19 min:55%~51.7% B,19~27 min:51.7%~48.5% B,27~28 min:48.5%~45% B,28~35 min:45%~23% B,35~40 min:23%~95% B,40~45 min:95%~90% B,45~60 min:90%~90% B。液相收集流出液的时间设定依次为17.51~18.10 min,22.01~22.30 min,22.33~ 22.55 min,24.30~ 24.70 min,30.55~31.01 min,34.01~34.60 min,37.01~37.50 min,44.71~ 45.00 min,液相收集的水平高度设置为350 mAU,洗脱时间为60 min,波长为280 nm,进样量20 μL,流速设置为0.80 mL/min,色谱柱为安捷伦TC-C18(250 mm ×4.6 mm,3.5 μm);检测条件为等度洗脱,A相为纯甲醇,B相为0.2%乙酸水,其占比分别为25%和75%。波长为280 nm,进样量20 μL,流速设置为0.80 mL/min,洗脱时间为30 min。
1.3.2 酚类化合物的抗氧化活性评价
1.3.2.1 DPPH自由基清除能力
DPPH自由基清除能力的测定参考SABIR等[8]的方法并略加修改:取0.50 mL样品与2.50 mL 0.50 mmol/L DPPH甲醇溶液混匀,室温避光反应30 min后,使用紫外可见分光光度计于517 nm下测定吸光度。DPPH自由基清除率的计算如公式(2)所示:
式中:A0为空白组吸光度;A1为样品组吸光度。
1.3.2.2 ABTS阳离子自由基的清除能力
ABTS阳离子自由基清除能力的测定参考ZHU等[9]的方法并稍作修改:分别取0.10 mL的样品与3.90 mL的ABTS阳离子自由基工作液混匀,室温避光反应10 min后,使用紫外可见分光光度计于734 nm处测定其吸光值(A样品);以蒸馏水和ABTS阳离子自由基工作液混合进行空白实验(A空白)。ABTS阳离子自由基清除率的计算如公式(3)所示:
式中:A空白,空白组吸光度;A样品,样品组吸光度。
1.3.2.3 抗氧化能力指数
银杏叶酚类化合物的ORAC参照JING等[10]的方法并略作修改。按表1(其中PBS浓度为75 mmol/L pH 7.4;维生素C浓度为10 μmol/L;荧光素钠浓度为1 μmol/L;AAPH浓度为18 mmol/L)所述加样后,样品在37 ℃下预热5 min,随后在37 ℃下于荧光分析仪中进行连续测定,激发波长和发射波长分别设置为485 nm和538 nm,检测间隔时间为2 min。抗氧化能力指数ORAC值如公式(4)所示:
式中:ORAC,抗氧化能力指数ORAC值,μmol维生素C/mg;AMCS,酚类化合物组荧光曲线下面积;AMC+AAPH,AAPH组荧光曲线下面积;AMCV,维生素C组荧光曲线下面积;MV,维生素C溶液浓度,μmol/mL;MS,不同酚类化合物质量浓度,mg/mL。
1.3.3 最高占据分子轨道(highest occupied molecular orbital,HOMO)和最低未占分子轨道(lowest unoccupied molecular orbital,LUMO)轨道能量计算
参照CHEN等[11]的方法计算银杏叶中8种酚类化合物的HOMO-LUMO轨道能量。本研究采用密度泛函理论的B3LYP方法,在Gaussian 16软件平台上对银杏叶8种酚类化合物进行几何优化计算,基组选择6-311G∗∗,溶剂环境设置为甲醇体系。
1.4 数据处理与分析
采用Excel 2019和Origin 7.0软件进行数据处理及相关性分析。采用Excel 2019的单因素ANOVA进行显著性分析,显著性差异水平选取P <0.05。相关性分析采用皮尔逊相关系数法,所有数据均以3次实验结果的“平均值±标准差”表示。
2 结果与分析
2.1 DES的筛选
由图1可知,DES13对银杏叶酚类化合物的提取率(76.39%)最为显著,其提取率显著优于其他DES提取及传统80% 甲醇超声辅助提取[12]的方法。其原因是DES中氢键供体的类型直接影响其组成、酸碱度、黏度和极性等特性,进而影响提取率。在碱性条件下酚类化合物易形成离子状态,溶解度提高。因此,具有更高碱性特征的DES12和DES13具出较优的提取率[13]。当氯化胆碱与尿素的摩尔比为1 ∶2时,所形成的DES流动性好、黏度低、渗透作用强[14]。因此,选择氯化胆碱与尿素的摩尔比为1 ∶2的DES进行后续的单因素试验。
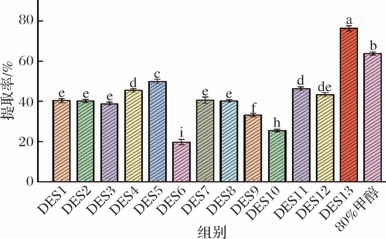
图1 DES对银杏叶酚类化合物提取率的影响
Fig.1 Effects of DES on the extraction yield of phenolic compounds from G.biloba leaves
注:不同小写字母表示差异显著(P <0.05)。
由表2可知,酚酸的得率相对高于黄酮,8种酚类化合物的含量高低依次为阿魏酸>绿原酸>表儿茶酸>香草酸>木犀草素>咖啡酸>芦丁>槲皮素。其原因可能是黄酮类化合物分子较大,在从银杏叶细胞内部向溶剂扩散的过程中,可能会受到细胞碎片、细胞壁残渣等的阻碍,其传质速率相对较慢,从而导致提取率低于酚酸。其次,酚酸因其较强的极性,能够与DES中的氢键供体和受体形成更有效的氢键相互作用,从而更容易溶解在DES中[12]。8种酚类化合物的标准曲线见附表2。
表2 银杏叶酚类化合物的含量测定 单位:μg/g
Table 2 Determination of phenolic compounds from G.biloba leaves
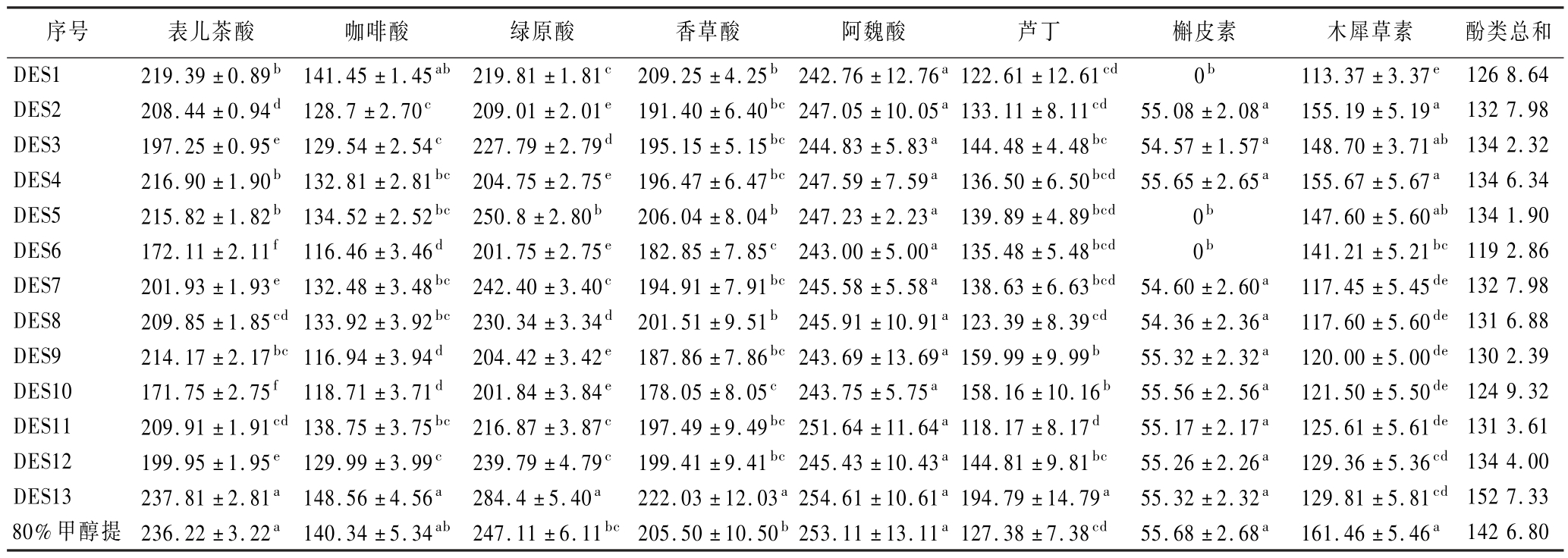
注:不同小写字母表示差异显著(P <0.05)。
2.2 银杏叶酚类化合物的超声波辅助提取工艺优化
如图2-a所示,随着超声功率的增大,银杏叶酚类化合物的提取率呈先上升后趋于平缓的变化趋势,在200 W时,达到峰值(48.12%)。超声功率的增加导致超声波以更大的振幅通过溶剂,导致气泡的崩塌,这种崩塌放大了多种物理效应(细胞壁破坏、界面湍流、局部能量扩散),进而促进了酚类化合物的溶出。此外,超声功率的增加也能提高氯化胆碱-尿素的温度,使DES黏度降低[15]。但当超声功率超过200 W时,超声功率的增加并未明显提高银杏叶酚类化合物的提取率,反而造成资源的浪费。因此,确定200 W为较佳的超声功率。
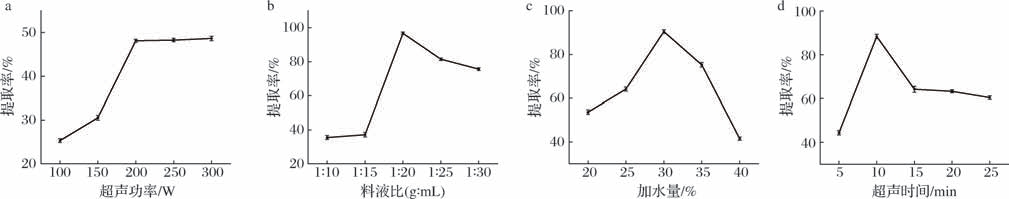
图2 超声功率、料液比、加水量和超声时间对提取率的影响
Fig.2 Effects of ultrasound power,material-liquid ratio,amount of water added and ultrasound time on the extraction yield
a-超声功率;b-料液比;c-加水量;d-超声时间
如图2-b所示,随着液料比的增加,银杏叶酚类化合物的提取率先上升后下降,在料液比为1 ∶20(g∶mL)时达到最大值(96.70%)。在低液料比条件下,氯化胆碱-尿素无法提供充足氢键且空化效应分布不均,导致溶解度受限;当料液比超过1∶20(g∶mL)时,提取率呈下降趋势,其原因可能是过量水分既破坏DES氢键网络促进溶质迁移,又削弱氢键作用[16]。因此,较佳的料液比为1∶20(g∶mL)。
如图2-c所示,随着水分的增加,银杏叶酚类化合物的提取率呈现先上升后下降的变化趋势,在水分含量为30%时达到最大值(90.46%)。适量的水分可以降低DES黏度和表面张力,促进空化气泡生成与破碎,增强溶剂和物料界面的振动,同时提升溶剂极性增强酚类物质溶解;但当水分超过30%时,其会破坏DES氢键网络,削弱其与目标分子的特异性相互作用[17]。因此,选择水分含量为30%的条件进行下一步研究。
如图2-d所示,随着提取时间的延长,银杏叶酚类化合物的提取率呈现先上升后下降的趋势,当提取时间为10 min时,银杏叶酚类化合物的提取率达到最大值(88.38%)。当提取时间小于10 min时,由于提取时间较短,DES溶解银杏叶酚类化合物不充分,导致提取率较低。随着提取时间的延长,超声空化效应通过机械破坏作用有效破坏细胞结构,促进DES向基质内部渗透,从而显著提高银杏叶酚类化合物的提取率;但过长时间的超声处理会导致体系局部温度异常升高,可能引发目标化合物的热降解反应,最终反而造成提取率的下降[18]。因此,最佳的提取时间为10 min。
由上述单因素试验的结果可知,从银杏叶中提取酚类的最佳条件为超声功率200 W,料液比为1 ∶20(g∶mL),水分含量为30%,超声时间10 min。在此条件下,银杏叶酚类化合物的提取率可达96.70%,高于传统超声辅助80%甲醇提取方法的提取率(69.64%)。8种酚类物质的液相色谱图如图3所示,经高效液相色谱定峰收集后(纯度达到95.00%),进一步用于抗氧化活性分析。
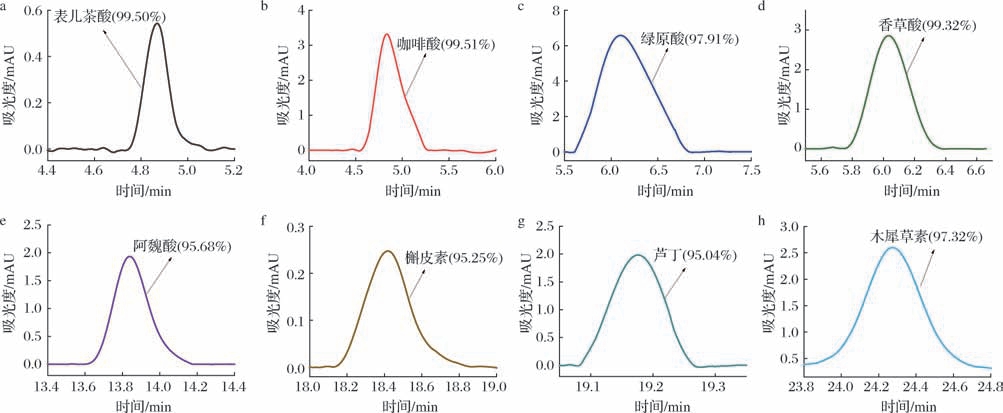
图3 提取的银杏叶中8种酚类化合物液相色谱图
Fig.3 Liquid chromatogram of 8 phenolic compounds extracted from G.biloba leaves
a-原儿茶酸;b-咖啡酸;c-绿原酸;d-香草酸;e-阿魏酸;f-槲皮素;g-芦丁;h-木犀草素
2.3 银杏叶酚类的抗氧化活性评价
2.3.1 银杏叶酚类清除DPPH自由基活性
银杏叶中8种酚类物质的DPPH自由基清除率如图4所示。DPPH自由基清除能力的强弱依次为槲皮素>木犀草素>咖啡酸>阿魏酸>绿原酸>芦丁>原儿茶酸>香草酸。其IC50 值依次为0.018 1、0.019 9、0.025 8、0.035 1、0.050 0、0.052 6、0.081 5、3.121 0 mg/mL。槲皮素、木犀草素、咖啡酸和阿魏酸强于维生素C的DPPH自由基清除能力(维生素C的IC50 值为0.034 7 mg/mL),绿原酸、芦丁、原儿茶酸和香草酸的DPPH自由基清除能力弱于维生素C。
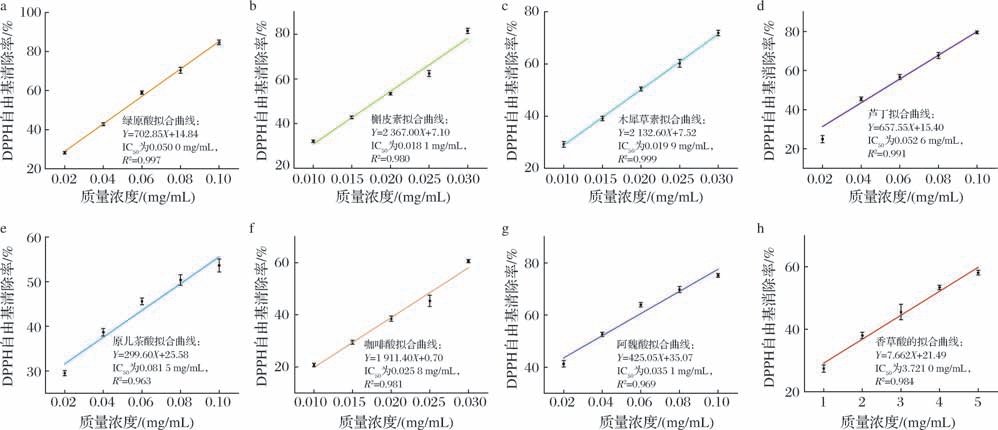
图4 银杏叶中8种酚类物质的DPPH自由基的清除率
Fig.4 Scavenging yield of DPPH free radical of 8 phenolic compounds from G.biloba leaves
a-绿原酸;b-槲皮素;c-木犀草素;d-芦丁;e-原儿茶酸;f-咖啡酸;g-阿魏酸;h-香草酸
槲皮素清除DPPH自由基的能力最强,其IC50 值最低,仅为0.018 1 mg/mL,这与ABDEL-MAGEED等[19]的研究结果一致。这种差异可能主要是由于这些化合物的化学结构及分子大小不同造成的。研究表明,分子中含有更多的酚羟基(—OH)基团,以及共轭双键结构的化合物,具有更强的自由基清除能力。槲皮素分子中含有5个酚羟基,且含有邻二酚羟基结构,同时分子中的共轭结构也会增强化合物的自由基清除能力。
2.3.2 银杏叶酚类清除ABTS阳离子自由基活性
银杏叶中8种酚类物质的ABTS阳离子自由基清除率如图5所示。ABTS阳离子自由基清除能力的强弱依次为槲皮素>阿魏酸>原儿茶酸>咖啡酸>绿原酸>木犀草素>芦丁>香草酸,其IC50 值依次为0.053 8、0.148 9、0.183 5、0.198 0、0.305 1、0.309 2、0.801 1、2.586 2 mg/mL。槲皮素、阿魏酸、原儿茶酸和咖啡酸的ABTS阳离子自由基清除能力与维生素C(IC50 为0.157 1 mg/mL)相近,绿原酸、木犀草素、芦丁和香草酸的ABTS阳离子自由基清除能力弱于维生素C。
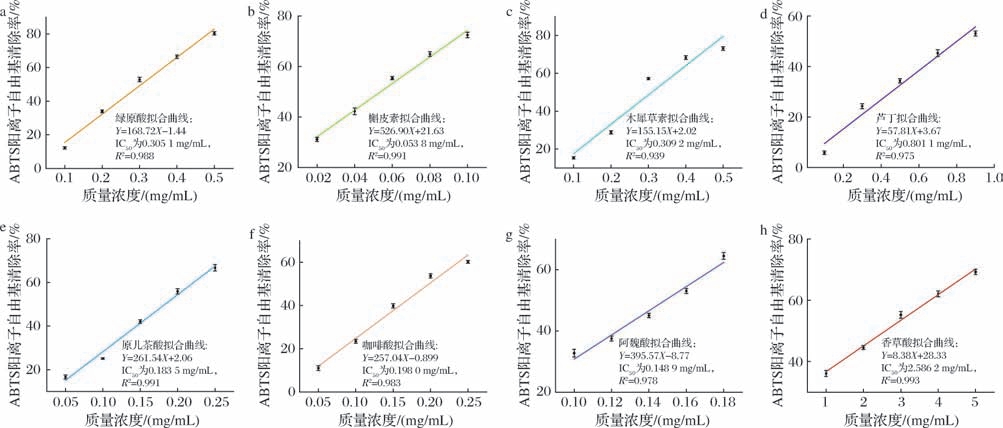
图5 银杏叶中8种酚类化合物的ABTS阳离子自由基的清除率
Fig.5 The ABTS cationic free radical scavenging yield of 8 phenolic compounds from G.biloba leaves
a-绿原酸;b-槲皮素;c-木犀草素;d-芦丁;e-原儿茶酸;f-咖啡酸;g-阿魏酸;h-香草酸
槲皮素的ABTS阳离子自由基清除能力最强,香草酸的ABTS阳离子自由基清除能力最弱,这可能与它们的化学结构有关,如羟基、氨基等官能团的数量和位置影响其自由基清除活性[20]。槲皮素含5个酚羟基(含邻二酚羟基结构),且共轭结构使得电子离域程度高,易通过电子转移清除自由基。香草酸为4-羟基-3-甲氧基苯甲酸结构,其只有1个酚羟基,且单酚羟基的氢供给能力远弱于邻二酚羟基。
2.3.3 银杏叶酚类ORAC抗氧化评价
由图6可知,抗氧化能力指数ORAC值分别为103.62、184.68、88.93、68.36、84.77、91.82、96.66、73.59 μmol维生素C/mg。抗氧化能力指数ORAC评价中,ORAC为正值,即表明受试物具有抗氧化活性,且抗氧化能力与ORAC值呈正相关,ORAC值越高,抗氧化能力越强[21]。由此可知,其ORAC抗氧化活性顺序为槲皮素>咖啡酸>木犀草素>绿原酸>阿魏酸>原儿茶酸>芦丁>香草酸。
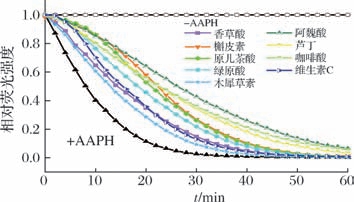
图6 图例计算ORAC值(以曲线下净面积表示)
Fig.6 Illustration of calculation the ORAC value expressed as the net area under the curve
注:咖啡酸、槲皮素、阿魏酸、香草酸、原儿茶酸、绿原酸、木犀草素和芦丁的质量浓度为0.000 2、0.000 1、0.000 3、0.000 13、0.000 2、0.000 15、0.000 067和0.000 267 mg/mL。
2.3.4 银杏叶酚类化合物的LUMO、HOMO及LUMO-HOMO能隙[LUMO-HOMO gap,ΔE(LUMO-HOMO)]与其抗氧化活性的相关性分析
银杏叶中8种酚类化合物的结构式及使用Gaussian16优化后的结构见附图1。如表3所示,8种酚类化合物——咖啡酸、槲皮素、木犀草素、芦丁、香草酸、原儿茶酸、阿魏酸和绿原酸的HOMO与LUMO值分别为-6.358~-6.197 eV和-2.468~-2.042 eV。相应的,它们的能级差ΔE(LUMO-HOMO)介于4.000~4.896 eV。
表3 LUMO、HOMO值及HOMO-HUMO能隙(ΔE)
Table 3 The HOMO,LUMO values and HOMO-HUMO energy gap (ΔE)
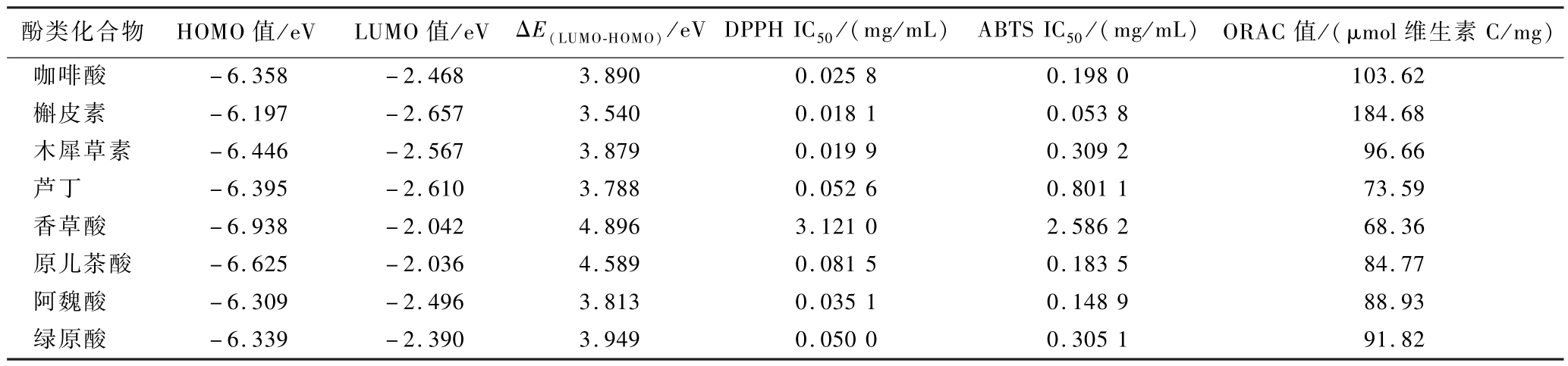
在氧化反应中,氧化剂的LUMO轨道能量水平越低,其氧化能力越强。研究表明,槲皮素等酚类化合物因具有较低的LUMO值而表现出较高的氧化能力[22]。即ΔE(LUMO-HOMO)值较小的化合物如槲皮素,其电子激发更容易,反应活性更高,具有较大的电子云密度[23]。据此,8种酚类化合物的反应活性排序为:槲皮素>芦丁>阿魏酸>木犀草素>咖啡酸>绿原酸>原儿茶酸>香草酸。在DPPH自由基清除率和ABTS阳离子自由基清除率实验中,槲皮素表现出最强的抗氧化活性香草酸和原儿茶酸的活性相对较弱。这一结果与通过能级差分析所得的抗氧化性顺序基本一致,进一步验证了通过量子化学参数预测抗氧化活性的可靠性。
将上述抗氧化活性结果与ΔE(LUMO-HOMO)进行相关性分析,结果如图7所示。ΔE(LUMO-HOMO)与DPPH自由基清除率和ABTS阳离子自由基清除率呈显著负相关。ΔE(LUMO-HOMO)值越小,电负性越高,电子云密度越大,电子激发能垒越低,抗氧化活性更强。IRFAN等[24]的研究同样说明了酚类化合物的ΔE(LUMO-HOMO)与其抗氧化活性显著相关,ΔE(LUMO-HOMO)越小,酚类化合物的抗氧化潜力越强,这与本实验的结果一致。ORAC值与ΔE(LUMO-HOMO)无相关性。其原因是由于DPPH自由基和ABTS阳离子自由基的模型主要基于单电子转移反应,而ORAC模型是基于氢原子转移反应[25]。
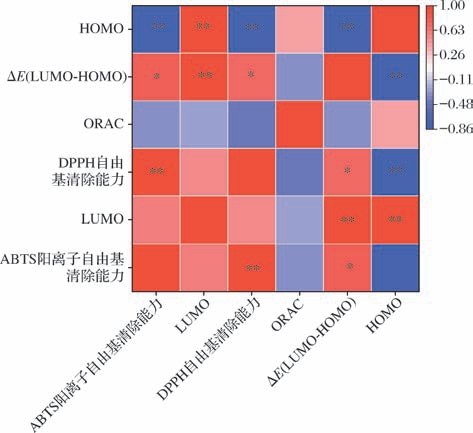
图7 银杏叶8种酚类化合物的LUMO、HOMO及ΔE(LUMO-HOMO)与其抗氧化活性的相关性
Fig.7 Correlation of LUMO,HOMO and ΔE(LUMO-HOMO)of 8 phenolic compounds from Ginkgo biloba leaves with their antioxidation
注:∗∗表示在P <0.01水平上极显著相关;∗表示在P <0.05水平上显著相关。
3 结论与讨论
本研究通过构建超声波辅助DES方法对银杏叶中酚类化合物进行了提取工艺的优化,获得的优化工艺条件为:DES为氯化胆碱-尿素(摩尔比1∶2)、含水量30%、料液比1∶20(g∶mL)、超声功率200 W、提取时间10 min,在此最优条件下,银杏叶酚类化合物的提取得率为96.70% (以咖啡酸、槲皮素、木犀草素、芦丁、香草酸、原儿茶酸、阿魏酸和绿原酸的总含量计),较传统80%甲醇方法提取得率提高了27.06%。
DPPH自由基清除、ABTS阳离子自由基清除和ORAC等抗氧化评价实验表明,槲皮素较其他7种酚类化合物的抗氧化活性更强,其DPPH自由基和ABTS阳离子自由基清除的IC50 值分别为0.018 1、0.053 8 mg/mL,ORAC值为184.68 μmol维生素C/mg。这些酚类化合物清除DPPH自由基、ABTS阳离子自由基的抗氧化能力与其ΔE(LUMO-HOMO)呈显著相关,但与其ORAC值无显著相关性。本实验研究结果将为银杏叶酚类化合物的高效提取以及其提取物在抗氧化功能食品的开发利用提供实践基础和理论依据。
[1]肖颗星.我国银杏产业国际竞争力战略研究[D].南京:南京林业大学,2018.XIAO K X.2018.Study on international competitiveness of Ginkgo industry in China[D].Nanjing:Nanjing Forestry University,2018.
[2]EISVAND F,RAZAVI B M,HOSSEINZADEH H.The effects of Ginkgo biloba on metabolic syndrome:A review[J].Phytotherapy Research,2020,34(8):1798-1811.
[3]付佳乐,耿直,郭亚敏,等.银杏叶总黄酮绿色提取工艺及抗氧化活性研究[J].化学与生物工程,2024,41(1):40-45.FU J L,GENG Z,GUO Y M,et al.Green extraction process and antioxidant activity of total flavonoids from Ginkgo biloba leaves[J].Chemistry &Bioengineering,2024,41(1):40-45.
[4]QIN H,HU X T,WANG J W,et al.Overview of acidic deep eutectic solvents on synthesis,properties and applications[J].Green Energy &Environment,2020,5(1):8-21.
[5]LIU L M,WANG Y T,ZHANG J C,et al.Advances in the chemical constituents and chemical analysis of Ginkgo biloba leaf,extract,and phytopharmaceuticals[J].Journal of Pharmaceutical and Biomedical Analysis,2021,193:113704.
[6]DONG Q H,CAO J,WU R,et al.Efficient removal of ginkgolic acids from Ginkgo biloba leaves crude extract by using hydrophobic deep eutectic solvents[J].Industrial Crops and Products,2021,166:113462.
[7]ZHANG Y,ZHANG C H,XU C,et al.Effect of geographical location and soil fertility on main phenolic compounds and fatty acids compositions of virgin olive oil from Leccino cultivar in China[J].Food Research International,2022,157:111207.
[8]SABIR S M,AHMAD S D,HAMID A,et al.Antioxidant and hepatoprotective activity of ethanolic extract of leaves of Solidago microglossa containing polyphenolic compounds [ J].Food Chemistry,2012,131(3):741-747.
[9]ZHU K X,LIAN C X,GUO X N,et al.Antioxidant activities and total phenolic contents of various extracts from defatted wheat germ[J].Food Chemistry,2011,126(3):1122-1126.
[10]JING P,ZHAO S J,RUAN S Y,et al.Quantitative studies on structure-ORAC relationships of anthocyanins from eggplant and radish using 3D-QSAR[J].Food Chemistry,2014,145:365-371.
[11]CHEN D P,WANG H.HOMO-LUMO energy splitting in polycyclic aromatic hydrocarbons and their derivatives[J].Proceedings of the Combustion Institute,2019,37(1):953-959.
[12]ŠALIC' A,BAJO M,CVJETKO BUBALO M,et al.Extraction of polyphenolic compounds from Ginkgo leaves using deep eutectic solvents:A potential solution for the sustainable and environmentally friendly isolation of biflavonoids[J].Industrial Crops and Products,2024,219:119068.
[13]SU M,JIN R Y,ZHU J,et al.Investigation of the microstructure and dynamical evolution following gradient hydration of deep eutectic solvent,with application to polyphenol extraction[J].ACS Sustainable Chemistry &Engineering,2024,12(5):1884-1896.
[14]GABRIELE F,CHIARINI M,GERMANI R,et al.Effect of water addition on choline chloride/glycol deep eutectic solvents:Characterization of their structural and physicochemical properties[J].Journal of Molecular Liquids,2019,291:111301.
[15]SAZALI A L,ALMASOUD N,AMRAN S K,et al.Physicochemical and thermal characteristics of choline chloride-based deep eutectic solvents[J].Chemosphere,2023,338:139485.
[16]KALYNIUKOVA A,HOLUŠA J,MUSIOLEK D,et al.Application of deep eutectic solvents for separation and determination of bioactive compounds in medicinal plants[J].Industrial Crops and Products,2021,172:114047.
[17]DHEYAB A S,ABU BAKAR M F,ALOMAR M,et al.Deep eutectic solvents (DESs) as green extraction media of beneficial bioactive phytochemicals[J].Separations,2021,8(10):176.
[18]WANG P X,CHENG C X,MA Y Q,et al.Degradation behavior of polyphenols in model aqueous extraction system based on mechanical and sonochemical effects induced by ultrasound[J].Separation and Purification Technology,2020,247:116967.
[19]ABDEL-MAGEED W M,BAYOUMI S A H,RADWAN A A,et al.Simmondsia chinensis:A rich source of bioactive flavonoids and lignans[J].Industrial Crops and Products,2014,60:99-103.
[20]LI X C,CHEN B,XIE H,et al.Antioxidant structure-activity relationship analysis of five dihydrochalcones[J].Molecules,2018,23(5):1162.
[21]PLATZER M,KIESE S,TYBUSSEK T,et al.Radical scavenging mechanisms of phenolic compounds:A quantitative structure-property relationship (QSPR) study[J].Frontiers in Nutrition,2022,9:882458.
[22]SARANYA M,AYYAPPAN S,NITHYA R,et al.Molecular structure,NBO and HOMO-LUMO analysis of quercetin on single layer graphene by density functional theory[J].Digest Journal of Nanomaterials and Biostructures,2018,13(1):97-105.
[23]HU X N,YUAN L,HAN L J,et al.Characterization of antioxidant and antibacterial gelatin films incorporated with Ginkgo biloba extract[J].RSC Advances,2019,9(47):27449-27454.
[24]IRFAN A,IMRAN M,KHALID N,et al.Molecular level interaction,HOMO-LUMO,MEP,UV-Vis,Hirshfeld,topological analysis,and in-vitro of isoflavones from Eremostachys vicaryi Benth.Ex Hook.f[J].Journal of Molecular Structure,2024,1303:137581.
[25]RODRÍGUEZ-BONILLA P,GANDÍA-HERRERO F,MATENCIO A,et al.Comparative study of the antioxidant capacity of four stilbenes using ORAC,ABTS +,and FRAP techniques[J].Food Analytical Methods,2017,10(9):2994-3000.