膳食脂肪的脂肪酸组成与结构深刻影响着机体调控脂质代谢、能量平衡及炎症反应等[1]。分析不同脂肪组分对健康的差异化影响,对优化膳食脂肪和开发功能性脂质产品具有重要价值。羊油因其独特风味和加工特性广泛应用于食品工业,但其较高的饱和脂肪酸(saturated fatty acids,SFA)与胆固醇含量常引发人们对健康的担忧[2]。油脂分提改性技术为解决这一矛盾提供了有效途径,可依据熔点差异将羊脂分离为性质稳定、功能特性各异的组分,显著改善了其食用品质与潜在营养特性[3]。新疆特色畜种阿勒泰羊的臀脂资源丰富(约占出栏体重的17%)[4],是极具开发价值的区域性动物油脂资源。充分利用分提技术对阿勒泰羊臀脂进行改性并科学评价其健康效应,对其高值化利用意义重大。
当前动物脂肪分提研究多集中于工艺优化与理化性质,其对机体深层代谢机制的影响则缺乏深入探讨。代谢紊乱不仅与脂肪摄入量相关,更与其塑造肠道菌群结构和功能的能力密切相关[5]。菌群代谢产生的短链脂肪酸(short chain fatty acids,SCFAs)是影响宿主健康的关键介质,其作为肠上皮细胞能量源及信号分子,能调控能量代谢、血糖稳态与炎症反应,其水平与肥胖、胰岛素抵抗等代谢性疾病密切关联[6-7]。研究表明,膳食脂肪的类型与结构显著影响SCFAs的合成[8],而SCFAs对肠道健康及疾病预防具有保护作用[9]。值得注意的是,脂肪不同熔点分提产物可通过影响消化吸收效率、血脂水平及炎症反应参与代谢调控[10],但其对SCFA的影响相关研究较少。
针对人们对羊油的健康顾虑及羊油深层代谢机制研究的不足问题,本研究以特色资源阿勒泰羊臀脂为研究对象,结合分提技术与动物实验,重点通过靶向代谢组学分析原脂及其分提产物对小鼠SCFAs的影响,科学评价其健康效应,为羊脂资源的高值化利用提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 油脂与试剂
阿勒泰羊臀脂,由新疆乌鲁木齐华凌牛羊屠宰场提供。原脂的制备:适量臀脂置于水浴中加热至100 ℃,保持2 h直至脂肪完全熔化。熔化过程中不断搅拌,随后冷却至60 ℃,通过双层纱布过滤得到原脂,并在-25 ℃下冻存备用。分提产物的制备:经过前期课题组对干法、水剂法、溶剂法、表面活性剂法、水酶法及超声辅助酶法养晶温度、降温速率和养晶时间等分提工艺的研究,确定阿勒泰羊臀脂分提工艺,将适量原脂加热至60 ℃完全融化后,按V(原脂)∶V(丙酮)=1∶2加入丙酮,充分摇匀,以6 ℃/h的速率降温至8 ℃,养晶16 h后,4 000 r/min离心15 min,离心分离高熔点硬脂(soild sheep oil,SSO)和低熔点液油(liquid sheep oil,LSO),在70 ℃、0.08 MPa条件下真空干燥4 h以去除油脂中的丙酮残留。
1.1.2 实验试剂
生理盐水,四川科伦药业股份有限公司;丙酮(分析纯),西安天茂化工有限公司;浓硫酸(分析纯),国药集团;37种脂肪酸甲酯混标(≥99.5%),源叶生物科技有限公司;甲基叔丁基醚(≥99.5%),CNW公司;短链脂肪酸(纯度均≥99.5%),Dr.Ehrenstorfer公司。
1.2 仪器与设备
Agilent 7890B气相色谱仪、HP-FFAP色谱柱(30 m ×250 μm ×0.25 μm),安捷伦科技有限公司;CD-2560毛细管气相色谱柱(100 m × 0.25 mm ×0.25 μm),上海安谱实验科技股份有限公司;GC-2030气相色谱、QP2020 NX质谱仪,岛津公司。
1.3 实验方法
1.3.1 阿勒泰羊臀脂及其分提产物基础理化指标的测定
熔点的测定参照GB/T 24892—2010《动植物油脂在开口毛细管中熔点(滑点)的测定》;酸价的测定参照GB 5009.229—2016《食品安全国家标准 食品中酸价的测定》;过氧化值的测定参照GB 5009.227—2023《食品安全国家标准 食品中过氧化值的测定》。
1.3.2 阿勒泰羊臀脂及其分提产物脂肪酸含量的测定
甲酯化按照REBECHI等[11]的方法并作适当修改。准确称取0.1 g油脂置于试管中,加入5 mL正己烷,振荡5 min使油脂完全溶解;随后加入2 mL 0.5 mol/L氢氧化钾-甲醇溶液,充分摇匀后置于60 ℃水浴中加热30 min完成甲酯化反应。静置1 h后分层,取上清液通过0.22 μm有机滤膜以去除杂质。根据HENMI等[12]的方法测定脂肪酸含量。使用装有CD-2560色谱柱的7890B气相色谱仪鉴定脂肪酸,使用氮气作为载气;进样口温度设定为240 ℃,采用100∶1分流模式,进样体积1 μL。色谱柱采用程序升温:初始温度140 ℃(保持5 min),以4 ℃/min升温至240 ℃(保持30 min)。氢火焰离子化检测器(flame ionization detector,FID)温度250 ℃,气体流速分别为:氢气30 mL/min、空气300 mL/min、氮气(尾吹气)30 mL/min。通过37种脂肪酸甲酯混合标准品进行脂肪酸定性,脂肪酸相对百分比含量采用面积归一化法计算。每个样品平行测定3次,结果取平均值。
1.3.3 实验动物及饲料
实验动物:40只清洁级昆明(KM)雄性小鼠(体重18~20 g),由新疆医科大学动物实验中心提供。试验期间饲养于新疆农业大学动物房,环境条件恒定为:温度(24±1) ℃、相对湿度50%~60%、12 h/12 h光暗循环。本研究经新疆农业大学实验动物福利伦理委员会审批通过(批准号:2024031)。基础日粮营养组成如表1所示。
表1 小鼠日粮营养成分
Table 1 Dietary nutrient composition of mice

1.3.4 动物试验分组设计及灌胃
雄性昆明小鼠40只,适应性喂养1周后,随机分为空白(CK)组、原脂(sheep oil,SO)组、SSO组和LSO组共4个处理组(饲喂时n=10,数据测定n=5),各组分别用阿勒泰羊臀脂原脂及其分提产物灌胃,CK组灌胃生理盐水。根据中国营养学会的统计调查,参照叶展等[13]的方法,按照我国居民日均烹调油脂摄入量为43.2 g/d,折算为灌胃剂量0.11 mg/20 g。每5 d称重并调整灌胃剂量,于第40天禁食12 h,不禁水,称重,断颈处死,测量相关指标。
1.3.5 盲肠内容物的采集
小鼠断颈处死后,于无菌操作台上取盲肠内容物,迅速装入冻存管保存在液氮中待测。
1.3.6 生长指标的测定
体重和体长的测定:每隔3 d在灌胃前进行体重和体长的测量,记录各组小鼠始末体重(g)和体长(cm)。
体重指数(body mass index,BMI)测定:小鼠BMI按照公式(1)计算:
李恩斯指数(Lee index,Lee’s)按照公式(2)计算:
1.3.7 脏器系数的测定
取小鼠各种脏器,使用生理盐水冲洗干净,用滤纸擦拭表面水分,并称重(g),按公式(3)计算:
1.3.8 短链脂肪酸的提取和分析
样品预处理:准确称取样本置于2 mL离心管中,加入1 mL超纯水涡旋振荡10 s,随后加入不锈钢研磨珠于冷冻研磨仪(40 Hz)处理4 min,冰水浴超声5 min,此研磨-超声循环重复3次。经4 ℃、5 000 r/min离心20 min后,移取0.8 mL上清液至新离心管,依次加入0.1 mL 50%(体积分数)H2SO4 和0.8 mL甲基叔丁基醚提取液(含25 mg/L 2-甲基戊酸内标),涡旋混匀10 s后水平振荡10 min,冰水浴超声10 min。混合液于4 ℃、10 000 r/min离心15 min,取上清液在-20 ℃静置30 min,最终移取澄清有机相,待测。
GC-MS条 件:采用HP-FFAP色谱柱(30 m ×250 μm ×0.25 μm),载气为高纯氦气(恒定流速1.2 mL/min),进样量1 μL,分流比5 ∶1,隔垫吹扫3 mL/min。程序升温:50 ℃保持1 min;150 ℃(50 ℃/min,保持1 min);170 ℃(10 ℃/min,保持0 min);240 ℃(25 ℃/min,保持1 min;40 ℃/min,保持1 min)。进样口温度220 ℃,离子源[电子轰击电离(electron impact,EI)模式]温度240 ℃,电离能量70 eV,四级杆温度150 ℃。
1.4 数据处理
实验统计数据以“平均值± 标准差”表示,理化指标每个样品重复测定3次,小鼠试验时每组重复测定5次,使用SPSS 27.0软件对实验数据进行单因素方差分析(one way analysis of variance,one way ANOVA),使用Origin 2024进行作图。
2 结果与分析
2.1 阿勒泰羊臀脂及其分提产物理化指标分析
对阿勒泰羊臀脂及其分提产物的熔点、酸价和过氧化值进行比较分析,由图1可知,SO组、SSO组和LSO组之间熔点、酸价和过氧化值指标均有显著性差异(P <0.01或P <0.001),熔点、酸价和过氧化值由高到低依次均为SSO >SO >LSO,SSO的熔点、酸价和过氧化值分别为43.67 ℃、0.73、0.11 mg/g,SO的熔点、酸价和过氧化值分别为34.17 ℃、0.60、0.09 mg/g,LSO的熔点、酸价和过氧化值分别为16.83 ℃、0.27、0.03 mg/g。
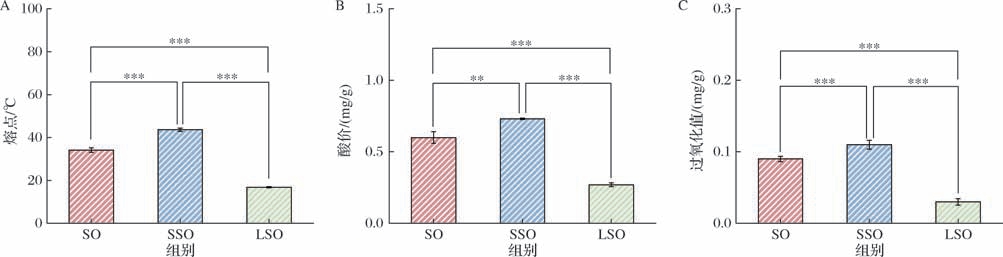
图1 阿勒泰羊臀脂及其分提产物理化指标
Fig.1 Altay sheep buttock fat and its fraction products
注:∗∗表示P <0.01,∗∗∗表示P <0.001(下同)。
A-阿勒泰羊臀脂及其分提产物熔点;B-阿勒泰羊臀脂及其分提产物酸价;C-阿勒泰羊臀脂及其分提产物过氧化值
2.2 阿勒泰羊臀脂及其分提产物主要脂肪酸含量分析
对阿勒泰羊臀脂及其分提产物主要脂肪酸进行比较,由表2可知,SO、SSO和LSO之间SFA、单不饱和脂肪酸(monounsaturated fatty acid,MUFA)和多不饱和脂肪酸(polyunsaturated fatty acid,PUFA)含量均有显著性差异(P <0.05),其中SFA含量LSO最低,为39.26%,其次为SO(47.47%),SSO最高,为65.04%,硬脂酸和棕榈酸含量差异与SFA趋势一致;不饱和脂肪酸(unsaturated fatty acid,UFA)含量最高为LSO(56.71%),其次为SO (49.01%),最低为SSO(32.28%);MUFA含量最高为LSO(50.50%),其次为SO(43.66%),最低为SSO(29.16%);而阿勒泰羊臀脂中含量比较多的油酸差异与MUFA的差异一致;PUFA含量最高为LSO(6.21%),其次为SO(5.35%),最低为SSO (3.11%);其中 LSO中 n-3PUFA、n-6PUFA均显著高于SO和LSO,分别为2.26% 和3.95%,与SO相比,n-3PUFA和n-6PUFA含量SSO均显著降低,分别为1.08%和2.03%(P <0.05)。
表2 阿勒泰羊臀脂及其分提产物脂肪酸组成
Table 2 Fatty acid composition of Altay sheep buttocks fat and its extracted products
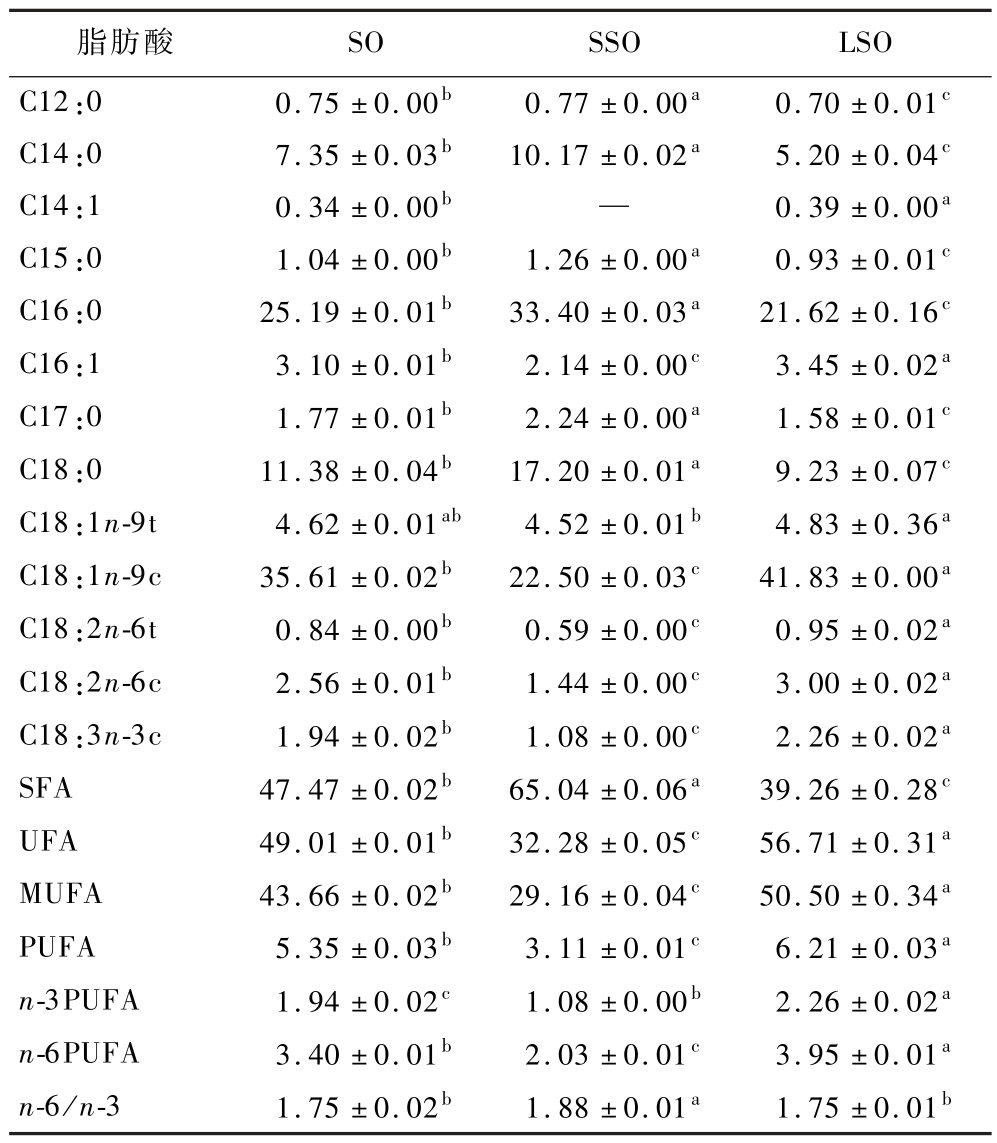
注:—表示未检出;同一行字母不同则为有显著性差异(P <0.05),字母相同则为没有显著性差异(P >0.05)(下同)。
2.3 阿勒泰羊臀脂及其分提产物对小鼠生长指标的影响
小鼠体重体、长增长量及BMI和Lee’s如图2所示,经过40 d灌胃后,CK组体重增长量最低,为13.32 g,其次为LSO组,体重增长量为14.32 g,且与CK组间无显著性差异(P >0.05),SO组和SSO组体重增长量显著高于CK组(P <0.05或P <0.001),分别为16.52、19.02 g;CK组体长增长量最低,为3.18 cm,SO组、SSO组和LSO组体长增长量之间均无显著性差异(P >0.05),分别为3.44、3.58、3.62 cm。与CK组BMI(0.32)相比,SO、SSO、LSO组BMI均升高,分别为0.33、0.35、0.33,其中SSO组与CK组有显著性差异(P <0.01),而SO组和LSO组与CK组无显著性差异(P >0.05);与CK组Lee’s(302.82)相比,SO组和SSO组Lee’s分别为304.93和312.27,LSO组Lee’s降低至300.46,其中SSO组与CK组有显著性差异(P <0.05),而SO组和LSO组与CK组无显著性差异(P >0.05)。
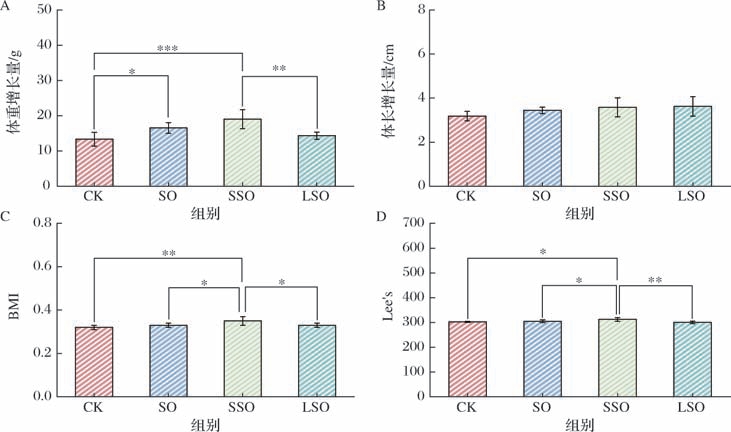
图2 阿勒泰羊臀脂及其分提产物摄入后小鼠生长指标
Fig.2 Growth indexes of Altay sheep buttocks and its fractions after ingestion
注:∗表示P <0.05(下同)。
A-体重增长量;B-体长增长量;C-BMI;D-Lee’s
2.4 阿勒泰羊臀脂及其分提产物对小鼠脏器系数的影响
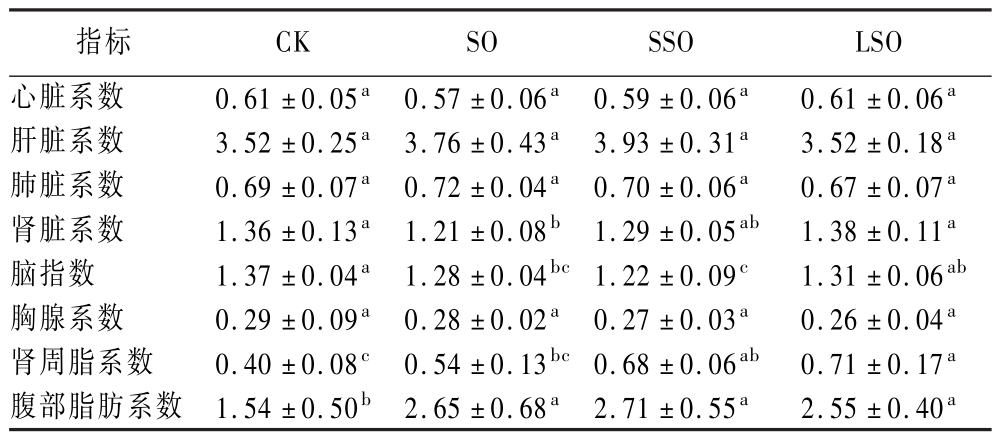
由表3可知,不同分提产物对于小鼠脏器系数有一定影响。40 d饲养期结束后,心脏系数、肝脏系数、肺脏系数和胸腺系数在各组之间均无显著性差异(P >0.05);肾脏系数CK组(1.36)、SSO组(1.29)和LSO组(1.38)之间无显著性差异(P >0.05),SO组(1.21)肾脏系数最低,且与CK组和LSO组之间有显著性差异(P <0.05);脑指数CK组最高为1.37,其次为LSO组1.31,其与CK组之间无显著性差异(P >0.05),SO组和SSO组脑指数与CK组相比均显著性降低(P <0.05),其中SSO组脑指数最低为1.22,而SSO组和LSO组有显著性差异(P <0.05);肾周脂系数LSO组(0.71) 最高,其次为SSO组(0.58),CK组(0.40)最低,且LSO组和SSO组与CK组有显著性差异(P <0.05),而SO组与CK组无显著性差异(P >0.05);腹部脂肪系数CK组最低为1.54,SSO组最高为2.71,其次为SO组和LSO组分别为2.65和2.55。
表3 阿勒泰羊臀脂及其分提产物摄入后小鼠脏器系数
Table 3 Organ coefficients of Altay sheep buttocks and its fractions after ingestion
2.5 阿勒泰羊臀脂及其分提产物对小鼠盲肠短链脂肪酸的影响
2.5.1 主成分分析(principal component analysis,PCA)
PCA是一种无监督模式识别的数据统计分析方法,可初步了解样品间的代谢差异以及组内的变异程度[14]。对摄入阿勒泰羊臀脂及其分提产物后小鼠盲肠SCFAs进行PCA,结果见图3。PCA散点图(PC1:40.9%;PC2:23.9%);各组之间呈现不同程度的分离,其中SSO组与CK组、SO组、LSO组分离最为明显,表明摄入阿勒泰羊臀脂分提产物后小鼠盲肠SCFAs存在显著差异,且摄入SSO后差异最为显著,可能是因为SSO含有更高含量的SFA和更低的UFA;然而SO组与CK组的分离程度较低,表明小鼠摄入阿勒泰羊臀脂原脂后,其盲肠SCFAs组成差异不显著;推测这可能是由于肠道微生物代谢的冗余性,进而产生了代谢补偿所致;同时,同一组内样品聚集紧密,组内变异度较小重复性好。
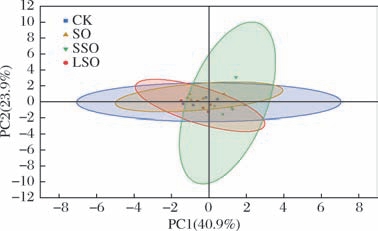
图3 阿勒泰羊臀脂及其分提产物摄入后小鼠盲肠短链脂肪酸PCA图
Fig.3 PCA diagram of short-chain fatty acids in the cecum of Altay sheep buttocks and its extracts after ingestion of mice in the paste
2.5.2 正交偏最小二乘判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA)
为了探索各组之间的代谢产物差异,使用OPLSDA模型比较各组之间的差异变量,并获取投影变量重要性(variable importance in projection,VIP) 值。R2Y和Q2 值接近1,表示模型具有更好的建模和预测能力。此外,建立的OPLS-DA模型经过了200次响应置换测试的验证,以检验模型是否存在过拟合。在正负离子模式下,各组有明显的分离。如图4置换检验结果显示,所有的OPLS-DA模型均不存在过拟合现象,具有良好的预测能力。因此可进行下一步差异代谢物的分析。
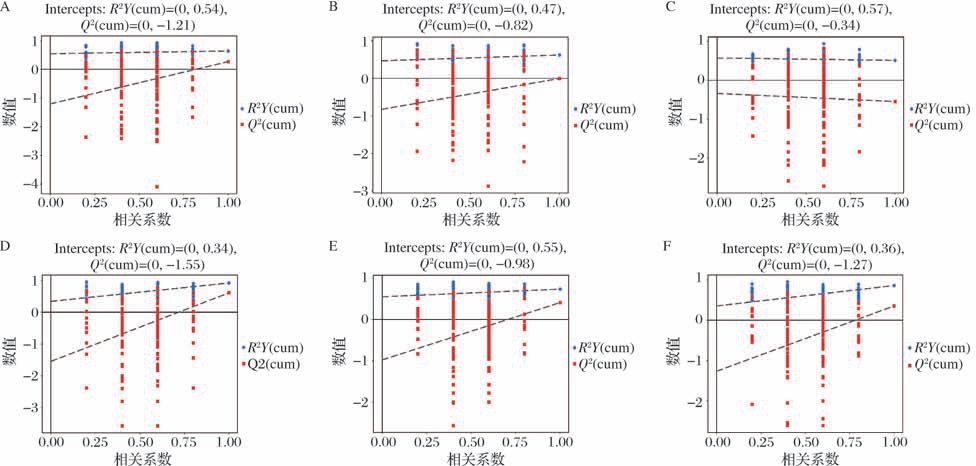
图4 阿勒泰羊臀脂及其分提产物摄入后小鼠盲肠短链脂肪酸置换检验结果点状图
Fig.4 Dot plot of short-chain fatty acid replacement test results in mouse cecum after ingestion of Altay sheep buttock fat and its fractions
A-CK组VS SO组;B-CK组VS SSO组;C-CK组VS LSO组;D-SO组VS SSO组;E-SO组VS LSO组;F-SSO组VS LSO组
2.5.3 热图分析
图5展示了阿勒泰羊臀脂及其分提产物摄入后小鼠在多种SCFAs上的相对含量变化。热图的颜色从蓝色到红色表示代谢物相对含量从低到高。
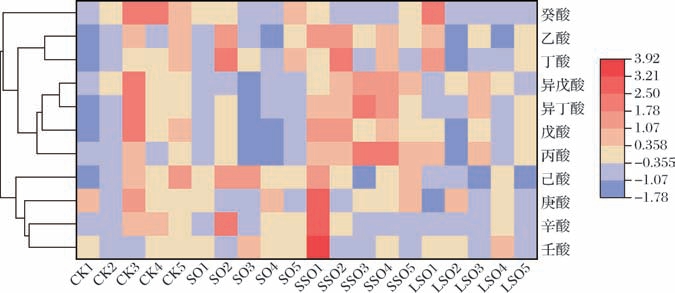
图5 阿勒泰羊臀脂及其分提产物摄入后小鼠盲肠SCFAs热图
Fig.5 Heatmap of SCFAs in the cecum of mice after intake of Altai sheep fat and its fractionated products
CK组代谢特征:在大部分SCFAs上,CK组的相对含量处于中等水平,没有特别突出的高或低表达代谢物。SO组代谢特征:与CK组相比,SO组丁酸和乙酸含量显著升高,丙酸含量显著降低。这说明小鼠摄入原脂后菌群平衡可能被破坏,从而影响短链脂肪酸的代谢,影响小鼠的肠道健康[15]。SSO组代谢特征:与CK组和SO组相比,SSO组SCFAs的相对含量整体较高,尤其是异戊酸和异丁酸,其相对含量显著高于其他组。与CK组相比,SSO组在大部分代谢物上的相对含量较高。这说明SSO的摄入对小鼠的影响较为复杂,可能引发肠道的炎症和机体代谢紊乱。LSO组代谢特征:LSO组在短链脂肪酸上的相对含量整体较为均衡,没有明显的高或低表达代谢物。与CK组和SSO组相比,LSO组在异戊酸和异丁酸上的相对含量则较低;与SO组相比,LSO组在丙酸、戊酸和癸酸相对含量较高。推测随着小鼠摄入低熔点液脂,能够抑制有害菌的生长,增强肠道黏膜,维持肠道健康。
综上所述,从热图的聚类结果来看,不同油脂的摄入对机体短链脂肪酸的代谢产生了不同的影响,导致各组在代谢特征上存在差异,推测低熔点液油的摄入对小鼠肠道健康有一定的调节作用。
2.5.4 k-means分析
图6展示了基于k-means聚类分析的代谢物标准化强度变化趋势。将所有分组中鉴定得到全部代谢物的相对含量进行z-score标准化,根据代谢物标准化强度在各处理组中的变化趋势分为4个聚类(聚类1~ 聚类4),每个聚类包含不同数量的代谢物。x轴表示阿勒泰羊臀脂及其分提产物灌胃小鼠,y轴表示代谢物的标准化强度。
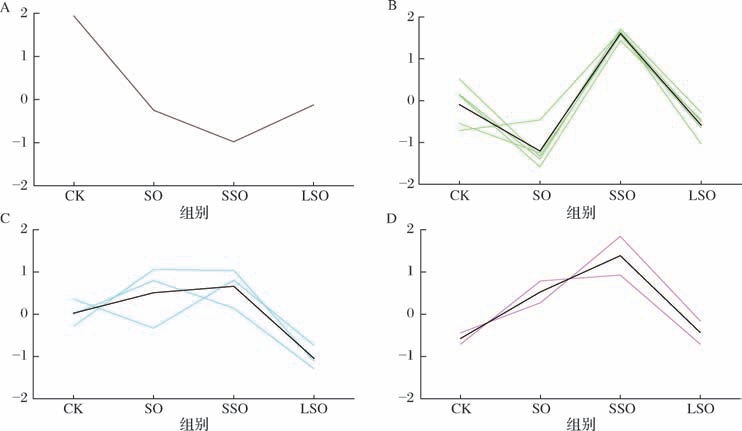
图6 阿勒泰羊臀脂及其分提产物摄入后小鼠盲肠短链脂肪酸k-means图
Fig.6 K-means diagram of short-chain fatty acids in the cecum of Altay sheep buttocks and its fractions after ingestion
A-聚类1(1个代谢物);B-聚类2(5个代谢物);C-聚类3(3个代谢物);D-聚类4(2个代谢物)
聚类1(癸酸)变化趋势:在CK组中标准化强度最高,随后在SO组保持较低水平,SSO组再次下降,LSO组回升。特征:该代谢物在CK组中表现出显著的高表达,而在其他组中则相对较低,可能表明阿勒泰羊臀脂及其分提产物对癸酸的产生或代谢有显著影响。聚类2(乙酸、丙酸、戊酸、异丁酸和异戊酸)变化趋势:整体呈现波动变化,在CK组中强度中等,SO下降,SSO组上升,LSO组再次下降至与CK组相近水平。特征:乙酸、丙酸、戊酸、异丁酸和异戊酸的强度在不同处理组间波动较大,没有明显的单一上升或下降趋势,反映了这些代谢物对不同油脂灌胃的复杂响应。聚类3(己酸、庚酸和辛酸)变化趋势:CK组中强度中等,SO组和SSO组中强度上升,LSO组强度较低。特征:己酸、庚酸和辛酸在原脂和高熔点硬脂灌胃小鼠中表现出较高的强度,而在液油相关处理组中强度较低,提示它们可能与原脂和高熔点硬脂中SFA含量较高,低熔点液油中UFA含量较高有关,从而影响小鼠的代谢途径。聚类4(丁酸和壬酸)变化趋势:CK组中强度较低,SO、组和SSO组上升,SSO组具有较高水平,LSO组下降至与CK组相似强度。特征:丁酸和壬酸在SSO组中表现出最高的强度,表明高熔点硬脂灌胃可能对这些代谢物的产生或代谢有显著影响。
通过k-means聚类分析,可以观察到不同处理组对代谢物强度的多样化影响。聚类1和聚类4中的代谢物在特定灌胃组中表现出显著的高或低表达,这可能与相应油脂的特定代谢效应有关。而聚类2和聚类3中的代谢物则显示出更复杂的响应模式,表明它们可能参与了多种代谢途径,受到综合影响。这些结果有助于进一步探究阿勒泰羊臀脂及其分提产物灌胃对小鼠代谢网络的具体作用机制。
2.5.5 代谢物的KEGG富集分析
根据代谢物在KEGG代谢通路中的富集结果,由图7可知,摄入阿勒泰羊臀脂及其分提产物后对小鼠碳水化合物代谢、消化系统和脂质代谢等代谢通路有显著性的影响,从碳水化合物代谢通路来看,丙酸酯代谢和丁酸酯代谢各组之间上调与下调无显著性差异(P >0.05),与CK组相比,SO组和SSO组糖酵解/糖异生和丙酮酸代谢呈显著上调趋势(P <0.05),而LSO组糖酵解/糖异生和丙酮酸代谢呈显著下调趋势(P <0.05);在消化系统代谢通路方面,与CK组相比,SO组和LSO组,蛋白质消化吸收呈显著下调趋势(P <0.001),碳水化合物消化吸收呈显著上调趋势(P <0.001),SSO组蛋白质消化吸收和碳水化合物消化吸收均呈显著上调趋势(P <0.001);在能量代谢、辅助因子和维生素代谢通路方面各组上调与下调趋势没有显著性(P >0.05);在脂质代谢通路方面,与CK组相比,LSO组显著下调(P <0.01);在内分泌和代谢疾病、聚糖生物合成和代谢、神经系统、牛磺酸和次牛磺酸代谢等通路方面,与CK组相比,SO组和SSO组内分泌和代谢疾病、聚糖生物合成和代谢、神经系统等通路均显著上调,LSO组显著下调(P <0.05或P <0.01)。
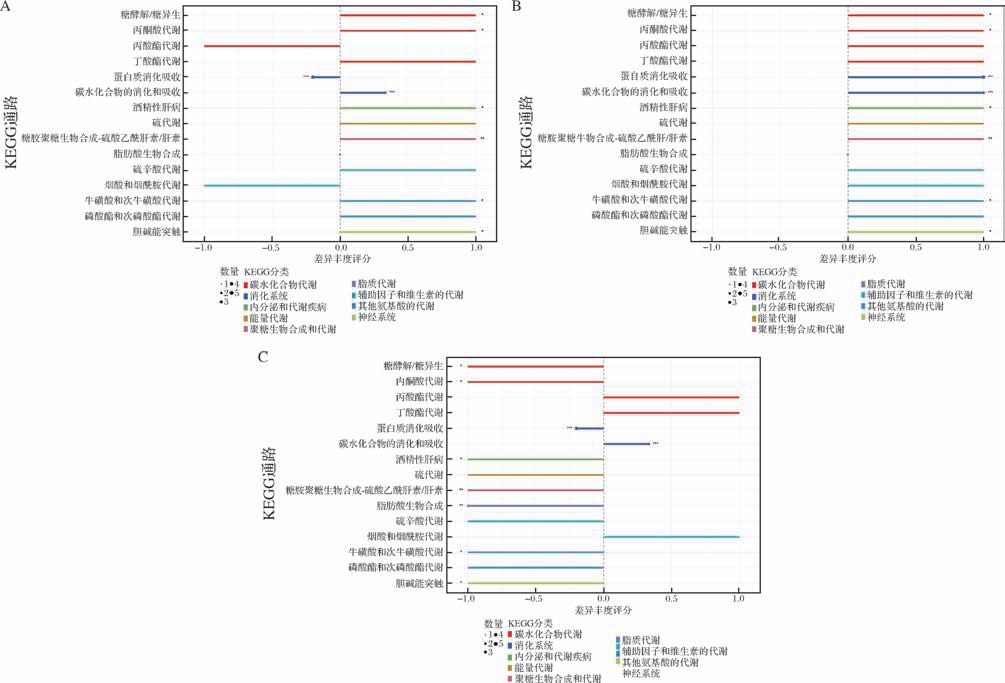
图7 阿勒泰羊臀脂及其分提产物摄入后小鼠盲肠短链脂肪酸KEGG富集差异得分图
Fig.7 Differential score of KEGG enrichment of short-chain fatty acids in the cecum of Altay sheep buttocks and their extracts after ingestion
A-CK组VS SO组;B-CK组VS SSO组;C-CK组VS LSO组
2.6 相关性分析
对小鼠摄入阿勒泰羊臀脂和其分提产物的脂肪酸组成,摄入后肥胖指数、脂肪系数及盲肠SCFAs含量进行相关性分析,由图8可知,小鼠SFA的摄入与小鼠BMI、Lee’s、肾周脂系数、腹部脂肪系数、乙酸、丁酸和壬酸呈显著正相关(P <0.05),与癸酸呈显著负相关(P <0.05);小鼠MUFA、PUFA的摄入与小鼠己酸和辛酸显著正相关(P <0.05);小鼠BMI、Lee’s的变化与小鼠肾周脂系数、腹部脂肪系数、乙酸、丁酸和壬酸呈显著正相关(P <0.05),与癸酸呈显著负相关(P <0.05);小鼠肾周脂系数、腹部脂肪系数的变化与小鼠乙酸、丁酸和壬酸呈显著正相关(P <0.05),与癸酸呈显著负相关(P <0.05);小鼠乙酸的变化与小鼠丁酸和壬酸呈显著正相关(P <0.05),与癸酸呈显著负相关(P<0.05);小鼠戊酸、庚酸、异丁酸和异戊酸的变化之间呈显著正相关(P<0.05)。
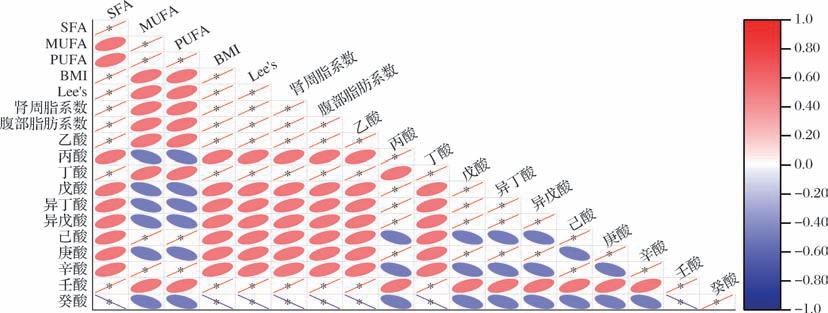
图8 相关性分析图
Fig.8 Correlation analysis chart
注:红色表示上调,蓝色表示下调,∗表示P <0.05。
3 讨论
本研究发现SSO具有较高的SFA,LSO不饱和脂肪酸远高于SO和SSO。油脂的熔点与脂肪酸组成具有显著相关性。SSO的高熔点与其SFA含量直接相关,因SFA分子间排列紧密,晶格能高,导致熔点升高[16]。相反,LSO的低熔点反映其高UFA含量,不饱和双键的存在破坏分子排列,降低熔点[17]。SO经分提后,SSO的SFA含量提升,而LSO的MUFA显著升高,表明分提技术可有效分离不同饱和度的脂肪酸,改变油脂物理特性,MAGALHÃES等[18]通过干法分提的方式从马草仁油中分提出了富含UFA且熔点及氧化稳定性较高的组分,本文研究结果与之相近。酸价和过氧化值作为反映油脂氧化的指标,与SO相比,SSO酸价和过氧化值显著提高,LSO显著下降,说明分提过程可能通过去除分离油脂氧化产物,降低脂质氧化风险[19]。
小鼠摄入阿勒泰羊臀脂及其分提产物后,SSO组小鼠体重增长量、BMI及Lee’s均显著高于CK组,且其腹部脂肪系数最高,肾周脂系数显著高于CK组,显示小鼠摄入SSO后有肥胖的风险;LSO组小鼠体重增长量、BMI及Lee’s与CK组小鼠相比均无显著性差异(P >0.05),且其腹部脂肪系数相较于SO组和SSO组增长量最小。相关性分析揭示,小鼠摄入阿勒泰羊臀脂及其分提产物SFA含量与肥胖指标呈显著正相关,BUETTNER等[20]研究发现富含SFA的猪油更容易诱导肥胖,也与本研究相似。此外,SSO组显著上调糖酵解/糖异生通路,驱动葡萄糖向脂肪转化,解释了小鼠摄入SSO后通过影响乙酸、丁酸等短链脂肪酸影响小鼠代谢通路,进而影响肥胖;而LSO组则下调糖酵解/糖异生通路,印证LSO通过抑制能量储存途径缓解肥胖[21]。XIANG等[22]研究发现糖异生通路持续激活是肥胖/糖尿病的关键特征,而下调糖异生通路能够改善肥胖,与本文结果一致。
SSO组异戊酸和异丁酸含量较CK组升高,这与SFA摄入量呈正相关。这2种支链SCFAs是蛋白质腐败发酵的标志物,其积累预示肠道菌群失调[23]。PCA证实SSO组代谢产物显著分离,且KEGG分析显示SSO组内分泌和代谢疾病通路激活,形成高SFA摄入,支链短链脂肪酸含量增加,炎症通路激活的代谢机制。LSO组丙酸和戊酸含量较SO组高,丙酸、戊酸能够降低胆固醇和脂质的合成、调节食欲与体重、降低肠道黏膜通透性从而减轻炎症[24],LSO抑制异丁酸和异戊酸积累并提升癸酸;同时,LSO组显著下调神经系统与内分泌和代谢疾病通路,体现为LSO的摄入通过影响短链脂肪酸含量维持小鼠代谢稳态。
4 结论
本研究通过溶剂法对阿勒泰羊臀脂进行分提改性,获得SSO和LSO,各分提产物理化性质及营养成分存在显著性差异,并且定向富集羊臀脂中的SFA和UFA,通过动物实验系统评估了其对小鼠健康的影响,摄入LSO对小鼠肥胖指数、主要脏器系数及短链脂肪酸无显著负面影响,且LSO氧化稳定性更优。此外,LSO摄入后盲肠支链短链脂肪酸含量显著降低,糖酵解/糖异生、神经系统、内分泌和代谢疾病等通路下调,推测将有助于降低炎症的发生,减少能量储存,缓解肥胖。综合表明,经分提后的LSO健康效应最优,为阿勒泰羊臀脂在食品工业中的合理化应用提供了科学依据,支持其作为功能性脂质产品的开发潜力。
[1]SWINBURN B A,SACKS G,HALL K D,et al.The global obesity pandemic:Shaped by global drivers and local environments[J].The Lancet,2011,378(9793):804-814.
[2]MICHA R,MOZAFFARIAN D.Saturated fat and cardiometabolic risk factors,coronary heart disease,stroke,and diabetes:A fresh look at the evidence[J].Lipids,2010,45(10):893-905.
[3]DEFFENSE E.Milk fat fractionation today:A review[J].Journal of the American Oil Chemists’ Society,1993,70(12):1193-1201.
[4]王金泉,王肖燕,叶青,等.阿勒泰大尾羊与小尾寒羊不同组织FTO基因的检测[J].动物医学进展,2013,34(12):84-88.WANG J Q,WANG X Y,YE Q,et al.Detection of FTO gene in different tissues of Altay big-tailed sheep and small-tailed Han sheep[J].Progress in Veterinary Medicine,2013,34(12): 84-88.
[5]WANG H R,TIAN J X,MI J.Clinical effectiveness of fecal microbial transplantation for metabolic syndrome:Advances in clinical efficacy and multi-omics research[J].Current Research in Microbial Sciences,2025,9:100415.
[6]MAZHAR M,ZHU Y,QIN L K,et al.The interplay of dietary fibers and intestinal microbiota affects type 2 diabetes by generating short-chain fatty acids[J].Foods,2023,12(5):1023.
[7]XIONG J,CHEN X,ZHAO Z J,et al.A potential link between plasma short-chain fatty acids,TNF-α level and disease progression in non-alcoholic fatty liver disease:A retrospective study[J].Experimental and Therapeutic Medicine,2022,24(3):598.
[8]SONG A K,LI Y B,WANG W,et al.Revealing the effect of sea buckthorn oil,fish oil and structured lipid on intestinal microbiota,colonic short chain fatty acid composition and serum lipid profiles in vivo[J].Natural Products and Bioprospecting,2024,14(1):41.
[9]LOUIS P,HOLD G L,FLINT H J.The gut microbiota,bacterial metabolites and colorectal cancer[J].Nature Reviews Microbiology,2014,12(10):661-672.
[10]MALPUECH-BRUGÈRE C,VERBOEKET-VAN DE VENNE W P H G,MENSINK R P,et al.Effects of two conjugated linoleic acid isomers on body fat mass in overweight humans[J].Obesity Research,2004,12(4):591-598.
[11]REBECHI S R,VÉLEZ M A,VAIRA S,et al.Adulteration of Argentinean milk fats with animal fats:Detection by fatty acids analysis and multivariate regression techniques[J].Food Chemistry,2016,192:1025-1032.
[12]HENMI A,SHOJI M,NOMURA M,et al.Fatty acid composition and applications of Eriobotrya japonica seed oil[J].Journal of Oleo Science,2019,68(7):599-606.
[13]叶展,刘元法.脂肪酸摄入形式对肠屏障的影响及食用油摄入模式探讨[J].中国食品学报,2025,25(2):451-462.YE Z,LIU Y F.Influence of fatty acid intake forms on intestinal barrier and exploration of edible oil intake patterns[J].Journal of Chinese Institute of Food Science and Technology,2025,25(2):451-462.
[14]于强,杨敏,潘萍,等.基于广泛靶向代谢组学技术的掌叶覆盆子不同部位代谢产物差异分析[J].食品科学,2025,46(17):231-243.YU Q,YANG M,PAN P,et al.Analysis on the difference of metabolites in different parts of Rubus chingii Hu based on widely targeted metabolomics[J].Food Science,2025,46(17):231-243.
[15]YE Z,CAO C,LI Q,et al.Different dietary lipid consumption affects the serum lipid profiles,colonic short chain fatty acid composition and the gut health of Sprague Dawley rats[J].Food Research International,2020,132:109117.
[16]ZHOU J,MAO Y L,LEE Y Y,et al.Physical,textural and crystallization characteristics of different chain length diacylglycerol-based solid fats[J].Journal of the American Oil Chemists’ Society,2024,101(11):1113-1126.
[17]GUNSTONE F D.Fatty Acid and Lipid Chemistry[M].Boston,MA:Springer,2012:352-368.
[18]MAGALHÃES K T,DE SOUSA TAVARES T,NUNES C A.The chemical,thermal and textural characterization of fractions from Macauba kernel oil [ J].Food Research International,2020,130:108925.
[19]FATOUH A E,SINGH R K,KOEHLER P E,et al.Physical,chemical and stability properties of buffalo butter oil fractions obtained by multi-step dry fractionation[J].Food Chemistry,2005,89(2):243-252.
[20]BUETTNER R,SCHÖLMERICH J,BOLLHEIMER L C.High-fat diets:Modeling the metabolic disorders of human obesity in rodents[J].Obesity,2007,15(4):798-808.
[21]金其贯,张奥英,刘瑜,等.有氧运动和补充魔芋葡甘聚糖通过调节PI3K/FoxO1通路有效预防高脂膳食大鼠肝脏胰岛素抵抗的形成[J].中国运动医学杂志,2018,37(8):685-691.JIN Q G,ZHANG A Y,LIU Y,et al.Aerobic exercise and konjac glucomannan administration effectively prevent the formation of hepatic insulin resistance in high-fat-diet rats through regulating the PI3K/FoxO1 pathway[J].Chinese Journal of Sports Medicine,2018,37(8):685-691.
[22]XIANG L P,ZHOU B,LUO Y C,et al.Hub biomarkers and their clinical relevance in glycometabolic disorders: A comprehensive bioinformatics and machine learning approach[J].Chinese Medical Journal,2025,138(16):2016-2027.
[23]姜菲,赖琦,高彦华,等.添加异丁酸、2-甲基丁酸和戊酸对牦牛瘤胃体外发酵参数和养分降解率的影响[J].动物营养学报,2022,34(9):5915-5930.JIANG F,LAI Q,GAO Y H,et al.Effects of supplementing isobutyric acid,2-methylbutyric acid and valeric acid on in vitro rumen fermentation parameters and nutrient degradation rates of yaks[J].Chinese Journal of Animal Nutrition,2022,34(9):5915-5930.
[24]ZHANG S,ZHANG Y J,LI J,et al.Butyrate and propionate are negatively correlated with obesity and glucose levels in patients with type 2 diabetes and obesity[J].Diabetes,Metabolic Syndrome and Obesity:Targets and Therapy,2024,17:1533-1541.