食窦魏斯氏菌(Weissella cibaria)作为典型的异型发酵乳酸菌[1],广泛存在于各种发酵蔬菜、乳制品、土壤及胃肠道等环境中[2]。其在发酵过程中能够产生有机酸、胞外多糖和细菌素等多种活性物质[3],具有抑制病原体的活性、增强人体免疫功能、缩短发酵周期及改善食品风味等作用。然而,微生物发酵过程中积累的乳酸、乙酸等有机酸,会导致发酵环境pH值逐渐下降[4],在强酸条件下,菌体的代谢能力会受到抑制,表现为生长缓慢、活性降低、发酵性能减弱,从而影响原料利用率,增加生产成本。因此,选育耐酸性强的食窦魏斯氏菌对提升发酵性能和开发功能性食品具有重要意义[5]。
在发酵工业中,优良菌株的选育主要通过自然筛选或诱变育种的方法完成。诱变育种常采用物理诱变、化学诱变及复合诱变。紫外诱变(ultraviolet,UV)作为物理诱变的常用方法,常采用的波长为200~300 nm的紫外线辐射,该波段可诱导DNA中相邻嘧啶碱基形成二聚体,干扰DNA的复制和转录,从而产生突变体[6]。甲基磺酸乙酯(ethyl methylsulfone,EMS)是一种高效的烷化剂,能够修饰DNA结构,其作用机制是通过烷基化鸟嘌呤(G),形成O6-乙基鸟嘌呤,导致该碱基与胸腺嘧啶(T)错误配对,而非正常的胞嘧啶(C),从而诱发点突变[7-8]。此外,复合诱变育种是结合物理与化学诱变方法来发挥协同效应,可显著提高突变率和育种效率[9]。
近年来,很多菌株并不能满足实际生产的需求,耐酸性菌株资源的筛选已成为当前研究的重点。随着微生物基因组测序的发展,大量耐酸相关基因被鉴定出来。林哲[10]通过对从饮料中分离得到的一株乳酸杆菌进行高通量测序分析发现,在环境信息相关的代谢途径中,多个与膜转运相关的基因可能影响菌株的生理特性,提示该菌株可能具备高效利用环境糖类或合成细菌素的能力。LI等[11]对高耐酸保加利亚乳杆菌进行全基因组测序时,发现赖氨酸合成途径中的3个关键基因表达显著上调,推测其通过调节能量代谢以适应酸性环境。本研究基于实验室菌种资源,对从辣白菜中筛选出的食窦魏斯氏菌进行复合诱变,结合体外益生特性和基因组分析,为后续揭示耐酸分子机制及工业应用提供依据。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
食窦魏斯氏菌W25:从泡菜中分离得到的菌株,由延边大学食品科学实验室菌种保藏库提供。
1.1.2 培养基
MRS肉汤培养基、MRS琼脂培养基,青岛海博生物技术有限公司;MRS-硫代硫酸钠培养基:称取0.5 g硫代硫酸钠溶于250 mL MRS肉汤培养基。
1.1.3 试剂
1 × PBS,青岛海博生物技术有限公司;EMS,西格玛化学公司;丙三醇、胃蛋白酶,北京奥博星生物技术有限责任公司;氯化钠、氯化钾、柠檬酸、柠檬酸钠、磷酸氢二钾、磷酸氢二钠、硫代硫酸钠、巯基乙酸钠、无水乙醇、二甲苯、氢氧化钠、盐酸,天津科密欧化学试剂有限公司;牛胆盐,广东环凯威微生物科技有限公司。
1.2 仪器与设备
SX-700高压蒸汽灭菌器,日本TOMY公司;SWCJ-IFD超净工作台,上海新苗医疗器械制造有限公司;U-3900紫外可见分光光度计,日本日立公司;Z 400K高速冷冻离心机,莱比信(中国)科技发展有限公司;QY-20紫外诱变灯,江苏巨光光电科技有限公司;SP-Max3500FL多功能荧光酶标仪,上海闪谱生物科技有限公司。
1.3 实验方法
1.3.1 UV诱变
在暗室中离心对数期菌液(4 ℃,7 000 r/min,5 min),生理盐水重悬至107 CFU/mL。紫外灯预热30 min后,取菌悬液于8 W紫外灯下30 cm处分别照射0、15、30、45、60、75、90 s(0 s为对照组),照射后稀释至105 CFU/mL涂布,30 ℃避光培养24 h,观察并记录菌落数并计算致死率[公式(1)],确定最佳诱变时间。
1.3.2 EMS诱变
分别用0.5% 和1.0% (体积分数)EMS处理5个时间梯度(0、15、30、45、60 min),以不加EMS的菌悬液作为对照组。加入5 g/L的Na2S2O3溶液终止反应后稀释至105 CFU/mL涂布,30 ℃恒温培养24 h,按公式(1)计算致死率,确定最佳诱变剂量。
1.3.3 UV-EMS复合诱变
选取1.3.1节方法中耐酸性最高菌株,按1.3.2节方法进行UV-EMS复合诱变。
1.3.4 EMS-UV复合诱变
选取1.3.2节方法中耐酸性最高菌株,按1.3.1节方法进行EMS-UV复合诱变。
1.3.5 突变株耐酸性筛选
参考尹义敏等[12]的方法,将突变株传代2次后接种MRS培养基,30 ℃恒温中培养24 h,再以2%接种量分别转移至pH 3.0、2.0、1.5的MRS肉汤培养24 h,测定OD600值并按公式(2)计算相对生长率:
式中:a,pH 6.3培养24 h的OD600值;b,pH 6.3培养0 h的OD600值;c,待测pH培养24 h的OD600值;d,待测pH培养0 h的OD600值。
1.3.6 生长曲线和产酸能力的测定
生长曲线:以2%接种量接种至MRS肉汤30 ℃恒温培养24 h,每2 h测OD600 值,绘制24 h生长曲线。产酸能力的测定:以2% 接种量接种至MRS肉汤30 ℃恒温培养24 h,用0.1 mol/L NaOH溶液滴定至终点,出现粉红色后维持30 s,按公式(3)计算产酸能力[以乳酸当量计,每一千万(107)个菌体细胞在此条件下发酵1 mL脱脂乳产生1 μg乳酸计为1个活力单位(U)]:
式中:c,NaOH浓度,mol/L;v1,NaOH消耗量,mL;v2,菌液体积,mL;M,乳酸摩尔质量,g/mol;n,菌液活菌数量,CFU/mL。
1.3.7 耐胃肠液能力的测定
参照梁楚容等[13]的方法,人工模拟胃液:将0.1 g NaCl和0.175 g胃蛋白酶溶于无菌水,使用HCl溶液调pH值至3.0、2.0和1.5后,分别定容至50 mL,过滤除菌;人工模拟肠液:称取0.34 g KH2 PO4 溶于25 mL无菌水中,用NaOH溶液将pH值调至6.8,与0.5 g胰蛋白酶混合定容至100 mL,过滤除菌。取对数期菌液离心洗涤(4 ℃,7 000 r/min,5 min),用1 ×PBS调至107 CFU/mL。取1 mL菌液加入9 mL人工胃液,30 ℃恒温培养3 h,测定活菌数;将1 mL消化3 h的菌液转接至人工肠液,30 ℃恒温培养8 h,测定活菌数,并按公式(4)计算存活率:
式中:A1,处理后的活菌数,CFU/mL;A0,初始的活菌数,CFU/mL。
1.3.8 耐胆盐能力的测定
3 g/L胆盐:溶解0.75 g牛胆盐于250 mL MRS-硫代硫酸钠培养基。接种2% 对数期菌液至含胆盐培养基,30 ℃培养8 h,每2 h测OD600值,按公式(5)计算生长率:
式中:A1,胆盐组OD600值;A0,对照组OD600值。
1.3.9 遗传稳定性试验
选择耐酸性最佳的突变株U-E18,以2%接种量传代培养12代后,于pH 5.5、4.5、3.5、2.5和1.5的酸性MRS肉汤中培养,测定OD600值并观察菌株遗传稳定性。
1.3.10 菌株全基因组测序及分析
各取1 mL原始菌株和突变株,4 ℃7 000 r/min离心5 min后,1 ×PBS洗涤3次。使用DNA提取试剂盒(生工生物技术公司)提取基因组DNA,经质检后送往上海派森诺生物有限公司进行Illumina NovaSeq PE150测序。基于蛋白质直系同源簇(cluster of orthologous groups of protein,COG)和KEGG数据库进行功能注释,分析耐酸相关基因潜在功能。
1.4 数据处理与分析
数据表示为“平均值±标准差”,SPSS 22.0进行单因素方差分析(P <0.05为显著差异),Origin 2021作图,所有试验重复3次。
2 结果与分析
2.1 紫外诱变条件的确定
由图1可知,当照射时间达到60 s时,致死率急剧增加,可达72.1%,表明菌株在此阶段对紫外线高度敏感,突变效果显著,这与卢承蓉等[14]的研究结果一致。一般认为,当UV诱变致死率处于60%~80%时,更易获得正向突变率高的菌株[15]。因此,确定最佳UV诱变时间为60 s。
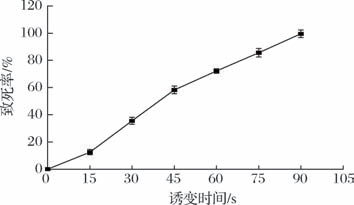
图1 食窦魏斯氏菌W25经紫外光不同照射时间下的致死率
Fig.1 Lethality of W.cibaria W25 by different UV irradiation durations
2.2 EMS诱变条件的确定
由图2可知,当诱变剂浓度为1.0%(体积分数)时,致死率不稳定且均不符合最适筛选范围;当诱变剂浓度为0.5%(体积分数)时,致死率随时间的延长稳定上升,培养30~45 min时,致死率在60%左右,能获得良好诱变效果[16]。因此,确定最佳诱变时间45 min,最佳诱变浓度0.5%(体积分数)。
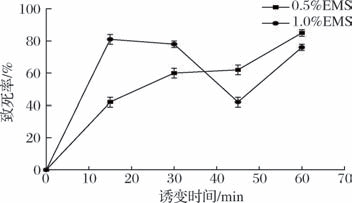
图2 食窦魏斯氏菌W25在不同浓度EMS处理条件下的致死率
Fig.2 Lethality of W.cibaria W25 with different concentrations of EMS treatments
2.3 突变株耐酸性筛选
通过梯度酸胁迫筛选出一株耐酸能力最强的突变株。如表1可知,所有突变株在pH 3.0、pH2.0、pH 1.5条件下的相对生长率均显著高于原始菌株W25,突变株U20、E7、U-E18与E-U28的相对生长率分别是原始菌株W25的1.15、0.64、3.72、2.40倍。复合诱变方法显著提升了菌株耐酸性,其中U-E18为最优耐酸突变株。
表1 突变株在不同pH值培养基中的相对生长率
Table 1 Relative growth rates of mutant strains in different pH media
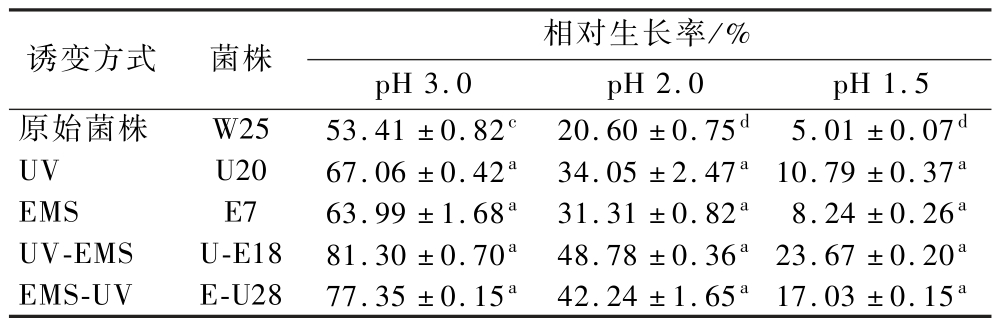
注:不同字母表示各菌株纵向比较差异显著(P <0.05)(下同)。
2.4 生长曲线
如图3所示,5株实验菌株的生长趋势整体呈现一致性,都经历了适应期、对数期、稳定期这3个阶段。0~4 h内,5组菌株生长曲线相近,从对数生长期开始,U20、E7、U-E18和E-U28的生长情况均优于W25,而U-E18始终优于各个菌株。
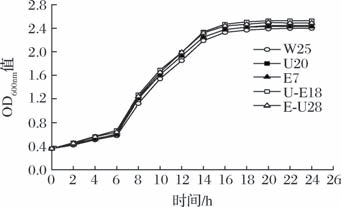
图3 原始菌株与突变株的生长曲线
Fig.3 Growth curve of original strain and mutagenic strains
2.5 产酸能力测定
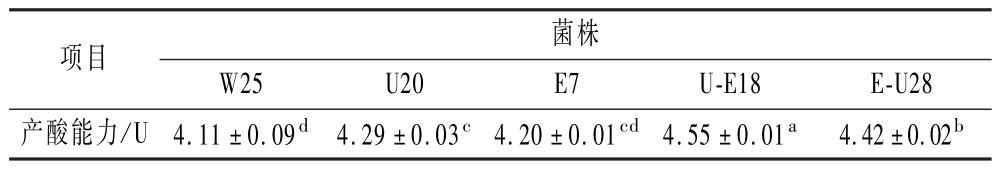
产酸能力作为乳酸菌发酵性能的关键指标,直接影响发酵制品的品质[17]。如表2所示,所有突变株的产酸能力均高于原始菌株,U-E18显著高于W25,产酸能力达4.55 U。
表2 原始菌株与突变株的产酸能力变化
Table 2 Changes in acid producion capacity of the original strain and the mutants
2.6 体外益生特性分析
2.6.1 人工模拟胃、肠液耐受性分析
人工胃液耐受性分析结果如图4所示,随着时间的延长,所有菌株存活率呈现下降趋势。原始菌株仅耐受pH 3.0和pH 2.0的酸性环境,而突变株在不同的pH环境下表现出更强的耐受性,存活率显著高于原始菌株,其中突变株U-E18在各pH条件下存活率均为最高。
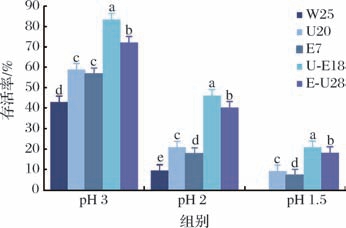
图4 原始菌株与突变株的人工模拟胃液存活情况
Fig.4 Artificial simulated gastric fluid survival of the original strain and the mutagenic strain
注:不同字母表示各菌株在相同pH下比较差异显著(P<0.05)(下同)。
人工肠液耐受性分析结果如图5所示,所有突变株均表现出良好的耐受性,存活率显著高于原始菌株,其中U-E18在人工模拟肠液中存活率最高,耐受性最优。
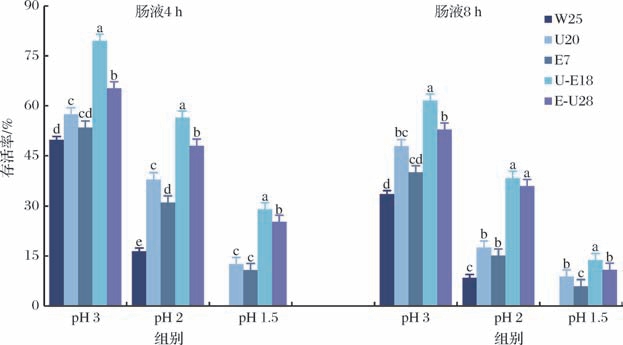
图5 原始菌株与突变株的人工模拟肠液存活情况
Fig.5 Artificial simulated intestinal fluid survival of the original strain and the mutagenic strain
2.6.2 胆盐耐受性分析
如表3所示,所有菌株的生长率均随时间延长而下降,其中原始菌株W25的耐受性最弱。
表3 原始菌株与突变株在胆盐环境中的生长情况
Table 3 Growth of original strain and mutagenic strains in bile salt environment
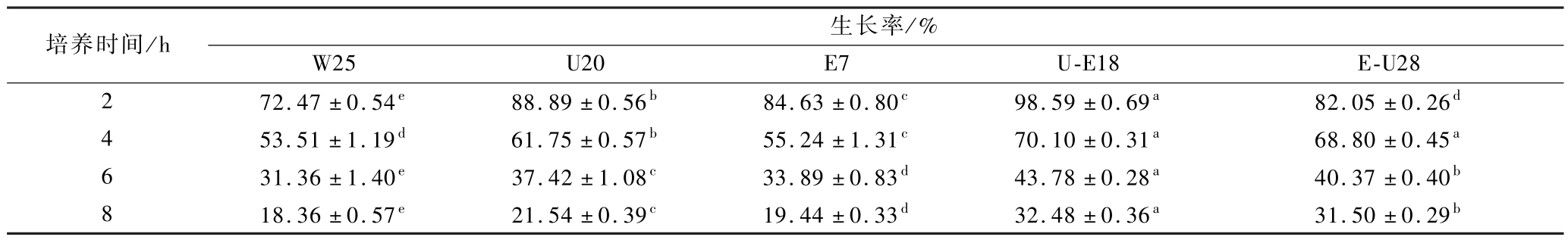
培养8 h时,突变株U-E18、E-U28、U20、E7的生长率分别较W25高出0.77、0.72、0.17和0.06倍,复合诱变的效果优于单一诱变,复合突变株U-E18在不同培养时间下均表现最佳,胆盐耐受性最强。
2.7 遗传稳定性分析
为了研究菌株的耐酸性是否由可遗传突变引起,将突变株U-E18连续培养12代,接种至不同pH培养基中进行耐酸性分析,结果如图6所示,菌株在传代过程中生长状态稳定,说明突变株具有良好的耐酸遗传稳定性。
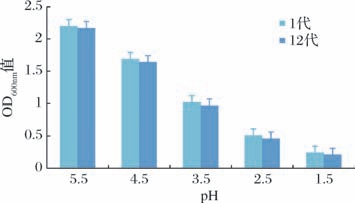
图6 U-E18在不同pH下的遗传稳定性评价
Fig.6 Evaluation of the genetic stability of U-E18 at different pH values
2.8 基因功能注释
2.8.1 蛋白编码基因的COG注释
如图7所示,在基因组编码的2 273个基因中,1 774个基因获得COG功能注释,占比78.05%。功能分类显示主要富集于以下五类,碳水化合物运输与代谢占比6.95%、翻译及核糖体结构与生物合成占比6.24%、细胞壁/膜/包膜生物发生占比5.89%、氨基酸转运代谢占比5.76% 以及复制重组修复占比5.32%。
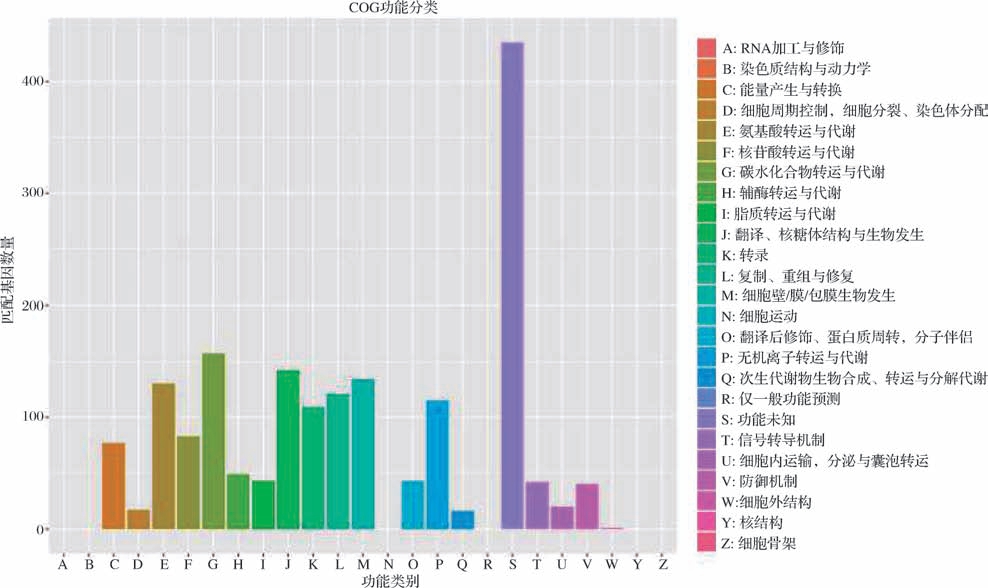
图7 COG功能分类图
Fig.7 COG functional classification chart
2.8.2 蛋白编码基因的KEGG注释
如图8所示,在2 273个编码基因中,1 101个基因获得功能注释,占48.44%。注释基因主要富集于以下通路,遗传信息处理有378个基因,占比34.3%、碳水化合物代谢有207个基因,占比18.8%、环境信息处理有140个基因,占比12.7%和细胞过程的基因数量有55个,占比5.0%。共鉴定到161条代谢通路,涉及657个基因,其中ABC转运蛋白有81个基因和次级代谢产物生物合成有16个基因显著富集。
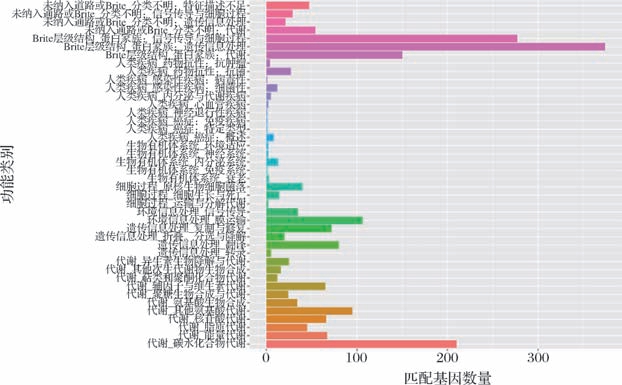
图8 KEGG统计图
Fig.8 KEGG statistical charts
3 结论与讨论
食窦魏斯氏菌的耐酸性是影响食品发酵效率与品质的关键因素,然而现有菌株往往难以满足工业化生产需求,亟需通过菌株改良提升其性能。诱变选育可通过物理或化学方法诱导变异,是筛选优良菌株的有效方法。本研究采用UV-EMS复合诱变技术选育出耐酸性显著增强的突变菌株U-E18,其在pH 3.0下的生长率显著高于原始菌株W25(P <0.05),如CONTRERAS等[18]的研究中,酒类酒球菌突变菌株E1在pH 3.5的合成葡萄酒和红葡萄酒中的生长率平均比原始菌株PSU-1提高39%。且本研究中,在pH 1.5条件下U-E18的相对生长率比原始菌株W25提升3.72倍,可见通过诱变提升了菌株的耐酸性。同时,U-E18产酸能力达4.55 U,显著优于W25,这与何彬彬等[19]和陶雨施[20]研究相似,也通过诱变分别获得产酸能力更强的嗜热链球菌和保加利亚乳杆菌突变株。这些结果表明,复合诱变可以通过改变其生理代谢过程获得耐酸性和产酸能力增强的优良菌株。
在益生特性评估方面,突变株U-E18展现出显著优于原始菌株W25的胃肠环境耐受能力。在pH 3的人工胃液中处理3 h时,原始菌株W25的存活率最高仅为42.79%,而突变株U-E18高达83.48%;将经人工模拟胃液处理后的菌株接种于人工模拟肠液中继续培养8 h,W25存活率最高仅为33.63%,其中U-E18最高可达61.54%。W25菌株在pH 1.5的模拟胃液中存活率极低,几乎完全失活,表明其缺乏强酸耐受能力。因此,即使后续进入pH适宜的模拟肠液环境,因胃酸已造成不可逆损伤,该菌株仍无法恢复活性或有效定植。相比之下,诱变后的菌株在相同pH 1.5的模拟胃肠液中仍能存活并成功定植,显示出诱变后显著提升了胃肠适应性。ŠEME等[21]通过UV-EMS复合诱变得到的2种突变株在连续暴露于胃肠液条件下菌落总数明显增多(P <0.05)。李荞荞[22]采用重离子辐照诱变获得的干酪乳杆菌突变株JY200-19在人工胃肠液中的存活率分别为125% 和279%,高于原始菌株的66.12%和37.01%,显著提高了菌株在胃肠环境中的存活率。耐胆盐实验显示U-E18具有更强的胆盐耐受性,培养2 h时存活率为98.59%,显著高于W25的72.74%;培养8 h时存活率更是达到W25的0.77倍。这些数据表明通过复合诱变得到的突变株不仅能够适应胃肠环境,也能在肠道中定植并发挥益生功能。
食窦魏斯氏菌U-E18的组学分析为解析其耐酸机制提供了重要线索。COG功能注释分析表明,碳水化合物转运代谢、核糖体生物合成及氨基酸转运代谢等关键通路显著富集,与文献报道的乙醇应激下副干酪乳杆菌的适应机制类似[23]。本研究菌株可能通过上调碳水化合物代谢相关基因的表达,重塑细胞膜通透性,从而增强营养物质的摄取和利用效率。KEGG通路分析进一步证实ABC转运蛋白系统的显著富集,该系统通过精确调控氨基酸和糖类等营养物质的跨膜转运,为细胞在酸性环境中维持稳态提供了物质基础[24]。本研究通过诱变育种和梯度酸胁迫筛选获得一株耐酸性显著增强的食窦魏斯氏菌突变株,其人工胃肠耐受性和胆盐耐受性均显著提升,依据代谢通路富集结果,初步揭示了其耐酸机制,为食品发酵工业的菌种选育与工艺优化提供了借鉴。
[1]文宇萍,金清.饲料提取物对食窦魏斯氏菌耐酸性的影响[J].延边大学农学学报,2023,45(3):45-50.WEN Y P,JIN Q.Effect of feed extract on acid resistance of Weissella cibaria[J].Agricultural Science Journal of Yanbian University,2023,45(3):45-50.
[2]张广峰,张楠笛,赵婷婷,等.一株食窦魏斯氏菌的分离鉴定及其质粒的序列分析[J].食品工业科技,2018,39(8):100-105.ZHANG G F,ZHANG N D,ZHAO T T,et al.Isolation and identification of Weissella cibaria and sequence analysis of its plasmid[J].Science and Technology of Food Industry,2018,39(8):100-105.
[3]热孜姑丽·库尔班,张志东,孙建,等.生鲜驼乳及发酵驼乳中益生乳酸菌的研究进展[J].食品科技,2024,49(1):1-8.REZIGULI Kuerban,ZHANG Z D,SUN J,et al.Research progress of probiotic lactic acid bacteria in fresh and fermented camel milk[J].Food Science and Technology,2024,49(1):1-8.
[4]赵皓静,王晓丹,邱树毅,等.液质发酵食品中微生物群落及与乳酸菌间相互作用研究进展[J].微生物学通报,2021,48(3):960-973.ZHAO H J,WANG X D,QIU S Y,et al.Microbial community and interaction between lactic acid bacteria and microorganisms in liquid fermented food:A review[J].Microbiology China,2021,48(3):960-973.
[5]UNNIKRISHNAN S.Functional aspects and potential applications of Weissella species in food and health[J].International Journal of Fermented Foods,2021,10(1):13-23.
[6]叶子晗,王文骏,周建伟,等.脉冲强光杀菌机理及其在食品领域应用的研究进展[J].食品科学,2025,46(4):295-305.YE Z H,WANG W J,ZHOU J W,et al.Research progress on the mechanism of pulsed light sterilization and its application in food field[J].Food Science,2025,46(4):295-305.
[7]颜菲,毕平,张涛,等.紫外和EMS诱变选育大肠杆菌赖氨酸营养缺陷型突变株的综合实验设计与实践[J].实验技术与管理,2021,38(9):204-209;223.YAN F,BI P,ZHANG T,et al.Design and practice of comprehensive experiment of screening lysine mutants by UV and EMS induced mutagenesis[J].Experimental Technology and Management,2021,38(9):204-209;223.
[8]刘彩月.胡麻EMS突变体库的构建及抗ALS类除草剂与高油酸突变体的鉴定分析[D].呼和浩特:内蒙古大学,2023.LIU C Y.Construction of EMS Mutant Library of Linum usitatissimum and identification and analysis of als herbicide-resistant and high oleic acid mutants[D].Hohhot:Inner Mongolia University,2023.
[9]GOPINATH S,VENKATAPRASAD R,RAJNISH K N,et al.Enhancement of serrapeptase hyper producing mutant by combined chemical and UV mutagenesis and its potential for fibrinolytic activity[J].Journal of Pure and Applied Microbiology,2020,14(2):1295-1303.
[10]林哲.乳酸菌(Lactobacillus shenzhenensis LY-73~ T)全基因组测序与应用分析[D].广州:华南理工大学,2016.LIN Z.Whole Genome sequencing and application analysis of Lactobacillus shenzhenensis LY-73~ T[D].Guangzhou:South China University of Technology,2016.
[11]LI W X,YANG L,NAN W L,et al.Whole-genome sequencing and genomic-based acid tolerance mechanisms of Lactobacillus delbrueckii subsp.bulgaricus LJJ[J].Applied Microbiology and Biotechnology,2020,104(17):7631-7642.
[12]尹义敏,田丰伟,翟齐啸,等.耐酸植物乳杆菌的紫外诱变选育及性质的研究[J].中国乳品工业,2015,43(3):8-10;14.YIN Y M,TIAN F W,ZHAI Q X,et al.Enhancement of the acid tolerant ability of Lactobacillus plantarum by UV mutation and properities study[J].China Dairy Industry,2015,43(3):8-10;14.
[13]梁楚容,王琴,马路凯,等.发酵多肽Asp-Asp-Asp-Tyr和Asp-Tyr-Asp-Asp的稳定性研究[J].轻工学报,2023,38(2):48-55.LIANG C R,WANG Q,MA L K,et al.Study on the stability of fermented polypeptides Asp-Asp-Asp-Tyr and Asp-Tyr-Asp-Asp[J].Journal of Light Industry,2023,38(2):48-55.
[14]卢承蓉,叶美芝,上官文丹,等.高产胞外多糖乳酸菌的诱变育种及其益生特性[J].食品与发酵工业,2020,46(12):14-20.LU C R,YE M Z,SHANGGUAN W D,et al.Mutation breeding for high-yield exopolysaccharide lactic acid bacteria and evaluation of its probiotic properties[J].Food and Fermentation Industries,2020,46(12):14-20.
[15]陆峰.高产蛋白酶芽孢杆菌的He-Ne激光和紫外联合诱变筛选及其机理研究[D].镇江:江苏大学,2023.LU F.Screening and mechanism study of high protease-producing bacillus by combined he-ne laser and ultraviolet mutagenesis[D].Zhenjiang:Jiangsu University,2023.
[16]郑琳.高产甘露醇柠檬明串珠菌的诱变筛选及发酵条件优化[D].延吉:延边大学,2017.ZHENG L.Mutagenesis screening and fermentation condition optimization of high mannitol-producing Leuconostoc citreum[D].Yanji:Yanbian University,2017.
[17]谷贵章,张帅,诸夔妞,等.糟醉鱼中高抗氧化活性乳酸菌的筛选与鉴定[J].食品与发酵工业,2022,48(22):89-94.GU G Z,ZHANG S,ZHU K N,et al.Screening and identification of lactic acid bacteria with high antioxidant activity from Zaozuiyu(fish fermented distiller’s grain)[J].Food and Fermentation Industries,2022,48(22):89-94.
[18]CONTRERAS Á,DÍAZ G,MENDOZA S N,et al.Metabolic behavior for a mutant Oenococcus oeni strain with high resistance to ethanol to survive under oenological multi-stress conditions[J].Frontiers in Microbiology,2023,14:1100501.
[19]何彬彬,邰佳慧,卢纹慧,等.嗜热链球菌半乳糖突变株的选育及其发酵特性[J].中国食品学报,2025,25(1):26-38.HE B B,TAI J H,LU W H,et al.Breeding and fermentation characteristics of galactose mutant strains of Streptococcus thermophilus[J].Journal of Chinese Institute of Food Science and Technology,2025,25(1):26-38.
[20]陶雨施.脉冲强光与硫酸二乙酯诱变选育保加利亚乳杆菌高产胞外多糖的比较研究[D].沈阳:沈阳农业大学,2018.TAO Y S.Comparative study on breeding of Lactobacillus bulgaricus with high exopolysaccharide production by pulsed light and diethyl sulfate mutagenesis[D].Shenyang:Shenyang Agricultural University,2018.
[21]ŠEME H,BOGOVICˇ MATIJAŠIC' B,ŠVIGELJ K,et al.Generation of Lactobacillus plantarum strains with improved potential to target gastrointestinal disorders related to sugar malabsorption[J].Food Research International,2017,94:45-53.
[22]李荞荞.重离子辐照诱变干酪乳杆菌优良菌株选育及在抗结肠癌中的应用[D].兰州市:中国科学院大学(中国科学院近代物理研究所),2020.LI Q Q.Breeding of excellent Lactobacillus casei strains by heavy ion irradiation mutagenesis and their application in anti-colon cancer[D].Lanzhou:University of Chinese Academy of Sciences (Institute of Modern Physics,Chinese Academy of Sciences),2020.
[23]YAN J M,WU M L,KWOK L Y,et al.Adenine DNA methylation is involved in regulating ethanol and osmotic stress responses in Lacticaseibacillus paracasei Zhang[J].Food Frontiers,2023,4(3):1347-1361.
[24]曲俊泽,陈天华,姚明东,等.ABC转运蛋白及其在合成生物学中的应用[J].生物工程学报,2020,36(9):1754-1766.QU J Z,CHEN T H,YAO M D,et al.ABC transporter and its application in synthetic biology[J].Chinese Journal of Biotechnology,2020,36(9):1754-1766.