生物被膜是细菌适应外界环境变化的一种策略,菌体与其分泌的多聚物质共同包绕聚集,形成附着于表面的复杂结构,具有独特的结构和代谢特征[1-3]。此种被膜形成能力被认为是微生物的普遍属性。约80%的微生物种群均以此方式存在[4-5]。对细菌而言,这是一种重要的生存保护机制。相较于浮游细菌,生物被膜状态赋予了细菌更强的抗逆能力[6]。得益于多聚基质的保护,生物被膜内细菌可以抵御免疫系统的攻击并降低抑/杀菌药物的敏感性,同时还能持续释放细菌,造成反复感染[7-8]。因此,如何有效控制或抑制细菌生物被膜具有重要意义。
金黄色葡萄球菌(Staphylococcus aureus),作为食品工业常见的食源性致病菌和腐败菌,易形成生物被膜,其分泌的肠毒素除了引起感染外,还会污染食物并导致食物中毒[9]。在医学研究领域中还发现金黄色葡萄球菌是多种感染性疾病的病原体,其引发的病症范围广泛,从皮肤溃疡、伤口感染,到心内膜炎、骨髓炎、肺炎,乃至中毒性休克综合症,严重威胁民众健康[10-15]。形成生物被膜会使金黄色葡萄球菌耐药性显著增强10~1 000倍[16]。为解决食品和医学领域有关金黄色葡萄球菌生物被膜污染问题,迫切需要探索高效、安全的新型药物制剂[17]。
抗菌肽(antimicrobial peptide,AMP)亦称肽抗生素,是生物体先天性免疫应答的重要物质,在自然界中广泛存在。这类肽具备分子质量小、抗菌谱广、不易诱发耐药性以及对细菌等病原体活性强等特点[18]。抗菌肽因其独特的生物学活性和区别于传统抗生素的作用机制,成为最具发展潜力的抗菌药物之一[19-20],在食品加工、畜牧兽医、农业种植及临床医药等领域具有广泛的应用价值[21-23]。
当前对抗菌肽作用机制的研究,文献多集中于阐述其直接杀伤敏感菌的途径[24]。这些途径主要包括:a)在靶细胞膜上形成疏水性孔隙,造成内容物泄漏和细胞裂解[25-26];b)与菌体内关键蛋白质(如酶)及核酸(DNA)结合,从而引发细胞死亡[25,27-29]。同时,部分抗菌肽也被证实具备抑制敏感细菌生物被膜形成的能力[30-31]。
基于抗菌肽-细胞膜相互作用原理,实验室前期构建了一种生物磁性脂质体分离-细胞膜色谱联用技术,用于大鲵皮肤黏液抗菌肽的筛选与纯化并获得大鲵皮肤黏液抗菌肽Andricin 01(Ala-IIe-Gly-His-Cys-Leu-Gly-Ala-Thr-Leu),区别于以往传统抗菌肽分离筛选方法,本实验为后续筛选其他新型抗菌肽提供技术支持[32-33]。实验室前期研究从大鲵皮肤黏液中筛选获得抗菌肽Andricin 01对金黄色葡萄球菌展现出显著的抑制效果,同时具备干扰该菌生物被膜形成的能力。本研究将探究大鲵皮肤黏液抗菌肽Andricin 01对S. aureus ATCC25923敏感菌及其生物被膜的抑制作用,为生物被膜形成污染控制及抗菌制剂开发应用提供参考。
1 材料与方法
1.1 菌种与材料
S. aureus ATCC25923,美国微生物菌种保藏中心;大鲵皮肤黏液抗菌肽Andricin 01(氨基酸序列AIGHCLGATL,纯度>95%),实验室利用前期已构建的生物磁性脂质体,通过细胞膜色谱法分离、筛选,经反向高效液相纯化,基质辅助激光解吸飞行时间质谱仪(matrix assisted laser desorption Ionization time of flight mass spectrometry,MALDI-TOF MS)鉴定抗菌肽Andricin 01氨基酸序列信息;LB液体培养基,青岛海博生物技术有限公司;碱性磷酸酶试剂盒,南京建成科技有限公司;SYTO 9、LIVE/DEAD Bacterial Viability Kits试剂盒,美国赛默飞有限公司;碘化丙啶(propidium iodide,PI)溶液,北京索莱宝科技有限公司;24孔培养板,美国康宁有限公司。
S.aureus ATCC25923甘油保藏菌株接种于新鲜灭菌LB液体培养基37 ℃、150 r/min摇床振荡培养至对数生长期(OD600约为0.7)备用。每次实验前,将活化好的菌液按照3%(体积分数)比例接种新鲜LB液体培养基,固体培养基加入1.5%(质量分数)琼脂。
1.2 仪器与设备
HVE-50高压蒸汽灭菌锅,日本Hirayama公司;SPX-250生化培养箱,上海博讯实业有限公司医疗设备厂;SpectraMax 190全波长酶标仪,美谷分子仪器(上海)有限公司;CytoFLEX流式细胞仪,美国Beckman Coulter有限公司;SU-8010扫描电子显微镜,日本Hitachi公司;FV1200激光共聚焦显微镜,日本Olympus公司。
1.3 实验方法
1.3.1 最小抑菌浓度(minimal inhibitory concentration,MIC)测定
LB液体培养基中,接种3%对数生长期S. aureus ATCC25923菌液,并加入系列终质量浓度(256~1 μg/mL,2倍稀释)的Andricin 01。空白对照采用等体积PBS缓冲液处理。37 ℃、150 r/min摇床培养24 h。肉眼初步评估培养物浊度变化后,吸取200 μL各质量浓度菌液于96孔板,600 nm处测定吸光度。判定MIC值。
1.3.2 抑菌动力学曲线
S.aureus ATCC25923于LB液体培养基中37 ℃振荡培养24 h至对数期。在96孔板中按梯度加入抗菌肽Andricin 01-菌液混合液200 μL(三复孔),600 nm检测吸光度。根据生长曲线分析Andricin 01各质量浓度对目标菌株的生长影响。
1.3.3 抗菌肽对S.aureus ATCC25923细胞壁的影响
S.aureus ATCC25923于LB培养基中振荡培养24 h至对数期。经梯度质量浓度Andricin 01处理,每间隔4 h收集样本。5 000 r/min离心15 min,取上清液根据碱性磷酸酶试剂盒操作流程测定酶活力。通过酶活力动力学曲线评估抗菌肽Andricin 01对目标菌株细胞壁的影响。
1.3.4 流式细胞分析
为了进一步研究抗菌肽Andricin 01对S. aureus ATCC25923细胞的损伤情况,选取SYTO 9和PI染料对细菌细胞进行检测。利用流式细胞仪测定细胞膜的损伤情况,取1.1节配制的S. aureus ATCC25923菌液10 mL,8 000 r/min离心3 min,弃上清液;加入1 mL生理盐水,重悬细胞。8 000 r/min离心3 min,弃上清液,重复一次。重悬细胞于500 μL生理盐水中;每管中移取300 μL与MIC浓度Andricin 01等比例混合,PBS缓冲液作为对照,37 ℃培养12 h,采用流式细胞仪FITC通道和PerCP通道检测细胞变化。
SYTO 9可以穿透活细胞的膜,PI无法进入具有完整细胞膜的活细胞,当细胞膜损伤不完整时,PI可进入细胞,与胞内遗传物质特异性结合,通过细菌细胞经处理前后结果差异,说明抗菌肽Andricin 01对胞膜完整性的影响。
1.3.5 结晶紫染色检测
吸取对数期的S.aureus ATCC25923菌液100 μL分别加入96孔板中,再分别加入100 μL抗菌肽Andricin 01溶液,使终质量浓度为1/4 MIC、1/2 MIC和3/4 MIC(为避免因Andricin 01质量浓度过高而对浮游S.aureus ATCC25923细菌产生杀灭作用从而干扰减少生物被膜的形成量,故试验采用亚抑菌浓度的抗菌肽Andricin 01),37 ℃下培养3 d至其生物被膜形成。对照组添加100 μL PBS缓冲液。吸去孔内悬浮菌液,生理盐水缓慢冲洗,甲醇固定15 min,倒掉液体,晾干后加入200 μL,2 mg/mL的结晶紫染色20 min,倒掉结晶紫,蒸馏水洗浮色后风干,再向各孔加入200 μL 95%(体积分数)乙醇摇床(100 r/min)脱色30 min后,吸取100 μL染液至另一孔板中,通过酶标仪测定595 nm下的OD值。
1.3.6 生物被膜菌落计数测定
参考1.3.5节方法,制备S. aureus ATCC25923生物被膜。吸去孔内菌悬液,蒸馏水清洗2次去除浮游菌。用洁净的枪头刮取各孔生物被膜,分别转移至另一无菌孔板中,加入200 μL生理盐水,超声波分散处理10 min后,均匀涂布于LB固体培养基上,37 ℃静置培养24 h,进行菌落计数。
1.3.7 扫描电镜(scanning electron microscope,SEM)观察抗菌肽对金黄色葡萄球菌生物被膜的抑制作用
LB液体培养基将菌液稀释至106 CFU/mL,吸取1 mL稀释菌悬液至孔板中,37 ℃恒温培养24 h,PBS溶液冲洗干净表面浮游菌,向样品处理组加入1 mL/孔培养基-Andricin 01溶液,空白对照组加入1 mL/孔培养基-生理盐水。37 ℃培养24 h。生理盐水轻柔冲洗表面浮游菌,2.5%(体积分数)戊二醛溶液固定30 min,0.1 mol/L pH 7.0的PBS缓冲液漂洗样品3次,每次15 min,1% (质量分数)锇酸溶液固定样品2 h后,PBS漂洗样品3次,每次15 min;依次梯度体积分数30%、50%、70%、80%、90%、95%、100% 的乙醇脱水处理后,乙醇与醋酸异戊酯的混合液(体积比1∶1)处理样品30 min,纯醋酸异戊酯处理样品1 h,CO2临界点干燥,镀膜,扫描电镜观察样品。
1.3.8 激光共聚焦显微镜(confocal laser scanning microscope,CLSM)观察抗菌肽对金黄色葡萄球菌生物被膜的抑制作用
LB液体培养基将菌液稀释至106 CFU/mL,吸取1 mL稀释菌悬液至孔板中,37 ℃孵育24 h,PBS冲洗干净表面浮游菌,向样品处理组加入1 mL/孔培养基-Andricin 01溶液,空白对照组加入1 mL/孔培养基-生理盐水。37 ℃孵育24 h,弃孔内溶液,按照LIVE/DEAD Bacterial Viability Kits中SYTO 9/PI对生物被膜进行染色处理,1 mL染色工作液37 ℃避光染色15 min。配制染色工作液(2 mL PBS-2 μL SYTO 9~2 μL PI),染色结束后,将样品测试面置于激光共聚焦显微镜上,使用600 × 油镜采集图像拍摄,观察生物膜内死活菌分布数及三维厚度。
1.4 数据分析
数据以“平均值±标准差”表示。采用SPSS 29.0进行单因素方差分析,P <0.05为差异显著。
2 结果与分析
2.1 抗菌肽Andricin 01的最小抑菌浓度测定
为研究Andricin 01对金黄色葡萄球菌的抗菌活性,遵循临床实验室标准化协会(Clinical &Laboratory Standards Institute,CLSI)标准操作流程,通过微量稀释法测定Andricin 01对S. aureus ATCC25923的MIC为16 μg/mL(图1)。一般来说,肽的疏水性氨基酸残基对其抑菌活性也起着关键作用,疏水残基百分比≥30.00%[34-35]。抗菌肽的疏水性有利于其插入细胞膜,进而发挥抗菌作用,可以通过适当提升疏水基团比例有效提升抗菌活性[24]。生物信息学分析显示,大鲵抗菌肽Andricin 01(序列:AIGHCLGATL)具有典型疏水肽特征,含多个疏水氨基酸残基(如Ala1、Ile2、Leu10),氨基酸序列中存在的多个疏水性氨基酸位点在一定程度上增强了抗菌活性,疏水性质可能是其发挥抗菌活性的基础,疏水性氨基酸有助于抗菌肽选择性靶向敏感菌胞膜,从而抑制或杀死敏感菌,但疏水性氨基酸与细胞膜相互作用的过程较复杂,具体互作路径关系有待进一步解析[21]。
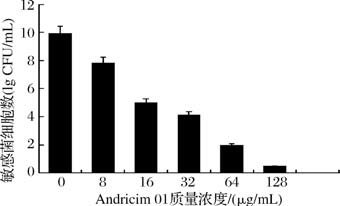
图1 抗菌肽Andricin 01对金黄色葡萄球菌ATCC25923的最小抑菌浓度
Fig.1 MIC of AMP Andricin 01 against S.aureus ATCC25923
2.2 抗菌肽Andricin 01对S. aureus ATCC25923的生长影响
由图2可知,S. aureus ATCC25923在抗菌肽Andricin 01处理质量浓度为16、32 μg/mL时,细菌生长受到抑制,与空白组生长曲线存在差异。前16 h抑制生长速率较慢,趋势平缓,16 h之后抑制效果更明显,呈现下降趋势,抑制速率较快,且整体数量较少,与空白组存在显著差异。
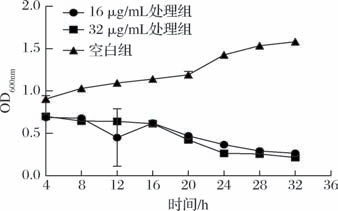
图2 抗菌肽Andricin 01对金黄色葡萄球菌ATCC25923的生长影响
Fig.2 The effect of AMP Andricin 01 on the growth of S.aureus ATCC25923
2.3 抗菌肽Andricin 01对S. aureus ATCC25923细胞壁的影响
细菌细胞壁与细胞膜之间通常存在碱性磷酸酶(alkaline phosphatase,ALP),在正常情况下,胞外环境无法检出其活性。当细胞壁或膜结构完整性受损时,ALP会外泄至胞外环境。当S.aureus ATCC25923分别暴露于16、32 μg/mL的Andricin 01溶液后,由图3可知,抗菌肽处理组细菌胞外ALP活力呈现浓度依赖性升高,抗菌肽Andricin 01浓度越大,破坏作用越强,经32 μg/mL Andricin 01处理组ALP活力显著高于16 μg/mL(P <0.05)。抗菌肽Andricin 01对S.aureus ATCC25923细胞具有一定的破坏作用,且胞外ALP活力受抗菌肽作用浓度和时间双因素调控,说明抗菌肽Andricin 01通过破坏敏感菌细胞屏障结构从而达到抑制其生长的目的。
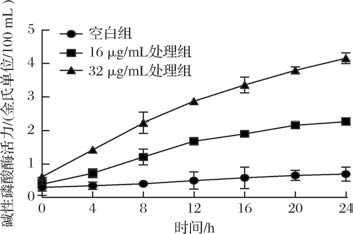
图3 金黄色葡萄球菌ATCC25923碱性磷酸酶活力曲线
Fig.3 ALP activity curves of S.aureus ATCC25923
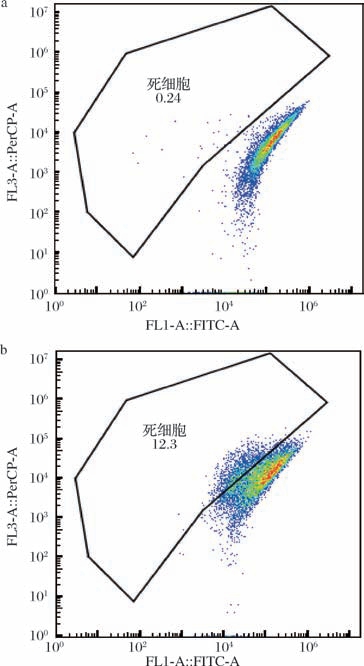
图4 抗菌肽Andricin 01对金黄色葡萄球菌ATCC25923的影响
Fig.4 The effect of AMP Andricin 01 on S.aureus ATCC25923
a-对照组;b-处理组
2.4 流式细胞结果分析
经MIC浓度Andricin 01处理后的S. aureus ATCC25923细胞PI染色细胞数明显增多,荧光信号增强,与空白对照差异显著,死细胞比例占12.3%,相比对照组死细胞比例仅占0.24%,相差近50倍,图 4中任意门内分布的散点即为 S. aureus ATCC25923死细胞的分布位点。流式结果进一步说明抗菌肽Andricin 01会影响金黄色葡萄球菌细胞膜通透性,损伤敏感菌胞膜,从而导致菌体死亡(图5)。
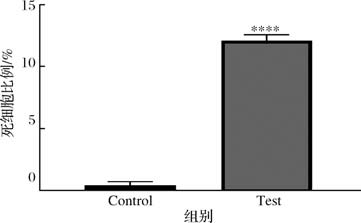
图5 抗菌肽Andricin 01对金黄色葡萄球菌ATCC25923细胞的影响
Fig.5 The effect of AMP Andricin 01 on S.aureus ATCC25923 cells
注:Control为对照组,Test为处理组,∗∗∗∗,与Control组相比,P<0.000 01。
2.5 结晶紫染色法对S. aureus ATCC25923生物被膜的形成抑制
采用结晶紫染色法定量分析Andricin 01对S.aureus ATCC25923生物被膜形成的影响,计算各组平均吸光度值,如公式(1)所示:
如表1所示,与对照组比较,亚抑菌浓度Andricin 01显著抑制生物被膜的生成(P <0.01),抑制效果随着质量浓度增加而增强,当处理浓度达到3/4 MIC时,Andricin 01对S. aureus ATCC25923生物被膜形成的抑制率高达50%以上。
表1 亚抑菌浓度Andricin 01对金黄色葡萄球菌ATCC25923生物被膜形成抑制率的影响
Table 1 Effect of sub-inhibitory concentration of Andricin 01 on the inhibition rate of biofilm formation in S.aureus ATCC25923
2.6 金黄色葡萄球菌生物被膜菌落计数结果
经表2亚抑菌浓度(3/4 MIC、1/2 MIC、1/4 MIC)Andricin 01处理的S. aureus ATCC25923生物被膜活菌计数显示,各处理组菌落总数较对照组显著降低(P <0.05),说明亚抑菌浓度的Andricin 01能够减少生物被膜结构中的活细菌数量,且随着质量浓度的增加,抑制效果增强。与结晶紫染色实验结果一致,计数结果表明Andricin 01能够减少S. aureus ATCC25923被膜的生物形成量。综合结晶紫染色和菌落计数结果得出Andricin 01对S.aureus ATCC25923生物被膜形成具有一定的抑制作用。
表2 亚抑菌浓度Andricin 01对生物被膜菌落计数的影响
Table 2 Effect of sub-inhibitory concentration of Andricin 01 on biofilm colony count
2.7 抗菌肽Andricin 01对S. aureus ATCC25923生物被膜的影响
扫描电镜采集到生物被膜内菌体聚集的超微结构状态如图6所示,在5.00 μm视野下发现未处理的对照组呈现典型致密细菌聚集,部分菌体出现联结形态,形成较紧密的生物被膜。经1/2 MIC质量浓度Andricin 01处理后的S. aureus ATCC25923生物被膜结构发生明显改变,排列分布疏松,菌体之间孔隙变大,膜表面附着的细菌数量较少,少量细菌胞膜表面出现凹陷甚至可见孔洞,部分细菌结构破坏,聚集态菌体数量减少。Andricin 01作用S.aureus ATCC25923细菌细胞正常结构遭到破坏,导致细胞内容物流出,由于其具有一定的黏稠性,故而可以解释电镜观察下抗菌肽Andricin 01处理组部分细菌细胞与旁侧结构损伤的细菌细胞出现相互黏合的现象。

图6 抗菌肽Andricin 01对金黄色葡萄球菌ATCC25923生物膜菌体聚集状态的影响
Fig.6 Effect of AMP Andricin 01 on cell aggregation of S.aureus ATCC25923 biofilm
2.8 CLSM观察S.aureus ATCC25923生物被膜内活菌和死菌的变化
通过CLSM结果观察到经Andricin 01处理S.aureus ATCC25923生物被膜内细菌情况与对照组差异明显,主要体现在成膜厚度和膜内死、活菌数的变化上,经SYTO 9染色后会使活细菌发出绿色荧光,死菌则显示为红色。如图7所示。随着对照组生物被膜内活菌不断成熟,菌落密度增大,细菌聚集体变多,排列致密,生物被膜结构趋于平整,厚度逐渐增加。对比Andricin 01处理组发现,处理组与对照组之间有明显差异,抗菌肽Andricin 01处理组生物被膜内活菌数量较少、菌落分布疏松、密度小,成熟菌斑量减少、死菌数量比对照组多,经Andricin 01处理后的生物被膜黏附细菌较少、结构松散、不致密、厚度较薄。
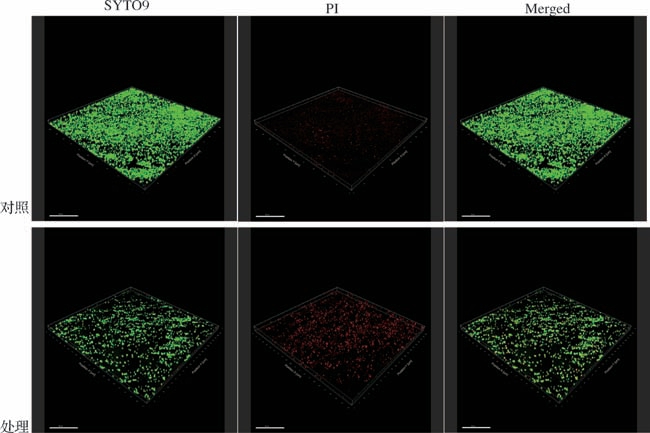
图7 抗菌肽Andricin 01对金黄色葡萄球菌ATCC25923生物被膜内细菌的影响
Fig.7 Effect of AMP Andricin 01 on the bacteria in the biofilm of S.aureus ATCC25923
3 讨论
金黄色葡萄球菌尤其易污染夹生或者未煮熟的肉、蛋、奶制品,导致食源性疾病爆发。以生物被膜形式存在的细菌与浮游菌相比,细菌聚集体数量大,排列致密,生物被膜结构中的细菌对环境条件(酸、碱、紫外线等)及抑/杀菌剂抵抗性强,同时会提高细菌对宿主免疫防御系统的抵御能力,出现食品交叉污染,危害公众健康。
大鲵抗菌肽Andricin 01对革兰氏阴性菌、阳性菌及真菌都表现出稳定的抗微生物活性,在药物开发领域应用广泛[32]。正如文献报道[21]抗菌肽抑菌作用机制,通过损伤细菌细胞膜结构,改变细胞膜通透性造成胞内物质泄漏,从而引发细菌死亡;或抗菌肽使细胞膜出现孔洞,进入细胞膜后作用于靶标,如遗传物质DNA和关键蛋白质,抑制正常生理功能从而导致细菌死亡。抗菌肽Andricin 01作用S. aureus ATCC25923时,ALP发生泄漏,Andricin 01浓度越大,碱性磷酸酶活力越高,菌体表面出现皱缩、细胞膜结构改变,细菌细胞屏障结构破坏程度与Andricin 01浓度存在剂量-效应关系。流式细胞结合扫描电镜结果揭示了Andricin 01作用S. aureus ATCC25923时,胞膜结构完整性遭到破坏,导致细菌生长被抑制,这与抗菌肽HJH-3作用S. aureus ATCC25923时通过破坏膜的完整性,导致细菌变形、破裂,达到抑制效果的作用途径相似[36]。本实验揭示大鲵抗菌肽Andricin 01对S.aureus ATCC25923的抑菌作用与笔者团队之前发表的圆二色光谱结果分析一致[32]。抗菌肽Andricin 01倾向于α-螺旋结构,这也是诸多靶向微生物细胞膜的抗菌肽的共同特征。然而不能排除抗菌肽Andricin 01是否存在其他作用机制,因为抗菌肽已被证明可通过多种途径发挥抗菌作用,如DNA损伤、抑制蛋白质合成或代谢途径、诱导凋亡等。
本实验验证了大鲵抗菌肽Andricin 01对敏感菌S.aureus ATCC25923自身以及形成生物被膜的抑制作用,激光共聚焦荧光染色观察生物被膜微观形态结构变化,Andricin 01处理组生物被膜荧光信号强度弱,菌落分布松散、膜结构破裂、厚度较薄。抗菌肽Andricin 01对S. aureus ATCC25923浮游细菌细胞的杀灭作用可以减少嵌入生物被膜内的活细菌,形成生物被膜的细菌细胞以与浮游菌细胞类似的方式受到抑制,减少构成生物被膜的活细菌数量,从而达到抑制生物被膜形成的效果。
4 结论
本研究探索了实验室前期分离获得的大鲵抗菌肽Andricin 01对S.aureus ATCC25923生物被膜的抑制作用及机理。MIC为16 μg/mL,结晶紫定量染色结果显示3/4 MIC浓度的Andricin 01对生物被膜形成抑制显著,抑制率达50% 以上,扫描电镜观察到Andricin 01处理S. aureus ATCC25923生物被膜结构遭到破坏,CLSM结果也证实了对生物被膜形成过程的抑制效果,经Andricin 01处理后的生物被膜厚度比对照组薄,被膜结构稀疏,膜内死菌数量多。实验结果证明了大鲵抗菌肽Andricin 01能够有效抑制S.aureus ATCC25923生物被膜的形成。
[1]张秀平,郭占达,陈陆,等.不同培养条件对鸭源鸡杆菌生物被膜形成的影响[J].中国兽医学报,2014,34 (7):1083-1088;1168.ZHANG X P,GUO Z D,CHEN L,et al.Influence of different culture conditions on the formation of Gallibacterium anatis biofilm[J].Chinese Journal of Veterinary Science,2014,34(7):1083-1088;1168.
[2]PACHECO T,GOMES AÉI,SIQUEIRA N M G,et al.SdiA,a quorum-sensing regulator,suppresses fimbriae expression,biofilm formation,and quorum-sensing signaling molecules production in Klebsiella pneumoniae[J].Frontiers in Microbiology,2021,12:597735.
[3]MENG F Q,ZHAO M W,LU Z X.The Lux S/AI-2 system regulates the probiotic activities of lactic acid bacteria[J].Trends in Food Science &Technology,2022,127:272-279.
[4]LEMON K P,EARL A M,VLAMAKIS H C,et al.Biofilm Development with An Emphasis on Bacillus subtilis[M].Bacterial Biofilms.Berlin,Heidelberg: Springer,2008,322:1-16.
[5]RICHARDS J J,MELANDER C.Controlling bacterial biofilms[J].Chembiochem,2009,10(14):2287-2294.
[6]GUO R,LUO X L,LIU J J,et al.Mass spectrometry based targeted metabolomics precisely characterized new functional metabolites that regulate biofilm formation in Escherichia coli[J].Analytica Chimica Acta,2021,1145:26-36.
[7]吴同垒,冀梦瑶,周诗淼,等.GlpK影响肠炎沙门菌生物被膜形成[J].中国兽医学报,2022,42(5):920-925.WU T L,JI M Y,ZHOU S M,et al.GlpK affects the biofilm formation of Salmonella Enteritis[J].Chinese Journal of Veterinary Science,2022,42(5):920-925.
[8]ZHAO A L,SUN J Z,LIU Y P.Understanding bacterial biofilms:From definition to treatment strategies[J].Frontiers in Cellular and Infection Microbiology,2023,13:1137947.
[9]刘美慧,李建科,刘柳,等.金黄色葡萄球菌生物膜形成相关基因及检测方法的研究进展[J].食品与发酵工业,2016,42(2):265-269.LIU M H,LI J K,LIU L,et al.Perspectives on the related genes and detection methods of Staphylococcus aureus biofilm formation[J].Food and Fermentation Industries,2016,42(2):265-269.
[10]李鑫,慈百全,王佳佳,等.噬菌体裂解酶TSPphg对金黄色葡萄球菌生物被膜的抑制作用及该过程转录组变化[J].微生物学杂志,2025,45(1):24-33.LI X,CI B Q,WANG J J,et al.Inhibition of Staphylococcus aureus biofilm by phage lyase TSPphg and transcriptome changes of the process[J].Journal of Microbiology,2025,45(1):24-33.
[11]徐重新,陈蔚,谢雅晶,等.食品中金黄色葡萄球菌检测及防控技术研究[J].农产品质量与安全,2019(3):49-56.XU C X,CHEN W,XIE Y J,et al.Detection and prevention and control technology on Staphylococcus aureus in food[J].Quality and Safety of Agro-Products,2019(3):49-56.
[12]KAASCH A J,MICHELS G.Staphylococcus aureus bloodstream infection:When is transthoracic echocardiography sufficient? [J].JACC.Cardiovascular Imaging,2015,8(8):932-933.
[13]LE MOING V,ALLA F,DOCO-LECOMPTE T,et al. Staphylococcus aureus bloodstream infection and endocarditis:A prospective cohort study[J].PLoS One,2015,10(5):e0127385.
[14]龚玲玉,罗青梅,冯莉,等.金黄色葡萄球菌引发食源性疾病的溯源分析[J].中国国境卫生检疫杂志,2024,47(2):167-170.GONG L Y,LUO Q M,FENG L,et al.Tracing analysis of foodborne disease caused by Staphylococcus aureus[J].Chinese Journal of Frontier Health and Quarantine,2024,47(2):167-170.
[15]谭慧林,吴忠红,金永生,等.食品中金黄色葡萄球菌的快速检测及其评估[J].新疆农业科学,2022,59(2):410-416.TAN H L,WU Z H,JIN Y S,et al.Determination of Staphlococcus aureus in food and evaluation of the fast kit[J].Xinjiang Agricultural Sciences,2022,59(2):410-416.
[16]温绍霞,孙竞.细菌生物膜形成及相关耐药性治疗研究进展[J].海南医学,2014,25(9):1331-1333.WEN S X,SUN J.Research progress of bacterial biofilm formation and related drug resistance treatment[J].Hainan Medical Journal,2014,25(9):1331-1333.
[17]WANG F,XIAO Y,LU Y,et al.Bacteriophage lytic enzyme P9ly as an alternative antibacterial agent against antibiotic-resistant Shigella dysenteriae and Staphylococcus aureus[J].Frontiers in Microbiology,2022,13:821989.
[18]李杰,杭柏林,秦爱建,等.牛血红蛋白源抗菌肽P3及其类似肽的生物信息学分析[J].中国畜牧兽医,2017,44(1):59-64.LI J,HANG B L,QIN A J,et al.Bioinformatics analysis of antimicrobial peptide P3 from bovine hemoglobin and its analogs[J].China Animal Husbandry &Veterinary Medicine,2017,44(1):59-64.
[19]GURYANOVA S V,OVCHINNIKOVA T V,GURYANOVA S V,et al.Immunomodulatory and allergenic properties of antimicrobial peptides[J].International Journal of Molecular Sciences,2022,23(5):2499.
[20]MA X,WANG Q,REN K X,et al.A review of antimicrobial peptides:Structure,mechanism of action,and molecular optimization strategies[J].Fermentation,2024,10(11):540.
[21]任婷,王金泽,郑天骄,等.大鲵血源抗菌肽AndricinB的生物信息学分析[J].黑龙江畜牧兽医,2021(22):123-126;153-154.REN T,WANG J Z,ZHENG T J,et al.Bioinformatics analysis of blood-derived antimicrobial peptide Andricin B of Andrias davidianus[J].Heilongjiang Animal Science and Veterinary Medicine,2021(22):123-126;153-154.
[22]XUAN J Q,FENG W G,WANG J Y,et al.Antimicrobial peptides for combating drug-resistant bacterial infections[J].Drug Resistance Updates,2023,68:100954.
[23]BREIJYEH Z,JUBEH B,KARAMAN R.Resistance of gram-negative bacteria to current antibacterial agents and approaches to resolve it[J].Molecules,2020,25(6):1340.
[24]SANCHIS I,SPINELLI R,ASCHEMACHER N,et al.Acetylcholinesterase inhibitory activity of a naturally occurring peptide isolated from Boana pulchella(Anura:Hylidae)and its analogs[J].Amino Acids,2020,52(3):387-396.
[25]王娅娅,李娜,曾键尧,等.抗菌肽的来源及其应用[J].生物学通报,2020,55(8):7-10.WANG Y Y,LI N,ZENG J Y,et al.Source and application of antimicrobial peptides[J].Bulletin of Biology,2020,55(8):7-10.
[26]辛本凯,王会岩.抗菌肽在抗菌材料中的研究进展[J].吉林医药学院学报,2021,42(1):53-55.XIN B K,WANG H Y.Research progress of antimicrobial peptides in antimicrobial materials[J].Journal of Jilin Medical University,2021,42(1):53-55.
[27]王铭遥,郑明静,任中阳,等.凡纳滨对虾抗菌肽的筛选及与DNA的结合机制[J].中国食品学报,2023,23(7):140-151.WANG M Y,ZHENG M J,REN Z Y,et al.Antimicrobial peptides screened from Penaeus vannamei shrimp and investigation of their DNA binding mechanism[J].Journal of Chinese Institute of Food Science and Technology,2023,23(7):140-151.
[28]陈飞龙,刘渔珠,彭勃,等.抗菌肽F1对金黄色葡萄球菌的胞内作用机制[J].食品科学,2017,38(6):36-41.CHEN F L,LIU Y Z,PENG B,et al.Intracellular mechanism of action of antimicrobial peptide F1 on Staphylococcus aureus[J].Food Science,2017,38(6):36-41.
[29]SUN A D,HUANG Z Y,HE L,et al.Metabolomic analyses reveal the antibacterial properties of a novel antimicrobial peptide MOp3 from Moringa oleifera seeds against Staphylococcus aureus and its application in the infecting pasteurized milk[J].Food Control,2023,150:109779.
[30]王雅蓉,朱明星,张帆,等.c-di-GMP的磷酸二酯酶PA4781在抗菌肽Merecidin抑制铜绿假单胞菌生物被膜中的作用[J].微生物学通报,2020,47(3):868-879.WANG Y R,ZHU M X,ZHANG F,et al.The role of c-di-GMP phosphodiesterase PA4781 in the inhibition of Pseudomonas aeruginosa biofilm by the antimicrobial peptide merecidin[J].Microbiology China,2020,47(3):868-879.
[31]蒲传奋,唐文婷.鳀鱼抗菌肽脂质体的制备与抗单增李斯特菌生物被膜活性研究[J].现代食品科技,2017,33(1):54-61.PU C F,TANG W T.Anchovy antibacterial peptide liposome preparation and antibiofilm activity against Listeria monocytogenes[J].Modern Food Science and Technology,2017,33(1):54-61.
[32]PEI J J,JIANG L.Antimicrobial peptide from mucus of Andrias davidianus:Screening and purification by magnetic cell membrane separation technique[J].International Journal of Antimicrobial Agents,2017,50(1):41-46.
[33]PEI J,FENG Z,REN T,et al.Purification,characterization and application of a novel antimicrobial peptide from Andrias davidianus blood[J].Letters in Applied Microbiology,2018,66(1):38-43.
[34]CHEN Y X,GUARNIERI M T,VASIL A I,et al.Role of peptide hydrophobicity in the mechanism of action of α-helical antimicrobial peptides[J].Antimicrobial Agents and Chemotherapy,2007,51(4):1398-1406.
[35]杨红艳.天然抗菌肽Cecropin衍生物的设计及抗菌活性研究[D].郑州:河南工业大学,2024.YANG H Y.Design and antimicrobial activity of naturalantimicrobial peptide Cecropin derivatives[D].Zhengzhou:Henan University of Technology,2024.
[36]王青,徐彦召,杨磊,等.一种广谱、低毒的抗菌肽类似物HJH-3的生物学活性和膜活性的测定[J].中国预防兽医学报,2019,41(8):800-806.WANG Q,XU Y Z,YANG L,et al.Determination of bioactivity and membrane activity of bovine antimicrobial peptide HJH-3[J].Chinese Journal of Preventive Veterinary Medicine,2019,41(8):800-806.